אבחון מניעה וטיפול בסיבוכי קרישיות יתר בהיריון - נייר עמדה
הופניתם מהדף אבחון מניעה וטיפול בסיבוכי קרישיות יתר בהיריון לדף הנוכחי.
|
| |
|---|---|
| אבחון מניעה וטיפול בסיבוכי קרישיות יתר בהיריון | |
| ניירות עמדה של האיגוד הישראלי למיילדות וגינקולוגיה | |
| תחום | מיילדות |
| האיגוד המפרסם | |
| קישור | באתר האיגוד הישראלי למיילדות וגינקולוגיה |
| תאריך פרסום | 17 באוקטובר 2012 |
| יוצר הערך | חברי הצוות להכנת נייר עמדה |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – פקקת ורידים , היריון
ניתן לחלק את סיבוכי קרישיות היתר (Hypercoagulability) בהיריון ל:
- טרומבואמבוליזם (TE, Thromboembolism)
- סיבוכי היריון
טרומבואמבוליזם כולל את פקקת הורידים העמוקים (DVT, Deep Vein Thrombosis) (80-75 אחוזים מסך כל אירועי הטרומבואמבוליזם) ואת התסחיף הריאתי (PE, Pulmonary Emboli) (25-20 אחוזים), ויחד מהווים את הסיבוכים הקשורים בעיקר למערכת הורידית האימהית ופחות למערכת העורקית, ולכן נקראים VTE (Venous Thrombo-Embolism). מדובר בתופעה חמורה הכרוכה בסיכון מוגבר לתחלואה אימהית ואף למוות, לדוגמא, 9% מסך מיקרי התמותה האימהית בארה"ב הם תוצאה של VTE. כמחצית מאירועי ה-VTE מתרחשים במהלך ההיריון וכמחצית בתקופת משכב הלידה. הסיבה לכך היא השילוב בין גורמים מיכניים (סטזיס) והורמונליים (השפעת אסטרוגן ופרוגסטרון) הגורמים לשינוי במערכת הקרישה הטרום הריונית לכיוון קרישיות יתר. הסיכון ל-VTE קיים כבר בשליש הראשון, עולה בשליש השלישי ומגיע לשיא בתקופת משכב הלידה. גורמי הסיכון העיקריים ל-VTE הם מאורע טרומבואמבולי בעבר, כאשר עד 25% מכלל האירועים הם אירועים חוזרים, ועדות לטרומבופיליה (מוגדרת כנטיית רקע מולדת או נרכשת לקרישיות יתר) ב-50-20 אחוזים מן המקרים. גורמי סיכון נוספים כוללים בין השאר: גיל, השמנת יתר, עישון, יתר לחץ דם וניתוח קיסרי.
סיבוכי היריון כוללים הפלות חוזרות, מות עובר ברחם מגורם לא ברור, פרה-אקלמפסיה (Preeclampsia), האטה בגדילה תוך רחמית (IUGR, Intra Uterine Growth Restriction) והפרדות שליה.
בעוד שהקשר בין טרומבופיליה מולדת לבין VTE הוא חזק ביותר, קיימת מחלוקת לגבי הקשר בין טרומבופיליה מולדת לסיבוכי היריון ולגבי יעילות טיפול במונעי קרישה (אנטיקואגולנטי - Anticoagulants) למניעת סיבוכי היריון בנשים עם טרומבופיליה מולדת. לעומת זאת, קיים קשר ברור ויתרון בטיפול בין טרומבופיליה נרכשת, ובעיקר תסמונת APLA (Anti Phospholipid Antibodies) וסיבוכי היריון.
אשר על כן עמדת האיגוד כדי למנוע ולטפל בסיבוכי קרישיות יתר בהיריון היא:
- מניעה וטיפול באירועי VTE בהיריון ובתקופת משכב הלידה שבחלקם קשורים לטרומבופיליה מולדת ונרכשת
- מניעת סיבוכי היריון הקשורים בעיקר לטרומבופיליה נרכשת (APLA)
הנחיות למניעה וטיפול באירועי VTE בהיריון ובמשכב הלידה
• כל אישה תעבור הערכה (Risk assessment) לגבי מידת הסיכון לאירוע טרומבואמבולי (VTE) על פי היסטוריה רפואית וגורמי סיכון וישקל הצורך בבירור לטרומבופיליה במהלך המפגש הרפואי הראשוני טרם או במהלך ההיריון. הטיפול המונע באישה ההרה יותאם באופן פרטני לכל אישה על פי גורמי הסיכון, ההיסטוריה הרפואית המילדותית, סיפור משפחתי וסוג הטרומבופיליה
• טיפול אנטיקואגולנטי במהלך ההיריון יינתן על פי התוויה, עם גילוי ההיריון, מוקדם ככל האפשר. טיפול הבחירה במהלך ההיריון הינו ב-LMWH (Heparin Low Molecular Weight)
• טיפול אנטיקואגולנטי יינתן לאחר הלידה על פי התוויה למשך תקופת משכב לידה (עד 6 שבועות) אלא אם כן צויין אחרת. טיפול אנטיקואגולנטי לאחר הלידה יכול להיות עם LMWH או VKA (Vitamin K Antagonists) לפי משך הטיפול המתוכנן, הטיפול שקדם להיריון ורצון היולדת. ככלל, מכיוון שהסיכון המחושב ליום לאירועי VTE גבוה יותר בתקופת משכב הלידה, מומלץ להחמיר בטיפול בתקופה זו ביחס לתקופה הטרום לידתית
• קיים קשר בין אירועי VTE להיפר-הומוציסטאינמיה ולכן בבירור VTE יש לבדוק רמת הומוציסטאין בצום. לעומת זאת, לא נמצא קשר ברור בין סיבוכי היריון להיפר-הומוציסטאינמיה או למוטציה ב-MTHFR (Methylene Tetra Hydro Folate Reductase), ולכן אין מקום לבדיקות אלו במסגרת בירור סיבוכי היריון
• הטיפול ברמות הומוציסטאין גבוהות הוא בחומצה פולית במינון גבוה [5 מיליגרם (מ"ג) ליום] ללא קשר להיריון או לסוג המוטציה ל-MTHFR, ובתנאי שרמת B12 בנסיוב תקינה
• לכל הנשים עם ארוע VTE בעברן ו/או טרומבופיליה בסיכון גבוה שתוגדר בהמשך ו/או נוכחות גורמי סיכון ל-VTE מומלץ על גרביים אלסטיות בתקופת ההיריון, במהלך הלידה ובתקופת משכב הלידה
• מועד תחילת הטיפול האנטיקואגולנטי לאחר הלידה ביחס לסוג האלחוש וכן המעבר בין טיפול ב-LMWH ל-VKA יהיה על פי המפורט בהמשך (ראה טרומבופרופילקסיס סביב ולאחר הלידה)
בשיקולים למידת הצורך בטיפול/מניעה של VTE ושל סיבוכי היריון יש להתייחס לסוג הטרומבופיליה
סוגי הטרומבופיליה
טרומבופיליה גנטית (מולדת)
טרומבופיליה בסיכון גבוה
- הומוזיגוטיות ל-Factor V Leiden
- הומוזיגוטיות ל-Factor II Mutation 20210
- Antithrombin deficiency
- טרומבופיליה גנטית משולבת (Combined thrombophilia) – שילוב של הטרוזיגוטיות ל-Factor V Leiden ול-Factor II mutation, או כל שילוב של שני סוגי טרומבופיליה ויותר
טרומבופיליה בסיכון נמוך
- הטרוזיגוטיות ל-Factor V Leiden
- הטרוזיגוטיות ל-Factor II Mutation 20210
- Protein C deficiency[1]
- Protein S deficiency[1]
טרומבופיליה נרכשת – APLA (Anti-Phospholipid Antibodies)
קריטריונים קליניים
- ארוע טרומבוטי עורקי/ורידי/כלי דם קטנים בכל רקמה שהיא, אשר הוכח באמצעי הדמייה או היסטולוגית
- סיבוכי היריון – לפחות אחד מהבאים:
- 3 הפלות ספונטניות רצופות לפני שבוע 10 להיריון לאחר שלילת סיבה אימהית (אנטומית, הורמונלית או גנטית) או אבהית (גנטית)
- הפלה אחת או יותר של עובר בעל מורפולוגיה תקינה בסונאר או בפתולוגיה, המתאים בגודלו לשבוע 10 להיריון ויותר, לאחר שלילת סיבה אימהית (גנטית או אנטומית) או אבהית (גנטית)
- לידה מוקדמת, בעיקר כאשר יש צורך ביילוד בגין אקלמפסיה ו/או רעלת היריון חמורה ו/או ממצאים המתאימים לאי ספיקה שליתית, כולל האטה בגדילה תוך רחמית, בעובר תקין מורפולוגית מתחת לשבוע 34 להיריון
קריטריונים מעבדתיים
- LAC (Lupus anticoagulant) חיובי בשתי בדיקות בהפרש של לפחות 12 שבועות. יש לבצע את הבדיקה ללא נטילת Coumadin (Warfarin sodium)
- ACL (Anticardiolipin antibody) מסוג IgG או IgM בכייל בינוני-גבוה (מעל 40 GPL או MPL, מעל אחוזון 99) בשתי בדיקות בהפרש של לפחות 12 שבועות
- B2GP1 (1 anti-β2-glycoprotein) מסוג IgG או IgM בטיטר בינוני-גבוה (מעל אחוזון 99) בשתי בדיקות בהפרש של לפחות 12 שבועות
- יש להבדיל בין
- APLA מעבדתית – לפחות קריטריון מעבדתי אחד ללא תמונה קלינית
- תסמונת APLA – שילוב של לפחות קריטריון אחד קליני ואחד מעבדתי
בירור טרומבופיליה
יש להציע בירור טרומבופיליה ל:
- טרומבופיליה גנטית:
- נשים עם ארוע קודם של VTE
- נשים עם קרוב משפחה בדרגה ראשונה נשא לטרומבופיליה בסיכון גבוה או שעבר אירוע VTE מתחת לגיל 50 שנה בהעדר גורם סיכון אחר כגון: גיל מבוגר, השמנת יתר, קרוב עם טרומבופיליה בסיכון נמוך וכדומה
- קיימת מחלוקת לגבי צורך בבירור סיבוכי היריון
- טרומבופיליה נרכשת (APLA): לבירור VTE וסיבוכי היריון
תרופות אנטיקואגולנטיות בשימוש למניעה וטיפול
- LMWH – הפרינים במשקל מולקולרי נמוך [לדוגמא: Clexane (Enoxaparin sodium), Fragmin (Dalteparin sodium)]. במידה ויש התווית נגד – קיים טיפול חלופי. במידה ומופיע דימום חריף תחת טיפול יש לתת מנות דם (כדוריות דחוסות) להרה ולבדוק רמת Anti-Xa
- UFH - Unfractionated Heparin - הפרין במשקל מולקולרי גבוה, יינתן רק בהתוויה מיוחדת ובעיקר במסתם תותב (ראה פירוט בהמשך)
- VKA - Vitamin K Antagonist – אנטגוניסטים לויטמין K. תרופת הבחירה הינה Coumadin. במידה ומופיע דימום חריף תחת טיפול יש לתת FFP (Fresh Frozen Plasma) עם או ללא ויטמין K ועירויי דם על פי צורך קליני
טווח מינוני טיפול מקובלים של LMWH
| Enoxaparin (clexane) [2] | |
| Prophylactic dose | SC40 mgxl/d [3] |
| Intermediate dose | SC40 mgx2/d or lmg/kg once a day |
| Adjusted-dose | SC lmg/kg >2/d [4] |
תרופות אנטיאגרגנטיות בשימוש למניעה וטיפול
אספירין – תרופה נוגדת איגור טסיות. למתן בהתוויה של תסמונת APLA שביטויה הקליני הינו סיבוך מיילדותי. מומלץ לתת טיפול באספירין לצורך הקטנת הסיכון לרעלת היריון בנשים בסיכון ללא קשר לתסמונת APLA. המינון המקובל: 100-75 מ"ג ליום. במידה ומתרחש דימום חריף תחת טיפול יש לתת טסיות ותוצרי דם נוספים לפי צורך קליני.
התאמת הטיפול האנטיקואגולנטי על פי קבוצות סיכון
מטופלות נוגדי ויטמין K (Coumadin) באופן קבוע המתכננות היריון (קבוצת סיכון גבוה במיוחד)
- בדיקות תכופות על מנת לוודא היריון מוקדם ככל האפשר
- מרגע אבחון היריון הפסקת טיפול ב-Coumadin והתחלת LMWH במינון טיפולי (Adjusted dose). יש לשקול תוספת מתן של ויטמין K פומי 10 מ"ג על פי בדיקת INR
- לאחר לידה מתבצעת חפיפה בין LMWH לבין VKA. אין התווית נגד להנקה בעת טיפול ב-LMWH או VKA
- במידה ויש APLA: תוספת של אספירין במינון 100-75 מ"ג מגילוי ההיריון ועד בסמוך למועד הלידה לפי מידת הסיכון למאורע טרומבואמבולי
- בנשים בסיכון טרומבואמבולי עורקי גבוה ניתן להמשיך אספירין סביב הלידה עד לחפיפה עם VKA
VTE חד בהיריון
- טיפול ב- Adjusted dose LMWH עד תום תקופת משכב לידה ובתנאי כי טופלה לפחות לתקופה של 3 חודשים מתחילת המאורע. ניתן לעבור ל-VKA לאחר הלידה להשלמת תקופת הטיפול
- לרוב יש להמשיך טיפול אנטיקואגולנטי סביב לידה ללא שינוי
- במקרה ויש התוית נגד לאלחוש איזורי, יינתן אלחוש חליפי על פי המלצת מרדים
נשים הרות עם ארוע VTE בעברן
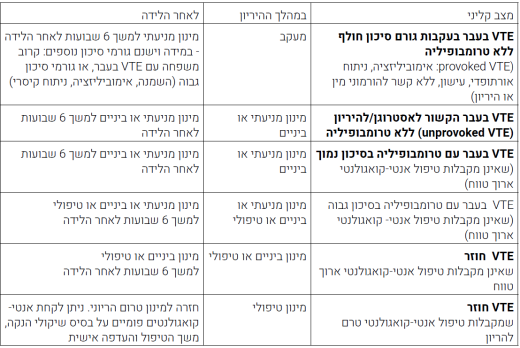
ככלל יש להמליץ על טיפול בתקופת משכב הלידה. יש להתאים את הטיפול פרטנית לכל הרה על פי סוג הטרומבופיליה, סיפור משפחתי, חומרת ארוע קודם וגורמי סיכון נוספים (טבלה מספר 1).
נשים ללא אירוע VTE בעברן עם טרומבופיליה
ככלל יש להמליץ על טיפול מונע בתקופת משכב הלידה. יש להתאים את הטיפול פרטנית לכל הרה על פי סוג הטרומבופיליה, סיפור משפחתי, חומרת ארוע קודם וגורמי סיכון נוספים (טבלה מס' 2).
| Thrombophilia | Antepartum | Postpartum |
| Antithrombin deficiency. Homozygote FVL or Factor II mutation, combined thrombophilia | Prophylactic or Intermediate dose | Prophylactic or Intermediate dose |
| Other thrombophilia | Surveillance/ Prophylactic dose | Surveillance/ Prophylactic dose |
נשים עם סיבוכי היריון בעברן (ללא אירוע טרומבוטי עורקי או ורידי) ו-APLA מעבדתי
| Thrombophilia | Antepartum | Postpartum |
| APLAand history of pregnancy complications | Prophylactic + Aspirin[5] | Prophylactic |
נשים עם סיבוכי היריון בעברן (ללא אירוע טרומבוטי עורקי או ורידי) וטרומבופיליה מולדת
הספרות שנויה במחלוקת לגבי המלצה לטיפול שגרתי מונע ב-LMWH לצורך מניעת סיבוכי היריון עם וללא טרומבופיליה מולדת.
טיפול בנשים עם מסתם לבבי תותב במהלך ההיריון והלידה
ניתן להציע אחת מ-2 האפשריות הבאות:
- LMWH במינון טיפולי (Adjusted dose) המותאם לפי רמות Anti-Xa
- UFH או LMWH במינון טיפולי עד שבוע 13, חפיפה ל-VKA והחלפה ל-UFH או LMWH סמוך ללידה
בנשים עם מסתם תותב הטיפול יישקל אינדיבידואלית בשיתוף קרדיולוג.
יש לשקול את האפשרות הטיפולית המיטבית והצורך בתוספת הטיפול באספירין על פי המלצת קרדיולוג.
ניטור הטיפול: במטופלות ב-VKA - INR רצוי 3.0-2.0.
במטופלות ב-LMWH יש לעקוב אחר רמות Anti-Xa, כאשר בזמן הטיפול רמות בדם רצויות הן בין 1.2-0.7 יחידות/מ"ל. רמה בדם נקבעת על ידי בדיקת דם המתבצעת שעה טרם מתן המנה המתוכננת הבאה (רמת שפל).
הכנה לביצוע דיקור מי שפיר/סיסי שליה
- אין בספרות מידע מספק לגבי הצורך בהפסקת טיפול באספירין ומועד חידושו
- הפסקת LMWH במינון מניעתי 12 שעות לפני פעולה
- הפסקת LMWH במינון טיפולי 24 שעות לפני פעולה
- ניתן לחדש טיפול ב-LMWH 24-12 שעות לאחר פעולה באם אין דמם משמעותי
התוויות נגד לטיפול LMWH
HIT (Heparin Induced Thrombocytopenia) בעבר, דמם פעיל, כיב פפטי פעיל, טסיות מתחת ל-30,000 לממ"ק, יתר לחץ דם לא נשלט, תפקודי קרישה מופרעים, מחלת דמם מולדת, טיפול קבוע ב-VKA, אי ספיקת כליות קשה (פינוי קראטינין מתחת ל-30 מ"ל לדקה) ורגישות עורית.
הנקה
- אין מניעה מהנקה בעת טיפול ב-VKA, LMWH, ORGARAN או UFH
- חל איסור להניק תוך טיפול בפנטסכרידים [Arixtra (Fondaparinux sodium)]
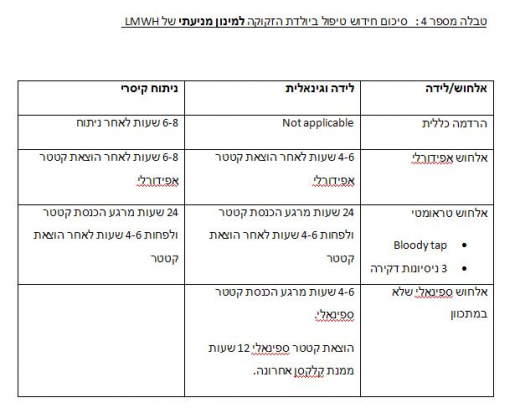
מניעה וטיפול ב-VTE סביב ולאחר הלידה
- טיפול אנטיקואגולנטי לאחר לידה בנשים ללא אירוע VTE בעברן וללא טרומבופיליה
ככלל, הטיפול האנטיקואגולנטי יינתן על פי גורמי סיכון (סיכון גבוה ונמוך) 12-8 שעות לאחר ניתוח קיסרי ו-6-4 שעות לאחר לידה רגילה.
ינתן טיפול ב-LMWH במינון מונע (Prophylactic dose) בנוכחות גורם סיכון גבוה אחד או יותר, או 2 גורמי סיכון נמוך או יותר. טווח הטיפול המונע יקבע באופן פרטני לפי מידת הסיכון ל-VTE וינוע ממוביליזציה מלאה ועד ל-6 שבועות לאחר הלידה.
שימוש בגרביים אלסטיות או IPC (Intermitted Pneumatic Compression) מוצע כאלטרנטיבה בעיקר כשיש הוראת נגד לטיפול תרופתי.
- גורמי סיכון גבוה
- אימוביליזציה (ריתוק למיטה במשך שבוע או יותר בתקופה שקדמה ללידה)
- רעלת היריון חמורה
- מחלה כרונית כגון: מחלת לב, SLE (Systemic Lupus Erythematosus), מחלת כליה כרונית או מחלת מעי דלקתית (IBD, Inflammatory Bowel Disease) פעילה
- Puerperal infection
- ניתוח קיסרי בסיכון (כגון: מתוך לידה ממושכת, חום בלידה וניתוח בהול)
- גורמי סיכון נמוך
- השמנת יתר (BMI מעל 30 ק"ג/מטר^2)
- גיל אם מבוגר (>35)
- עישון מעל 10 סיגריות ליום
- דליות משמעותיות בעיקר מעל גובה הברך
- Superficial vein thrombosis
- יילודה >3 לידות
- היריון מרובה עוברים
החדרת קטטר אפידורלי/ספינאלי
- יבוצע לפחות 12 שעות לאחר מתן מנה אחרונה של LMWH במינון מניעתי
- יבוצע לפחות 24 שעות לאחר מתן מנה אחרונה של LMWH במינון טיפולי
- אין מניעה לביצוע במהלך טיפול באספירין במינון נמוך
חפיפה ל-Coumadin
- מומלץ ביצוע חפיפה בין LMWH ל-VKA בהקדם אפשרי
- אין מניעה ממתן VKA מיד עם מתן LMWH לאחר לידה
- המינון הראשוני של VKA יהיה על פי המינון האחרון בו טופלה האישה טרם ההיריון
- יש לטפל במקביל ב-LMWH עד INR>2 בשתי בדיקות רצופות בהפרש של יממה
- תחילת האיזון יכולה להתבצע באשפוז והמשך איזון מלא במסגרת אמבולטורית
חברי הצוות להכנת נייר עמדה
- פרופ' קובי בר- יו"ר החברה לרפואת האם והעובר, מרכז רפואי וולפסון, חולון
- פרופ' יריב יוגב- מנהל חדרי לידה, מרכז רפואי רבין, פתח תקווה
- ד"ר דורית בליקשטיין- מנהלת שירות המטוגינקולוגי, מרכז רפואי רבין, פתח תקווה
- ד"ר רינת גבאי- אגף נשים, מרכז רפואי רבין, פתח תקווה
ושאר חברי הועד:
- ד"ר יורי פרליץ- מנהל יחידת רפואת אם-עובר, מרכז רפואי ע"ש ברוך פדה, פוריה, טבריה
- ד"ר מיכל קובו- מנהלת מחלקת יולדות, מרכז רפואי אדית וולפסון, חולון
- פרופ' סורינה גריסרו-גרנובסקי- אחראית אגף מיילדותי, מרכז רפואי שערי צדק, ירושלים
- ד"ר אלי גוטרמן- מנהל שירות מחוזי להיריון בסיכון גבוה, מחוז חיפה, בית חולים כרמל, שירותי בריאות כללית
- פרופ' אייל ענתבי- מנהל אגף נשים ויולדות, מרכז רפואי ברזילי, אשקלון
ביבליוגרפיה
- CHEST 2012, 141;e691S-e736S (Level III) R
- RCOG Green-top guideline no.37, November 2009 (Level III) A
- ACOG Practice Bulletin, Obstet Gynecol, 2011, 118, 730-740 (Level III) A
- ACOG Practice Bulletin, Obstet Gynecol, 2011, 118, 718-729 (Level III) A
- ASRA Practice Advisory, Reg Anesth Pain Med 2010, 35:64-101(Level III) D
הערות שוליים
- ↑ 1.0 1.1 קיימת מחלוקת בספרות לגבי ההשתייכות לדרגת סיכון גבוה או נמוך
- ↑ מינוני הטיפול המקובלים הן לפי התרופה בשימוש הנרחב ביותר בארץ
- ↑ במשקל מעל 100 קילוגרם (ק"ג) – מינון מניעתי SC 60mg X1/d
במשקל מתחת ל 50 ק"ג מינון מניעתי של SC 20mg X1/d - ↑ ניתן לעקוב אחר רמות Anti-Xa במקרים מיוחדים (דמם או טרומבוזיס תוך נטילת Clexane, אי ספיקת כליות, עלית משקל ניכרת). הבדיקה מתבצעת 4 שעות לאחר ההזרקה. רמה טיפולית דרושה היא בין 1-0.5 יחידות/מיליליטר (מ"ל) או עד 0.5 יחידות/מ"ל במינון מניעתי, למעט נשים עם מסתם תותב (ראה בהמשך).
- ↑ טיפול באספירין יינתן מתחילת ההיריון ועד בסמוך למועד, עם אפשרות המשך הטיפול סביב הלידה לפי מידת הסיכון והחלטת הרופא המטפל.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק