הליקובקטר פילורי - Helicobacter pylori
| הליקובקטר פילורי | ||
|---|---|---|
| Helicobacter pylori | ||
| ||
| ICD-9 | 041.86 | |
| MeSH | D016481 | |
| יוצר הערך | ד"ר מיקי דובלין (2010), עודכן ב-2025 על ידי ד"ר ליאור זורניצקי. | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – הליקובקטר פילורי
מבוא
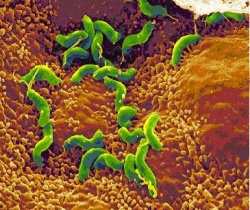
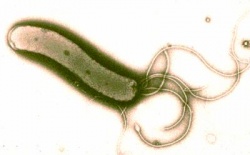
הליקובקטר פילורי (Helicobacter pylori), חיידק גרם שלילי, התגלה לראשונה באוסטרליה בשנת 1982 על ידי Professor Barry Marshall ו-Doctor Robin Warren. שמו, כפי שניתן לו על ידם, היה "Campylobacter pylori".
לחיידק זה יתרון התפתחותי ניכר על חיידקים אחרים במערכת העיכול, ומכאן פגיעתו הקשה. בניגוד לחיידקים אחרים, הוא בקיבה, יוצר סביבו תגובה דלקתית וגורם לפגיעה בתאי הקיבה מסביב. כתוצאה מכך התאים נפגעים ומסולקים על ידי תאי דלקת - דבר היכול ליצור נגע הולך וגדל. התהליך הדלקתי גורם למעשה לפצע בקיבה שהולך וגדל, Ulcer (אולקוס), ובעברית: "כיב". רוב הכיבים נרפאים מעצמם, אך כמו בכל פצע נוצרת הצטלקות הגורמת לנזק במבנה מערכת העיכול, ובמיוחד בתריסריון – שינויי צורה בתריסריון גורמים לתופעות קשות אותן אנו חשים כצרבת קשה. חלק מהכיבים אף עלולים להתנקב ולגרום למוות. דלקת כרונית של הקיבה יכולה לגרום (בצירוף של גורמים נוספים) לסרטן הקיבה.
כ-10 שנים לאחר גילויו של החיידק וכאשר הובנו פגיעותיו הרבות, נוצר צורך בהשמדתו, ואז שונה שמו ל-Helicobacter pylori. הטיפול המשולב בחיידק זה הוא יעיל מאוד, ואכן מונע היווצרות כיבים ומוריד בצורה ניכרת את שכיחות ההופעה של סרטן הקיבה. על התגלית שהובילה בסופו של דבר לריפוי קבוע של כיב פפטי על ידי מיגור החיידק, זכו Marshall ו-Warren בפרס נובל לפיזיולוגיה או לרפואה בשנת 2005.
אפידמיולוגיה
החיידק שכיח מאוד באוכלוסייה ובמיוחד בגיל המבוגר. בקרב מבוגרים ברוב חלקי ארצות הברית, אירופה ואוקיאניה שכיחותו קטנה מ-30 אחוזים, לעומת יותר מ-60 אחוזים בחלקים רבים של אפריקה, דרום אמריקה ומערב אסיה. בארצות הברית, השכיחות משתנה עם הגיל: עד 50 אחוזים מהאנשים בני 60, כ-20 אחוזים מבני ה-30 ופחות מ-10 אחוזים מהילדים. החיידק נרכש בדרך כלל בשנים הראשונות של הילדות. הקשר בין הגילאים נובע בעיקר מהשפעה של מחזור הלידה, לפיה בני 60 בהווה נדבקו יותר כילדים מאשר ילדים בהווה. עם זאת השכיחות בגילאי הילדות הולכת ועולה עם השנים כך שמדי שנה נוספים כ-1 עד 1.5 אחוזים של נשאים בקבוצת גיל זו. אמנם לא כל נשא מפתח מחלה חודרנית של החיידק.
בני אדם הם המאכסן העיקרי של החיידק וההדבקה מתרחשת מאדם לאדם. מקורות הדבקה אחרים כגון מקורות מים, חתולי בית וחרקים הוצעו בספרות אך אמיתותן של תאוריות אילו לא הוכחה עדיין. גורמי הסיכון להדבקות הם: מגורים עם אדם הנושא את החיידק, צפיפות מגורים גדולה, מחייה במדינות מתפתחות ותנאים סוציו-אקונומיים (Socio-economic) ירודים.
לא ברור האם ההדבקה מתרחשת לעיתים קרובות יותר בדרך fecal–oral או בדרך oral–oral. עם זאת, קל יותר לתרבת הליקובקטר פילורי מהקאות ומריפלוקס קיבה-ושט מאשר מצואה. כמו כן, יודעים שאם החיידק מדביק את אחד מבני המשפחה, במקרים רבים נמצא חיידק זה גם בשאר בני הבית. בתנאי היגיינה לקויה ההדבקה תהייה מהירה יותר בין בני הבית, אך לא נמצא קשר בין הדבקת כל בני הבית להתפתחות מחלה חודרנית. במקרים בהם כן מתפתחת מחלה חודרנית באחד מבני הבית נמצא בדרך כלל התפתחות כיבים בשאר בני המשפחה.
שכיחות החיידק בקרב אנשים שיש להם כיב בתריסריון היא גבוהה מאוד. החיידק נמצא ב-95 עד-99 אחוזים מהסובלים ממחלה חודרנית. כמו כן, החיידק נמצא בכ- 90 אחוזים מהאנשים שיש להם תסמינים קליניים של כיב קיבה. עד לגילוי החיידק והקשר שלו לכיב קיבה ותריסריון, הישנויות של הכיב לאחר הטיפול היו מאוד שכיחות. לאחר הכחדת החיידק, מספר ההישנויות פחת ב-85 אחוזים. החיידק לא גורם לכיב בעצמו, אלא מחיש את התהליך שנגרם מחומציות הקיבה ומהאנזימים בקיבה.
פתוגנזה
Helicobacter pylori שהגיע לקיבה יכול לעבור קולוניזציה (התיישבות) בדופן הקיבה, ולשם כך הוא נעזר בארבע תכונות ייחודיות: פעילות האנזים Urease, Flagella, המבנה המיוחד של החיידק ו-Adhesins. ה-Urease, שמפרק Urea ליוני (Ions) Ammonia, מנטרל את הסביבה החומצית של הקיבה ומאפשר לחיידק לשרוד ולהתרבות בחלל הקיבה. צורתו המיוחדת של ה-Helicobacter pylori יחד עם ה-Flagella שלו מקנים לו תנועתיות, וזו אחראית במידה רבה על יכולתו לחדור את שכבת ה-Mucin בדופן הקיבה.
ההידבקות של החיידק אל תאי האפיתל שבדופן הקיבה מתבצעת על ידי כ-20 צמתנים (פקטורי הדבקה) שונים. הקשר עם ה-Mucin של הקיבה נוצר על ידי היצמדות לחומצה סיאלית. החיידק מכיל לפחות שישה סוגים של צמתנים לחומצה סיאלית (Sialic acid), ובנוסף לכך ישנם חלבונים נוספים שנמצאים על פני התא של החיידק שיכולים גם כן להשתתף בתהליך ההתיישבות. בהמשך, החיידק משחרר אנטיגנים (Antigens) שמושכים תאים מסוג PolyMorphoNuclears) PMN) והתאים האפיתליאליים מפרישים Ilnterleukin 8 (IL-8) ו-Chemokines אחרים שתורמים למשיכת PMN.
בהמשך התהליך, תאים מציגי אנטיגנים כמו Macrophages, מציגים אנטיגנים של החיידק לתאים באיברים לימפטיים (Lymphatic), דבר הגורם לשפעול ומשיכה של תאי Plasma ולימפוציטים (Lympocytes) מסוג B ו-T לאזור הדלקת. בשלב זה החיידק מקבל את צורתו הכדורית בתנאים האנאירוביים (Anaerobic) של המעי הדק, ועובר בליעה פעילה על ידי תאים Dendritic שב-Peyer's patches שבמעי הדק. זהו כנראה האתר בו מתרחש שפעול של תאי T ייחודיים מסוג CD4+ על ידי אנטיגנים של Helicobacter pylori.
גורמי סיכון גנטיים וסביבתיים
פולימורפיזם גנטי המוביל להפעלה מוגברת של התגובה החיסונית המולדת כולל שינויים בגנים של ציטוקינים ובגנים המקודדים לחלבוני זיהוי חיידקים (TLR). לדוגמה, אנשים שעברו קולוניזציה ולהם פולימורפיזם בגן ל-IL-1 שמגביר את ייצור הציטוקין הזה בתגובה לזיהום Helicobacter pylori, נמצאים בסיכון מוגבר לאדנוקרצינומה בקיבה.
גורמים סביבתיים חשובים גם הם בפתוגנזה. למשל עישון מגביר את הסיכונים לכיבים בתריסריון ולסרטן קיבה בנשאים של Helicobacter pylori. בנוסף, דיאטות עשירות במלח ומזונות משומרים מגבירים את הסיכון לסרטן, בעוד שדיאטות עשירות בנוגדי חמצון וויטמין C מגנות במידה מסוימת.
קליניקה
למעשה, לכל נשאי Helicobacter pylori יש דלקת קיבה היסטולוגית, אך רק כ-10 עד 15 אחוזים מפתחים מחלות נלוות כגון כיב פפטי, אדנוקרצינומה או לימפומה של הקיבה. למרות שיעורים דומים של קולוניזציה, שיעורי המחלות הללו בקרב נשים הם פחות ממחצית מאלו שבקרב גברים.
רוב החולים סובלים מתסמינים של מערכת העיכול העליונה אך יש להם תוצאות תקינות באנדוסקופיה של מערכת העיכול העליונה. התלונה העיקרית בדרך כלל היא על צריבה ושריפה באזור הוושט, שמחמירה לאחר ארוחות גדולות ושכיבה במאוזן לאחר האוכל. הצרבות נגרמות בעקבות עלייה של מיצי חומצה לוושט, ובדרך כלל הן מפריעות עד מאוד. לעיתים דומה התחושה ללחץ בבית החזה המרכזי מה שיכול לדמות כאב תעוקתי.
לא הוכח קשר סיבתי בין זיהום בחיידק לבין הופעת צרבת, ובמקרים רבים אף נמצא כי באנשים הסובלים מצרבת נמצאה שכיחות נמוכה יותר של זיהום בחיידק לעומת אנשים שאינם סובלים מצרבת. באנשים עם משקל עודף שסובלים מ-Reflux ושטי-קיבתי, יהיו תופעות זהות של צרבת ללא כל זיהום עם Helicobacter pylori.
Functional Dyspepsia הוא מצב שבו קיימים תסמינים של כאבי בטן חוזרים עם הרגשת אי נוחות בבטן. יכולים להתלוות לכך גם בחילה, תפיחות בטנית, הרגשת שובע מוקדם וחוסר תיאבון, ולעיתים אף הרגשת סלידה מאוכל. לפעמים הכאבים דומים לאלו שנגרמים בעקבות כיב קיבה, אך בניגוד לכאבי כיב הקיבה, בכאבים אלו לא מוצאים שום כיב ולא כל פתולוגיה או מחלה אחרת הנראית לעין, לא בקיבה ולא בכל שאר חלקי מערכת העיכול. תופעה זו שכיחה מאד, ויוחסה בחלקה גם לזיהום של הקיבה ב-Helicobacter pylori. במחקר אקראי גדול, הודגם שבהכחדת החיידק יש השפעה חיובית מועטה ביותר על התלונות, כך שהוא אינו הגורם העיקרי לתופעת ה-Dyspepsia. (25 אחוזים מהנבדקים חשו הטבה לאחר הכחדת החיידק, לעומת 7 עד 21 אחוזים מהנבדקים שחשו הטבה לאחר טיפול ב-Omeprazole בלבד). המסקנה היא שכנראה המקור ל-Dyspepsia הוא Reflux ושטי-קיבתי.
ל-Helicobacter pylori תפקיד מוכר בפתולוגיות קיבה אחרות. הוא עלול לגרום בחולים מסוימים למחסור בברזל באמצעות איבוד דם סמוי ו/או היפוכלורידריה (מצב בו תאי הקיבה אינם מייצרים מספיק חומצה) וספיגה מופחתת של ברזל. בנוסף, מספר פתולוגיות מחוץ למערכת העיכול נקשרו עם קולוניזציה של החיידק, אם כי העדויות לסיבתיות פחות חזקות.
מחקרים על טיפול ב-Helicobacter pylori ב-ITP (idiopathic thrombocytopenic purpura) תיארו באופן עקבי שיפור או אפילו נורמליזציה של ספירת הטסיות. קשרים פוטנציאליים אך שנויים במחלוקת אף יותר הם עם מחלת לב איסכמית ומחלות כלי דם במוח. מספר הולך וגדל של מחקרים הראו קשר הפוך של cagA+ H. pylori עם אסתמה בילדות, קדחת השחת והפרעות אטופיות. הקשרים הללו הוכחו כסיבתיים במודלים של בעלי חיים, אך גודל ההשפעה בבני אדם טרם הוכח.
הנזקים לקיבה
Atrophic gastritis היא ביטוי היסטולוגי למצב בו רואים את רירית הקיבה במצב של Gastritis (דלקת כרונית) Atrophic תחת המיקרוסקופ. הממצאים כוללים תמונה של דלקת כרונית של הרירית והיעלמות של הבלוטות המפרישות את החומצה ברירית, שנמצאות שם בדרך כלל. Atrophic gastritis מאוד שכיחה לאחר שימוש כרוני (במשך שנים) בתרופות המפחיתות את יצירת החומצה בקיבה, כדוגמת Omeprazole, וכן יכולה להיגרם גם על ידי יצירת נוגדנים עצמוניים שהגוף מפריש כנגד רירית הקיבה.
אבחנה
השיטות לאבחנה של Helicobacter pylori מסווגות לשיטות פולשניות ולא פולשניות, כל אחת עם רגישות, ספציפיות ויישומים קליניים משתנים.
שיטות פולשניות - מבוססות על ביופסיה
בדיקת אוראז מהירה (RUT) - מבוססת על פעילותו של אנזים ה-Urease שבחיידק המפרק Urea, ויוצר Ammonia ו-Bicarbonate שמשנים את ה-PH של ערכת (Kit) הבדיקה ובעקבות כך משתנה צבע ה-Kit שמהווה סמן לנוכחות החיידק. למרות שמדובר בבדיקה אמינה, רגישה וספציפית, השימוש הרב באנטיביוטיקה ובסותרי חומצה מקבוצת PPI (Proton Pump Inhibitor) גרם לכך שישנו אחוז גבוה של False negative בקבוצת חולים זו. ההתפלגות הלא אחידה של החיידק בקיבה ונוכחות Intestinal metaplasia, מקטינים עוד יותר את מהימנות הבדיקה, ולכן יש צורך בהפסקת PPI למשך שבועיים וכן הפסקת אנטיביוטיקה או תרופות מקבוצת Bismuth כ- 4 שבועות לפני בדיקת מבחן Urease. אם תרופות אלו לא הופסקו מומלץ לקחת במקום - או בתוספת לבדיקת Urease מהיר - גם ביופסיות (Biopsies) לבדיקה היסטולוגית לגילוי נוכחות של Helicobacter pylori.
בדיקה היסטולוגית היא גם מדויקת, בתנאי שנעשה שימוש בצביעה מיוחדת (למשל: modified Giemsa, silver או immuno-stain) המאפשרת הדמיה מיטבית של החיידק. אם מתקבלות דגימות ביופסיה הן מהאנטרום והן מהקורפוס, הבדיקה ההיסטולוגית תספק מידע נוסף, כולל מידת ודפוס הדלקת ונוכחות של אטרופיה, מטפלזיה או דיספלזיה.
תרבית מיקרוביולוגית היא ספציפית ביותר אך עשויה להיות חסרת רגישות בגלל קושי בבידוד החיידק. לאחר תרבות החיידק, ניתן לאשר את זהותו על ידי המראה האופייני שלו בצביעת גראם והתגובות החיוביות שלו בבדיקות אוקסידאז, קטלאז ואוריאה. יתרה מכך, ניתן לקבוע את רגישותו של האורגניזם לאנטיביוטיקה, ומידע זה יכול להיות שימושי קלינית במקרים קשים.
שיטות לא פולשניות
הבדיקה הוותיקה ביותר היא בדיקת הנשיפה, בבדיקה פשוטה זו, המטופל שותה תמיסה של אוריאה המסומנת באיזוטופ C13 (אינו רדיואקטיבי) ולאחר מכן נושף לתוך מבחנה. אם האנזים urease קיים, האוריאה עוברת הידרוליזה, ופחמן דו-חמצני מסומן מתגלה בדגימות נשימה.
בדיקת אנטיגן (Antigen) בצואה, בדיקה פשוטה ומדויקת באמצעות נוגדנים חד שבטיים ספציפיים לאנטיגנים של החיידק, נוחה יותר ופחות יקרה מבדיקת הנשיפה, אך חלק מהמטופלים סולדים מדגימת צואה.
שתי השיטות הללו אמינות גם לשם גילוי החיידק וגם לווידוא השמדת החיידק. מאחר שגם בבדיקות אלו שימוש באנטיביוטיקה וב-PPI יכולים להביא לתוצאות שליליות כוזבות, הרי שמומלץ להפסיק PPI (Losec, Controloc) כשבועיים לפני הבדיקה ואנטיביוטיקה ו-Bismuth כ-4 שבועות לפני הבדיקה. נראה שההשפעה של סותרי חומצה שלא מקבוצת PPI על מהימנות בדיקות אלו פחותה הרבה יותר, אך בכל אופן מומלץ להפסיקן 24 עד 48 שעות לפני הבדיקה.
בדיקת נוגדנים לחיידק - נוכחות נוגדנים נבדקת בבדיקת דם פשוטה, עם רגישות גבוהה. אמנם, המצאות נוגדנים בדם אינה מעידה על המצאות מחלה פעילה אלא רק על חשיפה לחיידק בזמן כלשהו במהלך החיים. לכן, תשובה שלילית שוללת כמעט לחלוטין המצאות או חשיפה ל-Helicobacter pylori. תשובה חיובית אינה משמעותית מבחינה טיפולית.
יש לבדוק:
- אנשים שלהם יש קרוב משפחה מדרגה ראשונה שחלה בסרטן קיבה/Lymphoma של הקיבה
- אנשים שחלו בעבר או כעת בכיב תריסריון או קיבה וטרם נבדקו
- אנשים המטופלים לאורך שנים בתרופות המדכאות את יצירת חומציות הקיבה, כגון Omepradex או Losec
- אנשים הסובלים מחוסר כרוני בוויטמין Vitamin) B12)
- אנשים הסובלים מתופעות של Dyspepsia
יש לחזור על הבדיקות לאחר סיום הטיפול התרופתי. מומלץ לוודא חיסול מלא של החיידק אצל כל החולים שטופלו. מומלץ לוודא השמדה מלאה אצל חולים עם כיב פפטי, חולים דיספפטיים (Dyspeptic) שממשיכים להיות תסמיניים למרות הטיפול, בחולים עם Lymphoma של הקיבה ובחולים שעברו כריתת קיבה בגלל Carcinoma.
טיפול
יש לטפל:
התשובה לשאלה זו מורכבת ואינה אחידה. מאחר שמדובר בחיידק שתואר כגורם לסרטן עוד בשנת 1994, הרי שישנם עדיין הסבורים כי כדאי לבדוק את כל האוכלוסייה ולבצע אירדיקציה מלאה אצל כל אלו שנמצאו חיוביים. גישה מחמירה זו אינה מקובלת, וההמלצה המקובלת היא לבדוק ולטפל בחיידק זה רק את החולים הסובלים מהאבחנות הבאות:
- כיב פפטי מוכח בתריסריון או בקיבה (פעיל או בעבר)
- לימפומה MALT של תאי B
- Functional dyspepsia
- היסטוריה משפחתית של סרטן קיבה - קרובים מדרגה ראשונה
- חולים דיספפטיים מבוגרים עם ירידה במשקל
- Atrophic gastritis
- לאחר ניתוח משני לסרטן קיבה
- שימוש ממושך ב-PPI
- שימוש ממושך ב-Nonsteroidal anti-inflammatory drugs) NSAIDs)
- אנמיה מחסר ברזל או מחסר ויטמין B12 מסיבה לא ידועה
- Idiopathic Thrombocytopenic Purpura) ITP)
- חולים עם Helicobacter pylori, ללא קשר להתוויה שבגינה נבדקו, וזאת לאחר התייעצות עם הרופא המטפל
טיפול תרופתי
למרות ש-Helicobacter pylori רגיש למגוון רחב של אנטיביוטיקות במבחנה, מונותרפיה אינה מצליחה בדרך כלל, כנראה בגלל אספקת אנטיביוטיקה פעילה לא מספקת לאזור הקולוניזציה. כישלון קליני של מונותרפיה גרם להתפתחות של משטרי טיפול עם מספר תרופות. המשטרים הנוכחיים מורכבים מ-PPI ושניים או שלושה תרופות אנטי-מיקרוביאליות הניתנות למשך 10 עד 14 ימים.
טיפול מוצלח תלוי בעיקר במטופל תוך הקפדה על משטר הטיפול ושימוש באנטיביוטיקה יעילה נגד הזן הספציפי. ההקפדה על משטר הטיפול היא קריטית מכיוון שגם הפסקות קלות עלולות להוביל לכישלון הטיפול ולעמידות לאנטיביוטיקה.
החיידק עמיד לטיפולים אנטיביוטיים, ולכן הטיפול הראשוני הוא טיפול משולש הכולל PPI, Clarithromycin ו-Amoxicillin או Metronidazole למשך 14 ימים. בגלל אחוזי העמידות הגבוהים יותר ל-Metronidazole (37 עד 25 אחוזים) העדיפות היא ל-Clarithromycin (עמידות: 13 עד 10 אחוזים). לחלופין, ניתן לטפל בטיפול מרובע הכולל PPI, Bismuth, Tetracycline ו-Metronidazole למשך 10 עד 14 ימים. טיפול רציף (Sequential therapy) שתוצאות הארדיקציה שלו טובות יותר מאשר הטיפול המשולש, כולל Amoxicillin ו-PPI למשך 5 ימים שבהמשכו החולה מקבל Clarithromycin, Tinidazole ו-PPI ל-5 ימים נוספים. טיפול זה יכול לשמש כטיפול ראשוני. הוויכוח לגבי משך הטיפול המשולש לא בא על פתרונו גם בהמלצות הנוכחיות. קבוצת Maastricht מציינת אף היא שהטיפול במשך 14 ימים יעיל בקרב 7 אחוזים ועד 17 אחוזים יותר מאשר טיפול של 7 ימים. עם זאת ההבדל בין טיפול למשך 10 ימים לעומת שבועיים אינו מובהק. לא משנה באיזה משטר אנטיביוטי נעשה שימוש, מטא-אנליזות מראות ששימוש במינונים גבוהים ולא מתונים של PPI עם האנטיביוטיקה מגביר את יעילות הטיפול. בישראל רופאים רבים נוקטים בפשרה ומטפלים במשך 10 ימים.
הטיפול המומלץ לחולה שנכשל בטיפול המשולש
טעות נפוצה היא לחזור על הטיפול המשולש הלא יעיל ויש להימנע מכך. הטיפול המומלץ במקרים אלו הוא טיפול מרובע על בסיס Bismuth בתוספת PPI ושתי אנטיביוטיקות שלא נרשמו בטיפול המשולש הקודם. משך הטיפול המועדף הוא בין 7 עד 14 ימים.
פורסמו עבודות אודות שילובים שונים במטרה למצוא טיפול קל ויעיל יותר מאשר הטיפול המרובע. בין הטיפולים הללו שניים נראים כמבטיחים יותר:
- שילוב של Levofloxacin עם Amoxicillin ו-PPI. המינון המומלץ של ה-Levofloxacin ומשך הטיפול משתנה בעבודות שפורסמו ונע בין 500 מיליגרם ליום ל-1000 מיליגרם ליום למשך 7 עד 10 ימים. שתי עבודות סקירה שפורסמו ב-2006 הראו שטיפול משולש הכולל Levofloxacin כקו טיפול שני, יעיל יותר מהטיפול המרובע עם פחות תופעות לוואי
- Rifabutin עם Amoxicillin ו-PPI. Rifabutin היא אנטיביוטיקה שימושית בשחפת, וניתנת במינון של 150 מיליגרם ליום פעמיים ביום. תופעות הלוואי העיקריות שלה הן פריחה, תופעות במערכת העיכול כמו בחילה, דיספפסיה, הקאות ושלשול.
Helicobacter pylori ופרוביוטיקה
הרציונל להוסיף פרוביוטיקה (Probiotic) לטיפול ב-Helicobacter pylori. נבע משני טעמים: ראשית כדי להעלות את אחוזי האירדיקציה, ושנית כדי להפחית תופעות לוואי הקשורות בטיפול האנטיביוטי. כבר בתחילת שנות האלפיים פורסמו עבודות על ההשפעה האנטימיקרוביאלית (Antimicrobial) הטובה של זני חיידקים פרוביוטיים מסוימים, כמו זני Lactobacillus, על ההחלמה מ-Helicobacter pylori. אם כי ברור שטיפול פרוביוטי לבדו אינו יכול להביא לארדיקציה מלאה של החיידק.
בסקירה גדולה שפורסמה על ידי Tong ועמיתיו על ההשפעה של פרוביוטיקה בארדיקציה של Helicobacter pylori, נמצא שתוספת פרוביוטיקה יכולה לשפר אחוזי ארדיקציה (83.6 אחוזים לעומת 74.8 אחוזים) וכן להפחית תופעות לוואי - בעיקר בהפחתת שלשולים בצורה משמעותית (24.7 אחוזים לעומת 38.5 אחוזים).
במטא-אנליזה שפורסמה על ידי Yue Wang בשנת 2023, התוצאות, שנגזרו מ-34 מחקרים הצביעו על כך שרוב הטיפולים המשופרים בפרוביוטיקה עלו על הטיפול המשולש הסטנדרטי בלבד. טיפול עם שילוב של Bifidobacterium-Lactobacillus ו-Bifidobacterium-Lactobacillus-Saccharomyces היו יעילים במיוחד, והשיגו שיעורי ארדיקציה של 78.3 אחוזים ו-88.2אחוזים , בהתאמה, תוך מזעור תופעות הלוואי.
מניעה
חיסון נחשב לשיטת המניעה הפשוטה ביותר, ניסויים בבעלי חיים הראו הבטחה, וניסויים ראשוניים בבני אדם מצביעים על יעילות מסוימת, עם מחקרים נוספים שעדיין נמצאים בעבודה. עם זאת, מניעת קולוניזציה של Helicobacter pylori עשויה להוות סכנה ביולוגית וקלינית בשל האבולוציה הארוכה והמשותפת שלו עם בני אדם. לדוגמה, העדר קולוניזציה של Helicobacter pylori יכולה להגביר את הסיכון ל-GERD ולאדנוקרצינומה של הוושט. מיגור החיידק עשוי גם להעלות את הסיכון למחלות אורח חיים מודרניות כמו אסתמה ואלרגיות בילדים, מה שנתמך על ידי מחקרים אפידמיולוגיים וניסויים בבעלי חיים.
פרוגנוזה
Helicobacter pylori וסרטן קיבה:
הדלקת הכרונית הנגרמת על ידי Helicobacter pylori מובילה בסופו של התהליך להתפתחות Adenocarcinoma של הקיבה. תהליך זה עובר דרך מספר שלבים טרום סרטניים הכוללים Atrophic gastritis (נזק ניווני כרוני של רירית הקיבה), Intestinal metaplasia (שינויים בצורת התאים), Dysplasia (שינויים טרום סרטניים) ולבסוף Carcinoma (סרטן) של הקיבה. תהליך זה נמשך עשרות שנים והוא מושפע מגורמים גנטיים (Genetic) וסביבתיים נוספים בנוסף לחיידק זה, הכוללים: עישון, צריכת אלכוהול, מזון עשיר בניטרטים (Nitrates) ומזון מלוח.
מחקרים עדכניים שבחנו את השלבים בהתפתחות סרטן קיבה הגיעו למסקנה שמתוך 100 חולים עם מחלה חודרנית של Helicobacter pylori, כולם יפתחו Gastritis כרונית (דלקת כרונית של רירית הקיבה). השכיחות של השלבים הבאים משתנה בין מחקרים שונים, אך המגמה הכללית נשארת דומה, עם ירידה הדרגתית בשכיחות ככל שהשלב מתקדם יותר.
Correa, שתיאר שרשרת התפתחויות זו עוד לפני עידן ה-Helicobacter pylori, עמד לא פעם בפני השאלה מהו הגורם המתחיל את כל התהליך הזה ומביא ל-Gastritis כרונית. גילוי החיידק בשנת 1982 פתר חידה זו. מהרגע שהייתה הסכמה על שרשרת השלבים המביאה להתפתחותו של סרטן קיבה, נעשו מאמצים גדולים לקבוע מהו שלב ה"אל חזור" - אותו שלב שבו ארדיקציה של ה-Helicobacter pylori לא תוכל עוד להחזיר את הגלגל לאחור ולמנוע התפתחות סרטן קיבה. מקובל שארדיקציה בשלב ה-Atrophic gastritis ולא בשלב מאוחר יותר (Intestinal metaplasia) יכולה למנוע התפתחות סרטן קיבה. אמנם, במספר מחקרים אחרונים נמצא כי ארדיקציה של Helicobacter pylori יכולה לשפר את המטפלזיה של המעי בהשוואה לאינבו או למצב ללא טיפול. למשל, במחקר שנערך במקסיקו על ידי Jaime Alberto ועמיתיו נמצא שיעור נסיגה של 54.3 אחוזים במטפלזיה של המעי שנה לאחר חיסול החיידק באמצעות טיפול משולש סטנדרטי.
Helicobacter pylori נחשב כגורם סיכון משמעותי ביותר בהתפתחות סרטן קיבה ו-Lymphoma מסוג B. בארצות המערב הסיכון לפתח סרטן קיבה שלא באזור ה-Cardia הוא פי 6 עד 8 גדול יותר בקרב החולים עם Helicobacter pylori לעומת אלו ללא החיידק. ממצאים אלו הובילו למחשבה האם ניתן להקטין את השכיחות של סרטן קיבה שלא ב-Cardia על ידי ארדיקציה של החיידק, זאת בעיקר בארצות המזרח ויפן, שם שכיחות סרטן זה גבוהה בצורה משמעותית בהשוואה לארצות המערב. העבודה הגדולה ביותר בנושא זה פורסמה על ידי You ועמיתיו שגייסו מעל 3,000 חולים כדי לענות על שאלה זו. לאחר 7 שנות מעקב, שכיחות סרטן קיבה בקרב החולים שעברו ארדיקציה הייתה 2.4 אחוזים לעומת 1.7 אחוזים אצל אלו שלא עברו ארדיקציה. לאכזבת כולם הבדלים אלו לא היו מובהקים, ולא ניתן להסיק מסקנות פסקניות מעבודה זו ויש צורך בעבודות נוספות עם מעקב ממושך יותר על מנת לראות האם ארדיקציית החיידק אכן תביא לירידה משמעותית בשכיחותה של מחלה קשה זו.
לגבי Lymphoma של הקיבה התוצאות מעודדות יותר. ארדיקציה של החיידק הוא הטיפול הראשון שיש לתת לכל חולה הסובל מ-Lymphoma מסוג B ו-Helicobacter pylori בקיבה. טיפול זה כשלעצמו יכול להביא לריפוי החולה ללא צורך בטיפולים נוספים. פורסם שחולים מסוימים עם Lymphoma של הקיבה הגיבו לטיפול אנטיביוטי גם בהיעדר הוכחה להימצאות של ה-Helicobacter pylori.
המידע שבדף זה נכתב על ידי ד"ר מיקי דובלין, מומחה ברפואת ילדים, עודכן ב-2025 על ידי ד"ר ליאור זורניצקי, רופא במחלקה פנימית ב', המרכז הרפואי איכילוב-תל אביב


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק