סרטן בלוטת התריס - טיפול - Thyroid cancer - treatment
| סרטן בלוטת התריס - טיפול | ||
|---|---|---|
| Thyroid cancer - treatment | ||

| ||
סמל המודעות לסרטן בלוטת התריס
| ||
| שמות נוספים | חידושים בטיפול בסרטן בלוטת התריס | |
| יוצר הערך | ד"ר איל רובינשטוק
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן בלוטת התריס
סרטן בלוטת התריס (Thyroid cancer) הוא הסרטן האנדוקריני (Endocrine) השכיח ביותר, כאשר קצב אבחונו כמעט והוכפל במהלך 20 השנים האחרונות. במקביל לעלייה בשכיחות המחלה, חלו שינויים משמעותיים בטיפול בעקבות התקדמות בהבנת מהלך המחלה, עלייה בהתעניינות בטיפול מותאם אישית וכניסת תרופות חדשות לשימוש. מטרת הטיפול בחולי סרטן בלוטת התריס היא לתת את הטיפול היעיל ביותר תוך צמצום הופעת תופעות הלוואי. בעוד הטיפול המסורתי כלל ניתוח, יוד רדיואקטיבי (Radioactive iodine) ודיכוי הורמון ממריץ בלוטת התריס (TSH ,Thyroid Stimulating Hormone) בכל החולים, בשנים האחרונות משתנה הגישה לטיפול מוכוון סיכון, אשר מצד אחד יביא לטיפול עוצמתי בחולים בסיכון גבוה, ומצד שני ימנע טיפולים מיותרים בחולים בסיכון נמוך. שינויי גישה אלו באים לידי ביטוי בהנחיות איגוד בלוטת התריס האמריקאי (ATA ,American Thyroid Association) מ- 2009, וצפויים להיות בולטים אף יותר בהנחיות הנמצאות בכתיבה בימים אלו. סקירה זו תעסוק בחידושים בטיפול בסרטנים ממוינים של בלוטת התריס מסוגים פפילרי (Papillary) וזקיקי (Follicular).
העלייה בשכיחות המחלה
שכיחות אבחון סרטן בלוטת התריס מוערכת בכ- 48,000 מקרים חדשים בשנה בארצות הברית ו- 500 מקרים חדשים בשנה בישראל, עם קצב עלייה שנתי של כ- 3%. הדעות חלוקות באשר לסיבה לעלייה בשכיחות המחלה בעשורים האחרונים. אין ספק כי השימוש ההולך וגובר בשיטות אבחון משופרות ובאמצעי הדמיה רגישים, בראשם בדיקת על-שמע (Ultrasound) וטומוגרפיה ממוחשבת (CT ,Computed Tomography), הביא לעלייה משמעותית באבחון קשריות בבלוטת התריס. עם זאת, מחקרים אחדים הראו עלייה ממשית בשכיחות המחלה גם לאחר תיקון למידת השימוש בבדיקות ההדמיה [1]. ייתכן והעלייה בשכיחות המחלה נובעת מחשיפה לקרינה (למשל, דרך שימוש בבדיקות CT), זיהום סביבתי, השמנה, שינויים בתזונה או גורמים אחרים שטרם הובררו.
הקווים המנחים של ה- ATA לטיפול בקשריות וגידולים בבלוטת התריס ממליצים לברר רק גושים הגדולים מ- 1 סנטימטר (פרט לחולים בסיכון גבוה) [2]. זאת מאחר וגידולים זעירים "תת-קליניים" שכיחים באוכלוסייה ונוטים להיות יציבים שנים רבות [3], כך שאיתור וטיפול בכולם אינו נחוץ ויגרום לנזק רב מתועלת. בשלב זה אין סמנים בשימוש שוטף המאפשרים לצפות אילו גושים יהפכו למשמעותיים קלינית. ייתכן שבעתיד יימצאו סמנים שונים (כגון BRAF, RAS ואחרים) שבעזרתם תוכל להתקבל החלטה מושכלת אודות הצורך בטיפול.
טיפול ביוד רדיואקטיבי
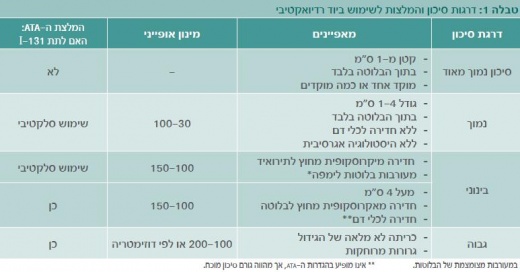
יוד רדיואקטיבי מהווה מרכיב מרכזי בטיפול בסרטן בלוטת התריס כבר יותר מ- 50 שנים, ובשנות השישים והשבעים פורסמו מספר עבודות פורצות דרך שהדגימו ירידה בחזרת המחלה ובתמותה בחולים שקיבלו טיפול זה [4]. עבודות אלו הובילו לשימוש נרחב בחומר, ובמשך שנים הוצע טיפול זה לכל מטופל הסובל מסרטן בלוטת התריס. עם זאת, בשנים האחרונות מתרבות הדעות על פיהן חולים בסיכון נמוך (טבלה 1) ואף חלק מהחולים בסיכון בינוני אינם מפיקים תועלת משמעותית מטיפול ביוד רדיואקטיבי. שינוי הגישה נובע בעיקרו מהבנה טובה יותר של מהלך המחלה והכרה בתופעות הלוואי הכרוכות בטיפול [5]. שינויים אלו באו לידי ביטוי בהנחיות ה- ATA משנת 2009, שהגדירו קבוצה גדולה של חולים בהם הטיפול ביוד רדיואקטיבי צריך להינתן על בסיס בררני.
התוויות לטיפול ביוד רדיואקטיבי
על מנת להגדיר בצורה טובה יותר באילו מקרים יש לטפל ביוד רדיואקטיבי, מקובל להתייחס להתוויות הבאות לטיפול:
- צריבה (Ablation): הרס רקמת התריס התקינה שנותרה בצוואר לאחר הניתוח, לצורך שיפור יכולת המעקב תוך שימוש בתירוגלובולין (Thyroglobulin) ומיפוי כלל גופי.
- טיפול ממרץ (Adjuvant): הרס תאי סרטן שנותרו בצוואר על מנת להפחית את הסיכון לחזרת המחלה. פעמים רבות הצריבה תכלול מרכיב של טיפול ממרץ (למשל, כאשר יש עדות לקליטת החומר בבלוטות לימפה צוואריות).
- טיפול במחלה גרורתית או שארית: כאשר יש עדות מבנית לרקמה סרטנית בצוואר או בגרורות מרוחקות.
טיעונים להעדפת טיפול בררני ביוד רדיואקטיבי
השימוש הנרחב ביוד רדיואקטיבי נובע מהדעה שטיפול צריבה וטיפול ממרץ נחוץ במרבית החולים לשיפור יכולת המעקב והפחתת הסיכון לחזרת המחלה, ומתוך ההנחה שטיפול ביוד רדיואקטיבי הוא בטוח וגורם לתופעות לוואי חולפות בעיקרן. טיעונים אלו נתונים לביקורת הולכת וגוברת בשל סיבות אחדות. ראשית, השימוש בעל-שמע ככלי מעקב אחר חולי סרטן בלוטת התריס עלה משמעותית בשני העשורים האחרונים. מעבר להיותו כלי זמין, לא יקר ושאינו כרוך בחשיפה לקרינה, בדיקת על-שמע נמצאה יעילה במיוחד בקבוצת החולים בסיכון נמוך המהווים חלק הולך וגדל מאוכלוסיית החולים. בקבוצה זו נמצאה בדיקת על-שמע כיעילה יותר מבדיקת תירוגלובולין בזיהוי חזרת המחלה, עם יכולת זיהוי מוקדמת יותר ורגישה יותר [6]. כמו כן, אין דרך לדעת אם מקור התירוגלובולין הוא מרקמת הגידול או מרקמה תקינה, כך שההשתנות בערכים לאורך המעקב היא אשר משמשת בעיקר לזיהוי התפתחות רקמה סרטנית. לאור זאת, גם ללא צריבה ניתן לזהות בצורה יעילה את חזרת המחלה.
כמו כן, עולה ספק האם המרכיב הממרץ נחוץ בכל החולים: ייתכן והסיכון הנמוך הנמוך יחסית לחזרת המחלה כיום נובע מהמהלך הטבעי של מחלה המאובחנת ומטופלת בשלב מוקדם ולא מהטיפול ביוד רדיואקטיבי. במחקר רב-מרכזי בארצות הברית נבדקו תוצאות הטיפול ב- 2,936 חולים עם או ללא טיפול ביוד רדיואקטיבי לאחר כריתת בלוטת התריס [7]. בעוד בחולים בסיכון גבוה ובינוני (שלבים 3-4) הייתה תועלת ברורה לטיפול, בחולים בסיכון נמוך שיעור חזרת המחלה היה דומה בחולים שטופלו ובחולים שלא טופלו.
במחקר של וייסמן (Vaisman) ושותפיו דווחו תוצאי המחלה ב- 289 חולים שלא קיבלו טיפול ביוד רדיואקטיבי לאחר ניתוח בבית החולים מוריאל סלואן-קטרינג (Memorial Sloan-Kettering) בניו יורק [8]. החולים שנכללו במחקר היו בשלבים 1-2 ובנוסף מספר חולים בשלב 3 (חדירה מזערית מחוץ לבלוטה ומעורבות מזערית של בלוטות לימפה). אחוזי חזרת המחלה בקבוצה זו היו 2.3% לאחר כריתה שלמה של הבלוטה ו- 4.3% לאחר כריתת מחצית הבלוטה, בדומה לדיווחים מעבודות קודמות שתיארו אחוזי חזרת מחלה של 2-5% בחולים בסיכון נמוך שטופלו ביוד רדיואקטיבי [9]. דיווחים אלו ואחרים מעידים על כך שבחולים בסיכון נמוך הטיפול ביוד רדיואקטיבי אינו משנה מהותית את הסיכון לחזרת המחלה.
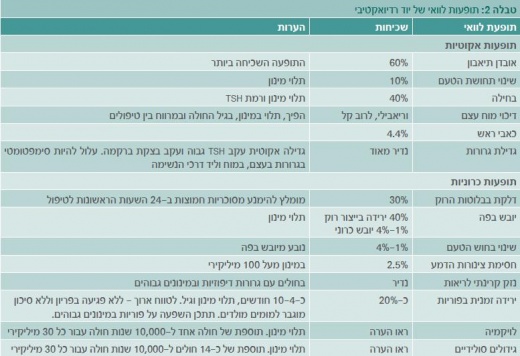
טיעון נוסף אשר הוביל לשימוש נרחב ביוד רדיואקטיבי הוא ההנחה שמדובר בטיפול בטוח עם תופעות לוואי קלות וחולפות (טבלה 2). במקרים שבהם הטיפול מאריך חיים ומונע חזרת מחלה, תופעות הלוואי הן מחיר מוצדק לשלם בעבור תועלת ניכרת, ואין ספק שהטיפול קל לאין שיעור מטיפולים כימותרפיים. לעומת זאת, במקרים שבהם יעילות הטיפול מוטלת בספק, יש לבחון בצורה מדוקדקת את תופעות הלוואי, כך שהטיפול לא יהיה גרוע מהמחלה. מתאר תופעות הלוואי מתועד בצורה טובה, כאשר חומרת התופעות תלויה במינון המצטבר [10]. בניתוח הסיכון לתופעות הלוואי יש לקחת בחשבון הן את הפגיעה האפשרית באיכות החיים והן את הסיכון לממאירויות משניות אשר פעמים רבות מסוכנות יותר מסרטן בלוטת התריס. כדאי לציין שאחת מתופעות הלוואי העלולה לפגוע בצורה קשה ביותר באיכות חיי המטופל היא יובש כרוני בפה. לחולים עם יובש בפה קשה לדבר זמן רב ברציפות (כפי שנדרש ממורים, עורכי דין וכדומה), טעם המזון משתנה (משמעותי לעוסקים בתחום המזון וכאחת מהנאות החיים) והם סובלים מעששת מואצת. לאור זאת, עיסוקו והעדפותיו של החולה צריכים לבוא בחשבון בניתוח העלות-תועלת ובהתאמה האישית של הטיפול.
מנת היוד הרדיואקטיבי המומלצת
המינונים המומלצים על פי ה- ATA לטיפול צריבה לאחר כריתת בלוטת התריס הם 30-100 מיליקירי לחולים בסיכון נמוך, ו- 100-200 מיליקירי לחולים בסיכון גבוה יותר. טווחים רחבים אלו נובעים ממיעוט במחקרים השוואתיים. מרבית המחקרים תיארו תוצאת טיפול תוך שימוש במינונים ניסיוניים (Empirical) קבועים מראש, השונים ממחקר למחקר. באחרונה הסתיימו מספר מחקרים מבוקרים בעלי הקצאה אקראית (Randomized controlled trials) הנותנים מענה טוב לשאלת המינון המומלץ לטיפול צריבה. ראשית, מחקר מאיטליה השווה מינונים של 50 ו- 100 מיליקירי יוד רדיואקטיבי תוך שימוש בתירוטרופין אנושי הצרפי (rhTSH ,Recombinant Human Thyrotropin), והדגים שיעורי הצלחה דומים [11]. שנית, שני מחקרים בעלי הקצאה אקראית שהסתיימו לאחרונה, HiLo מאנגליה ו- ESTAMBL מצרפת, השוו טיפול ב- 30 ו- 100 מיליקירי עם הכנה בעזרת rhTSH או תת-פעילות בלוטת התריס (Hypothyroidism), והדגימו שיעורי הצלחה שווים בכל הקבוצות [12]. לאור נתונים אלו, העדויות תומכות באפשרות לביצוע צריבה תוך שימוש במינונים נמוכים של 30-50 מיליקירי. עם זאת, למחקרים אלו יש חסרונות אחדים: הם בדקו את היעילות בהרס רקמת תריס תקינה לצורך שיפור יכולת מעקב (מרכיב הצריבה), ולא העריכו את יעילות הטיפול בהפחתת סיכון לחזרת המחלה (המרכיב הטיפול הממרץ). כמו כן, החולים שנכללו במחקרים אלו הם אותם חולים שייתכן שכלל אינם זקוקים לטיפול ביוד רדיואקטיבי (הנמצאים בקבוצה בה הטיפול צריך להינתן באופן בררני על פי הנחיות ה- ATA).
בחולים בסיכון בינוני או גבוה לחזרת המחלה המינונים המומלצים הם גבוהים יותר: 100-150 מיליקירי בחולים עם גרורות לבלוטות לימפה אזוריות, ו- 100-200 מיליקירי בחולים עם גרורות מרוחקות או עם מחלה שלא ניתנת לכריתה מלאה. בקרב חולים הזקוקים למינונים גבוהים, עולה השאלה האם שימוש במדידת מנות קרינה (Dosimetry) עדיף על מינונים קבועים מראש (מינונים ניסיוניים). עד היום אין תשובה ברורה לשאלה זו, ופרט למקרים יוצאי דופן, השימוש במינונים ניסיוניים נחשב דומה ביעילותו לשימוש במדידת מנות קרינה כאשר מגיעים למינון מצטבר דומה. עם זאת, בהיבט הבטיחותי, ייתכן שלמדידת מנות קרינה יש יתרון בחולים קשישים שבהם המינון הניסיוני פעמים רבות חוצה את סף הבטיחות למוח העצם.
טיפול נלווה ליוד רדיואקטיבי
את העלייה ברמת TSH הדרושה לטיפול ביוד רדיואקטיבי אפשר להשיג בעזרת השראת תת-פעילות של בלוטת התריס או בשימוש ב- rhTSH. השימוש ב- rhTSH חוסך לחולה את הסבל שבתת-פעילות ממושכת של בלוטת התריס, ושיפר באופן משמעותי את איכות החיים של חולי סרטן בלוטת התריס. בעוד יש עדויות מוצקות ליעילות דומה של שתי השיטות בטיפול הצריבה, קיים חשש שבמחלה גרורתית יעילות ה- rhTSH פחותה בהשוואה לזו של תת-פעילות בלוטת התריס. הכנה לטיפול עם rhTSH מאושרת לשימוש בארצות הברית ובאירופה בכלל החולים עם סרטן בלוטת התריס, פרט לאלו עם גרורות מרוחקות.
הערכת הסיכון לחזרת המחלה במטופלי יוד רדיואקטיבי
הערכת הסיכון הראשונית לאחר הניתוח צריכה לסייע בהחלטה האם החולה יפיק תועלת משמעותית מטיפול ביוד רדיואקטיבי. בקווים המנחים של ה- ATA נכללת קבוצה גדולה של חולים בקטגוריית הטיפול הבררני ביוד רדיואקטיבי. עם זאת, אין קריטריונים ברורים במסמך כיצד לקבוע את הצורך בטיפול בחולה המסוים, פרט לציון כי יש לטפל בחולים שבהם התועלת עולה על הסיכון. מאז פרסום הקווים המנחים עוסקים חוקרים רבים וצוותי עבודה של ה- ATA בהגדרה טובה יותר של הסיכון לחזרת המחלה. שיטת ה- TNM אשר פותחה על ידי הוועדה האמריקאית המשותפת לסרטן (AJCC ,American Joint Committee on Cancer) ונמצאת בשימוש נרחב לדירוג המחלה, מנבאת בצורה סבירה את הסיכון לתמותה מהמחלה, אך היא אינה טובה בניבוי הסיכון לחזרת המחלה.
הערכת הסיכון מבוססת בעיקרה על הבדיקה הפתולוגית. בבדיקה זו מרכיבים רבים המעידים על דרגת הסיכון, ביניהם גודל וסוג הגידול, חדירה לכלי דם, חדירה מחוץ לבלוטה, מספר וגודל בלוטות לימפה. מספר עבודות שפכו אור על החשיבות היחסית של כל אחד מרכיבים אלו: אף על פי שלחדירה מזערית מחוץ לבלוטה אין משמעות רבה בנוגע לסכות (Prognosis) באם הושגה כריתה ניתוחית טובה, יש חשיבות משמעותית לחדירת הגידול לתוך כלי דם. מרבית החוקרים בתחום מסכימים כי בחולים שבהם נצפית חדירה לכלי דם יש לתת טיפול ביוד רדיואקטיבי. כמו כן, בעוד סף הגודל שבו משתמשים רופאים רבים הוא סביב 1 סנטימטר, ככל הנראה אין תוספת סיכון משמעותית גם בגידולים בגודל של עד 3-4 סנטימטרים, בתנאי שהושגה כריתה ניתוחית טובה ואין ממצאים מדאיגים אחרים [8].
צוות מומחים מטעם ה- ATA בחן את הסיכון המתקבל מנוכחות מבלוטות לימפה גרורתיות בצוואר, והסיק כי מדובר בטווח רחב של דרגות סיכון. מעורבות של בלוטות אחדות (פחות מ- 3-5) הקטנות מ- 1 סנטימטר כמעט שלא משפיעה על הסיכון, אך כאשר מדובר ביותר מ- 10 בלוטות הגדולות מ- 1 סנטימטר, הסיכון לחזרת המחלה גבוה (כ- 30%). ככל שהניתוח הראשוני יהיה נרחב יותר (למשל, כאשר מבוצעת כריתה מניעתית של בלוטות הצוואר המרכזי) הסיכוי למצוא גרורות זעירות עולה. ככל הנראה, ממצאים מקריים אלו אינם משנים משמעותית את סכות החולה, ולא בהכרח מצדיקים טיפול ביוד רדיואקטיבי.
לאור הנתונים שהוצגו עד כה ברור כי המעבר לטיפול בררני ביוד רדיואקטיבי הופך את הטיפול למורכב יותר, ובשלב זה הקווים המנחים מותירים מקום רב לשיקול דעת הרופא המטפל. חשוב שניהול המקרה יבוצע על ידי רופאים המיומנים בטיפול בחולים אלו תוך שקילת התועלת הצפויה, תופעות הלוואי האפשריות, ותוך שיתוף המטופלים בהחלטה הטיפולית.
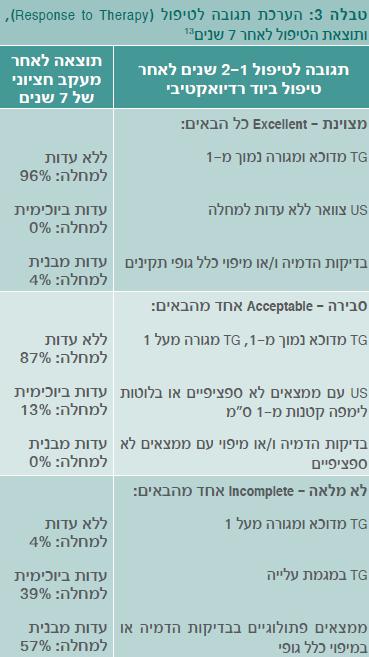
במהלך המעקב לאחר טיפול ביוד רדיואקטיבי, יש חשיבות עליונה להערכת סיכון מתמשכת על פי התגובה לטיפול. במקרים רבים התגובה לטיפול משמעותית יותר לסכות מאשר הערכת הסיכון הראשונית. למשל, הגישה לטיפול תהיה שונה בחולה בסיכון בינוני שהגיב היטב לטיפול הראשוני ולאחר שנה ערך התירוגלובולין שלו אינו מדיד ובדיקת העל-שמע שלו תקינה (תגובה מיטבית), בהשוואה לחולה בסיכון בינוני שלאחר שנה ערך התירוגולובולין שלו מדיד ובבדיקת על-שמע קיימים ממצאים חשודים (תגובה לא מלאה). טבלה 3 מפרטת את הגדרת התגובה לטיפול שאותה מבצעים שנה עד שנתיים לאחר הטיפול הראשוני ואת תוצאות הטיפול לאחר מעקב חציוני של 7 שנים [12]. התגובה לטיפול מכתיבה במידה רבה את אופי המעקב אחר החולים ואת הצורך בטיפולים נוספים. יש להדגיש שהערכת התגובה לטיפול מבוצעת רק בחולים שטופלו ביוד רדיואקטיבי.
נוסף לשיטות המסורתיות להערכת סיכון, השימוש בבדיקה המשלבת טומוגרפיה של חומרים רדיואקטיביים פולטי פוזיטרונים וטומגרפיה ממוחשבת (PET-CT ,Computed Tomography-Positron Emission Tomography) נמצא יעיל ביותר בהערכת הסיכון בחולים עם מחלה שארית, בעיקר בחולים בסיכון גבוה. גרורות חיוביות בבדיקה נוטות להיות תוקפניות יותר, ולהעיד על סיכון מוגבר לגדילה ולחדירה לאיברים סמוכים. נגעים חיוביים ב- PET אינם קולטים יוד רדיואקטיבי. בחולים אלו הנטייה תהיה לטיפול עוצמתי יותר, כגון הפניה לניתוח חוזר, קרינה חיצונית או טיפולים מקומיים.
טיפול במחלה גרורתית שאינה מגיבה ליוד רדיואקטיבי
הכלי היעיל ביותר לטיפול בגרורות של סרטן בלוטת התריס הוא יוד רדיואקטיבי במנות חוזרות, וזאת אם הנגעים קולטים את החומר ומגיבים לטיפול. במקרים שבהם הגרורות אינן מגיבות ליוד רדיואקטיבי (כ- 50% מהמקרים) קיימת כיום כמות הולכת וגדלה של כלים טיפוליים, הכוללים שיטות להרס מקומי של גרורות באזורים מסוימים, טיפולים לחיזוק העצם במקרים של גרורות גרמיות ותרופות מערכתיות לבלימת התקדמות הגידול. כמות המחקרים הקליניים בתחום גדולה מאי פעם, עם מעל 20 מחקרים קליניים פעילים לבחינת תרופות חדשות למחלה גרורתית. אף שהטיפולים הזמינים כיום טרם הוכיחו יעילות במדד החשוב מכולם של הארכת חיים, יש מקום לתקווה שאחת מהתרופות הנבחנות כיום תימצא יעילה בכך.
טיפולים ביולוגיים
מרבית התרופות המערכתיות לטיפול בסרטן בלוטת התריס שייכות לקבוצת מעכבי טירוזין קינאז (Tyrosine-kinase inhibitor). שלוש התרופות הנמצאות בשימוש מחוץ למסגרת מחקרים קליניים (אך אינן מאושרות על ידי מנהל המזון והתרופות האמריקאי להתוויה זו) כוללות את Nexavar (Sorafenib), Sutent (Sunitinib) ו- Votrient (Pazopanib). הטיפול בתרופות אלו אינו מביא לריפוי, כי אם לייצוב המחלה ב- 40-50% ולנסיגה חלקית של הנגעים ב- 10-20%. עם זאת, השפעת התרופות היא זמנית ונמשכת כשנה עד שנה וחצי, ולאחר מכן לרוב מופיעה התקדמות מחודשת של המחלה. לאור משך ההשפעה המוגבל של התרופות, אחת ההחלטות החשובות ביותר היא מתי להתחיל טיפול על מנת להפיק את מרב התועלת מהטיפול [14]. גם בחולים עם מחלה גרורתית נרחבת, כל עוד המחלה יציבה, מומלץ להמתין עם הטיפול עד להוכחת התקדמות מבנית משמעותית. ההמלצה במרבית ההנחיות הקליניות היא להפנות חולים עם מחלה גרורתית מתקדמת להשתתפות במחקר קליני בעדיפות ראשונה, מתוך תקווה שתרופות חדשות יהיו יעילות יותר ויביאו להפחתה בתמותה.
טיפולים נוספים
כשלב מעבר או בשילוב עם טיפולים מערכתיים, טיפולים מקומיים יכולים לסייע בטיפול בגרורות באזורים מסוימים המאיימים על מבנים סמוכים או הגורמים לתסמינים. מגוון הטיפולים הזמין כיום הוא גדול, וכולל תסחוף (Embolization) כלי דם, הרס בעזרת גלי רדיו (Radio-frequency), קרינה סטראוטקטית (Sereotactic radiation therapy), הזרקת אתנול (Ethanol) לגרורות צוואריות, וכמובן ניתוח להוצאת הנגע הבעייתי. מאחר וחולים עם גרורות סרטניות בבלוטת התריס יכולים לחיות שנים רבות עם המחלה, טיפולים אלו בעלי חשיבות גדולה לשמירה על איכות חיי המטופלים, ויש לנסות ולאתרם.
בחולים עם גרורות גרמיות שבהן לא נמצאה התוויה לטיפול מקומי, יש לשקול טיפול בתרופות לחיזוק העצם מקבוצת הביספוספונטים (Bisphosphonate) התוך ורידיים או ב- Prolia (Denosumab). תרופות אלו מוכחות היטב כמפחיתות סיכון לשברים בגרורות גרמיות מסרטנים אחרים, ויש עבודות המעידות על יעילות גם בסרטן בלוטת התריס [15], אם כי אינן רשומות להתוויה זו. המינונים המומלצים דומים לאלו הניתנים בסרטנים גרורתיים אחרים.
מעקב אחר חולים שלא טופלו ביוד רדיואקטיבי
הערכת הסיכון והמעקב בחולים שלא טופלו ביוד רדיואקטיבי דורשת התייחסות ייחודית. בקבוצה זו אין משמעות לרמת תירוגלובולין ולמיפוי כלל גופי, שכן קיימות בצוואר שאריות מזעריות של רקמת התריס התקינה. במקרים אלו עיקר המידע מתקבל מבדיקות על-שמע של הצוואר ומהשינוי ברמות תירוגלובולין לאורך זמן. מאחר ובדיקת על-שמע לאחר ניתוח שונה מבדיקה בצוואר תקין, חשוב שהבדיקה תבוצע על ידי רופא המיומן בהערכת הצוואר. עם זאת, צפוי שבקבוצת חולים זו חזרת מחלה תאובחן בשלב מאוחר יותר, שכן זיהוי המחלה יהיה לרוב על פי התקדמות מבנית (בבלוטות לימפה או במיטת הבלוטה) ולא ביוכימית (Biochemical) [6]. על פי עבודות קטנות שפורסמו עד כה, במקרים אלו גם אם אכן חזרת המחלה מאובחנת בשלב מאוחר יותר, יעילות טיפול ההצלה (Salvage therapy) דומה בהשוואה לחולים שטופלו בעברם ביוד רדיואקטיבי.
ביבליוגרפיה
- ↑ Morris LG, Myssiorek D. 2010. Improved detection does not fully explain the rising incidence of well-differentiated thyroid cancer: a population-based analysis. American journal of surgery 200:454-61.
- ↑ Cooper DS, Doherty GM, Haugen BR, Kloos RT, Lee SL, et al. 2009. Revised American Thyroid Association management guidelines for patients with thyroid nodules and differentiated thyroid cancer. Thyroid 19:1167-214.
- ↑ Ito Y, Miyauchi A, Inoue H, Fukushima M, Kihara M, et al. 2010. An observational trial for papillary thyroid microcarcinoma in Japanese patients. World journal of surgery 34:28-35.
- ↑ Mazzaferri EL, Young RL, Oertel JE, Kemmerer WT, Page CP. 1977. Papillary thyroid carcinoma: the impact of therapy in 576 patients. Medicine 56:171-96.
- ↑ Hay ID. 2006. Selective use of radioactive iodine in the postoperative management of patients with papillary and follicular thyroid carcinoma. Journal of surgical oncology 94:692-700.
- ↑ 6.0 6.1 Durante C, Filetti S. 2011. Management of papillary thyroid cancer patients in absence of postoperative radioiodine remnant ablation: tailoring follow-up by neck sonography. The Journal of clinical endocrinology and metabolism 96:3059-61.
- ↑ Jonklaas J, Sarlis NJ, Litofsky D, Ain KB, Bigos ST, et al. 2006. Outcomes of patients with differentiated thyroid carcinoma following initial therapy. Thyroid 16:1229-42.
- ↑ 8.0 8.1 Vaisman F, Shaha A, Fish S, Tuttle R. 2011. Initial therapy with either thyroid lobectomy or total thyroidectomy without radioactive iodine remnant ablation is associated with very low rates of structural disease recurrence in properly selected patients with differentiated thyroid cancer. Clinical endocrinology 75: 112-119.
- ↑ Ross DS, Litofsky D, Ain KB, Bigos T, Brierley JD, et al. 2009. Recurrence after treatment of micropapillary thyroid cancer. Thyroid 19(10):1043-8.
- ↑ Tala H, Tuttle RM. 2010. Contemporary post surgical management of differentiated thyroid carcinoma. Clinical oncology 22:419-29.
- ↑ Pilli T, Brianzoni E, Capoccetti F, Castagna MG, Fattori S, et al. 2007. A comparison of 1850 (50 mCi) and 3700 MBq (100 mCi) 131-iodine. administered doses for recombinant thyrotropin-stimulated postoperative thyroid remnant ablation in differentiated thyroid cancer. The Journal of clinical endocrinology and metabolism 92:3542-6.
- ↑ 12.0 12.1 1Comparison of Four Strategies of Radioiodine Ablation on 752 Low-Risk Thyroid Cancer Patients: Final Results of the Estimabl Study 2011. Abstracts of the 81st Annual Meeting of the American Thyroid Association. October 26-30, 2011. Indian Wells, California, USA. Thyroid 21 Suppl 1:A6-110.
- ↑ Tuttle RM, Tala H, Shah J, Leboeuf R, Ghossein R, et al. 2010. Estimating risk of recurrence in differentiated thyroid cancer after total thyroidectomy and radioactive iodine remnant ablation: using response to therapy variables to modify the initial risk estimates predicted by the new American Thyroid Association staging system. Thyroid 20:1341-9.
- ↑ Gild ML, Bullock M, Robinson BG, Clifton-Bligh R. 2011. Multikinase inhibitors: a new option for the treatment of thyroid cancer. Nature reviews. Endocrinology 7:617-24.
- ↑ Orita Y, Sugitani I, Toda K, Manabe J, Fujimoto Y. 2011. Zoledronic acid in the treatment of bone metastases from differentiated thyroid carcinoma. Thyroid 21:31-5.
קישורים חיצוניים
- חידושים בטיפול בסרטן בלוטת התריס, מדיקל מדיה
המידע שבדף זה נכתב על ידי ד"ר איל רובינשטוק
- המכון לאנדוקרינולוגיה ומטבוליזם, מרכז רפואי רבין, קמפוס בילינסון
- Endocrine service, Memorial Sloan-Kettering Cancer Center, New York


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק