סרטן האשכים - גוש שיורי לאחר כימותרפיה - Testicular cancer - post-chemotherapy residual mass
| סרטן האשכים - גוש שיורי לאחר כימותרפיה | ||
|---|---|---|
| Testicular cancer - post-chemotherapy residual mass | ||

| ||
| יוצר הערך | ד"ר דוד קקיאשווילי, ד"ר ירון עופר 
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן האשכים
השילוב בין שילובי התרופות הכימותרפיות ובין הטיפול התומך והשיטות הניתוחיות, שינו בצורה דרמטית את תוצאות הטיפול בחולי סרטן האשכים הגרורתי. השילוב בין שיטת ניתוח המשמרת את העצבוב ובין כימותרפיה המבוססת על Cisplatin שיפר את שיעורי ההישרדות מהמחלה, הוריד את שיעורי התחלואה ושיפר את איכות החיים[1].
למרות זאת חלק נכבד של הגברים המתייצגים עם מחלה מתקדמת ועברו טיפולים כימותרפיים, נשארים עם גוש שיורי אחרי הטיפול.
גושים שיוריים אלה נמצאים לרוב ברטרופריטונאום, אך יכולים להיות גם במקומות אחרים. דיסקציה דו-צדדית של בלוטות לימפה ברטרופריטונאום תוך שמירת העצבים היא השיטה המקובלת לטיפול בסרטן האשכים בשלב מתקדם. התוצאה מושפעת מבחירת החולים ומהיקף הניתוח. שמירת העצבוב הסימפטתי אפשרית גם לאחר טיפול כימותרפי. על אף שכריתה שלמה של גוש שיורי בחולי סרטן האשכים מסוג שאינו סמינומה היא השיטה המקובלת, מעקב אחרי חולים עם נסיגה מלאה של המסה ונרמול סמני הסרטן לאחר טיפול כימותרפי - נראה טיפול בטוח.
מטרת הטיפול
ההיגיון העומד מאחורי הטיפול על ידי דיסקציה של בלוטות לימפה רטרופריטונאליות אחרי כימותרפיה, מבוסס על המהלך הטבעי של גושים שיוריים, ביסוס האבחנה ויעילות טיפול וזאת יחד עם ירידת התחלואה מהניתוח.
כריתת הגוש השיורי הוא הכלי המדויק ביותר לדירוג (Staging) ברטרופריטונאום. הגדרה מדויקת של ההיסטולוגיה חשובה להחלטה על המשך הטיפול והמעקב[2]. הניתוח יכול לגלות נמק או לייפת (Fibrosis), טרטומה (Teratoma), או תאי סרטן חיים. באופן כללי, נמק או לייפת מתגלים בכמחצית מהמקרים, טרטומה מתגלה בכ- 35% מהמקרים ותאי סרטן חיים בכ- 15% מהמקרים. לא קיים כלי שיכול לחזות מראש או לאבחן את הרכב הגוש השיורי, ולכן כריתתו כה חשובה לאבחנה ולטיפול[3][4].
הסרה שלמה של הגוש השיורי יכולה להיות טיפולית, במיוחד במקרים של הימצאות תאי סרטן חיים בגוש. קבוצה מאוניברסיטת אינדיאנה דיווחה על 580 גברים שעברו דיסקציה של בלוטות לימפה ברטרופריטונאום. מהם 417 אחרי כימותרפיה ראשונית ו- 163 אחרי טיפול בקו שני של כימותרפיה (Salvage). ב- 43 (10%) מהחולים שעברו כימותרפיה ראשונית וב- 90 (55%) מהחולים שעברו כימותרפיית הצלה, נמצאו תאי סרטן חיים בדגימה שנכרתה. בחולים שבהם נמצאו תאי סרטן חיים ושעברו טיפול כימותרפי וכריתה לא שלמה של הגוש השיורי, נמצא שיעור גבוה יותר של תמותה מסרטן אשכים (88% לעומת 40% אחרי כריתה שלמה). יתרון ההישרדות בחולים שעברו כריתה שלמה היה משמעותי, אפילו בהשוואה לקבוצה שלא טופלה בטיפול כימותרפי, דבר המראה על יעילות הכריתה הכירורגית.
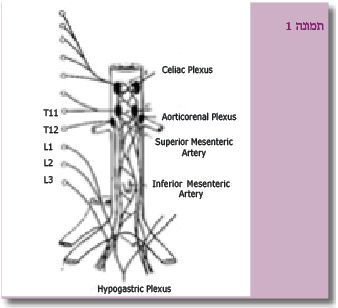
זאת ועוד, הכריתה הכירורגית היא שיטת הטיפול היחידה עבור טרטומה. לטרטומה שלא עוברת כריתה שלמה יש יכולת לגדול ואפשרות להפוך לממאירה[5][6][7][8]. הירידה בתחלואה מניתוח לאחר טיפול כימותרפי נבעה משינוי תבנית הניתוח לחד-צדדי, תוך שימור סיבי העצבים הסימפטיים והפלקסוס ההיפוגסטרי (תמונה 1). שיפור הטיפול הבתר-ניתוחי הוריד אף הוא את שיעור התחלואה.
בחירת החולים וההוריות לניתוח
ההוריות לניתוח תלויות בכמה גורמים: סוג הגידול הראשוני, גודל הגוש השיורי באמצעי הדימות, ורמת סמני הסרטן. כמה תבניות חיזוי עבור גושים המכילים תאי גידול חיים הוצעו במטרה להוריד את שיעורי התחלואה שנבעו מהטיפול, תוך שמירה על יעילות הטיפול האונקולוגי [9][10][11][12]. למרות זאת, הצורך בניתוח זה והרחבתו עדיין שנויה במחלוקת בארצות שונות ובמרכזים שונים. גוש שיורי לאחר טיפול כימותרפי או אחרי טיפול קרינתי בחולים עם גידולי אשך מסוג סמינומה (Seminoma), אינו מנותח באופן גורף ללא תלות בגודל הגוש. במקרים אלה מומלץ מעקב צמוד דימותי, ואחרי סמני הסרטן בלבד[13][14][15][16].
בדיקת דימות באמצעות FDG במכשיר PET יעילה מאוד במעקב אחרי חולים מסוג זה. בחולים עם גוש שיורי קטן משלושה ס"מ - המעקב עם מיפוי מסוג זה הוא אפשרי. בחולים עם גוש שיורי גדול משלושה ס"מ שלא קטן אחרי טיפול כימותרפי, ההמלצה היא ביצוע מיפוי, ואם אין קליטה במיפוי - אין צורך בכריתת הגוש או כל טיפול אחר. בחולים שבהם יש קליטה במיפוי, סריקת ה- PET היא אמצעי חיזוי למחלה פעילה, אם היא מתבצעת 4-6 שבועות אחרי תום הטיפול הכימותרפי או הקרינתי[17][18]. אם הסריקה היא חיובית - יש ליטול דוגמת רקמה או לכרות את הגוש השיורי.
טיפול נוסף מבוסס על הממצאים ההיסטולוגיים. בחולים עם מחלה מתקדמת אחרי טיפול כימותרפי בקו ראשון הטיפול בקו שני (Salvage) ניתן רק אחרי הוכחה של ממאירות[19][20]. ההתייחסות לגוש שיורי בחולי סרטן האשכים מסוג שאינו סמינומה שנוי במחלוקת, וזאת מהסיבה שאף אמצעי דימות או כל מודל פרוגנוסטי אחר, לא יכולים לחזות את הסוג ההיסטולוגי של הגוש השיורי[21][22][23][24]. לכן, כל גוש שיורי יש לכרות כאשר סמני הסרטן יורדים לרמה נורמלית לאחר טיפול כימותרפי[25][26][27][28].
ההתפלגות ההיסטולוגית של הגוש השיורי אחרי טיפול בקו ראשון של כימותרפיה יכול להראות: נמק, טרטומה או תאי סרטן ברי-קיימא ב- 50% ,35% וב- 15% מהמקרים בהתאמה.
אם קיימת נסיגה שלמה של המסה הרטרופריטונלית לאחר הטיפול הכימותרפי (1 ס"מ>) ונרמול סמני הסרטן, אין הכרח בדיסקציה של בלוטות הלימפה הרטרופריטונליות ומומלץ מעקב בלבד [29] [30] [31].
קבוצה מבית החולים על שם הנסיכה מרגרט מטורונטו דיווחה על מעקב של 30 שנה (1978-2007) אחר חולים שאובחנו כסובלים מסרטן האשכים מסוג שאינו סמינומה (Nonseminoma) בשלב גרורתי, ושעברו דיסקציה של בלוטות לימפה של הרטרופריטונאום (Post chemotherapy retroperitoneal lymph node dissection - pcRPLND)[32].
346 חולים טופלו תחילה בכימותרפיה. 240 עברו דיסקציה של בלוטות מהרטרופריטונאום לאחר הטיפול הכימותרפי אשר בהם נמצא גוש שיורי. ב- 106 חולים שבהם הייתה נסיגה שלמה של הגוש ונירמול סמני הסרטן, בוצע מעקב בלבד, והם לא עברו ניתוח מיידי. אורך המעקב החציוני היה 7.5 שנים (Median follow-up).
רק בשלושה חולים הייתה הישנות מאוחרת של המחלה (2.8%). בחולים אלה לא נמצאה עדות למחלה פעילה לאחר ניתוח ההצלה (Salvage surgery). מכאן שבחולים בהם קיימת נסיגה מלאה של המסה הרטרופריטונלית אחרי טיפול כימותרפי ונירמול סמני הסרטן – מעקב בלבד היא שיטה בטוחה.
בהתייחסות להיקף הניתוח - דיסקציה שלמה דו-צדדית של בלוטות הלימפה (Modified template) היא הטיפול המקובל [33]. שינוי תבנית הניתוח או כריתה של גוש שיורי בלבד (Lumpectomy) עלולה להסתיים בהשארת הגידול.
מתוך 240 חולים בקבוצה מטורונטו, 235 עברו דיסקציה דו צדדית שלמה. לאחר קבלת התשובה ההיסטולוגית של כל החולים האלה, בוצעה בדיקה השערתית בדיעבד: מה היה קורה אילו היו מבצעים דיסקציה חלקית וכריתת הגוש בלבד. מבדיקה זו עלה כי הגידול היה נשאר ב- 4.7% במקרה של שינוי תבנית הניתוח, ואילו אם היו כורתים רק את המסה השיורית (Lumpectomy) הגידול היה נשאר ב- 21.3% מהמקרים. לעומת זאת, במרכזים אחרים הראו שאם מתבצעת בחירת חולים קפדנית - התוצאות טובות יותר[34][35].
גושים שיוריים שאינם ברטרופריטונאום צריכים גם כן להיכרת כיוון שנמצא חוסר התאמה היסטולוגית ב- 35-50%[36][37]. רק אם המסה מהרטרופריטונאום מראה נמק בלבד, אזי גושים קטנים (1-1.5 ס"מ) במקומות אחרים למעט הרטרופריטונאום, יכולים להיות למעקב בלבד, ולא להסרה. הכריתה של הגוש השיורי יכולה להיעשות בצורה כירורגית מקובלת או באמצעות שיטה לפרוסקופית-רובוטית [38] [39] [40].
תוצאות לאחר הניתוח
תוצאות הניתוח תלויות בסוג ההיסטולוגי, בשלמות הכריתה ובטיפול שלאחר מכן. הימצאות תאי סרטן בגוש השיורי מחייבת טיפול נוסף, בדרך כלל שני מחזורים נוספים של כימותרפיה. מספר חוקרים מערערים על הצורך בטיפול כימותרפי נוסף וטוענים שכריתה שלמה חשובה יותר[41].
הטיפול המקובל הנו מתן כימותרפיה אם נמצאו תאי סרטן בגוש השיורי[42][43].
שיעור ההישרדות הכולל לחמש שנים נע בין 83% ל- 96% [44].
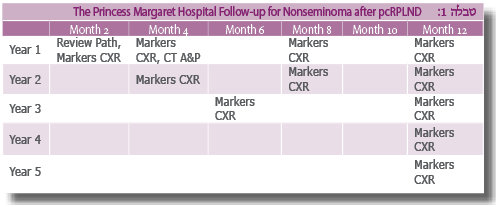
טבלה 1 מראה את תוכנית המעקב של בית החולים על שם הנסיכה מרגרט אחרי חולים עם סרטן האשכים מסוג שאינו סמינומה אחרי דיסקציה של בלוטות לימפה רטרופריטונאליות לאחר טיפול כימותרפי [32].
תחלואה בתר-ניתוחית
דיסקציה של בלוטות לימפה רטרופריטונליות היא אתגר כירורגי, במיוחד אחרי טיפול כימותרפי. שיעור התחלואה אחרי ניתוח כזה נע בין 18% ל- 39% [45] [46] [47]. אין ספק שניתוח מסוג זה צריך להתבצע על ידי מרכזים שלישוניים ומומחים בתחום.
כיוון שמדובר במחלה של גברים צעירים בגיל הפוריות המטרה בניתוחים ברטרופריטונאום היא שימור סיבי העצב הסימפתטיים והפלקסוס ההיפוגסטרי שאחראים על השפיכה. שימוש בשיטה לשימור עצבים אלו אפשרי במרבית המקרים, אפילו אחרי טיפול כימותרפי. בקבוצה מטורונטו דיווחו 54% מהחולים על שפיכה תקינה [32].
ביבליוגרפיה
- Baniel J, Foster RS, Rowland R.G, et al. Complications of post-chemotherapy retroperitoneal lymph node dissection. J Urol 1995;153:
(3 Pt 2) 976–980
- Heidenreich A, Albers P, Hartmann M, et al. Complications of primary nerve sparing retroperitoneal lymph node dissection for clinical stage I nonseminomatous germ cell tumors of the testis: experience of the German Testicular Cancer Study Group. J?Urol 2003;169(50):1710–1714
- ↑ Donohue JP, Foster RS. Retroperitoneal lymphadenectomy in staging and treatment. The development of nerve-sparing techniques. Urol Clin North Am 1998;25(3):461–468
- ↑ Fox EP, Weathers TD, Williams SD, et al. Outcome analysis for patients with persistent nonteratomatous germ cell tumor in postchemotherapy retroperitoneal lymph node dissections. J Clin Oncol 1993;11(7):1294–1299
- ↑ Hendry WF, Norman AR, Dearnaley DP, et al. Metastatic nonseminomatous germ cell tumors of the testis: results of elective and salvage surgery for patients with residual retroperitoneal masses. Cancer 2002;94(6):1668–1676
- ↑ Muramaki M, Hara I, Miyake H, et al. Clinical outcome of retroperitoneal lymph node dissection after induction chemotherapy for metastatic non-seminomatous germ cell tumors. Int J Urol 2004;11(9):763–767
- ↑ Logothetis CJ, Samuels ML, Trindade A, et al. The growing teratoma syndrome. Cancer 1982;50(8):1629–1635
- ↑ Motzer ML, Amsterdam A, Prieto V, et al. Teratoma with malignant transformation: diverse malignant histologies arising in men with germ cell tumors. J?Urol 1998;159(1):133–138
- ↑ Ahmed T, Bosl GJ, Hajdu SI. Teratoma with malignant transformation in germ cell tumors in men. Cancer 1985;56(4):860–863
- ↑ Donadio AC, Motzer RJ, Bajorin DF, et al. Chemotherapy for teratoma with malignant transformation. J Clin Oncol 2003;21(23):4285–4291
- ↑ Steyerberg EW, Keizer HJ, Fossa SD, et al. Prediction of residual retroperitoneal mass histology after chemotherapy for metastatic nonseminomatous germ cell tumor: multivariate analysis of individual patient data from six study groups. J Clin Oncol 1995;13(5):1177–1187
- ↑ Vergouwe Y, Steyerberg EW, de Wit R, et al. External validity of a prediction rule for residual mass histology in testicular cancer: An evaluation for good prognosis patients. Br J Cancer 2003; 88(6):843–847
- ↑ Matsuyama H, Yamamoto N, Sakatoku J, et al. Predictive factors for the histologic nature of residual tumor mass after chemotherapy in patients with advanced testicular cancer. Urology 1994;44(3):392–398 Discussion 398–399
- ↑ Onozawa M, Kawai K, Yamamoto T, et al. Clinical parameters that predict histology of postchemotherapy retroperitoneal lymph node mass in testicular cancer. Int J
- ↑ Kamat MR, Kulkarni JN, Tongoankar HB, et al. Value of retroperitoneal lymph node dissection in advanced testicular seminoma. J Surg Oncol 1992;51:65–67
- ↑ Hofmockel G, Gruss A, Theiss M, Chemotherapy in advanced seminoma and the role of postcytostatic retroperitoneal lymph node dissection. Urol Int 1996;57:38–42
- ↑ Herr HW, Sheinfeld J, Puc HS, et al. Surgery for a post-chemotherapy residual mass in seminoma. J Urol 1997;157:860–862
- ↑ Mosharafa AA, Foster RS, Leibovich BC, et al. Is the postchemotherapy resection of seminomatous elements associated with higher acute morbidity?, J Urol 2002;167-172
- ↑ de Santis M, Bokemeyer C, Becherer A, et al. Predictive impact of 2-18 FDG PET (Fluoro 2 Deoxy D Glucose Positron Emission Tomography) for residual postchemotherapy masses in patients with bulky seminoma, J Clin Oncol 2001;19:3740–3744
- ↑ de Santis M, Becherer A, Bokemeyer C, et al. 2-18 fluoro-deoxy-D-glucose positron emission tomography is a reliable predictor for viable tumor in postchemotherapy seminoma: an update from the multicenter sempet trial. J Clin Oncol 2004;22:1034–1039
- ↑ Duchesne GM, Stenning SP, Aass N, et al. Radiotherapy after chemotherapy for metastatic seminoma: a diminishing role. Eur J Cancer 1997;33:829–835
- ↑ Puc H, Heelan R, Mazumdar M, et al. Management of residual mass in advanced seminoma: results and recommendations from Memorial Sloan-Kettering Cancer Center. J Clin Oncol 1996;14:454–460
- ↑ Vergouwe Y, Steyerberg EW, de Wit R, et al. External validity of a prediction rule for residual mass histology in testicular cancer: an evaluation for good prognosis patients. Br J Cancer 2003;88:843–847
- ↑ Hartmann JT, Candelaria M, Kuczyk MA, et al. Comparison of histological results from the resection of residual masses at different sites after chemotherapy for metastatic non-seminomatous germ cell tumours. Eur J Cancer 1997;33:843–847
- ↑ Hendry WF, Norman AR, Dearnaley DP, et al. Metastatic nonseminomatous germ cell tumors of the testis: results of elective and salvage surgery for patients with residual retroperitoneal masses. Cancer 2002;94:1668–1676
- ↑ Sheinfeld J. The role of adjunctive postchemotherapy surgery for nonseminomatous germ-cell tumors: current concepts and controversies. Semin Urol Oncol 2002;20:262–271
- ↑ Herr HW. Does necrosis on frozen-section analysis of a mass after chemotherapy justify a limited retroperitoneal resection in patients with advanced testis cancer? Br J Urol 1997;80:653–657
- ↑ Wood DP, Herr HW, Heller G, et al. Distribution of retroperitoneal metastases after chemotherapy in patients with nonseminomatous germ cell tumors. J Urol 1992;148:1812–1816
- ↑ Hartmann JT, Schmoll HJ, Kuczyk MA, et al. Postchemotherapy resections of residual masses from metastatic non-seminomatous germ cell tumors. Ann Oncol 1997;8:531–538
- ↑ Rabbani F, Goldenberg SL, Gleave ME, et al. Retroperitoneal lymphadenectomy for post-chemotherapy residual masses: is a modified dissection and resection of the residual mass sufficient? Br J Urol 1998;81:295–300
- ↑ Fossa SD, Ous S, Lien HH, et al. Post-chemotherapy lymph node histology in radiologically normal patients with metastatic nonseminomatous testicular cancer. J Urol 1989;141:557–559
- ↑ Toner GC, Panicek DM, Heelan RT, et al. Adjunctive surgery after chemotherapy for nonseminomatous germ cell tumors: recommendations for patient selection. J Clin Oncol 1990;8:1683–1694
- ↑ Kuczyk M, Machtens S, Stief C, et al. Management of the postchemotherapy residual mass in patients with advanced stage non-seminomatous germ cell tumors (GCT). Int J Cancer 1999;83:852–855
- ↑ 32.0 32.1 32.2 Kakiashvili D, Anson-Cartwright L, Jewett M, et al. Post-chemotherapy retroperitoneal lymph node dissection for testicular germ cell tumors: is surgery indicated in all and is bilateral template necessary? Toronto, ON, Canada; Abstract EUA 2009; AUA, 2009
- ↑ Carver B, Shayegan B, Sheinfeld J, et al. Incidence of metastatic nonseminomatous germ cell tumor outside the boundaries of a modified postchemotherapy retroperitoneal lymph node dissection. J Clin Oncol 2007;25-28:4365-4369
- ↑ Beck S, Foster R, Einhorn L, et al. Is full bilateral retroperitoneal lymph node dissection always necessary for postchemotherapy residual tumor? Cancer 2007;110(6):1235-1240
- ↑ Heidenreich A, Pfister D, Albers P, et al. Postchemotherapy retroperitoneal lymph node dissection in advanced testicular cancer: radical or modified template resection. Eur Urol. 2009;55(1):217-224
- ↑ Hartmann JT, Candelaria M, Kuczyk MA, et al. Comparison of histological results from the resection of residual masses at different sites after chemotherapy for metastatic non-seminomatous germ cell tumours. Eur J Cancer 1997;33:843–847
- ↑ Hendry WF, Barrett A, McElwain JJ, et al. The role of surgery in the combined management of metastases from malignant teratomas of the testis. Br J Urol 1980;52:38–44
- ↑ Steiner H, Peschel R, Janetschek G, et al. A long-term results of laparoscopic retroperitoneal lymph node dissection: a single-center 10-year experience. Urology 2004;63:550–555
- ↑ Rassweiler JJ, Frede T, Lenz E, et al. Long-term experience with laparoscopic retroperitoneal lymph node dissection in the management of low-stage testis cancer. Eur Urol 2000;37:251–260
- ↑ Janetschek G, Peschel R, Hobisch A, et al. Laparoscopic retroperitoneal lymph node dissection. J Endourol 2001;15:449–455
- ↑ Fizazi K, Tjulandin S, Salvioni R, et al. Viable malignant cells after primary chemotherapy for disseminated nonseminomatous germ cell tumors: prognostic factors and role of postsurgery chemotherapy–results from an international study group. J Clin Oncol 2001;19(10):2647–2657
- ↑ NCCN Prostate Cancer Panel. NCCN guidelines on testicular cancer. Accessed 2006
- ↑ Krege S, Beyer J, Albers P, et al. European consensus conference on diagnosis and treatment of germ cell cancer: A report of the second meeting of the European Germ Cell Cancer Consensus group (EGCCCG) part I. Eur. Urol. 2008;53(3):478-496
- ↑ Sim HG, Lange PH, Lin DW. Role of post-chemotherapy surgery in germ cell tumors, Urol Clin North Am 2007;34(2):199-217
- ↑ Gels ME, Nijboer AP, Hoekstra HJ, et al. Complications of the post-chemotherapy resection of retroperitoneal residual tumour mass in patients with non-seminomatous testicular germ cell tumours. Br J Urol 1997;79(2):263–268
- ↑ McKiernan JM, Motzer RJ, Bajorin DF, et al. Reoperative retroperitoneal surgery for nonseminomatous germ cell tumor: Clinical presentation, patterns of recurrence, and outcome. Urology 2003;62(4):732–736
- ↑ Heidenreich A, Ohlmann C, Hegele A, et al. Repeat retroperitoneal lymphadenectomy in advanced testicular cancer. Eur Urol 2005;47(1):64–71
קישורים חיצוניים
- גוש שיורי אחרי כימותרפיה בחולה סרטן האשכים, מדיקל מדיה
המידע שבדף זה נכתב על ידי ד"ר דוד קקיאשווילי, ד"ר ירון עופר


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק