הבדלים בין גרסאות בדף "תירוקסין - Tetraiodothyronine - T4"
| (6 גרסאות ביניים של 2 משתמשים אינן מוצגות) | |||
| שורה 1: | שורה 1: | ||
| − | |||
{{בדיקת מעבדה | {{בדיקת מעבדה | ||
|שם עברי=תירוקסין T4 | |שם עברי=תירוקסין T4 | ||
| שורה 6: | שורה 5: | ||
|תמונה= | |תמונה= | ||
|כיתוב תמונה= | |כיתוב תמונה= | ||
| − | |מעבדה=אנדוקרינולוגיה בדם | + | |מעבדה=[[אנדוקרינולוגיה בדם]] |
|תחום=מדידת רמת ההורמון של בלוטת התריס החיוני לפעילויות פיזיולוגיות ומטבוליות מרכזיות בגוף | |תחום=מדידת רמת ההורמון של בלוטת התריס החיוני לפעילויות פיזיולוגיות ומטבוליות מרכזיות בגוף | ||
|יחידות מדידה= | |יחידות מדידה= | ||
| שורה 13: | שורה 12: | ||
|אחראי הערך= | |אחראי הערך= | ||
}} | }} | ||
| − | + | {{הרחבה|הורמוני בלוטת התריס}} | |
==מטרת הבדיקה== | ==מטרת הבדיקה== | ||
| שורה 30: | שורה 29: | ||
היוד הנחוץ ליצירת הורמוני התירואיד, מגיע לגוף מן המזון והוא מתפזר בגוף בצורתו המיוננת, היודיד (<sup>-</sup>I). לניצול יעיל של היוד, קיים מנגנון בתאי הזקיק של בלוטת התריס, המרכז את היוד בשיעור הגבוהה פי 20-40 מריכוזו בדם. הנשא הגליקופרוטאיני החיוני להחדרת יוד לבלוטה ידוע כ- Na<sup>+</sup>/I<sup>-</sup> symporter, שמהווה חלק בלתי נפרד מקרום התא, והוא ייחודי בהעברת יוני יוד ונתרן ביחד מהדם לתאי הזקיק, וכינויו SIM. טרנספורטר זה מעביר 2 יוני נתרן ויון יוד אחד, באופן שהאנרגיה האלקטרו-כימית הנוצרת מהעברת נתרן במפל ריכוזים חיובי מריכוזו הגבוה מחוץ לתא אל תוך תאי הזקיק, משמשת להעברת יודיד כנגד מפל הריכוזים, שכן ריכוז יוד בזקיק גבוה יותר פי-30 מאשר בפלזמה. העברת יוני יוד על ידי ה-SIM נתמכת על ידי TSH, אך מעוכבת על ידי יוני תיוציאנט (<sup>-</sup>SCN) או יוני פרכלוראט (<sup>-</sup>ClO4). הטרנספורטר SIM אינו מסוגל להבחין בין יוד רגיל ליוד רדיואקטיבי, שיכול להיות בעייתי, בעת ספיגה לא מבוקרת של יוד רדיואקטיבי לתירואיד בחשיפה לדליפת קרינה מוגזמת של יוד רדיואקטיבי בתקלה גרעינית כפי שקרה באסון צ'רנוביל. יודיד זה נכנס ל-lumen הפוליקולארי על ידי טרנספורטר נוסף הידוע כ-pendrin, הממוקם על הממברנה האפיקאלית (לומינאלית) של התאים הפוליקולאריים. | היוד הנחוץ ליצירת הורמוני התירואיד, מגיע לגוף מן המזון והוא מתפזר בגוף בצורתו המיוננת, היודיד (<sup>-</sup>I). לניצול יעיל של היוד, קיים מנגנון בתאי הזקיק של בלוטת התריס, המרכז את היוד בשיעור הגבוהה פי 20-40 מריכוזו בדם. הנשא הגליקופרוטאיני החיוני להחדרת יוד לבלוטה ידוע כ- Na<sup>+</sup>/I<sup>-</sup> symporter, שמהווה חלק בלתי נפרד מקרום התא, והוא ייחודי בהעברת יוני יוד ונתרן ביחד מהדם לתאי הזקיק, וכינויו SIM. טרנספורטר זה מעביר 2 יוני נתרן ויון יוד אחד, באופן שהאנרגיה האלקטרו-כימית הנוצרת מהעברת נתרן במפל ריכוזים חיובי מריכוזו הגבוה מחוץ לתא אל תוך תאי הזקיק, משמשת להעברת יודיד כנגד מפל הריכוזים, שכן ריכוז יוד בזקיק גבוה יותר פי-30 מאשר בפלזמה. העברת יוני יוד על ידי ה-SIM נתמכת על ידי TSH, אך מעוכבת על ידי יוני תיוציאנט (<sup>-</sup>SCN) או יוני פרכלוראט (<sup>-</sup>ClO4). הטרנספורטר SIM אינו מסוגל להבחין בין יוד רגיל ליוד רדיואקטיבי, שיכול להיות בעייתי, בעת ספיגה לא מבוקרת של יוד רדיואקטיבי לתירואיד בחשיפה לדליפת קרינה מוגזמת של יוד רדיואקטיבי בתקלה גרעינית כפי שקרה באסון צ'רנוביל. יודיד זה נכנס ל-lumen הפוליקולארי על ידי טרנספורטר נוסף הידוע כ-pendrin, הממוקם על הממברנה האפיקאלית (לומינאלית) של התאים הפוליקולאריים. | ||
| − | לאחר כניסת יוני יוד דרך הממברנה האפּיקאלית אל תוך החומר הקולואידי של תאי הזקיק, יש צורך לשפעל את היוד שאינו פעיל בצורת <sup>-</sup>I ולחמצן אותו לצורת I<sub>2</sub>. תכשיר כמו goitrin יכול להפחית את ייצור הורמוני התירואיד על ידי הפרעה לחמצון היודיד ליוד מולקולארי. לצורך זה האנזים TPO או thyroid peroxidase המקובע בממברנת תא הזקיק מחמצן את היודיד למולקולת יוד וקושר אותה לשייר ההידרוקסיל של טירוזין שהוא אחד מתוך 120 שיירי טירוזין על פני תירוגלובולין. תהליך היודינציה דורש נוכחות של H<sub>2</sub>O<sub>2</sub> והיודינציה מתרחשת על שיירי פחמן 3 או פחמן 5 במולקולת טירוזין. בשלב הבא טירוזין חד-יודי (monoiodotyrosine, MIT) עובר שלב יודינציה נוסף ליצירת Diodotyrosine או DIT. בשלב הסופי פרוקסידאז התירואיד מבצע צימוד (coupling) של שני מולקולות DIT ליצירת T4 כאשר צימוד של מולקולות DIT ו-MIT יוצרות מולקולת T3. | + | לאחר כניסת יוני יוד דרך הממברנה האפּיקאלית אל תוך החומר הקולואידי של תאי הזקיק, יש צורך לשפעל את היוד שאינו פעיל בצורת <sup>-</sup>I ולחמצן אותו לצורת I<sub>2</sub>. תכשיר כמו goitrin יכול להפחית את ייצור הורמוני התירואיד על ידי הפרעה לחמצון היודיד ליוד מולקולארי. לצורך זה האנזים [[TPO]] או thyroid peroxidase המקובע בממברנת תא הזקיק מחמצן את היודיד למולקולת יוד וקושר אותה לשייר ההידרוקסיל של טירוזין שהוא אחד מתוך 120 שיירי טירוזין על פני תירוגלובולין. תהליך היודינציה דורש נוכחות של H<sub>2</sub>O<sub>2</sub> והיודינציה מתרחשת על שיירי פחמן 3 או פחמן 5 במולקולת טירוזין. בשלב הבא טירוזין חד-יודי (monoiodotyrosine, MIT) עובר שלב יודינציה נוסף ליצירת Diodotyrosine או DIT. בשלב הסופי פרוקסידאז התירואיד מבצע צימוד (coupling) של שני מולקולות DIT ליצירת T4 כאשר צימוד של מולקולות DIT ו-MIT יוצרות מולקולת T3. |
| שורה 36: | שורה 35: | ||
| − | יש חשיבות לאופן הצימות (conjugation) של DIT ו-MIT: כאשר (triiodothyronine{{כ}} → MIT +{{כ}} DIT{{כ}} | + | יש חשיבות לאופן הצימות (conjugation) של DIT ו-MIT: כאשר (normal T3), (triiodothyronine){{כ}} → MIT +{{כ}} DIT{{כ}} לעומת זאת כאשר צימות טירוזין חד-יודי וטירוזין דו-יודי מתקיים באופן חלופי, מתקבלת מולקולת T3 חסרת פעילות ביולוגית: r-T3 (biologically inactive){{כ}} → DIT + {{כ}}MIT. |
חומצת האמינו טירוזין משמשת חומר מוצא להורמוני התריס. הטירוזין מסופק על ידי החלבון thyroglobulin, המיוחד לבלוטת התריס. תירוגלובולין הוא גליקופרוטאין גדול המכיל 134 שיירי טירוזין, אך אינו מכיל יוד. רק אחדים משיירי הטירוזין של תירוגלובולין משמשים כחומר גלם ליצירת הורמוני התריס. התירוגלובולין נוצר ברטיקולום האנדופלזמי של תאי הזקיק ומופרש יחד עם היוד המולקולארי לתוך הקולואיד שבחלל הזקיק. בהיות התירוגלובולין על פני קרום תא הזקיק התוחמת את הקולואיד מתבצעת ריאקצית יודינציה. לפיכך, הקולואיד שבחלל הזקיק משמש מאגר לתירוגלובולין נושא יוד, ומשמש מאגר להורמוני התריס. פעילות פרוטאוליטית מביאה לשחרור T4 ו-T3 ממולקולת תירוגלובולין שעברה יודינציה ושני הורמונים אלה חוצים את ממברנת התאים בקלות יחסית כתוצאה מהיותם חומרים ליפופיליים. יחד עם זאת זוהו באדם לפחות 10 מנגנוני טרנספורט אקטיביים התלויים באנרגיה, האחראיים לכך שהרמה התוך-תאית של הורמוני התירואיד, תישמר גבוהה יותר מאשר רמתם בפלזמה או בנוזל האינטרסטיציאלי. | חומצת האמינו טירוזין משמשת חומר מוצא להורמוני התריס. הטירוזין מסופק על ידי החלבון thyroglobulin, המיוחד לבלוטת התריס. תירוגלובולין הוא גליקופרוטאין גדול המכיל 134 שיירי טירוזין, אך אינו מכיל יוד. רק אחדים משיירי הטירוזין של תירוגלובולין משמשים כחומר גלם ליצירת הורמוני התריס. התירוגלובולין נוצר ברטיקולום האנדופלזמי של תאי הזקיק ומופרש יחד עם היוד המולקולארי לתוך הקולואיד שבחלל הזקיק. בהיות התירוגלובולין על פני קרום תא הזקיק התוחמת את הקולואיד מתבצעת ריאקצית יודינציה. לפיכך, הקולואיד שבחלל הזקיק משמש מאגר לתירוגלובולין נושא יוד, ומשמש מאגר להורמוני התריס. פעילות פרוטאוליטית מביאה לשחרור T4 ו-T3 ממולקולת תירוגלובולין שעברה יודינציה ושני הורמונים אלה חוצים את ממברנת התאים בקלות יחסית כתוצאה מהיותם חומרים ליפופיליים. יחד עם זאת זוהו באדם לפחות 10 מנגנוני טרנספורט אקטיביים התלויים באנרגיה, האחראיים לכך שהרמה התוך-תאית של הורמוני התירואיד, תישמר גבוהה יותר מאשר רמתם בפלזמה או בנוזל האינטרסטיציאלי. | ||
| שורה 133: | שורה 132: | ||
אין צורך בצום או בהכנות מיוחדות. יש לקחת דם במחנה כימיה (פקק אדום או צהוב) ובשום פנים לא להשתמש במבחנת הפארין (פקק ירוק). דגימת הנסיוב יציבה 7 ימים בטמפרטורת החדר, אך עדיף לאחסן בקירור. בהקפאה ניתן לאחסן עד 30 יום. דגימות המוליטיות עלולות להפריע לביצוע במדידה באופן שיש נטייה לתוצאות מופחתות. אין להשתמש בדגימות ליפמיות. | אין צורך בצום או בהכנות מיוחדות. יש לקחת דם במחנה כימיה (פקק אדום או צהוב) ובשום פנים לא להשתמש במבחנת הפארין (פקק ירוק). דגימת הנסיוב יציבה 7 ימים בטמפרטורת החדר, אך עדיף לאחסן בקירור. בהקפאה ניתן לאחסן עד 30 יום. דגימות המוליטיות עלולות להפריע לביצוע במדידה באופן שיש נטייה לתוצאות מופחתות. אין להשתמש בדגימות ליפמיות. | ||
| + | |||
| + | ==ראו גם== | ||
| + | * [[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | ||
| + | * [[תפקוד בלוטת התריס|בדיקות מעבדה - תפקוד בלוטת התריס]] | ||
{{ייחוס|[[משתמש:בן עמי סלע|פרופ' בן-עמי סלע]]}} | {{ייחוס|[[משתמש:בן עמי סלע|פרופ' בן-עמי סלע]]}} | ||
| − | [[קטגוריה:בדיקות מעבדה]] | + | |
| + | [[קטגוריה:בדיקות מעבדה: אנדוקרינולוגיה]] | ||
| + | [[קטגוריה:בדיקות מעבדה - תפקוד בלוטת התריס]] | ||
גרסה אחרונה מ־12:19, 23 במרץ 2015
| מדריך בדיקות מעבדה | |
| תירוקסין T4 | |
|---|---|
| Tetraiodothyronine T4 | |
| מעבדה | אנדוקרינולוגיה בדם |
| תחום | מדידת רמת ההורמון של בלוטת התריס החיוני לפעילויות פיזיולוגיות ומטבוליות מרכזיות בגוף |
| טווח ערכים תקין | סך-תירוקסין (total T4) ביחידות מיקרוגרם לד"ל: בדם טבורי - 7.4-13.0; בגיל 1-3 ימים - 11.8-22.6; בגיל שבוע עד שבועיים - 9.8-16.6; בגיל חודש עד 4 חודשים - 7.2-14.4; בגיל 4-12 חודשים - 7.8-16.5; בגיל שנה עד 5 שנים - 7.3-15.0; בגיל 5-10 שנים - 6.4-13.3; בגיל 10-15 שנים - 5.6-11.7; בגברים - 4.6-11.5; בנשים - 5.5-11.5; בנשים הרות (בשבועות 15-40 להיריון) - 9.1-14.0. רמת סך-תירוקסין מוגברת בהיריון עקב עלייה ברמת הגלובולין הקושר T4 (TBG) בדם. במבוגרים מעל גיל 60 שנה - 5.0-10.7. בדמם של זכרים רמות סך-T4 יורדת בהדרגה עם ההתבגרות המינית, אך בנשים לא ידועה תופעה זו. רמת סך-תירוקסין הנקבעת בדגימת דם מלא של יילודים הנלקחת מהעקב על נייר Guthrie במסגרת סקר יילודים בגיל 1-5 ימים - יותר מ-7.5 מיקרוגרם לד"ל, ובדגימות הנלקחות בגיל שמעל 6 ימים - יותר מ-6.5 מיקרוגרם לד"ל. רמות T4 נמוכות יותר בדם טבורי מיילודים פגים בהשוואה ליילודים full term, והן נמצאות במתאם עם משקל היילוד. רמות סך-T4 מוגברות משמעות ביילודים בהם מוגברות רמות גלובולין קושר תירוקסין (TBG), לעומת רמות T4 חופשי בדמם של יילודים הדומה לזה של מבוגרים. מדידת תירוקסין בנוזל מי שפיר: מתחת לשבוע ההיריון ה-17 רמת תירוקסין היא בתחום בין 0.06-0.35 מיקרוגרם לד"ל; בשבוע ההיריון 17 עד השבוע ה-22 עולה רמת תירוקסין ל-0.08-1.16 מיקרוגרם לד"ל, ובשבועות ה-35-42 להיריון רמת תירוקסין יורדת מעט ל-0.08-0.65 מיקרוגרם לד"ל. רמת תירוקסין הנמדדת במי השפיר נמוכה יותר אם האם נוטלת תכשירי יוד, מטופלת ביוד רדיואקטיבי, ב-propylthiouracil או ב-methimazole. רמת תירוקסין במי השפיר אינה מושפעת מציון ה-Apgar של היילוד. רמת תירוקסין-חופשי (free thyroxine או fT4): ביילודים (ימים 1-4) - 2.2-5.3 ננוגרם לד"ל; בילדים ונערים מגיל שבועיים עד גיל 20 שנה - 0.8-2.0 ננוגרם לד"ל; במבוגרים מעל גיל 20 שנה- 0.8-3.1 ננוגרם לד"ל. בנשים הרות בשליש ההיריון הראשון - 0.7-2.0 ננוגרם לד"ל, ובשני שלישי ההיריון המתקדמים - 0.5-1.6 ננוגרם לד"ל. |
| יוצר הערך | פרופ' בן-עמי סלע |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – הורמוני בלוטת התריס
מטרת הבדיקה
בדיקת סך-T4 או T4 חופשי מתבצעת בדרך כלל כבדיקת המשך לתוצאה בלתי תקינה של בדיקת TSH במקרים של חשד לאי סדירות של בלוטת התירואיד מתבצעת בדיקת T4 במקביל למדידת TSH. מדידת הורמוני התירואיד מתבצעת כשיש חשד שתוצאה לא סדירות אלה משקפות באופן שניוני בעיה בתפקוד ההיפותאלאמוס או בלוטת יותרת המוח, שכן ההורמונים TRH ו-TSH המופרשים על ידי בלוטות אלה, בהתאמה, מגרים את התירואיד להפרשת ההורמונים T3 ו-T4. לרוב תתבצע מדידה של שני הורמוני בלוטת התריס, שכן במצבים אחדים של יתר פעילות של הבלוטה T3 יכול להימצא מוגבר, בעוד רמת T4 תקינה. תרחישים קליניים רבים יביאו למדידת רמת הורמוני הבלוטה כגון היפרתירואידיזם ראשוני ושניוני, תת-פעילות של יותרת המוח (hypopituitarism), וכן thyrotoxic thyroiditis ו-Toxic nodular goiter(זפק קשרירי רעלני). בדיקת רמת T4 תעשה כחלק מברור אבחוני של מחלת Graves וכן של Hashimoto thyroiditis, וכן במצבים של שאת בתירואיד, כאשר רמת T4 תסייע בניטור ומעקב אחר יעילות הטיפול במפגעים אלה. בדיקת תירוקסין יכולה להידרש במקרים של בירור בעיות חוסר פוריות בנשים. מדידת תירוקסין מתבצעת גם במקרים של חשד ל-myxedema.
בסיס פיזיולוגי
תירוקסין (להלן T4) הוא למעשה פרו-הורמון שהופך על ידי הסרת שייר יוד אחד לטרי-יודו-תירונין (להלן T3), שהוא למעשה ההורמון הפעיל ביולוגית, ומשפיע על תהליכים פיזיולוגיים מגוונים בגוף כמו שגשוג, התפתחות, חילוף חומרים, טמפרטורת הגוף וקצב הלב. תאי הזקיק (follicle) של בלוטת התריס מסנתזים ומפרישים שני הורמונים מכילי-יוד: T4 (thyroxine) לו 4 אטומי יוד, ו-T3 (triiodothyronine) לו 3 אטומי יוד.
ייצורם של שני הורמונים אלה משופעל על ידי ההורמון Thyroid stimulating hormone (להלן TSH), המשתחרר מתאים תירוטרופיים בקדמת בלוטת יותרת המוח (pituitary), תהליך המגורה על ידי ההורמון TRH המופרש מבלוטת ההיפותאלאמוס במוח. הציר היפותאלאמוס- בלוטת יותרת המוח- תירואיד מווסת על ידי משוב שלילי (negative feedback), כאשר רמות מוגברות של T3 ו-T4 בפלזמה יעכבו ייצור TSH, ובהתאם הפרשת הורמוני התירואיד תיחלש; היפוכו של דבר כאשר רמות T3 ו-T4 בפלזמה פוחתות. חסר יוד והפחתת ייצור T3 ו-T4 גורם להגדלת הבלוטה ולתופעת הזפק. במצב תקין כמות T4 בדם גדולה מזו של T3 ביחס שיכול להגיע עד פי-20, ולכך אחראית חלקית העובדה שתקופת מחצית החיים של T4 ארוכה יותר מזו של T3.
מנגנון היצירה של הורמוני בלוטת התריס
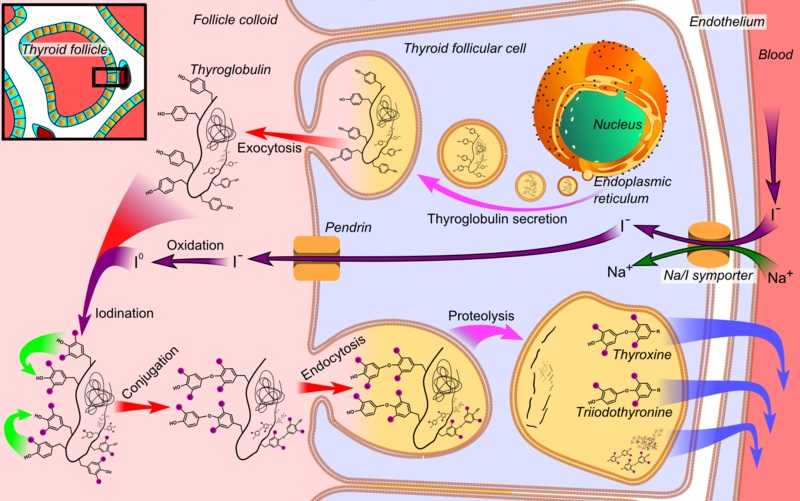
בלוטת התריס במבוגר מורכבת מלמעלה מ-20 מליון זקיקים (follicles) שהן היחידות התפקודיות שלה. זקיקים הם נאדיות שגודלן נע בין 0.05-0.5 מ"מ, אשר בהיקפם נמצא שכבת תאי אֶפִּיתֶל המייצרים את הורמוני התריס, הזקיק מכיל קולואיד שהוא נוזל צמיג עשיר בחלבונים ובמלחים. הזקיקים צמודים זה לזה וביניהם קיימת רקמת חיבור רופפת המכילה קצות עצבים, שעוטפת כל זקיק וזקיק ואת בלוטת התריס עצמה. רשת כלי דם עשירה משמשת להעברת חמצן, מזון, יוד ואת ההורמון TSH אל תאי הזקיק, וכן לקליטת הורמונים המופרשים במישרין מתאי הזקיקים ולהפרשתם לדם. ההורמון TSH נקשר לקולטנים המופיעים על הממברנה הבאזו-לטראלית של תאי הזקיק תוך עידוד אנדוציטוזה של קולואיד לתאים אלה. חלקיקים (vesicles) המכילים קולואיד ובתוכו תירוגלובולין שעבר יודינציה, עוברים איחוי עם ליזוזומים בתא הזקיק, כאשר האנזימים הליזוזומאליים מבקעים יחידות T4 מחלבון תירוגלובולין שעבר יודינציה. בשלב זה אותם חלקיקים (vesicles) עוברים אקסוציטוזה והורמוני התירואיד מופרשים לדם.
היוד הנחוץ ליצירת הורמוני התירואיד, מגיע לגוף מן המזון והוא מתפזר בגוף בצורתו המיוננת, היודיד (-I). לניצול יעיל של היוד, קיים מנגנון בתאי הזקיק של בלוטת התריס, המרכז את היוד בשיעור הגבוהה פי 20-40 מריכוזו בדם. הנשא הגליקופרוטאיני החיוני להחדרת יוד לבלוטה ידוע כ- Na+/I- symporter, שמהווה חלק בלתי נפרד מקרום התא, והוא ייחודי בהעברת יוני יוד ונתרן ביחד מהדם לתאי הזקיק, וכינויו SIM. טרנספורטר זה מעביר 2 יוני נתרן ויון יוד אחד, באופן שהאנרגיה האלקטרו-כימית הנוצרת מהעברת נתרן במפל ריכוזים חיובי מריכוזו הגבוה מחוץ לתא אל תוך תאי הזקיק, משמשת להעברת יודיד כנגד מפל הריכוזים, שכן ריכוז יוד בזקיק גבוה יותר פי-30 מאשר בפלזמה. העברת יוני יוד על ידי ה-SIM נתמכת על ידי TSH, אך מעוכבת על ידי יוני תיוציאנט (-SCN) או יוני פרכלוראט (-ClO4). הטרנספורטר SIM אינו מסוגל להבחין בין יוד רגיל ליוד רדיואקטיבי, שיכול להיות בעייתי, בעת ספיגה לא מבוקרת של יוד רדיואקטיבי לתירואיד בחשיפה לדליפת קרינה מוגזמת של יוד רדיואקטיבי בתקלה גרעינית כפי שקרה באסון צ'רנוביל. יודיד זה נכנס ל-lumen הפוליקולארי על ידי טרנספורטר נוסף הידוע כ-pendrin, הממוקם על הממברנה האפיקאלית (לומינאלית) של התאים הפוליקולאריים.
לאחר כניסת יוני יוד דרך הממברנה האפּיקאלית אל תוך החומר הקולואידי של תאי הזקיק, יש צורך לשפעל את היוד שאינו פעיל בצורת -I ולחמצן אותו לצורת I2. תכשיר כמו goitrin יכול להפחית את ייצור הורמוני התירואיד על ידי הפרעה לחמצון היודיד ליוד מולקולארי. לצורך זה האנזים TPO או thyroid peroxidase המקובע בממברנת תא הזקיק מחמצן את היודיד למולקולת יוד וקושר אותה לשייר ההידרוקסיל של טירוזין שהוא אחד מתוך 120 שיירי טירוזין על פני תירוגלובולין. תהליך היודינציה דורש נוכחות של H2O2 והיודינציה מתרחשת על שיירי פחמן 3 או פחמן 5 במולקולת טירוזין. בשלב הבא טירוזין חד-יודי (monoiodotyrosine, MIT) עובר שלב יודינציה נוסף ליצירת Diodotyrosine או DIT. בשלב הסופי פרוקסידאז התירואיד מבצע צימוד (coupling) של שני מולקולות DIT ליצירת T4 כאשר צימוד של מולקולות DIT ו-MIT יוצרות מולקולת T3.
יש חשיבות לאופן הצימות (conjugation) של DIT ו-MIT: כאשר (normal T3), (triiodothyronine) → MIT + DIT לעומת זאת כאשר צימות טירוזין חד-יודי וטירוזין דו-יודי מתקיים באופן חלופי, מתקבלת מולקולת T3 חסרת פעילות ביולוגית: r-T3 (biologically inactive) → DIT + MIT.
חומצת האמינו טירוזין משמשת חומר מוצא להורמוני התריס. הטירוזין מסופק על ידי החלבון thyroglobulin, המיוחד לבלוטת התריס. תירוגלובולין הוא גליקופרוטאין גדול המכיל 134 שיירי טירוזין, אך אינו מכיל יוד. רק אחדים משיירי הטירוזין של תירוגלובולין משמשים כחומר גלם ליצירת הורמוני התריס. התירוגלובולין נוצר ברטיקולום האנדופלזמי של תאי הזקיק ומופרש יחד עם היוד המולקולארי לתוך הקולואיד שבחלל הזקיק. בהיות התירוגלובולין על פני קרום תא הזקיק התוחמת את הקולואיד מתבצעת ריאקצית יודינציה. לפיכך, הקולואיד שבחלל הזקיק משמש מאגר לתירוגלובולין נושא יוד, ומשמש מאגר להורמוני התריס. פעילות פרוטאוליטית מביאה לשחרור T4 ו-T3 ממולקולת תירוגלובולין שעברה יודינציה ושני הורמונים אלה חוצים את ממברנת התאים בקלות יחסית כתוצאה מהיותם חומרים ליפופיליים. יחד עם זאת זוהו באדם לפחות 10 מנגנוני טרנספורט אקטיביים התלויים באנרגיה, האחראיים לכך שהרמה התוך-תאית של הורמוני התירואיד, תישמר גבוהה יותר מאשר רמתם בפלזמה או בנוזל האינטרסטיציאלי.
השפעת חסר יוד על סינתזת הורמוני התירואיד
חסר של יוד במזון, או אך רמת יוד נמוכה במי-שתייה באזורים גיאוגרפיים שונים, תפחית את יצירת הורמוני התירואיד. מצב זה יגרום להפחתת המשוב השלילי על בלוטת יותרת המוח, ויוביל לייצור מוגבר של TSH, להגדלת בלוטת התריס עד כדי יצירת זפק (goiter). לתרחיש זה השפעה בהגדלת יכולת התירואיד לקלוט יוד, כדי לפצות על החסר ביסוד זה.
מנגנון הפעולה של הורמוני התירואיד
T3 ו-T4 נקשרים לקולטנים ספציפיים בגרעין התא, הקשורים לאלמנטים מגיבים על פני genes promoter, שיכולים לשפעל או לדכא את השעתוק (transcription) ברמת ה-DNA. ההורמון T4 מגביר את הקצב המטבולי הבסיסי (basal metabolic rate), וכתוצאה מכך את צריכת האנרגיה והחמצן בגוף. במצבי תת-תריסיות קצב חילוף החומרים עשוי לרדת ב-20%-40% ואילו ביתר-תריסיות הוא עשוי לעלות ב-75%.
תירוקסין (אך בעיקר T3) פועל לגירוי ייצור האנזים RNA Polymerase, ובכך מעודד את קצב הסינתזה של חלבונים. אך באותה מידה מגביר הורמוני התירואיד את קצב פירוק חלבונים. התירונינים מעודדים את השפעת הקולטנים ה-β אדרנרגיים על חילוף החומרים של הסוכר גלוקוזה, וכתוצאה מכך מגבירים את קצב הפירוק של גליקוגן וסינתזה של גלוקוזה בתהליך הגלוקונאוגנזה. כמו כן מעודד הורמוני התירואיד את הפירוק של כולסטרול ומגדיל את מספר הקולטנים ל-LDL, מה שמזוהה עם הגברת קצב הליפוליזה. הורמוני התירואיד חיוניים להתפתחות תקינה והתמיינות (דיפרנציאציה) של כל התאים בגוף האדם. הם מווסתים את חילוף החומרים של חלבונים, שומנים ופחמימות, ומשפיעים על האופן בו תאי הגוף מנצלים מולקולות עתירות-אנרגיה. להורמוני התירואיד השפעה על המטבוליזם של מספר ויטמינים.
הורמוני התריס קשורים לפריון ולהפרשת חלב בנשים. יתר-תריסיות כרוכה לעתים בהפרעות במחזור החודשי ולקושי להיכנס להריון, ייתכן על ידי עיבוי יתר של האנדומטריום. לעומת זאת תת-תריסיות יכולה לגרום לדימום מוגבר, וכן לאי-סדירות במחזור החודשי. תת-תריסיות בגברים עלולה לדכא את היצר המיני ואילו יתר-תריסיות עלולה לגרום לאי תפקוד מיני.
הורמוני התירואיד מגבירים את קצב הלב ואת עוצמת כיווץ הלב, וכך מגדיל את תפוקת הדם של הלב (cardiac output), על ידי הגדלת רמת הקולטנים ה-β אדרנגיים בשריר הלב. פעילות זו מגבירה את לחץ הדם הסיסטולי, ומפחיתה את לחץ הדם הדיאסטולי. שתי ההשפעות האחרונות אופייניות אמנם ליתר-פעילות של התירואיד. במקרים של תת-תריסיות יתכן ולחץ הדם דווקא יעלה בגלל הצרת כלי דם היקפיים המתרחבים בדרך כלל ביתר-פעילות של התירואיד לסייע בפליטת חום. הורמוני התירואיד מחזקים את פעילות קטכולאמינים דהיינו מגבירים את הפעילות הסימפתטית.
פעולת הורמוני התירואיד חיונית גם להבשלה וצמיחה לינארית של עצמות השלד הארוכות בסינרגיה עם הורמון הגדילה. תת-תריסיות מלידה עלולה להסתיים בנמיכות קומה, ואילו יתר-תריסיות עלולה לגרום לירידה בצפיפות העצם. הורמון התריס חיוני להתפתחות ולתפקוד תקינים של מערכת השרירים. יתר-תריסיות גורמת לחולשת שרירים. התירונינים מגבירים את רגישות תאי הגוף לקטכולאמינים (דוגמת אדרנלין). יתר-תריסיות מגבירה את פעילות המעיים והפרשת מיצי קיבה, מה שמביא לעתים לשלשולים.
הורמון התירואיד חיוני לתקינות מערכת העצבים ולהבשלה של תאי העצב, כאשר יתר-תריסיות עלולה לגרום לחרדות, עצבנות ואי-שקט, הפרעות בשינה ובעיות זיכרון, תת-תריסיות קשורה לתחושת עייפות, להפרעות זיכרון, ועלולה לגרום לדיכאון במיוחד בנשים. יתר-תריסיות בילדים עלול לגרום להרטבה לילית, להפרעות שינה, לחוסר ריכוז וירידה בלימודים, להפרעות התנהגות, ולגדילה מהירה.
השפעתו ההורמונאלית של T3 על רקמות המטרה שלו גדולה בערך פי-4 מזו של T4. כ-80% מההורמונים שמייצרת בלוטת התירואיד הם מסוג T4 ורק כ-20% מסוג T3. משמעות הדבר היא שרק חלק קטן מהפיכת T4 ל- T3 על ידי הסרת שייר יוד אחד מפחמן 5# בטבעת החיצונית של T4 מתבצע בבלוטת התירואיד, בעוד שרוב ההסבה של T4 ל-T3, מתבצעת ברקמות מחוץ לבלוטה. האנזים המסיר את היוד מ-T4 הוא iodothyronine deiodinase, שיש לו שלושה איזואנזימים: Type I- נמצא בכבד בכליה ובבלוטת התריס ואחראי ל-80% מכלל הדה-יודינציה של T4; איזואנזים type II - המצוי במוח, בבלוטת יותרת המוח וברקמות שומן חומות; Type III- מצוי במיוחד במוח, בעור ובשליה. פעילות האנזים מהסוג הראשון מעוכבת על ידי התרופה Propyl-Thiocil או Propylthiouracil, ואילו הסוגים II ו-III אינם רגישים לתרופה זו, המונעת ייצור הורמוני בלוטת התריס. הסרת יוד אחד מהטבעת השנייה של T4, יוצרת T3 ואילו הסרת יוד אחד מהטבעת הראשונה של T4, יוצרת T3 מהופך (reverse T3) שאינו פעיל בחילוף החומרים. מטבוליטים נוספים של T3 עוברים תהליכים עוקבים של דה-קרבוקסילציה ודה-יודינציה ליצירה של iodothyronamine או T1a ו-thyronamine או T0a.
דרגת הזמינות של הורמוני התירואיד בפלזמה
70% מסך הורמונים אלה קשור לחלבון הנשא TBG או thyroxine-binding globulin; בין 10-15% משני ההורמונים קשורים לנשא transthyretin הידוע גם בשמות prealbumin וגם TBPA או thyroxine –binding prealbumin; ואילו 15-20% משני ההורמונים קשורים ל-PA או para-albumin; רק 0.03% של T4 אינו קשור וידוע כ-T4 חופשי (fT4) ו-0.3% של T3 אינו קשור וידוע כ-T3 חופשי (fT3). ריכוז T3 בפלזמה הוא בערך 1/40 מזה של T4, והבדל זה נובע בחלקו מזמן מחצית החיים הקצר יותר של T3 העומד על 2.5 ימים, לעומת 6.5 ימים של T4. ל-TBG זיקה גדולה יותר ל-T4 מאשר ל-T3; ל-transthyretin זיקה גדולה יותר ל-T3 מאשר ל-T4; לשני ההורמונים זיקה חלשה יחסית לאלבומין אך בגלל הריכוז הגבוה של אלבומין בפלזמה, כושר הנשיאה שלו לגבי שני הורמוני התירואיד הוא גבוה.
טרנספורט של הורמוני התירואיד בפלזמה
הורמוני התירואיד נעים בפלזמה קשורים לחלבוני טרנספורט, כאשר רק מקטע קטן שלהם הוא חופשי (בלתי קשור) והוא המקטע הפעיל ביולוגית. לכן קביעת רמת ההורמון החופשי היא בעלת משמעות אבחונית רבה. יתרה מכך, כאשר רמת הגלובולין הקושר תירוקסין (TBG) גבוהה במיוחד כמו בהיריון, לכן תוצאת המקטע החופשי חיונית עוד יותר.
יצירת הורמוני התירואיד בעובר
הורמוני ההיפותאלאמוס ובלוטת יותרת המוח, TRH ו-TSH, מתחילים להיות מופרשים כבר בשבוע ה-18-20 להריון, ויצירת T4 המגיעה כבר בשלב זה לערכים משמעותיים קלינית. לעומת זאת T3 נותר עדיין נמוך ברמתו בשבוע ה-18-20 (פחות מ-15 ננוגרם לדציליטר) עד לשבוע ה-30 של ההיריון, ובלידה רמתו ביילוד עולה עד ל-150 ננוגרם לדציליטר. האספקה העצמית של הורמוני התירואיד בעובר שומרת עליו מפני אי-סדירוּת בהתפתחות המוח שעלולה להיגרם כתוצאה מתת-תריסיות של האם בהיריון.
הציר בלוטת התריס-בלוטת יותרת-המוח אינו תלוי כנראה במערכת האימהית, שכן TSH אינו עובר דרך השליה. אם כי תרומת הורמוני התריס של האם לעובר מוגבלת החל ממחצית ההיריון ואילך, נראה שלנשים הרות עם תת-תריסיות שאינן מטופלות לפני ההיריון או במהלכו, סיכון מוגבר ללידת ילדים עם מנת משכל נמוכה. הסברה היא שעד החודש הרביעי להיריון קיימת תלות של העובר בהורמוני התירואיד של האם שכן התפתחות המוח העוברי מקדימה את ההבשלה המלאה של בלוטת התריס בעובר. אמנם מפגעים קבועים או ארעיים של התירואיד באישה ההרה עלולים להשפיע באופן ניכר על תפקוד התירואיד בעובר או ביילוד. נוגדנים מסוג IgG המופיעים באם בדלקת בלוטת התריס אוטו-אימונית, יכולים לעבור דרך השליה ולדכא את פעולת בלוטת התריס. תרופות ממשפחת ה-thioamides, כגון Carbimazole המוסב בגוף ל-Mercaptizol ו-Methimazole ו-propyl-thiocyl הניתנות לאם כחלק מטיפול ביתר-תריסיות, גם כן עלולות לעכב יצירת הורמוני התריס בעובר.
הורמוני התריס חיוניים להתפתחות תקינה של מערכת העצבים בעובר ובתינוק. התקופה החשובה ביותר להתפתחות המוח המושפעת מתת-תריסיות היא בשלוש שנות השנים הראשונות, אך התקופה הקריטית ביותר מצטמצמת לשבועות או החודשים הראשונים לחיי התינוק. הורמוני התריס מגבירים את הפקת החום בגוף על ידי הגברה של מתח השרירים וההתכווצויות שלהם. ייתכן שהנסיקה המהירה בריכוז הורמוני התריס בדם של יילודים והירידה רק לאחר 48-72 שעות, קשורה להפרשי טמפרטורה ניכרים בדם יילוד בלידה הנחשף להבדלי טמפרטורה חדים בין הסביבה החיצונית לרחם.
להורמוני התירואיד יש השפעה ניכרת על ההתפתחות העוברית כמו גם על זו של תינוקות וילדים. הורמונים אלה משפיעים על הריאות, והם משפיעים על התפתחות שלאחר הלידה של מערכת העצבים המרכזית. השפעתם בעידוד יצירת מיאלין ונוירוטרנסמיטורים, כמו גם גדילה של אקסונים. יש השערה שהורמוני התירואיד יכולים להגביר את ריכוז סרוטונין במוח, בעיקר בקליפת המוח ולווסת רמת נוראפינפרין ו-GABA במוח.
פיענוח תוצאות הבדיקה
בעת האחרונה יש מגמה לבצע קודם מדידה רגישה הקיימת להערכת רמת תירוטרופין שהיא מדידת TSH כמבדק ראשוני להערכת תפקוד התירואיד, כאשר מדידת סך-T4 מתבצעת רק להבנת ואישוש תוצאות לא תקינות של TSH.
מדידת רמת T4 צריכה תמיד להיות חלק מהערכה כוללת של תפקודי בלוטת התריס ולכן היא מתבצעת ברוב המקרים כחלק מפרופיל בדיקות הכולל גם את TSH ו-T3. התוצאות המופיעות להלן מייצגות את התרחישים הבאים: א.TSH מוגבר בעוד רמת T4 ו-T3 תקינה, מצביעים על תת-תריסיות מתונה (תת-קלינית); ב. TSH מוגבר בעוד רמת רמת T4 נמוכה ורמת T3 נמוכה או תקינה, מצביעים על תת-תריסיות; ג.TSH נמוך בעוד רמות T4 ו-T3 תקינות, מצביעים על יתר-תריסיות מתונה (תת-קלינית); ד. TSH נמוך בעוד רמות T3 ו-T4 תקינות, מצביעים על יתר-תריסיות; ה. TSH נמוך בעוד רמות 4T ו-T3 נמוכות או תקינות, מצביעים על תת-תריסיות שלא ממקור התירואיד אלא כתגובה שניונית נדירה לבעיה בבלוטת יותרת המוח; ו. TSH מוגבר בעוד רמות T4 ו-T3 גבוהות, יכולים להצביע על אי סדירות של בלוטת יותרת המוח.
רמה גבוהה של סך-T4 מעל 13.1 מיקרוגרם לד"ל מזוהה עם יתר-פעילות של הבלוטה (כדוגמת מחלת Grave), או בסרטן של התירואיד כמו בגידול שפיר (אדנומה) המפריש T3, בשלבים מוקדמים של Hashimoto thyroiditis, במקרים של תירואידיטיס חריפה, בשלבים מוקדמים של כשל הבלוטה, זפק מחסר ביוד, ב-thyrotoxicosis factitia, ומצבים בהם רמת TBG גבוהה (כמו בהיריון, נטילת אמצעי מניעה, בתרחישים של רמות TBG מוגברות גנטית, ב-acute intermittent porphyria, ובצמקת מרתית ראשונית). כן יכולות להתקבל תוצאות מוגברות של סך-T4 בהפאטיטיס (לאחר 4 שבועות מתחילת התסמינים), במפגעים פסיכיאטריים חריפים, ובהיפראמסיס גרבידרום. רמה מוגברת של סך-T4 וכן של fT4 תיתכן אחרי נטילת חומרי ניגוד לצורך צילומי X.
רמת סך-T4 נמצאת מוגברת גם בנבדקים עם פעילות תקינה של התירואיד (euthyroidism) אך מאובחנים עם FDH1 או Familial dysalbuminemic hyperthyroxinemia. זהו מפגע בו רמת סך-T4 מוגברת בדם במיוחד, למרות התקינות הפיזיולוגית של הבלוטה, הנגרם כתוצאה ממוטציות בגן לאלבומין, הגורמות ליצירת חלבון עם זיקה הגדולה בערך פי-60 לתירוקסין, מאשר זיקת האלבומין הרגיל לתירוקסין. סך-T4 מוגבר המצבים בהם מוגבר קישור תירוקסין לחלבון TBPA או thyroxine-binding pre-albumin או transthyretin ברמתו גבוהה יותר ב-CSF מאשר בפלזמה. במצבים אחרונים אלה רמת T3 נורמאלית. יש מצבים בהם הרמה הכללית של T4 יכולה להיות גבוהה אך רמת T4 חופשי (fT4) תהיה תקינה: דלקת כבד נגיפית; חולשת שרירים (myasthenia gravis); הריון; רעלת הריון. הסיבה השכיחה ביותר לרמת סך-T4 מוגברת במחלה לא-תירואידלית היא מחלת כבד. רמות T4 הגבוהות מ-20 מיקרוגרם לד"ל אפשריות במצבי "סערה תירואידלית".
רמה נמוכה של T4 מתחת ל-2.5 מיקרוגרם לד"ל מזוהה עם תת-פעילות של הבלוטה, שלבים מאוחרים של מחלת השימוטו, מחלות כרוניות אחדות, או תזונה לקויה, במפגעים עם רמה נמוכה של TBG (שיכולים להופיע בתסמונת נפרוטית, במחלת כבד כרונית, במחלות ספיגת מעי עם איבוד חלבון (protein-losing enteropathies), או מפגעים גנטיים על חסר TBG, במצב של תת פעילות של בלוטת יותרת המוח (היפופיזה), או בעקבות פעילות גופנית מאוד מאומצת. יש לציין שבמצבי תת-פעילות של בלטת התריס רמת סך-T4 בנסיוב פוחתת לפני שרמת T3 פוחתת. כמו כן ראוי להדגיש שבמקרים של חסר תירוקסין וטיפולים משלימים באלתרוקסין, מציאת רמות מוגברות של סך-T4 ושל T4 חופשי, אינן בהכרח מעידות על מינון יתר הורמונאלי: במקרים אלה ראוי למדוד גם רמת T3 לסייע בהערכת פעילות הבלוטה בעקבות הטיפול באלתרוקסין.
כצפוי, בתרחישים של תת-פעילות של הבלוטה כמו Hashimoto's thyroiditis, רמות T4 ו-T3 בדם נמוכות. הופעת נוגדנים כנגד תירוקסין אופיינית לתירואידיטיס ע"ש השימוטו, ולהיפותירואידיזם ראשוני (ב-54% מהמקרים), למחלת Graves (ב-26% מהמקרים), לזפק קשרירי או דיפוזי (ב-9% מהמקרים) ולסרטן התירואיד (ב-1% מהמקרים).
ייצור הורמוני התירואיד נעשה בעודף במחלת Grave, ובמחלת Plummer (זפק רעלני קשרירי), ואילו ב-myxedema יש הפחתה בייצורם. רמת סך-T4 הנמוכה מ-2.0 מיקרוגרם לד"ל ב-myxedema תבוא לביטוי בתרדמת מאופיינת על ידי היפותרמיה. במצב של cretinism ייצור הורמוני התירואיד אפסי. במצבים של היפרתירואידיזם, זמן מחצית החיים של T4 בדם שהוא 6.5 יום באופן תקין, יורד ל-3.5 ימים, ואילו במצבי היפותירואידיזם כגון מיקסאדמה זמן מחצית החיים של T4 עולה ל-9 עד 10 ימים. מחלת Grave, עם רמה מוגברת של T4 ו-T3 חופשיים בפלזמה, שכיחה יותר בקרב נשים (2% בנשים ו-0.2% בגברים). תרחיש אחר של יתר פעילות של הבלוטה הפוגע בעיקר בנשים הוא thyrotoxicosis, שבא לביטויו בעליה בהורמוני התירואיד בדם, אלא שהוא יכול להיגרם או על ידי נטילת גלולות תירוקסין בעודף, אך גם כתוצאה מבלוטת תריס פעילה ביתר.
בחינת רמת T4 במסגרת סקר יילודים
הנתונים הסטטיסטיים הגלובאליים הרב שנתיים מצביעים על מפגעי תת-תריסיות בתחום של אחד ל-3,500-4,800 לידות. דגימת היילודים לרמות T4 ו-TSH לגילוי היפותירואידיזם מולד, נעשית כחלק מסקר יילודים שהתבצע מתחילת שנות ה-60 ביחד עם בדיקת PKU, והחל משנות ה-90 המאוחרות כחלק מפרופיל מורחב של סקר יילודים המסוגל לגלות עד 25 מפגעים מולדים ברי תיקון. נטילת הדם המיטבית נעשית מעקב הרגל והספגת הדם על נייר גאטרי, 2-7 ימים לאחר הלידה, כאשר התינוק כבר הוזן לפחות 24 שעות על ידי הנקה או בפורמולה מקובלת. מומלץ שדגימת הדם במקרה של פגים או ילודים full term במשקל הנמוך מ-1.5 ק"ג, תילקח בפרק זמן של 4-10 ימים לאחר הלידה.
כצפוי, רמת T4 ביילודים גבוהה מזו שבמבוגרים, כאשר הסיבות לחשש של תת-תריסיות הן רמת TSH גבוהה, ורמת T4 נמוכה מ-6.5 מיקרוגרם לד"ל בתינוק בן פחות מ-7 ימים, או רמה הנמוכה מ-5 מיקרוגרם לד"ל בתינוק בן יותר מ-8ימים. במקרים של חסר מולד של תירוגלובולין, תתקבל כצפוי תוצאת T4 נמוכה, למרות שאין פגיעה בתפקוד התירואיד. מדידת TSH רגישה יותר לזיהוי היפותירואידיזם ראשוני, אם כי TSH יכול להתקבל נמוך בחסר של TBG הקליטה של T3 היא גבוהה. ידועים גם מקרים של היפו- או היפר-תירוקסינמיה. במקרים של תוצאות T4 נמוכות המתגלות בסקר ראשוני, חייבים לבצע בדיקה מאשרת חוזרת, שיש הכוללים בה מדידת T4 משולבת במדידת TSH ולעתים אף מדידת T3 וכן TBG.
שימושים רפואיים בהורמוני התירואיד
T4 וכן T3 משמשים לטיפול במקרים של תת-תריסיות. שני ההורמונים נספגים היטב במעי ולכן ניתן הטיפול באופן פומי. הצורה הפיזיולוגית של T4 ידועה כ-levothyroxine, והיא עוברת בגוף פירוק מטבולי איטי יותר מאשר T3, לכן היא ניתנת בטיפול יומי אחד בלבד. ניתן להשתמש בתכשירים טבעיים של ההורמון שעברו תהליך ייבוש מיוחד, ומקורם בבלוטת התירואיד של חזירים, אך ידוע שתכשיר "טבעי" זה מכיל בנוסף ל-T4, כ-20% של T3 וכן עקבות של T2, כמו גם T1 וקלציטונין. תירוקסין בודד לראשונה מחזירים במאיו-קליניק בשנת 1914, וסונתז לראשונה על ישי כימאים בריטיים בשנת 1927. הטיפול ב-L- תירוקסין הידוע בשם המותג Eltroxine יעיל גם במקרים של זפק (goiter), שכן הוא מפחית את רמת TSH המשרה זפק.
המינון היומי המקובל הוא טבלית אחת של 25 מיקרוגרם, כאשר מינוני יתר עלולים להבא לתופעות לוואי בין 6 שעות למספר ימים לאחר מינון היתר. כיוון ש- levothyroxine מכיל תירוקסין טהור, הוא לא יהיה יעיל לטיפול באלה שאינם מסוגלים להמיר T4 ל-T3, ולכן באחרונים יומלץ ליטול את התכשיר הטבעי המכיל גם T3 או לחילופין להיות מטופלים בתכשיר T3 סינטתי (liothyronine).
הורמוני תירואיד בדרך כלל נסבלים היטב ללא תופעות תוואי ניכרות, ואינם מסוכנים לשימוש על ידי נשים הרות או מניקות. יוצא דופן אחד הוא שהורמוני התירואיד עלולים להחמיר את תפקוד הלב במטופלים בגיל מתקדם, ובאלה רצוי להתחיל את הטיפול במינוניים נמוכים ולהעלותם בהדרגה כל זאת על ידי פיקוח רפואי הדוק.
תרופות המשפיעות להעלאת רמת סך-T4
גלולות למניעת הריון, אסטרוגנים, amiodarone, אמפטמינים, D-T4 או דקסטרו-תירוקסין, הרואין, clofibrate ,perphenazine, מתאדון, levaterenol ,levodopa, פרופרנולול, שתיית חומרי ניגוד דוגמת iopanoic acid או ipodate בהדמיה של דרכי מרה, טיפול ב-dinoprost tromethamine (תחליף לפרוסטגלנדין F2α), מתן תכשירי תירואיד, TSH ו-TRH. טיפול בהפארין ייתן אף הוא רמה מוגברת של T4, אך זאת לא באופן פיזיולוגי אלא בגלל השפעת אנאליטית של הפארין.
תרופות המשפיעות בהורדת רמת סך-T4
סליצילאטים במינון גבוה, diphenylhydantoin, כלורפרומאזין, נוגדי פרכוסים דוגמת פניטואין או חומצה ואלפרואית, טסטוסטרון, tolbutamide ,reserpine, פניצילין, ליתיום, קורטיקוסטרואידים, קורטיקוטרופין, danazol, אנדרוגנים, asparaginase, אספירין, ריפמפיצין, חומצה אמינוסאליצילית, סולפונאמידים, סומאטוטרופין, isotretinoin ,propylthiouracil ,T3 ,methymazole ,oxyphenbutazone ,phenylbutazone, iodides ,aminoglutethimide ,amiodarone (לעתים נדירות), הורמון גדילה (השפעה קלה), ethionamide וכן furosemide (במינונים גבוהים). גם התכשיר goitrin שהוא נגזר מכיל גפרית של oxazolidine מעכב יעיל של יצירת T4 על ידי שהוא מעכב את שלב חמצון היודיד.
אינטראקציות של תרופות, תכשירים ופריטי מזון עם טיפול בהורמוני תירואיד
יש להימנע מנטילת תכשירי סידן או ברזל 4 שעות לפני נטילת תירוקסין., וכן יש להימנע מצריכת מאכלי סויה עד 3 שעות לפני טיפול בתירוקסין, שכן אלה מפריעים בתהליך ספיגת ההורמון. מיץ ענבים מעכב את הספיגה אך אינו מונע אותה. ליתיום יכול לגרום בנסיבות שונות להגברת האפקט של אלתרוקסין או לעיכובו. חומרים אחרים המפחיתים ספיגת תירוקסין הם תכשירים המכילים אלומיניום ומגנזיום, כגון antacids ,simethicone או sucralfate ,cholestyramine ,colestipol ,kayexcalate.
מבחן היחס בין תירוקסין ל-TBG או T4/TBG ratio: מבחן זה שימושי באותם מקרים בהם רמות TBG משתנות מסיבות משניות, מה שלול להשפיע על רמת סך-T4. היחס הנמדד מייצג תוצאה מקורבת לריכוזי תירוקסין חופשי (fT4). תחום התוצאות התקין של מבחן זה הוא 3-5, והוא מייצג את היחס בין T4 מבוטא במיקרוגרם לד"ל לבין TBG המבוטא במיליגרם לד"ל.
תוצאות מוגברות של היחס T4/TBG, מתקבלות במצבי היפרתירואידיזם, במצבים של חסר מוּלד של TBG, ובתרחיש של familial dysalbuminemic hyper thyroxinemia. תוצאות מופחתות של היחס T4/TBG, מתקבלות במצבי היפותירואידיזם, בטרימסטר השלישי להיריון, ובמצבים של עודף מוּלד של TBG.
- סיבות לקישור מוגבר של T4 ל-TBG
בסמוך ללידה יש זיקה גדולה יותר ל- TBG, וסיבות נוספות כוללות טיפול באסטרוגנים, גלולות למניעת הריון, הרואין, מתאדון, 5-פלואורו-אוראציל, clofibrate. כן גדל הקישור של תירוקסין ל-TBG בהפאטיטיס (חריפה או כרונית), בצמרת מרתית ראשונית, ב-acute intermittent porphyria, בלימפוסארקומה, וכמובן בפגם מולד של TBG מוגבר.
- סיבות לקישור מופחת של T4 ל-TBG
מפגעים בהם רמות חלבונים בדם מופחתות דוגמת תסמונת נפרוטית, באקרומגליה, במחלות כבד שונות, מצבי עקה חריפה, טיפולים תרופתיים באנדרוגנים, סטרואידים מטבוליים, פרדניזון, ובפגם מולד של חסר TBG.
הוראות לביצוע הבדיקה
אין צורך בצום או בהכנות מיוחדות. יש לקחת דם במחנה כימיה (פקק אדום או צהוב) ובשום פנים לא להשתמש במבחנת הפארין (פקק ירוק). דגימת הנסיוב יציבה 7 ימים בטמפרטורת החדר, אך עדיף לאחסן בקירור. בהקפאה ניתן לאחסן עד 30 יום. דגימות המוליטיות עלולות להפריע לביצוע במדידה באופן שיש נטייה לתוצאות מופחתות. אין להשתמש בדגימות ליפמיות.
ראו גם


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק