הבדלים בין גרסאות בדף "אדנוזין דאמינאזה - Adenosine deaminase"
מ (שיפור קל) |
|||
| (3 גרסאות ביניים של 2 משתמשים אינן מוצגות) | |||
| שורה 9: | שורה 9: | ||
|יחידות מדידה=U/L | |יחידות מדידה=U/L | ||
|טווח ערכים תקין= | |טווח ערכים תקין= | ||
| − | '''בשיטת מדידה קולורימטרית''' באורך גל 340 ננומטר בטמפ. C°37 בנסיוב:{{ש}}גיל | + | '''בשיטת מדידה קולורימטרית''' באורך גל 340 ננומטר בטמפ. C°37 בנסיוב:{{ש}}גיל 0–2 שנים - 22.4±3.8; גיל 3–5 שנים - 19.6±4.0; גיל 6–8 שנים - 18.1±3.1; גיל 9–11 שנים - 15.8±2.6; גיל 12–14 שנים - 13.7±2.6; גיל 20–30 שנים - 12.6±2.0.{{ש}}'''בשיטת מדידה פלואורסצנטית''' של טיפות דם מיובשות על נייר סופג:{{ש}}ביילודים - <div style="text-align: left; direction: ltr">750-1,850 mU/gHb;</div>{{ש}}במבוגרים -<div style="text-align: left; direction: ltr">700-1,900 mU/g Hb.</div>{{ש}}'''בשיטת מדידה ספקטרופוטומטרית''' בהמוליזאט של תאי דם אדומים:{{ש}}<div style="text-align: left; direction: ltr">1.11±0.23 U/g Hb;{{כ}} 32.3±6.67 U/10<sup>12</sup>erythrocytes;{{כ}} 0.377±0.078 U/ml rythrocytes |
| − | </div>{{ש}}'''בנוזל פלאורלי''': פחות מ- | + | </div>{{ש}}'''בנוזל פלאורלי''': פחות מ-30–40 U/L. |
|יוצר הערך=[[משתמש:בן עמי סלע|פרופ' בן-עמי סלע]] | |יוצר הערך=[[משתמש:בן עמי סלע|פרופ' בן-עמי סלע]] | ||
|אחראי הערך= | |אחראי הערך= | ||
}} | }} | ||
| − | |||
| − | |||
==מטרת הבדיקה== | ==מטרת הבדיקה== | ||
| + | מדידת רמת האנזים ADA בנסיוב, בכדוריות דם אדומות או בדגימת דם מיובש מסייעת לאתר מקרים של תסמונת הכשל החיסוני המשולב הקשה (SCID). מדידת רמת האנזים בנוזל הצדר (pleural fluid) מסייעת בהערכה או בשלילה של תרחיש שחפתי מהדבקה ב- Mycobacterium tuberculosis של הנוזל הפלאורלי, מה שעשוי לסייע באבחון שחפת. בדיקה זו עשויה להידרש כאשר נבדק עם כאבים בחזה, חולשה, שיעול כרוני טורדני, כיח דמי, חום, צמרמורות, זיעת לילה מרובה, איבוד משקל בלתי מוסבר, ו/או קשיי נשימה נחשד כמי שנדבק בשחפת שהתפשטה לעטיפת צדר הריאות. | ||
| − | |||
| − | |||
==בסיס פיזיולוגי== | ==בסיס פיזיולוגי== | ||
| − | |||
האנזים ADA הוא אנזים מפתח במטבוליזם של פורינים. האנזים גורם לדאמינציה בלתי הפיכה של adenosine ומסב אותו לנוקלאוזיד inosine, על ידי המרה של שייר אמינו על ידי שייר הידרוקסיל. ה-inosine יכול להיות מורחק מה-ribose אליו הוא קשור על ידי האנזים PNP או purine nucleoside phosphorylase, ליצירת hypoxanthine. | האנזים ADA הוא אנזים מפתח במטבוליזם של פורינים. האנזים גורם לדאמינציה בלתי הפיכה של adenosine ומסב אותו לנוקלאוזיד inosine, על ידי המרה של שייר אמינו על ידי שייר הידרוקסיל. ה-inosine יכול להיות מורחק מה-ribose אליו הוא קשור על ידי האנזים PNP או purine nucleoside phosphorylase, ליצירת hypoxanthine. | ||
===איזופורמים=== | ===איזופורמים=== | ||
| − | |||
לאנזים ADA שני איזופורמים, ADA1 ו-ADA2. את ADA1 מוצאים ברוב תאי הגוף, בעיקר בלימפוציטים ומקרופאגים, שם האנזים מופיע לא רק בציטופלזמה ובגרעין אלא גם על פני ממברנת התא מחובר ל-4dipeptidyl peptidase ליצירת המרכיב הממברנלי CD26. לעומתו, ADA1 כרוך בעיקר בפעילות תוך-תאית ומופיע בצורת מונומר או דימר. לאנזים שני שיירי thiol פעילים. | לאנזים ADA שני איזופורמים, ADA1 ו-ADA2. את ADA1 מוצאים ברוב תאי הגוף, בעיקר בלימפוציטים ומקרופאגים, שם האנזים מופיע לא רק בציטופלזמה ובגרעין אלא גם על פני ממברנת התא מחובר ל-4dipeptidyl peptidase ליצירת המרכיב הממברנלי CD26. לעומתו, ADA1 כרוך בעיקר בפעילות תוך-תאית ומופיע בצורת מונומר או דימר. לאנזים שני שיירי thiol פעילים. | ||
| − | האיזופורם ADA2 התגלה לראשונה בטחול באדם ושם ריכוזו הגבוה ביותר, אך ניתן למצאו ברקמות נוספות כולל במקרופאגים ובמונוציטים בהם הוא נמצא ביחד עם ADA1. ניתן למצוא את ADA2 בעיקר בפלזמת הדם בה הוא מופיע רק כמונומר. | + | האיזופורם ADA2 התגלה לראשונה בטחול באדם ושם ריכוזו הגבוה ביותר, אך ניתן למצאו ברקמות נוספות כולל במקרופאגים ובמונוציטים בהם הוא נמצא ביחד עם ADA1. ניתן למצוא את ADA2 בעיקר בפלזמת הדם בה הוא מופיע רק כמונומר. |
===מבנה האנזים ADA ומנגנון פעולתו=== | ===מבנה האנזים ADA ומנגנון פעולתו=== | ||
| − | |||
בצורתו המונומרית האנזים הוא פוליפפטיד חד-שרשרתי, המקופל לשמונה גדילים מקבילים של α/β barrels, שבמרכזם "כיס" עמוק המהווה את האתר הפעיל של האנזים. אתר פעיל זה מכיל יון אבץ בודד, שהקואורדינציה שלו נקבעת על ידי 5 אטומים: ארבעה שיירי His15, His17, His214 ו-Asp295 של האנזים וכן שייר נוסף על פני adenosine, המצע של האנזים. אבץ הוא קו-פקטור הנחוץ לפעילות האנזים. האנזים נקשר למצע שלו adenosine תוך יצירת תשעה קשרי מימן. | בצורתו המונומרית האנזים הוא פוליפפטיד חד-שרשרתי, המקופל לשמונה גדילים מקבילים של α/β barrels, שבמרכזם "כיס" עמוק המהווה את האתר הפעיל של האנזים. אתר פעיל זה מכיל יון אבץ בודד, שהקואורדינציה שלו נקבעת על ידי 5 אטומים: ארבעה שיירי His15, His17, His214 ו-Asp295 של האנזים וכן שייר נוסף על פני adenosine, המצע של האנזים. אבץ הוא קו-פקטור הנחוץ לפעילות האנזים. האנזים נקשר למצע שלו adenosine תוך יצירת תשעה קשרי מימן. | ||
| שורה 38: | שורה 32: | ||
# ריאקצית קינטיקה מסדר שני Sn2. | # ריאקצית קינטיקה מסדר שני Sn2. | ||
| − | בכל אחד משני המנגנונים המוצעים, יון אבץ משמש כאלקטרופיל חזק המשפעל מוליקולת מים, העוברת דפרוטונציה על ידי שייר Asp295 הבסיסי ליצירת הידרוקסיד פעיל ותוקף. באותה עת מכוון שייר His238 את מולקולת המים ומייצב את המטען החשמלי של ההידרוקסיד התוקף. שייר Glu217 עובר דפרוטונציה כדי לתרום פרוטון לשייר N1 של המצע אדנוזין. הריאקציה היא סטראוספציפית בגלל מיקומו של שייר האבץ ושיירי Asp295 ו-His238, שכולם פונים לאותו צד של טבעת הפורין של מצע האדנוזין. | + | בכל אחד משני המנגנונים המוצעים, יון אבץ משמש כאלקטרופיל חזק המשפעל מוליקולת מים, העוברת דפרוטונציה על ידי שייר Asp295 הבסיסי ליצירת הידרוקסיד פעיל ותוקף. באותה עת מכוון שייר His238 את מולקולת המים ומייצב את המטען החשמלי של ההידרוקסיד התוקף. שייר Glu217 עובר דפרוטונציה כדי לתרום פרוטון לשייר N1 של המצע אדנוזין. הריאקציה היא סטראוספציפית בגלל מיקומו של שייר האבץ ושיירי Asp295 ו-His238, שכולם פונים לאותו צד של טבעת הפורין של מצע האדנוזין. |
===פתופיזיולוגיה=== | ===פתופיזיולוגיה=== | ||
| + | תפקיד מרכזי של ADA הוא בהרחקת המטבוליט deoxyadenosine הנוצר בשבירת DNA שהוא רעיל ללימפוציטים, על ידי הסבתו ל-deoxyinosine שאינו רעיל. חסר האנזים יביא להצטברות deoxyadenosine ולנזק ללימפוציטים. לימפוציטים בלתי בשלים בתימוס רגישים במיוחד ל-deoxyadenosine, אך גם הלימפוציטים ברקמות אחרות רגישים לנזק זה ומספרם פוחת מה שגורם לתסמיני SCID. האיזופורם של ADA שהחסר שלו נכרך במצבי SCID הוא ADA1. | ||
| − | + | חסר באנזים ADA גורם להצטברות deoxyadenosine, מה שגורם להעלאת הרמה של dATP בכל התאים, מה שמעכב את פעילות ribonucleotide reductase ומונע סינתזת DNA, והתחלקות תאים. כיון שתאי T ו-B הם תאים בעלי פעילות מיטוטית חזקה, הם רגישים במיוחד לחסר ADA. גם תאי NK נפגעים בחסר ADA. חסר ADA גורם גם לעליה ברמת S-adenosylhomocysteine, חומר רעלני ללימפוציטים בלתי בשלים, הפוגע ביכולתם להבשיל ללימפוציטים בוגרים. כיוון שתאי T משגשגים ומתפתחים בבלוטת ההרת (טימוס), באלה עם חסר ב-ADA מוצאים בדרך כלל טימוס קטן ומפותח באופן חלקי. כתוצאה מכך מערכת החיסון נפגעת קשות. | |
| − | חסר באנזים ADA | + | חסר באנזים ADA היא מחלה תורשתית המועברת באופן אוטוזומאלי-רצסיבי. האנזים מקודד באדם על ידי גן הממוקם על כרומוזום 20. האוניברסליות של אנזים זה באה לביטוי בעובדה שהוא מופיע גם בחיידקים, בצמחים, בחסרי ובבעלי חוליות, כאשר בכל אלה יש דרגת זהות גבוהה ברצף חומצות האמינו של האנזים. האנזים פעיל למעשה בכל תאי הגוף ביונקים, אך הוא פעיל במיוחד בלימפוציטים כאשר תפקידו העיקרי באדם הוא בהתפתחות ובייצוב מערכת החיסון. ADA קשור גם להתמיינות של תאי אפיתל, בהעברת מסרים עצביים (neurotransmission), ובשמירת ההיריון. |
| − | + | חסר באנזים ADA נכרך לעיתים בתרחישים של דלקת ריאות, מוות של תאי טימוס ואיתות (signaling) פגום של קולטן תאי T. האיזופורם ADA2 היא הצורה הדומיננטית בפלזמה והוא מוגבר במספר מחלות, בעיקר אלה הכרוכות במפגעי מערכת החיסון כגון rheumatoid arthritis, פסוריאזיס וסרקואידוזיס. רמת ADA2 מוגברת בפלזמה ברוב המחלות הסרטניות. | |
| − | |||
| − | חסר באנזים ADA נכרך | ||
===האנזים ADA ומחלת הכשל החיסוני המשולב הקשה ([[SCID]])=== | ===האנזים ADA ומחלת הכשל החיסוני המשולב הקשה ([[SCID]])=== | ||
| + | תסמונת נדירה המשלבת פגיעה תאית והומוראלית, בה הפגם גורם לנטייה קיצונית ללקות בזיהומים קשים ומהלך ממית בגיל תינוקות, בהיעדר אבחנה וטיפול מהירים. הטיפול כולל בידוד קפדני והקניית מערכת חיסון חדשה. | ||
| − | + | התסמונת גורמת לפגם קשה בהתפתחות ותפקוד לימפוציטים מסוג T ו-B ובמקרים מסוימים מערבת גם הפרעה בלימפוציטי NK. וקיימים כ־12 וריאנטים גנטיים שונים שלה. השכיח ביותר הם (כ־46% מהמקרים) נובע מחסר המרכיב גמא בקולטן למספר ציטוקינים שונים (2, 4, 7, 9, 15, 21), שמועבר בתאחיזה לכרומוזום ה- X ומתבטא בבנים. שאר הפגמים הגנטיים הגורמים למחלה הקשה מועברים בתאחיזה אוטוסומלית רצסיבית, כאשר חסר ב-ADA מהווה כ-16% (ראו איור). | |
| − | |||
| − | התסמונת | ||
| − | |||
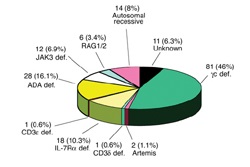
[[קובץ:אדנוזין.jpg|מרכז|ממוזער|800px|שכיחות הוריאנטים הגנטיים השונים הגורמים לתסמונת החסר החיסוני המשולב הקשה]] | [[קובץ:אדנוזין.jpg|מרכז|ממוזער|800px|שכיחות הוריאנטים הגנטיים השונים הגורמים לתסמונת החסר החיסוני המשולב הקשה]] | ||
| + | רוב אלה עם חסר ADA מאובחנים עם SCID ב-6 חודשי החיים הראשונים. ב-10-15% מהמקרים, ההופעה של החסר החיסוני מתעכבת עד לגיל 6–24 חודשים או אפילו עד לגיל הבגרות. בצורות המחלה המאוחרות היא מתונה יותר במהלכה ומתבטאת בעיקר בהדבקות חוזרות של דרכי הנשימה העליונים, ובדלקות אוזניים. עם הזמן עלולה להתפתח מחלת ריאות כרונית, אלרגיות ובעיות רפואיות אחרות. ניתן לזהות חסר ב-ADA כבר בחודשי ההיריון תוך שימוש בסיסי שליה, או שניתן למדוד רמתו בדגימת דם טבורי. | ||
| + | חסר ב-ADA מאוד נדיר, ומוערך כמקרה אחד לכל 200,000 עד מיליון לידות באוכלוסיות אתניות שונות. חסר ב-ADA אחראי ל-15% מכלל מקרי SCID או severe combined immunodeficiency, והתסמינים הקליניים שלו יכולים להתגלות בינקות, בילדות, בשנות הנעורים או בבגרות, כאשר גיל הופעתם ודרגת חומרתם תלויה ב-29 הגנוטיפים השונים שאופיינו עד עתה, הכרוכים בחסר ADA. מדי שנה מאובחנים בארצות הברית 10–20 ילדים עם חסר האנזים. | ||
| − | + | הטיפול בחסר ADA: אין תרופה של ממש אך נעשים ניסיונות להגביר רמות ADA על ידי השתלת מח עצם מתאום, עירוי של תאי דם אדומים מתורם בריא המכילים רמות גבוהות של ADA, הזרקת האנזים החסר, תרפיה גנית על ידי החדרה של DNA סינתטי המכיל את הגן התקין ל-ADA, לתוך תאי חיסון. Gene therapy נערך לראשונה בספטמבר 1990 ב-NIH לילדה בת 4 שנים. | |
| − | |||
| − | |||
| − | |||
| − | הטיפול בחסר ADA: אין תרופה של ממש אך נעשים ניסיונות להגביר רמות ADA על ידי השתלת מח עצם מתאום, עירוי של תאי דם אדומים מתורם בריא המכילים רמות גבוהות של ADA, הזרקת האנזים החסר, תרפיה גנית על ידי החדרה של DNA סינתטי המכיל את הגן התקין ל-ADA, לתוך תאי חיסון. Gene therapy נערך לראשונה בספטמבר 1990 ב-NIH לילדה בת 4 שנים. | ||
השתלת תאי גזע המטופואטיים אלוגניים מותאמים אנטיגנית בתרחיש SCID כתוצאה מחסר ADA עשוי להביא להחלמה אימונולוגית ארוכת טווח ולתיקון מטבולי, אם כי במקרים שהשתלת מח עצם בלתי תואמת יופיעו תחלואה ותמותה ניכרים. יש דיווחים על ניסויים בהיקף קטן של טיפול בילדים ללא תורם בעל HLA זהה, שעברו אבלציה של מח העצם עם busulfan, וקבלו עירוי של תאי אב ותאי מח עצם אוטולוגיים (+CD34), שעברו טרנסדוקציה עם vector גאמא-רטרו-ויראלי עם DNA המקודד ל-ADA. תוצאות מעקב חציוני לאחר 43 חודשים היו מעודדות, כאשר כל המטופלים היו בחיים, עם השתלבות יציבה של תאי הגזע ההמטופויטים שניתנו. תאים אלה עברו התמיינות לתאים מיאלואידים המכילים פעילות ADA. מחקר ברוח זו התפרסם בינואר 2009 ב-New England Journal of Medicine. | השתלת תאי גזע המטופואטיים אלוגניים מותאמים אנטיגנית בתרחיש SCID כתוצאה מחסר ADA עשוי להביא להחלמה אימונולוגית ארוכת טווח ולתיקון מטבולי, אם כי במקרים שהשתלת מח עצם בלתי תואמת יופיעו תחלואה ותמותה ניכרים. יש דיווחים על ניסויים בהיקף קטן של טיפול בילדים ללא תורם בעל HLA זהה, שעברו אבלציה של מח העצם עם busulfan, וקבלו עירוי של תאי אב ותאי מח עצם אוטולוגיים (+CD34), שעברו טרנסדוקציה עם vector גאמא-רטרו-ויראלי עם DNA המקודד ל-ADA. תוצאות מעקב חציוני לאחר 43 חודשים היו מעודדות, כאשר כל המטופלים היו בחיים, עם השתלבות יציבה של תאי הגזע ההמטופויטים שניתנו. תאים אלה עברו התמיינות לתאים מיאלואידים המכילים פעילות ADA. מחקר ברוח זו התפרסם בינואר 2009 ב-New England Journal of Medicine. | ||
===ADA ונוזל פלאורלי לזיהוי שחפת=== | ===ADA ונוזל פלאורלי לזיהוי שחפת=== | ||
| − | |||
תרחישים המגרים את מערכת החיסון כגון הידבקות בחיידק השחפת, יכולים להגביר את רמות האנזים ADA באזורים בהם יש נוכחות של החיידק. כיוון שקרומי הצדר עוטפים את חלל החזה, כמויות קטנות של נוזל צדר נוצרות לצורך סיכה של הריאות הנעות ומתחככות בקרומים אלה בשעת שאיפה ונשיפה. מנגד, יש מגוון של תרחישים קליניים בהם נגרמת דלקת של קרומי הפלאורה (pleuritis) מה שגורם להצטברות מוגברת של נוזל פלאורלי (pleural effusion). | תרחישים המגרים את מערכת החיסון כגון הידבקות בחיידק השחפת, יכולים להגביר את רמות האנזים ADA באזורים בהם יש נוכחות של החיידק. כיוון שקרומי הצדר עוטפים את חלל החזה, כמויות קטנות של נוזל צדר נוצרות לצורך סיכה של הריאות הנעות ומתחככות בקרומים אלה בשעת שאיפה ונשיפה. מנגד, יש מגוון של תרחישים קליניים בהם נגרמת דלקת של קרומי הפלאורה (pleuritis) מה שגורם להצטברות מוגברת של נוזל פלאורלי (pleural effusion). | ||
| − | זיהוי חיידקי מיקובקטריום בנוזל הפלאורה עלול להיות מסובך, הן בשל נפח נוזל גדול ומספר מאוד קטן של חיידקים הנמצאים בו בעת נתונה. | + | זיהוי חיידקי מיקובקטריום בנוזל הפלאורה עלול להיות מסובך, הן בשל נפח נוזל גדול ומספר מאוד קטן של חיידקים הנמצאים בו בעת נתונה. אף על פי שמבדק ADA אינו ספציפי ולא יכול להחליף תרבית של נוזל פלאורלי לזיהוי חיידק השחפת, תוצאת מבדק זה יכולה להיות חיובית אפילו בנוכחות מספר זעום של חיידקי שחפת, ולכן נוטים להשתמש בו כמבדק עזר במקביל למבדקי PCR המולקולארי ול-acid-fast bacillus (AFB) smear and culture לסיוע באבחון המחלה. |
המגבלות של שיטות אחרות לגילוי נוכחות של חיידקי שחפת בנוזל הפלאורלי נובעות מרגישותן הנמוכה. ברוב המקרים הצביעה של AFB מתקבלת שלילית, ורק ב-25% ממקרי שחפת מוכחת מתקבלת תרבית חיובית למיקובקטריה. מנגד, ביופסיה פלאורלית תדגים granulonatous pleuritis ב-80% של נבדקים עם TPE או tuberculous pleural effusion. | המגבלות של שיטות אחרות לגילוי נוכחות של חיידקי שחפת בנוזל הפלאורלי נובעות מרגישותן הנמוכה. ברוב המקרים הצביעה של AFB מתקבלת שלילית, ורק ב-25% ממקרי שחפת מוכחת מתקבלת תרבית חיובית למיקובקטריה. מנגד, ביופסיה פלאורלית תדגים granulonatous pleuritis ב-80% של נבדקים עם TPE או tuberculous pleural effusion. | ||
| שורה 79: | שורה 67: | ||
;תרחישים קליניים בהם רמת ADA בפלזמה מוגברת | ;תרחישים קליניים בהם רמת ADA בפלזמה מוגברת | ||
| − | הפאטיטיס, צמקת הכבד (צירוזיס), המוכרומאטוזיס, צהבת חסימתית הכרוכה במחלה ממארת, סרטן הערמונית ושלפוחית השתן, אנמיה המוליטית, rheumatoid fever ,typhoid fever, צינית (gout), בהתקפים חריפים של סרקואידוזיס, תלסמיה מאיור, לויקמיה מיאלואידית, שחפת, איידס, מחלות אוטואימוניות, אי-ספיקת לב, infectious mononucleosis. יש לציין שבצורה נדירה של אנמיה המוליטית מולדת (אוטוזומאלית שלוטנית) רמת ADA גבוהה פי | + | [[הפאטיטיס]], [[צמקת הכבד]] (צירוזיס), המוכרומאטוזיס, צהבת חסימתית הכרוכה במחלה ממארת, [[סרטן הערמונית]] ושלפוחית השתן, [[אנמיה המוליטית]], rheumatoid fever ,typhoid fever, צינית (gout), בהתקפים חריפים של סרקואידוזיס, תלסמיה מאיור, [[לויקמיה מיאלואידית]], [[שחפת]], [[איידס]], מחלות אוטואימוניות, [[אי-ספיקת לב]], infectious mononucleosis. יש לציין שבצורה נדירה של אנמיה המוליטית מולדת (אוטוזומאלית שלוטנית) רמת ADA גבוהה פי 35–70 מהרמה הנורמאלית. |
;תרחישים בהם רמת ADA בפלזמה פחותה | ;תרחישים בהם רמת ADA בפלזמה פחותה | ||
| שורה 85: | שורה 73: | ||
;תרחישים בהם רמת ADA מוגברת בנוזל פלאורלי | ;תרחישים בהם רמת ADA מוגברת בנוזל פלאורלי | ||
| − | שחפת. רמה של ADA מעל U/L 40 אינה תקינה ומחשידה לשחפת ואילו רמת אנזים בנוזל הפלאורלי מעל U/L100 ספציפית במידה רבה לשחפת. כאשר רמת ADA בנוזל הפלאורלי מוגברת באופן מתון באזור | + | שחפת. רמה של ADA מעל U/L 40 אינה תקינה ומחשידה לשחפת ואילו רמת אנזים בנוזל הפלאורלי מעל U/L100 ספציפית במידה רבה לשחפת. כאשר רמת ADA בנוזל הפלאורלי מוגברת באופן מתון באזור גאוגרפי עם שכיחות נמוכה של שחפת, ייתכן שהעלייה ברמת ADA פלאורלי נובעת מסיבה אחרת כמו לימפומה, תסחיף ריאתי, סרקואידוזיס, .SLE. |
רמה נמוכה של ADA בנוזל פלאורלי מפחיתה את הסבירות לאבחון שחפת, אך עדיין אינה שוללת לחלוטין אבחון של שחפת, שכן רמת האנזים יכולה להיות מוגברת בנוזלי גוף אחרים כגון נוזל פריטונאלי, או CSF. | רמה נמוכה של ADA בנוזל פלאורלי מפחיתה את הסבירות לאבחון שחפת, אך עדיין אינה שוללת לחלוטין אבחון של שחפת, שכן רמת האנזים יכולה להיות מוגברת בנוזלי גוף אחרים כגון נוזל פריטונאלי, או CSF. | ||
==הוראות לביצוע הבדיקה== | ==הוראות לביצוע הבדיקה== | ||
| − | |||
רמת ADA בפלזמה יכולה להימדד בטכנולוגיית HPLC, או בשיטות אנזמטיות או קולורימטריות. בשיטה הפשוטה ביותר על ידי מדידת רמת אמוניה המשתחררת מ-adenosine כאשר זה מתפרק ל-inosine . לאחר הדגרה של פלזמה בתמיסת בופר של אדנוזין, מגיבה אמוניה עם ריאגנט Berthelot ליצירת צבע כחול במתאם עם רמת פעילות האנזים. כדי למדוד פעילות ADA2, מוסיפים טרם התחלת הריאקציה את הריאגנט EHNA או erythro-9-(2-hydroxy-3-nonyl) adenine, כדי לעכב את פעילות האנזים ADA1 בפלזמה. | רמת ADA בפלזמה יכולה להימדד בטכנולוגיית HPLC, או בשיטות אנזמטיות או קולורימטריות. בשיטה הפשוטה ביותר על ידי מדידת רמת אמוניה המשתחררת מ-adenosine כאשר זה מתפרק ל-inosine . לאחר הדגרה של פלזמה בתמיסת בופר של אדנוזין, מגיבה אמוניה עם ריאגנט Berthelot ליצירת צבע כחול במתאם עם רמת פעילות האנזים. כדי למדוד פעילות ADA2, מוסיפים טרם התחלת הריאקציה את הריאגנט EHNA או erythro-9-(2-hydroxy-3-nonyl) adenine, כדי לעכב את פעילות האנזים ADA1 בפלזמה. | ||
לפני ביצוע הבדיקה יש להפסיק ליטול תרופות על בסיס sodium benzoate בהן משתמשים לטיפול בתרחישי hyperammonemia. זאת כיוון שבפירוק אדנוזין משתחררת אמוניה, הנקשרת לסודיום בנזואט. אין להשתמש לצורך מדידה רמת ADA בדגימות דם המכילות p-chloromercuribenzoate, שהוא מעכב פרוטאזות מקובל בביולוגיה מולקולארית, כיון שהתוצאות שתתקבלנה בנוכחות חומר זה מראות רמה נמוכה כזובה של ADA. אם מודדים רמת ADA בדגימת דם של מטופל הנוטל dipyridamole (המשמש כנוגד-צימות תסיות במנותחי חזה ולטיפול מונע בתעוקת החזה) עלולים לקבל תשובה שלילית כזובה שכן תכשיר זה מעכב פעילות האנזים. | לפני ביצוע הבדיקה יש להפסיק ליטול תרופות על בסיס sodium benzoate בהן משתמשים לטיפול בתרחישי hyperammonemia. זאת כיוון שבפירוק אדנוזין משתחררת אמוניה, הנקשרת לסודיום בנזואט. אין להשתמש לצורך מדידה רמת ADA בדגימות דם המכילות p-chloromercuribenzoate, שהוא מעכב פרוטאזות מקובל בביולוגיה מולקולארית, כיון שהתוצאות שתתקבלנה בנוכחות חומר זה מראות רמה נמוכה כזובה של ADA. אם מודדים רמת ADA בדגימת דם של מטופל הנוטל dipyridamole (המשמש כנוגד-צימות תסיות במנותחי חזה ולטיפול מונע בתעוקת החזה) עלולים לקבל תשובה שלילית כזובה שכן תכשיר זה מעכב פעילות האנזים. | ||
| − | מדידת רמת האנזים מתבצעת בנסיוב כאשר דגימת הדם נלקחת במבחנה כימית (פקק אדום או צהוב). הדגימה יציבה בטמפרטורת החדר למשך | + | מדידת רמת האנזים מתבצעת בנסיוב כאשר דגימת הדם נלקחת במבחנה כימית (פקק אדום או צהוב). הדגימה יציבה בטמפרטורת החדר למשך 6–12 שעות, בקירור מעל שבוע, ובהקפאה במינוס 70 מעלות צלזיוס הדגימה יציבה 6 חודשים. |
אם הבדיקה מתבצעת בשיטה פלואורסצנטית על טיפות דם מיובשות על נייר פילטר כגון נייר גאטרי, הדגימה יציבה בטמפרטורת החדר עד שבוע, ואם מקפיאים את הנייר המכיל את הדם עטוף בניילון, הדגימה יציבה בערך חודש ימים. | אם הבדיקה מתבצעת בשיטה פלואורסצנטית על טיפות דם מיובשות על נייר פילטר כגון נייר גאטרי, הדגימה יציבה בטמפרטורת החדר עד שבוע, ואם מקפיאים את הנייר המכיל את הדם עטוף בניילון, הדגימה יציבה בערך חודש ימים. | ||
| − | אם הבדיקה מתבצעת במדידה ספקטרופוטומטרית בהמוליזאט של אריתרוציטים רחוצים, יש לדגום את הדם במבחנת ציטראט (פקק תכול), מבחנת ספירת דם (EDTA, פקק סגלגל) או מבחנת הפארין (פקק ירוק). כדוריות הדם לצורך מדידת ADA יציבות מעל 20 יום במבחנות ציטראט או ספירת דם מעל 20 יום בקירור, אך רק | + | אם הבדיקה מתבצעת במדידה ספקטרופוטומטרית בהמוליזאט של אריתרוציטים רחוצים, יש לדגום את הדם במבחנת ציטראט (פקק תכול), מבחנת ספירת דם (EDTA, פקק סגלגל) או מבחנת הפארין (פקק ירוק). כדוריות הדם לצורך מדידת ADA יציבות מעל 20 יום במבחנות ציטראט או ספירת דם מעל 20 יום בקירור, אך רק 5–7 ימים במבחנת הפארין בקירור. |
לצורך איסוף נוזל פלאורלי יש שימוש במזרק ומחט בפרוצדורה של thoracentesis. | לצורך איסוף נוזל פלאורלי יש שימוש במזרק ומחט בפרוצדורה של thoracentesis. | ||
| − | |||
| − | |||
| − | |||
==ראו גם== | ==ראו גם== | ||
* [[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | * [[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | ||
* [[בדיקות מערכת החיסון|בדיקות מעבדה - מערכת החיסון]] | * [[בדיקות מערכת החיסון|בדיקות מעבדה - מערכת החיסון]] | ||
| + | |||
| + | {{ייחוס בן עמי}} | ||
[[קטגוריה:בדיקות מעבדה - מערכת החיסון]] | [[קטגוריה:בדיקות מעבדה - מערכת החיסון]] | ||
[[קטגוריה:בדיקות מעבדה: כימיה בדם]] | [[קטגוריה:בדיקות מעבדה: כימיה בדם]] | ||
גרסה אחרונה מ־22:25, 10 בדצמבר 2021
| מדריך בדיקות מעבדה | |
| אדנוזין דאמינזה | |
|---|---|
| adenosine deaminase | |
| שמות אחרים | ADA |
| מעבדה | כימיה בדם וכימיה בנוזל הפלאורלי |
| תחום | הערכת חסר חיסוני משולב וחמור (SCID) והערכת שחפת |
| יחידות מדידה | U/L |
| טווח ערכים תקין | בשיטת מדידה קולורימטרית באורך גל 340 ננומטר בטמפ. C°37 בנסיוב: גיל 0–2 שנים - 22.4±3.8; גיל 3–5 שנים - 19.6±4.0; גיל 6–8 שנים - 18.1±3.1; גיל 9–11 שנים - 15.8±2.6; גיל 12–14 שנים - 13.7±2.6; גיל 20–30 שנים - 12.6±2.0. בשיטת מדידה פלואורסצנטית של טיפות דם מיובשות על נייר סופג: ביילודים - 750-1,850 mU/gHb; במבוגרים - 700-1,900 mU/g Hb. בשיטת מדידה ספקטרופוטומטרית בהמוליזאט של תאי דם אדומים: 1.11±0.23 U/g Hb; 32.3±6.67 U/1012erythrocytes; 0.377±0.078 U/ml rythrocytes
בנוזל פלאורלי: פחות מ-30–40 U/L. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
מדידת רמת האנזים ADA בנסיוב, בכדוריות דם אדומות או בדגימת דם מיובש מסייעת לאתר מקרים של תסמונת הכשל החיסוני המשולב הקשה (SCID). מדידת רמת האנזים בנוזל הצדר (pleural fluid) מסייעת בהערכה או בשלילה של תרחיש שחפתי מהדבקה ב- Mycobacterium tuberculosis של הנוזל הפלאורלי, מה שעשוי לסייע באבחון שחפת. בדיקה זו עשויה להידרש כאשר נבדק עם כאבים בחזה, חולשה, שיעול כרוני טורדני, כיח דמי, חום, צמרמורות, זיעת לילה מרובה, איבוד משקל בלתי מוסבר, ו/או קשיי נשימה נחשד כמי שנדבק בשחפת שהתפשטה לעטיפת צדר הריאות.
בסיס פיזיולוגי
האנזים ADA הוא אנזים מפתח במטבוליזם של פורינים. האנזים גורם לדאמינציה בלתי הפיכה של adenosine ומסב אותו לנוקלאוזיד inosine, על ידי המרה של שייר אמינו על ידי שייר הידרוקסיל. ה-inosine יכול להיות מורחק מה-ribose אליו הוא קשור על ידי האנזים PNP או purine nucleoside phosphorylase, ליצירת hypoxanthine.
איזופורמים
לאנזים ADA שני איזופורמים, ADA1 ו-ADA2. את ADA1 מוצאים ברוב תאי הגוף, בעיקר בלימפוציטים ומקרופאגים, שם האנזים מופיע לא רק בציטופלזמה ובגרעין אלא גם על פני ממברנת התא מחובר ל-4dipeptidyl peptidase ליצירת המרכיב הממברנלי CD26. לעומתו, ADA1 כרוך בעיקר בפעילות תוך-תאית ומופיע בצורת מונומר או דימר. לאנזים שני שיירי thiol פעילים.
האיזופורם ADA2 התגלה לראשונה בטחול באדם ושם ריכוזו הגבוה ביותר, אך ניתן למצאו ברקמות נוספות כולל במקרופאגים ובמונוציטים בהם הוא נמצא ביחד עם ADA1. ניתן למצוא את ADA2 בעיקר בפלזמת הדם בה הוא מופיע רק כמונומר.
מבנה האנזים ADA ומנגנון פעולתו
בצורתו המונומרית האנזים הוא פוליפפטיד חד-שרשרתי, המקופל לשמונה גדילים מקבילים של α/β barrels, שבמרכזם "כיס" עמוק המהווה את האתר הפעיל של האנזים. אתר פעיל זה מכיל יון אבץ בודד, שהקואורדינציה שלו נקבעת על ידי 5 אטומים: ארבעה שיירי His15, His17, His214 ו-Asp295 של האנזים וכן שייר נוסף על פני adenosine, המצע של האנזים. אבץ הוא קו-פקטור הנחוץ לפעילות האנזים. האנזים נקשר למצע שלו adenosine תוך יצירת תשעה קשרי מימן.
הוצעו 2 מנגנונים להסבר מנגנון הדאמינציה על ידי ADA:
- ריאקציה סטריאו-ספציפית תוך יצירת תוצר ביניים טטרה-הדראלי;
- ריאקצית קינטיקה מסדר שני Sn2.
בכל אחד משני המנגנונים המוצעים, יון אבץ משמש כאלקטרופיל חזק המשפעל מוליקולת מים, העוברת דפרוטונציה על ידי שייר Asp295 הבסיסי ליצירת הידרוקסיד פעיל ותוקף. באותה עת מכוון שייר His238 את מולקולת המים ומייצב את המטען החשמלי של ההידרוקסיד התוקף. שייר Glu217 עובר דפרוטונציה כדי לתרום פרוטון לשייר N1 של המצע אדנוזין. הריאקציה היא סטראוספציפית בגלל מיקומו של שייר האבץ ושיירי Asp295 ו-His238, שכולם פונים לאותו צד של טבעת הפורין של מצע האדנוזין.
פתופיזיולוגיה
תפקיד מרכזי של ADA הוא בהרחקת המטבוליט deoxyadenosine הנוצר בשבירת DNA שהוא רעיל ללימפוציטים, על ידי הסבתו ל-deoxyinosine שאינו רעיל. חסר האנזים יביא להצטברות deoxyadenosine ולנזק ללימפוציטים. לימפוציטים בלתי בשלים בתימוס רגישים במיוחד ל-deoxyadenosine, אך גם הלימפוציטים ברקמות אחרות רגישים לנזק זה ומספרם פוחת מה שגורם לתסמיני SCID. האיזופורם של ADA שהחסר שלו נכרך במצבי SCID הוא ADA1.
חסר באנזים ADA גורם להצטברות deoxyadenosine, מה שגורם להעלאת הרמה של dATP בכל התאים, מה שמעכב את פעילות ribonucleotide reductase ומונע סינתזת DNA, והתחלקות תאים. כיון שתאי T ו-B הם תאים בעלי פעילות מיטוטית חזקה, הם רגישים במיוחד לחסר ADA. גם תאי NK נפגעים בחסר ADA. חסר ADA גורם גם לעליה ברמת S-adenosylhomocysteine, חומר רעלני ללימפוציטים בלתי בשלים, הפוגע ביכולתם להבשיל ללימפוציטים בוגרים. כיוון שתאי T משגשגים ומתפתחים בבלוטת ההרת (טימוס), באלה עם חסר ב-ADA מוצאים בדרך כלל טימוס קטן ומפותח באופן חלקי. כתוצאה מכך מערכת החיסון נפגעת קשות.
חסר באנזים ADA היא מחלה תורשתית המועברת באופן אוטוזומאלי-רצסיבי. האנזים מקודד באדם על ידי גן הממוקם על כרומוזום 20. האוניברסליות של אנזים זה באה לביטוי בעובדה שהוא מופיע גם בחיידקים, בצמחים, בחסרי ובבעלי חוליות, כאשר בכל אלה יש דרגת זהות גבוהה ברצף חומצות האמינו של האנזים. האנזים פעיל למעשה בכל תאי הגוף ביונקים, אך הוא פעיל במיוחד בלימפוציטים כאשר תפקידו העיקרי באדם הוא בהתפתחות ובייצוב מערכת החיסון. ADA קשור גם להתמיינות של תאי אפיתל, בהעברת מסרים עצביים (neurotransmission), ובשמירת ההיריון.
חסר באנזים ADA נכרך לעיתים בתרחישים של דלקת ריאות, מוות של תאי טימוס ואיתות (signaling) פגום של קולטן תאי T. האיזופורם ADA2 היא הצורה הדומיננטית בפלזמה והוא מוגבר במספר מחלות, בעיקר אלה הכרוכות במפגעי מערכת החיסון כגון rheumatoid arthritis, פסוריאזיס וסרקואידוזיס. רמת ADA2 מוגברת בפלזמה ברוב המחלות הסרטניות.
האנזים ADA ומחלת הכשל החיסוני המשולב הקשה (SCID)
תסמונת נדירה המשלבת פגיעה תאית והומוראלית, בה הפגם גורם לנטייה קיצונית ללקות בזיהומים קשים ומהלך ממית בגיל תינוקות, בהיעדר אבחנה וטיפול מהירים. הטיפול כולל בידוד קפדני והקניית מערכת חיסון חדשה.
התסמונת גורמת לפגם קשה בהתפתחות ותפקוד לימפוציטים מסוג T ו-B ובמקרים מסוימים מערבת גם הפרעה בלימפוציטי NK. וקיימים כ־12 וריאנטים גנטיים שונים שלה. השכיח ביותר הם (כ־46% מהמקרים) נובע מחסר המרכיב גמא בקולטן למספר ציטוקינים שונים (2, 4, 7, 9, 15, 21), שמועבר בתאחיזה לכרומוזום ה- X ומתבטא בבנים. שאר הפגמים הגנטיים הגורמים למחלה הקשה מועברים בתאחיזה אוטוסומלית רצסיבית, כאשר חסר ב-ADA מהווה כ-16% (ראו איור).
רוב אלה עם חסר ADA מאובחנים עם SCID ב-6 חודשי החיים הראשונים. ב-10-15% מהמקרים, ההופעה של החסר החיסוני מתעכבת עד לגיל 6–24 חודשים או אפילו עד לגיל הבגרות. בצורות המחלה המאוחרות היא מתונה יותר במהלכה ומתבטאת בעיקר בהדבקות חוזרות של דרכי הנשימה העליונים, ובדלקות אוזניים. עם הזמן עלולה להתפתח מחלת ריאות כרונית, אלרגיות ובעיות רפואיות אחרות. ניתן לזהות חסר ב-ADA כבר בחודשי ההיריון תוך שימוש בסיסי שליה, או שניתן למדוד רמתו בדגימת דם טבורי.
חסר ב-ADA מאוד נדיר, ומוערך כמקרה אחד לכל 200,000 עד מיליון לידות באוכלוסיות אתניות שונות. חסר ב-ADA אחראי ל-15% מכלל מקרי SCID או severe combined immunodeficiency, והתסמינים הקליניים שלו יכולים להתגלות בינקות, בילדות, בשנות הנעורים או בבגרות, כאשר גיל הופעתם ודרגת חומרתם תלויה ב-29 הגנוטיפים השונים שאופיינו עד עתה, הכרוכים בחסר ADA. מדי שנה מאובחנים בארצות הברית 10–20 ילדים עם חסר האנזים.
הטיפול בחסר ADA: אין תרופה של ממש אך נעשים ניסיונות להגביר רמות ADA על ידי השתלת מח עצם מתאום, עירוי של תאי דם אדומים מתורם בריא המכילים רמות גבוהות של ADA, הזרקת האנזים החסר, תרפיה גנית על ידי החדרה של DNA סינתטי המכיל את הגן התקין ל-ADA, לתוך תאי חיסון. Gene therapy נערך לראשונה בספטמבר 1990 ב-NIH לילדה בת 4 שנים.
השתלת תאי גזע המטופואטיים אלוגניים מותאמים אנטיגנית בתרחיש SCID כתוצאה מחסר ADA עשוי להביא להחלמה אימונולוגית ארוכת טווח ולתיקון מטבולי, אם כי במקרים שהשתלת מח עצם בלתי תואמת יופיעו תחלואה ותמותה ניכרים. יש דיווחים על ניסויים בהיקף קטן של טיפול בילדים ללא תורם בעל HLA זהה, שעברו אבלציה של מח העצם עם busulfan, וקבלו עירוי של תאי אב ותאי מח עצם אוטולוגיים (+CD34), שעברו טרנסדוקציה עם vector גאמא-רטרו-ויראלי עם DNA המקודד ל-ADA. תוצאות מעקב חציוני לאחר 43 חודשים היו מעודדות, כאשר כל המטופלים היו בחיים, עם השתלבות יציבה של תאי הגזע ההמטופויטים שניתנו. תאים אלה עברו התמיינות לתאים מיאלואידים המכילים פעילות ADA. מחקר ברוח זו התפרסם בינואר 2009 ב-New England Journal of Medicine.
ADA ונוזל פלאורלי לזיהוי שחפת
תרחישים המגרים את מערכת החיסון כגון הידבקות בחיידק השחפת, יכולים להגביר את רמות האנזים ADA באזורים בהם יש נוכחות של החיידק. כיוון שקרומי הצדר עוטפים את חלל החזה, כמויות קטנות של נוזל צדר נוצרות לצורך סיכה של הריאות הנעות ומתחככות בקרומים אלה בשעת שאיפה ונשיפה. מנגד, יש מגוון של תרחישים קליניים בהם נגרמת דלקת של קרומי הפלאורה (pleuritis) מה שגורם להצטברות מוגברת של נוזל פלאורלי (pleural effusion).
זיהוי חיידקי מיקובקטריום בנוזל הפלאורה עלול להיות מסובך, הן בשל נפח נוזל גדול ומספר מאוד קטן של חיידקים הנמצאים בו בעת נתונה. אף על פי שמבדק ADA אינו ספציפי ולא יכול להחליף תרבית של נוזל פלאורלי לזיהוי חיידק השחפת, תוצאת מבדק זה יכולה להיות חיובית אפילו בנוכחות מספר זעום של חיידקי שחפת, ולכן נוטים להשתמש בו כמבדק עזר במקביל למבדקי PCR המולקולארי ול-acid-fast bacillus (AFB) smear and culture לסיוע באבחון המחלה.
המגבלות של שיטות אחרות לגילוי נוכחות של חיידקי שחפת בנוזל הפלאורלי נובעות מרגישותן הנמוכה. ברוב המקרים הצביעה של AFB מתקבלת שלילית, ורק ב-25% ממקרי שחפת מוכחת מתקבלת תרבית חיובית למיקובקטריה. מנגד, ביופסיה פלאורלית תדגים granulonatous pleuritis ב-80% של נבדקים עם TPE או tuberculous pleural effusion.
בשנת 1999 התפרסמה ב-Chest סקירתו של Roth ממנה משתמע שרמה מוגברת של ADA בנוזל הפלאורלי היא בעלת יכולת ניבוי של tuberculous pleuritis, ברגישות של 90-100% וספציפיות של 89-100%. האיזופורם ADA2 הוא הדומיננטי ב-TPE, אם כי בעשייה הקלינית המקובלת בונים רמת ADA באופן מקובץ, שכן המבדק של ADA2 יקר בהרבה ואינו זמין. בניסויים קליניים אחדים ערך הסף של ADA להערכת TPE נע בין U/L 47-60. הספציפיות של ממצא זה גדלה כאשר נמצא בנוזל הפלאורלי יחס של לימפוציטים לנויטרופילים הגדול מ-0.75.
- תרחישים קליניים בהם רמת ADA בפלזמה מוגברת
הפאטיטיס, צמקת הכבד (צירוזיס), המוכרומאטוזיס, צהבת חסימתית הכרוכה במחלה ממארת, סרטן הערמונית ושלפוחית השתן, אנמיה המוליטית, rheumatoid fever ,typhoid fever, צינית (gout), בהתקפים חריפים של סרקואידוזיס, תלסמיה מאיור, לויקמיה מיאלואידית, שחפת, איידס, מחלות אוטואימוניות, אי-ספיקת לב, infectious mononucleosis. יש לציין שבצורה נדירה של אנמיה המוליטית מולדת (אוטוזומאלית שלוטנית) רמת ADA גבוהה פי 35–70 מהרמה הנורמאלית.
- תרחישים בהם רמת ADA בפלזמה פחותה
סוכרת type 2, מחלת דרכי מרה.
- תרחישים בהם רמת ADA מוגברת בנוזל פלאורלי
שחפת. רמה של ADA מעל U/L 40 אינה תקינה ומחשידה לשחפת ואילו רמת אנזים בנוזל הפלאורלי מעל U/L100 ספציפית במידה רבה לשחפת. כאשר רמת ADA בנוזל הפלאורלי מוגברת באופן מתון באזור גאוגרפי עם שכיחות נמוכה של שחפת, ייתכן שהעלייה ברמת ADA פלאורלי נובעת מסיבה אחרת כמו לימפומה, תסחיף ריאתי, סרקואידוזיס, .SLE.
רמה נמוכה של ADA בנוזל פלאורלי מפחיתה את הסבירות לאבחון שחפת, אך עדיין אינה שוללת לחלוטין אבחון של שחפת, שכן רמת האנזים יכולה להיות מוגברת בנוזלי גוף אחרים כגון נוזל פריטונאלי, או CSF.
הוראות לביצוע הבדיקה
רמת ADA בפלזמה יכולה להימדד בטכנולוגיית HPLC, או בשיטות אנזמטיות או קולורימטריות. בשיטה הפשוטה ביותר על ידי מדידת רמת אמוניה המשתחררת מ-adenosine כאשר זה מתפרק ל-inosine . לאחר הדגרה של פלזמה בתמיסת בופר של אדנוזין, מגיבה אמוניה עם ריאגנט Berthelot ליצירת צבע כחול במתאם עם רמת פעילות האנזים. כדי למדוד פעילות ADA2, מוסיפים טרם התחלת הריאקציה את הריאגנט EHNA או erythro-9-(2-hydroxy-3-nonyl) adenine, כדי לעכב את פעילות האנזים ADA1 בפלזמה.
לפני ביצוע הבדיקה יש להפסיק ליטול תרופות על בסיס sodium benzoate בהן משתמשים לטיפול בתרחישי hyperammonemia. זאת כיוון שבפירוק אדנוזין משתחררת אמוניה, הנקשרת לסודיום בנזואט. אין להשתמש לצורך מדידה רמת ADA בדגימות דם המכילות p-chloromercuribenzoate, שהוא מעכב פרוטאזות מקובל בביולוגיה מולקולארית, כיון שהתוצאות שתתקבלנה בנוכחות חומר זה מראות רמה נמוכה כזובה של ADA. אם מודדים רמת ADA בדגימת דם של מטופל הנוטל dipyridamole (המשמש כנוגד-צימות תסיות במנותחי חזה ולטיפול מונע בתעוקת החזה) עלולים לקבל תשובה שלילית כזובה שכן תכשיר זה מעכב פעילות האנזים.
מדידת רמת האנזים מתבצעת בנסיוב כאשר דגימת הדם נלקחת במבחנה כימית (פקק אדום או צהוב). הדגימה יציבה בטמפרטורת החדר למשך 6–12 שעות, בקירור מעל שבוע, ובהקפאה במינוס 70 מעלות צלזיוס הדגימה יציבה 6 חודשים.
אם הבדיקה מתבצעת בשיטה פלואורסצנטית על טיפות דם מיובשות על נייר פילטר כגון נייר גאטרי, הדגימה יציבה בטמפרטורת החדר עד שבוע, ואם מקפיאים את הנייר המכיל את הדם עטוף בניילון, הדגימה יציבה בערך חודש ימים.
אם הבדיקה מתבצעת במדידה ספקטרופוטומטרית בהמוליזאט של אריתרוציטים רחוצים, יש לדגום את הדם במבחנת ציטראט (פקק תכול), מבחנת ספירת דם (EDTA, פקק סגלגל) או מבחנת הפארין (פקק ירוק). כדוריות הדם לצורך מדידת ADA יציבות מעל 20 יום במבחנות ציטראט או ספירת דם מעל 20 יום בקירור, אך רק 5–7 ימים במבחנת הפארין בקירור.
לצורך איסוף נוזל פלאורלי יש שימוש במזרק ומחט בפרוצדורה של thoracentesis.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק