הבדלים בין גרסאות בדף "פנטניל - Fentanyl"
| שורה 78: | שורה 78: | ||
[[קובץ:Gupta 1.png|ממוזער|מרכז|600 פיקסלים|'''שיטת Gupta לייצור פנטניל'''.]] | [[קובץ:Gupta 1.png|ממוזער|מרכז|600 פיקסלים|'''שיטת Gupta לייצור פנטניל'''.]] | ||
| + | [[קובץ:Seigfried 1.png|ממוזער|מרכז|600 פיקסלים|'''שיטת Seigfried לסינתזה של פנטניל'''.]] | ||
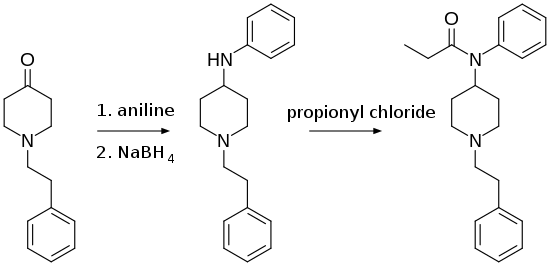
| − | שיטת Seigfried לסינתזה של פנטניל | + | שיטת Seigfried פועלת לסינתזה מוקדמת של N-phenethyl-4-piperidone (או NPP), כאשר תוצר זה עובר אמינציה ל-anilino-N-phenethylpiperidine{{כ}}-4(או ANPP{{כ}}-4}}. פנטניל מיוצר על ידי ריאקציה של ANPP{{כ}}-4 עם acyl chloride. שיטת Seigfried שימשה בשנות 2000 המוקדמות במעבדות רבות. |
| − | + | שיטת Suh: מדלגת מעל השימוש הישיר בקודמנים של piperidine ומגיעה ל-NPP ישירות (Suh וחב' ב-Arch Pharma Res משנת 1998). | |
| − | |||
| − | שיטת : | ||
| − | |||
| − | |||
| + | ==הקשר בין המבנה ומנגנון הפעולה של פנטניל== | ||
המבנה של אופיואידים הוא בעל זהות רבה. בזמן שאופיואידים דוגמת ,codeine הידרוקודון, oxycodone ו-hydromorphone מסונתזים על ידי מודיפיקציות של מורפין, פנטניל ונגזרותיו מסונתזים על ידי מודיפיקציות של,meperidine שהוא אופיואיד סינתטי במלואו, וחברים אחרים במשפחת ה-phenylpiperidine כגון alfetanyl ו-sufentanyl הם גרסאות מורכבות של meperidine. כמו אופיואידים אחרים, fentanyl הוא בסיס חלש, שמתמוסס מאוד בליפידים, נקשר לחלבונים, ועובר פרוטונציה ב-pH פיזיולוגי. כל התכונות הללו מאפשרות לו לחצות במהירות ממברנות ביולוגיות, מה שתורם להשפעתו המהירה בגוף ובעיקר במערכת העצבים המרכזית. פנטניל, כמו אופיואידים אחרים פועל על ידי קישור לקולטנים של אופיואידים. קולטנים אלה קשורים לחלבוני G, המכילים 7 אזורים טרנס-ממברנליים, לולאות תוך-תאיות, לולאות חוץ-תאיות, קצה C-טרמינלי תוך תאי, וקצה -N טרמינלי חוץ-תאי. הקצה ה N-טרמינלי החוץ-תאי, חיוני להבדלה ביכולת הקישור של מצעים שונים. כאשר פנטניל נקשר לקולטנו, מערכת איתותים. תוך תאיים, המובילים להשפעות מעכבות, כגון הפחתה ביצירה של cAMP, הפחתה בחדירה של יוני סידן לתוך התא, והפחתה ביציאה של אשלגן מהתא החוצה. תהליכים אלה מעכבים את המסלולים "העולים" במערכת העצבים המרכזית, ובכך מגבירים את סף הכאב על ידי שינויים בתחושת הכאב. זאת בתיווך ירידה בהשפעה של איתותים נוסיספטיביים (nociceptive signals) מה שמביא להשפעה של שיכוך כאבים. נדגיש כמו כן שכאב נוסיספטיבי הוא כאב שמקורו בפגיעה ברקמות שונות. נוסיספטורים, הם מרכיבים המעבירים סיגנל של כאב לאחר פגיעה כלשהי ברקמות, כמו רקמת השריר, העצם, העור ואיברים פנימיים אחרים. | המבנה של אופיואידים הוא בעל זהות רבה. בזמן שאופיואידים דוגמת ,codeine הידרוקודון, oxycodone ו-hydromorphone מסונתזים על ידי מודיפיקציות של מורפין, פנטניל ונגזרותיו מסונתזים על ידי מודיפיקציות של,meperidine שהוא אופיואיד סינתטי במלואו, וחברים אחרים במשפחת ה-phenylpiperidine כגון alfetanyl ו-sufentanyl הם גרסאות מורכבות של meperidine. כמו אופיואידים אחרים, fentanyl הוא בסיס חלש, שמתמוסס מאוד בליפידים, נקשר לחלבונים, ועובר פרוטונציה ב-pH פיזיולוגי. כל התכונות הללו מאפשרות לו לחצות במהירות ממברנות ביולוגיות, מה שתורם להשפעתו המהירה בגוף ובעיקר במערכת העצבים המרכזית. פנטניל, כמו אופיואידים אחרים פועל על ידי קישור לקולטנים של אופיואידים. קולטנים אלה קשורים לחלבוני G, המכילים 7 אזורים טרנס-ממברנליים, לולאות תוך-תאיות, לולאות חוץ-תאיות, קצה C-טרמינלי תוך תאי, וקצה -N טרמינלי חוץ-תאי. הקצה ה N-טרמינלי החוץ-תאי, חיוני להבדלה ביכולת הקישור של מצעים שונים. כאשר פנטניל נקשר לקולטנו, מערכת איתותים. תוך תאיים, המובילים להשפעות מעכבות, כגון הפחתה ביצירה של cAMP, הפחתה בחדירה של יוני סידן לתוך התא, והפחתה ביציאה של אשלגן מהתא החוצה. תהליכים אלה מעכבים את המסלולים "העולים" במערכת העצבים המרכזית, ובכך מגבירים את סף הכאב על ידי שינויים בתחושת הכאב. זאת בתיווך ירידה בהשפעה של איתותים נוסיספטיביים (nociceptive signals) מה שמביא להשפעה של שיכוך כאבים. נדגיש כמו כן שכאב נוסיספטיבי הוא כאב שמקורו בפגיעה ברקמות שונות. נוסיספטורים, הם מרכיבים המעבירים סיגנל של כאב לאחר פגיעה כלשהי ברקמות, כמו רקמת השריר, העצם, העור ואיברים פנימיים אחרים. | ||
גרסה מ־17:54, 15 במאי 2023
| מדריך בדיקות מעבדה | |
| פנטניל | |
|---|---|
| Fentanyl | |
| שמות אחרים | Dance Fever Friend, Goodfellas, Jackpot, Apache, sublimaze ,Murder 8, PHENTANYL |
| מעבדה | כימיה בדם, וכימיה בשתן |
| תחום | חומרים טוקסיים, שיכוך כאבים אופיואידי., |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה: ניטור של תרפיה עם פנטניל.
פנטניל הוא תכשיר אופיואידי פוטנטי פיפרידיני המשמש בעיקר כמשכך כאבים. כיוון שפנטניל פוטנטי פי 50 עד 100 יותר מאשר מורפין, השימוש הקליני בו להתנהלות עם מצבי כאב בחולי סרטן המתאוששים מניתוחים. פנטניל משמש גם להרגעה (Ramos-Motos וחב' ב-StatPearls משנת 2022). בתלות בצורת נטילתו פנטניל עשוי להיות פועל בצורה מאוד מהירה, ונטילה קטנה יחסית שלו עלולה לגרום לנטילת-יתר. פנטניל פועל על ידי שפעול של קולטנים מסוג μ-opioides, והוא ידוע גם כפנטניל-ציטראט, ונמכר תחת שם המותג Sublimaze.
פנטניל פותח במהלך בחינת תכשירים הדומים ל-pethidine (meperidine) בגין הפעילות האופיואידית שלו. השימוש הנרחב בפנטניל הביא ליצירת fentanyl citrate, המלח הנוצר על ידי חיבור פנטניל וחומצה ציטרית ביחס סטיכומטרי של 1:1 (Mandal ב-News-Med.net משנת 2010). פנטניל ציטראט נכנס לשימוש קליני כמרדים כללי בשנת 1968, יוצר על ידי מעבדות McNeil תחת שם המותג Sublimaze. באמצע שנות ה-90 פיתחו Janssen Pharmaceuticals את ה-Duragesic patch שהכיל פנטניל וג'ל אלכוהולי, שסיפק החדרה קבועה של פנטניל למשך 48–72 שעות. בשנת 1998 נכנס לשימוש ה-lolipop הארומטי בו פנטניל ציטראט (שם המותג Actiq שהפך לתכשיר הראשון לפעולה מהירה בשעת כאבים כרוניים. בשנת 2009, אישר ה-FDA תכשיר פנטניל מסיס לספיגה בוקלית תחת השם Onsolis, לשימוש בטכנולוגיית העברת פנטניל הידועה כ-BEMA או Bio Erodible Muco Adhesive בו פילם של פולימר מסיס המכיל כמויות שונות של פנטניל מוחדר לחלק הפנימי של הלחי.
מידע קליני
פנטניל הוא אופיואיד סינתטי בעל פעילות מהירה ביותר הקשור ל-phenylpiperidines (Gutstein ו-Akil ב-The Pharmacological Basis of Therapeutics משנת 2006, ו-Kerrigen ו-Goldberger ב-Opioides משנת 2003). פנטניל זמין בגישת הזרקה לשריר או טרנס-דרמלית, והוא מגיב בעיקר עם הקולטן האופיואידי mu המפוזר במוח האדם, בעמוד השדרה, וברקמות אחרות. כ-80 עד 85% מהפנטניל קשור לחלבונים, ויכולת הקישור לחלבונים של פנטניל פוחתת ככל שהיוניזציה של התכשיר הזה גדלה. שינויים ב-pH יכולה לשנות את מציאותו בפלזמה או ב-CNS באדם. פנטניל עובר מטבוליזם בעיקר על ידי oxidative N-dealkylation ל-norfentanyl ולמטבוליטים לא פעילים אחרים שאינם תורמים לפעילות התכשיר. תוך 72 שעות מעירוי ורידי של פנטניל, בערך 75% מהחומר מופרשים בשתן (Baselt ב-Disposition Toxic Drugs Chemicals Man משנת 2014).
תקופת מחצית החיים הממוצעת היא 2 עד 4 שעות לגבי חומר הניתן בעירוי. בהזרקה יונטופורטית לתוך העור תקופת מחצית החיים 16 שעות. בדיסקית טרנס-דרמלית תקופת מחצית החיים 17 שעות. בלַכְסָנִית למציצה תקופת מחצית החיים 7 שעות. בטבלית פומית (100-200 מיליגרם) הנלקחת באופן buccal לספיגה בחלק הלחי הפנימי, תקופת מחצית החיים 3–4 שעות. במערכות קליניות פנטניל משפיע פרמקולוגית בעיקר ב-CNS. כיוון שהשפעותיו של פנטניל דומות לאלו של הרואין ושל אופיואידים אחרים, הוא הפך לתכשיר פופולרי של שימוש לרעה.
תופעות הלוואי השליליות של פנטניל דומות לאלו של אופיואידים נרקוטיים אחרים, וכוללות התמכרות, תחושת בלבול, דיכוי נשימתי ישנוניות, בחילה, הפרעות ראייה, הזיות, דיסקינזיה (סוג של הפרעת תנועה, המאופיינת בתנועות שרירים לא רצוניות, כמו טיקים או כוריאה) דליריום (ותת צורה שלו הידועה כ- narcotic delirium), עצירות, anagesia (שיכוך כאב היא דרך להעלאת סף הרגישות לכאב אצל אדם הסובל מכאבים), קשיות שרירים, narcotic ileus (או חסימת מעיים), לחץ-דם ירוד, איבוד הכרה, תרדמת ומוות. אלכוהול ותכשירים אחרים כגון קוקאין והרואין, יכולים באופן סינרגיסטי להחמיר את תופעות הלוואי של פנטניל. לעומת זאת, naloxone (שם מותג Narcan) מסוגל להפיג את ההשפעות של מנת-יתר של פנטניל.
פנטניל משמש גם בהתנהלות במקרים של כאב כרוני כולל במחלת הסרטן. במקרים אלה מקובל להשתמש בדיסקית עורית כאשר פנטניל המשתחרר מהדיסקית חודר דרך העור לדם למשך 48 עד 72 שעות, מה שמאפשר פעילות משככת כאב ארוכת טווח. שיעור הספיגה דרך העור תלוי בטמפרטורת הגוף, סוג העור, רמת השומן התת-עורי והמיקום של הדיסקית המודבקת על פני הגוף. בתנאים רגילים השפעת פנטניל המופרש מהדיסקית מגיעה לשיא פעילותה תוך 12 עד 24 שעות. לא ברור האם פנטניל משכך גם כאבים נוירופתיים. נטילת טבליות פנטניל במציצה תת-לשונית מביאה להמסה וספיגה מהירה שלו דרך הרירית התת-לשונית להשיג הפגת כאבים מהירה. כיוון שפנטניל נספג היטב בשומן, הוא מגיע לדם מהר יחסית, והוא נסבל היטב. פנטניל בדיסקית עורית בזרוע המשחררת אותו במינון של 12 מיקרוגרם לשעה, טובה לטיפול תומך-פליאטיבי במטופלים עם קשיי בליעה של טבליות, ואינם מסוגלים לקבל את התכשיר בהזרקה תת--עורית, במטופלים עם אי-ספיקת כליות מתונה עד קשה, או במטופלים עם תופעות לוואי בנטילה פומית של מורפין, הידרומורפון, או אוקסיקודון. פנטניל במינון מבוקר יעיל גם במצבים של קוצר נשימה (dyspnea) הכרוכה בכאבים. מתן פנטניל כתרסיס אפי, הוא אמנם בעל השפעה מהירה יותר ורמתו בדם גבוהה תוך פרק זמן קצר יותר, אך תופעות הלוואי שלו במינון-יתר עלולות להיות קשות יותר. מקובל שתרסיס אפי של פנטניל יעיל כמו עירוי ורידי של מורפין, ואף עדיף על הזרקת מורפין לשריר, במקרים של מאושפזים עם כאב חריף.
תופעות לוואי של פנטניל
בין למעלה מ-70,200 מקרי מוות בארצות הברית בשנת 2017 מצריכת-יתר של תרופות, נרשמו למעלה מ-28,400 מקרי מוות שיוחסו לפנטניל ולאנלוגים שלו, או כ-40%. תופעות הלוואי השכיחות ביותר של פנטניל המשפיעות על כ-10% מצורכי תכשיר זה, הן בחילה, הקאות, עצירות, יובש בפה, רדימות, בלבול וחולשה. ב-3 עד 10% מהמקרים, צריכת פנטניל תגרום לכאבי בטן, כאבי ראש, עייפות, אנורקסיה, טשטוש, איבוד משקל, עצבנות ודאגנות, דיכאון, תופעות דמויות-שפעת, קשיי עיכול, קוצר נשימה והיפו-ונטילציה, קשיי דיבור (aphasia) ואצירת שתן. יתרון של פנטניל על מורפין שהוא גורם פחות לגרד. רק בשנת 2006 החל ה-FDA לאתר מספר מקרים של מוות מסיבות נשימתיות, ובבריטניה החלו בחקירות על מעורבות פנטניל במקרי מוות רק בספטמבר 2008. באפריל 2012, דיווח ה-FDA על 12 ילדים שמתו, ועל עוד 12 ילדים שחלו באופן קריטי מחשיפה לפנטניל בדסקיות עור.
דיכוי מערכת הנשימה
תופעת הלוואי המסוכנת ביותר היא השפעת פנטלין על מערכת הנשימה במובן של הפחתת הרגישות לדו-תחמוצת הפחמן, מה שעלול להפחית את קצב הנשימה שעלול לגרום לאנוקסיה של המוח ולמוות. סכנה זו גדולה יותר בקרב אלה הסובלים מחסימת נשימה בשינה. גורמים אחרים המגבירים את הסכנה של דיכוי נשימתי הם: מינון גבוה של פנטניל, גיל מתקדם, צריכה סימולטנית של מדכאי מערכת העצבים המרכזית כגון בנזודיאזפינים, ברביטורטים, אלכוהול, נשימת חומרי הרדמה, היפר-ונטילציה, רמות נמוכות של CO2 בדם וכן חמצת נשימתית.
סיבוך נוסף מצריכת-יתר של פנטניל, ידוע כ-wooden chest syndrome או תסמונת מוצא בית החזה הנגרמת מלחץ שנוצר על עצבים וכלי דם בין החלק התחתון של הצוואר לבית השחי. תסמונת זו כוללת קשיחות פתאומית של שרירי הבטן והסרעפת, מגוון סימנים באזורי הצוואר, הכתף והזרוע, כגון כאבי צוואר, תסמינים עצביים לאורך הגפה העליונה. חסרים נוירולוגיים אופייניים כוללים חולשה ונימול, פגיעה חמורה למערכת הנשימה וכן שינויים בטמפרטורה ובגוון של העור. תסמונת זו מתרחשת באופן מובהק יותר בקרב נשים בגיל 20 עד 50 שנה. תסמונת מוצא החזה נגרמת כנראה מהפרשה של נור-אדרנלין המשפעל את הקולטנים האלפא-אדרנרגיים כמו גם כנראה משפעול של קולטנים כולינרגיים, והיא ניתנת לטיפול על ידי naloxone.
השפעת פנטניל על כלי הדם והלב
ברדיקרדיה: פנטניל מפחית את קצב הלב על ידי הגברת הטונוס של העצב התועה בגזע המוח, מה שמגביר את ההשפעה הפארא-סימפטתית.
הרחבת כלי הדם: פנטניל עלול להרחיב את העורקים והוורידים על ידי מנגנון מרכזי, בעיקר על ידי האטת מרכזים וזומוטוריים בגזע המוח. השפעה אחרונה זו הרבה יותר עמוקה במטופלים עם פעילות סימפטתית חזקה, כמו כאלה עם יתר לחץ-דם או עם אי-ספיקת לב גדושה.
פנטניל סונתז לראשונה בשנת 1959 על ידי Paul Janssen ואושר לשימוש למטרות רפואיות בארצות הברית בשנת 1968 (Stanley ב-J Pain Symptom Management משנת 1992). בשנת 2015, 1,600 ק"ג של פנטניל נמצאו בשימוש גלובאלי למטרות רפואיות, ובשנת 2017, פנטניל היה האופיואיד הסינתטי השכיח ביותר שנמצא בשימוש רפואי. בשנת 2019, פנטניל היה תרופת המרשם במקום ה-278 בארצות הברית, עם למעלה ממיליון מרשמים, והוא נמצא ברשימת התרופות החיוניות של ה-WHO. פנטניל ממשיך לתדלק את מגפת התמותה מצריכת-יתר של אופיואידים בארצות הברית שעלתה בתלילות בין השנים 2011 עד 2021, מ-2,600 מקרי מוות לשנה עד ל-76,238 מקרי מוות לשנה. מאז שנת 2018, פנטניל והאנלוגים שלו היו אחראיים למספר הפטירות הגדול ביותר כשהוא גרם ל-71,238 פטירות בשנת 2021, ובכך עלה למקום הראשון כגורם פטירות בהדיחו את הרואין מעמדה זו בשנת 2018. המעבדות הפורנזיות בארצות הברית דיווחו על מצוקות בגין צריכת פנטניל שעלו מ-4,697 מקרים בשנת 2014, ל-117,045 מקרים בשנת 2020 (Falco בדו"ח של חבר הקונגרס David Trone משנת 2023). פנטניל נלקח לעיתים ביחד עם קוקאין או הרואין, והוא משווק לעיתים בצורת גלולות המחקות oxycodone, מה שגורם לצריכה מוגברת שלו בהיסח הדעת.
=הסטאטוס החוקי של פנטניל
בהולנד, פנטניל מופיע ברשימת חוק האופיום (Shelley ב-Pharmaceut Commerce משנת 2011). בארצות הברית, פנטניל מוגדר כחומר Schedule II ברשימת התכשירים תחת בקרה, על מנת למנוע שימוש לרעה, מבטחי בריאות רבים דורשים הגבלת כמויות של מרשמי Actiq (Naylor ב-Vice משנת 2020). בקנדה, פנטניל נחשב כתכשיר Schedule I ברשימת החומרים תחת בקרה (Townsend ב-The Guardian משנת 2018, ו-Buddiger ב-Lancet משנת 2006). אסטוניה שהפכה למדינה המובילה בעולם בתחום מגפת הפנטניל, הפכה לכזו בעקבות האיסור שהטיל הטאליבן באפגניסטן לגדל פרג לתעשיית האופיום. באסטוניה מרובה התמותה מצריכה של 3-methylfentanyl כיוון שנגזרת זו של פנטניל החליפה שם את השימוש בהרואין (Marset ב-Addiction משנת 2019). מגפת הפנטניל הביאה לסכסוך בין ארצות הברית ומקסיקו, בו הואשמה האחרונה כמחדירת תכשיר זה לארצות הברית על ידי קבוצות פשע. בתגובה הכריז נשיא מקסיקו Lopez Obrador שהמקור העיקרי של תכשיר זה היא יבשת אסיה (Ducharme ב-Time משנת 2018).
חלק מסוחרי פנטניל מערבבים אבקת פנטניל עם הרואין להגביר את ההשפעה של הרואין באיכות נמוכה. בשנת 2006, תכשירים לא-חוקיים של פנטניל מעורבב עם קוקאין או הרואין, גרמו לגל תמותה ניכר בארצות הברית ובקנדה (Burgmann וחב' ב-CTV News משנת 2015). הערים הפגועות ביותר בגל תמותה זה היו דייטון, שיקגו, דטרויט ופילדלפיה. בנובמבר 2016 גילו אנשי DEA (או Drug Enforcement Agency) פעילות גדולה של ייצור לא חוקי של תערובת oxycodone ו-Xanax ביוטה (Tanner ב-The Salt City Tribune משנת 2016), והתבררה המעורבות של סין במשלוח כמויות גדולות של פנטניל בצורת אבקה לארצות הברית (Kram וחב' ב-Anal Chem משנת 1981). בפברואר 2019 גילו אנשי המכס בארצות הברית 115 ק"ג פנטניל בקרקעית של מכולה שהובילה מלפפונים. הסינים התמחו בייצור של AMF או α-methylfentanyl שזכה לכינוי "China White" ואשר "יתרונו" במשך השפעה ארוך יותר.
ביוני 2013, ה-CDC באטלנטה פרסם אזהרה לפיה היו 14 מקרים של מוות ממנת-יתר של מזריקי סמים לווריד ברוד איילנד, שנגרמו משימוש ב-acetylfantanyl, נגזרת של פנטניל שמעולם לא קיבל אישור לשימוש. החל משנת 2015 גילתה קנדה מקרי שימוש-יתר בפנטניל, וחושדת שמקור החומר הן קבוצות פשע שהבריחו חומר זה כ-pseudo-OxyContin (Cooper וחב' ב-Global News משנת 2018). מספר מקרי המוות היה גדול במיוחד בקולומביה הבריטית כולל העיר ונקובר עם 1,716 פטירות בשנת 2020. בשנת 2018, מתיחות דיפלומטית בין סין וקנדה פגעה בשיתוף הפעולה בין 2 המדינות למנוע ייבוא חומר זה מסין. בשנת 2017, נתגלו מקרים של מכירת פנטניל לא חוקי באוסטרליה (Bonini ב-ABC News משנת 2017), כמו גם מקרים של מקרים כאלה בניו זילנד בשנת 2018 (Buchanan ב-HealthCentral NZ משנת 2018).
שימושים רפואיים של פנטניל
הרדמה: עירוי תוך-ורידי של פנטניל משמש לעיתים להרדמה או לשיכוך כאבים (Gropper וחב' ב-Anesthesia משנת 2019). כדי להשרות הרדמה, פנטניל ניתן ביחד עם תכשיר היפנוטי-מרגיע כגון propofol או thiopental ומרגיע שרירים (Godwin וחב' ב-Ann Energ Med משנת 2024). על מנת להפיג כאבים לאחר ניתוח.
הרדמה מקומית
פנטניל הוא האופיואיד השימושי ביותר לטיפול intrathecal (הקוּרים במוח או בחוט השדרה) בגלל האופי הליפופילי שמאפשר פעולה מהירה (5 עד 10 דקות), ומשך ממוצע של השפעה (60 עד 120 דקות) (Buggy ב-BMJ משנת 2008). החדרה לתוך חוט השדרה של bupivacaine היפרברי ופנטניל, נראה כטיפול משולב אידיאלי. ההשפעה הכמעט מיידית של פנטניל, מפחיתה אי-נוחות ויסצרלית, ואת הבחילה בפרוצדורה זו (Bujedo ב-Korean J Pain משנת 2014).
פנטניל ומיילדות
פנטניל ניתן לעיתים בצורה intrathecal כחלק מהרדמה ספינלית או אפידוראלית. כיוון שפנטניל מסיס בשומנים, השפעתו מקומית יותר מזו של מורפין. ולכן חלק מהרופאים מעדיפים שימוש במורפין על מנת לקבל פיזור רחב יותר של שיכוך כאבים. במיילדות יש צורך להקפיד על אי מתן מינון גבוה מדי לאם בשעת הלידה, שכן הוא עלול לגרום ליילוד מצוקה נשימתית שלאחר הלידה (White וחב' ב-Int J Obstet Anesthesiol nab משנת 2019). מסיבה זו נגזרות כגון alfentanyl ו-remifentanyl עשויים להיות מתאימים יותר (Karlsen וחב' ב-Ann Emerg Med משנת 2014).
צריכת-יתר
פנטניל הוא בעל סיכון מוגבר לאדם בשימוש בריכוז גבוהה. זאת כיוון שכמותו הנדרשת לגרום לטוקסיות אינה צפויה. רוב מקרי המוות משימוש-יתר מיוחסים לריכוז פנטניל בנסיוב של 0.025 מיקרוגרם/מ"ל (Cheema וחב' ב-J Pain Res משנת 2020, Petrou ב-MJH Life Sci משנת 2016, Burns וחב' ב-Clin Toxicol ו-Bulow וחב' ב-Acta Anesthesiol Scand משנת 1995). ריכוז פנטניל בדם של 7 ננוגרם/מ"ל, יוחס למקרי מוות. ביולי 2914 פרסמה סוכנות הבקרה על תרופות בבריטניה (MHRH) אזהרה מפני הסכנה לחיים בצריכת יתר של פנטניל במיוחד בילדים. בשנת 2016, מספר מקרי המוות מצריכת-יתר של פנטניל הגיע ל-2 מקרים ביום, ובשנת 2017 מספר הפטירות מסיבה זו עלה פי-2 ל-368 פטירות בקולומביה הבריטית בתקופה שבין ינואר ואפריל (Scaccia ב-Rolling Stone משנת 2018). כמות הפנטניל המוזרק לווריד הגורמת לתמותה ב-50% מהמקרים (LD50) היא 3 מיליגרם/ק"ג בחולדות, 1 מיליגרם/ק"ג בחתולים, 14 מיליגרם/ק"ג בכלבים, ו-0.03 מיליגרם/ק"ג בקופים (Yadav וחב' ב-Interdisciplinary Toxicol משנת 2014). בעכברים, ערכי LD50 הם 6.9 מיליגרם/ק"ג בעירוי ורידי, 17.5 מיליגרם/ק"ג בהחדרה תוך-פריטונאלית, 27.8 מיליגרם/ק"ג במתן פומי. ה-LD50 באדם אינו ידוע, אך הוא מוערך להיות כ־2 מיליגרם באנשים בתלות במשקלם, סבילותם לתכשיר וחשיפה לפנטניל בעבר. (Ross ב-Stat News משנת 2017). פנטניל החל לזהם הרואין, קוקאין, מטאמפטמין, קטמין, MDMA ותכשירים אחרים (Daly ב-Vice משנת 2019). אף על פי שמקסיקו וסין נחשבות ל-2 המדינות המחדירות פנטניל לארצות הברית, נראה שהודו מתחילה להסתמן כמקור נוסף של אבקת פנטניל.
התנהלות עם כאבים
הזמינות של ריסוס תוך-אפי של פנטניל היא כ-70 עד 90%, אך יכולה להשתנות במקרים של נחיריים סתומים. למקרים של כאבי חירום או בסיוע למניעת כאב כרוני, פנטניל אפי יכול להינתן במינונים של 50, 100 ו-200 מיקרוגרם. בילדים, פנטניל תוך-אפי מועיל במקרים של כאב מתון וקשה (Coombs ב-Scand J Pain ו בבני פחות מ-5 שנים, השוקלים פחות מ-13 ק"ג, ולכסניות של פנטניל יעילות אף הן (Plante ו-VanItallie ב-metabolism משנת 2011). במקרים של כאב כרוני כולל זה במחלת הסרטן נעשה גם כן שימוש בפנטניל (Jasek ב-Austria Codex משנת 2007). לעיתים נעשה שימוש בדיסקית טרנס-דרמלית המאפשרת החדרת התכשיר לדם למשך 48–72 שעות. לא ברור האם פנטניל מאפשר הקלה מכאבים נוירופתיים (Roy וחב' ב-Curr Opin Nephrol Hypertens משנת 2020). נעשה פיתוח של פנטניל טרנז-דרמלי המאפשר טיפול בכאבים שלאחר ניתוחים (Chelly וחב' ב-Anesthesia Analgesia משנת 2004). משך ההשפעה של פנטניל נמצא לעיתים שגוי, מה שעלול לגרום לנזק קליני (Van Leeuwen וחב' ב-Der Anesthesist משנת 1981, Brown ב-Chest משנת 1985, ו-Nilsson ו-Rosberg ב-Acta Anesthesiol Scand משנת 1982).
פנטניל ודיכוי נשימתי
תופעת הלוואי המסוכנת ביותר של פנטניל היא מצוקה נשימתית (Hemmings ו-Egan ב-Pharmacol Physiol Anesthesia משנת 2018), דהיינו רגישות מופחתת ל-CO2 הגורמת לקצב מופחת של נשימה מה שעלול לגרום למוח אנוקסי או למוות. סכנה זו מוגברת באלה עם בעיות של חסימת נשימה (McLoughlin ו-McQuillan ב-Palliative Med משנת 1997).
הסינתזה של פנטניל
פנטניל הוא אופיואיד סינתטי מסוג anilopiperidine-4 והסינתזה שלו מושגת על ידי אחת מ-4 שיטות עיקריות: Gupta ,Siegfried ,Janssen ו-Suh.
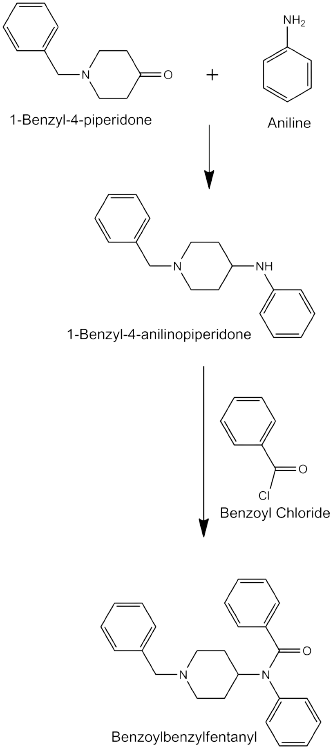
שיטת Janssen: השיטה המקורית הוכנסה על ידי Janssen בשנת 1964, והיא כורכת סינתזה של benzylfentanyl מ-N-Benzyl-4-Piperidone.
שיטת Gupta: בשיטה זו מתחילים מ-4-בנזילפנטניל המייתר את השימוש הישיר ב-4-ANPP/NPP שכן התרכובות נוצרות רק כתוצרי ביניים ארעיים (Gupta ב-ChemInform משנת 2005). בשנת 2021, מחקר שנערך ב-318 דגימות, מצא ששיטת Gupta הייתה השיטה הדומיננטית לייצור פנטניל. דרגת הטיהור הממוצעת של דגימות מסונתזות בשיטת Gupta הייתה 13.6% (על פי Lopez-Munoz ו-Alamo ב-Brain Res Bull משנת 2009).
שיטת Seigfried פועלת לסינתזה מוקדמת של N-phenethyl-4-piperidone (או NPP), כאשר תוצר זה עובר אמינציה ל-anilino-N-phenethylpiperidine-4(או ANPP-4}}. פנטניל מיוצר על ידי ריאקציה של ANPP-4 עם acyl chloride. שיטת Seigfried שימשה בשנות 2000 המוקדמות במעבדות רבות.
שיטת Suh: מדלגת מעל השימוש הישיר בקודמנים של piperidine ומגיעה ל-NPP ישירות (Suh וחב' ב-Arch Pharma Res משנת 1998).
הקשר בין המבנה ומנגנון הפעולה של פנטניל
המבנה של אופיואידים הוא בעל זהות רבה. בזמן שאופיואידים דוגמת ,codeine הידרוקודון, oxycodone ו-hydromorphone מסונתזים על ידי מודיפיקציות של מורפין, פנטניל ונגזרותיו מסונתזים על ידי מודיפיקציות של,meperidine שהוא אופיואיד סינתטי במלואו, וחברים אחרים במשפחת ה-phenylpiperidine כגון alfetanyl ו-sufentanyl הם גרסאות מורכבות של meperidine. כמו אופיואידים אחרים, fentanyl הוא בסיס חלש, שמתמוסס מאוד בליפידים, נקשר לחלבונים, ועובר פרוטונציה ב-pH פיזיולוגי. כל התכונות הללו מאפשרות לו לחצות במהירות ממברנות ביולוגיות, מה שתורם להשפעתו המהירה בגוף ובעיקר במערכת העצבים המרכזית. פנטניל, כמו אופיואידים אחרים פועל על ידי קישור לקולטנים של אופיואידים. קולטנים אלה קשורים לחלבוני G, המכילים 7 אזורים טרנס-ממברנליים, לולאות תוך-תאיות, לולאות חוץ-תאיות, קצה C-טרמינלי תוך תאי, וקצה -N טרמינלי חוץ-תאי. הקצה ה N-טרמינלי החוץ-תאי, חיוני להבדלה ביכולת הקישור של מצעים שונים. כאשר פנטניל נקשר לקולטנו, מערכת איתותים. תוך תאיים, המובילים להשפעות מעכבות, כגון הפחתה ביצירה של cAMP, הפחתה בחדירה של יוני סידן לתוך התא, והפחתה ביציאה של אשלגן מהתא החוצה. תהליכים אלה מעכבים את המסלולים "העולים" במערכת העצבים המרכזית, ובכך מגבירים את סף הכאב על ידי שינויים בתחושת הכאב. זאת בתיווך ירידה בהשפעה של איתותים נוסיספטיביים (nociceptive signals) מה שמביא להשפעה של שיכוך כאבים. נדגיש כמו כן שכאב נוסיספטיבי הוא כאב שמקורו בפגיעה ברקמות שונות. נוסיספטורים, הם מרכיבים המעבירים סיגנל של כאב לאחר פגיעה כלשהי ברקמות, כמו רקמת השריר, העצם, העור ואיברים פנימיים אחרים.
כאגוניסט של μ-receptors פנטניל נקשר לקולטניו פי- 50–100 יותר מאשר מורפין. הוא יכול גם להיקשר לקולטנים האופיואידיים delta ו-kappa בזיקה קצת יותר נמוכה. בגלל המסיסות הגדולה שלו בליפידים, מתאפשר לפנטניל לחדור בקלות יתר למערכת העצבים המרכזית. פנטניל מחליש את ה"כאב השני" על ידי השפעתו על העברת כאב איטית של סיבי C מחוסרי מיאלין, והוא פחות יעיל בהחלשת כאב נוירופתי, ופחות יעיל בהחלשת האיתותים של ה"כאב הראשון" המועברים על ידי סיבי עצב מסוג A שהם קטנים ומכילים מיאלין.
זיהוי פנטניל בנוזלים ביולוגיים
ניתן למדוד ריכוז פנטניל בשתן למטרת ניטור של שימוש אסור, לצורך אישור של הרעלה, או לסייע בזיהוי מדיקו-לגלי של מקרה מוות. ערכות מסחריות זמינות של immunoassay משמשות בהערכה ראשונית של מקרים אלה, אך שיטות כרומטוגרפיות משמשות בדרך כלל למטרות אישור וכימות. בדיקת הצבע של Marquis יכולה אף היא לשמש לגילוי נוכחות של פנטניל. שימוש בפורמאלדהיד וחומצה גופריתנית עשוי לגרום לנוזל הבדיקה להפוך לסגול (Vandergrift וחב' ב-Blin Biochem משנת 2018). ריכוז פנטניל בפלזמת הדם אמור להיות בתחום שבין 3.0 ל-0.3 מיקרוגרם/ליטר באנשים הצורכים פנטניל באופן טיפולי, ובריכוז של 1.0-10.0 מיקרוגרם/ליטר באלה עם השפעה טוקסית של פנטניל, ובריכוז של 3–300 מיקרוגרם/ליטר בקורבנות של מנת יתר חריפה של פנטניל. שיטה שלpaper spray-mass spectrometry (להלן PS-MS)) עשויה להיות מועילה לבדיקה ראשונית של הדגימה (Vardanyan ו-Hruby ב-Future Med Chem משנת 2014).
הוראות לביצוע הבדיקה
את הדם יש לדגום במבחנה כימית (פקק אדום). אין להשתמש במבחנת ג'ל שכן פנטניל עלול להיספג לתוך הג'ל ולגרום לתוצאות שליליות כזובות. יש לסרכז את הדם ולהעביר את הנסיוב המופרד למבחנת פלסטיק תוך שעתיים מנטילת הדם. יש לפסול דגימות מאוד המוליטיות, ליפמיות או איקטריות. הדגימות יציבות למשך 22 שעות בטמפרטורת החדר, 14 יום בקירור, ו-28 יום כדגימות קפואות.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק