הבדלים בין גרסאות בדף "אימונותרפיה על המדף לטיפול בלימפומה פוליקולרית"
| שורה 29: | שורה 29: | ||
נדרש ”conditioning" באמצעות מתן תרופות כימותרפיות לפני החזרת התאים, והליך ההחזרה דורש אשפוז של בין שבועיים לחודש. טיפול בתאי CAR-T רשום בישראל בקו שלישי ומעלה ונמצא בסל שירותי הבריאות החל מקו טיפול רביעי. | נדרש ”conditioning" באמצעות מתן תרופות כימותרפיות לפני החזרת התאים, והליך ההחזרה דורש אשפוז של בין שבועיים לחודש. טיפול בתאי CAR-T רשום בישראל בקו שלישי ומעלה ונמצא בסל שירותי הבריאות החל מקו טיפול רביעי. | ||
| − | ==מוסונטוזומאב, נוגדן | + | ==מוסונטוזומאב, נוגדן בי-ספציפי "על המדף" לטיפול בקו השלישי== |
מוסונטוזומאב, נוגדן בי־ספציפי CD20xCD3 המפעיל תאי T-cell engaging bispecific) T antibody). הוא טיפול אימונותרפי הפועל במנגנון שונה. | מוסונטוזומאב, נוגדן בי־ספציפי CD20xCD3 המפעיל תאי T-cell engaging bispecific) T antibody). הוא טיפול אימונותרפי הפועל במנגנון שונה. | ||
| שורה 39: | שורה 39: | ||
תוצאות המחקר הדגימו את יעילותו הגבוהה של מוסונטזומאב בחולי FL בקו מתקדם. 80% מהחולים הגיבו לטיפול (ORR) ו־60% מהחולים השיגו תגובה מלאה לטיפול (CR), שיעור גבוה משמעותית מהמושג עם הטיפולים הזמינים בסל בקו טיפול שלישי. שיעור תגובה גבוה הודגם גם בחולים בעלי גורמים פרוגנוסטיים רעים: | תוצאות המחקר הדגימו את יעילותו הגבוהה של מוסונטזומאב בחולי FL בקו מתקדם. 80% מהחולים הגיבו לטיפול (ORR) ו־60% מהחולים השיגו תגובה מלאה לטיפול (CR), שיעור גבוה משמעותית מהמושג עם הטיפולים הזמינים בסל בקו טיפול שלישי. שיעור תגובה גבוה הודגם גם בחולים בעלי גורמים פרוגנוסטיים רעים: | ||
| − | + | בחולי POD24 שיעור התגובה המלאה עמד על 57% ובחולים רפקטורים כפולים שיעור התגובה המלאה עמד על 50%. מרבית המטופלים לא נזקקו למתן כל 17 מחזורי הטיפול והשיגו תגובה תוך שמונה מחזורים, כאשר הזמן החציוני להשגת תגובה מלאה עמד על שלושה חודשים בלבד. | |
| − | + | בעדכון מעקב ארוך טווח של ממצאי המחקר, כפי שפורסם בכנס ICML בחודש יוני 2023, עלה כי בחולים שהשיגו תגובה מלאה בסיום הטיפול, משך התגובה החציוני median duration of complete response {{כ}}(DOCR) וה-PFS החציוני לא הושגו לאחר מעקב של 28.3 חודשים(12). עוד הודגם כי משכי התגובה המצוינים לא הושפעו מהזמן הנדרש להשגת התגובה, כך שגם חולים שהשיגו תגובה מלאה מאוחר יותר הרוויחו מהטיפול. | |
| − | |||
| − | + | בהיבט פרופיל הבטיחות, הטיפול במוסונטוזומאב נסבל היטב עם הפסקות טיפול מועטות בשל תופעות לוואי. תופעת הלוואי השכיחה ביותר הייתה תסמונת שחרור ציטוקינים, אך ברוב המכריע של המקרים חומרת התסמונת הייתה בדרגה 2-1 והופעתה הייתה בקורלציה לעומס מחלה במח העצם. בנוסף, תופעת לוואי זו, כמו גם תופעות לוואי נוירולוגיות (שגם היו בדרגת חומרה נמוכה), אם התפתחו, הופיעו בעיקר במהלך מחזור הטיפול הראשון בעת ההגעה למינון המקסימלי. | |
| − | + | ||
| − | + | לסיכום, מוסונטוזומאב מהווה אפשרות טיפול עם יעילות גבוהה, זמינה לשימוש (off the shelf), הניתנת בפרק זמן מוגבל וללא צורך באשפוז, עם פרופיל בטיחותי טוב. | |
גרסה מ־11:01, 18 בנובמבר 2024
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| אימונותרפיה "על המדף" לטיפול בלימפומה פוליקולרית | ||
|---|---|---|
| ' | ||

| ||
הגדלה מיקרוסקופית של לימפומה פוליקולרית, המראה את הזקיקים הלימפואידים החריגים האופייניים שהעניקו למחלה את שמה.
| ||
| יוצר הערך | ד"ר שמרית רינגלשטיין | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – לימפומה
לימפומה פוליקולרית (FL) היא הלימפומה השנייה בשכיחותה מכלל ה־non-Hodgkin lymphomas (NHL) ומהווה כ־22% מכלל המקרים[1][2]. FL היא השכיחה ביותר מכלל הלימפומות האינדולנטיות והגיל החציוני בזמן האבחנה עומד על 65 שנים. למרות שהשרידות החציונית של המטופלים היא מעל 15 שנים, FL נחשבת למחלה שאינה בת ריפוי[3].
בעת אבחנת המחלה לא כל החולים יזדקקו לטיפול, אך לאורך השנים עלולים להופיע סימפטומים שמהווים אינדיקציה להתחלת טיפול. למרות התגובה הטובה לרוב לטיפולים בקו הראשון, המחלה מאופיינת במהלך של הפוגות שלאחריהן חזרת מחלה (remitting-relapsing) והחולים נזקקים פעמים רבות לקווי טיפול מרובים. עם התקדמות קווי הטיפול, ההפוגות הולכות ומתקצרות, ובעוד שהשרידות החציונית ללא התקדמות מחלה (PFS) בקו טיפול ראשון עומדת על יותר מחמש שנים, בקו טיפול שלישי מדובר על פרק זמן של שנה ואף פחות מכך בקווי טיפול מאוחרים יותר, והפרוגנוזה של חולים מתקדמים אלה רעה[3][4].
בנוסף, יש חולים שלא מגיבים לטיפולים או שמחלתם מתקדמת בתוך פחות מ־24 חודשים מהתחלת טיפול קו ראשון (חולים אלה מכונים POD24) וכן חולים "רפרקטורים כפולים", דהיינו עמידים הן ל־alkylating agents והן לנוגדנים כנגד CD20 ומהווים תת קבוצות של חולים בעלי הפרוגנוזה הגרועה ביותר[3].
טיפולים זמינים לחולי FL בקו הראשון והשני
קו הטיפול הראשון המקובל בישראל הוא שילוב של כימותרפיה ונוגדנים חד-שבטיים כנגד CD20 (Rituximab או Obinutuzumab). מטופלים שמשיגים תגובה חלקית (partial response) ומעלה על פי רוב יקבלו טיפול משמר עם הנוגדן שהיווה חלק מטיפול האינדוקציה, וזאת על סמך מעקב ארוך שנים אחרי חולים שטופלו במסגרת מחקר PRIMAL שהראה הארכה משמעותית של ה־PFS במתן טיפול משמר[5].
בקו טיפול שני ניתן לטפל עם תרופות כימותרפיות ונוגדן מונוקלונלי שלא נעשה בהם שימוש טיפולי בקו הראשון, או לטפל במשלב של Lenalidomide וריטוקסימאב. חלק מהחולים אשר מגיבים לטיפול קו שני יתקדמו להשתלת מוח עצם עצמית להעמקת התגובה[2].
טיפול בחולי FL בקווים מתקדמים חולים שמחלתם התקדמה על שני קווי טיפול מהווים קבוצה המאופיינת בפרוגנוזה רעה עם אפשרויות טיפול מוגבלות. עבור חולים אלה קיימות מספר תרופות המאושרות לשימוש על ידי ה־FDA ו/או ה־EMA. בהן, תרופות מקבוצת המולקולות הקטנות, הכוללות מעכבי PI3K ומעכבי EZH2, אשר אינם נכללים בסל הבריאות. אחוזי התגובות המלאות למעכבי ה־ PI3K נמוכים והשימוש בהם מוגבל ביותר בשל פרופיל הבטיחות הבעייתי שלהם[6]. מעכב האנזים EZH2 (tazemetostat) גם כן מאופיין בשיעורי תגובה מלאה נמוכים והוא יעיל בעיקר בחולי FL עם מוטציה ב־EZH2[7].
נכנסו לשימוש ב־FL גם טיפולים אימונותרפיים מתקדמים המאושרים ברשויות הבריאות בעולם ובארץ, בהם טיפול בתאי CAR-T וכן התרופה Mosunetuzumab, הפועלים באמצעות הפעלת מערכת החיסון כנגד תאי הלימפומה[8][9][10][11]. טיפול בתאי CAR-T בחולי FL בקו מתקדם הדגים שיעורי תגובה גבוהים עם אחוז נמוך יחסית של תסמונת שחרור ציטוקינים מדרגה גבוהה וסיבוכים נוירולוגיים[10][11]. עם זאת, מתן הטיפול מורכב: נדרשת הכנה של התאים (כחודש מיום האיסוף) אשר לעתים אינה צולחת ובמהלך ההמתנה לחזרת התאים הלימפומה עלולה להתקדם ולדרוש מתן טיפולים נוספים. כמו כן נדרש ”conditioning" באמצעות מתן תרופות כימותרפיות לפני החזרת התאים, והליך ההחזרה דורש אשפוז של בין שבועיים לחודש. טיפול בתאי CAR-T רשום בישראל בקו שלישי ומעלה ונמצא בסל שירותי הבריאות החל מקו טיפול רביעי.
מוסונטוזומאב, נוגדן בי-ספציפי "על המדף" לטיפול בקו השלישי
מוסונטוזומאב, נוגדן בי־ספציפי CD20xCD3 המפעיל תאי T-cell engaging bispecific) T antibody). הוא טיפול אימונותרפי הפועל במנגנון שונה.
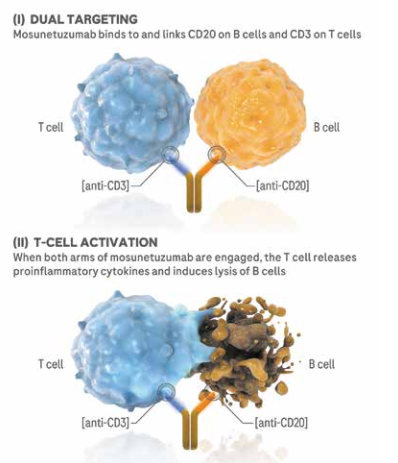
מוסונטוזומאב רותמת את תאי ה־T כנגד הלימפומה, זאת באמצעות קישור בזרוע האחת ל־CD20 הנמצא על פני רוב תאי ה־B, ובזרוע השנייה ל־CD3 הנמצא על פני תאי T אפקטורים. בעקבות הקישור של שני התאים בו זמנית, יש הפעלה של תאי ה־T ושחרור רעלנים מתאי ה־T לעבר תאי ה־3 אשר מובילים להרג של תאי ה־B.
רישומה של מוסנטוזומאב ברשויות הבריאות בישראל ומחוץ לה לטיפול ב־FL התבסס על מחקר פאזה 2 שממצאיו פורסמו בכתב העת Lancet Oncology ב־2022[9]. במחקר השתתפו כ־90 מטופלים עם FL אשר קיבלו מוסונטוזומאב כקו טיפול מתקדם. חציון הטיפולים הקודמים של המשתתפים עמד על שלושה, כך שלמעשה כלל המשתתפים נחשפו בעבר לנוגדנים כנגד CD20 ול־alkylating agents ומרביתם היו בעלי גורמי סיכון הכרוכים בפרוגנוזה רעה: 52% היו POD24 (חולים שהתקדמו תוך 24 חודשים מהתחלת הטיפול) ו־53% רפרקטורים כפולים (הן לטיפול קודם כנגד CD20 והן לאלקילטורים). מוסונטוזומאב ניתן תוך־ורידית ללא צורך באשפוז, במחזורים של 21 ימים (למשך שמונה או 17 מחזורים, כתלות בתגובה לטיפול). מדד ההערכה הראשוני היה שיעור התגובה המלאה (CR).
תוצאות המחקר הדגימו את יעילותו הגבוהה של מוסונטזומאב בחולי FL בקו מתקדם. 80% מהחולים הגיבו לטיפול (ORR) ו־60% מהחולים השיגו תגובה מלאה לטיפול (CR), שיעור גבוה משמעותית מהמושג עם הטיפולים הזמינים בסל בקו טיפול שלישי. שיעור תגובה גבוה הודגם גם בחולים בעלי גורמים פרוגנוסטיים רעים: בחולי POD24 שיעור התגובה המלאה עמד על 57% ובחולים רפקטורים כפולים שיעור התגובה המלאה עמד על 50%. מרבית המטופלים לא נזקקו למתן כל 17 מחזורי הטיפול והשיגו תגובה תוך שמונה מחזורים, כאשר הזמן החציוני להשגת תגובה מלאה עמד על שלושה חודשים בלבד.
בעדכון מעקב ארוך טווח של ממצאי המחקר, כפי שפורסם בכנס ICML בחודש יוני 2023, עלה כי בחולים שהשיגו תגובה מלאה בסיום הטיפול, משך התגובה החציוני median duration of complete response (DOCR) וה-PFS החציוני לא הושגו לאחר מעקב של 28.3 חודשים(12). עוד הודגם כי משכי התגובה המצוינים לא הושפעו מהזמן הנדרש להשגת התגובה, כך שגם חולים שהשיגו תגובה מלאה מאוחר יותר הרוויחו מהטיפול.
בהיבט פרופיל הבטיחות, הטיפול במוסונטוזומאב נסבל היטב עם הפסקות טיפול מועטות בשל תופעות לוואי. תופעת הלוואי השכיחה ביותר הייתה תסמונת שחרור ציטוקינים, אך ברוב המכריע של המקרים חומרת התסמונת הייתה בדרגה 2-1 והופעתה הייתה בקורלציה לעומס מחלה במח העצם. בנוסף, תופעת לוואי זו, כמו גם תופעות לוואי נוירולוגיות (שגם היו בדרגת חומרה נמוכה), אם התפתחו, הופיעו בעיקר במהלך מחזור הטיפול הראשון בעת ההגעה למינון המקסימלי.
לסיכום, מוסונטוזומאב מהווה אפשרות טיפול עם יעילות גבוהה, זמינה לשימוש (off the shelf), הניתנת בפרק זמן מוגבל וללא צורך באשפוז, עם פרופיל בטיחותי טוב.
ספרות:
1. The Non-Hodgkin’s Lymphoma Classification Project. Blood;1997;89:3909-18
2. NCCN Clinical Practice Guidelines in Oncology. B-cell lymphomas. V5.2023
3. Carbone A et al. Follicular Lymphoma. Nat Rev Dis Primers. 2019 Dec 12;5(1):83.
4. Batlevi et al. Follicular lymphoma in the modern era: survival, treatment outcomes, and identification of high- risk subgroups. Blood Cancer Journal (2020) 10:74
5. Bachy E. et al, Sustained Progression-Free Survival Benefit of Rituximab Maintenance in Patients With Folicullar Lymphoma: Long-Term Results of the PRIMA Study. J Clin Oncol. 2019 Nov 1;37(31):2815-2824
6. Sapon-Cousineau V et al. PI3K Inhibitors and Their Role < as Novel Agents for Targeted Therapy in Lymphoma. Curr. Treat. Options in Oncol. (2020) 21: 51
7. Morschhauser F, Tilly H, Chaidos A, et al. Tazemetostat for patients with relapsed or refractory follicular lymphoma: an open-label, single-arm, multicentre, phase 2 trial. The Lancet Oncology 2020;21:1433-42.
8. Budde LE et al. Single-Agent Mosunetuzumab
Shows Durable Complete Responses in Patients With Relapsed or Refractory B-Cell Lymphomas: Phase I Dose-Escalation Study. Journal of Clinical Oncology 2022;40:481-91.
9. Budde LE et al. Safety and efficacy of mosunetuzumab, a bispecific antibody, in patients with relapsed or refractory follicular lymphoma: a single-arm, multicentre, phase 2 study. Lancet Oncol. 2022 Aug;23(8):1055-1065.
10. Fowler NH, Dickinson M, Dreyling M, et al. Tisagenlecleucel in adult relapsed or refractory follicular lymphoma: the phase 2 ELARA trial. Nature medicine 2022;28:325-32.
11. Sattva S. Neelapu, Long-Term Follow-up Analysis of ZUMA-5: A Phase 2 Study of Axicabtagene Ciloleucel (Axi-Cel) in Patients with Relapsed/Refractory (R/R) Indolent Non-Hodgkin Lymphoma (iNHL), ASH Annual Meeting and Exposition December 11-14, 2021, Oral presentation.
12. Sehn L.H et al, Mosunetuzumab demonstrates durable responses in patients with relapsed and/or refractory follicular lymphoma who have received >2 prior therapies: updated analysis of a pivotal Phase II study. Presented at the 2023 International Conference Malignant Lymphoma (ICML) Annual Meeting, June 13-17, 2023
ביבליוגרפיה
- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה1 - ↑ 2.0 2.1 שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה2 - ↑ 3.0 3.1 3.2 שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה3 - ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה4 - ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה5 - ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה6 - ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה7 - ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה8 - ↑ 9.0 9.1 שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה9 - ↑ 10.0 10.1 שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה10 - ↑ 11.0 11.1 שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה11
המידע שבדף זה נכתב על ידי ד"ר שמרית רינגלשטיין, מנהלת שירות לימפומה, המרכז הרפואי רמב"ם


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק