הבדלים בין גרסאות בדף "למינין - Laminin"
| (6 גרסאות ביניים של אותו משתמש אינן מוצגות) | |||
| שורה 3: | שורה 3: | ||
|שם לועזי=Laminin | |שם לועזי=Laminin | ||
|קיצור= | |קיצור= | ||
| − | |תמונה=[[Laminin111.png|מרכז|250 פיקסלים]] | + | |תמונה=[[קובץ:Laminin111.png|מרכז|250 פיקסלים]] |
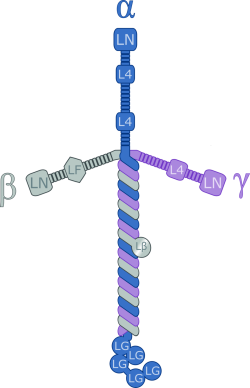
| − | |כיתוב תמונה= | + | |כיתוב תמונה=איור של קומפלקס למינין-111. |
|מעבדה=[[כימיה בדם]] | |מעבדה=[[כימיה בדם]] | ||
|תחום=מולקולה על פני התא הכרוכה בנגעים שונים כגון סרטן. | |תחום=מולקולה על פני התא הכרוכה בנגעים שונים כגון סרטן. | ||
|יחידות מדידה= | |יחידות מדידה= | ||
| − | |טווח ערכים תקין=ממוצע: 0.79 ננוגרם/מ"ל. | + | |טווח ערכים תקין=ממוצע: 0.79 ננוגרם/מ"ל. |
|יוצר הערך=[[משתמש:בן עמי סלע|פרופ' בן-עמי סלע]] | |יוצר הערך=[[משתמש:בן עמי סלע|פרופ' בן-עמי סלע]] | ||
|אחראי הערך= | |אחראי הערך= | ||
}} | }} | ||
| − | למינינים הם משפחה של גליקופרוטאינים של המשתית החוץ-תאית בכל בעלי החיים. הם מרכיבים מרכזיים בממברנת הבסיס, (דהיינו ה-basal lamina). למינינים משפיעים על הפעילות הביולוגית כגון ההתמיינות של תאים, על תנועת תאים ועל ספיחתם (Timpl וחב' ב-J Biol Chem משנת 1979, ו-Durbeej ב-Cell | + | ==מטרת הבדיקה== |
| + | הערכה וניטור של חלבון דמוי צלב הכרוך בתכונות מרובות של תאים כגון ספיחה, ניידות, וחודרנות. | ||
| + | |||
| + | ==כללי== | ||
| + | למינינים הם משפחה של גליקופרוטאינים של המשתית החוץ-תאית בכל בעלי החיים. הם מרכיבים מרכזיים בממברנת הבסיס, (דהיינו ה-basal lamina). למינינים משפיעים על הפעילות הביולוגית כגון ההתמיינות של תאים, על תנועת תאים ועל ספיחתם (Timpl וחב' ב-J Biol Chem משנת 1979, ו-Durbeej ב-Cell Tissue Res משנת 2010). למינינים הם קומפלקסים חלבוניים הטרוטרימרים עם משקל מולקולרי גבוה (400–900 קילו-דלטון) ומכילים שלוש שרשרות שונות (אלפא, בטא וגאמה) המקודדים על ידי חמישה, ארבעה ושלושה גנים פאראלוגיים באדם, בהתאמה. מולקולות למינין קרויות על פי הרכב השרשרת שלהם, לדוגמה laminin-511 מכילה שרשרות β1, α5 ו-γ1 ({{כ}}Aumailley וחב' ב-Matrix Biol משנת 2005). החלבונים הטרימרים הם בעלי צורת צלב ומסוגלים להיקשר למולקולות אחרות במשתית החוץ-תאית או בממברנת התא (Haralson ו-Hassell ב-IRL Press משנת 1995). שלוש הזרועות הקצרות הן בעלות זיקה למולקולות למינין אחרות, בעוד שהזרוע הארוכה מסוגלת להיקשר לתאים, ובכך לסייע עיגון של של תאים לממברנת הבסיס. הלמינינים מהווים חלק אינטגרלי מהשלד המבני של כמעט כל רקמה באורגניזם, והם מופרשים ועוברים אינקורפורציה למשתיות חוץ-תאיות הקשורות לתאים. גליקופרוטאינים אלה הכרחיים לעמיות ולחיוניות של הרקמה: למינינים פגומים עלולים לגרום לשרירים להיווצר בצורה לא ראויה, תוך שהם גורמים ל-muscular dystrophy, לפגמים בסינון הכלייתי ([[תסמונת נפרוטית]]), ולמחלה קטלנית של שלפוחיות בעור (junctional epidermolysis bullosa) ({{כ}}Yurchenco ו-Patton ב-Current Pharmaceut Design משנת 2009). | ||
[[קובץ:Laminin1.png|מרכז|600px]] | [[קובץ:Laminin1.png|מרכז|600px]] | ||
| שורה 19: | שורה 23: | ||
==סוגי הלמינינים== | ==סוגי הלמינינים== | ||
| − | באדם, זוהו 15 טרימרים של למינין | + | באדם, זוהו 15 טרימרים של למינין, כאשר הלמינינים הם קומבינציות של שרשרות אלפא, בטא וגאמא שונות (Colognato ו-Yurchenco ב-Develop Dynamics משנת 2000). חמישה איזופורמים של שרשרת אלפא: LAMA5, LAMA4, LAMA3, LAMA2, LAMA1; ארבעה איזופורמים של שרשרת בטא:LAMB4, LAMB3, LAMB2, LAMB1; שלושה איזופורמים של שרשרת גאמא: LAMC3, LAMC2, LAMC1. |
| − | + | ||
{| class="wikitable" | {| class="wikitable" | ||
! שם המולקולה!!הרכב השרשרת | ! שם המולקולה!!הרכב השרשרת | ||
| שורה 30: | שורה 34: | ||
|Laminin-3||α1β2γ1 | |Laminin-3||α1β2γ1 | ||
|- | |- | ||
| − | |Laminin | + | |Laminin 4 ||α2β2γ1 |
|- | |- | ||
|Laminin-5 / Laminin-5A ||α3Aβ3γ2 | |Laminin-5 / Laminin-5A ||α3Aβ3γ2 | ||
| שורה 54: | שורה 58: | ||
|Laminin-15||α5β2γ3 | |Laminin-15||α5β2γ3 | ||
|} | |} | ||
| + | |||
| + | ==תפקוד== | ||
| + | למינינים יוצרים רשתות בלתי-תלויות וכרוכים עם קולאגן type IV דרך entactin (ל{{כ}}Smith ו-Ockleford ב-Placenta משנת 1994), דרך פיברונקטין (Ockleford וחב' ב-Philosophical Transactions Royal Soc London משנת 1993), ודרך perlecan. החלבונים נקשרים גם כן לממברנות התאים דרך integrins ומולקולות של הממברנה כגון הקומפלקס של הגליקופרוטאין dystroglycan ודרך הגליקופרוטאין הלוטראני של קבוצת הדם. על ידי אינטראקציות אלו. למינינים תורמים ליכולת הספיחה של תאים ולהתמיינות שלהם, כמו גם להישרדות של רקמות. אחדים מתפקודים אלה של למינין נכרכו ברצפים ספציפיים של חומצות אמינו. לדוגמה הרצף הפפטידי GTFALRGDNGDNGQ הממוקם בשרשרת אלפא של למינין, מסייע לספיחה של תאי אנדותל. למינין alpha4 מפוזר במגוון של רקמות, כולל עצבים היקפיים, שרירי שלד, קפילרות ו-dorsal root ganglion, וכן בצומת הנוירו-שרירית והוא חיוני לפעילות הסינפסה (Ichikawa וחב' ב-Biochemistry משנת 2005). המבנה של מקטע של laminin-G דומה לזה של pentraxin ({{כ}}Beckmann וחב' ב-J Mol Biol משנת 1998). | ||
| + | |||
| + | ==התפקיד של למינין בהתפתחות הנוירלית== | ||
| + | למינין-111 הוא מצע עיקרי דרכו אקסונים של תאי עצב גדלים, in vivo ו־in vitro. לדוגמה, למינין זה מונח במסלול בו התפתחות של תאי גנגליון של הרשתית מתקדמת מהרשתית ל-tectum (שהוא אזור במוח, הממוקם בחלק הגבי של המוח האמצעי. הטקטום אחראי לרפלקסים שמיעתיים וחזותיים). הנוכחות של למינין-111 יכולה להשפיע על תגובת ה-cones האחראיים ברשתית לחישה של צבע. השפעה זו של למינין-111 מתרחשת על ידי הפחתה של cyclic AMP תוך-תאי. | ||
| + | |||
| + | == התפקיד של למינין בשיקום של עצב היקפי== | ||
| + | למינינים מועשרים באזורי נגעים לאחר פגיעה בעצב היקפי והם מופרשים על ידי תאי Schwann ({{כ}}Nieuwenhuis וחב' ב-Biol Rev Cambridge Philosoph Soc משנת 2018). נוירונים של מערכת העצבים ההיקפיים מבטאים קולטנים של integrin נקשרים על ידי למינינים ותומכים בנוירו-רגנרציה לאחר פציעה. | ||
| + | |||
| + | ==פתולוגיה== | ||
| + | פגיעה בתפקוד של laminin-211, היא הסיבה לצורה אחת של muscular dystrophy מולדת (Hall וחב' ב-Proc Natl Acad Sci USA משנת 2007). למינין-211 מורכב משרשרות β1, α2 ו-γ1. למינין זה מופע בעיקר במוח, ובסיבי שריר. בשריר הוא נקשר ל-alpha-dystroglycan, ול-integrin alpha7-beta1, וקצהו השני נקשר למשתית החוץ-תאית. Laminin-332 חיוני לספיחה של תאי אפיתל לממברנת הבסיס וכאשר הוא אנומלי מוביל הדבר ל-junctional epidermolysis bullosa המאופיינת על ידי שלפוחיות, רקמת גרנולציה חיונית של העור והרירית ושיניים מגולענות. Laminin-521 רב-תפקודי בכליות גורם לדליפה של חלבון לתוך השתן ולתסמונת נפרוטית. | ||
| + | |||
| + | ==תפקיד למינין בסרטן== | ||
| + | איזופורמים אחדים של למינין נכרכו בפתו-פיזיולוגיה של סרטן. אירוע חיוני בהתפתחות סרטן, הוא מה שמוגדר כ-epithelial-to-mesenchymal transition (EMT), המאפשר לתאי קרצינומה לרכוש תכונות של חודרנות. השפעול של מרכיבי המשתית החוץ-תאית הידוע כ-laminin B1 (להלן LAMB1) במהלך ה-EMT דווח. ביחד עם עוד מרכיבים עיקריים במשתית החוץ-תאית, כגון קולאגנים ופיברונקטין, למינינים שימשו לעודד תאי אב (stem cells) רב-פוטנטיים, כמו גם תאים ראשוניים בתרבית, שקשה להביא לשגשוגם. | ||
| + | |||
| + | שני סוגים של למינינים טבעיים זמינים מסחרית: למינין-111 המופק מסרקומות בעכברים, ותערובות של למינין משליית אדם, המתאימים ללמינין 411,211 או 511, בתלות בחברה המספקת אותם (Wondimu וחב' ב-Matrix Biol משנת 2006). בידוד של איזופורמים של למינין קשה פרקטית לבודד מרקמות בצורה נקייה בגלל cross linking אקסטנסיבי והצורך בתנאי מיצוי קשים, כגון אנזימים פרוטאוליטים או pH נמוך, הגורמים לדגרדציה של הלמינינים. לפיכך, יוצרו למינינים ריקומביננטיים מאז שנת 2000 (Kortesmaa וחב' ב-J Biol Chem משנת 2000). בשנת 2008, שתי קבוצות הראו באופן בלתי-תלוי שניתן לגדל תאי-אב מעוברים של עכברים למשך חודשים בסיוע למינין-511 ({{כ}}Domogatskaya וחב' ב-Stem Cells משנת 2008, ו-Miyazaki וחב' ב-Biochem Biophys Res Commun מאותה שנה). לאחר מכן נמצא שלמינין-511 רקומביננטי, יכול להיות מנוצל ליצור תנאים מוגדרים בתרבית רקמה לגדל תאי אב עובריים (ESC) פלוריפוטנטיים (שיכולים לצמוח לכיוונים שונים) ותאי IPS (או Induced pluripotent stem cells) של אדם (Rodin וחב' ב-Nature Biotechnol משנת 2010). | ||
| + | |||
| + | == למינין B == | ||
| + | מקטע למינין B (הידוע גם כמקטע IV) הוא מודול חוץ-תאי עם תפקוד לא ברור. הוא נמצא במספר חלבונים שונים הכוללים heparan sulphate proteoglycan מממברנת הבסיס, וחלבון דמוי-למינין ממקור של Caenorhabditis elegans. המקטע של למינין IV אינו נמצא בשרשרות הקצרות של למינין (alpha4 או beta3). | ||
| + | |||
| + | ==למינין דמוי-EGF== | ||
| + | מלבד סוגים שונים של מקטעים גלובולריים כל תת-יחידה של למינין מכילה בקצה הראשון שלה החזרים של בערך 60 חומצות אמינו הכוללים 8 שיירים משומרים של ציסטאין (Engel ב-FEBS Lett משנת 1989). המבנה השלישוני של מקטע זה דומה בקצה ה-N טרמינלי שלו לזה של המודול דמוי-EGF ({{כ}}Stetefeld וחב' ב-J Mol Biol משנת 1996, ו-Baumgartner וחב' באותו כתב-עת מאותה שנה). מספר העותקים של המקטע שלל למינין דמוי-EGF מאוד וריאבילי כאשר בין 3 ל-22 עותקים נמצאו בשרשרת laminin gamma-1 בעכבר, כאשר המקטע השביעי נמצא להיות היחיד הנקשר בזיקה גדולה ל-nidogen שהוא חלבון חשוב בממברנת הבסיס ({{כ}}Mayer וחב' ב-FEBS Lett משנת 1995). | ||
| + | |||
| + | ==למינין G== | ||
| + | המקטע הגלובולרי (G) של למינין הוא בעל 177 חומצות אמינו, ויכול להימצא ב-1 עד 6 עותקים בחברים שונים של משפחת הלמינינים כמו גם במספר גדול של חלבונים חוץ-תאיים אחרים. לדוגמה, כל שרשרות אלפא של למינין מכילים 54 מקטעי למינין G, בה בשעה ש-neurexin 1 ו-2 מכילים 6 מקטעי למינין G. התפקיד המדויק של מקטע למינין G נותר בלתי ברור. לדוגמה, שרשרות אלפא 1 ו-אלפא 2 של למינין מכילות חמישה מקטעי למינין G ללC-טרמינלים, בעוד שרק מקטעי LG4 ו-LG5 מכילים אתרי קישור להפארין, לסולפטידים ולקולטן של dystroglycan ({{כ}}Tisi וחב' ב-EMBO J משנת 2000). נראה שחלבוני למינין G הם בעלי מספר תפקידים בספיחת תאים, נדידתם והתמיינותם. | ||
| + | |||
| + | ==הביולוגיה המבנית של למינינים== | ||
| + | מחקרים מבניים על ידי אלקטרון מיקרוסקופיה שהחלו בראשית שנות ה-80, גילו מולקולה דמוית-צלב, שהתבררה לאחר מכן כמכילה שלוש שרשרות פוליפפטידיות. מחקרים קריסטלוגרפיים מאז אמצע שנות ה-90 הוסיפו מידע על ההטרוטרימרים של למינין. שלושת הזרועות הקצרים של מבנה דמוי-צלב זה היו עשירים במקטעים עשירים בדיסולפידים. המקטעים הגלובולריים בקצות הזרועות הקצרים סייעו לפולימריזציה של למינין. הזרוע הארוכה של מבנה הצלב היא אלפא-הליקלית הכרוכה באזור גלובולי הנספח לתאים. מחקרים מבניים של למינין החלו ב-1996, כאשר Stetefeld וחב' קבעו את המבנים הגבישיים של המקטעים 7-9 של שרשרת γ1 ב-aminin-type epidermal growth factor-like domain במאמר שהתפרסם ב-J Mol Biol. המבנה דמוי המוט של למינין γ1 LE7-9 חסר מבנה הידרופובי אך במקומו מבנה ה-LE מיוצב על ידי ארבעה קשרים דיסולפידיים כאשר קשרים אלה המיוצבים על ידי γ1 LE7-9 (דהיינו שמונה ציסטאינים המחברים את מקטעים 1–3, 2–4, 5–6 ו-7–8) נמצאו לאחר מכן בכל המבנים של LE ({{כ}} Kalkhof וחב' ב-Biochemistry משנת 2010). | ||
| + | |||
| + | בראשית שנות ה-80 של המאה ה-20 שתי מעבדות ניקו באופן בלתי-תלוי גליקופרוטאין גדול מהמשתית החוץ-תאית של תאי סרטן בעכברים (Timpl וחב' ב-J Biol Chem משנת 1979, ו-Chung וחב' ב-Cell מאותה שנה). ידוע שיונקים מכילים לפחות 15 איזופורמים של למינין (כאשר חסרי-חוליות מכילים רק 2 איזופורמים), ושלמינינים חיוניים: בחסר שלהם, לא נוצרת ממברנת הבסיס ונמנע גידול של עוברים בשלב ההיריון המוקדם. בדומה לפיברונקטין, למינינים יוצרים רשתות ונקשרים לקולטנים תאיים. אי הצלחת היקשרות של למינינים לתאים גורמת לחלות אנושיות קשות כגון דיסטרופיות של שרירים (Mercury ו-Muntoni ב-Lancet משנת 2013), או שלפוחיות בעור (Uitto וחב' ב-Matrix Biol משנת 2017). כאמור, למינינים הם הטרוטרימרים המורכבים משרשרת אחת של β, α ו- γ . גנומים של יונקים מקודדים ל-5 שרשרות α, ל-4 שרשרות β, ול-3 שרשרות γ : רק 15 מתוך 60 הטרוטרימרים אפשריים אושרו ביוכימית (Aumailley וחב' ב-Matrix Biol משנת 2005, ו-Coble וחב' ב-Hum Mol Genet משנת 2017). הלמינין שבודד במקור מהמשתית של גידול סרטני בעכבר הוא הטרוטרימר α1β1γ1, שקרוי laminin-111 שמשקלו המולקולרי בערך 900 קילו-דלטון. שרשרות למינין זה קשורות קו-ולנטית על ידי קשרים די-סולפידיים. ההיבטים הראשונים של המבנה של למינין-111 הושגו על ידי rotary shadowing electron microscopy, שגילה ארבעה זרועות: זרוע ארוכה שאורכה בערך 77 ננומטר, המסתיימת במבנה גלובולרי הידוע כמקטע G, ושלושה זרועות קצרים יותר באורך של בערך 34 ננומטר, המסתיימים בזוג של מבנים גלובולרים קטנים יותר (Engel וחב' ב-J Mol Biol משנת 1981). | ||
| + | |||
| + | ==הוראות לביצוע הבדיקה== | ||
| + | לאחר נטילת דם ורידי לתוך מבחנה כימית (פקק אדום או צהוב) בטמפרטורת החדר יבוצע סרכוז למשך 10 דקות במהירות 4,000 סיבובים לדקה. הנסיוב מוקפא מיד לאחר הסרכוז עד לאנליזה. ורמת למינין בנסיוב נמדדת בשיטת ELISA שעשתה שימוש בשיטת סנדוויץ של נוגדן כפול. דגימות הנסיוב מוספות לתוך בארות שמצופות קודם לכן עם נוגדן חד-שבטי כנגד למינין אנושי תוצרת Wuhan EIAab Science Co. China. לאחר הדגרה, נוגדנים כנגד למינין המסומנים עם ביוטין ובשילוב עם streptavidin-horseradish peroxidase הם מוספים ליצור קומפלקס חיסוני לאחר הדגרה של שעה אחת. חומר בלתי קשור צריך להישטף ולאחר מכן יש להוסיף את תמיסת הכרומוגן על מנת להמיר את התמיסה הבלתי צבועה לתמיסה בצבע כחול, שעוצמתו פרופורציונית לריכוז הלמינין בדגימה. הצבע אמור להתחלף לצבע צהוב כשמוסיפים תמיסת עצירה חומצית. את הצבע הצהוב מודדים על ידי "קורא ELISA" אוטומטי (ChroMate, 4300 Microplate Reader; Awareness Technology, Inc., Palm City, USA). התוצאה מבוטאת בערכי ננוגרם/מ"ל. | ||
| + | |||
| + | ==ראו גם== | ||
| + | * [[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | ||
| + | * [[בדיקות ביוכימיות|בדיקות מעבדה - בדיקות ביוכימיות]] | ||
| + | |||
| + | {{ייחוס בן עמי}} | ||
| + | |||
| + | [[קטגוריה:בדיקות מעבדה - בדיקות ביוכימיות]] | ||
| + | [[קטגוריה:בדיקות מעבדה: כימיה בדם]] | ||
גרסה אחרונה מ־15:11, 13 באפריל 2026
| מדריך בדיקות מעבדה | |
| למינין | |
|---|---|
| Laminin | |
איור של קומפלקס למינין-111.
| |
| מעבדה | כימיה בדם |
| תחום | מולקולה על פני התא הכרוכה בנגעים שונים כגון סרטן. |
| טווח ערכים תקין | ממוצע: 0.79 ננוגרם/מ"ל. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
הערכה וניטור של חלבון דמוי צלב הכרוך בתכונות מרובות של תאים כגון ספיחה, ניידות, וחודרנות.
כללי
למינינים הם משפחה של גליקופרוטאינים של המשתית החוץ-תאית בכל בעלי החיים. הם מרכיבים מרכזיים בממברנת הבסיס, (דהיינו ה-basal lamina). למינינים משפיעים על הפעילות הביולוגית כגון ההתמיינות של תאים, על תנועת תאים ועל ספיחתם (Timpl וחב' ב-J Biol Chem משנת 1979, ו-Durbeej ב-Cell Tissue Res משנת 2010). למינינים הם קומפלקסים חלבוניים הטרוטרימרים עם משקל מולקולרי גבוה (400–900 קילו-דלטון) ומכילים שלוש שרשרות שונות (אלפא, בטא וגאמה) המקודדים על ידי חמישה, ארבעה ושלושה גנים פאראלוגיים באדם, בהתאמה. מולקולות למינין קרויות על פי הרכב השרשרת שלהם, לדוגמה laminin-511 מכילה שרשרות β1, α5 ו-γ1 (Aumailley וחב' ב-Matrix Biol משנת 2005). החלבונים הטרימרים הם בעלי צורת צלב ומסוגלים להיקשר למולקולות אחרות במשתית החוץ-תאית או בממברנת התא (Haralson ו-Hassell ב-IRL Press משנת 1995). שלוש הזרועות הקצרות הן בעלות זיקה למולקולות למינין אחרות, בעוד שהזרוע הארוכה מסוגלת להיקשר לתאים, ובכך לסייע עיגון של של תאים לממברנת הבסיס. הלמינינים מהווים חלק אינטגרלי מהשלד המבני של כמעט כל רקמה באורגניזם, והם מופרשים ועוברים אינקורפורציה למשתיות חוץ-תאיות הקשורות לתאים. גליקופרוטאינים אלה הכרחיים לעמיות ולחיוניות של הרקמה: למינינים פגומים עלולים לגרום לשרירים להיווצר בצורה לא ראויה, תוך שהם גורמים ל-muscular dystrophy, לפגמים בסינון הכלייתי (תסמונת נפרוטית), ולמחלה קטלנית של שלפוחיות בעור (junctional epidermolysis bullosa) (Yurchenco ו-Patton ב-Current Pharmaceut Design משנת 2009).
סוגי הלמינינים
באדם, זוהו 15 טרימרים של למינין, כאשר הלמינינים הם קומבינציות של שרשרות אלפא, בטא וגאמא שונות (Colognato ו-Yurchenco ב-Develop Dynamics משנת 2000). חמישה איזופורמים של שרשרת אלפא: LAMA5, LAMA4, LAMA3, LAMA2, LAMA1; ארבעה איזופורמים של שרשרת בטא:LAMB4, LAMB3, LAMB2, LAMB1; שלושה איזופורמים של שרשרת גאמא: LAMC3, LAMC2, LAMC1.
| שם המולקולה | הרכב השרשרת |
|---|---|
| Laminin-1 | α1β1γ1 |
| Laminin-2 | α2β1γ1 |
| Laminin-3 | α1β2γ1 |
| Laminin 4 | α2β2γ1 |
| Laminin-5 / Laminin-5A | α3Aβ3γ2 |
| Laminin-6 / Laminin-6A | α3Aβ1γ1 |
| Laminin-7 / Laminin-7A | α3Aβ2γ1 |
| Laminin-8 | α4β1γ1 |
| Laminin-9 | α4β2γ1 |
| Laminin-10 | α5β1γ1 |
| Laminin-11 | α5β2γ1 |
| Laminin-12 | α2β1γ3 |
| Laminin-14 | α4β2γ3 |
| α5β2γ2 | |
| Laminin-15 | α5β2γ3 |
תפקוד
למינינים יוצרים רשתות בלתי-תלויות וכרוכים עם קולאגן type IV דרך entactin (לSmith ו-Ockleford ב-Placenta משנת 1994), דרך פיברונקטין (Ockleford וחב' ב-Philosophical Transactions Royal Soc London משנת 1993), ודרך perlecan. החלבונים נקשרים גם כן לממברנות התאים דרך integrins ומולקולות של הממברנה כגון הקומפלקס של הגליקופרוטאין dystroglycan ודרך הגליקופרוטאין הלוטראני של קבוצת הדם. על ידי אינטראקציות אלו. למינינים תורמים ליכולת הספיחה של תאים ולהתמיינות שלהם, כמו גם להישרדות של רקמות. אחדים מתפקודים אלה של למינין נכרכו ברצפים ספציפיים של חומצות אמינו. לדוגמה הרצף הפפטידי GTFALRGDNGDNGQ הממוקם בשרשרת אלפא של למינין, מסייע לספיחה של תאי אנדותל. למינין alpha4 מפוזר במגוון של רקמות, כולל עצבים היקפיים, שרירי שלד, קפילרות ו-dorsal root ganglion, וכן בצומת הנוירו-שרירית והוא חיוני לפעילות הסינפסה (Ichikawa וחב' ב-Biochemistry משנת 2005). המבנה של מקטע של laminin-G דומה לזה של pentraxin (Beckmann וחב' ב-J Mol Biol משנת 1998).
התפקיד של למינין בהתפתחות הנוירלית
למינין-111 הוא מצע עיקרי דרכו אקסונים של תאי עצב גדלים, in vivo ו־in vitro. לדוגמה, למינין זה מונח במסלול בו התפתחות של תאי גנגליון של הרשתית מתקדמת מהרשתית ל-tectum (שהוא אזור במוח, הממוקם בחלק הגבי של המוח האמצעי. הטקטום אחראי לרפלקסים שמיעתיים וחזותיים). הנוכחות של למינין-111 יכולה להשפיע על תגובת ה-cones האחראיים ברשתית לחישה של צבע. השפעה זו של למינין-111 מתרחשת על ידי הפחתה של cyclic AMP תוך-תאי.
התפקיד של למינין בשיקום של עצב היקפי
למינינים מועשרים באזורי נגעים לאחר פגיעה בעצב היקפי והם מופרשים על ידי תאי Schwann (Nieuwenhuis וחב' ב-Biol Rev Cambridge Philosoph Soc משנת 2018). נוירונים של מערכת העצבים ההיקפיים מבטאים קולטנים של integrin נקשרים על ידי למינינים ותומכים בנוירו-רגנרציה לאחר פציעה.
פתולוגיה
פגיעה בתפקוד של laminin-211, היא הסיבה לצורה אחת של muscular dystrophy מולדת (Hall וחב' ב-Proc Natl Acad Sci USA משנת 2007). למינין-211 מורכב משרשרות β1, α2 ו-γ1. למינין זה מופע בעיקר במוח, ובסיבי שריר. בשריר הוא נקשר ל-alpha-dystroglycan, ול-integrin alpha7-beta1, וקצהו השני נקשר למשתית החוץ-תאית. Laminin-332 חיוני לספיחה של תאי אפיתל לממברנת הבסיס וכאשר הוא אנומלי מוביל הדבר ל-junctional epidermolysis bullosa המאופיינת על ידי שלפוחיות, רקמת גרנולציה חיונית של העור והרירית ושיניים מגולענות. Laminin-521 רב-תפקודי בכליות גורם לדליפה של חלבון לתוך השתן ולתסמונת נפרוטית.
תפקיד למינין בסרטן
איזופורמים אחדים של למינין נכרכו בפתו-פיזיולוגיה של סרטן. אירוע חיוני בהתפתחות סרטן, הוא מה שמוגדר כ-epithelial-to-mesenchymal transition (EMT), המאפשר לתאי קרצינומה לרכוש תכונות של חודרנות. השפעול של מרכיבי המשתית החוץ-תאית הידוע כ-laminin B1 (להלן LAMB1) במהלך ה-EMT דווח. ביחד עם עוד מרכיבים עיקריים במשתית החוץ-תאית, כגון קולאגנים ופיברונקטין, למינינים שימשו לעודד תאי אב (stem cells) רב-פוטנטיים, כמו גם תאים ראשוניים בתרבית, שקשה להביא לשגשוגם.
שני סוגים של למינינים טבעיים זמינים מסחרית: למינין-111 המופק מסרקומות בעכברים, ותערובות של למינין משליית אדם, המתאימים ללמינין 411,211 או 511, בתלות בחברה המספקת אותם (Wondimu וחב' ב-Matrix Biol משנת 2006). בידוד של איזופורמים של למינין קשה פרקטית לבודד מרקמות בצורה נקייה בגלל cross linking אקסטנסיבי והצורך בתנאי מיצוי קשים, כגון אנזימים פרוטאוליטים או pH נמוך, הגורמים לדגרדציה של הלמינינים. לפיכך, יוצרו למינינים ריקומביננטיים מאז שנת 2000 (Kortesmaa וחב' ב-J Biol Chem משנת 2000). בשנת 2008, שתי קבוצות הראו באופן בלתי-תלוי שניתן לגדל תאי-אב מעוברים של עכברים למשך חודשים בסיוע למינין-511 (Domogatskaya וחב' ב-Stem Cells משנת 2008, ו-Miyazaki וחב' ב-Biochem Biophys Res Commun מאותה שנה). לאחר מכן נמצא שלמינין-511 רקומביננטי, יכול להיות מנוצל ליצור תנאים מוגדרים בתרבית רקמה לגדל תאי אב עובריים (ESC) פלוריפוטנטיים (שיכולים לצמוח לכיוונים שונים) ותאי IPS (או Induced pluripotent stem cells) של אדם (Rodin וחב' ב-Nature Biotechnol משנת 2010).
למינין B
מקטע למינין B (הידוע גם כמקטע IV) הוא מודול חוץ-תאי עם תפקוד לא ברור. הוא נמצא במספר חלבונים שונים הכוללים heparan sulphate proteoglycan מממברנת הבסיס, וחלבון דמוי-למינין ממקור של Caenorhabditis elegans. המקטע של למינין IV אינו נמצא בשרשרות הקצרות של למינין (alpha4 או beta3).
למינין דמוי-EGF
מלבד סוגים שונים של מקטעים גלובולריים כל תת-יחידה של למינין מכילה בקצה הראשון שלה החזרים של בערך 60 חומצות אמינו הכוללים 8 שיירים משומרים של ציסטאין (Engel ב-FEBS Lett משנת 1989). המבנה השלישוני של מקטע זה דומה בקצה ה-N טרמינלי שלו לזה של המודול דמוי-EGF (Stetefeld וחב' ב-J Mol Biol משנת 1996, ו-Baumgartner וחב' באותו כתב-עת מאותה שנה). מספר העותקים של המקטע שלל למינין דמוי-EGF מאוד וריאבילי כאשר בין 3 ל-22 עותקים נמצאו בשרשרת laminin gamma-1 בעכבר, כאשר המקטע השביעי נמצא להיות היחיד הנקשר בזיקה גדולה ל-nidogen שהוא חלבון חשוב בממברנת הבסיס (Mayer וחב' ב-FEBS Lett משנת 1995).
למינין G
המקטע הגלובולרי (G) של למינין הוא בעל 177 חומצות אמינו, ויכול להימצא ב-1 עד 6 עותקים בחברים שונים של משפחת הלמינינים כמו גם במספר גדול של חלבונים חוץ-תאיים אחרים. לדוגמה, כל שרשרות אלפא של למינין מכילים 54 מקטעי למינין G, בה בשעה ש-neurexin 1 ו-2 מכילים 6 מקטעי למינין G. התפקיד המדויק של מקטע למינין G נותר בלתי ברור. לדוגמה, שרשרות אלפא 1 ו-אלפא 2 של למינין מכילות חמישה מקטעי למינין G ללC-טרמינלים, בעוד שרק מקטעי LG4 ו-LG5 מכילים אתרי קישור להפארין, לסולפטידים ולקולטן של dystroglycan (Tisi וחב' ב-EMBO J משנת 2000). נראה שחלבוני למינין G הם בעלי מספר תפקידים בספיחת תאים, נדידתם והתמיינותם.
הביולוגיה המבנית של למינינים
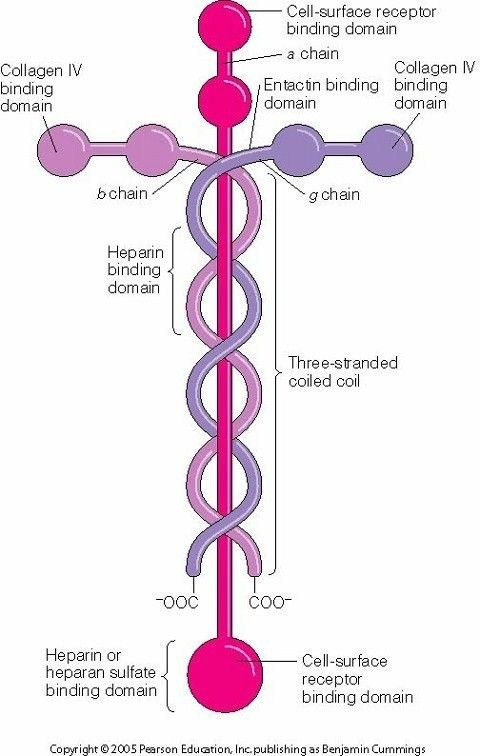
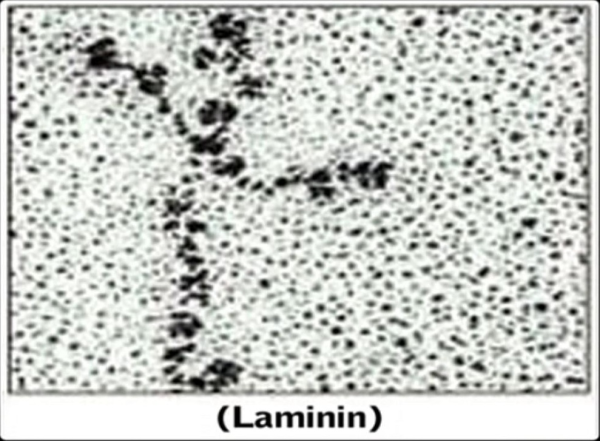
מחקרים מבניים על ידי אלקטרון מיקרוסקופיה שהחלו בראשית שנות ה-80, גילו מולקולה דמוית-צלב, שהתבררה לאחר מכן כמכילה שלוש שרשרות פוליפפטידיות. מחקרים קריסטלוגרפיים מאז אמצע שנות ה-90 הוסיפו מידע על ההטרוטרימרים של למינין. שלושת הזרועות הקצרים של מבנה דמוי-צלב זה היו עשירים במקטעים עשירים בדיסולפידים. המקטעים הגלובולריים בקצות הזרועות הקצרים סייעו לפולימריזציה של למינין. הזרוע הארוכה של מבנה הצלב היא אלפא-הליקלית הכרוכה באזור גלובולי הנספח לתאים. מחקרים מבניים של למינין החלו ב-1996, כאשר Stetefeld וחב' קבעו את המבנים הגבישיים של המקטעים 7-9 של שרשרת γ1 ב-aminin-type epidermal growth factor-like domain במאמר שהתפרסם ב-J Mol Biol. המבנה דמוי המוט של למינין γ1 LE7-9 חסר מבנה הידרופובי אך במקומו מבנה ה-LE מיוצב על ידי ארבעה קשרים דיסולפידיים כאשר קשרים אלה המיוצבים על ידי γ1 LE7-9 (דהיינו שמונה ציסטאינים המחברים את מקטעים 1–3, 2–4, 5–6 ו-7–8) נמצאו לאחר מכן בכל המבנים של LE ( Kalkhof וחב' ב-Biochemistry משנת 2010).
בראשית שנות ה-80 של המאה ה-20 שתי מעבדות ניקו באופן בלתי-תלוי גליקופרוטאין גדול מהמשתית החוץ-תאית של תאי סרטן בעכברים (Timpl וחב' ב-J Biol Chem משנת 1979, ו-Chung וחב' ב-Cell מאותה שנה). ידוע שיונקים מכילים לפחות 15 איזופורמים של למינין (כאשר חסרי-חוליות מכילים רק 2 איזופורמים), ושלמינינים חיוניים: בחסר שלהם, לא נוצרת ממברנת הבסיס ונמנע גידול של עוברים בשלב ההיריון המוקדם. בדומה לפיברונקטין, למינינים יוצרים רשתות ונקשרים לקולטנים תאיים. אי הצלחת היקשרות של למינינים לתאים גורמת לחלות אנושיות קשות כגון דיסטרופיות של שרירים (Mercury ו-Muntoni ב-Lancet משנת 2013), או שלפוחיות בעור (Uitto וחב' ב-Matrix Biol משנת 2017). כאמור, למינינים הם הטרוטרימרים המורכבים משרשרת אחת של β, α ו- γ . גנומים של יונקים מקודדים ל-5 שרשרות α, ל-4 שרשרות β, ול-3 שרשרות γ : רק 15 מתוך 60 הטרוטרימרים אפשריים אושרו ביוכימית (Aumailley וחב' ב-Matrix Biol משנת 2005, ו-Coble וחב' ב-Hum Mol Genet משנת 2017). הלמינין שבודד במקור מהמשתית של גידול סרטני בעכבר הוא הטרוטרימר α1β1γ1, שקרוי laminin-111 שמשקלו המולקולרי בערך 900 קילו-דלטון. שרשרות למינין זה קשורות קו-ולנטית על ידי קשרים די-סולפידיים. ההיבטים הראשונים של המבנה של למינין-111 הושגו על ידי rotary shadowing electron microscopy, שגילה ארבעה זרועות: זרוע ארוכה שאורכה בערך 77 ננומטר, המסתיימת במבנה גלובולרי הידוע כמקטע G, ושלושה זרועות קצרים יותר באורך של בערך 34 ננומטר, המסתיימים בזוג של מבנים גלובולרים קטנים יותר (Engel וחב' ב-J Mol Biol משנת 1981).
הוראות לביצוע הבדיקה
לאחר נטילת דם ורידי לתוך מבחנה כימית (פקק אדום או צהוב) בטמפרטורת החדר יבוצע סרכוז למשך 10 דקות במהירות 4,000 סיבובים לדקה. הנסיוב מוקפא מיד לאחר הסרכוז עד לאנליזה. ורמת למינין בנסיוב נמדדת בשיטת ELISA שעשתה שימוש בשיטת סנדוויץ של נוגדן כפול. דגימות הנסיוב מוספות לתוך בארות שמצופות קודם לכן עם נוגדן חד-שבטי כנגד למינין אנושי תוצרת Wuhan EIAab Science Co. China. לאחר הדגרה, נוגדנים כנגד למינין המסומנים עם ביוטין ובשילוב עם streptavidin-horseradish peroxidase הם מוספים ליצור קומפלקס חיסוני לאחר הדגרה של שעה אחת. חומר בלתי קשור צריך להישטף ולאחר מכן יש להוסיף את תמיסת הכרומוגן על מנת להמיר את התמיסה הבלתי צבועה לתמיסה בצבע כחול, שעוצמתו פרופורציונית לריכוז הלמינין בדגימה. הצבע אמור להתחלף לצבע צהוב כשמוסיפים תמיסת עצירה חומצית. את הצבע הצהוב מודדים על ידי "קורא ELISA" אוטומטי (ChroMate, 4300 Microplate Reader; Awareness Technology, Inc., Palm City, USA). התוצאה מבוטאת בערכי ננוגרם/מ"ל.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק