הבדלים בין גרסאות בדף "פוספו-גליצרט קינאז - Phosphoglycerate kinase"
(←מבנה) |
|||
| שורה 27: | שורה 27: | ||
== התפקיד של מגנזיום== | == התפקיד של מגנזיום== | ||
| − | יוני מגנזיום באופן נורמלי מחוברים לקבוצות פוספאט של המצע הנוקלאוטידי של PGK. ידוע שבחסר של מגנזיום, נמנעת פעילות האנזים (Varga וחב' ב-Biochemistry משנת 2012). המתכת הדו-ערכית מסייעת לליגנדים של האנזים למסך את המטענים השליליים של קבוצות הפוספאט הקשורות, מה שמאפשר התרחשות התקפה נוקלאופילית האופיינית לריאקציה של phosphotransfer ({{כ}}Cliff וחב' ב- J Am Chem Soc משנת 2010). | + | יוני [[מגנזיום]] באופן נורמלי מחוברים לקבוצות פוספאט של המצע הנוקלאוטידי של PGK. ידוע שבחסר של מגנזיום, נמנעת פעילות האנזים (Varga וחב' ב-Biochemistry משנת 2012). המתכת הדו-ערכית מסייעת לליגנדים של האנזים למסך את המטענים השליליים של קבוצות הפוספאט הקשורות, מה שמאפשר התרחשות התקפה נוקלאופילית האופיינית לריאקציה של phosphotransfer ({{כ}}Cliff וחב' ב- J Am Chem Soc משנת 2010). |
==מנגנון== | ==מנגנון== | ||
ללא קישור של המצעים, PGK מצוי בקונפורמציה "פתוחה". לאחר שמצעים שהן triose והן נוקלאוטידים נקשרים למקטעים ה-N וה-C טרמינליים בהתאמה, יש התרחשות של hinge bending שמביאה את המצעים הללו והמצעים הקשורים אליהם לקרבה הדוקה ולקונפורמציה "סגורה" (Banks וחב' ב-Nature משנת 1979). בנקודה זו, במקרה של ריאקציה גליקוליטית ישירה, ה-beta-phosphate של ADP מאתחל התקפה נוקלאופילית על 1phosphate של 1,3BPG. שייר Lys219 על פני האנזים, מכוון את קבוצת הפוספאט למצע. במסלול הגליקוליטי 1,3BPG הוא תורם הפוספאט והוא בעל פוטנציאל גבוה של טרנספר של פוספוריל. הטרנספר המקוטלז על ידי PGK של קבוצת פוספאט מ- 1,3BPG לקבלת ATP יכול ל"תדלק" את ריאקציית חמצון הפחמן משלב הגליקוליזה הקודם המתמיר glyceraldehyde 3-phosphate ל- 3phosphoglycerate. | ללא קישור של המצעים, PGK מצוי בקונפורמציה "פתוחה". לאחר שמצעים שהן triose והן נוקלאוטידים נקשרים למקטעים ה-N וה-C טרמינליים בהתאמה, יש התרחשות של hinge bending שמביאה את המצעים הללו והמצעים הקשורים אליהם לקרבה הדוקה ולקונפורמציה "סגורה" (Banks וחב' ב-Nature משנת 1979). בנקודה זו, במקרה של ריאקציה גליקוליטית ישירה, ה-beta-phosphate של ADP מאתחל התקפה נוקלאופילית על 1phosphate של 1,3BPG. שייר Lys219 על פני האנזים, מכוון את קבוצת הפוספאט למצע. במסלול הגליקוליטי 1,3BPG הוא תורם הפוספאט והוא בעל פוטנציאל גבוה של טרנספר של פוספוריל. הטרנספר המקוטלז על ידי PGK של קבוצת פוספאט מ- 1,3BPG לקבלת ATP יכול ל"תדלק" את ריאקציית חמצון הפחמן משלב הגליקוליזה הקודם המתמיר glyceraldehyde 3-phosphate ל- 3phosphoglycerate. | ||
גרסה מ־16:19, 27 באפריל 2026
| מדריך בדיקות מעבדה | |
| פוספו-גליצרט קינאז | |
|---|---|
| Phosphoglycerate kinase | |
| שמות אחרים | PGK1, קינאז פוספוגליצרטי |
| מעבדה | כימיה בדם |
| תחום | שיבושים בגליקוליזה. |
| טווח ערכים תקין | מגיל 12 חודשים ומעלה - 142-232 יחידות/גרם המוגלובין. ערכי נורמה לא נקבעו לבני פחות מ-12 חודשים. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
הערכת מטופלים עם אנמיה המוליטית לא-ספרוציטית Coombs שלילים, בעיקר עם מתווה תורשתי הכרוך עם כרומוזום X. הערכה של מטופלים עם תסמינים מיופתיים או נוירולוגיים.
כללי
PGK1 הוא אנזים המקטלז את הטרנספר של קבוצת פוספאט מחומצה 1,3-ביספוספוגליצרית (1,3-bisphosphoglyceric acid (להלן 1,3BPG)) לאדנוזין דיפוספט (ADP) תוך יצירת חומצה של 3-פוספוגליצרית (3phosphoglyceric acid (להלן 3PG)) ואדנוזין טריפוספט (ATP) במהלך הגליקוליזה. האנזים משופעל על ידי רמות נמוכות של אניונים מולטי-ולנטיים שונים כגון pyrophosphate, sulfate וציטראט. ריכוזים גבוהים של MgATP ושל 3PG משפעלים את PGK, בעוד ש- 2+Mg בריכוזים גבוהים מעכב באופן לא-תחרותי את האנזים (Bernstein ו-Hot ב-Biochemistry משנת 1998). ל-PGK יש ספציפיות רחבה כלפי מצעים נוקלאוטידיים (Varga וחב' ב- Mol BioSyst משנת 2011). פעילותו מעוכבת על ידי סליצילטים, הנראים כמחקים את המצע הנוקלאוטידי של האנזים (Larsson-Raźnikiewicz ו-Wiksell ב-Biochim Biophys Acta משנת 1978).
בדומה לכל הקינאזות, PGK הוא גם טרנספראז. PGK הוא אנזים מרכזי המשמש בגליקוליזה, בצעד הראשון של יצירת ATP במסלול הגליקוליטי. בגלוקונאוגנזה, הריאקציה מקוטלזת על ידי PGK מתקדמת בכיוון הפוך ומייצרת ADP ו-BPG1-3. באדם, שני אנזימים של PGK זוהו עד כה, PGK1 ו-PGK2. שני איזואנזימים אלו הם בעלי הומולוגיה של 87% ברצף חומצות האמינו שלהם, ולמרות שהם דומים מבנית ותפקודית, הם ממוקמים במקומות שונים. PGK1 המקודד על ידי גן הממוקם בכרומוזום X באתר q13.3 מבוטא בכל התאים, ואילו PGK2 המקודד על ידי גן אוטוסומלי הממוקם בכרומוזום 6 באתר p21-q12 ייחודי לתאים ספרמטוגניים מיוטיים ובתר-מיוטיים (Chiarelli וחב' ב-PLoS One משנת 2012).
התפקוד הביולוגי
PGK מצוי בכל האורגניזמים כאחד משני אנזימים המייצרים ATP במסלול הגליקוליזה. בתנאים ביולוגיים סטנדרטיים, הכיוון הגליקוליטי מועדף במסלול Calvin באורגניזמים פוטוסינטתיים, בו PGK מקטלז את הפוספורילציה של 3PG, לייצור של 1,3BPG ו-ADP כחלק מהריאקציות המבצעות רה-גנרציה של ribulose-1,5-bisphosphate. דווח ש-PGK הוא בעל פעילות של thiol reductase על פלזמין, המובילה ליצירה של אנגיוסטטין, אשר מעכב אנגיוגנזה לגדילת תאי סרטן. האנזים נמצא גם משתתף ברפליקציה של DNA, ובתיקון של גרעינים בתאי יונקים (Lay וחב' ב-Nature משנת 2000). האיזואנזים האנושי PGK2 המבוטא רק במהלך הספרמטוגנזה, נמצא כחיוני לתפקוד תאי זרע בעכברים (Danshina וחב' ב-Biol Reprduct משנת 2010).
מבנה
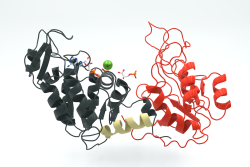
PGK נמצא בכל האורגניזמים החיים כאחד משני האנזימים המייצרים ATP בגליקוליזה והרצף שלו נמצא משומר באופן בולט במהלך האבולוציה. האנזים הוא מונומר המכיל 415 חומצות אמינו, ומכיל שני מקטעים בגודל כמעט שווה (Dhar וחב' ב- Proc Natl Acad Sci USA משנת 2019). 3-phosphoglycerate (להלן 3PG) נקשר לקצה ה-N-טרמינלי, בעוד שהמצעים הנוקלאוטידים, MgATP או MgADP, נקשרים למקטע ה-C-טרמינלי של האנזים. מבנה שני-מקטעים זה כרוך בסקלה גדולה של "hinge bending" הדומה לאלה שמוצאים ב-hexokinase (Kumar וחב' ב-Cell Biochem Biophys משנת 1999). שני המקטעים של החלבון מופרדים על ידי בקיע וקשורים על ידי שני סלילי אלפא. בליבה של כל מקטע יש שישה beta-sheets מקבילים המוקפים על ידי סלילי אלפא. שתי האונות מסוגלות לעבור קיפול באופן בלתי-תלוי, בהתאמה עם הנוכחות של תוצרי ביניים במסלול הקיפול של מקטע בודד (Yon וחב' ב-Biochimie משנת 1990, ו-Zerrad וחב' ב-J Biol Chem משנת 2011). לאנזים יש נטייה להיות קיים בקונפורמציה פתוחה עם פרקי זמן קצרים של קונפורמציה סגורה וקטליזה, המאפשרים דיפוזיה מהירה של המצע ותוצרי הריאקציה דרך אתרי קישור; הקונפורמציה הפתוחה של PGK היא יותר יציבה כתוצאה מהחשיפה של האזור ההידרופובי של החלבון בסגירת המקטע.
התפקיד של מגנזיום
יוני מגנזיום באופן נורמלי מחוברים לקבוצות פוספאט של המצע הנוקלאוטידי של PGK. ידוע שבחסר של מגנזיום, נמנעת פעילות האנזים (Varga וחב' ב-Biochemistry משנת 2012). המתכת הדו-ערכית מסייעת לליגנדים של האנזים למסך את המטענים השליליים של קבוצות הפוספאט הקשורות, מה שמאפשר התרחשות התקפה נוקלאופילית האופיינית לריאקציה של phosphotransfer (Cliff וחב' ב- J Am Chem Soc משנת 2010).
מנגנון
ללא קישור של המצעים, PGK מצוי בקונפורמציה "פתוחה". לאחר שמצעים שהן triose והן נוקלאוטידים נקשרים למקטעים ה-N וה-C טרמינליים בהתאמה, יש התרחשות של hinge bending שמביאה את המצעים הללו והמצעים הקשורים אליהם לקרבה הדוקה ולקונפורמציה "סגורה" (Banks וחב' ב-Nature משנת 1979). בנקודה זו, במקרה של ריאקציה גליקוליטית ישירה, ה-beta-phosphate של ADP מאתחל התקפה נוקלאופילית על 1phosphate של 1,3BPG. שייר Lys219 על פני האנזים, מכוון את קבוצת הפוספאט למצע. במסלול הגליקוליטי 1,3BPG הוא תורם הפוספאט והוא בעל פוטנציאל גבוה של טרנספר של פוספוריל. הטרנספר המקוטלז על ידי PGK של קבוצת פוספאט מ- 1,3BPG לקבלת ATP יכול ל"תדלק" את ריאקציית חמצון הפחמן משלב הגליקוליזה הקודם המתמיר glyceraldehyde 3-phosphate ל- 3phosphoglycerate.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק