הבדלים בין גרסאות בדף "Thyroid stimulating immunoglobulin"
| (3 גרסאות ביניים של אותו משתמש אינן מוצגות) | |||
| שורה 37: | שורה 37: | ||
==משמעותן של תוצאות מוגברות במדידת TSI== | ==משמעותן של תוצאות מוגברות במדידת TSI== | ||
| − | תוצאה מוגברת | + | |
| + | תוצאה מוגברת של TSI יכולה להעיד באופן מובהק על נוכחות מחלת Graves, אך באופן לא שכיח על Hashimoto toxicosis בה יש פעילות מוגברת של התירואיד הנגרמת מדלקת הקשורה ל-Hashimoto’s thyroiditis (הידוע גם כ-chronic thyroiditis), המתבטאת בבלוטת תריס נפוחה עם פעילות מופחתת (hypothyroidism) של הבלוטה לעתים. רמות גבוהות של TSI נמצא בתרחיש של neonatal thyrotoxicosis כאשר לוולד יש רמה גבוהה של הורמוני תירואיד בלידה בגלל מפגע של התירואיד באם, אם כי מצב זה חולף בתינוק לאחר טיפול. רמות לא תקינות של TSI נמצא ב- toxic multinodular goiter, בו מוצאים בבלוטה התפוחה nodules המייצרים רמה מוגברת של הורמוני התירואיד. | ||
| + | |||
==היבטים קליניים== | ==היבטים קליניים== | ||
| − | מחלת Graves היא המפגע השכיח ביותר הגורם ל-hyperthyroidism, והוא מאופיין על ידי נוכחות | + | מחלת Graves היא המפגע השכיח ביותר הגורם ל-hyperthyroidism, והוא מאופיין על ידי נוכחות של TSI שניתן למצאם בכמעט 90% מהמקרים. TSI מחקה את הפעילות של TSH, והוא גורם ליצירה מוגברת של הורמוני הבלוטה. כאשר לא ניתן טיפול, מחלת Graves עלולה לגרום להפלות, למומי לידה, למחלות עיניים ובעיקר לבלט-עין (אקסופתלמוס), ואף לגרום לסכנת חיים. לנשים יש סיכון גדול פי- 10-20 ללקות במחלה זו, מאשר לגברים. כל צורות ה-autoimmune thyrotoxicosis (כגון מחלת Graves, השימוטו טוקסיקוזיס ו- neonatal thyrotoxicosis), יכולות להיגרם על ידי יצירה של נוגדנים עצמיים המגיבים עם הקולטן של TSH. התפקיד של נוגדנים עצמיים כנגד thyroid peroxidase או כנגד תירוגלובולין, במצבים של autoimmune thyrotoxicosis או ב- autoimmune hypothyroidismפחות ברור, והם יכולים לייצג רק epiphenomena. ריכוזים ניתנים לגילוי של נוגדנים כנגד TPO מוצאים ברוב המטופלים עם מחלות אוטו-אימוניות של התירואיד כמו Hashimoto's thyroiditis, מחלת Graves או idiopathic myxedema. |
| − | נוגדנים עצמיים שיכולים להיקשר ולשפעל את ה-TSHR, יכולים להביא לגירוי בלוטת התריס באופן שהוא בלתי-תלוי ב-feedback הנורמאלי הנובע מגירי קולטנים אלה על ידי TSH. נוגדן עצמי כגון TSI המגיב | + | |
| + | נוגדנים עצמיים שיכולים להיקשר ולשפעל את ה-TSHR, יכולים להביא לגירוי בלוטת התריס באופן שהוא בלתי-תלוי ב-feedback הנורמאלי הנובע מגירי קולטנים אלה על ידי TSH. נוגדן עצמי כגון TSI המגיב עם TSHR ידוע גם בשל פעילותו ארוכת הטווח וככן מכונה גם LATS או Long-Acting Thyroid Stimulator. לאחדים מהמטופלים עם מחלת Graves, יש גם TSHR-blocking antibodies, והאיזון בין TSI לבין TSHR-blocking antibodies, קובעים את חומרת מחלת Graves. לפחות ב- 20% מאלה עם היפו-תירואידיזם אוטו-אימוני, יש עדות לנוכחות TSHR-blocking antibodies או באופן פחות שכיח גם TSI. | ||
| + | |||
נוגדנים עצמים המגיבים עם TSHR ניתן למצוא עוד לפני שתסמיני תירו-טוקסיקוזיס אוטו-אימונית באים לביטוי קליני וביוכימי. כיוון שאף לא אחד מהטיפולים של מחלת Graves מכוונים כנגד תהליך המחלה, אלא נועד לפגוע בבלוטה או לחסום את סינתזת הורמוני הבלוטה, ניתן למצוא עדיין TSI גם לאחר הריפוי הנראה לעין.TSI הם נוגדנים מסוג IgG ולכן יכולים לעבור את מחסום השליה ולגרום לעובר thyrotoxicosis (על פי Jevalikar וחב' בJ Pediatr Endocrinol Metab משנת 2014, ו-Chen ו-Yu ב- Clin Endocrinol (Oxf) משנת 2011, וכן Thangaratinam וחב' ב-BMJ משנת 2011). מדידת TSHR-Ab מגלה את רמת TSI כמו גם את רמת נוגדנים העצמיים שהם TSHR-blocking. | נוגדנים עצמים המגיבים עם TSHR ניתן למצוא עוד לפני שתסמיני תירו-טוקסיקוזיס אוטו-אימונית באים לביטוי קליני וביוכימי. כיוון שאף לא אחד מהטיפולים של מחלת Graves מכוונים כנגד תהליך המחלה, אלא נועד לפגוע בבלוטה או לחסום את סינתזת הורמוני הבלוטה, ניתן למצוא עדיין TSI גם לאחר הריפוי הנראה לעין.TSI הם נוגדנים מסוג IgG ולכן יכולים לעבור את מחסום השליה ולגרום לעובר thyrotoxicosis (על פי Jevalikar וחב' בJ Pediatr Endocrinol Metab משנת 2014, ו-Chen ו-Yu ב- Clin Endocrinol (Oxf) משנת 2011, וכן Thangaratinam וחב' ב-BMJ משנת 2011). מדידת TSHR-Ab מגלה את רמת TSI כמו גם את רמת נוגדנים העצמיים שהם TSHR-blocking. | ||
| + | |||
הרגישות והספציפיות של רמה מוגברת של נוגדני TSI באבחון מחלת Graves תלויים באם הנבדק הוא בעיצומו של מהלך פעיל של המחלה, או שהוא אינו מטופל, או באם הוא מטופל בתכשירים אנטי-תירואידאליים. אם משתמשים במאובחנים חדשים ולא מטופלים במדד של רמת TSI הגבוה פי 1.3 מהנורמה, הרגישות והספציפיות של מבדק זה עולים על 90%. | הרגישות והספציפיות של רמה מוגברת של נוגדני TSI באבחון מחלת Graves תלויים באם הנבדק הוא בעיצומו של מהלך פעיל של המחלה, או שהוא אינו מטופל, או באם הוא מטופל בתכשירים אנטי-תירואידאליים. אם משתמשים במאובחנים חדשים ולא מטופלים במדד של רמת TSI הגבוה פי 1.3 מהנורמה, הרגישות והספציפיות של מבדק זה עולים על 90%. | ||
| + | |||
תרחיש משמעותי של neonatal thyrotoxicosis ייתכן באישה בהיריון עם היסטוריה של מחלת Graves ותוצאת TSI הגבוהה בלמעלה מ-290% מעל הנורמה בשליש ההיריון האחרון, בלי כל קשר לסטאטוס הרמיסיה שלה. תוצאות TSI פחות מוגברות, עלולות להיות כרוכות רק לעתים מזומנות עם neonatal thyrotoxicosis. נתונים אלה רלוונטיים עבור נשים שעברו בעבר טיפול לאבלציה של הבלוטה, או עבור נשים המטופלות באופן פעיל עם תכשירים אנטי-תירואידאליים, ואינן בעלות תסמינים ביוכימיים או קליניים של thyrotoxicosis. | תרחיש משמעותי של neonatal thyrotoxicosis ייתכן באישה בהיריון עם היסטוריה של מחלת Graves ותוצאת TSI הגבוהה בלמעלה מ-290% מעל הנורמה בשליש ההיריון האחרון, בלי כל קשר לסטאטוס הרמיסיה שלה. תוצאות TSI פחות מוגברות, עלולות להיות כרוכות רק לעתים מזומנות עם neonatal thyrotoxicosis. נתונים אלה רלוונטיים עבור נשים שעברו בעבר טיפול לאבלציה של הבלוטה, או עבור נשים המטופלות באופן פעיל עם תכשירים אנטי-תירואידאליים, ואינן בעלות תסמינים ביוכימיים או קליניים של thyrotoxicosis. | ||
| − | תירו-טוקסיקוזיס בהיריון, הנובע משילוב של פעילות צולבת של human chorionic gonadotropin עם TSHR ושינויים חולפים בפעילות הורמוני הבלוטה, ואינו כרוך בעלייה ברמת TSI. נוכחות של רמה מוגברת של TSI בתרחיש זה מצביע על מחלת Graves. כמו כן, רמה מוגברת | + | |
| + | תירו-טוקסיקוזיס בהיריון, הנובע משילוב של פעילות צולבת של human chorionic gonadotropin עם TSHR ושינויים חולפים בפעילות הורמוני הבלוטה, ואינו כרוך בעלייה ברמת TSI. נוכחות של רמה מוגברת של TSI בתרחיש זה מצביע על מחלת Graves. כמו כן, רמה מוגברת של TSI בסיום של מחזור טיפולים בתכשירים אנטי-תירואידאליים מצביע בסבירות גבוהה של הׅשנׅוּת מחלת Graves. יחד עם זאת, תוצאה נורמאלית של TSI אינה מעידה בהכרח על רמיסיה ממושכת. במטופלים בהם תוצאות המבחנים של בלוטת התריס נעות לסירוגין בין היפו- והיפר-תירואידיזם, רמות מוגברות של נוגדני TSHR במקביל לרמות תקינות או מוגברות באופן קל של TSI, מרמזות על אבחון אפשרי של Hashimoto toxicosis. יצוין כמו כן שאם כי תוצאות מוגברות של TSI מהוות אינדיקציה חזקה למחלת Graves, אין הן תואמות תמיד מצב של היפר-תירואידיזם או את חומרתו. במטופלים עם מחלת השימוטו ניתן למצוא רמות TSI מוגברות, שיכולות להגיע עד 1.8 מהנורמה. רמות TSI שבין 1.3-1.8 מהנורמה, נצפות לעתים המספר מפגעים אחרים של הבלוטה, כולל nodular goiter ו- subacute thyroiditis (על פי Saravanan ו-Dayan ב- Endocrinol Metab Clin North Amמשנת 2001). | ||
| + | |||
== הוראות לביצוע הבדיקה == | == הוראות לביצוע הבדיקה == | ||
אין צורך בהכנה מוקדמת כגון צום. הדם נלקח במבחנה כימית (פקק אדום) או במבחנת ג'ל, ויש לשלחו למעבדה בקירור. יש לפסול דגימות שהגיעו למעבדה לא מקוררות. לאחר הסרכוז והפרדת הנסיוב מהתאים, ניתן לשמור את הנסיוב בטמפרטורת החדר ל-24 שעות, בקירור למשך 14 יום, או בהקפאה למשך 90 יום. יש לפסול דגימות מאוד המוליטיות, ליפמיות או איקטריות, אך ניתן לקבל דגיות עם המולידה, ליפמיה או איקטריה מתונה. | אין צורך בהכנה מוקדמת כגון צום. הדם נלקח במבחנה כימית (פקק אדום) או במבחנת ג'ל, ויש לשלחו למעבדה בקירור. יש לפסול דגימות שהגיעו למעבדה לא מקוררות. לאחר הסרכוז והפרדת הנסיוב מהתאים, ניתן לשמור את הנסיוב בטמפרטורת החדר ל-24 שעות, בקירור למשך 14 יום, או בהקפאה למשך 90 יום. יש לפסול דגימות מאוד המוליטיות, ליפמיות או איקטריות, אך ניתן לקבל דגיות עם המולידה, ליפמיה או איקטריה מתונה. | ||
==גישות מתודולוגיות למדידת רמת TSI== | ==גישות מתודולוגיות למדידת רמת TSI== | ||
| − | הסקירה של Morris וחב' ב-Mayo Clin Proc משנת 1988 ייחדה דיון מקיף להשוואה בין שיטות להערכת קישור נוגדנים עצמיים לקולטן של TSH. בין השאר הושוו שיטות | + | הסקירה של Morris וחב' ב-Mayo Clin Proc משנת 1988 ייחדה דיון מקיף להשוואה בין שיטות להערכת קישור נוגדנים עצמיים לקולטן של TSH. בין השאר הושוו שיטות radio-receptor ושיטות bioassay, זאת בעידן בו הרבו להשתמש ב- quantitative recombinant bioassayאו ב- quantitative chemiluminescent immunoassay. בשנים האחרונות הוכנסו שיטות משופרות למדידת רמת TSI : Lahooti וחב' פרסמו בשנת 2014 ב-Austin J Clin Ophthalmol שיטה הידועה כ-Thyretain TSI reporter cAMP luciferase bioassay, שפורסמה לראשונה על ידי Lytton וחב' בשנת 2010 ב-Clin Exp Immunol. עיקרון השיטה מבוסס על כך ש-TSI עשוי גם לעודד יצירת cAMP , וניתן אם כך ב-bioassay למדוד יכולת זו בשורת-תאים (cell line) המבטאת את הקולטן ל-TSH. לשיטת luciferase יש רגישות אמליטית של 75% אך יש בה מגבלה בכך שתוצאות false negative עלולות להתקבל בנוכחות נוגדנים חוסמי TSH. |
| + | [[קובץ:TSI 1.jpg|מרכז|500 פיקסלים]] | ||
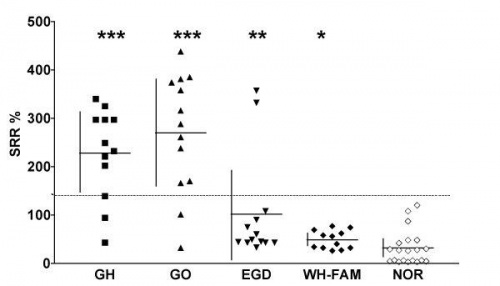
| + | רמות TSI הנבדקים עם Graves hyperthyroidism ללא אופתלמופתיה (GH), עם אופתלמופתיה (GO), עם euthyroid Graves disease {{כ}}(EGD), נבדקים עם תפקוד תירואיד תקין שהם בני-משפחה בודדת עם שכיחות גבוהה של מחלת Graves ואופתלמופתיה (WH-FAM), וכן נבדקים בריאים ללא כל מפגעי תירואיד (NOR). קו ה-cut-off של יצרן הערכה הוא 140% ומסומן כקו מקוטע. | ||
| − | + | גישה מתודולוגית אחרת פורסמה על ידי Pierce וחב' ממעבדות Arup והמכון האנדוקריני באוניברסיטת יוטה, בכתב העת Clin Exp Immunol בשנת 2012. בשיטה זו הידועה כ-GNAS נמדדות רמות TSI גם כן תוך ניצול הגברת יצירת cAMP על ידי TSI, ושימוש בתאי CHO או Chinese hamster ovary. בשיטה זו ניתן היה להגיע לרגישות של 93%, ולספציפיות של 99%, ולסך יעילות של 98%, בהשוואה של דגימות נסיוב של חולי Graves לאלה מאנשים בריאים. | |
| − | גישה מתודולוגית אחרת פורסמה על ידי Pierce וחב' ממעבדות Arup והמכון האנדוקריני באוניברסיטת יוטה, בכתב העת Clin Exp Immunol בשנת 2012. בשיטה זו הידועה כ-GNAS נמדדות רמות TSI גם כן תוך ניצול הגברת יצירת cAMP על ידי TSI, ושימוש | ||
באוקטובר 2015 הודיעה חברת Siemens על השקת הערכה הראשונה המאפשרת מדידה אוטומטית וכמותית את רמת TSI לצורך אבחון מבדיל של מחלת Graves הפוגעת ב-32 מיליון איש ברחבי העולם. הבדיקה זמינה במכשור של מערכות immunoassay כגון IMMULITE 2000 ו-IMMULITE 2000 XPi. שלא כמו במבדקי TRAb או TSH receptor antibody המגלים נוגדנים מגרים אך גם חוסמים, ב-Siemens TSI assay מגלים רק את הנוגדנים המגרים (stimulating) שהם הגורם הקובע במחלת Graves. כך הופכת שיטת Siemens למדויקת מאוד באבחון Graves עם רגישות של 98.3% וספציפיות של 99.7%. | באוקטובר 2015 הודיעה חברת Siemens על השקת הערכה הראשונה המאפשרת מדידה אוטומטית וכמותית את רמת TSI לצורך אבחון מבדיל של מחלת Graves הפוגעת ב-32 מיליון איש ברחבי העולם. הבדיקה זמינה במכשור של מערכות immunoassay כגון IMMULITE 2000 ו-IMMULITE 2000 XPi. שלא כמו במבדקי TRAb או TSH receptor antibody המגלים נוגדנים מגרים אך גם חוסמים, ב-Siemens TSI assay מגלים רק את הנוגדנים המגרים (stimulating) שהם הגורם הקובע במחלת Graves. כך הופכת שיטת Siemens למדויקת מאוד באבחון Graves עם רגישות של 98.3% וספציפיות של 99.7%. | ||
גרסה אחרונה מ־08:40, 14 בינואר 2016
| מדריך בדיקות מעבדה | |
| Thyroid stimulating immunoglobulin | |
|---|---|
| שמות אחרים | LATS (Long-Acting Thyroid Stimulator); Long-Acting Thyroid Stimulator (LATS); Thyroid Receptor Antibody; Thyroid Stimulating Antibody (TSAb); TSH Receptor Binding Inhibitory Immunoglobulin; TSH receptor stimulating antibody; TSI (Thyroid-Stimulating Immunoglobulin); Thyretain; Autoimmune thyroid stimulator. |
| מעבדה | אנדוקרינולוגיה בדם |
| תחום | הערכת תפקוד בלוטת התריס בהקשר של מחלות אוטו-אימוניות של בלוטה זו. |
| טווח ערכים תקין | ערכי הנורמה של TSI ניתנים באחוזים והם מתאימים לכל הגילים: ערכים שהם פחות מ130-140%- מערכי הנורמה נחשבים תקינים (על פי Normal Hormone Reference Ranges. Greenspan's Basic & Clinical Endocrinology. 9th ed. the McGraw-Hill Companies; 2011 ). |
| יוצר הערך | פרופ' בן-עמי סלע |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – בלוטת התריס
מטרת הבדיקה
קביעת רמת TSI נחשבת בדיקת קו-שני בהערכת מחלות אוטו-אימוניות של התירואיד, כולל:
- אבחון מבדיל של האטיולוגיה של thyrotoxicosis במטופלים עם תסמינים קליניים השנויים במחלוקת, על מנת להימנע לדוגמה מסריקות רדיו-איזטופיות של הבלוטה בנשים הרות או מיניקות;
- אבחון של מחלת Graves הנחשדת קלינית (התבטאות חוץ-תירואידית של מחלת Graves, אקסופתלמיה אנדוקרינית, pretibial myxedema וכן thyroid acropachy) אך עם תפקודים תקינים של הבלוטה;
- קביעת הסיכון להיפרתירואידיזם או ל-thyrotoxicosis של העובר במקרה של היריון של אישה עם מחלת Graves פעילה או כזו שהייתה בעבר;
- אבחון מבדיל של thyrotoxicosis בהיריון, לעומת תסמינים של הטרימסטר הראשון או ביטוי של מחלת Graves חוזרת;
- הערכה של הסיכון של relapse של מחלת Graves לאחר טיפולים בתכשירים אנטי-תירואידיים;
- קביעה של דרגת המחלה;
- הבדיקה יכולה להידרש כאשר מוצאים לנבדק רמות בלתי-נורמאליות של TSH או של T4 או תסמינים הנובעים מרמות גבוהות או נמוכות הורמוני הבלוטה, או בנוכחות של toxic multinodular goiter;
- בדיקת רמת TSI יכולה להתבקש גם עבור מטופלים עם Graves' hyperthyroidism תת-קלינית, או במקרים של מטופלים עם unilateral ophthalmopathy;
- מטופלים המועמדים לטיפול עם תכשירים אנטי-תירואידאליים עלולים לא להגיב לטיפול זה אם רמת TSI בדם גבוהה משמעותית. לכן חיוני במקרים אלה למדוד את רמת TSI.
נוגדנים עצמיים במפגעי תירואיד
מחלה אוטו-אימונית של התירואיד, כולל מחלות Hashimoto ו-Graves, מתאפיינת על ידי הסננה של לימפוציטים, וניסויים בחיות הצביעו על לימפוציטים מסוג B, בבלוטה כמקור העיקרי של הנוגדנים האנטי-תירואידיים, שהם נוגדנים כנגד thyroid peroxidase {כ}}(anti TPO Abs), נוגדנים כנגד תירוגלובולין (anti thyroglobulin Abs או TgAb), ונוגדנים המכוונים כנגד הקולטן של TSH הידועים כ-anti TSH receptor Abs או TRAb. יצוין ש-TPOAb ו-TgAb הם נוגדנים רב-שבטיים (polyclonal) מסוג IgG, בעלי תכונות ציטוטוקסיות ויכולת לקבע משלים, לא ברור עדיין תפקידם במחלת השימוטו, ונראה שהם מופיעים בתגובה לנזק הנגרם לבלוטת התירואיד במחלה זו.
הנוגדנים מסוג TRAb מתחלקים ל-3 סוגים ביחס לתפקוד הבלוטה: מגרים (stimulating), חוסמים (blocking) וניטראליים. הנוגדנים המגרים הם אוליגו-קלונאליים מסוג IgG1. הם נקשרים לקולטני TSH ומשפעלים את האיתות המועבר דרכם. הם מסוגלים להשרות את שגשוג הבלוטה, כמו גם את ייצור הורמוני הבלוטה T3 ו-T4, והפרשתם. נתון זה מצביע על נוגדנים אלה כעל הגורמים העיקריים למחלת Graves. ההשערה כיום היא שמחלות Graves ו-Hashimoto קרובות זו לזו. במחלת Graves יצירת הזפק (goiter) נובעת מגירוי הקולטן ל-TSH, בעוד שבמחלת Hashimoto הוא נוצר מהסננה לימפוציטארית הגורמת להרס תאים פוליקולאריים.
בדיקות המעבדה שהן לעזר רב באבחון וניטור מטופלים עם מחלת Graves כוללות רמות הורמוני הבלוטה החופשיים T4 ו-T3, רמת TSH ורמת TSI. רמה מוגברת של TSI תתקבל ברוב המאובחנים עם מחלת Graves (83.4%), וניתן למצוא רמות מוגברות גם בקבוצה קטנה של מטופלים עם toxic multinodular goiter (15.9%).
נוגדנים כנגד TSHR מכילים שני סוגים של נוגדנים עצמיים הנקשרים לקולטנים אליהם נקשר באופן נורמאלי ההורמון TSH: הנוגדנים מסוג TSI בהיקשרם לקולטנים אלה מעודדים את יצירת הורמוני הבלוטה, ומובילים להיפר-תירואידיזם. לעומתם, הנוגדנים הידועים כ-thyroid binding inhibitory immunoglobulin או TBII, חוסמים את קישור TSH לקולטניו, חוסמים את יצירת הורמוני הבלוטה וגורמים להיפו-תירואידיזם. בשגרת המעבדה אין מודדים באופן רוטיני את רמת TBII, בעוד שמדידת TSI משמשת לעתים קרובות לסייע באבחון מחלת Graves. מצבים הכרוכים ברמות מוגברות של TBII כוללים את מחלת Graves (בלמעלה מ-90% מהחולים הבלתי מטופלים), ומחלת Hashimoto (ב-15% מהמקרים). במבחן של TSI מודדים את כושרו של IgG להיקשר לקולטני TSH על פני תאים, ולעודד יצירה של האנזים adenylate cyclase. על פי Macchia וחב' ב-Autoimmunity משנת 1989, ו-Takasu וחב' ב- J Endocrinol Invest משנת 1997 ניתן למצוא רמה מוגברת של TSI ב-77.8-92.0% מהמטופלים עם Graves. בשגרה הקלינית לא נדרשת בדיקת TSI לאבחון של מחלת Graves, אך ניתן להשתמש בבדיקה זו לניבוי של relapse או של remission לאחר טיפול במחלה עם יוד רדיואקטיבי או עם methimazole (על פי Chiovato וחב' ב-J Clin Endocrinol Metabol משנת 1998), שכן עליה עיקשת ברמת TSI תואמת את פעילות המחלה, ורמיסיה באופן נורמאלי מלווה על ידי ירידה ברמת TSI.
משמעותן של תוצאות מוגברות במדידת TSI
תוצאה מוגברת של TSI יכולה להעיד באופן מובהק על נוכחות מחלת Graves, אך באופן לא שכיח על Hashimoto toxicosis בה יש פעילות מוגברת של התירואיד הנגרמת מדלקת הקשורה ל-Hashimoto’s thyroiditis (הידוע גם כ-chronic thyroiditis), המתבטאת בבלוטת תריס נפוחה עם פעילות מופחתת (hypothyroidism) של הבלוטה לעתים. רמות גבוהות של TSI נמצא בתרחיש של neonatal thyrotoxicosis כאשר לוולד יש רמה גבוהה של הורמוני תירואיד בלידה בגלל מפגע של התירואיד באם, אם כי מצב זה חולף בתינוק לאחר טיפול. רמות לא תקינות של TSI נמצא ב- toxic multinodular goiter, בו מוצאים בבלוטה התפוחה nodules המייצרים רמה מוגברת של הורמוני התירואיד.
היבטים קליניים
מחלת Graves היא המפגע השכיח ביותר הגורם ל-hyperthyroidism, והוא מאופיין על ידי נוכחות של TSI שניתן למצאם בכמעט 90% מהמקרים. TSI מחקה את הפעילות של TSH, והוא גורם ליצירה מוגברת של הורמוני הבלוטה. כאשר לא ניתן טיפול, מחלת Graves עלולה לגרום להפלות, למומי לידה, למחלות עיניים ובעיקר לבלט-עין (אקסופתלמוס), ואף לגרום לסכנת חיים. לנשים יש סיכון גדול פי- 10-20 ללקות במחלה זו, מאשר לגברים. כל צורות ה-autoimmune thyrotoxicosis (כגון מחלת Graves, השימוטו טוקסיקוזיס ו- neonatal thyrotoxicosis), יכולות להיגרם על ידי יצירה של נוגדנים עצמיים המגיבים עם הקולטן של TSH. התפקיד של נוגדנים עצמיים כנגד thyroid peroxidase או כנגד תירוגלובולין, במצבים של autoimmune thyrotoxicosis או ב- autoimmune hypothyroidismפחות ברור, והם יכולים לייצג רק epiphenomena. ריכוזים ניתנים לגילוי של נוגדנים כנגד TPO מוצאים ברוב המטופלים עם מחלות אוטו-אימוניות של התירואיד כמו Hashimoto's thyroiditis, מחלת Graves או idiopathic myxedema.
נוגדנים עצמיים שיכולים להיקשר ולשפעל את ה-TSHR, יכולים להביא לגירוי בלוטת התריס באופן שהוא בלתי-תלוי ב-feedback הנורמאלי הנובע מגירי קולטנים אלה על ידי TSH. נוגדן עצמי כגון TSI המגיב עם TSHR ידוע גם בשל פעילותו ארוכת הטווח וככן מכונה גם LATS או Long-Acting Thyroid Stimulator. לאחדים מהמטופלים עם מחלת Graves, יש גם TSHR-blocking antibodies, והאיזון בין TSI לבין TSHR-blocking antibodies, קובעים את חומרת מחלת Graves. לפחות ב- 20% מאלה עם היפו-תירואידיזם אוטו-אימוני, יש עדות לנוכחות TSHR-blocking antibodies או באופן פחות שכיח גם TSI.
נוגדנים עצמים המגיבים עם TSHR ניתן למצוא עוד לפני שתסמיני תירו-טוקסיקוזיס אוטו-אימונית באים לביטוי קליני וביוכימי. כיוון שאף לא אחד מהטיפולים של מחלת Graves מכוונים כנגד תהליך המחלה, אלא נועד לפגוע בבלוטה או לחסום את סינתזת הורמוני הבלוטה, ניתן למצוא עדיין TSI גם לאחר הריפוי הנראה לעין.TSI הם נוגדנים מסוג IgG ולכן יכולים לעבור את מחסום השליה ולגרום לעובר thyrotoxicosis (על פי Jevalikar וחב' בJ Pediatr Endocrinol Metab משנת 2014, ו-Chen ו-Yu ב- Clin Endocrinol (Oxf) משנת 2011, וכן Thangaratinam וחב' ב-BMJ משנת 2011). מדידת TSHR-Ab מגלה את רמת TSI כמו גם את רמת נוגדנים העצמיים שהם TSHR-blocking.
הרגישות והספציפיות של רמה מוגברת של נוגדני TSI באבחון מחלת Graves תלויים באם הנבדק הוא בעיצומו של מהלך פעיל של המחלה, או שהוא אינו מטופל, או באם הוא מטופל בתכשירים אנטי-תירואידאליים. אם משתמשים במאובחנים חדשים ולא מטופלים במדד של רמת TSI הגבוה פי 1.3 מהנורמה, הרגישות והספציפיות של מבדק זה עולים על 90%.
תרחיש משמעותי של neonatal thyrotoxicosis ייתכן באישה בהיריון עם היסטוריה של מחלת Graves ותוצאת TSI הגבוהה בלמעלה מ-290% מעל הנורמה בשליש ההיריון האחרון, בלי כל קשר לסטאטוס הרמיסיה שלה. תוצאות TSI פחות מוגברות, עלולות להיות כרוכות רק לעתים מזומנות עם neonatal thyrotoxicosis. נתונים אלה רלוונטיים עבור נשים שעברו בעבר טיפול לאבלציה של הבלוטה, או עבור נשים המטופלות באופן פעיל עם תכשירים אנטי-תירואידאליים, ואינן בעלות תסמינים ביוכימיים או קליניים של thyrotoxicosis.
תירו-טוקסיקוזיס בהיריון, הנובע משילוב של פעילות צולבת של human chorionic gonadotropin עם TSHR ושינויים חולפים בפעילות הורמוני הבלוטה, ואינו כרוך בעלייה ברמת TSI. נוכחות של רמה מוגברת של TSI בתרחיש זה מצביע על מחלת Graves. כמו כן, רמה מוגברת של TSI בסיום של מחזור טיפולים בתכשירים אנטי-תירואידאליים מצביע בסבירות גבוהה של הׅשנׅוּת מחלת Graves. יחד עם זאת, תוצאה נורמאלית של TSI אינה מעידה בהכרח על רמיסיה ממושכת. במטופלים בהם תוצאות המבחנים של בלוטת התריס נעות לסירוגין בין היפו- והיפר-תירואידיזם, רמות מוגברות של נוגדני TSHR במקביל לרמות תקינות או מוגברות באופן קל של TSI, מרמזות על אבחון אפשרי של Hashimoto toxicosis. יצוין כמו כן שאם כי תוצאות מוגברות של TSI מהוות אינדיקציה חזקה למחלת Graves, אין הן תואמות תמיד מצב של היפר-תירואידיזם או את חומרתו. במטופלים עם מחלת השימוטו ניתן למצוא רמות TSI מוגברות, שיכולות להגיע עד 1.8 מהנורמה. רמות TSI שבין 1.3-1.8 מהנורמה, נצפות לעתים המספר מפגעים אחרים של הבלוטה, כולל nodular goiter ו- subacute thyroiditis (על פי Saravanan ו-Dayan ב- Endocrinol Metab Clin North Amמשנת 2001).
הוראות לביצוע הבדיקה
אין צורך בהכנה מוקדמת כגון צום. הדם נלקח במבחנה כימית (פקק אדום) או במבחנת ג'ל, ויש לשלחו למעבדה בקירור. יש לפסול דגימות שהגיעו למעבדה לא מקוררות. לאחר הסרכוז והפרדת הנסיוב מהתאים, ניתן לשמור את הנסיוב בטמפרטורת החדר ל-24 שעות, בקירור למשך 14 יום, או בהקפאה למשך 90 יום. יש לפסול דגימות מאוד המוליטיות, ליפמיות או איקטריות, אך ניתן לקבל דגיות עם המולידה, ליפמיה או איקטריה מתונה.
גישות מתודולוגיות למדידת רמת TSI
הסקירה של Morris וחב' ב-Mayo Clin Proc משנת 1988 ייחדה דיון מקיף להשוואה בין שיטות להערכת קישור נוגדנים עצמיים לקולטן של TSH. בין השאר הושוו שיטות radio-receptor ושיטות bioassay, זאת בעידן בו הרבו להשתמש ב- quantitative recombinant bioassayאו ב- quantitative chemiluminescent immunoassay. בשנים האחרונות הוכנסו שיטות משופרות למדידת רמת TSI : Lahooti וחב' פרסמו בשנת 2014 ב-Austin J Clin Ophthalmol שיטה הידועה כ-Thyretain TSI reporter cAMP luciferase bioassay, שפורסמה לראשונה על ידי Lytton וחב' בשנת 2010 ב-Clin Exp Immunol. עיקרון השיטה מבוסס על כך ש-TSI עשוי גם לעודד יצירת cAMP , וניתן אם כך ב-bioassay למדוד יכולת זו בשורת-תאים (cell line) המבטאת את הקולטן ל-TSH. לשיטת luciferase יש רגישות אמליטית של 75% אך יש בה מגבלה בכך שתוצאות false negative עלולות להתקבל בנוכחות נוגדנים חוסמי TSH.
רמות TSI הנבדקים עם Graves hyperthyroidism ללא אופתלמופתיה (GH), עם אופתלמופתיה (GO), עם euthyroid Graves disease (EGD), נבדקים עם תפקוד תירואיד תקין שהם בני-משפחה בודדת עם שכיחות גבוהה של מחלת Graves ואופתלמופתיה (WH-FAM), וכן נבדקים בריאים ללא כל מפגעי תירואיד (NOR). קו ה-cut-off של יצרן הערכה הוא 140% ומסומן כקו מקוטע.
גישה מתודולוגית אחרת פורסמה על ידי Pierce וחב' ממעבדות Arup והמכון האנדוקריני באוניברסיטת יוטה, בכתב העת Clin Exp Immunol בשנת 2012. בשיטה זו הידועה כ-GNAS נמדדות רמות TSI גם כן תוך ניצול הגברת יצירת cAMP על ידי TSI, ושימוש בתאי CHO או Chinese hamster ovary. בשיטה זו ניתן היה להגיע לרגישות של 93%, ולספציפיות של 99%, ולסך יעילות של 98%, בהשוואה של דגימות נסיוב של חולי Graves לאלה מאנשים בריאים.
באוקטובר 2015 הודיעה חברת Siemens על השקת הערכה הראשונה המאפשרת מדידה אוטומטית וכמותית את רמת TSI לצורך אבחון מבדיל של מחלת Graves הפוגעת ב-32 מיליון איש ברחבי העולם. הבדיקה זמינה במכשור של מערכות immunoassay כגון IMMULITE 2000 ו-IMMULITE 2000 XPi. שלא כמו במבדקי TRAb או TSH receptor antibody המגלים נוגדנים מגרים אך גם חוסמים, ב-Siemens TSI assay מגלים רק את הנוגדנים המגרים (stimulating) שהם הגורם הקובע במחלת Graves. כך הופכת שיטת Siemens למדויקת מאוד באבחון Graves עם רגישות של 98.3% וספציפיות של 99.7%.
ראו גם


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק