הבדלים בין גרסאות בדף "תסמונת המעי הקצר - טיפול ארוך טווח בטדוגלוטיד - Short bowel syndrome - long term treatment with Teduglutide"
| (30 גרסאות ביניים של 2 משתמשים אינן מוצגות) | |||
| שורה 1: | שורה 1: | ||
| − | |||
| − | |||
| − | |||
{{מחלה | {{מחלה | ||
|תמונה= | |תמונה= | ||
| שורה 16: | שורה 13: | ||
}} | }} | ||
{{הרחבה|תסמונת המעי הקצר}} | {{הרחבה|תסמונת המעי הקצר}} | ||
| − | '''תסמונת המעי הקצר (SBS,{{כ}} Short Bowel Syndrome)''' היא תסמונת של [[תת-ספיגה כירורגית - Surgical malabsorption|תת ספיגה]], הנובעת מכריתה נרחבת של המעי הדק. מדובר לרוב במטופלים הסובלים ממחלות כרוניות של המעי, כדוגמת [[מחלת קרוהן - Crohn's disease|מחלת קרוהן]] (Crohn's disease), | + | '''תסמונת המעי הקצר (SBS,{{כ}} Short Bowel Syndrome)''' היא תסמונת של [[תת-ספיגה כירורגית - Surgical malabsorption|תת ספיגה]], הנובעת מכריתה נרחבת של המעי הדק. מדובר לרוב במטופלים הסובלים ממחלות כרוניות של המעי, כדוגמת [[מחלת קרוהן - Crohn's disease|מחלת קרוהן]] (Crohn's disease), אירועים מזנטרים (Mesenteric Ischemia) הגורמים לצורך בניתוחי כריתה חוזרים. התסמונת כרוכה באחוזי תמותה ותחלואה גבוהים. |
כשל תפקודי של המעי (SBS-IF{{כ}}, Short Bowel Syndrome associated Intestinal Failure) מופיע כאשר נותרו פחות מ-200 סנטימטרים (ס"מ) של מעי דק. | כשל תפקודי של המעי (SBS-IF{{כ}}, Short Bowel Syndrome associated Intestinal Failure) מופיע כאשר נותרו פחות מ-200 סנטימטרים (ס"מ) של מעי דק. | ||
| − | עקב אובדן שטח ספיגה במעי, המחלה מתבטאת בכישלון ספיגה של רכיבים חיוניים: הפרעה בספיגת [[הפרעה בשומני הדם|שומנים]], ויטמינים מסיסים בשומן, חוסר במינרלים, תופעות לוואי כגון [[שלשול]], צואה שומנית, [[ירידה במשקל|אובדן משקל]] והפרעות במאזן נוזלים ואלקטרוליטים, המובילים למצב של [[תת תזונה]] והמחייבים תלות בתמיכה תוך ורידית הכוללת הזנה תוך ורידית (TPN{{כ}}, Total Parenteral Nutrition) ונוזלים. | + | עקב אובדן שטח ספיגה במעי, המחלה מתבטאת בכישלון ספיגה של רכיבים חיוניים: הפרעה בספיגת [[הפרעה בשומני הדם|שומנים]], [[בדיקות ויטמינים|ויטמינים]] מסיסים בשומן, חוסר במינרלים, תופעות לוואי כגון [[שלשול]], צואה שומנית, [[ירידה במשקל|אובדן משקל]] והפרעות במאזן נוזלים ואלקטרוליטים, המובילים למצב של [[תת תזונה]] והמחייבים תלות בתמיכה תוך ורידית הכוללת הזנה תוך ורידית (TPN{{כ}}, Total Parenteral Nutrition) ונוזלים. |
| − | |||
| − | חולים המטופלים ב-TPN באופן קבוע סובלים מסיבוכים רבים: | + | ;חולים המטופלים ב-TPN באופן קבוע סובלים מסיבוכים רבים: |
| − | '''סיבוכים הקשורים | + | '''סיבוכים הקשורים בצנתר התוך ורידי''' - זיהום, [[פקקת ורידים|קריש]] באזור ההכנסה ותעלת הצנתר וסיכון להופעת חזה אוויר (Pneumothorax). |
| − | '''סיבוכים מטבוליים''' - הפרעות ברמות גלוקוז בדם, פגיעה כבדית עד לצורך ב[[השתלות כבד - Liver transplantation|השתלת כבד]]-מעי במקרי קיצון, הדרדרות נוספת של מצב המעי ומחלות עצם. | + | '''סיבוכים מטבוליים''' - הפרעות ברמות [[גלוקוז]] בדם, [[מחלות כבד|פגיעה כבדית]] עד לצורך ב[[השתלות כבד - Liver transplantation|השתלת כבד]]-מעי במקרי קיצון, הדרדרות נוספת של מצב המעי ומחלות עצם. |
| + | ==טדוגלוטיד, Teduglutide {{כ}} (Gattex)== | ||
| − | + | [[t:Teduglutide|Teduglutide]] היא תרופה יתומה (היחידה הקיימת) לטיפול במצב של אי ספיקת המעי על רקע תסמונת המעי הקצר, המהווה פריצת דרך בטיפול הרפואי במחלה חשוכת מרפא ורבת סבל זו. מדובר בפרדיגמה (Paradigm) טיפולית חדשה וייחודית, לראשונה מזה 40 שנה, במחלה בה הטיפול הקיים עד היום הוא תמיכתי בלבד: נוזלים, סותרי חומצה, [[אנטיביוטיקה]] ואנלוגים של [[סומטוסטטין - Somatostatin|סומטוסטסין]] (Somatostatin analogues). | |
| − | |||
| − | Teduglutide הוא אנלוג רקומביננטי (שעבר תהליף של שחלוף) של החלבון 2-Glucagon Like Peptide-2) GLP), המופרש מתאי L של המעי לאחר תחילת תהליך העיכול ונמצא בעיקר במעי הדק. האנלוג נבדל מן החלבון המקורי בחומצה אמינית אחת | + | Teduglutide הוא אנלוג רקומביננטי (Recombinant analog, שעבר תהליף של שחלוף) של החלבון 2-Glucagon Like Peptide-2) GLP), המופרש מתאי L של המעי לאחר תחילת תהליך העיכול ונמצא בעיקר במעי הדק. האנלוג נבדל מן החלבון המקורי בחומצה אמינית אחת [החלפת גליצין (Glycine) באלנין (Alanine)]. שינוי זה גורם להארכת זמן מחצית החיים של החלבון מ-7 דקות לשעתיים. חלבון זה גורם להגדלת שטח ספיגת רירית המעי וכתוצאה מכך מגביר ספיגת חומרי הזנה ונוזלים, ממריץ זרימת דם במעי משפר את תפקוד המסתם האילאוצקלי (Ileocecal valve). |
'''צורת מתן:''' תת עורית, פעם ביום במינון של 0.05 מיליגרם (מ"ג) לקילוגרם (ק"ג) באופן כרוני. | '''צורת מתן:''' תת עורית, פעם ביום במינון של 0.05 מיליגרם (מ"ג) לקילוגרם (ק"ג) באופן כרוני. | ||
| שורה 46: | שורה 42: | ||
התרופה נרשמה לשימוש באיחוד האירופי מאוגוסט 2012, תחת השם Revestive, וזמינה מסחרית מספטמבר 2014. | התרופה נרשמה לשימוש באיחוד האירופי מאוגוסט 2012, תחת השם Revestive, וזמינה מסחרית מספטמבר 2014. | ||
| − | + | בארצות הברית (ארה"ב), שם התרופה Gattex, רשומה לשימוש מדצמבר 2012, וזמינה מסחרית מאז פברואר 2013. | |
בישראל, התרופה רשומה בשם Gattex. מאוגוסט 2014 זמינה לרכישה פרטית. | בישראל, התרופה רשומה בשם Gattex. מאוגוסט 2014 זמינה לרכישה פרטית. | ||
| − | |||
מספר מטופלים: בארה"ב יש כ-500 מטופלי Gattex, בגרמניה 33. בישראל ישנו ניסיון טיפולי בחמישה מטופלים. | מספר מטופלים: בארה"ב יש כ-500 מטופלי Gattex, בגרמניה 33. בישראל ישנו ניסיון טיפולי בחמישה מטופלים. | ||
| שורה 55: | שורה 50: | ||
==מחקרים== | ==מחקרים== | ||
| − | '''תוצאות המחקרים הקליניים שבוצעו | + | '''תוצאות המחקרים הקליניים שבוצעו ב- Teduglutide ברחבי העולם:''' |
| − | במחקר הראשון, STEPS{{כ}} (Study of Teduglutide Effectiveness in Parenteral nutrition-dependent Short-bowel syndrome subjects), שהיה פרוספקטיבי, כפול | + | במחקר הראשון, STEPS{{כ}} (Study of Teduglutide Effectiveness in Parenteral nutrition-dependent Short-bowel syndrome subjects), שהיה פרוספקטיבי (Prospective), כפול סמיות (Double blind) ומושווה פלצבו (Placebo) נכללו 86 מטופלים. תקופת המעקב הייתה 24 שבועות, כאשר נקודת הסיום המיועדת (ה-Primary end point), הייתה הפחתה בנפח התמיכה התוך ורידית של 100-20 אחוזים. בתום תקופת המעקב נמצא כי 63 אחוזים מקבוצת ה-Teduglutide הגיעו לנקודת הסיום לעומת 30 אחוזים בלבד בקבוצת הפלצבו. |
מחקר ההמשך היה 2 STEPS, שהיה מחקר פתוח. כאשר משך המעקב היה 24 חודשים. | מחקר ההמשך היה 2 STEPS, שהיה מחקר פתוח. כאשר משך המעקב היה 24 חודשים. | ||
| − | תכנון שני המחקרים, 1 STEPS ו־2 STEPS מתואר בתרשים מספר 1. סך הכל נכללו 88 מטופלים, כאשר 65 מתוכם סיימו את תקופת המעקב. 93 | + | תכנון שני המחקרים, 1 STEPS ו־2 STEPS מתואר בתרשים מספר 1. סך הכל נכללו 88 מטופלים, כאשר 65 מתוכם סיימו את תקופת המעקב. 93 אחוזים מהמטופלים בקבוצת ה-Teduglutide (מהמחקר הראשון) ושטופלו סך הכל במשך שנתיים וחצי הגיעו לנקודת הסיום המיועדת לעומת 55 אחוזים בקבוצה שטופלה ב-Teduglutide בשנתיים בלבד. 38 מתוך 65 מטופלים השיגו הפחתת יום אחד בשבוע לפחות של תמיכה תוך ורידית (PS{{כ}}, Parenteral Support){{כ}}, 25 מתוך 65 מטופלים השיגו הפחתת שלושה ימים ויותר בשבוע של PS ואילו 13 מטופלים נגמלו לחלוטין מצורך בתמיכה זו. |
| שורה 68: | שורה 63: | ||
| − | תיאור גרפי של תוצאות המחקר מוצגים בגרף מספר 1. יש לציין כי גמילה מ-PS הושגה לאחר 24 | + | תיאור גרפי של תוצאות המחקר מוצגים בגרף מספר 1. יש לציין כי גמילה מ-PS הושגה לאחר 117-24 שבועות של טיפול ב-Teduglutide. |
| שורה 76: | שורה 71: | ||
המחקר הבא שבוצע הוא 3 STEPS, מחקר פתוח גם הוא, ולמעשה המשיכו מעקב לשנה נוספת, כאשר מטרת המחקר הייתה לבדוק תגובה ארוכת | המחקר הבא שבוצע הוא 3 STEPS, מחקר פתוח גם הוא, ולמעשה המשיכו מעקב לשנה נוספת, כאשר מטרת המחקר הייתה לבדוק תגובה ארוכת | ||
| − | טווח לטיפול ב- | + | טווח לטיפול ב-Teduglutide. נכללו במחקר 14 מטופלים, כאשר 13 מתוכם השלימו את תקופת המעקב. סך כל תקופת המעקב בשלושת המחקרים הייתה 42 חודשים. |
| − | 6 | + | 6 מתוך 14 מטופלים השיגו הפחתה של 3 ימים ומעלה בתמיכה התוך ורידית ואילו 2 מטופלים נוספים נגמלו לחלוטין מהצורך ב-PS. סיכום הנתונים מוצג בתרשים מספר 2. |
| שורה 85: | שורה 80: | ||
;סיכום המחקרים הקליניים שבוצעו במחקרי ה-STEPS | ;סיכום המחקרים הקליניים שבוצעו במחקרי ה-STEPS | ||
| − | במעקב של 42 חודשים, 16 | + | במעקב של 42 חודשים, 16 מתוך 134 מטופלים נגמלו לחלוטין מהצורך ב-PS, כאשר היה צורך בטיפול של 130-12 שבועות עד לגמילה מלאה. |
| − | == | + | ==תוצאות הטיפול התרופתי בפרקטיקה הקלינית== |
| − | + | בכנס הגסטרואנטרולוגי האירופאי בשנת 2014 פורסם פוסטר על הניסיון בקליבלנד, פלורידה במעקב של 6 מטופלים. טווח גילאי המטופלים היה 71-26 שנים, לשלושה מתוכם היה מעי גס, ואורך המעי הדק הנותר היה בין 120-30 ס"מ. במשך טיפול של 15-4 חודשים ב-Teduglutide,{{כ}} 4 מתוך 6 מטופלים נגמלו לחלוטין מ-PS כאשר בשני האחרים נצפתה ירידה של לפחות 20 אחוזים בנפח ה-PS שהיו זקוקים לו, דהיינו לפחות יום אחד בשבוע ללא צורך בתמיכה תוך ורידית. | |
==נתוני בטיחות התרופה== | ==נתוני בטיחות התרופה== | ||
| − | שלוש תופעות הלוואי העיקריות שנצפו היו תופעות גסטרואינטסטינליות הכוללות: [[כאב בטן|כאבי בטן]], [[בחילות]] ותפיחות בטנית. נצפה מקרה אחד של [[דלקת חדה של כיס המרה - Acute cholecystitis|דלקת בכיס המרה]] ומקרה אחר של היצרות במעי הדק. שניהם טופלו ללא סיבוכים וחלפו. עיקר החשש מהתרופה היה קשור לעובדה שהיא בעלת אפקט טרופי (השפעה הגורמת לגדילה וריבוי של תאי המעי), היא עלולה לגרום לעלייה בשכיחות [[גידול|גידולים]], בעיקר ממקור דרכי העיכול. נצפו שני מקרים בלבד של ממאירויות: האחד, [[סרטן המעי הגס והחלחולת - Colorectal cancer|אדנוקרצינומה גרורתית]] שייתכן שהוא קשור לתרופה והשני [[ | + | שלוש תופעות הלוואי העיקריות שנצפו היו תופעות גסטרואינטסטינליות הכוללות: [[כאב בטן|כאבי בטן]], [[בחילות]] ותפיחות בטנית. נצפה מקרה אחד של [[דלקת חדה של כיס המרה - Acute cholecystitis|דלקת בכיס המרה]] ומקרה אחר של היצרות במעי הדק. שניהם טופלו ללא סיבוכים וחלפו. עיקר החשש מהתרופה היה קשור לעובדה שהיא בעלת אפקט טרופי (Trophic effect, השפעה הגורמת לגדילה וריבוי של תאי המעי), ולכן היא עלולה לגרום לעלייה בשכיחות [[גידול|גידולים]], בעיקר ממקור דרכי העיכול. נצפו שני מקרים בלבד של ממאירויות: האחד, [[סרטן המעי הגס והחלחולת - Colorectal cancer|אדנוקרצינומה גרורתית]] (Metastatic Adenocarcinoma) שייתכן שהוא קשור לתרופה והשני [[סרטן ריאה]] במטופל [[עישון|מעשן]] שאיננו קשור לשימוש בתרופה. לא נצפו מקרים נוספים והמחשבה היא כי האפקט הגידולי של התרופה הוא מינימלי, אם בכלל. על כל פנים, ההנחיות הן לבצע קולונוסקופיה (Colonoscopy) אחת לשנה במטופל שיש לו מעי גס (שארי) וכן מעקב אנזימי כבד [[אספרטאט טרנסאמינאזה - Aspartate transaminase|{{כ}}AST]] ({{כ}}Aspartate transaminase), [[אלנין טרנסאמינאזה - Alanine transaminase|{{כ}}ALT]] ({{כ}}Alanine transaminase) ואנזימי לבלב ([[עמילאזה - Amylase|Amylase]],{{כ}} [[ליפאזה - Lipase|Lipase]]) כל מספר חודשים. |
למרות עלותה הגבוהה, השימוש בתרופה זו יכול לגרום, בסופו של דבר, להפחתה בעלות הטיפולית הגבוהה הכוללת הקשורה בנטל המחלה היסודית ותופעות הלוואי הקשורות בחיבור מתמשך להזנה תוך ורידית, כגון: אשפוזים חוזרים בעקבות זיהומים הקשורים בצנתר, [[שחמת הכבד - Liver cirrhosis|שחמת הכבד]] ופגיעה בתפקוד המעי הנותר, המובילים בסופו של דבר לצורך בהשתלת כבד ומעי דק. | למרות עלותה הגבוהה, השימוש בתרופה זו יכול לגרום, בסופו של דבר, להפחתה בעלות הטיפולית הגבוהה הכוללת הקשורה בנטל המחלה היסודית ותופעות הלוואי הקשורות בחיבור מתמשך להזנה תוך ורידית, כגון: אשפוזים חוזרים בעקבות זיהומים הקשורים בצנתר, [[שחמת הכבד - Liver cirrhosis|שחמת הכבד]] ופגיעה בתפקוד המעי הנותר, המובילים בסופו של דבר לצורך בהשתלת כבד ומעי דק. | ||
| − | |||
| − | |||
| − | {{ייחוס| | + | {{ייחוס|ד"ר אריאלה שטרית, גםטרואנטרולוגית בכירה, המערך הגסטרו-כירורגי, בית החולים שערי צדק, ירושלים}} |
[[קטגוריה: גסטרואנטרולוגיה]] | [[קטגוריה: גסטרואנטרולוגיה]] | ||
| + | [[קטגוריה: ילדים]] | ||
| + | [[קטגוריה: פנימית]] | ||
[[קטגוריה: כירורגיה]] | [[קטגוריה: כירורגיה]] | ||
| − | [[קטגוריה: | + | [[קטגוריה: תזונה]] |
| + | [[קטגוריה: פרמקולוגיה קלינית ]] | ||
גרסה אחרונה מ־11:27, 18 בינואר 2021
| תסמונת המעי הקצר- טיפול ארוך טווח בטדוגלוטיד | ||
|---|---|---|
| Short bowel syndrome - Long term treatment with Teduglutide | ||
| יוצר הערך | ד"ר אריאלה שטרית | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – תסמונת המעי הקצר
תסמונת המעי הקצר (SBS, Short Bowel Syndrome) היא תסמונת של תת ספיגה, הנובעת מכריתה נרחבת של המעי הדק. מדובר לרוב במטופלים הסובלים ממחלות כרוניות של המעי, כדוגמת מחלת קרוהן (Crohn's disease), אירועים מזנטרים (Mesenteric Ischemia) הגורמים לצורך בניתוחי כריתה חוזרים. התסמונת כרוכה באחוזי תמותה ותחלואה גבוהים.
כשל תפקודי של המעי (SBS-IF, Short Bowel Syndrome associated Intestinal Failure) מופיע כאשר נותרו פחות מ-200 סנטימטרים (ס"מ) של מעי דק.
עקב אובדן שטח ספיגה במעי, המחלה מתבטאת בכישלון ספיגה של רכיבים חיוניים: הפרעה בספיגת שומנים, ויטמינים מסיסים בשומן, חוסר במינרלים, תופעות לוואי כגון שלשול, צואה שומנית, אובדן משקל והפרעות במאזן נוזלים ואלקטרוליטים, המובילים למצב של תת תזונה והמחייבים תלות בתמיכה תוך ורידית הכוללת הזנה תוך ורידית (TPN, Total Parenteral Nutrition) ונוזלים.
- חולים המטופלים ב-TPN באופן קבוע סובלים מסיבוכים רבים
סיבוכים הקשורים בצנתר התוך ורידי - זיהום, קריש באזור ההכנסה ותעלת הצנתר וסיכון להופעת חזה אוויר (Pneumothorax).
סיבוכים מטבוליים - הפרעות ברמות גלוקוז בדם, פגיעה כבדית עד לצורך בהשתלת כבד-מעי במקרי קיצון, הדרדרות נוספת של מצב המעי ומחלות עצם.
טדוגלוטיד, Teduglutide (Gattex)
Teduglutide היא תרופה יתומה (היחידה הקיימת) לטיפול במצב של אי ספיקת המעי על רקע תסמונת המעי הקצר, המהווה פריצת דרך בטיפול הרפואי במחלה חשוכת מרפא ורבת סבל זו. מדובר בפרדיגמה (Paradigm) טיפולית חדשה וייחודית, לראשונה מזה 40 שנה, במחלה בה הטיפול הקיים עד היום הוא תמיכתי בלבד: נוזלים, סותרי חומצה, אנטיביוטיקה ואנלוגים של סומטוסטסין (Somatostatin analogues).
Teduglutide הוא אנלוג רקומביננטי (Recombinant analog, שעבר תהליף של שחלוף) של החלבון 2-Glucagon Like Peptide-2) GLP), המופרש מתאי L של המעי לאחר תחילת תהליך העיכול ונמצא בעיקר במעי הדק. האנלוג נבדל מן החלבון המקורי בחומצה אמינית אחת [החלפת גליצין (Glycine) באלנין (Alanine)]. שינוי זה גורם להארכת זמן מחצית החיים של החלבון מ-7 דקות לשעתיים. חלבון זה גורם להגדלת שטח ספיגת רירית המעי וכתוצאה מכך מגביר ספיגת חומרי הזנה ונוזלים, ממריץ זרימת דם במעי משפר את תפקוד המסתם האילאוצקלי (Ileocecal valve).
צורת מתן: תת עורית, פעם ביום במינון של 0.05 מיליגרם (מ"ג) לקילוגרם (ק"ג) באופן כרוני.
יתרונות הטיפול:
- שיפור יכולת ספיגת המעי באמצעות שיפור השלמות המבנית והתפקודית של המעי הדק הנותר
- הפחתת התלות בהזנה תוך ורידית עד לגמילה מוחלטת מ-TPN המושגת בחלק מהחולים
- הפחתה למינימום של תופעות הלוואי הנלוות להזנה תוך ורידית ולקבלת נוזלים ממושכת
רישום התרופה
התרופה נרשמה לשימוש באיחוד האירופי מאוגוסט 2012, תחת השם Revestive, וזמינה מסחרית מספטמבר 2014.
בארצות הברית (ארה"ב), שם התרופה Gattex, רשומה לשימוש מדצמבר 2012, וזמינה מסחרית מאז פברואר 2013.
בישראל, התרופה רשומה בשם Gattex. מאוגוסט 2014 זמינה לרכישה פרטית.
מספר מטופלים: בארה"ב יש כ-500 מטופלי Gattex, בגרמניה 33. בישראל ישנו ניסיון טיפולי בחמישה מטופלים.
מחקרים
תוצאות המחקרים הקליניים שבוצעו ב- Teduglutide ברחבי העולם:
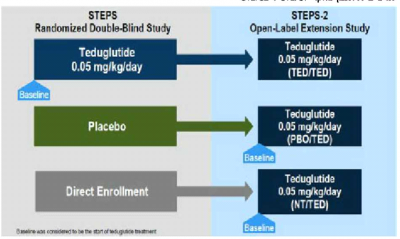
במחקר הראשון, STEPS (Study of Teduglutide Effectiveness in Parenteral nutrition-dependent Short-bowel syndrome subjects), שהיה פרוספקטיבי (Prospective), כפול סמיות (Double blind) ומושווה פלצבו (Placebo) נכללו 86 מטופלים. תקופת המעקב הייתה 24 שבועות, כאשר נקודת הסיום המיועדת (ה-Primary end point), הייתה הפחתה בנפח התמיכה התוך ורידית של 100-20 אחוזים. בתום תקופת המעקב נמצא כי 63 אחוזים מקבוצת ה-Teduglutide הגיעו לנקודת הסיום לעומת 30 אחוזים בלבד בקבוצת הפלצבו.
מחקר ההמשך היה 2 STEPS, שהיה מחקר פתוח. כאשר משך המעקב היה 24 חודשים.
תכנון שני המחקרים, 1 STEPS ו־2 STEPS מתואר בתרשים מספר 1. סך הכל נכללו 88 מטופלים, כאשר 65 מתוכם סיימו את תקופת המעקב. 93 אחוזים מהמטופלים בקבוצת ה-Teduglutide (מהמחקר הראשון) ושטופלו סך הכל במשך שנתיים וחצי הגיעו לנקודת הסיום המיועדת לעומת 55 אחוזים בקבוצה שטופלה ב-Teduglutide בשנתיים בלבד. 38 מתוך 65 מטופלים השיגו הפחתת יום אחד בשבוע לפחות של תמיכה תוך ורידית (PS, Parenteral Support), 25 מתוך 65 מטופלים השיגו הפחתת שלושה ימים ויותר בשבוע של PS ואילו 13 מטופלים נגמלו לחלוטין מצורך בתמיכה זו.
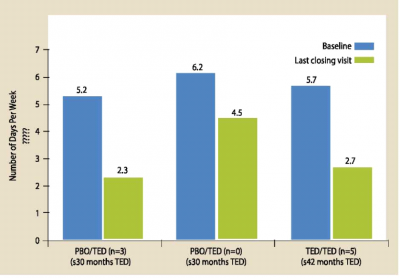
תיאור גרפי של תוצאות המחקר מוצגים בגרף מספר 1. יש לציין כי גמילה מ-PS הושגה לאחר 117-24 שבועות של טיפול ב-Teduglutide.
המחקר הבא שבוצע הוא 3 STEPS, מחקר פתוח גם הוא, ולמעשה המשיכו מעקב לשנה נוספת, כאשר מטרת המחקר הייתה לבדוק תגובה ארוכת
טווח לטיפול ב-Teduglutide. נכללו במחקר 14 מטופלים, כאשר 13 מתוכם השלימו את תקופת המעקב. סך כל תקופת המעקב בשלושת המחקרים הייתה 42 חודשים.
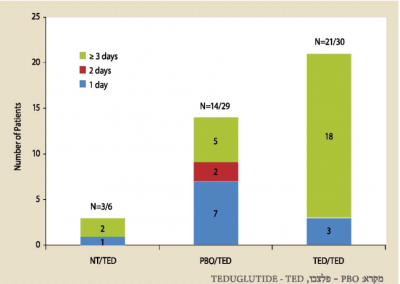
6 מתוך 14 מטופלים השיגו הפחתה של 3 ימים ומעלה בתמיכה התוך ורידית ואילו 2 מטופלים נוספים נגמלו לחלוטין מהצורך ב-PS. סיכום הנתונים מוצג בתרשים מספר 2.
- סיכום המחקרים הקליניים שבוצעו במחקרי ה-STEPS
במעקב של 42 חודשים, 16 מתוך 134 מטופלים נגמלו לחלוטין מהצורך ב-PS, כאשר היה צורך בטיפול של 130-12 שבועות עד לגמילה מלאה.
תוצאות הטיפול התרופתי בפרקטיקה הקלינית
בכנס הגסטרואנטרולוגי האירופאי בשנת 2014 פורסם פוסטר על הניסיון בקליבלנד, פלורידה במעקב של 6 מטופלים. טווח גילאי המטופלים היה 71-26 שנים, לשלושה מתוכם היה מעי גס, ואורך המעי הדק הנותר היה בין 120-30 ס"מ. במשך טיפול של 15-4 חודשים ב-Teduglutide, 4 מתוך 6 מטופלים נגמלו לחלוטין מ-PS כאשר בשני האחרים נצפתה ירידה של לפחות 20 אחוזים בנפח ה-PS שהיו זקוקים לו, דהיינו לפחות יום אחד בשבוע ללא צורך בתמיכה תוך ורידית.
נתוני בטיחות התרופה
שלוש תופעות הלוואי העיקריות שנצפו היו תופעות גסטרואינטסטינליות הכוללות: כאבי בטן, בחילות ותפיחות בטנית. נצפה מקרה אחד של דלקת בכיס המרה ומקרה אחר של היצרות במעי הדק. שניהם טופלו ללא סיבוכים וחלפו. עיקר החשש מהתרופה היה קשור לעובדה שהיא בעלת אפקט טרופי (Trophic effect, השפעה הגורמת לגדילה וריבוי של תאי המעי), ולכן היא עלולה לגרום לעלייה בשכיחות גידולים, בעיקר ממקור דרכי העיכול. נצפו שני מקרים בלבד של ממאירויות: האחד, אדנוקרצינומה גרורתית (Metastatic Adenocarcinoma) שייתכן שהוא קשור לתרופה והשני סרטן ריאה במטופל מעשן שאיננו קשור לשימוש בתרופה. לא נצפו מקרים נוספים והמחשבה היא כי האפקט הגידולי של התרופה הוא מינימלי, אם בכלל. על כל פנים, ההנחיות הן לבצע קולונוסקופיה (Colonoscopy) אחת לשנה במטופל שיש לו מעי גס (שארי) וכן מעקב אנזימי כבד AST (Aspartate transaminase), ALT (Alanine transaminase) ואנזימי לבלב (Amylase, Lipase) כל מספר חודשים.
למרות עלותה הגבוהה, השימוש בתרופה זו יכול לגרום, בסופו של דבר, להפחתה בעלות הטיפולית הגבוהה הכוללת הקשורה בנטל המחלה היסודית ותופעות הלוואי הקשורות בחיבור מתמשך להזנה תוך ורידית, כגון: אשפוזים חוזרים בעקבות זיהומים הקשורים בצנתר, שחמת הכבד ופגיעה בתפקוד המעי הנותר, המובילים בסופו של דבר לצורך בהשתלת כבד ומעי דק.
המידע שבדף זה נכתב על ידי ד"ר אריאלה שטרית, גםטרואנטרולוגית בכירה, המערך הגסטרו-כירורגי, בית החולים שערי צדק, ירושלים


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק