הבדלים בין גרסאות בדף "Cholylglycine"
(←ראו גם) |
|||
| (גרסת ביניים אחת של אותו משתמש אינה מוצגת) | |||
| שורה 44: | שורה 44: | ||
| − | {{ייחוס | + | {{ייחוס בן עמי}} |
| − | [[קטגוריה:בדיקות מעבדה - תפקודי כבד ודרכי מרה] | + | [[קטגוריה:בדיקות מעבדה - תפקודי כבד ודרכי מרה]] |
[[קטגוריה:בדיקות מעבדה: כימיה בדם]] | [[קטגוריה:בדיקות מעבדה: כימיה בדם]] | ||
גרסה אחרונה מ־07:33, 4 באוקטובר 2016
| מדריך בדיקות מעבדה | |
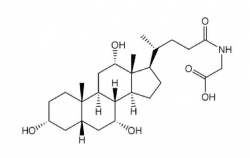
| Cholylglycine | |
|---|---|
| שמות אחרים | glycocholic acid |
| |
| מעבדה | כימיה בדם |
| תחום | הערכת חומצת מרה כאינדיקציה למחלת כבד |
| טווח ערכים תקין | בנסיוב (בצום של 8-12 שעות) פחות מ-68 מיקרוגרם/דציליטר (רמה ממוצעת של 5±23 מיקרוגרם/דציליטר). בנסיוב לאחר ארוחה (postprandial) בערך פי-3 גבוה יותר מרמת cholylglycine בצום. |
| יוצר הערך | פרופ' בן-עמי סלע |
בסיס פיזיולוגי
Cholylglycine (להלן כו"ג) היא חומצת מרה גבישית, המעורבת בתחלוּב (emulsification) של שומנים, ומופיעה כמלח נתרן בנוזל המרה ביונקים. חומר זה הוא שילוב (conjugate) של חומצה כולית עם גליצין. כו"ג מסונתז בכבד מכולסטרול ליצירת cholic acid בשלב הראשון, ואז נוצר הצימוד עם חומצת האמינו גליצין ליצירת חומצת מרה מצומדת. כו"ג הוא מרכיב עיקרי בקרב חומצות המרה, ומטבוליט חשוב של כולסטרול. רוב כו"ג נמצא בצירקולציה של הכבד כאשר רק 1% של כו"ג עובר לצירקולציה הסיסטמית, שם הוא נקשר לחלבונים. לאחר הסינתזה שלו בתאי הכבד, כו"ג מצטבר במרה, משם הוא עובר עם מיץ המרה למעי הדק עם המזון המעוכל, ומסייע לספיגת שומנים מהמזון. כאשר תאי כבד ניזוקים, הם אינם מסוגלים לספוג בצורה יעילה כו"ג על ידי הצירקולציה האנטרו-הפאטית, ואז גם רמות כו"ג בנסיוב עולות.
בשנת 1948 היו אלה Sherlock ו-Walshe במאמרם ב-Clin Sci הראשונים שדווחו על רמות מוגברות של חומצות מרה בנסיוב של נבדקים עם מחלות הפאטו-ביליאריות, ומאז היו דיווחים רבים על מפגעים עם עלייה ברמת חומצות מרה. מחקר שהתפרסם ב-Korean J Pathol משנת 1982, נמדדו בשיטת RIA רמות של כו"ג בדגימות נסיוב של 25 אנשים בריאים ושל 98 מטופלים עם תפקודי כבד לא תקינים. התוצאות היו כדלקמן: הרמה הממוצעת של נסיוב של אנשים בריאים בצום הייתה 10.7±8.9 מיקרוגרם/דציליטר, ללא הבדלים בין גברים ונשים. רמות כו"ג היו מוגברות משמעותית ב-94 מתוך 98 הנבדקים עם מחלות הפאטו-ביליאריות שונות. רמות כו"ג הגבוהות ביותר נמצאו באלה עם הפאטיטיס נגיפית חריפה, כאשר בשלבי התאוששות מהתרחיש האחרון, הדעיכה ברמת כו"ג הייתה מהירה יותר מאשר הירידה ברמות המדדים הקונבנציונאליים של תפקודי כבד. באלה שאובחנו עם הפאטיטיס עיקשת כרונית, המדד של כו"ג היה פחות רגיש מאשר מדדי ALT ו-AST, אך הוא נמצא רגיש יותר מאשר מדידת רמת פוספטאזה בסיסית (ALP), או מהרמה של סך-בילירובין.
כבר בשנת 1986 התפרסם ב-Austr NZ Med J מחקר שהצביע על היתרון של מדידת כו"ג בנסיוב על פני שיטת הרטנציה של bromsulphalein בזיהוי שלבים מוקדמים או מאוחרים של מחלת כבד אלכוהולית. רמת כו"ג בנסיוב היא אחד הגורמים החשובים להערכת מצב העובר ברחם, בהיריון בו האם סובלת מ-ICP או intrahepatic cholestasis of pregnancy. יש חשיבות למדידת רמת כו"ג בדמו של היילוד בשלבים מוקדמים לאחר הלידה, שכן ככל שרמת כו"ג בדמה של האם גבוה יותר במהלך ההיריון, עובדה זו עולה להשפיע על הסינתזה של EPO (אריתרופויאטין) ביילוד. רמה נמוכה של EPO עלולה לגרום ליילוד היפוקסיה.
רמת כו"ג בנסיוב הייתה מאוד רגישה באבחון של הפאטיטיס פעילה כרונית, ושל צמקת הכבד. מדד כו"ג נחשב בעל ערך באבחון מבדיל של chronic persistent hepatitis מ-chronic active hepatitis. רמת כו"ג ממוצעת בנסיוב של אנשים בריאים מיד לאחר ארוחה, נקבעה כ-22±32 מיקרוגרם/דציליטר, ללא הבדל בין גברים ונשים. ערכי כו"ג בנסיוב של אלה עם מחלות הפאטוביליאריות היו גבוהות יותר בדגימות שנלקחו 2 שעות לאחר ארוחה, בהשוואה לגימות שנלקחו בצום, בין אם דגימות הנסיוב בצום היו של נבדקים בריאים או חולים. יחד עם זאת, רמות כו"ג לאחר ארוחה, היו גבוהות יותר בין חולים עם מחלות הפאטו-ביליאריות. נמצא מתאם לינארי טוב בין רמות כו"ג בנסיוב לבין רמות בילירובין במחלות הפאטו-ביליאריות.
בשנת 1982 התפרסם ב-Gastroenterol Jpn מחקרם של Tanggo וחב' שבחן אף הוא את יעילות מדידת רמת כו"ג במחלות כבד שונות. גם כאן נמדדו בשיטתRIA רמות אלו בצום, או לאחר העמסה של 300 מיליגרם של UDCA או ursodeoxycholic acid, ב-313 מטופלים עם מחלות כבד שונות. נמצא שרמות מוגברות של כו"ג נמצאו ב-66.6% של אלה עם הפאטיטיס חריפה, ב-34.8% של CIA או chrobnic inactive hepatitis, ב-79.3% של אלה עם CHA או chronic active hepatitis, ב-97.1% של אלה עם LC או liver cirrhosis, ב-94.7% באלה עם HCC או hepatocellular carcinoma, וב-80% של אלה עם אבני מרה. השינויים ברמת כו"ג בצום באלה עם הפאטיטיס חריפה (AH) נמצאו מקבילים עם ערכי אנזימי טרנסאמינאזה. בהעמסה פומית של UDCA, תגובות שונות של כו"ג נמצאו ב-CIH וב-CAH וכן בצמקת כבד נשלטת ושאינה נשלטת. תוצאות אלו הביאו למסקנה שקביעת רמות כו"ג בנסיוב מספקות מידע נוסף על מחלות הכבד השונות.
קביעת היחס בין cholylglycine לבין chenodeoxycholylglycine הוא בעל ערך אבחוני משמעותי, שכן ב-80% מהמטופלים עם מחלה הפאטוצלולארית יחס זה קטן מ-1.0, ואילו ב-80% מאלה עם מחלה חסימתית כולסטטית יחס זה גדול מ-1.0.
עיקרון שיטות המדידה של כו"ג
לשיטה אחת קוראים Diazyme cholylglicine immmunoassay או DCI, הנחשבת לשיטה המקובלת והאמינה ביותר, הניתנת ליישום. לשיטה זו רגישות גבוהה עם תחום לינארי של 2.0 מיליגרם/דציליטר. לשיטת DCI יש מקדם שונות של אותה דגימה (inter-assay coefficient variance) של CV=0.024%, כאשר מגבלת הריכוז הנמוך ביותר כל כו"ג הניתנת למדידה היא של 25 מיקרוגרם/דציליטר. מבדק בערכה זו מבוסס על תחרות על אתרי קישור של נוגדן ספציפי, בין כו"ג בדגימת בנסיוב לבין cholylglycine-G6PDH שמוסיפים באופן אקסוגני. קישור הנוגדן לקומפלקס כו"ג-G6PDH מעכב חלקית את פעילות האנזים G6PDH. כו"ג חופשי שבדגימת הנסיוב נקשר ביתר יעילות על ידי הנוגדן המכוון נגדו בהשוואה לקישור הנוגדן לקומפלקס, ולכן פחות נוגדן ייקשר לקומפלקס כו"ג-אנזים, ולכן ככל שרמת כו"ג בדם גבוהה יותר, פחות נוגדן ייקשר לקומפלקס באופן שסך פעילות G6PDH תהיה גבוהה יותר, וניתן יהיה למדוד אותה על מצע ספציפי כאשר רמת כו"ג ניתנת למדידה בספקטרופוטומטר באורך גל 340 ננומטר.
שיטה נוספת היא שיטת CLIA או competitive immunolumnometric assay: בשיטה זו נעשה שימוש במיקרו-חלקיקים ננו-מגנטיים אליהם קשור נוגדן רב-שבטי לכו"ג. לאחר הדגרה קצרה של 15 דקות, כו"ג בנסיוב נקשר על ידי מיקרו-חלקיקים אלה. לאחר שטיפה בבופר מתאים, מוסף לריאקציה נוגדן שני המכוון כנגד כו"ג הספוח כעת אל המיקרו-חלקיקים, כאשר הנוגדן השני קשור לאנזים HRP או (horse radish peroxidase). הוספה של מצע כמילומינוצנטי של אנזים זה, תביא ליצירת אור שעוצמתו נמצאת במתאם ישיר לכמות הנגדן השני שנקשר לכו"ג, וממילא לרמת כו"ג בנסיוב. עוצמת האור נמדדת ביחידות של RLU או Relative Light Units. היתרון בשיטת CLIA ברגישותה, ובכך שהיא אינה מושפעת על ידי אותות רקע. בנוסף, כיום קיים מבחר של אנלייזרים הפועלים בשיטה זו, כגון: Advia Centaur ו- Immulite 2000XPi של חברת Siemens, כמו גם Architect i2000 של חברת Abbott ו-EEE Mddular של חברת Roche.
הוראות לביצוע הבדיקה
יש לדגום דם בצום של 8-12 שעות. הדם נלקח במבחנה כימית, פקק אדום או צהוב, ולאחר סרכוז הנסיוב מועבר למבחנת פלסטיק ריקה ומוקפא מיד. לצורך הבדיקה יש צורך בכמות מינימאלית של 3 מ"ל. אם מעדיפים לשמור את דגימת הנסיוב בהקפאה, הדגימה יציבה למשך 30 יום, ואילו בקירור רגיל הדגימה יציבה עד 12 שעות.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק