הבדלים בין גרסאות בדף "ליזוזים - Lysozyme"
(←ראו גם) |
(←ראו גם) |
||
| שורה 91: | שורה 91: | ||
*[[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | *[[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | ||
| + | * [[בדיקות ביוכימיות|בדיקות מעבדה - בדיקות ביוכימיות]] | ||
* [[בדיקת מחלות מעי|בדיקות מעבדה - מחלות מעי]] | * [[בדיקת מחלות מעי|בדיקות מעבדה - מחלות מעי]] | ||
| שורה 100: | שורה 101: | ||
[[קטגוריה:בדיקות מעבדה: כימיה בדם]] | [[קטגוריה:בדיקות מעבדה: כימיה בדם]] | ||
[[קטגוריה:בדיקות מעבדה: כימיה בשתן]] | [[קטגוריה:בדיקות מעבדה: כימיה בשתן]] | ||
| + | [[קטגוריה: בדיקות מעבדה - בדיקות ביוכימיות]] | ||
[[קטגוריה:בדיקות מעבדה - מחלות מעי]] | [[קטגוריה:בדיקות מעבדה - מחלות מעי]] | ||
גרסה אחרונה מ־07:30, 26 במאי 2017
| מדריך בדיקות מעבדה | |
| ליזוזים | |
|---|---|
| Lysozyme | |
| שמות אחרים | Muamidase ,N-acetylmuramide glycanhydrolase |
| מעבדה | כימיה בדם, בשתן או בצואה |
| תחום | מעקב או ניטור מספר לויקמיות, ודלקות מעי |
| טווח ערכים תקין | בדם-(מגיל 12 חודשים ומעלה)- 3.0-8.8-מיקרוגרם/מ"ל; בשתן (איסוף 24 שעות)-1.3-3.6 מיליגרם/24 שעות, ויש הגורסים פחות מ-2.0 מיקרוגרם/מ"ל שתן. בצואה-פחות מ-10 מיקרוגרם/גרם צואה. |
| יוצר הערך | פרופ' בן-עמי סלע |
- מטרת הבדיקה
אישוש העליות הבולטות ברמת האנזים בלויקמיות גרנולוציטיות או מונוציטיות, במפגעים מיאלו-פרוליפרטיביים, ובהיסטיוציטוזיס ממאירה. מעקב או ניטור של המהלך הטיפולי במקרים של לויקמיה כרונית גרנולוציטית, או לויקמיה כרונית מונוציטית.
נתונים פיזיולוגיים על ליזוזים
ליזוזים (מורמידאזה-muramidase) הוא אנזים בקטריוליטי המצוי במספר תאים הִמוֹ-פּויִאטיים, בעיקר בגרנולוציטים, מונוציטים, והיסטיוציטים. אנזים זה נמצא אך בכמות זעירה בלימפוציטים, ולא נמצא כלל בבזופילים, במיאלובלסטים ואיאוזינופילים. הליזוזים בפלזמה מקורו בעיקר מפירוק של גרנולוציטים ומונוציטים, וריכוזו בפלזמה מבטא את ה-turnover של תאים אלה. רמת ליזוזים גדלה במצבים שפירים כזיהומים ודלקות, או בתהליכים ממאירים כמו בלויקמיות אחדות. ואכן, ליזוזים מוגבר בפלזמה של מטופלים עם לויקמיות מונוציטיות או גרנולוציטיות כרוניות וחריפות (M2, M4 ו-M5), ורמתו במקרים אלה יכולה להגיע מעל 200 מיקרוגרם/מ"ל. פוחתת במהלך טיפול מוצלח. היפוכו של דבר במטופלים עם לויקמיה לימפוציטית. גם חולים עם מפגעי כליות כולל אלה עם דחייה של כליה מושתלת, אי-ספיקת כליות, UTI, nephrosis, pyelonephritis ו- glomerulonephritis , וכן אלה עם מחלת קרוהן או עם ulcerative colitis נוטים לרמות מוגברות של ליזוזים בפלזמה.
ליזוזים, הוא אנזים אנטי-בקטריאלי המיוצר בבעלי חיים ומהווה חלק מה-innate immune system. ליזוזים הוא glycoside hydrolase, המקטלז הידרוליזה של קשרי 1,4-β בין שיירי N-acetylmuramic acid ו-N-acetyl-D-glucosamine בפפטידו-גליקאן, שהוא המרכיב העיקרי של דופן חיידקים גראם-חיוביים. פעולה זו של האנזים גורמת לתמס של החיידקים. ליזוזים מצוי בהפרשות גוף כגון דמעות, רוק, זיעה, חלב-אדם, וריר של איברים פנימיים, בתאים לבנים וברקמות נוספות, כמו גם בחלבון ביצה, ובחלב. כמו כן מוצאים ליזוזים גם בצמחים דוגמת פאפאיה ופיקוס, וכן ליזוזים נמצא בבקטריופאז'ים ומסייע להם בחדירה אל תוך החיידקים.
ליזוזים מצוי כמו כן בגרנולות הציטופלזמיות של מקרופאגים ושל PMNs או polymorphonuclear neutrophils, וכמויות גדולות של ליזוזים (כ-3%) מצויות בלובן הביצה. ליזוזים type C דומה ל-α-lactalbumin הן במבנה והן ברצף חומצות האמינו, מה שמצביע על היות 2 חלבונים אלה שייכים לאותה משפחה (Williams ו-Vocadlo ב- Glycoside hydrolase family 22 משנת 2017). באדם ליזוזים מקודד על ידי הגן LYZ (על פי Yoshimura וחב' ב-Biochem Biophys Res Commun משנת 1988, ו-Peters וחב' ב-Europ J Biochem משנת 1989). ליזוזים יציב בחימום, עם נקודת התכה בטמפרטורה של ℃72 ב-pH5.0 על פי Venkataramani וחב' ב-Pharm Bioallied Sci משנת 2013. יחד עם זאת, בחלב אדם מאבד ליזוזים את פעילותו מהר מאוד בטמפרטורה זו (Chandan וחב' ב-Nature משנת 1964). הנקודה האיזואלקטרית של ליזוזים היא 11.35, והוא יכול לשרוד בטווח רחב של pH בין 6-9. ליזוזים שהופק מחלבון ביצת תרנגולת (ליזוזים C), הוא אנזים קטן יחסית, שהוא מונומר פוליפפטידי המונה 129 חומצות אמינו. מבנהו המרחבי גלובולרי והוא כולל 4 קשרים דיסולפידיים (קשרי S-S) הנוצרים בין 8 שיירי חומצת האמינו ציסטאין.
ההיסטוריה של גילוי ליזוזים
המאפיין האנטי-בקטריאלי של לובן ביצת תרנגולת, עקב הליזוזים שהיא מכילה, נצפה לראשונה על ידי החוקר הרוסי לאכטצ'נקו (Laschtschenko) ב -1909, הוא תאר זאת ב-Z. Hyg. infekt Krankh.
האנזים קיבל בשנת 1921 את השם ליזוזים על ידי אלכסנדר פלמינג (Alexander Fleming) אבי נפניצילין (Proc Royal Soc משנת 1922), אך הוא כבר התייחס לפעילות אנזים זה ברקמות ובהפרשות גוף. פלמינג הבחין לראשונה בפעילות האנטי-בקטריאלית של ליזוזים כאשר טיפל בתרבית חיידקים עם הפרשה רירית מהאף של אדם שסבל משפעת וגודש ניכר בחללי האף (Blake וחב' ב-Nature משנת 1965).
מחקרים על מבנה ליזוזים
בשנת 1965 היה זה Phillips שתיאר לראשונה את המבנה התלת-ממדי של ליזוזים מחלבון ביצה, ברזולוציה של 2 אנגסטרום על ידי קריסטלוגרפיה עם קרני X (על פי Blake וחב' ב-Nature משנת 1965, ו-Johnson ו-Phillips באותו כתב עת מאותה שנה. פענוח המבנה תלת-ממדי התאפשר לאחר הגיבוש של האנזים שבוצע לראשונה על ידי Edward Abraham בשנת 1937. ליזוזים היה החלבון השני והאנזים הראשון שהמבנה שלו נפתר בשיטות של X-ray diffraction, והוא אף היה האנזים הראשון שרוצף במלואו ואשר הכיל את כל 20 חומצות האמינו (Canfield ב-J Biol Chem משנת 1963). כתוצאה ממחקריו של Phillips, ליזוזים היה האנזים הראשון שהובהר מנגנון פעולתו הקטליטית (Rupley ב-Proc Royal Soc London ונתן שרון באותו כתב עת מאותה שנה).
הסינתזה של ליזוזים
הסינתזה הכימית הראשונה של ליזוזים נוסתה על ידי Kenner ואנשיו בליברפול והתפרסמה ב- Soc Proc Royal London בשנת 1977, אך מטרה זו הושגה רק בשנת 2007 באוניברסיטת שיקאגו על ידי Kent וחב' שהצליחו לסנתז ליזוזים פונקציונאלי (Durek וחב' ב-Proc Natl Acad Sci USA).
ליזוזים וסרקואידוזיס
Tomita וחב' סיכמו בסקירתם ב-Lung משנת 1999, על ליזוזים כסמן בנסיוב בהקשר למאפיינים הקליניים והפעילות של סרקואידוזיס, ואת השימושיות הקלינית של מדד זה בסריקה של אוכלוסייה גדולה. מאה ועשרה מטופלים עם סרקואידוזיס ממרכז יפן נבחנו לשלב הקליני של המחלה וכן לרמת ליזוזים בביקורם הראשון במרפאת בית החולים, וכן באופן תקופתי בביקורים הבאים באותה מרפאה. הרגישות של ליזוזים בנסיוב לניבוי סרקואידוזיס נקבעה כ-79.1%, בעוד זו של ACE או angiotensin-converting enzyme נקבעה כ-59.0%. אפילו במקרים ללא רמה מוגברת של ACE בנסיוב, נמצאה רגישות של 72.1% של מבדק ליזוזים. רמת ליזוזים בנסיוב הפגינה נטייה משמעותית לגדול ביחס ישר למספר האיברים המעורבים בתרחיש הסרקואידוזיס. נמצאו הבדלים משמעותיים בין 4 שלבים רדיוגרפיים של המחלה, לבין רמות ליזוזים בנסיוב: רמות ליזוזים המקסימליות הופיעו במטופלים ללא היעלמות של הצלליות הלא נורמאליות ברדיוגרפיה של החזה במהלך 5 שנים, היות גבוהות משמעותית מרמות ליזוזים במטופלים בהם הייתה היעלמות של צלליות אלו. נמצא מתאם חיובי בין רמות ליזוזים ו-ACE בנסיוב, אך כיוון שרמת ליזוזים פחות ספציפית לסרקואידוזיס מזו של ACE, הערך האבחוני שלו יכול להיות מוגבל. יחד עם זאת, הרגישות של בדיקת ליזוזים הייתה גבוהה גם כאשר רמות ACE היו בגבולות הנורמה, והיא הייתה במתאם טוב עם הקליניקה של סרקואידוזיס. לכן, מדד ליזוזים נראה הולם את מהלכי ניטור המחלה במקרים מוכחים שלה.
התפקיד של ליזוזים בתחלואה וברפוי
אנזים זה מהוה חלק ממערכת החיסון הטבעית או המולדת (innate immune system). רמות נמוכות של ליזוזים נכרכו עם מחלת ריאות כרונית של הפג או היילוד הידועה כ-bronchopulmonary dysplasia על פי Ravenis ו- Kaliner ב-J Pediatr משנת 1992). הריכוז של ליזוזים בחלב אדם גדול פי-1,600-3,000 מאשר ריכוזו בחלב בקר. ליזוזים אדם פעיל יותר מזה של לובן הביצה. Cooper וחב' יצרו שורת עזים טרנסגניות על ידי ששתלו ב-DNA שלהם את הגן האנושי המקודד לליזוזים, כדי שהן תייצרנה את האנזים האנושי להגן על ילדים מפני שלשולים אם אלה אינם זוכים לינוק מחלב אימם (PloS One משנת 2013). כיוון שליזוזים מהוה צורה טבעית של הגנה מפני פתוגנים גראם-חיוביים דוגמת bacillus ו-streptococcus, הוא משחק תפקיד חשוב בחיסון המתקבל בתינוקות כתוצאה מהנקה (Chandra ב-Nutr Rev משנת 1978). בעוד שהעור הוא מחסום הגנתי בגלל היובש והחומציות שלו, לחמית העין (conjunctiva) מוגנת על ידי הפרשת אנזימים, בעיקר ליזוזים ו-defensin, כאשר אלה אמצעי הגנה אלה נכשלים, מופיעה בדלקת הלחמית (conjunctivitis). בסוגי סרטן אחדים (בעיקר לויקמיה מיאלומונוציטית) יצירה מופרזת של ליזוזים על ידי התאים הסרטניים עלולה לגרום לרמות טוקסיות של אנזים זה בדם. רמות גבוהות של ליזוזים בדם עלולות לפגוע בכליות ולהיפוקלמיה.
ליזוזים משמש באופן סדיר בתעשיית המזון בתור חומר משמר. לרוב מוסיפים אנזים זה למוצרי חלב וגבינות או שהוא משמש בתעשיית היין כגורם השבחה שכן הוא פועל כנגד מגוון רחב של חיידקים המייצרים חומצת חלב (Oenococcus, Pediococcus ו-Lactobacillus, העלולים לפגוע ביציבות היין וליצירת ריח בלתי רצוי. ליזזוזים הורג כמו כן חיידק כ-Leuconostoc, האחראי להסב חומצה מאלית לחומצת חלב במהלך תסיסה מאלו-לקטית. לאלה עם נטייה לאלרגיה הצריכה של ליזוזים עלולה להיות פוגענית, שכן גם בריכוזים מאוד נמוכים ליזוזים מהווה אלרגן שעלול ליצור תגובה אלרגית. לפיכך, קיימת בארה"ב הוראה לסמן באופן בולט פריטי מזון להם הוסף ליזוזים. אכן, בנוסף ל-ovabumin, ליזוזים מייצג את החלבון האלרגני העיקרי בלובן הביצה.
מנגנון פעולת ליזוזים
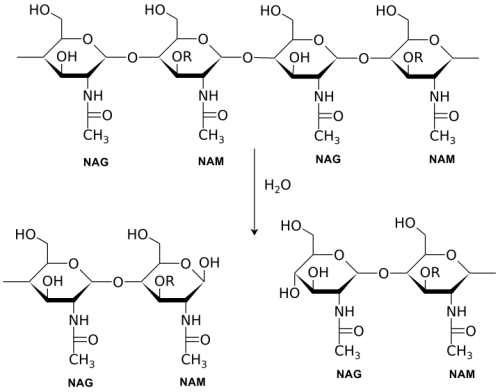
האנזים פועל על ידי שהוא מתקיף ומבקע את הקשרים הגליקוזידים בפפטידו-גליקנים הנמצאים בדופן של חיידקים גראם-חיוביים: האתר הפעיל הנמצא בשסע בין המקטעים של ליזוזים נקשר למולקולת הפפטידו-גליקן ותוקף את המצע הטבעי שלו בין N-acetylmuramic acid (להלן NAM) ואטום הפחמן הרביעי של N-acetylglucosamine (להלן NAG).
פותחו מצעים מלאכותיים שיכולים לשמש גם מצעים לליזוזים (Sharon ב-Proc Royal Soc of London משנת 1967).
דופן החיידק
למרבית החיידקים דופן המקיפה את קרום התא. דופן החיידק קובעת ושומרת על צורת החיידק ובכך מאפשרת לו להתקיים גם בסביבה היפוטונית . הדופן עשויה מחומר מיוחד הנקרא: פפטידוגליקן. הפפטידוגליקן הוא פולימר קשיח היוצר מבנה מרושת בעל חוזק מכני רב. יחידות המבנה הבסיסיות של הפפטידוגליקן, הן שני סוכרים ייחודיים לחיידקים הנקראים בקצרה NAG ו- NAM. סוכרים אלה קשורים ביניהם לסירוגין ויוצרים רשת של שרשראות ארוכות המחוברות ביניהן באמצעות שרשראות רוחב של חומצות אמינו. רשת זו אחראית למבנהו הקשיח של הפפטידוגליקן.
האנזים מזרז את פירוק הקשר הכימי בין יחידות הסוכר (בין NAM לNAG ) של הפפטידוגליקן ע"י הידרוליזה. חיידקים חיים בסביבות היפוטוניות בדרך כלל ולכן כתוצאה מפעולת הליזוזים תא החיידק מתפוצץ בעקבות כניסת מים לתוכו באוסמוזה.
ליזוזים בצואה
ליזוזים משמש להגנה אנטי-בקטריאלית במערכת העיכול, והוא מופרש על ידי גרנולוציטים, מקרופאגים, תאי Paneth, Brunner's Glands כמו גם על ידי תאי קריפטות נורמאליים במעי הגס. המקור העיקרי של ליזוזים בצואה הם גרנולוציטים במעי. רמות מוגברות של ליזוזים בצואה זוהו במחלות דלקתיות של המעי (IBD) בהשוואה לביקורת של בריאים (Van der Sluys Veer וחב' ב- Dig Dis Sciמשנת 1998, ו-Klass וחב' ב-Gut משנת 1978).
ליזוזים בצואה בהערכה של פעילות מחלת מעי דלקתית (IBD)
van der Sluys Veer וחב' ניסו לבדוק האם מדידת רמת ליזוזים בצואה מסייעת בקביעת פעילות של IBD. מחקרו כלל 112 חולים עם Crohn, 46 חולים עם ulcerative colitis, ו-40 אנשים בריאים כביקורת, בהם נמדדה רמת ליזוזים בצואה. התוצאות נכרכו עם דרגות CDAI ו-AI במחלת קרוהן, ועם דרוג Truelove ו-Witts' ב-.ulcerative colitis רמת ליזוזים בצואה נמצאה משמעותית גבוהה יותר במחלת קרוהן (75±14 מיקרוגרם/גרם, p<0,001), וב- ulcerative colitis(238±33 מיקרוגרם/גרם, p<0.001), בהשוואה לביקורת הבריאה (1±6 מיקרוגרם/גרם). נמצא רק מתאם חלש בין רמת ליזוזים בצואה לבין CDAI (r=0.32) או לבין AI (r=0.38) בחולים עם מחלת קרוהן, או עם מדרג Truelove and Witts' ב-ulcerative colitis (r=0.47). מחקר זה הצביע על כך שמדידת ליזוזים בצואה היא בעלת יתרון קטן באבחון או בקביעת דרגת מחלת מעי דלקתית, אם כי היא עשויה לסייע בהערכת פעילות של IBD במעי הגס.
עלייה מתונה ברמת ליזוזים בצואה כרוכה לרוב עם צמיחה משמעותית באנטרו-פתוגנים כגון שמרים או חיידקים דיסביוטיים. במחלת קרוהן, עודף ליזוזים עלול להיות כתוצאה מהפרשות פעילות של מקרופאגים ב- lamina propriaאו של מונוציטים בגרנולומות. לעומת זאת, ב-ulcerative colitis ההשערה היא שהעלייה בליזוזים הצואתי היא משנית לאובדן של גרנולוציטים במעי, כאשר האנזים מופרש מהגרנולות המפרישות של תאים אלה. בנוסף, מטפלזיה של תאי Paneth, תופעה המתרחשת במצבי דלקת מעי-גס שונים, היא רק תורם שולי לעלייה של ליזוזים בצואה. תאי Paneth הם חלק משכבת החיפוי האפיתליאלית הנמצאת בחלק העמוק ביותר של קריפטות המעי הידועות כקריפטות של Lieberkohn. תאי Paneth מכילים ליזוזים בגרנולות המפרישות שלהם, וביחד עם היכולת הפגוציטית שלהם, הדבר מסייע לווסת את הפלורה המיקרוביאלית במעי. ניתן לומר שליזוזים מסייע לקביעת הפעילות של האנזים במעי הגס יותר מאשר במעי הדק.
מנגנוני הפעולה של ליזוזים
המנגנון על פי Phillips
מנגנון זה מציע שהפוטנציאל הקטליטי של ליזוזים מקורו הן מהלחץ הסטרי על המצע הקשור וכן מייצוב אלקטרוסטטי של תוצר הביניים oxo-carbenium. על בסיס נתונים של הגביש התלת-ממדי, הציע Phillips שהאתר הפעיל של האנזים הוא במקום הקישור של ה-hexasaccaride. האנזים מעוות את מצג הסוכר הרביעי ב-hexasaccaride לקונפורמציה של "חצי כסא", ובמצב לחוץ זה, הקשר הגליקוזידי נשבר ביתר קלות (Holtje ב-Exs משנת 1996). נוצר תוצר ביניים יוני המכיל oxo-carbenium כתוצאה משבירת קשר גליקוזידי, והוא מסייע להפחית את המחסום האנרגטי של הריאקציה (Dahlquist ןחב' ב-Biochemistry משנת 1969).
תוצר הביניים המוצע, oxo-carbonium, נחשב כגורם המיוצב אלקטרוסטטית על ידי שיירי glutamate35 ועל ידי aspartate52 באתר הפעיל בשנת 1978 על ידי אריה וורשל. הייצוב האלקטרוסטטי התבסס על ההשוואה עם מים, שכן הרה-אוריינטציה של dipoles של מים יכולה לבטל את האנרגיה המייצבת של אינטראקציה המבוססת על מטען חשמלי. במודל של וורשל, האנזים פועל כסולבנט-על, המייצב את האוריינטציה של זוגות יונים, ובמיוחד מפחית את האנרגיה כאשר היונים מתקרבים זה לזה (Warshel ב-Proc Natl Acad Sci משנת 1978).
השלב מגביל הקצב (rate-determining step או RDS) כרוך ביצירת תוצר הביניים oxo-carbenium, אם כי התקבלו מספר תוצאות סותרות למקם את RDS. על ידי זיהוי תוצר הריאקציה (p-nitrophenol) נמצא שה-RDS יכול להשתנות בטמפרטורות שונות, וזו הייתה כנראה הסיבה לתוצאות הסותרות. בטמפרטורה גבוהה יותר ה-RDS נובע מיצירת של תוצר ביניים glycosyl-enzyme, ואילו בטמפרטורה נמוכה יותר ה-RDS נקבע כתוצאה שבירה של אותו תוצר-ביניים (Weber ו-Fink ב-J Biol Chem משנת 1980).
המנגנון על פי Koshland
בשנת 1969 הציע Dahlquist במאמר ב-Biochemistry מנגנון קו-ולנטי לפעילות ליזוזים, המבוסס על kinetic isotope effect, אך למשך פרק זמן ארוך המנגנון היוני של פיליפס היה יותר מקובל. בשנת 2001 הוצע על ידי Vocadlo וחב' ב-Nature מנגנון מתוקן בו שיחק תפקיד תוצר ביניים קו-ולנטי ולא יוני, זאת על פי אנליזת ESI-MS. האחרונים עשו שימוש במצע מסומן על ידי fluoro-2 על מנת להפחית את קצב הריאקציה ולצבור תוצר ביניים לאיפיון. נמצא ש-2 חומצות האמינו Glu35 ו-Asp52, היו קריטיות לפעילות ליזוזים. Glu35 פועל כתורם פרוטון לקשר הגליקוזידי, המבקע את הקשר C-O במצע, ואילו Asp52 פועל כנוקלאופיל היוצר תוצר ביניים של אנזים-גליקוזיל. ה-Glu35 מגיב עם מים ליצירת יון הידרוקסיל, שהוא נוקלאופיל חזק יותר ממים, התוקף לאחר מכן את תוצר הביניים אנזים-גליקוזיל, להביא ליצירת תוצר הריאקציה ולהותיר את האנזים ללא כל שינוי. מנגנון קו-ולנטי זה נקרא על שם Koshland שהציע אותו כבר בשנת 1953 ב-Biol Rev.
Bowman וחב' ב-Chem Commun משנת 2008 הציעו את מציאותו של תוצר ביניים קו-ולנטי תוך שימוש ב- QM/MM ((quantum mechanics/ molecular mechanics. חישובים העלו שתוצר הביניים הקו-ולנטי ממנגנון קושלנד, יציב ביותר מ- ~30 kcal/mol מאשר תוצר הביניים היוני של מנגנון פיליפס. חישובים אלה קבעו שתוצר הביניים היוני אינו מועדף אנרגטית בהשוואה לתוצר הביניים הקו-ולנטי.
שינויים בקונפורמציה של האנזים
ליזוזים יכול להופיע ב-2 קונפורמציות: מצב "פתוח" ופעיל, ומצב "סגור" ובלתי-פעיל. במצבו הפעיל ליזוזים מסוגל לבקע את המצע שלו, תוך שבירת 100 קשרים גליקוזידים בממוצע, תוך 15 שניות. על מנת להיקשר למצע חדש תוך מעבר מהמצב הסגור והבלתי-פעיל למצב פתוח ופעיל, נדרשים 2 שלבים של שינוי קונפורמציה, ואילו במעבר לצורה הבלתי-פעילה נדרש רק שלב אחד של שינוי קונפורמציה.
תפקיד ליזוזים בתחלואה ובתרפיה
ליזוזים הוא חלק מהחסינות הטבעית של הגוף (innate system). רמות מופחתות של ליזוזים נכרכו עם דיספלזיה ברונכו-פולמונארית ביילודים (Choi וחב' ב-Science משנת 2012). ולדות של חזירים שהוזנו עם חלב אדם עשיר בליזוזים, התאוששו מהר יותר ממחלות שלשוליות שנגרמו על ידי E. Coli. נמצא שרמת ליזוזים בחלב אדם גדולה פי-1,600-3,000 מריכוזה בחלב של בקר. ליזוזים אדם פעיל יותר מזה של לובן ביצת תרנגולת. גזע טרנסגני של עזים פותח, המייצר חלב עם ליזוזים אנושי, כדי שיהיה ניתן להשתמש בחלב עזים להגן על ילדים מפני שלשולים (Revenis ו-Kaliner ב-J Pediatr משנת 1992, ו-Cooper וחב' ב-PLos One משנת 2013).
כיוון שפעולת ליזוזים היא צורה טבעית של הגנה מפני פתוגנים גראם-חיוביים כמו בצילוס וסטרפטוקוקוס (Molteni ב-Science משנת 2016), משחק אנזים זה תפקיד חשוב בחסינות של תינוקות על ידי יניקה של חלב אם (Chandra ב-Nutrition Rev משנת 1978). בה בשעה שעור הגוף מהווה מחסום הגנתי בשל היובש והחומציות שלו, לחמית העין (conjunctiva) מוגנת על ידי אנזימים כגון ליזוזים ו-defensin. כשל של אנזימים אלה גורם לדלקת הלחמית (conjunctivitis).
שימושים נוספים של ליזוזים
האנזים משמש לרוב להמסתם של חיידקים גראם-שליליים (Salton ב-Bacteriol Rev משנת 1957). פעילות ליזוזים עולה עם העלייה בטמפרטורה עד 60 מעלות, עם טווח pH6.0-7.0 . גם מלחים משפיעים על פעילות האנזים. נתרן כלורידי מחיש המסת חיידקים, אם כי בריכוזים גבוהים, NaCl מעכב פעיל של תהליך הליזיס. תצפיות דומות נעשו עם מלחי אשלגן, אם כי זנים חיידקים שונים יכולים להשפיע על האופן בו ריכוזי מלחים שונים, משנים את יעילות הליזיס על ידי ליזוזים.
הוראות לביצוע הבדיקה
הבדיקה בדם מועדפת לביצוע בנסיוב, ודגימת הדם צריכה להתבצע במבחנה כימית (פקק אדום או צהוב) תוך הימנעות מהקפאות והפשרות חוזרות לאחר הפרדת בנסיוב בסרכוז. ניתן גם לדגום את הדם במבחנת ספירת-דם (EDTA) כאשר הסרכוז צריך להתבצע לא יאוחר משעתיים לאחר נטילת הדם, והנוזל המופרד צריך להישלח למעבדה בקירור או כנסיוב/פלזמה קפואים. יציבות הדגימה היא של 8 שעות בטמפרטורת החדר, 7 ימים בקירור, 30 יום בהקפאה במינוס 20 מעלות, ו-90 יום בהקפאה במינוס 70-80 מעלות. יש להימנע מדגימות דם מאוד המוליטיות, ליפמיות או איקטריות.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק