הבדלים בין גרסאות בדף "Orosomucoid"
| (18 גרסאות ביניים של אותו משתמש אינן מוצגות) | |||
| שורה 22: | שורה 22: | ||
התפקיד הפיזיולוגי היחיד המוסכם לגבי ORM, הוא לשמש נשא של חומרים ליפופיליים בסיסיים או כאלה שהם ניטרליים מבחינת מטענם. ברפואה, ORM ידוע כנשא עיקרי של תרופות בסיסיות (הטעונים מטען שלילי), בעוד שאלבומין הוא הנשא של תרופות חומציות (שמטענן החשמלי שלילי) או הניטרליות מבחינת מטענן. ORM נשא של סטרואידים, של פרוגסטרון ו[[ויטמין B12]] ושל [[מעכבי פרוטאזות]] (Urien וחב' ב-Biochem J משנת 1991). הזדקנות גורמת לעלייה קלה ביותר ברמת ORM, ואכן ההשפעה של שינויים קלים אלה על הקישור של תרופות שונות ל-ORM זעירה (Barash ב- Clinical Anesthesia משנת 209). ל-ORM יש אינטראקציה מורכבת עם הגורמים להומאוסטאזיס של בלוטת התריס: ORM בריכוזים נמוכים מעודד את הקולטן ל-TSH ולהצטברות התוך-תאית של c-AMP. לעומת זאת, ORM בריכוזים גבוהים מעכבים את פעילות TSH (Zimmermann-Belsing וחב' ב- Molecular and Cellular Endocrinology משנת 2002, ו-Dietrich וחב' ב- J Thyroid Resמשנת 2012). | התפקיד הפיזיולוגי היחיד המוסכם לגבי ORM, הוא לשמש נשא של חומרים ליפופיליים בסיסיים או כאלה שהם ניטרליים מבחינת מטענם. ברפואה, ORM ידוע כנשא עיקרי של תרופות בסיסיות (הטעונים מטען שלילי), בעוד שאלבומין הוא הנשא של תרופות חומציות (שמטענן החשמלי שלילי) או הניטרליות מבחינת מטענן. ORM נשא של סטרואידים, של פרוגסטרון ו[[ויטמין B12]] ושל [[מעכבי פרוטאזות]] (Urien וחב' ב-Biochem J משנת 1991). הזדקנות גורמת לעלייה קלה ביותר ברמת ORM, ואכן ההשפעה של שינויים קלים אלה על הקישור של תרופות שונות ל-ORM זעירה (Barash ב- Clinical Anesthesia משנת 209). ל-ORM יש אינטראקציה מורכבת עם הגורמים להומאוסטאזיס של בלוטת התריס: ORM בריכוזים נמוכים מעודד את הקולטן ל-TSH ולהצטברות התוך-תאית של c-AMP. לעומת זאת, ORM בריכוזים גבוהים מעכבים את פעילות TSH (Zimmermann-Belsing וחב' ב- Molecular and Cellular Endocrinology משנת 2002, ו-Dietrich וחב' ב- J Thyroid Resמשנת 2012). | ||
| − | ORM זוהה כאחד מתוך ארבעה סמנים שימושיים בצירקולציה להערכה של הסיכון לתמותה מסיבה כלשהי במהלך 5 השנים הבאות, כאשר יתר הסמנים הם רמת אלבומין, רמת ציטראט וגודל החלקיק של very low-density lipoprotein {{כ}}(Fischer וחב' ב- PLos | + | ORM זוהה כאחד מתוך ארבעה סמנים שימושיים בצירקולציה להערכה של הסיכון לתמותה מסיבה כלשהי במהלך 5 השנים הבאות, כאשר יתר הסמנים הם רמת אלבומין, רמת ציטראט וגודל החלקיק של very low-density lipoprotein {{כ}}(Fischer וחב' ב- PLos Med משנת 2014). ORM גדל בריכוזו בצהבות חסימתיות, ופוחת בריכוזו בצהבת הפאטו-תאית ובזיהומי מעי. |
| + | |||
| + | ==המבנה של ORM== | ||
| + | משקלו המולקולארי של ORM הוא 41-43 אלף דלטון, אם כי יש הגורסים תחומי משקל מולקולארי רחבים יותר, של 37-54 אלף דלטון, וזאת כתוצאה משיעורי גליקוזילציה שונים המתבטאים בתכולה משתנה של המרכיב הסוכרי של המולקולה. כל חמש השרשרות הסוכריות העשירות בחומצה סיאלית, מחוברות לשלד הפפטידי של ORM בקשרי N-linkage {{כ}}(Yoshima וחב' ב-J Biol Chem משנת 1981). ORM גובש כמלח עופרת ליצירת דו-פירמידות בעלות 6 צלעות. נמצא של-ORM יש מסיסות גבוהה במיוחד במים ובממיסים אורגניים קוטביים, מה שמוסבר על ידי התכולה הגבוהה של סוכרים במבנה המולקולה. באדם, הקודמן ORM1 היא שרשרת פוליפפטידית אחת עם 201 חומצות אמינו, כאשר בקצה ה-N טרמינאלי שלה מופיע signal peptide בן 18 חומצות אמינו המבוקע בתהליך העיבוד של החלבון, ומוליך לחלבון המונומרי הבשל המכיל באדם 183 חומצות אמינו או 187 חומצות אמינו בחולדה, עם שני קשרים דיסולפידים באדם, וקשר דיסולפידי בודד בחולדה. יש הבדל של 22 חומצות אמינו בין 2 הואריאנטים ORM1 ו-ORM2 המקודדים על ידי 2 גנים פולימורפיים (ORM1 ו-ORM2) שמיקומם בכרומוזום 9 בעמדה q31-qter. בנוסף, בעמדות 32 ו-47 ייתכן שחלוף של חומצות האמינו, מה שמשקף כנראה פולימורפיות באוכלוסייה האנושית. נתון מעניין נוסף הוא דרגת ההומולוגיה הגבוהה בין ORM לבין מולקולת IgG מאדם (Schmid וחב' ב-Biochemistry משנת 1973), וכן בין ORM לבין הקולטן של EGF (Toh וחב' ב-Nature משנת 1985). | ||
| + | |||
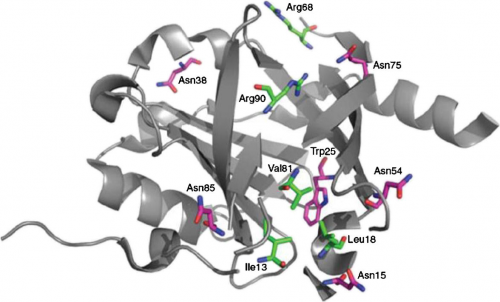
| + | כפי שרואים בתרשים למטה לגבי המבנה של אתר הקישור של ORM {{כ}}(Filip וחב' ב-Expert Opin drug Metabol Toxicol משנת 2013), נמצא 2 שרשרות צדדיות טעונות חיובית (Arg68 ו-Arg90) הממוקמות מצדו האחד של הגומחה (cleft) של אתר הקישור, כאשר שאר הגומחה בעיקרה אינה קוטבית. החלק הפנימי של שקע זה מקביל לשרשרת צדדית בו משחקים תפקיד חיוני השיירים Tyr27, Phe49, Phe51, Leu62, Leu79, Ile88, Leu101, Tyr110, Leu112 ו-Tr127. החלק התחתון של הגומחה נוצר על ידי Ile13, Leu18 ו-Val81. בתרשים מצוינים חמשת שיירי האספרגין (Asn), אליהם נקשרות חמשת השרשרות הסוכריות. מולקולת ORM בחולדה היא בעלת הומולוגיה של 59% ברצף חומצות האמינו לזו של האדם. עם זאת, המקטע (domain) התפקודי של ORM משומר ביותר בין אדם, חולדה ועכבר. | ||
| + | |||
| + | |||
| + | [[קובץ:ORM1.png|ממוזער|מרכז|500 פיקסלים|המבנה השלישוני של גומחת הקישור של ORM]] | ||
| + | |||
| + | |||
| + | ==החלק הסוכרי של ORM== | ||
| + | המרכיב הסוכרי של ORM נחקר היטב שכן זהו אחד הגליקופרוטאינים הבודדים המכיל שרשרות סוכריות עם הסתעפויות טטרה-אנטנריות, תלת-אנטנריות ודו-אנטנריות, כאשר כל חמשת השרשרות הצדדיות מחוברות לשייר אספרגין בעמדות 15, 38, 54, 75 ו-85, (תרשים למטה): | ||
| + | |||
| + | |||
| + | [[קובץ:ORM2.png|מרכז|500 פיקסלים]] | ||
| + | |||
| + | |||
| + | יתרה מכך, סוכר הקצה של השרשרות הסוכריות ב-ORM הוא חומצה סיאלית או N-acetyl-neuraminic acid , מהווה 10-12% מכלל הסוכרים במולקולה, ובגלל מטענו השלילי מתקבלת הנקודה האיזואלקטרית הנמוכה של המולקולה. סוכר טרמינאלי זה יכול להיות קשור בקשרי α2-3 או α2-6 לסוכר galactose. גם הסוכר fucose הוא סוכר קצה ב-ORM, שיכול להיות קשור בקשר α1-3 לסוכר GlcNAc. התגלו 12-20 גליקופורמים של ORM בנסיוב תקין, אם כי במצבים פתולוגיים יש עדיפות להופעת גליקאנים עם מבנה של שרשרת סוכרית דו-אנטנארית, שניתן לגלותם לדוגמה בשלב המוקדם של ריאקציית acute phase. נמצא שהציטוקינים IL-1, IL-6 ו-TNF-α וכן גלוקו-קורטיקואידים קשורים למודיפיקציות אלו במבנה הסוכרי של ORM {{כ}}(Van Dijk ב-Glycoconj J משנת 1995). השינויים בגליקוזילציה של מולקולת ORM אינם מוגבלים רק למצבים חריפים של דלקת, אלא מופיעים במגוון של מצבים פתו-פיזיולוגיים כמו הריון, דלקת מפרקים שגרונית חמורה, צמקת כבד מאלכוהוליזם, והפאטיטיס (Biou וחב' ב-Clin Chim Acta משנת 1991). | ||
| + | |||
| + | ==הפעילות הביולוגית של ORM== | ||
| + | תכונות ביולוגיות רבות יוחסו ל-ORM על ידי Kremer וחב' ב-Pharmacol Rev משנת 1988: ההגנה שהוא מעניק כנגד ספסיס נאונטלי, האינטראקציה שלו עם פוספוליפידים בממברנה, יכולתו לקשור היסטמין, כמו גם לעכב צימות טסיות, כימוטקסיס של ניטרופילים, יצירת סופר-אוקסידים, והשפעתו על שגשוג לימפוציטים. ORM נחשב כגורם טבעי נוגד-דלקות ואימונו-מודולטורי בעיקר בהקשר של פעילות נוגדת המשלים (complement) והאנטי-ניטרופילית (Williams וחב' ב-Am J Physiol משנת 1997). ואמנם, הודגם הן in-vitro כמו גם in vivo ש-ORM היא מולקולה אימונו-מודולטורית: In vitro, ORM מעכב שפעול ניטרופילים (Vasson וחב' ב-Clin Chim Acta משנת 1994) ומגביר את ההפרשה של מעכב IL-1 על ידי מקרופאגים בעכבר [שהוא כנראה אנטגוניסט של הקולטן ל-IL-1 (Tilg וחב' ב-J Exp Med משנת 1993), וכמו כן מאפנן את הפרשת ציטוקינים המושרית על ידי ליפופוליסכרידים (LPS) (Boutten וחב' ב-Eur J Immunol משנת 1992). מאוחר יותר הודגם ש-ORM מגיב באופן ישיר עם LPS {{כ}}(Moore וחב' ב-Inflammation משנת 1997). מחקרים in vitro עם מונוציטים מאדם, הראו שהפרשת TNF-α המושרית על ידי ORM תלויה בשפעול של האנזים טירוזין קינאזה (Su וחב' ב-Immunopharmacol משנת 1999). כמו כן הוצע ש-ORM דרוש לשמור על חדירותן של קפילרות כנראה על ידי הגברת הסלקטיביות של המטען הפולי-אניוני במחסום האנדותליאלי (Curry וחב' ב-Am J Physiol משנת 1989). | ||
| + | |||
| + | In vivo, עירוי של ORM נמצא מגן על עכברים מפני הפאטיטיס וכן מפני הלם קטלני המושרה על ידי TNF-α {{כ}}(Libert וחב' ב-J Exp Med משנת 1994). עלתה השערה שפעילות עיכוב צימות הטסיות והיכולת של ORM לעכב כמוטקסיס של ניטרופילים ולעכב מטבוליזם חמצוני, עומדים בבסיס פעילויותיו המגוננות (Costello וחב' ב-Nature משנת 1979). כן נמצא ש-ORM מעכב באופן ספציפי אפופטוזיס המושרה על ידיTNF-α בעכברים, אך נראה שההגנה שמעניק ORM לתאים פועלת על ידי מנגנון בלתי-ישיר, שכן in vitro ORM נכשל בהגנה על תאי הפאטומה אנושיים, מפני אפופטוזיס המושרה בתאים אלה על ידי TNF-α בשילוב עם אקטינומיצין D {{כ}}(Van Molle וחב' ב-J Immunol משנת 1997). | ||
| + | |||
| + | הפעילות האימונו-מודולטורית של ORM נמצאה תלויה בדרגת הגליקוזילציה שלו. לדוגמה, העיכוב של שגשוג לימפוציטים תלוי בדרגת ההסתעפות של השרשרות הסוכריות של ORM {{כ}}(Pos וחב' ב-Inflammation משנת 1990), ועיכוב צימות הטסיות מוגבר כאשר מולקולת ORM עוברת דה-סיאליזציה. הדגמה נוספת של חשיבות השרשרות הסוכריות של ORM לפעילותו הביולוגית, מוצאים בנתון הבא: ORM עם מבנה סוכרי של sialyl Lewis X הנוצר במהלך דלקת, משדרג את הנזקים הנגרמים על ידי המשלים וכן על ידי ניטרופילים , ואילו ORM ללא המבנה הסוכרי של sialyl Lewis X אינו פועל באופן דומה (De Graaf וחב' ב-J Exp Med משנת 1993). {{כ}} sialyl Lewis X הוא הליגנד אליו נקשרות מולקולות הספיחה E-selectin ו-P-selectin בתהליכי הספיחה של ניטרופילים, מונוציטים או תאי T לתאי האנדותל או לטסיות במצבי דלקת (Lasky ב-Science משנת 1992). | ||
| + | |||
| + | בשיטת surface plasmon resonance spectroscopy נמצא ש-ORM מאנשים עם דלקת חריפה, בו יש תכולה גבוהה של sialyl Lewis X, משמש כליגנד ספציפי למולקולה כימרית של E-selectin-IgG. נמצא שאוליגו-סככרידים עם סיאליזציה מלאה הגנו כנגד נזק לריאות בחולדות in vivo {{כ}}(Mulligan וחב' ב- J Exp Med משנת 1993). נראה אם כן, שהגדלת החלק של sialyl Lewis X המושרה על ידי מצבי דלקת בקומפלקס הגליקני של ORM, מייצגת מנגנון של עיכוב על ידי משוב-חוזר של חדירת גרנולוציטים לתוך הרקמות הדלקתיות. במקובץ, נתונים אלה מראים שהשרשרות הסוכריות של ORM הן בעלת תפקיד קריטי בפעילויות האימונו-מודולטוריות של גליקופרוטאין זה. | ||
| + | |||
| + | ==קישור של תרופות ל-ORM== | ||
| + | אלבומין, ליפופרוטאין ו-ORM הם החלבונים החשובים ביותר בהיבט של קישור תרופות בפלזמה, מה שחיוני מאוד לתכונות הפרמאקו-קינטיות של תרופות אלה. שינויים ברמת ORM מתרחשים בתרחישים דלקתיים, מה שיכול לשנות את ריכוזי התרופות החופשיות בפלזמה בלי לשנות את סך רמתן של תרופות אלו בפלזמה. לפיכך, רמת התרופה החופשית תשקף באופן נאמן יותר את עוצמת ההשפעה הפארמקולוגית של התרופה. בגין תכונותיו הביופיזיות של ORM, הוא קושר בעיקר תרופות בעלות מטען חשמלי בסיסי, או כאלה הניטראליות מבחינת מטענן החשמלי כמוdiazepam ו-carbamazepine. ל-ORM יש יכולת לקשור תרופות בסיסיות כמו טמוקסיפן ו-propanolol {{כ}}(Albani וחב' ב-Br J Clin Pharmacol משנת 1984). כמו כן יכול ORM לקשור vanilloids דוגמת capsaicin ו-resiniferatoxin {{כ}}( Szallai וחב' ב-J Pharmacol Exp Ther משנת 1992), הפארין, IgG3, סרוטונין, PAF או platelet activating factor {{כ}}(McNamara וחב' ב-Biochem Pharmacol משנת 1986), מלטונין (Morin וחב' ב-Pharmacology משנת 1997), והיסטמין (Chachaj וחב' ב-Arch Immunol Ther Exp משנת 1980). | ||
| + | |||
| + | ואריאנטים של ORM הם בעלי כושר קישור שונה לתרופות. לדוגמה, atazanavir מעדיף את הואריאנט ORM1*F1, בעוד ש-lopinavir ו-indinavir מעדיפים את הואריאנט ORM1*S {{כ}}(Barrail-Tran וחב' ב-Antimicrob Sgents Chemother משנת 2010). יתרה מכך, המציאות של 2 צורות של אותו חלבון בדם, משפיעה על הזיקה של קישור תרופות. נמצא שתרופות דוגמת מתאדון, disopyramide, deramciclane, propafenone ו-amitriptyline נקשרות באופן סלקטיבי ל-ORM2, בניגוד ל-קומאדין, prazosin, imatinib,quinidine ו-dipyridamole הנקשרים באופן מועדף ל-ORM1. | ||
| + | |||
| + | באופן מעניין, ORM קושר ונושא מולקולות הקשורות למודולציה של ביטוי הגן המקודד ל- ORM עצמו, כמו phorbol esters, וכן תרופות חומציות כמו phenobarbital {{כ}}(Schley ו-Mueller ב-Pharmacopsychiatry משנת 1983), חומצה רטינואית (Israili ו-El-Attar ב-Clin Pharmacol Ther משנת 1983) וסטרואידים דוגמת קורטיזול (Grimaldi וחב' ב-Prog Clin Biol Res משנת 1989). תכונתו של ORM לשאת סטרואידים הודגמה כבר בסוף שנות ה-60 על ידי Westphal וחב' ב-Biochim Biophys Acta משנת 1968, וכיום כבר ידוע ש-ORM מסוגל גם לשאת סטרואידים סינטתיים כמו mifepristone. בעוד שלסטרואידים יש כנראה אתר קישור יחיד על פני ORM, הרי שלגבי אסטרדיול יש ל-ORM כנראה עד 7 אתרי קישור, ול-phenobarbital יש ל-ORM רק 2 אתרי קישור. כמו כן נמצא ש-ORM קושר ונושא חוסמי-β, חומרי הרדמה מקומית, תרופות ממשפחת phenothiazine, חוסם טירוזין קינאזה כמו imatinib וכן מעכבי HIV protease. | ||
| + | |||
| + | למרות שהקישור של תרופות ל-ORM היא בעיקר הידרופובי, ישנם מספר נתונים המצביעים גם על אינטראקציה אלקטרוסטטית, ומחקרים אחדים דווחו על כל שבפלזמה קישור התרופות ל-ORM הוא סטראו-סלקטיבי, בעיקר כשמדובר בתרופות בעלות מטען חשמלי בסיסי, וכן שקישור התרופות בפלזמה עולה עם העלייה ב-pH {{כ}}(Ponganis ו-Stanski ב-J Pharmacol Sci משנת 1985). דה-סיאליזציה של ORM גם כן משפיעה על קישור תרופות, וכך לדוגמה היא מפחיתה את קישור propranolol, אך אין בה להשפיע על קישור פרוגסטרון (Wong ו-Hsia ב-Can J Biochem Cell Biol משנת 1983). המשמעות של רמות ORM מוגברות בפלזמה שמוצאים במצבי מחלה אחדים, לגבי הפרמאקו-קינטיקה של תרופות נבחנה גם בחיות טרנסגניות. Holladay וחב' דווחו בשנת 1996 ב-Drug Metab Dispos נתונים על קינטיקת steady-state של imipramine ובשנת 1998 דווחה קבוצת חוקרים זו על הפרמאקו-קינטיקה של fluoxetine בעכברים טרנסגניים המבטאים בנסיוב רמת ORM הגבוהה פי-9 מרמת ORM הנורמאלית בעכברים. | ||
| + | |||
| + | ==הביטוי הכבדי של ORM והרגולציה של החלבון== | ||
| + | למרות ש-ORM הוא חלבון פלזמה המסונתז בכבד בעיקרו, יש גם ביטוי חוץ-כבדי של הגן המקודד לחלבון זה. הייצור בכבד של חלבוני acute phase גדל דרמטית בתגובה לגירויים של עקה (stress) כגון טראומה פזית כניתוח או פציעה, זיהומים בקטריאליים, או גירויים דלקתיים לא מוגדרים כמו לדוגמה הזרקה תת-עורית של turpentine {{כ}}(Fey ו-Füller ב-Mol Biol Med משנת 1987). חלבוני acute phase מתחלקים ל-2 סוגים עיקריים בתלות בתגובתם לציטוקינים. אלה הנחשבים כ-type 1 כוללים את ORM, serum amyloid A, C-reactive protein, הפטוגלובין, complement C3 ו-hemopexin. כל אלה מווסתים על ידי IL-1, IL-6 וכן על ידי גלוקו-קורטיקואידים. ORM מופיע בבעלי חוליות רבים, ושיעור עלייתו בתגובה לפגיעה סיסטמית או עקה, משתנה בין המינים השונים, והוא אף יכול להיות מוגבר ב-2 סדרי גודל מעל רמתו ברגיעה (Cooper ב-J Biol Chem משנת 1986). לדוגמה, בחולדות, עכברים וארנבות רמת ORM בפלזמה יכולה לעלות פי-10 עד פי-200 תוך 24 שעות לאחר השרייה ניסויית של דלקת. יש גם מחקר של Wigmore וחב' ב-Am J PhysioL משנת 1997, שהראה שאינטרלויקין נוסף, IL-8, מגביר אף הוא יצירת ORM בהפטוציטים מבודדים. | ||
| + | |||
| + | בנוסף לתווכים דלקתיים, ביטויו של הגן של ORM יכול להיות מושפע מסדרה של מולקולות אחרות. נמצא שהחדרה חוזרת של phenobarbital שהוא משרה חזק של אנזימים בכבד (בעיקר ציטוכרומים P4502B1 ו-P4502B2) הקשורים למטבוליזם של תרופות, מגבירה את רמות ORM בנסיוב של כלבים וחולדות (Lin וחב' ב-Drug Metab Dispos משנת 1987). ממצא אחר הוא טיפול in vitro בהפטוציטים מבודדים של חולדה בהורמון גדילה (GH), מעכב את ביטוי הגן של ORM ברמת תרגום הגן (Mejdoubi וחב' ב-Hepatology משנת 1999). ראוי לציין שרמת ה-mRNA של ORM בכבד גדלה באופן ניכר בחולדות שעברו כריתה של בלוטת יותרת המוח, וטיפול של חולדות אלה בהורמון הגדילה הביא להפחתת הביטוי של mRNA זה. נראה אם כן שהורמון הגדילה הוא רגולטור אנדוגני של ביטוי הגן ל-ORM. | ||
| + | |||
| + | ==הביטוי החוץ-כבדי של ORM והרגולציה של החלבון== | ||
| + | העדות הראשונה לכך שיש נוכחות של ORM גם ברקמות חוץ-כבדיות הגיעה בעקבות מחקרים על שינויים כמותיים של רמות של גליקופרוטאינים נורמאליים במחלות סרטניות (Rudman וחב' ב-Cancer Res משנת 1972, ו-Papsidero וחב' ב-Cancer Biochem Biophys משנת 1978). בשנת 1977, זיהו Twining ו-Brecher (ב-Clin Chim Acta), בשיטות אימונולוגיות, את ORM, אנטי-תרומבין III ו-α-2 macroglobulin כמרכיבים של מקטע נוזלי העליון לאחר סרכוז במהירות של 90.000g של רקמות סרטניות ונורמאליות של השד, מעי גס, קיבה ופי הטבעת, בעוד שרקמה סרטנית מהריאות הכילה רק ORM. חוקרים אחרים דווחו על גילוי ORM ברקמות נורמאליות כמו שריר הלב (Siegel וחב' ב-Lab Invest משנת 1985). Gahmberg ו-Andersson תיארו ב-1978 ב-J Exp Med משנת 1978 שנוגדנים ספציפיים כנגד ORM הגיבו עם לויקוציטים מאדם, כגון לימפוציטים, גרנולוציטים ומונוציטים. מחקרים מוקדמים אלה רק הדגימו נוכחות ORM ברקמות האמורות, אך לא הביאו הוכחות ישירות לסינתזה פעילה של גליקופרוטאין זה ברקמות חוץ כבדיות בריאות או פתולוגיות. | ||
| + | |||
| + | עדות לסינתזה פעילה של ORM ברקמות חוץ-כבדיות בתאי אפיתל של רקמת שד באדם התקבלה התקבלה על ידי Gendler וחב' ב-Cancer Res משנת 1982. רמות גבוהות של mRNA המקודד ל-ORM התגלו בשלייה בשלבי היריון ראשונים בחולדה. ביטוי זה היה מוגבל ל-decidua ברחם, והוא אובחן לראשונה בערך יום אחד לאחר ההשרשה, כאשר השגשוג של ה-decidua נמצא כבר בשלב מתקדם (Thomas וחב' בJ Biol Chem- משנת 1989). חוקרים שוודים בחנו את האפשרות שתאי אנדותל מייצרים ORM{{כ}} (Sörensson וחב' ב-American J Physiol משנת 1999). על ידי שימוש בתרביות ראשוניות של תאי אנדותל מיקרו-וסקולאריים מרקמה דרמאלית באדם, הדגימו חוקרים אלה ש-mRNA של ORM והחלבון עצמוהיו מבוטאים בתאי האפיתל באופן קונסטיטוטיבי. כמו סיפקו מחקרים עדות לכך שגרנולוציטים של אדם בתרבית כשורת התאים המונובלסטואידית THP-1, וכן מונוציטים מאדם סנתזו והפרישו ORM, בה בשעה שלימפוציטים T ו-B לא עשו כן (Shibata וחב' ב-Microbiol Immunol משנת 1984, ו-Fournier וחב' ב-J Immunol משנת 1999). | ||
| + | |||
| + | מחקרים אלה הצביעו על כך ש-ORM יכולים להיות מיוצרים על ידי מספר תאים מרקמות שונות שאינם הפטוציטים. Dube וחב' הראו ב-Prostate משנת 1989, על ידי שימוש בטכניקת Immunoperoxidase ש-ORM ממוקם גם בתאי אפיתל של בלוטת הערמונית, בגברים על מחלה דלקתית של הבלוטה. Kalmovarin וחב' דווחו ב-Inflammation משנת 1991, שהזרקה תוך-פריטונאלית של LPS בקטריאלי לחולדות, השרתה סינתזה של mRNA של ORM רק בכליה, אך לא ברקמות חוץ-הפטיות אחרות כמו התימוס, הטחול, האשכים, רקמת השומן, המוח, הלב, והריאות. מחקר אחר סיפק הוכחה שגלוקו-קורטיקואידים השרו את ביטוי הגן של ORM בתאי אפיתל של מעי חולדה המופיעים כשורת תאים IEC-6, וכן ש-TGFβ גרם לתגובה אנטגוניסטית לפעילות של השריית יצירתORM על ידי גלוקו-קוטיקואידים (Boudreau וחב' ב-DNA Cell Biol משנת 1998). | ||
| + | |||
| + | נתונים לגבי הביטוי של ORM בריאות שנויים במחלוקת. חלבון זה התגלה ברקמות סרטניות של הריאה (Twining ו-Brecher ב-Clin Chim Acta משנת 1977), והביטוי של הגן ל-ORM הושרה בריאות אדם וחולדה בתהליך דלקתי (Crestani וחב' ב-J Immunol משנת 1998). ההשערה שצמחה מנתונים אלה הייתה שבהיעדר דלקת סיסטמית, ביטוי מקומי של חלבון אימונו-מודולטורי דוגמת ORM, עשוי להיות במיוחד רלוונטי בחלל האלבאולארי האחראי לשימור התפקוד הריאתי. אכן, ריכוז ORM נמצא בריאות עם דלקת חריפה או בריאות פיברוטיות, אך לא ברקמות של ריאות בריאות מאדם או מחולדה. אכן, המחקר המצוטט האחרון מצא שהחדרה מקומית לריאות של LPS, או הזרקה סיסטמית של LPS או של דקסמתאזון לפריטונאום שגרמה לדלקת חריפה, הגבירה את ביטוי הגן ל-ORM בריאות. התפקיד של תאי אפיתל אלבאולאריים type II ושל מקרופאגים אלבאולאריים בביטוי של ORM בריאות, הודגם in vivo ו-in vitro. מחקרים בחולדות הראו שבניגוד להפטוציטים , כמעט ולא מוצאים בריאות ביטוי קונסטיטוטיבי של ORM. יחד עם זאת, לאחר הדגרה עם דקסמתאזון, הושרתה הגברה ניכרת בביטוי ORM בריאות, כאשר הציטוקין IL1beta מסייע להשפעה האמורה של דקסמתאזון. | ||
| + | |||
| + | בנוסף לציטוקינים, תוצר דלקתי נוסף של של מקרופאגים, התווך הליפידי PGE2, גם כן הגביר את רמות mRNA של ORM במאקרופאגים האלבאולאריים. נמצא שבתאים מקרופאגים הגביר PGE2 את רמות cAMP התוך-תאיות, וכן הגביר את פעילות האנזים protein kinase A (על פי Fournier וחב' ב-J Immunol משנת 1995). כמו כן נמצא ש-PGE2 הוא המטבוליט של חומצה אראכידונית המועדף בהפרשה ממקרופאגים בתהליכי דלקת, בעוד שבמצבים תקינים תאים מיצרים בעיקר PGD2, שאינו מגביר את פעילות האנזים protein kinase A, ואינו מגביר את ביטוי הגן ל-ORM (על פי Fournier וחב' ב-J Biol Chem משנת 1997). | ||
| + | |||
| + | ==הוראות לביצוע הבדיקה== | ||
| + | הבדיקה מתבצעת בנסיוב, ולשם כך יש לגדם את הדם למבחנה כימית (פקק אדום או צהוב), וגם מבחנת ג'ל מקובלת. יש לסרכז את הדם לאחר קרישתו, ולשלוח למעבדה מקורר או להקפיא אם הבדיקה אינה מתבצעת מידית. יש להעדיף נטילת דם לאחר צום של 8-10 שעות. יש לפסול דגימה שהגיעה למעבדה בטמפרטורת החדר מעל 6 שעות מלקיחת הדם. דם המוליטי באופן מתון או ליפמי אינם מפריעים לביצוע הבדיקה. הבדיקה יציבה כאשר היא מקוררת למשך 7 ימים, או כאשר היא בהקפאה למשך 90 יום. | ||
| + | |||
| + | |||
| + | ==ראו גם== | ||
| + | * [[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | ||
| + | * [[בדיקות ביוכימיות|בדיקות מעבדה - בדיקות ביוכימיות]] | ||
| + | * [[סמני דלקת|בדיקות מעבדה - סמני דלקת]] | ||
| + | |||
| + | |||
| + | {{ייחוס בן עמי}} | ||
| + | |||
| + | |||
| + | [[קטגוריה: בדיקות מעבדה - בדיקות ביוכימיות]] | ||
| + | [[קטגוריה: בדיקות מעבדה: כימיה בדם]] | ||
| + | [[קטגוריה:בדיקות מעבדה - מדדי דלקת]] | ||
גרסה אחרונה מ־09:18, 18 ביוני 2017
| מדריך בדיקות מעבדה | |
| Orosomucoid | |
|---|---|
| שמות אחרים | ORM ;AGP1 ;AGP-A ;HEL-S-153w ,α-1-acid glycoprotein |
| מעבדה | כימיה בדם |
| תחום | חלבון acute phase הפעיל במצבי דלקת ומודולציה של התגובה החיסונית |
| טווח ערכים תקין | בגברים בטווח הגילים 5-50 שנה-0.6-1.2 גרם /ליטר, בנשים באותו טווח גילים-0.4-1.0 גרם/ליטר. מעל גיל 50 שנה ערכי ORM בגברים ובנשים-0.8-1.2 גרם/ליטר. בילדים מתחת גיל שנה הערכים נמוכים יותר |
| יוצר הערך | פרופ' בן-עמי סלע |
- מטרת הבדיקה
רמת ORM משמשת לאבחון וניטור של מחלות מעי דלקתיות, והערכה של מחלת קרוהן, בעיקר בשלביה המוקדמים. רמות מוגברות של ORM כרוכות בתגובת acute phase לדלקת, זיהומים, נזק רקמתי וממאירות, כאשר רמות מופחתות של ORM מופיעות במהלך היריון ומחלת כבד כרונית.
החלבון ORM
החלבון ORM התגלה בעת ובעונה אחת על ידי Schmid במחצית המאה הקודמת (J Am Chem Soc משנת 1950), ו-Winzler וחב' ב-J Biol Chem משנת 1950). התברר עד מהרה שמדובר בחלבון מאוד בלתי רגיל הן בנקודה האיזואלקטרית המאוד נמוכה שלו (pI 2.8-3.8) וכן בשל האחוז המאוד גבוה של סוכרים המהווה 45% מכלל המולקולה. משך 30 שנה נחשב ORM כגליקופרוטאין עם אחוז הסוכר הגבוה ביותר, עד לגילויו בשנות ה-80 של ה-galactoglycoprotein המכיל 76% סוכר (Schmid וחב' ב-J Biol Chem משנת 1980). למרות מחקרים לא מעטים על ORM במשך למעלה מ-60 שנה, תפקידו הביולוגי אפוף סימני שאלה. יחד עם זאת, מספר פעילויות פיזיולוגיות פוטנציאליות יוחסו ל-ORM כגון מספר השפעות אימונו-מודולטוריות, יכולתו לקשור תרופות בעלות מטען שלילי, כמו גם יכולתו לקשור הורמונים סטרואידיים, מה שהביא להשערה ש-ORM יכול להיות חבר במשפחת ה-lipocalin. בנוסף, ריכוזי ORM בנסיוב יציבים בתנאים פיזיולוגיים (כ-1 גרם/ליטר באדם, ו-0.2 גרם/ליטר בחולדה), אך עולים פי כמה בריאקציות acute phase, ולכן הוא נחשב לאחד ממגיבי acute phase הבולטים.
Orosomucoid (להלן ORM) הידוע גם כ-α-1-acid glycoprotein (להלן α1AGP) הוא חלבון של הפאזה החריפה (acute phase protein), ששייך למשפחת plasma globulins α1. הגליקופרוטאין ORM מאופנן על ידי החלבון ORM מסונתז בעיקר בהפטוציטים וריכוזו התקין בפלזמה במבוגרים הוא 0.6-1.2 גרם/ליטר, והוא מהווה 1-3% מכלל חלבוני הפלזמה (Colombo וחב' ב-Clin Pharmacol Ther משנת 2006. בהיותו acute phase protein רמתו בפלזמה עולה משמעותית במצבי דלקת, בכוויות, בנשאי HIV ובשימוש בתרופות מסוימות.
התפקיד הפיזיולוגי היחיד המוסכם לגבי ORM, הוא לשמש נשא של חומרים ליפופיליים בסיסיים או כאלה שהם ניטרליים מבחינת מטענם. ברפואה, ORM ידוע כנשא עיקרי של תרופות בסיסיות (הטעונים מטען שלילי), בעוד שאלבומין הוא הנשא של תרופות חומציות (שמטענן החשמלי שלילי) או הניטרליות מבחינת מטענן. ORM נשא של סטרואידים, של פרוגסטרון וויטמין B12 ושל מעכבי פרוטאזות (Urien וחב' ב-Biochem J משנת 1991). הזדקנות גורמת לעלייה קלה ביותר ברמת ORM, ואכן ההשפעה של שינויים קלים אלה על הקישור של תרופות שונות ל-ORM זעירה (Barash ב- Clinical Anesthesia משנת 209). ל-ORM יש אינטראקציה מורכבת עם הגורמים להומאוסטאזיס של בלוטת התריס: ORM בריכוזים נמוכים מעודד את הקולטן ל-TSH ולהצטברות התוך-תאית של c-AMP. לעומת זאת, ORM בריכוזים גבוהים מעכבים את פעילות TSH (Zimmermann-Belsing וחב' ב- Molecular and Cellular Endocrinology משנת 2002, ו-Dietrich וחב' ב- J Thyroid Resמשנת 2012).
ORM זוהה כאחד מתוך ארבעה סמנים שימושיים בצירקולציה להערכה של הסיכון לתמותה מסיבה כלשהי במהלך 5 השנים הבאות, כאשר יתר הסמנים הם רמת אלבומין, רמת ציטראט וגודל החלקיק של very low-density lipoprotein (Fischer וחב' ב- PLos Med משנת 2014). ORM גדל בריכוזו בצהבות חסימתיות, ופוחת בריכוזו בצהבת הפאטו-תאית ובזיהומי מעי.
המבנה של ORM
משקלו המולקולארי של ORM הוא 41-43 אלף דלטון, אם כי יש הגורסים תחומי משקל מולקולארי רחבים יותר, של 37-54 אלף דלטון, וזאת כתוצאה משיעורי גליקוזילציה שונים המתבטאים בתכולה משתנה של המרכיב הסוכרי של המולקולה. כל חמש השרשרות הסוכריות העשירות בחומצה סיאלית, מחוברות לשלד הפפטידי של ORM בקשרי N-linkage (Yoshima וחב' ב-J Biol Chem משנת 1981). ORM גובש כמלח עופרת ליצירת דו-פירמידות בעלות 6 צלעות. נמצא של-ORM יש מסיסות גבוהה במיוחד במים ובממיסים אורגניים קוטביים, מה שמוסבר על ידי התכולה הגבוהה של סוכרים במבנה המולקולה. באדם, הקודמן ORM1 היא שרשרת פוליפפטידית אחת עם 201 חומצות אמינו, כאשר בקצה ה-N טרמינאלי שלה מופיע signal peptide בן 18 חומצות אמינו המבוקע בתהליך העיבוד של החלבון, ומוליך לחלבון המונומרי הבשל המכיל באדם 183 חומצות אמינו או 187 חומצות אמינו בחולדה, עם שני קשרים דיסולפידים באדם, וקשר דיסולפידי בודד בחולדה. יש הבדל של 22 חומצות אמינו בין 2 הואריאנטים ORM1 ו-ORM2 המקודדים על ידי 2 גנים פולימורפיים (ORM1 ו-ORM2) שמיקומם בכרומוזום 9 בעמדה q31-qter. בנוסף, בעמדות 32 ו-47 ייתכן שחלוף של חומצות האמינו, מה שמשקף כנראה פולימורפיות באוכלוסייה האנושית. נתון מעניין נוסף הוא דרגת ההומולוגיה הגבוהה בין ORM לבין מולקולת IgG מאדם (Schmid וחב' ב-Biochemistry משנת 1973), וכן בין ORM לבין הקולטן של EGF (Toh וחב' ב-Nature משנת 1985).
כפי שרואים בתרשים למטה לגבי המבנה של אתר הקישור של ORM (Filip וחב' ב-Expert Opin drug Metabol Toxicol משנת 2013), נמצא 2 שרשרות צדדיות טעונות חיובית (Arg68 ו-Arg90) הממוקמות מצדו האחד של הגומחה (cleft) של אתר הקישור, כאשר שאר הגומחה בעיקרה אינה קוטבית. החלק הפנימי של שקע זה מקביל לשרשרת צדדית בו משחקים תפקיד חיוני השיירים Tyr27, Phe49, Phe51, Leu62, Leu79, Ile88, Leu101, Tyr110, Leu112 ו-Tr127. החלק התחתון של הגומחה נוצר על ידי Ile13, Leu18 ו-Val81. בתרשים מצוינים חמשת שיירי האספרגין (Asn), אליהם נקשרות חמשת השרשרות הסוכריות. מולקולת ORM בחולדה היא בעלת הומולוגיה של 59% ברצף חומצות האמינו לזו של האדם. עם זאת, המקטע (domain) התפקודי של ORM משומר ביותר בין אדם, חולדה ועכבר.
החלק הסוכרי של ORM
המרכיב הסוכרי של ORM נחקר היטב שכן זהו אחד הגליקופרוטאינים הבודדים המכיל שרשרות סוכריות עם הסתעפויות טטרה-אנטנריות, תלת-אנטנריות ודו-אנטנריות, כאשר כל חמשת השרשרות הצדדיות מחוברות לשייר אספרגין בעמדות 15, 38, 54, 75 ו-85, (תרשים למטה):
יתרה מכך, סוכר הקצה של השרשרות הסוכריות ב-ORM הוא חומצה סיאלית או N-acetyl-neuraminic acid , מהווה 10-12% מכלל הסוכרים במולקולה, ובגלל מטענו השלילי מתקבלת הנקודה האיזואלקטרית הנמוכה של המולקולה. סוכר טרמינאלי זה יכול להיות קשור בקשרי α2-3 או α2-6 לסוכר galactose. גם הסוכר fucose הוא סוכר קצה ב-ORM, שיכול להיות קשור בקשר α1-3 לסוכר GlcNAc. התגלו 12-20 גליקופורמים של ORM בנסיוב תקין, אם כי במצבים פתולוגיים יש עדיפות להופעת גליקאנים עם מבנה של שרשרת סוכרית דו-אנטנארית, שניתן לגלותם לדוגמה בשלב המוקדם של ריאקציית acute phase. נמצא שהציטוקינים IL-1, IL-6 ו-TNF-α וכן גלוקו-קורטיקואידים קשורים למודיפיקציות אלו במבנה הסוכרי של ORM (Van Dijk ב-Glycoconj J משנת 1995). השינויים בגליקוזילציה של מולקולת ORM אינם מוגבלים רק למצבים חריפים של דלקת, אלא מופיעים במגוון של מצבים פתו-פיזיולוגיים כמו הריון, דלקת מפרקים שגרונית חמורה, צמקת כבד מאלכוהוליזם, והפאטיטיס (Biou וחב' ב-Clin Chim Acta משנת 1991).
הפעילות הביולוגית של ORM
תכונות ביולוגיות רבות יוחסו ל-ORM על ידי Kremer וחב' ב-Pharmacol Rev משנת 1988: ההגנה שהוא מעניק כנגד ספסיס נאונטלי, האינטראקציה שלו עם פוספוליפידים בממברנה, יכולתו לקשור היסטמין, כמו גם לעכב צימות טסיות, כימוטקסיס של ניטרופילים, יצירת סופר-אוקסידים, והשפעתו על שגשוג לימפוציטים. ORM נחשב כגורם טבעי נוגד-דלקות ואימונו-מודולטורי בעיקר בהקשר של פעילות נוגדת המשלים (complement) והאנטי-ניטרופילית (Williams וחב' ב-Am J Physiol משנת 1997). ואמנם, הודגם הן in-vitro כמו גם in vivo ש-ORM היא מולקולה אימונו-מודולטורית: In vitro, ORM מעכב שפעול ניטרופילים (Vasson וחב' ב-Clin Chim Acta משנת 1994) ומגביר את ההפרשה של מעכב IL-1 על ידי מקרופאגים בעכבר [שהוא כנראה אנטגוניסט של הקולטן ל-IL-1 (Tilg וחב' ב-J Exp Med משנת 1993), וכמו כן מאפנן את הפרשת ציטוקינים המושרית על ידי ליפופוליסכרידים (LPS) (Boutten וחב' ב-Eur J Immunol משנת 1992). מאוחר יותר הודגם ש-ORM מגיב באופן ישיר עם LPS (Moore וחב' ב-Inflammation משנת 1997). מחקרים in vitro עם מונוציטים מאדם, הראו שהפרשת TNF-α המושרית על ידי ORM תלויה בשפעול של האנזים טירוזין קינאזה (Su וחב' ב-Immunopharmacol משנת 1999). כמו כן הוצע ש-ORM דרוש לשמור על חדירותן של קפילרות כנראה על ידי הגברת הסלקטיביות של המטען הפולי-אניוני במחסום האנדותליאלי (Curry וחב' ב-Am J Physiol משנת 1989).
In vivo, עירוי של ORM נמצא מגן על עכברים מפני הפאטיטיס וכן מפני הלם קטלני המושרה על ידי TNF-α (Libert וחב' ב-J Exp Med משנת 1994). עלתה השערה שפעילות עיכוב צימות הטסיות והיכולת של ORM לעכב כמוטקסיס של ניטרופילים ולעכב מטבוליזם חמצוני, עומדים בבסיס פעילויותיו המגוננות (Costello וחב' ב-Nature משנת 1979). כן נמצא ש-ORM מעכב באופן ספציפי אפופטוזיס המושרה על ידיTNF-α בעכברים, אך נראה שההגנה שמעניק ORM לתאים פועלת על ידי מנגנון בלתי-ישיר, שכן in vitro ORM נכשל בהגנה על תאי הפאטומה אנושיים, מפני אפופטוזיס המושרה בתאים אלה על ידי TNF-α בשילוב עם אקטינומיצין D (Van Molle וחב' ב-J Immunol משנת 1997).
הפעילות האימונו-מודולטורית של ORM נמצאה תלויה בדרגת הגליקוזילציה שלו. לדוגמה, העיכוב של שגשוג לימפוציטים תלוי בדרגת ההסתעפות של השרשרות הסוכריות של ORM (Pos וחב' ב-Inflammation משנת 1990), ועיכוב צימות הטסיות מוגבר כאשר מולקולת ORM עוברת דה-סיאליזציה. הדגמה נוספת של חשיבות השרשרות הסוכריות של ORM לפעילותו הביולוגית, מוצאים בנתון הבא: ORM עם מבנה סוכרי של sialyl Lewis X הנוצר במהלך דלקת, משדרג את הנזקים הנגרמים על ידי המשלים וכן על ידי ניטרופילים , ואילו ORM ללא המבנה הסוכרי של sialyl Lewis X אינו פועל באופן דומה (De Graaf וחב' ב-J Exp Med משנת 1993). sialyl Lewis X הוא הליגנד אליו נקשרות מולקולות הספיחה E-selectin ו-P-selectin בתהליכי הספיחה של ניטרופילים, מונוציטים או תאי T לתאי האנדותל או לטסיות במצבי דלקת (Lasky ב-Science משנת 1992).
בשיטת surface plasmon resonance spectroscopy נמצא ש-ORM מאנשים עם דלקת חריפה, בו יש תכולה גבוהה של sialyl Lewis X, משמש כליגנד ספציפי למולקולה כימרית של E-selectin-IgG. נמצא שאוליגו-סככרידים עם סיאליזציה מלאה הגנו כנגד נזק לריאות בחולדות in vivo (Mulligan וחב' ב- J Exp Med משנת 1993). נראה אם כן, שהגדלת החלק של sialyl Lewis X המושרה על ידי מצבי דלקת בקומפלקס הגליקני של ORM, מייצגת מנגנון של עיכוב על ידי משוב-חוזר של חדירת גרנולוציטים לתוך הרקמות הדלקתיות. במקובץ, נתונים אלה מראים שהשרשרות הסוכריות של ORM הן בעלת תפקיד קריטי בפעילויות האימונו-מודולטוריות של גליקופרוטאין זה.
קישור של תרופות ל-ORM
אלבומין, ליפופרוטאין ו-ORM הם החלבונים החשובים ביותר בהיבט של קישור תרופות בפלזמה, מה שחיוני מאוד לתכונות הפרמאקו-קינטיות של תרופות אלה. שינויים ברמת ORM מתרחשים בתרחישים דלקתיים, מה שיכול לשנות את ריכוזי התרופות החופשיות בפלזמה בלי לשנות את סך רמתן של תרופות אלו בפלזמה. לפיכך, רמת התרופה החופשית תשקף באופן נאמן יותר את עוצמת ההשפעה הפארמקולוגית של התרופה. בגין תכונותיו הביופיזיות של ORM, הוא קושר בעיקר תרופות בעלות מטען חשמלי בסיסי, או כאלה הניטראליות מבחינת מטענן החשמלי כמוdiazepam ו-carbamazepine. ל-ORM יש יכולת לקשור תרופות בסיסיות כמו טמוקסיפן ו-propanolol (Albani וחב' ב-Br J Clin Pharmacol משנת 1984). כמו כן יכול ORM לקשור vanilloids דוגמת capsaicin ו-resiniferatoxin ( Szallai וחב' ב-J Pharmacol Exp Ther משנת 1992), הפארין, IgG3, סרוטונין, PAF או platelet activating factor (McNamara וחב' ב-Biochem Pharmacol משנת 1986), מלטונין (Morin וחב' ב-Pharmacology משנת 1997), והיסטמין (Chachaj וחב' ב-Arch Immunol Ther Exp משנת 1980).
ואריאנטים של ORM הם בעלי כושר קישור שונה לתרופות. לדוגמה, atazanavir מעדיף את הואריאנט ORM1*F1, בעוד ש-lopinavir ו-indinavir מעדיפים את הואריאנט ORM1*S (Barrail-Tran וחב' ב-Antimicrob Sgents Chemother משנת 2010). יתרה מכך, המציאות של 2 צורות של אותו חלבון בדם, משפיעה על הזיקה של קישור תרופות. נמצא שתרופות דוגמת מתאדון, disopyramide, deramciclane, propafenone ו-amitriptyline נקשרות באופן סלקטיבי ל-ORM2, בניגוד ל-קומאדין, prazosin, imatinib,quinidine ו-dipyridamole הנקשרים באופן מועדף ל-ORM1.
באופן מעניין, ORM קושר ונושא מולקולות הקשורות למודולציה של ביטוי הגן המקודד ל- ORM עצמו, כמו phorbol esters, וכן תרופות חומציות כמו phenobarbital (Schley ו-Mueller ב-Pharmacopsychiatry משנת 1983), חומצה רטינואית (Israili ו-El-Attar ב-Clin Pharmacol Ther משנת 1983) וסטרואידים דוגמת קורטיזול (Grimaldi וחב' ב-Prog Clin Biol Res משנת 1989). תכונתו של ORM לשאת סטרואידים הודגמה כבר בסוף שנות ה-60 על ידי Westphal וחב' ב-Biochim Biophys Acta משנת 1968, וכיום כבר ידוע ש-ORM מסוגל גם לשאת סטרואידים סינטתיים כמו mifepristone. בעוד שלסטרואידים יש כנראה אתר קישור יחיד על פני ORM, הרי שלגבי אסטרדיול יש ל-ORM כנראה עד 7 אתרי קישור, ול-phenobarbital יש ל-ORM רק 2 אתרי קישור. כמו כן נמצא ש-ORM קושר ונושא חוסמי-β, חומרי הרדמה מקומית, תרופות ממשפחת phenothiazine, חוסם טירוזין קינאזה כמו imatinib וכן מעכבי HIV protease.
למרות שהקישור של תרופות ל-ORM היא בעיקר הידרופובי, ישנם מספר נתונים המצביעים גם על אינטראקציה אלקטרוסטטית, ומחקרים אחדים דווחו על כל שבפלזמה קישור התרופות ל-ORM הוא סטראו-סלקטיבי, בעיקר כשמדובר בתרופות בעלות מטען חשמלי בסיסי, וכן שקישור התרופות בפלזמה עולה עם העלייה ב-pH (Ponganis ו-Stanski ב-J Pharmacol Sci משנת 1985). דה-סיאליזציה של ORM גם כן משפיעה על קישור תרופות, וכך לדוגמה היא מפחיתה את קישור propranolol, אך אין בה להשפיע על קישור פרוגסטרון (Wong ו-Hsia ב-Can J Biochem Cell Biol משנת 1983). המשמעות של רמות ORM מוגברות בפלזמה שמוצאים במצבי מחלה אחדים, לגבי הפרמאקו-קינטיקה של תרופות נבחנה גם בחיות טרנסגניות. Holladay וחב' דווחו בשנת 1996 ב-Drug Metab Dispos נתונים על קינטיקת steady-state של imipramine ובשנת 1998 דווחה קבוצת חוקרים זו על הפרמאקו-קינטיקה של fluoxetine בעכברים טרנסגניים המבטאים בנסיוב רמת ORM הגבוהה פי-9 מרמת ORM הנורמאלית בעכברים.
הביטוי הכבדי של ORM והרגולציה של החלבון
למרות ש-ORM הוא חלבון פלזמה המסונתז בכבד בעיקרו, יש גם ביטוי חוץ-כבדי של הגן המקודד לחלבון זה. הייצור בכבד של חלבוני acute phase גדל דרמטית בתגובה לגירויים של עקה (stress) כגון טראומה פזית כניתוח או פציעה, זיהומים בקטריאליים, או גירויים דלקתיים לא מוגדרים כמו לדוגמה הזרקה תת-עורית של turpentine (Fey ו-Füller ב-Mol Biol Med משנת 1987). חלבוני acute phase מתחלקים ל-2 סוגים עיקריים בתלות בתגובתם לציטוקינים. אלה הנחשבים כ-type 1 כוללים את ORM, serum amyloid A, C-reactive protein, הפטוגלובין, complement C3 ו-hemopexin. כל אלה מווסתים על ידי IL-1, IL-6 וכן על ידי גלוקו-קורטיקואידים. ORM מופיע בבעלי חוליות רבים, ושיעור עלייתו בתגובה לפגיעה סיסטמית או עקה, משתנה בין המינים השונים, והוא אף יכול להיות מוגבר ב-2 סדרי גודל מעל רמתו ברגיעה (Cooper ב-J Biol Chem משנת 1986). לדוגמה, בחולדות, עכברים וארנבות רמת ORM בפלזמה יכולה לעלות פי-10 עד פי-200 תוך 24 שעות לאחר השרייה ניסויית של דלקת. יש גם מחקר של Wigmore וחב' ב-Am J PhysioL משנת 1997, שהראה שאינטרלויקין נוסף, IL-8, מגביר אף הוא יצירת ORM בהפטוציטים מבודדים.
בנוסף לתווכים דלקתיים, ביטויו של הגן של ORM יכול להיות מושפע מסדרה של מולקולות אחרות. נמצא שהחדרה חוזרת של phenobarbital שהוא משרה חזק של אנזימים בכבד (בעיקר ציטוכרומים P4502B1 ו-P4502B2) הקשורים למטבוליזם של תרופות, מגבירה את רמות ORM בנסיוב של כלבים וחולדות (Lin וחב' ב-Drug Metab Dispos משנת 1987). ממצא אחר הוא טיפול in vitro בהפטוציטים מבודדים של חולדה בהורמון גדילה (GH), מעכב את ביטוי הגן של ORM ברמת תרגום הגן (Mejdoubi וחב' ב-Hepatology משנת 1999). ראוי לציין שרמת ה-mRNA של ORM בכבד גדלה באופן ניכר בחולדות שעברו כריתה של בלוטת יותרת המוח, וטיפול של חולדות אלה בהורמון הגדילה הביא להפחתת הביטוי של mRNA זה. נראה אם כן שהורמון הגדילה הוא רגולטור אנדוגני של ביטוי הגן ל-ORM.
הביטוי החוץ-כבדי של ORM והרגולציה של החלבון
העדות הראשונה לכך שיש נוכחות של ORM גם ברקמות חוץ-כבדיות הגיעה בעקבות מחקרים על שינויים כמותיים של רמות של גליקופרוטאינים נורמאליים במחלות סרטניות (Rudman וחב' ב-Cancer Res משנת 1972, ו-Papsidero וחב' ב-Cancer Biochem Biophys משנת 1978). בשנת 1977, זיהו Twining ו-Brecher (ב-Clin Chim Acta), בשיטות אימונולוגיות, את ORM, אנטי-תרומבין III ו-α-2 macroglobulin כמרכיבים של מקטע נוזלי העליון לאחר סרכוז במהירות של 90.000g של רקמות סרטניות ונורמאליות של השד, מעי גס, קיבה ופי הטבעת, בעוד שרקמה סרטנית מהריאות הכילה רק ORM. חוקרים אחרים דווחו על גילוי ORM ברקמות נורמאליות כמו שריר הלב (Siegel וחב' ב-Lab Invest משנת 1985). Gahmberg ו-Andersson תיארו ב-1978 ב-J Exp Med משנת 1978 שנוגדנים ספציפיים כנגד ORM הגיבו עם לויקוציטים מאדם, כגון לימפוציטים, גרנולוציטים ומונוציטים. מחקרים מוקדמים אלה רק הדגימו נוכחות ORM ברקמות האמורות, אך לא הביאו הוכחות ישירות לסינתזה פעילה של גליקופרוטאין זה ברקמות חוץ כבדיות בריאות או פתולוגיות.
עדות לסינתזה פעילה של ORM ברקמות חוץ-כבדיות בתאי אפיתל של רקמת שד באדם התקבלה התקבלה על ידי Gendler וחב' ב-Cancer Res משנת 1982. רמות גבוהות של mRNA המקודד ל-ORM התגלו בשלייה בשלבי היריון ראשונים בחולדה. ביטוי זה היה מוגבל ל-decidua ברחם, והוא אובחן לראשונה בערך יום אחד לאחר ההשרשה, כאשר השגשוג של ה-decidua נמצא כבר בשלב מתקדם (Thomas וחב' בJ Biol Chem- משנת 1989). חוקרים שוודים בחנו את האפשרות שתאי אנדותל מייצרים ORM (Sörensson וחב' ב-American J Physiol משנת 1999). על ידי שימוש בתרביות ראשוניות של תאי אנדותל מיקרו-וסקולאריים מרקמה דרמאלית באדם, הדגימו חוקרים אלה ש-mRNA של ORM והחלבון עצמוהיו מבוטאים בתאי האפיתל באופן קונסטיטוטיבי. כמו סיפקו מחקרים עדות לכך שגרנולוציטים של אדם בתרבית כשורת התאים המונובלסטואידית THP-1, וכן מונוציטים מאדם סנתזו והפרישו ORM, בה בשעה שלימפוציטים T ו-B לא עשו כן (Shibata וחב' ב-Microbiol Immunol משנת 1984, ו-Fournier וחב' ב-J Immunol משנת 1999).
מחקרים אלה הצביעו על כך ש-ORM יכולים להיות מיוצרים על ידי מספר תאים מרקמות שונות שאינם הפטוציטים. Dube וחב' הראו ב-Prostate משנת 1989, על ידי שימוש בטכניקת Immunoperoxidase ש-ORM ממוקם גם בתאי אפיתל של בלוטת הערמונית, בגברים על מחלה דלקתית של הבלוטה. Kalmovarin וחב' דווחו ב-Inflammation משנת 1991, שהזרקה תוך-פריטונאלית של LPS בקטריאלי לחולדות, השרתה סינתזה של mRNA של ORM רק בכליה, אך לא ברקמות חוץ-הפטיות אחרות כמו התימוס, הטחול, האשכים, רקמת השומן, המוח, הלב, והריאות. מחקר אחר סיפק הוכחה שגלוקו-קורטיקואידים השרו את ביטוי הגן של ORM בתאי אפיתל של מעי חולדה המופיעים כשורת תאים IEC-6, וכן ש-TGFβ גרם לתגובה אנטגוניסטית לפעילות של השריית יצירתORM על ידי גלוקו-קוטיקואידים (Boudreau וחב' ב-DNA Cell Biol משנת 1998).
נתונים לגבי הביטוי של ORM בריאות שנויים במחלוקת. חלבון זה התגלה ברקמות סרטניות של הריאה (Twining ו-Brecher ב-Clin Chim Acta משנת 1977), והביטוי של הגן ל-ORM הושרה בריאות אדם וחולדה בתהליך דלקתי (Crestani וחב' ב-J Immunol משנת 1998). ההשערה שצמחה מנתונים אלה הייתה שבהיעדר דלקת סיסטמית, ביטוי מקומי של חלבון אימונו-מודולטורי דוגמת ORM, עשוי להיות במיוחד רלוונטי בחלל האלבאולארי האחראי לשימור התפקוד הריאתי. אכן, ריכוז ORM נמצא בריאות עם דלקת חריפה או בריאות פיברוטיות, אך לא ברקמות של ריאות בריאות מאדם או מחולדה. אכן, המחקר המצוטט האחרון מצא שהחדרה מקומית לריאות של LPS, או הזרקה סיסטמית של LPS או של דקסמתאזון לפריטונאום שגרמה לדלקת חריפה, הגבירה את ביטוי הגן ל-ORM בריאות. התפקיד של תאי אפיתל אלבאולאריים type II ושל מקרופאגים אלבאולאריים בביטוי של ORM בריאות, הודגם in vivo ו-in vitro. מחקרים בחולדות הראו שבניגוד להפטוציטים , כמעט ולא מוצאים בריאות ביטוי קונסטיטוטיבי של ORM. יחד עם זאת, לאחר הדגרה עם דקסמתאזון, הושרתה הגברה ניכרת בביטוי ORM בריאות, כאשר הציטוקין IL1beta מסייע להשפעה האמורה של דקסמתאזון.
בנוסף לציטוקינים, תוצר דלקתי נוסף של של מקרופאגים, התווך הליפידי PGE2, גם כן הגביר את רמות mRNA של ORM במאקרופאגים האלבאולאריים. נמצא שבתאים מקרופאגים הגביר PGE2 את רמות cAMP התוך-תאיות, וכן הגביר את פעילות האנזים protein kinase A (על פי Fournier וחב' ב-J Immunol משנת 1995). כמו כן נמצא ש-PGE2 הוא המטבוליט של חומצה אראכידונית המועדף בהפרשה ממקרופאגים בתהליכי דלקת, בעוד שבמצבים תקינים תאים מיצרים בעיקר PGD2, שאינו מגביר את פעילות האנזים protein kinase A, ואינו מגביר את ביטוי הגן ל-ORM (על פי Fournier וחב' ב-J Biol Chem משנת 1997).
הוראות לביצוע הבדיקה
הבדיקה מתבצעת בנסיוב, ולשם כך יש לגדם את הדם למבחנה כימית (פקק אדום או צהוב), וגם מבחנת ג'ל מקובלת. יש לסרכז את הדם לאחר קרישתו, ולשלוח למעבדה מקורר או להקפיא אם הבדיקה אינה מתבצעת מידית. יש להעדיף נטילת דם לאחר צום של 8-10 שעות. יש לפסול דגימה שהגיעה למעבדה בטמפרטורת החדר מעל 6 שעות מלקיחת הדם. דם המוליטי באופן מתון או ליפמי אינם מפריעים לביצוע הבדיקה. הבדיקה יציבה כאשר היא מקוררת למשך 7 ימים, או כאשר היא בהקפאה למשך 90 יום.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק