הבדלים בין גרסאות בדף "תסמונת מרפן - Marfan syndrome"
יאיר שוורץ (שיחה | תרומות) (דף חדש: {{ערך בבדיקה}} תסמונת מרפן היא מחלה של רקמת חיבור עם שכיחות של ל-1/4000. התורשה היא אוטוסומלית דומיננטית ע...) |
|||
| (59 גרסאות ביניים של 4 משתמשים אינן מוצגות) | |||
| שורה 1: | שורה 1: | ||
| − | {{ | + | {{מחלה |
| + | |תמונה=[[קובץ:Myxomatous aortic valve.jpg|300px]] | ||
| + | |כיתוב תמונה=Micrograph demonstrating myxomatous degeneration of the aortic valve, a common manifestation of Marfan syndrome | ||
| + | |שם עברי=תסמונת מרפן | ||
| + | |שם לועזי=Marfan syndrome | ||
| + | |שמות נוספים=Marfan's syndrome | ||
| + | |ICD-10={{ICD10|Q|87|4|q|80}} | ||
| + | |ICD-9={{ICD9|759.82}} | ||
| + | |MeSH={{MeSH|D008382}} | ||
| + | |יוצר הערך=ד"ר אברהם מתתיהו | ||
| + | |אחראי הערך= | ||
| + | }} | ||
| + | '''תסמונת מרפן''' (Marfan syndrome) היא מחלה של רקמת חיבור. התורשה היא אוטוזומלית דומיננטית (Autosomal dominant) עם העברה מלאה אך הביטוי הקליני משתנה בחומרתו אפילו בתוך המשפחה. | ||
| + | למחלה יש תסמינים רבים אך המעורבות של הלב וכלי הדם היא זו שעלולה לגרום למוות מוקדם. ניתן בקלות לטעות ולא לאבחן ילדים במחשבה כי הם "פשוט" ילדים גבוהים או שחקני כדורסל, מבלי להתייחס לפתולוגיה הקרדיווסקולרית (Cardiovascular pathology) המשמעותית המסתתרת אצלם. יש חשיבות רבה לקיום מודעות מוגברת בקרב רופאי הילדים לאיתור החולים והפנייתם לבדיקות הנדרשות כדי להתחיל מוקדם בטיפול המונע ולהתערב בזמן לפני הופעה של אירועים מסכני חיים. | ||
| − | + | ==אפידמיולוגיה== | |
| − | ב-25 | + | שכיחות של מקרה אחד ל-4000. ב-25 אחוזים מהמקרים אין סיפור משפחתי והם מהווים מוטציות (Mutations) חדשות. |
| − | מבחינה גנטית המחלה נובעת ממוטציות בגן | + | |
| − | בסיבים האלסטיים. | + | ==אטיולוגיה== |
| − | החלבון מקודד | + | מבחינה גנטית המחלה נובעת ממוטציות בגן (Gene) פיברילין 1 (Fibrilin 1, FBN1). הפיברילין הוא חלבון חשוב בתוך המיקרופיברילים (Microfibrils), שהם מבנים מורכבים שמכילים חלבונים רבים וסמוכים לאלסטין (Elastin) – בסיבים האלסטיים. |
| − | מוטציה נוספת שנמצאה | + | |
| − | השינויים בחלבון (עדיין לא ברורים לגמרי כל השלבים) גורמים לפתולוגיה של שבירות ונזק לסיבים האלסטים ואיבוד תאי שריר חלק שמתבטא | + | החלבון מקודד על ידי גן בכרומוזום 15(15q21.1{{כ}} Chromosome) שהתגלה ב-1991. |
| − | מחשבה נוספת היא | + | |
| − | מאות מוטציות שונות נמצאו | + | מוטציה נוספת שנמצאה בשנת 2004 כגורמת לתמונה שיכולה להתאים למרפן נמצאת על גן בכרומוזום 3 (3p24.1) מוטציות ב-[[Transforming Growth Factor β]] Receptor Type II{{כ}} (TGFBR2). |
| − | כלומר מציאת מוטציה | + | |
| − | + | השינויים בחלבון (עדיין לא ברורים לגמרי כל השלבים) גורמים לפתולוגיה של שבירות ונזק לסיבים האלסטים ואיבוד תאי שריר חלק שמתבטא באבי העורקים (Aorta) בשכבת המדיה (Medial degeneration). | |
| − | מחלקים בדומה מעט ל | + | |
| − | במקרים שיש סיפור משפחתי של מרפן או הוכחה לקיום מוטציה | + | מחשבה נוספת היא שלפיברילין 1 והמיקרופיברילים תפקיד של בקרה על גורמי גדילה מקבוצת TGF-β שלהם יש השפעות על תפקוד והתפתחות התאים ברקמות רבות בגוף. |
| − | כאשר אין סיפור משפחתי ואין מידע על מוטציה | + | מאות מוטציות שונות נמצאו בפיברילין 1 שקשורות לתסמונת מרפן ויש עוד מאות רבות של מוטציות שקשורות למצבים דמויי מרפן, כמו ביטויים רק בשלד או רק בעיניים או רק באבי העורקים וכדומה. |
| + | |||
| + | כלומר, מציאת מוטציה בפיברילין 1 עדיין אינה אומרת שיש לחולה מרפן. | ||
| + | |||
| + | ==קליניקה== | ||
| + | בלב יש בדרך כלל מעורבות של שורש אבי העורקים עם הרחבה מתקדמת (Progressive) של אזור הסינוסים (Sinuses) של Valsalwa (תמונות 11,10). | ||
| + | |||
| + | [[קובץ:מרפן9.jpg]] | ||
| + | |||
| + | ההרחבה המתקדמת גורמת לכך שעלי מסתם אבי העורקים אינם יכולים להיסגר היטב (הרחבה של טבעת המסתם - Annulus) – ויכולה להופיע דליפה מאבי העורקים (Aortic regurgitation/insufficiency) בדרגות שונות. | ||
| + | |||
| + | כמו כן הרחבה מתקדמת של שורש אבי העורקים – עלולה להביא לקרע של אבי העורקים (Aortic aneurysm) [שיכולה לגרום למוות מטמפונדה (Tamponade) או איבוד דם] וכן יכולה להיגרם דיסקציה של אבי העורקים (Aortic dissection) (תמונות 12–14). | ||
| + | |||
| + | במקרים שיש מעורבות של המסתם הדו צניפי (Mitral valve) – יש צניחה של המסתם (Mitral prolapse) (יותר שכיח בילדים ובנשים) עם דרגות שונות של דליפה (תמונה 15). | ||
| + | |||
| + | [[קובץ:מרפן3.jpg]] | ||
| + | |||
| + | ==אבחנה== | ||
| + | |||
| + | ניתן למצוא בטכניקות של היום מוטציות בפיברילין 1 רק ב- 70 אחוזים מהחולים שיש להם ממצאים קליניים ברורים של מרפן. מכאן ניתן להבין שהאבחון הגנטי במרפן הוא עדיין בעייתי ועיקר האבחנה היא קלינית (טבלה מצורפת). | ||
| + | |||
| + | מחלקים בדומה מעט ל[[קדחת השגרון]] (Rheumatic fever) לקריטריונים עיקריים (Major criteria) במערכות שונות של הגוף שהם אופיניים יותר לתסמונת מרפן ופחות קיימים באוכלוסייה וקריטריונים משניים (Minor criteria) שהם פחות ספציפיים. | ||
| + | |||
| + | במקרים שיש סיפור משפחתי של מרפן או הוכחה לקיום מוטציה בפיברילין 1 בחולה המדובר, מספיק סימן עיקרי אחד ומעורבות נוספת פחות ספציפית במערכת אחרת. | ||
| + | כאשר אין סיפור משפחתי ואין מידע על מוטציה בפיברילין 1 יש צורך לאבחן בשני קריטריונים עיקריים ומעורבות ספציפית פחות במערכת שלישית (תמונות 1–9). | ||
בילדים – לא תמיד יש את כל הקריטריונים בהתחלה ובמקרה של חשד יש להמשיך ולעקוב ולראות מה קורה במשך השנים הבאות. חשוב לקחת סיפור משפחתי ולערוך בדיקה פיסיקלית מקיפה, לשלוח לרופא עיניים שיבדוק אפשרות של דיסלוקציה של העדשה בהרחבה מלאה של האישון ולשלוח לקרדיולוג להעריך בעזרת האקו – מעורבות לבבית. | בילדים – לא תמיד יש את כל הקריטריונים בהתחלה ובמקרה של חשד יש להמשיך ולעקוב ולראות מה קורה במשך השנים הבאות. חשוב לקחת סיפור משפחתי ולערוך בדיקה פיסיקלית מקיפה, לשלוח לרופא עיניים שיבדוק אפשרות של דיסלוקציה של העדשה בהרחבה מלאה של האישון ולשלוח לקרדיולוג להעריך בעזרת האקו – מעורבות לבבית. | ||
| − | + | [[קובץ:מרפן4.jpg|מרכז|800px]] | |
| + | |||
| + | |||
| + | [[קובץ:מרפן1.jpg]] [[קובץ:מרפן6.jpg]] | ||
| − | + | ==טיפול== | |
| − | + | ===מעקב קרדיולוגי=== | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | במסגרת המעקב הקרדיולוגי מלבד בדיקה פיסיקלית עוקבים בעזרת בדיקת אקו לב (Echocardiogram) אחרי שורש אבי העורקים [וזאת ביחס לנורמוגרמות (Nomograms) לפי משקל או שטח גוף] ותמיד גם בודקים את המסתם הדו צניפי ומחפשים גם אפשרות של דיסקציה של אבי העורקים. | |
| − | במסגרת המעקב הקרדיולוגי מלבד בדיקה פיסיקלית | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | ;לאחר בדיקת האקו הראשונה – | |
| − | + | חוזרים על האקו כעבור כ-6 חודשים – כדי לקבל רושם על קצב ההרחבה של שורש אבי העורקים – ואז בדרך כלל מעקב של אחת לשנה. כאשר שורש אבי העורקים מגיע לכ-4.5 סנטימטר (ס“מ) המעקב נעשה תכוף יותר. | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | כאשר שורש אבי העורקים מגיע ל-6-5 ס“מ, גדל בצורה ניכרת הסיכוי לקרע של אבי העורקים שעלול להביא למוות. | |
| − | |||
| − | |||
| + | כאשר יש קושי טכני להעריך את שורש אבי העורקים באקו, ניתן לעשות בדיקות כמו CTA{{כ}} (Computer Tomography Angiography) או MRA{{כ}} (Magnetic Resonance Angiogram). בדיקות אלה גם טובות יותר במקרים של חשד לדיסקציה. | ||
| − | ==טיפול | + | ===טיפול תרופתי=== |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | # [[t:Beta blocking agents - S01ED|חוסמי בטא]] (Beta blockers): הוכח שמתן חוסמי בטא בחולי מרפן באופן כללי מקטין את קצב ההרחבה של אבי העורקים, מפחית קצב התפתחות דליפה מאבי העורקים מקטין הסיכוי לדיסקציה, ל[[אי-ספיקת לב]] ולמוות (זאת כנראה על ידי האטה בדופק והפחתה בקצב השינוי בנפח ובלחץ החלק העולה של אבי העורקים בזמן התכווצות הלב) | |
| − | + | ## השפעה של חוסמי בטא טובה יותר אם מתחילים אותם מוקדם במחלה ובמינון טוב | |
| + | ## מנסים בדרך כלל לתת מינונים שיביאו לדופק בסיסי של פחות מ-70 לדקה במנוחה ופחות מ-100 במאמץ בינוני (בילדים פחות מ-80 במנוחה ופחות מ-110 במאמץ בינוני) | ||
| + | ## בילדים במיוחד יש לשים לב לתופעות לוואי כמו החמרה של [[גנחת הסימפונות]] (Asthma) או הפרעות בלימודים ואם יש בעיות ניתן להחליף ל[[t:Calcium channel blockers - C08|חוסמי סידן]] | ||
| + | # טיפול מונע ל[[דלקת פנים לב זיהומית תת-חריפה]] (Sub acute Bacterial Endocarditis, SBE) במקרים שיש דליפה במסתם אבי העורקים, במסתם הדו צניפי או צניחה של המסתם הדו צניפי יש לתת טיפול מונע | ||
| − | == | + | ===הגבלות במאמץ=== |
| − | אבחון מוקדם וטיפול נכון בחולי מרפן כבר מגיל הילדות | + | |
| − | + | יש למנוע מחולי מרפן עיסוק בספורט מגע (ספורט בו ייתכנו חבללות בחזה) וכן יש להגביל בספורט תחרותי (שבו לעיתים התחרותיות גורמת לאתלטים להשקיע מעבר ליכולתם). כמו כן יש לאסור על חולי מרפן מאמץ איזומטרי (Isometric) (כמו הרמת משקולות כבדות או מתח) בגלל העלייה הניכרת בלחץ הדם שאינה רצויה בחולים אלה. | |
| − | + | ||
| + | ===טיפול ניתוחי=== | ||
| + | |||
| + | ;שורש אבי העורקים | ||
| + | מקובל להתערב ניתוחית – כאשר שורש אבי העורקים מגיע לגודל של 5 ס“מ (באופן רגיל, במבוגרים, שורש אבי העורקים הוא בערך 3 ס“מ יש מקרים שבהם נוהגים לנתח עוד לפני ששורש אבי העורקים מגיע ל-5 ס“מ וזאת כאשר יש סיפור משפחתי של קרע של אבי העורקים בערך נמוך מ-5 ס“מ או שיש התרחבות מהירה של אבי העורקים בקצב של יותר מ-1 ס“מ לשנה). | ||
| + | |||
| + | ;אפשרויות טיפוליות | ||
| + | # '''Composite Valve Graft''' (תמונה 16) שבו מחליפים את המסתם של אבי העורקים במסתם מלאכותי שמחובר לצינור (Tube) שמחליף את החלק העולה המורחב של אבי העורקים. את העורקים הכליליים מחברים אל השתל (גרפט) בעזרת טכניקת כפתורים (כמו בניתוח Switch להיפוך כלי הדם הגדולים - [[Transposition of the great arteries]]).{{ש}}הניתוח נחשב למוצלח והתמותה אינה גבוהה. המסתם המלאכותי מחזיק מעמד זמן רב. וכמובן על החולה להיות מטופל ב[[נוגדי קרישה]] (Anticoagulants) תוך בדיקת [[INR]]{{כ}} (International Normalized Ratio) למשך כל החיים [ לעיתים קרובות מוסיפים טיפול ב[[אספירין]] (Acetylsalicylic acid: Aspirin, Micropirin, Cardiopirin) במינון נמוך].{{ש}}יש לזכור שחולים שעברו ניתוח אינם מוגנים מדיסקציה של אבי העורקים מסוג B [בחלק היותר דיסטלי (Distal) של אבי העורקים] ויש להיות זהירים ולשים לב לתסמינים של דיסקציה גם לאחר הניתוח – המצריכים התערבות כירורגית.{{ש}}בילדים קטנים, בעבר, כאשר היה קושי לבצע החלפת מסתם מלאכותי בגודל מתאים – היו משתמשים ב-Homograft אשר לא היה מחזיק מעמד זמן רב והיה צורך בהתערבות נוספת | ||
| + | # '''ניתוח משמר מסתם''' (Valve Sparing Aortic Surgical Repair) בגלל הקשיים סביב הטיפול בנוגדי קרישה במיוחד בנשים ב[[היריון]] וילדים, ובגלל קושי בשימוש במסתמים מלאכותיים בילדים קטנים בוצעו טכניקות ניתוחיות לטיפול בשורש אבי העורקים תוך שימור המסתם של אבי העורקים (בהרבה מקרים המסתם עצמו דולף בגלל ההרחבה של הסינוסים).{{ש}}יש התאמות (Modifications) שונות לניתוחים הללו, ישנן שתיים בעיקר הנמצאות בשימוש:{{ש}}'''שיטת Remodeling''' – שהוכנסה על ידי הכירורג Yacoub Magdi, ובה מחברים Tube graft מעל הקומיסורות (Commissure) עם חיבור מחדש של העורקים הכליליים{{ש}}במקרים אלה המסתם האורטלי חופשי והוא יכול לגדול, לכן ניתן לבצע טכניקה מסוג זה גם בילדים (תמונה 17){{ש}}'''שיטת Reimplantation''' – שהוכנסה על ידי כירורג מטורונטו Tirone David – שבו מחברים גם את ה-Tube graft למוצא חדר שמאל מסביב למסתם (ועל ידי כך מקבעים את גודל ה-Annulus) ולכן לא טוב לעשותו בילדים קטנים (תמונה 18) | ||
| + | |||
| + | יתרונם של ניתוחים אלה הוא אי שימוש במסתם מלאכותי ולכן אין צורך בטיפול בנוגד קרישה, אך הבעיה לאורך זמן היא שחלק מהחולים מפתחים דליפה משמעותית ממסתם אבי העורקים שמצריכה התערבות נוספת. | ||
| + | |||
| + | לאחר הניתוחים להחלפת החלק העולה של אבי העורקים (Ascending aorta), יש להמשיך במתן חוסמי בטא, ויש להמשיך מעקב אחרי שאר אזורי אבי העורקים (על ידי MRA/CTA בערך אחת לשנה) כדי לשלול מפרצת (Aneurysm) או דיסקציה באזורים אחרים של אבי העורקים. | ||
| + | |||
| + | ===היריון ומרפן=== | ||
| + | |||
| + | נשים עם מרפן והרחבה של שורש אבי העורקים מעל 4 ס“מ הן בסכנה מוגברת של דיסקציה של אבי העורקים במיוחד בשליש השלישי להריון, יש לעקוב אחרי הנשים, לתת להן חוסמי בטא גם בזמן ההיריון, ובמקרים של אבי עורקים רחב – לשקול [[לידה]] בניתוח קיסרי. | ||
| + | |||
| + | ==פרוגנוזה== | ||
| + | |||
| + | אבחון מוקדם וטיפול נכון בחולי מרפן כבר מגיל הילדות יכול להאריך ולהציל חיים. לפני הטפולים הכירורגיים במרפן תוחלת החיים הייתה כ-45 שנים ורוב החולים היו מתים מקרע של אבי העורקים. כיום עם אבחון, מעקב וטיפול מתאימים חולים יכולים להגיע עד גיל 70. | ||
| + | |||
| + | ==דגלים אדומים== | ||
==ביבליוגרפיה== | ==ביבליוגרפיה== | ||
| − | + | ||
| − | + | <blockquote> | |
| − | + | <div style="text-align: left; direction: ltr"> | |
| − | + | # Dianna M. Milewicz et al: Treatment of Aortic Disease in Patients with Marfan Syndrome. Circulation 2005;111:e150-e157 | |
| + | # De paepe a et al: Revised Diagnostic Criteria for the Marfan Syndrome. Am j med genet 1996;62:417-26 | ||
| + | # Dietz hc. Et al: Mutations in the Human Gene for Fibrillin-1 in the Marfan Syndrome and Related Disorders. Hum mol genet 1995;4:1799-1809 | ||
| + | # Shores j et al: Progression of Aortic Dilatation and the Benefit of Long-Term Beta-Adrenergic Blockade in Marfan’s Syndrome. N engl j med 1994;330:1335-41. | ||
| + | </div> | ||
| + | </blockquote> | ||
| + | |||
| + | ==קישורים חיצוניים== | ||
| + | |||
| + | |||
| + | {{ייחוס|ד"ר אברהם מתתיהו, מומחה לקרדיולוגית ילדים, מנהל יחידת הלב לילדים, מרכז רפואי קפלן, רחובות}} | ||
| + | |||
| + | [[קטגוריה:ילדים]] | ||
| + | [[קטגוריה:פנימית]] | ||
| + | [[קטגוריה:קרדיולוגיה]] | ||
| + | [[קטגוריה:ראומטולוגיה]] | ||
גרסה אחרונה מ־12:30, 25 ביולי 2021
| תסמונת מרפן | ||
|---|---|---|
| Marfan syndrome | ||
| 250px | ||
Micrograph demonstrating myxomatous degeneration of the aortic valve, a common manifestation of Marfan syndrome
| ||
| שמות נוספים | Marfan's syndrome | |
| ICD-10 | Chapter Q 87.4 | |
| ICD-9 | 759.82 | |
| MeSH | D008382 | |
| יוצר הערך | ד"ר אברהם מתתיהו | |
תסמונת מרפן (Marfan syndrome) היא מחלה של רקמת חיבור. התורשה היא אוטוזומלית דומיננטית (Autosomal dominant) עם העברה מלאה אך הביטוי הקליני משתנה בחומרתו אפילו בתוך המשפחה.
למחלה יש תסמינים רבים אך המעורבות של הלב וכלי הדם היא זו שעלולה לגרום למוות מוקדם. ניתן בקלות לטעות ולא לאבחן ילדים במחשבה כי הם "פשוט" ילדים גבוהים או שחקני כדורסל, מבלי להתייחס לפתולוגיה הקרדיווסקולרית (Cardiovascular pathology) המשמעותית המסתתרת אצלם. יש חשיבות רבה לקיום מודעות מוגברת בקרב רופאי הילדים לאיתור החולים והפנייתם לבדיקות הנדרשות כדי להתחיל מוקדם בטיפול המונע ולהתערב בזמן לפני הופעה של אירועים מסכני חיים.
אפידמיולוגיה
שכיחות של מקרה אחד ל-4000. ב-25 אחוזים מהמקרים אין סיפור משפחתי והם מהווים מוטציות (Mutations) חדשות.
אטיולוגיה
מבחינה גנטית המחלה נובעת ממוטציות בגן (Gene) פיברילין 1 (Fibrilin 1, FBN1). הפיברילין הוא חלבון חשוב בתוך המיקרופיברילים (Microfibrils), שהם מבנים מורכבים שמכילים חלבונים רבים וסמוכים לאלסטין (Elastin) – בסיבים האלסטיים.
החלבון מקודד על ידי גן בכרומוזום 15(15q21.1 Chromosome) שהתגלה ב-1991.
מוטציה נוספת שנמצאה בשנת 2004 כגורמת לתמונה שיכולה להתאים למרפן נמצאת על גן בכרומוזום 3 (3p24.1) מוטציות ב-Transforming Growth Factor β Receptor Type II (TGFBR2).
השינויים בחלבון (עדיין לא ברורים לגמרי כל השלבים) גורמים לפתולוגיה של שבירות ונזק לסיבים האלסטים ואיבוד תאי שריר חלק שמתבטא באבי העורקים (Aorta) בשכבת המדיה (Medial degeneration).
מחשבה נוספת היא שלפיברילין 1 והמיקרופיברילים תפקיד של בקרה על גורמי גדילה מקבוצת TGF-β שלהם יש השפעות על תפקוד והתפתחות התאים ברקמות רבות בגוף. מאות מוטציות שונות נמצאו בפיברילין 1 שקשורות לתסמונת מרפן ויש עוד מאות רבות של מוטציות שקשורות למצבים דמויי מרפן, כמו ביטויים רק בשלד או רק בעיניים או רק באבי העורקים וכדומה.
כלומר, מציאת מוטציה בפיברילין 1 עדיין אינה אומרת שיש לחולה מרפן.
קליניקה
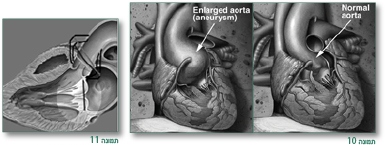
בלב יש בדרך כלל מעורבות של שורש אבי העורקים עם הרחבה מתקדמת (Progressive) של אזור הסינוסים (Sinuses) של Valsalwa (תמונות 11,10).
ההרחבה המתקדמת גורמת לכך שעלי מסתם אבי העורקים אינם יכולים להיסגר היטב (הרחבה של טבעת המסתם - Annulus) – ויכולה להופיע דליפה מאבי העורקים (Aortic regurgitation/insufficiency) בדרגות שונות.
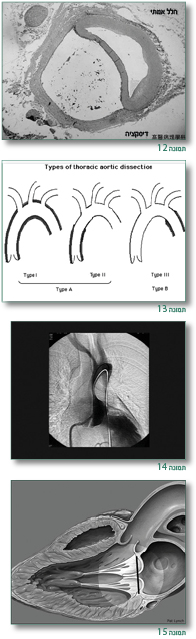
כמו כן הרחבה מתקדמת של שורש אבי העורקים – עלולה להביא לקרע של אבי העורקים (Aortic aneurysm) [שיכולה לגרום למוות מטמפונדה (Tamponade) או איבוד דם] וכן יכולה להיגרם דיסקציה של אבי העורקים (Aortic dissection) (תמונות 12–14).
במקרים שיש מעורבות של המסתם הדו צניפי (Mitral valve) – יש צניחה של המסתם (Mitral prolapse) (יותר שכיח בילדים ובנשים) עם דרגות שונות של דליפה (תמונה 15).
אבחנה
ניתן למצוא בטכניקות של היום מוטציות בפיברילין 1 רק ב- 70 אחוזים מהחולים שיש להם ממצאים קליניים ברורים של מרפן. מכאן ניתן להבין שהאבחון הגנטי במרפן הוא עדיין בעייתי ועיקר האבחנה היא קלינית (טבלה מצורפת).
מחלקים בדומה מעט לקדחת השגרון (Rheumatic fever) לקריטריונים עיקריים (Major criteria) במערכות שונות של הגוף שהם אופיניים יותר לתסמונת מרפן ופחות קיימים באוכלוסייה וקריטריונים משניים (Minor criteria) שהם פחות ספציפיים.
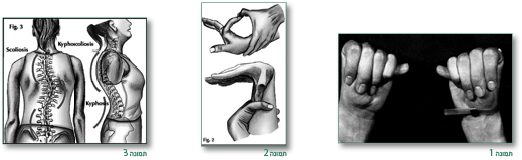
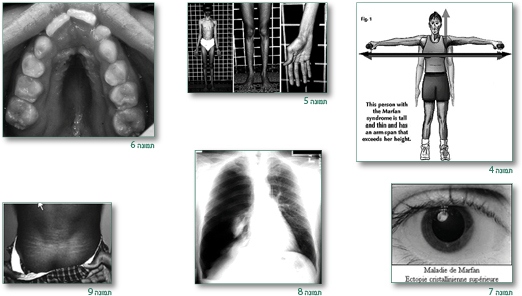
במקרים שיש סיפור משפחתי של מרפן או הוכחה לקיום מוטציה בפיברילין 1 בחולה המדובר, מספיק סימן עיקרי אחד ומעורבות נוספת פחות ספציפית במערכת אחרת. כאשר אין סיפור משפחתי ואין מידע על מוטציה בפיברילין 1 יש צורך לאבחן בשני קריטריונים עיקריים ומעורבות ספציפית פחות במערכת שלישית (תמונות 1–9). בילדים – לא תמיד יש את כל הקריטריונים בהתחלה ובמקרה של חשד יש להמשיך ולעקוב ולראות מה קורה במשך השנים הבאות. חשוב לקחת סיפור משפחתי ולערוך בדיקה פיסיקלית מקיפה, לשלוח לרופא עיניים שיבדוק אפשרות של דיסלוקציה של העדשה בהרחבה מלאה של האישון ולשלוח לקרדיולוג להעריך בעזרת האקו – מעורבות לבבית.
טיפול
מעקב קרדיולוגי
במסגרת המעקב הקרדיולוגי מלבד בדיקה פיסיקלית עוקבים בעזרת בדיקת אקו לב (Echocardiogram) אחרי שורש אבי העורקים [וזאת ביחס לנורמוגרמות (Nomograms) לפי משקל או שטח גוף] ותמיד גם בודקים את המסתם הדו צניפי ומחפשים גם אפשרות של דיסקציה של אבי העורקים.
- לאחר בדיקת האקו הראשונה –
חוזרים על האקו כעבור כ-6 חודשים – כדי לקבל רושם על קצב ההרחבה של שורש אבי העורקים – ואז בדרך כלל מעקב של אחת לשנה. כאשר שורש אבי העורקים מגיע לכ-4.5 סנטימטר (ס“מ) המעקב נעשה תכוף יותר.
כאשר שורש אבי העורקים מגיע ל-6-5 ס“מ, גדל בצורה ניכרת הסיכוי לקרע של אבי העורקים שעלול להביא למוות.
כאשר יש קושי טכני להעריך את שורש אבי העורקים באקו, ניתן לעשות בדיקות כמו CTA (Computer Tomography Angiography) או MRA (Magnetic Resonance Angiogram). בדיקות אלה גם טובות יותר במקרים של חשד לדיסקציה.
טיפול תרופתי
- חוסמי בטא (Beta blockers): הוכח שמתן חוסמי בטא בחולי מרפן באופן כללי מקטין את קצב ההרחבה של אבי העורקים, מפחית קצב התפתחות דליפה מאבי העורקים מקטין הסיכוי לדיסקציה, לאי-ספיקת לב ולמוות (זאת כנראה על ידי האטה בדופק והפחתה בקצב השינוי בנפח ובלחץ החלק העולה של אבי העורקים בזמן התכווצות הלב)
- השפעה של חוסמי בטא טובה יותר אם מתחילים אותם מוקדם במחלה ובמינון טוב
- מנסים בדרך כלל לתת מינונים שיביאו לדופק בסיסי של פחות מ-70 לדקה במנוחה ופחות מ-100 במאמץ בינוני (בילדים פחות מ-80 במנוחה ופחות מ-110 במאמץ בינוני)
- בילדים במיוחד יש לשים לב לתופעות לוואי כמו החמרה של גנחת הסימפונות (Asthma) או הפרעות בלימודים ואם יש בעיות ניתן להחליף לחוסמי סידן
- טיפול מונע לדלקת פנים לב זיהומית תת-חריפה (Sub acute Bacterial Endocarditis, SBE) במקרים שיש דליפה במסתם אבי העורקים, במסתם הדו צניפי או צניחה של המסתם הדו צניפי יש לתת טיפול מונע
הגבלות במאמץ
יש למנוע מחולי מרפן עיסוק בספורט מגע (ספורט בו ייתכנו חבללות בחזה) וכן יש להגביל בספורט תחרותי (שבו לעיתים התחרותיות גורמת לאתלטים להשקיע מעבר ליכולתם). כמו כן יש לאסור על חולי מרפן מאמץ איזומטרי (Isometric) (כמו הרמת משקולות כבדות או מתח) בגלל העלייה הניכרת בלחץ הדם שאינה רצויה בחולים אלה.
טיפול ניתוחי
- שורש אבי העורקים
מקובל להתערב ניתוחית – כאשר שורש אבי העורקים מגיע לגודל של 5 ס“מ (באופן רגיל, במבוגרים, שורש אבי העורקים הוא בערך 3 ס“מ יש מקרים שבהם נוהגים לנתח עוד לפני ששורש אבי העורקים מגיע ל-5 ס“מ וזאת כאשר יש סיפור משפחתי של קרע של אבי העורקים בערך נמוך מ-5 ס“מ או שיש התרחבות מהירה של אבי העורקים בקצב של יותר מ-1 ס“מ לשנה).
- אפשרויות טיפוליות
- Composite Valve Graft (תמונה 16) שבו מחליפים את המסתם של אבי העורקים במסתם מלאכותי שמחובר לצינור (Tube) שמחליף את החלק העולה המורחב של אבי העורקים. את העורקים הכליליים מחברים אל השתל (גרפט) בעזרת טכניקת כפתורים (כמו בניתוח Switch להיפוך כלי הדם הגדולים - Transposition of the great arteries).
הניתוח נחשב למוצלח והתמותה אינה גבוהה. המסתם המלאכותי מחזיק מעמד זמן רב. וכמובן על החולה להיות מטופל בנוגדי קרישה (Anticoagulants) תוך בדיקת INR (International Normalized Ratio) למשך כל החיים [ לעיתים קרובות מוסיפים טיפול באספירין (Acetylsalicylic acid: Aspirin, Micropirin, Cardiopirin) במינון נמוך].
יש לזכור שחולים שעברו ניתוח אינם מוגנים מדיסקציה של אבי העורקים מסוג B [בחלק היותר דיסטלי (Distal) של אבי העורקים] ויש להיות זהירים ולשים לב לתסמינים של דיסקציה גם לאחר הניתוח – המצריכים התערבות כירורגית.
בילדים קטנים, בעבר, כאשר היה קושי לבצע החלפת מסתם מלאכותי בגודל מתאים – היו משתמשים ב-Homograft אשר לא היה מחזיק מעמד זמן רב והיה צורך בהתערבות נוספת - ניתוח משמר מסתם (Valve Sparing Aortic Surgical Repair) בגלל הקשיים סביב הטיפול בנוגדי קרישה במיוחד בנשים בהיריון וילדים, ובגלל קושי בשימוש במסתמים מלאכותיים בילדים קטנים בוצעו טכניקות ניתוחיות לטיפול בשורש אבי העורקים תוך שימור המסתם של אבי העורקים (בהרבה מקרים המסתם עצמו דולף בגלל ההרחבה של הסינוסים).
יש התאמות (Modifications) שונות לניתוחים הללו, ישנן שתיים בעיקר הנמצאות בשימוש:
שיטת Remodeling – שהוכנסה על ידי הכירורג Yacoub Magdi, ובה מחברים Tube graft מעל הקומיסורות (Commissure) עם חיבור מחדש של העורקים הכליליים
במקרים אלה המסתם האורטלי חופשי והוא יכול לגדול, לכן ניתן לבצע טכניקה מסוג זה גם בילדים (תמונה 17)
שיטת Reimplantation – שהוכנסה על ידי כירורג מטורונטו Tirone David – שבו מחברים גם את ה-Tube graft למוצא חדר שמאל מסביב למסתם (ועל ידי כך מקבעים את גודל ה-Annulus) ולכן לא טוב לעשותו בילדים קטנים (תמונה 18)
יתרונם של ניתוחים אלה הוא אי שימוש במסתם מלאכותי ולכן אין צורך בטיפול בנוגד קרישה, אך הבעיה לאורך זמן היא שחלק מהחולים מפתחים דליפה משמעותית ממסתם אבי העורקים שמצריכה התערבות נוספת.
לאחר הניתוחים להחלפת החלק העולה של אבי העורקים (Ascending aorta), יש להמשיך במתן חוסמי בטא, ויש להמשיך מעקב אחרי שאר אזורי אבי העורקים (על ידי MRA/CTA בערך אחת לשנה) כדי לשלול מפרצת (Aneurysm) או דיסקציה באזורים אחרים של אבי העורקים.
היריון ומרפן
נשים עם מרפן והרחבה של שורש אבי העורקים מעל 4 ס“מ הן בסכנה מוגברת של דיסקציה של אבי העורקים במיוחד בשליש השלישי להריון, יש לעקוב אחרי הנשים, לתת להן חוסמי בטא גם בזמן ההיריון, ובמקרים של אבי עורקים רחב – לשקול לידה בניתוח קיסרי.
פרוגנוזה
אבחון מוקדם וטיפול נכון בחולי מרפן כבר מגיל הילדות יכול להאריך ולהציל חיים. לפני הטפולים הכירורגיים במרפן תוחלת החיים הייתה כ-45 שנים ורוב החולים היו מתים מקרע של אבי העורקים. כיום עם אבחון, מעקב וטיפול מתאימים חולים יכולים להגיע עד גיל 70.
דגלים אדומים
ביבליוגרפיה
- Dianna M. Milewicz et al: Treatment of Aortic Disease in Patients with Marfan Syndrome. Circulation 2005;111:e150-e157
- De paepe a et al: Revised Diagnostic Criteria for the Marfan Syndrome. Am j med genet 1996;62:417-26
- Dietz hc. Et al: Mutations in the Human Gene for Fibrillin-1 in the Marfan Syndrome and Related Disorders. Hum mol genet 1995;4:1799-1809
- Shores j et al: Progression of Aortic Dilatation and the Benefit of Long-Term Beta-Adrenergic Blockade in Marfan’s Syndrome. N engl j med 1994;330:1335-41.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר אברהם מתתיהו, מומחה לקרדיולוגית ילדים, מנהל יחידת הלב לילדים, מרכז רפואי קפלן, רחובות


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק