הבדלים בין גרסאות בדף "הם אוקסידאז - Heme oxidase"
| (5 גרסאות ביניים של אותו משתמש אינן מוצגות) | |||
| שורה 6: | שורה 6: | ||
|כיתוב תמונה= | |כיתוב תמונה= | ||
|מעבדה=[[כימיה בדם]] | |מעבדה=[[כימיה בדם]] | ||
| − | |תחום=מולקולה אנזימטית המקטלזת את פירוק ה- | + | |תחום=מולקולה אנזימטית המקטלזת את פירוק ה- heme והיא מעורבת בתהליכים מטבוליים רבים, בתהליכים סרטניים ובמחלות נוספות. |
|יחידות מדידה= | |יחידות מדידה= | ||
| שורה 14: | שורה 14: | ||
}} | }} | ||
==ההיסטוריה של HMOX1== | ==ההיסטוריה של HMOX1== | ||
| − | אנזים זה אופיין לראשונה על ידי Tenhunen ו-Scmidtftar שתיארו את היותו אחראי לקטליזה של הפיכת heme ל[[בילירובין]] (Hupper וחב' ב-Nitric Oxide משנת 2021). מספר מעבדות ניסו להסביר את המהלך של התמרת heme ל-biliverdin, ואכן הופיעו מספר הסברים להפיכה לא-אנזימטית של ריאקציה זו. הראיה המוקדמת ביותר של ביו-טרנספורמציה זו פורסמה על ידי Plieninger ו- Fischer בשנת 1942. המוגלובין תואר לראשונה בשנות ה-40 של המאה ה-19, על ידי Hunefeld (Boor ב-General Physiology משנת 1930), וגרעין ה-heme שלו תואר לראשונה על ידי Teichmann ב-1853, אך רק כמעט 100 שנים מאוחר יותר, | + | אנזים זה אופיין לראשונה על ידי Tenhunen ו-Scmidtftar שתיארו את היותו אחראי לקטליזה של הפיכת heme ל[[בילירובין]] (Hupper וחב' ב-Nitric Oxide משנת 2021). מספר מעבדות ניסו להסביר את המהלך של התמרת heme ל-biliverdin, ואכן הופיעו מספר הסברים להפיכה לא-אנזימטית של ריאקציה זו. הראיה המוקדמת ביותר של ביו-טרנספורמציה זו פורסמה על ידי Plieninger ו- Fischer בשנת 1942. המוגלובין תואר לראשונה בשנות ה-40 של המאה ה-19, על ידי Hunefeld (Boor ב-General Physiology משנת 1930), וגרעין ה-heme שלו תואר לראשונה על ידי Teichmann ב-1853, אך רק כמעט 100 שנים מאוחר יותר, תיאר Irving London את היצירה של המוגלובין. חד תחמוצת הפחמן (CO) באוויר הננשף מהריאות זוהה בשנת 1869, כאשר von Fodor פיתח את המדידה הכמותית הראשונה של קרבוקסי-המוגלובין. הדיווח הראשון של זיהוי CO בדם אנושי היה בשנת 1923 על ידי Sayers וחב', אף על פי שחוקרים אלה התכחשו לתגליתם זו בהנחה שמדובר בטעות אקראית. בשנת 1933 אישר Gettler של-CO יש נוכחות נורמלית בדם, אך הוא פרש זאת לחשיפה בלתי נמנעת למזהמים סביבתיים, או שמקורו במיקרוביום האנושי (Hopper וחב' משנת 2020). רק בשנת 1952 הדגים Sjostrand שיצירת CO נובעת מתהליך הפירוק של המוגלובין. |
| − | + | ||
==Heme אוקסידאז== | ==Heme אוקסידאז== | ||
Heme oxidase (להלן HMOX) הוא אנזים המקטלז את הפירוק של heme ליצירה של יון ברזל דו-ערכי, biliverdin ו-CO (Ryter וחב' ב- Physiol Rev משנת 2006). ישנם אנזימים מפרקי heme רבים, אך רק אלה מהם המפרקים heme אארובי נחשבים ל-אנזימים דומי-HMOX בעוד שאנזימים אנארוביים אינם משתייכים למשפחת HMOX. | Heme oxidase (להלן HMOX) הוא אנזים המקטלז את הפירוק של heme ליצירה של יון ברזל דו-ערכי, biliverdin ו-CO (Ryter וחב' ב- Physiol Rev משנת 2006). ישנם אנזימים מפרקי heme רבים, אך רק אלה מהם המפרקים heme אארובי נחשבים ל-אנזימים דומי-HMOX בעוד שאנזימים אנארוביים אינם משתייכים למשפחת HMOX. | ||
| − | הגנום האנושי יכול לקודד לשלושה איזופורמים של HMOX. הפירוק של heme יוצר שלושה כרומוגנים, וריאקציה זו יכולה להתרחש בכל תא או תרומבוציט, כאשר הדוגמה הקלאסית היא תהליך הריפוי של חבלה, בה נוצרים שלושה כרומוגנים שונים בתהליך הריפוי: | + | הגנום האנושי יכול לקודד לשלושה איזופורמים של HMOX. הפירוק של heme יוצר שלושה כרומוגנים, וריאקציה זו יכולה להתרחש בכל תא או תרומבוציט, כאשר הדוגמה הקלאסית היא תהליך הריפוי של חבלה, בה נוצרים שלושה כרומוגנים שונים בתהליך הריפוי: כרומוגן אדום, ההופך לירוק ביצירת biliverdin ההופך צהוב בהופעת בילירובין. אף על פי ש-HMOX מופיע בכל הגוף, הוא פעיל במיוחד בטחול בו הוא מסייע לפירוק של המוגלובין במהלך המחזור של אריתרוציטים. מלבד הטחול, ריכוזים גבוהים שלו מוצאים בכבד, ובכליות, וברמה התאית HMOX1 ממוקם בעיקר ברטיקולום האנדופלזמטי, וניתן לאתר אותו גם במיטוכונדריה, בגרעין התא, ובממברנה החיצונית של התא (Hopper וחב' ב-Curr Pharmaceut Design משנת 2018). HMOX יכול גם לשמש כחלבון chaperone, המעורב באינטראקציות בין חלבונים, וכן הוא יכול להיות מופרש אל תוך ציטופלזמת התא ולהשתתף בריאקציות שונות מעבר לתפקידו הקטליטי. |
| − | |||
| − | |||
| − | + | '''Heme oxydase 1:''' איזופורם זה, HMOX1, הוא חבר במשפחת ה-heat shock proteins המכונה גם HSP32.כיוון שמשקלו המולקולרי הוא 32,000 דלטון, והוא מכיל 288 חומצות אמינו, ומקודד על ידי הגן HMOX1 חלבון זה אינו hemoprotein כיוון שהוא אינו מכיל קבוצות פרוסטתיות של heme (Kikuchi וחב' ב-Biochem Biophys Res Commun משנת 2005). הפעילות של HMOX1 תלויה באנזים NADPH-cytochrome P450 reductase (Wang וחב' ב-J Biol Chem משנת 2003). HMOX1 הוא אנזים חיוני אך יש רק מצבים נדירים של חסר שלו מה מסתיים במוות. במחלות אחדות פעילותו של HMOX1 בעייתית. לדוגמה, חלבון זה מסוגל לפעול נגד פעילותם של תרופות כימותרפויטיות, ובכך הוא עלול לתרום לשגשוגם של תאים סרטניים (Schipper וחב' ב-Prog Neurobiol משנת 2019, Jozkowiicz וחב' ב-Antioxidants Redox Signaling משנת 2007, ו-Podkalicka וחב' ב-Contemp Oncol משנת 2018). HMOX1 מעוכב על ידי מספר פורפירינים כגון zinc protoporphyrin (Vreman וחב' ב-Canadian J Physiol Phermacol משנת 1996). | |
| − | ' | + | cDNA של HMOX1 שובט לראשונה מטחול של חולדה בשנת 1985 (Alam וחב' ב-J Biol Chem משנת 1989), ורצף חומצות האמינו גילה מקטע הידרופובי בקצה ה-C-טרמינלי, הדרוש לתאחיזה ברטיקולום האנדופלמטי. HMOX1 מבוטא במידה רבה באיברים האחראיים להרס של אריתרוציטים מזדקנים, וכן תאי טחול ותאים רטיקולו-אנדותליאליים בכבד ובמח העצם. אף על פי שהביטוי הבסיסי של HMOX1 נמוך ברקמות שאינן אחראיות ישירות במטבוליזם של המוגלובין, HMOX1 מבוטא בחוזקה בתאים הנחשפים לעקה על ידי מתכות כבדות, אנדוטוקסין, ציטוקינים, heme, היפוקסיה, NO ו-קרינת UV ( Keise וחב' ב-Mol Cell Biol משנת 1990, Lizzardini וחב' ב-Biochem J משנת 1993, Cantoni וחב' באותו כתב עת משנת 1991,ו- Lee וחב' ב-J Biol Chem משנת 1997). |
| − | '''Heme | + | '''Heme oxydas 2:''' איזופורם זה, HMOX2, הוא חלבון קונסטיטוטיבי המתבטא בתנאים הומאוסטטיים באשכים, במערכת העיכול, בתאי אנדותל, ובמוח (Munoz--Snschez ו-Chanes-Cardenaz ב-Oxidative Med Cell Longevity משנת 2014). איזופורם זה שמשקלו המולקולרי 36,000 דלטון מקודד על ידי הגן HMOX2 ויש לו זהות של 47% ברצף חומצות האמינו עם HMOX1. הוא שונה מ-HMOX1 בהכילו מקטע נוסף של 20 חומצות אמינו בקצה ה-N-טרמינלי, וכן בהיות HMOX2 הפופרוטאין בהכילו שיירי heme. בנוסף, בעוד ש-HMOX1 מושרה על ידי מספר משרנים, HMOX2 מושרה רק על ידי גלוקו-קורטיקואידים מהאדרנל, אם כי מספר מולקולות נוספות יכולות להגביר את מהירותו הקטליטית, ואילו אופיואידים יכולים לעכב את פעילותו. |
| − | '''Heme oxygenase מיקרוביאליים:''' האנזים heme oxygenase משומר פילוגנטית ביצורים מ-species מרוחקים (Li ו-Stocker ב-Redox Rep משנת 2009). המיקרוביום האנושי מכיל עשרות הומולוגים של HMOX מיקרוביאלי כגון HMX1 ממקור של Saccharomyces cerevisiae, ChuS ממקור של | + | '''Heme oxydase 3:''' איזופורם שנוי במחלוקת זה, אינו פעיל קטליטית, וההשערה היא שהוא מעורב בחישת heme או בדה-טוקסיפיקציה שלו. HMOX3 הוא בעל משקל מולקולרי של 33,000 דלטון, והנוכחות הגדולה ביותר שלו היא בכבד, בבלוטת הערמונית ובכליות. |
| + | |||
| + | '''Heme oxygenase מיקרוביאליים:''' האנזים heme oxygenase משומר פילוגנטית ביצורים מ-species מרוחקים (Li ו-Stocker ב-Redox Rep משנת 2009). המיקרוביום האנושי מכיל עשרות הומולוגים של HMOX מיקרוביאלי כגון HMX1 ממקור של Saccharomyces cerevisiae, ChuS ממקור של E.Coli, ו-HmuO ממקור של Corynebacterium diphtheriiae. התפקיד הקריטי של מערכות HMOX היפרוקריוטיות, הוא לסייע לקליטה של ברזל תזונתי מהפונדקאי האאוקריוטי (Frankenberg -Dinkel ב-Antioxidants Redox Signaling משנת 2004). | ||
==משרנים של HMOX1== | ==משרנים של HMOX1== | ||
| − | HMOX1 מושרה על ידי מספר רב של מולקולות הכוללות מתכות כבדות, [[סטאטינים]], paclitaxel, חד תחמוצת הפחמן, rapamycin, probucol, ,NO ,sildenafil ומספר פורפירינים (Ferrandiz ו-Deesa ב-Curr Pharmaceut Design משנת 2008). משרנים אנדוגניים כוללים ליפידים כגון | + | HMOX1 מושרה על ידי מספר רב של מולקולות הכוללות מתכות כבדות, [[סטאטינים]], paclitaxel, חד תחמוצת הפחמן, rapamycin, probucol, ,NO ,sildenafil ומספר פורפירינים (Ferrandiz ו-Deesa ב-Curr Pharmaceut Design משנת 2008). משרנים אנדוגניים כוללים ליפידים כגון lipoxin ו-epoxyeicosatrienoic acid, ופפטידים כגון adrenomedullin ו-apolipoprotein, וכן הוא מושרה על ידי hemin, hydroxycoumarin, genistein, חומצה ניטרואולאית, H2O2, succinykacetone ועוד (Ma ו-He ב-Pharmacol Rev משנת 2012). |
==התפקידים הפיזיולוגיים של HMOX== | ==התפקידים הפיזיולוגיים של HMOX== | ||
| − | HMOX משתתף במספר תהליכים תאיים (Kim וחב' ב-Cell Mol Immunol משנת 2018, ו-Ryter וחב' ב-Cell Mol Biochem משנת 2002). היתרונות ההגנתיים התאיים של HMOX הגבירו את כמות המחקרים על פעילותיו הפרמוקולוגיות והשפעותיו הפוטנציאליות (Cheng ו-Rong ב-Curr Pharmceut Design משנת 2017). | + | HMOX משתתף במספר תהליכים תאיים (Kim וחב' ב-Cell Mol Immunol משנת 2018, ו-Ryter וחב' ב-Cell Mol Biochem משנת 2002). היתרונות ההגנתיים התאיים של HMOX הגבירו את כמות המחקרים על פעילותיו הפרמוקולוגיות והשפעותיו הפוטנציאליות (Cheng ו-Rong ב-Curr Pharmceut Design משנת 2017). |
==חד תחמוצת הפחמן (CO) ו-HMOX== | ==חד תחמוצת הפחמן (CO) ו-HMOX== | ||
| − | המרכיב העיקרי ביצירת CO אנדוגני הוא HMOX1{{כ}} (Motterlini וחב' ב-Nat Rev Drug Discov משנת 2010), | + | המרכיב העיקרי ביצירת CO אנדוגני הוא HMOX1{{כ}} (Motterlini וחב' ב-Nat Rev Drug Discov משנת 2010), אף על פי שמולקולות נוספות תורמות באופן מופחת ליצירת CO. מולקולה זו מיוצרת בקצב של 16.4 מיקרומול/שעה בגוף האדם, כאשר 86% בערך מגיעים מפירוק Heme על ידי HMOX, ו-14% הנותרים מקורם ממקור שאינו heme, כולל פוטו-אוקסידציה, פראוסידציה של ליפידים ושל חומצות keto מהמיקרוביום או מקסנוביוטיקה (Hopper וחב' ב-Chem Rev משנת 2020). רמת קרבוקסי-המוגלובין (CO-Hb) הממוצעת בדם של לא-מעשנים היא בין 0.2 עד 0.85%, בעוד שרמתו בדמם של מעשנים יכולה להגיע ל-4 עד 10%. המִחְזוּר של אריתרוציטים בטחול הוא המקור של כ-80% של ה-CO ממקור ה-heme הנוצר אנדוגנית. יתר 20 האחוזים של יצירת CO ממקור heme מיוחסים לתהליכים קטבוליים של hemoproteins כגון מיוגלובין, ציטוכרומים, catalases, פראוקסידאזות, guanylate cyclase מסיס, והאנזים nitric synthase בכבד, וכן אריתרפויאזה בלתי יעילה במח העצם (Vreman וחב' ב-CRC Press משנת 2001). בנוסף להיות heme מקור של CO, ה-heme הוא גם מעביר איתותים קריטיים הקשורים בחישה של CO (Shimizu וחב' ב-Chem Rev משנת 2019). כגורם מאותת, CO קשור לתהליכים פיזיולוגיים נורמליים ויש לו יתרונות תרפויטיים בשיפור של מצבי דלקת והיפוקסיה (Motterlini ו-Foresti ב-Am J Physiol משנת 2017). עם זאת נשאלת השאלה באיזה מידה HMOX מעורב בהשפעה מגינה של כנגד היפוקסיה, שכן שלושה שווי-ערך של חמצן נדרשים כדי לייצר CO מתהליכי קטבוליזם של heme במקביל לאלה של רמת הזמינות של heme (Leung וחב' ב-Proc Natl Acad Sci USA משנת 2021), ובנוסף היצירה האיטית של heme שנמשכת מספר שעות (Pellacani וחב' ב-Circulation Res משנת 1998). |
==Biliverdin HMOX ו-Bilirubin== | ==Biliverdin HMOX ו-Bilirubin== | ||
| − | קיים תיעוד עתיק על הבילירובין הנוצר אנדוגנית בכתבי היפוקרטס (Watson בכינוס על הפיזיולוגיה של בילירובין משנת 1977). ברוב המקרים, HMOX מבקע את ה-heme של protoporphyrin IX בגשר α-methine, ליצירת הבילירובין. Biliverdin IXα עובר ביו-טרנספורמציה דרך biliverdin reductase ליצירה של bilirubin IXα (Wegiel ו-Otterbain ב-Front Pharmacol משנת 2012).ה-bilins משחקים תפקיד חשוב בממלכות הפילוגנטיות (Takemoto וחב' ב-Israel J Chem משנת 2019). | + | קיים תיעוד עתיק על הבילירובין הנוצר אנדוגנית בכתבי היפוקרטס (Watson בכינוס על הפיזיולוגיה של בילירובין משנת 1977). ברוב המקרים, HMOX מבקע את ה-heme של protoporphyrin IX בגשר α-methine, ליצירת הבילירובין. Biliverdin IXα עובר ביו-טרנספורמציה דרך biliverdin reductase ליצירה של bilirubin IXα (Wegiel ו-Otterbain ב-Front Pharmacol משנת 2012).ה-bilins משחקים תפקיד חשוב בממלכות הפילוגנטיות (Takemoto וחב' ב-Israel J Chem משנת 2019). |
| − | '''יון ferrous:''' יון הברזל הדו-ערכי המשתחרר מ-HMOX "נלכד" במהירות על ידי [[פריטין]]. עם זאת, יוני חמצן פעילים (ROS, המשתחררים בריאקציות Fenton או Haber-Weiss) מסוגלים לשגר איתותים תאיים (Sies ו-Jones ב-Nat Rev Mol Cell Biol משנת 2020, ו-NaveenKumar וחב' ב-ACS Cell Biol משנת 2018, ו- Frankenberg -Dinkel ב-Antioxidants | + | '''יון ferrous:''' יון הברזל הדו-ערכי המשתחרר מ-HMOX "נלכד" במהירות על ידי [[פריטין]]. עם זאת, יוני חמצן פעילים (ROS, המשתחררים בריאקציות Fenton או Haber-Weiss) מסוגלים לשגר איתותים תאיים (Sies ו-Jones ב-Nat Rev Mol Cell Biol משנת 2020, ו-NaveenKumar וחב' ב-ACS Cell Biol משנת 2018, ו- Frankenberg -Dinkel ב-Antioxidants Redox Signaling משנת 2004). |
==הריאקציה המקוטלזת על ידי HMOX1== | ==הריאקציה המקוטלזת על ידי HMOX1== | ||
| − | ריאקציה זו יכולה להתרחש בכל תא. במושגים של מנגנונים מולקולריים, האנזים מסייע להידרוקסילציה של פחמן meso אחד במרכז ה-heme (Yoshida ו-Mikita ב-J Inorganic Chem משנת 2000). HMOX1 אחראי להגבלת הקצב של הקטבוליזם של heme התלוי ב-NADPH-cytochrome p450 reductase ובחמצן כדי לבקע את טבעת הפורפירין של heme בגשר של α-methene ליצירה של biliverdin. הריאקציה מתבצעת בשלושה שלבים (Evans וחב' ב-J Biol Chem משנת 2008): | + | ריאקציה זו יכולה להתרחש בכל תא. במושגים של מנגנונים מולקולריים, האנזים מסייע להידרוקסילציה של פחמן meso אחד במרכז ה-heme (Yoshida ו-Mikita ב-J Inorganic Chem משנת 2000). HMOX1 אחראי להגבלת הקצב של הקטבוליזם של heme התלוי ב-NADPH-cytochrome p450 reductase ובחמצן כדי לבקע את טבעת הפורפירין של heme בגשר של α-methene ליצירה של biliverdin. הריאקציה מתבצעת בשלושה שלבים (Evans וחב' ב-J Biol Chem משנת 2008): |
Heme b<sup>3</sup>+ + O2 + NADPH + H+→ α-meso-hydroxyheme<sup>3+</sup> + NADP++ H2O | Heme b<sup>3</sup>+ + O2 + NADPH + H+→ α-meso-hydroxyheme<sup>3+</sup> + NADP++ H2O | ||
| שורה 65: | שורה 65: | ||
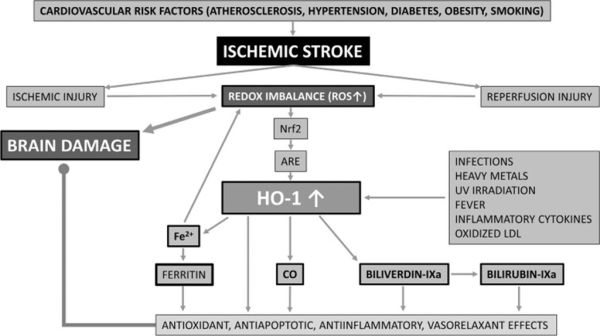
==הרלוונטיות הקלינית של HO-1 בשבץ-מוחי איסכמי== | ==הרלוונטיות הקלינית של HO-1 בשבץ-מוחי איסכמי== | ||
| − | שבץ-מוחי הוא הגורם השני במעלה למוות בעולם האחראי ל-6 מיליון מקרי מוות בשנה וגורם חשוב לפגיעה ממושכת בתפקוד הגופני, ולנכות קבועה. (Mozaffarian ב-Circulation משנת 2000). | + | שבץ-מוחי הוא הגורם השני במעלה למוות בעולם האחראי ל-6 מיליון מקרי מוות בשנה וגורם חשוב לפגיעה ממושכת בתפקוד הגופני, ולנכות קבועה. (Mozaffarian ב-Circulation משנת 2000). עקה חמצונית היא גורם מרכזי באיסכמיה מוחית, הגורמת לנזק נוירונלי בלתי הפיך. אחד ממנגנוני ההגנה התאית הוא הציר Nfr2-HO-1. שבץ איסכמי הוא תרחיש של אי-תפקוד נוירונלי הנגרם על ידי אוטם מוחי, ספינלי או רטינלי (Sacco וחב' ב-Stroke משנת 2013). עקה חמצונית עם ROS הגורמת נזק למרכיבים תאיים כולל חלבונים, ליפידים וחומצות גרעין, משחקת תפקיד מרכזי במהלך איסכמיה מוחית, מה שמוביל לנזק לנוירונים עד כדי מותם (Chen וחב' ב-Brain Res משנת 2012, Yamauchi וחב' ב-Neuroscience משנת 2016, ו-Lv וחב' ב-Cell Physiol Biochem משנת 2017). |
| − | בין מודלים של שבץ מוחי בחיות חסימה של עורק המוח המרכזי נבחנה במספר רב של ניסויים על שבץ איסכמי (Howells וחב' ב-J Cereb Blood Flow Metab משנת 2010, ו-Fluri וחב' ב-Drug Des Devel Ther משנת 2015). מודל MCAO נחשב כמודל מתאים לחקות שבץ איסכמי באדם, עם מוות של נוירונים, דלקת מוחית ונזק למחסום דם-מוח. | + | בין מודלים של שבץ מוחי בחיות חסימה של עורק המוח המרכזי נבחנה במספר רב של ניסויים על שבץ איסכמי (Howells וחב' ב-J Cereb Blood Flow Metab משנת 2010, ו-Fluri וחב' ב-Drug Des Devel Ther משנת 2015). מודל MCAO נחשב כמודל מתאים לחקות שבץ איסכמי באדם, עם מוות של נוירונים, דלקת מוחית ונזק למחסום דם-מוח. ניסוי מוקדם תוך שימוש ב- MACO בעכברים טרנסגניים הראה שביטוי-יתר של HO-1, הפחית משמעותית את נפח האוטם (Panahian וחב' ב-J Neurochem משנת 1999). לעומת זאת, בעכברי knockout ללא HO-1. נפח האוטם נמצא גדול יותר משמעותית בהשוואה לזן הבר שלהם. באדם, הביטוי של HO-1 מראה שונוּת רבה בגין promoter מאוד פולימורפי, שנכרך עם גורמי סיכון קרדיו-וסקולריים. הווריאנט הנחקר ביותר היה האורך של מקטע ה-(GT)n-repeat, שהיה כרוך באופן הופכי עם הביטוי של HO-1 (Chen וחב' ב-Hum Gen משנת 2002). בסקר אוכלוסייה פרוספקטיבי, נמצא שאלה עם repeats ארוכים יותר (מעל 32) על 2 האללים של HO-1 היו בעלי סיכון קרדיו-וסקולרי מוגבר, התפתחות מואצת של התהליך הטרשתי, ונטייה לרמות גבוהות יותר של פוספוליפידים מחומצנים על apolipoprotein B-100 (Pechlaner וחב' ב-Thromb Vasc Biol Arteriosclr משנת 2015). סקירה סיסטמטית עדכנית של הספרות האפידמיולוגית על פולימורפיזמים של HO-1(GT)n, מצאה שאלה עם repeats קצרים של הגנוטיפ SS (פחות מ-24–27) (דהיינו עם פעילות HO-1 מוגברת) נמצאו באחוז גבוה יותר באלה ללא מחלה קרדיו-וסקולרית ידועה. |
[[קובץ:1HO-1.jpg|ממוזער|מרכז|600 פיקסלים|הקשר בין מסלולי HO-1 באדם וגורמי הסיכון למחלה קרדיו-וסקולרית]] | [[קובץ:1HO-1.jpg|ממוזער|מרכז|600 פיקסלים|הקשר בין מסלולי HO-1 באדם וגורמי הסיכון למחלה קרדיו-וסקולרית]] | ||
| − | ==HMOX | + | ==HMOX ויתר לחץ-דם== |
| − | הראיות על הקשר בין ביטוי HMOX1 ויתר לחץ-דם מגיעות מניסויים בחיות תוך שימוש בחולדות המפתחות באופן ספונטני [[לחץ-דם גבוה]]. כאשר מבצעים עירוי כרוני של angiotensin II לחולדות לחץ הדם הגבוה המושרה, מגביר את הביטוי של HMOX1 בוותין של החולדות (Ishizaka וחב' ב-Circulaion | + | הראיות על הקשר בין ביטוי HMOX1 ויתר לחץ-דם מגיעות מניסויים בחיות תוך שימוש בחולדות המפתחות באופן ספונטני [[לחץ-דם גבוה]]. כאשר מבצעים עירוי כרוני של angiotensin II לחולדות לחץ הדם הגבוה המושרה, מגביר את הביטוי של HMOX1 בוותין של החולדות (Ishizaka וחב' ב-Circulaion משנת 1997). יתרה מכך, כאשר מזריקים לחולדות אלו HMOX1 אנושי, מוצאים חחלשה של התפתחות יתר לחץ-דם, המיוחסת להרחבת כלי הדם על ידי CO (Sabaawy וחב' ב-Hypertension משנת 2001). ההשפעה המורידה לחץ-דם של טיפול למשך 3 חודשים עם olmesartan יוחסה בחלקה לעלייה בריכוז של ho-1 בפלזמה (Calò וחב' ב-Blood Press משנת 2011). בין המטבולים הקטבוליים של HO-1, הריכוזים של בילירובין נמצאו מופחתים משמעותית במטופלים עם יתר לחץ-דם בלתי מטופל, בעוד שריכוזי בילירובין לא השתנו באלה עם לחץ-דם נורמלי או במטופלים עם יתר לחץ-דם מטופלים כנגדו (Papadakis וחב' ב-Am J Hypertens משנת 1999). יתרה מכך, במעקב שנמשך 10 שנים בקוריאנים עם לחץ-דם תקין, רמות בילירובין בנסיוב ורמות מוגברות של לחץ-דם נמצאו עם מתאם שלילי (Chin וחב' ב-J Korean Med Sci משנת 2009). בנשים עם יתר לחץ-דם בהיריון, או באלו עם pre-eclampsia, רמות CO באוויר הנשאף היו נמוכות משמעותית בהשוואה לרמות אלה בנשים בריאות (Kreiser וחב' ב-J Perinatol משנת 2004). |
==HMOX וסוכרת== | ==HMOX וסוכרת== | ||
| − | הביטוי של HO-1 בסוכרת נמצאו במתאם רציפרוקלי בניסויים בחיות, דהיינו ביטוי יתר של HO-1 היה כרוך בהתקדמות סוכרת בעכברי NOD, | + | הביטוי של HO-1 בסוכרת נמצאו במתאם רציפרוקלי בניסויים בחיות, דהיינו ביטוי יתר של HO-1 היה כרוך בהתקדמות סוכרת בעכברי NOD, או השרייה של HO-1 בחולדות Zucker סוכרתיות, שפרה את הרגישות לאינסולין (Hu וחב' ב-Diabetes משנת 2007, ו-Nicolai וחב' ב-Hypertension משנת 2009). בבני-אדם הביטוי של HO-1 נמצא מופחת בדם ההיקפי בתאים מונו-נוקלאריים של חולי סוכרת (Song וחב' ב-Am J Epidemiol משנת 2009), בעוד שרמות ביטוי גבוהות של HO-1 בשלבי היריון מוקדמים, נכרכו עם סיכון מופחת של [[סוכרת הריונית]] (Qiu וחב' ב-One PLoS משנת 2012). יתרה מכך, ריכוזים מוגברים של HO-1 בפלזמה, היו קשורים עם סיכון מוגבר לפתח סוכרת type II (Bao וחב' ב-PLos One משנת 2010). המשרן של HO-1 ,Nrf2, נמצא בריכוז נמוך יותר במטופלים סוכרתיים וקדם-סוכרתיים, מה שמרמז שמנגנונים אנטי אוקסידנטים מוחלשים כתוצאה מירידה בריכוז Nrf2, עשויים להיות קשורים בהתפתחות של סוכרת (Jiménez-Osario וחב' ב-Int J Mol Sci משנת 2014). מטופלים עם רמות מוגברות של בילירובין בנסיוב, היו בסיכון מופחת לחלות בסוכרת (Cheriyath וחב' ב-J Clin Med Res משנת 2010). במטופלים עם תסמונת Gilbert וסוכרת, היפר-בילירובינמיה נכרכה על שכיחות מופחתת של אירועי סיבוכים וסקולריים, בהשוואה לאלה שהם סוכרתיים בלבד (Inoguchi וחב' ב-JAMA משנת 2007). בהתחשב בתוצאות הניסויים האחרונים היפר-בילירובינמיה מושרית ניסויית משך 3 ימים עם atazanavir בבני-אדם עם סוכרת type2 בניסוי כפול-סמיות ומבוקר כנגד פלצבו, נמצא גורם לשיפור משמעותי בתפקוד האנדותליאלי (Dekker וחב' ב- Atheriosclr Thromb Vasc biol משנת 2011). |
| − | |||
| − | |||
| − | בנוסף, HO-1 מגביר את האנגיוגניות של תאים סרטניים על ידי שהוא משרה את הביטוי של גורמים אנגיוגניים כגון VEGF{{כ}}(Miyake וחב' ב-Oncol Rep משנת 2011). יש ראיות מתגברות המדגימות את המעורבות של שפעול שעתוקי בתיווך Nfr2 של גנים נוגדי חמצון מה שמסייע להתמרת תאים והפיכתם לטומורוגניים (DeNicola וחב' ב-Nature משנת 2011). מוטציות ב-Nfr2 ובמעכב שלו, KEAP1, זוהו בסוגי סרטן שונים באדם (Geismann | + | בין גורמי השעתוק, Nrf2 (או nuclear factor erythroid 2-related factor 2) הוא בעל תפקיד מרכזי בהגנה מפני עקה חמצונית (Ishii וחב' ב-J Biol Chem משנת 2000). במצבים של חוסר איזון ב-redox, Nrf2 משפעל אנזימים אנטי-אוקסידנטים אחדים, כגון glutathione-S-trnsferase glutamyl cysteine synthetase ,γ, וריאקציה זו יכולה להתרחש בכל תא. במושגים של מנגנונים מולקולריים, האנזים מסייע להידרוקסילציה של פחמן meso אחד במרכז ה-heme (Yoshida ו-Mikita ב-J Inorganic Chem משנת 2000), ו-heme oxygenase או HO-1 על ידי התקשרות עם AREs (או antioxidant response elements) ועל ידי כך מושרה ביטוי גני (Kobayashi וחב' ב-Meth Enzymol משנת 2004). בין אנזימים אלה, HO-1 דווח כאנזים המכיל את הכי הרבה AREs על הפרומוטר שלו (Chumboutong וחב' ב-Neurochem Int משנת 2017), מה שהופך אותו ליעד תרפויטי מבטיח כנגד נזק מוחי בעת יצירת אוטם מוחי. HO-1 יכול להיות משופעל על ידי גירויים שונים כגון אינפקציות, מתכות כבדות, קרינת UV, חום, ציטוקינים דלקתיים ו-LDL מחומצן (Ameriso וחב' ב-Stroke משנת 2005). {{כ}}HO-1 מקטלז פירוק heme ליצירה של כמויות אקווי-מולריות של ברזל (Fe<sup>2+</sup>) חד תחמוצת הפחמן (CO) ו-biliverdin-IX. הברזל המשתחרר משרה ביטוי של פריטין, הגורם להַפְקָעָה של Fe<sup>2+</sup> והגבלת הנזק לתאים המתווך על ידי ברזל (Balla וחב' ב-J Biol Chem משנת 1992, ו-Balla וחב' ב-Antioxid Redox Signal משנת 2007). תוצר אחר של פעילות HO-1 הוא CO הידוע כבעל תכונות מרחיבות כלי-דם, אנטי-דלקתיות ואנטי-אפופטוטיות (Motterlini ו-Otterbeiun ב- Nat Rev Drug Discoc משנת 2010), בעוד ש-biliverdin ו-bilirubin ידועים כמולקולות אנדוגניות פוטנטיות אנטיאוסידנטיות ואנטי-דלקתיות. גם פריטין נמצא בעל השפעה אנטי-דלקתית (Bolisetti וחב' ב-Kidney Int משנת 2015). |
| + | |||
| + | בנוסף, HO-1 מגביר את האנגיוגניות של תאים סרטניים על ידי שהוא משרה את הביטוי של גורמים אנגיוגניים כגון VEGF{{כ}}(Miyake וחב' ב-Oncol Rep משנת 2011). יש ראיות מתגברות המדגימות את המעורבות של שפעול שעתוקי בתיווך Nfr2 של גנים נוגדי חמצון מה שמסייע להתמרת תאים והפיכתם לטומורוגניים (DeNicola וחב' ב-Nature משנת 2011). מוטציות ב-Nfr2 ובמעכב שלו, KEAP1, זוהו בסוגי סרטן שונים באדם (Geismann וחב' ב-Onco Targets Ther משנת 2014). כיוון ש-HO-1 מהגנים המווסתים על ידי Nfr2, נראה שהתגובה נוגדת החמצון בתיווך של HO-1 תורמת לפחות חלקית לתהליך הסרטני על ידי רמת HO-1 מוגברת. | ||
== HO-1 ו-atherosclerosis== | == HO-1 ו-atherosclerosis== | ||
| − | LDL מחומצן ביחד עם ROS משחקים תפקיד מרכזי ביצירת [[טרשת עורקית]] | + | LDL מחומצן ביחד עם ROS משחקים תפקיד מרכזי ביצירת [[טרשת עורקית]] (Anwar וחב' ב-Free Radic Biol Med משנת 2005). התפקיד של HO-1 בהגנה של דופן כלי הדם מפני טרשת, התגלתה במקרה המדווח הראשון של מטופל ללא HO-1 שניתוח לאחר המוות גילה אצלו רצועות שומן ורבדים סיביים בוותין כבר בגיל 6 שנים (Yachie וחב' ב-J Clin Invest משנת 1999). הנוכחות של HO-1 נמצאה ברבדים טרשתיים של אנשים, בעוד שלא נמצא ביטוי של HO-1 באלה עם עורקים נורמליים (Wang וחב' ב-Am J Pathol משנת 1998). תוך עיבוי של עובי הרובד ומציאות של תאי שריר חלק וסקולרי (Cheng וחב' ב-Circulation משנת 2009). בעורקים כליליים שהתקבלו מניתוחים לאחר המוות באוכלוסייה היפנית, השכיחות של HO-1 גדלה ככל שהייתה התקדמות בגודל הנגע הטרשתי ודרגת היצרות כלי הדם (stenosis) והייתה משמעותית גבוהה יותר במטופלים סוכרתיים (Song וחב' ב-Atherosclerosis משנת 2009). כמו כן, הביטוי של HO-1 גדל עם חומרת הטרשת (Morsi וחב' ב-Clin Biochem משנת 2006). השרייה של HO-1 התבררה כגורם מייצב של רובדי טרשת על ידי הפחתה של הצטברות שומנים בתוך הרובד, תוך עיבוי של עובי הרובד ומציאות של תאי שריר חלק וסקולריים (Cheng וחב' ב-Circulation משנת 2009). |
| − | סקירה סיסטמטית עדכנית של הספרות האפידמיולוגית על פולימורפיזמים של HO-1(GT)n מצאה שאלה עם repeats קצרים של הגנוטיפ SS (פחות מ- | + | סקירה סיסטמטית עדכנית של הספרות האפידמיולוגית על פולימורפיזמים של HO-1(GT)n מצאה שאלה עם repeats קצרים של הגנוטיפ SS (פחות מ-24–27) (דהיינו עם פעילות HO-1 מוגברת) היו שכיחים באחוז גבוה יותר באלה ללא מחלה קרדיו-וסקולרית ידועה. לעומת זאת, אלה עם repeats ארוכים יותר (מעל 32) על 2 האללים של HO-1 היו בעלי סיכון קרדיו-וסקולרי מוגבר, התפתחות מואצת של התהליך הטרשתי, ונטייה לרמות גבוהות יותר של פוספוליפידים מחומצנים על apolipoprotein B-100 (Pechlaner וחב' ב-Arteriosclr Thromb Vasc Biol משנת 2015). |
==הרגולציה של ביטוי HO-1 בתאי סרטן== | ==הרגולציה של ביטוי HO-1 בתאי סרטן== | ||
| − | תאי סרטן מפגינים עקה חמצונית מוגברת בגין הקצב המטבולי הגבוה שלהם. יתרה מכך, תאי סרטן מוקפים על ידי מיקרו-סביבה מורכבת, ומושפעים משמעותית עם מרכיבי סטרומה, ובעיקר על ידי הסננה של תאי דלקת (Quail ו-Joyce ב-Nat Med משנת 2013). משערים שהעקה החמצונית והגירוי על ידי מספר גורמי גדילה וציטוקינים המופרשים מתאי סטרומה, מסוגלים להשרות שעתוק של הגן של HO-1 בתאי הסרטן, על ידי שפעול של מסלולים מאותתים וגורמי שעתוק כגון Nrf-2 ,NF-κB ,AP2 ואחרים (Kappas ו-Abraham ב-Proc Natl Acad Sci USA משנת 1994. גם היפוקסיה נמצאה משרה ביטוי של HO-1. יתרה מכך, ביטוי הגן של HO-1 משודרג על ידי אונקוגנים כגון | + | תאי סרטן מפגינים עקה חמצונית מוגברת בגין הקצב המטבולי הגבוה שלהם. יתרה מכך, תאי סרטן מוקפים על ידי מיקרו-סביבה מורכבת, ומושפעים משמעותית עם מרכיבי סטרומה, ובעיקר על ידי הסננה של תאי דלקת (Quail ו-Joyce ב-Nat Med משנת 2013). משערים שהעקה החמצונית והגירוי על ידי מספר גורמי גדילה וציטוקינים המופרשים מתאי סטרומה, מסוגלים להשרות שעתוק של הגן של HO-1 בתאי הסרטן, על ידי שפעול של מסלולים מאותתים וגורמי שעתוק כגון Nrf-2 ,NF-κB ,AP2 ואחרים (Kappas ו-Abraham ב-Proc Natl Acad Sci USA משנת 1994. גם היפוקסיה נמצאה משרה ביטוי של HO-1. יתרה מכך, ביטוי הגן של HO-1 משודרג על ידי אונקוגנים כגון BCR/ABL kinase(Mayerhofer וחב' ב-Cancer Res משנת 2004). |
==ההשפעות ההמטופויאטיות של HO-1 על התהליך הסרטני== | ==ההשפעות ההמטופויאטיות של HO-1 על התהליך הסרטני== | ||
| − | נמצא ש-HO-1 יכול לאפנן (modulate) תפקודים חיסוניים רגולטוריים של תאים מיאלואידים על ידי דיכוי של ביטוי ציטוקינים מחישי-דלקת, כגון [[TNF-α]], אך באותה מידה זירוז הביטוי של ציטוקינים מדכאי-חיסון, כגון IL-10. ידוע ש-HO-1 מעודד אנגיוגניות על ידי שדרוג הביטוי של VEGF במקרופאגים. נראה ש-HO-1 יכול להשפיע על התפתחות הסרטן בדרכים שונות. HO-1 אמנם מספק הגנה כנגד התהליך הסרטני בשלבי קרצינוגנזה מוקדמים, אך הוא מעודד את ההישרדות של תאים סרטניים, את שגשוגם וגם את התהליך הגרורתי בשלבים מתקדמים של המחלה. | + | נמצא ש-HO-1 יכול לאפנן (modulate) תפקודים חיסוניים רגולטוריים של תאים מיאלואידים על ידי דיכוי של ביטוי ציטוקינים מחישי-דלקת, כגון [[TNF-α]], אך באותה מידה זירוז הביטוי של ציטוקינים מדכאי-חיסון, כגון IL-10. ידוע ש-HO-1 מעודד אנגיוגניות על ידי שדרוג הביטוי של VEGF במקרופאגים. נראה ש-HO-1 יכול להשפיע על התפתחות הסרטן בדרכים שונות. HO-1 אמנם מספק הגנה כנגד התהליך הסרטני בשלבי קרצינוגנזה מוקדמים, אך הוא מעודד את ההישרדות של תאים סרטניים, את שגשוגם וגם את התהליך הגרורתי בשלבים מתקדמים של המחלה. |
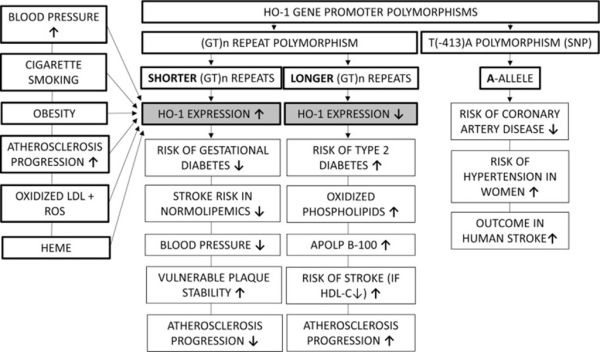
| − | [[קובץ:2HO-1.jpg|ממוזער|מרכז|600 פיקסלים|הקשר בין גורמי סיכון קרדיו-וסקולריים והביטוי של HO-1: רמות גבוהות של HO-1 כרוכות בסיכון מופחת לסוכרת, מפחיתות את לחץ הדם ומגינות מפני התקדמות תהליך טרשת העורקים.]] | + | [[קובץ:2HO-1.jpg|ממוזער|מרכז|600 פיקסלים|הקשר בין גורמי סיכון קרדיו-וסקולריים והביטוי של HO-1: רמות גבוהות של HO-1 כרוכות בסיכון מופחת לסוכרת, מפחיתות את לחץ הדם ומגינות מפני התקדמות תהליך טרשת העורקים.]] |
| − | בנוסף לתפקידו הראשי בקטבוליזם של heme{{כ}}, HMOX1 הוא בעל תכונות נוגדות חמצון ונוגדות דלקת דרך הפעילויות של biliverdin ו-CO, בהתאמה. HMOX1 מושרה במידה רבה במחלות שונות כולל סרטן. מספר ראיות תומכות במעורבות של מולקולה זו בקרצינוגניות ובהתפתחות סרטן, כאשר חסר שלו בתאים נורמליים מגביר את הנזק ל-DNA ולקרצינוגנזה, ואילו ביטוי-יתר שלו בתאים סרטניים מגביר את שגשוגם ואת הישרדותם. יתרה מכך, HMOX1 משרה אנגיוגניות. | + | בנוסף לתפקידו הראשי בקטבוליזם של heme{{כ}}, HMOX1 הוא בעל תכונות נוגדות חמצון ונוגדות דלקת דרך הפעילויות של biliverdin ו-CO, בהתאמה. HMOX1 מושרה במידה רבה במחלות שונות כולל סרטן. מספר ראיות תומכות במעורבות של מולקולה זו בקרצינוגניות ובהתפתחות סרטן, כאשר חסר שלו בתאים נורמליים מגביר את הנזק ל-DNA ולקרצינוגנזה, ואילו ביטוי-יתר שלו בתאים סרטניים מגביר את שגשוגם ואת הישרדותם. יתרה מכך, HMOX1 משרה אנגיוגניות. אף על פי ש-HMOX1 הוא חלבון הממוקם ברטיקולום האנדופלזמטי, מוצאים אותו בגרעין של תאים סרטניים, והוא משפיע על התקדמות התהליך הסרטני על ידי מודולציה של המיקרו-סביבה של הגדול הסרטני. |
| − | |||
| − | |||
| − | |||
| − | + | מספר מחקרים נערכו על מנת לאשש את הקשר בין הפולימורפיזם של הגן ל-HO-1 והסיכון לחלות ב[[סרטן הפה]] (Chang וחב' ב-Br J Cancer משנת 2004), [[אדנוקרצינומה של הריאה]] (Kikuchi וחב' ב-Hum Genet משנת 2005), [[מלנומה]] (Okamoto וחב' ב-Int J Cancer משנת 2006), [[אדנוקרצינומה של הקיבה]] (Lo וחב' ב-Ann Surg Oncol משנת 2007), [[סרטן השד]] (Hong וחב' ב-Cancer Epidemiol Biomarkers Prev משנת 2007), אדנומה קשקשית של הוושט (Hu וחב' ב-Neoplasma משנת 2010), [[סרטן הלבלב]] (Vashist וחב' ב-J Surg Oncol משנת 2011), ו[[מזותליומה]] (Muraklami וחב' ב-Lung משנת 2012). ביטוי-יתר של HO-1 נמצא באופן כללי במספר סוגי סרטן באדם כולל [[סרטן הערמונית]] (Maines ו-Abrahamsson ב-Urology משנת 1996), [[סרטן הכליות]] (Proc Soc Exp Biol Med משנת 2007), [[סרטן הקיבה]] (Yin וחב' ב-Exp Biol Med משנת 2012), [[סרטן המעי הגס]] (Yin וחב' ב-BMC Cancer משנת 2014), [[סרטן הריאות]] (Degese וחב' ב-Lung Cancer משנת 2012), [[סרטן התירואיד]] (Wang וחב' ב-Histopathology משנת 2014), [[סרטן שלפוחית השתן]] (Miyata וחב' ב-Transl Res משנת 2014), סרטן השד (Noh וחב' ב-BMC Cancer משנת 2013), סרטן הפה (Tsuji וחב' ב-Cancer Lett משנת 1999), ו[[גליומה]] (Gandini וחב' ב-Tumor Biol משנת 2014). יתרה מכך, רמת הביטוי של HO-1 נמצאה במתאם חיובי עם שלב המחלה ועם הפרוגנוזה שלה. מספר מחקרים הראו ש-HO-1 התגלה לא רק בציטופלזמה, אלא גם בגרעין של תאי סרטן הערמונית (Sacca וחב' ב-Br J Cancer משנת 2007), סרטן ריאות (Hsu וחב' ב-Oncogene משנת 2014) וסרטן הפה (Gandini וחב' ב-Exp Mol Pathol משנת 2012). דרגת הנוכחות של HO-1 בגרעין התאים הסרטניים, הייתה כרוכה עם דרגת המחלה המתקדמת ופרוגנוזה גרועה, במטופלים עם סרטן הערמונית (Weigel וחב' ב-Cancer Res משנת 2013), ובאלה עם קרצינומה של הפה (Gandini וחב' ב-Exp Mol Pathol משנת 2012). | |
| − | נזק ל-DNA הנגרם על ידי מולקולות עתירות | + | ==תפקודים פרדוקסליים של HO-1 בטומורוגניות== |
| + | נזק ל-DNA הנגרם על ידי מולקולות עתירות חמצן (ROS) הוא גורם משמעותי למוטציות. בהפחתת ביטוי של HO-1 יש הגדלה ברמת ROS וממילא נזק ל-DNA בתאים. זאת ועוד, CO משפר את הישרדות התאים על ידי שהוא משרה תיקון בנזקי DNA (Otterbein וחב' ב-Proc Natl Acad Sci USA משנת 2011). לפיכך הגברת הביטוי של HO-1 מונעת נזק ל-DNA ואתחול התהליך הטומורוגני בתאים נורמלים. עם זאת, בשלב מאוחר של טומורוגנזה, ביטוי-יתר של HO-1 מגביר את הפרוליפרציה של תאי הסרטן ואת היכולת שלהם לייצר גרורות (Sunamura וחב' ב-Angiogenesis משנת 2003, Chen וחב' ב-J Cell Biochem משנת 2004, ו-Was וחב' ב-Am J Pathol משנת 2006). HO-1 מגן על תאים סרטניים מפני apoptosis שגורמים חומרים כימו-טוקסיים או קרינה, מה שמרמז על מעורבות HO-1 בעמידות תאים סרטניים לטיפולים תרפויטיים שונים (Liu וחב' ב-Oncogene משנת 2004, Berberat וחב' ב-Clin Cancer Res משנת 2005, Kweon וחב' ב-J Biol Chem משנת 2006, Kocanova וחב' ב-Apoptosis משנת 2007, Furfaro וחב' ב-Biochim Biophys Acta משנת 2014, Kongpetch וחב' ב-PLos One משנת 2012). | ||
| − | השפעול | + | ==השפעול של Nfr2== |
| + | הפעילות כנגד HO-1 מצטיירת כגישה יעילה לפחות בסרטן הערמונית העמיד לטיפול הורמונלי (Sporn ו-Liby ב-Nat Rev Cancer משנת 2012), והיא גם מתגברת על העמידות ל-imatinib ב-CML (Alaoui-Jamali וחב' ב-Cancer Res משנת 2009). פעילות זו של HO-1 גם מגבירה את הרגישות של הפאטומה, ושל סרטני הערמונית ומערכת השתן לכימותרפיה (Mayerhofer וחב' ב-Blood משנת 2008). המיקום של HO-1 בתוך גרעין התא, מעודד את הגידול הסרטני ואת הגרורתיות שלו, באופן בלתי-תלוי בפעילותו האנזימטית. | ||
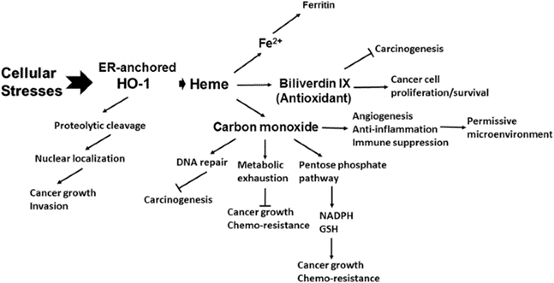
| − | + | [[קובץ:3HO-1.png|ממוזער|מרכז|600 פיקסלים|תפקידים מגוונים של HO-1 בתהליך הסרטני: CO ו-biliverdin הנובעים מפירוק heme על ידי HO-1, מקנים הגנה לתאים נורמליים מפני התמרה ששלבים המוקדמים של טומורוגניות, אך מסייע לשגשוג ולהישרדות של תאים סרטניים בשלבי מחלה מאוחרים.]] | |
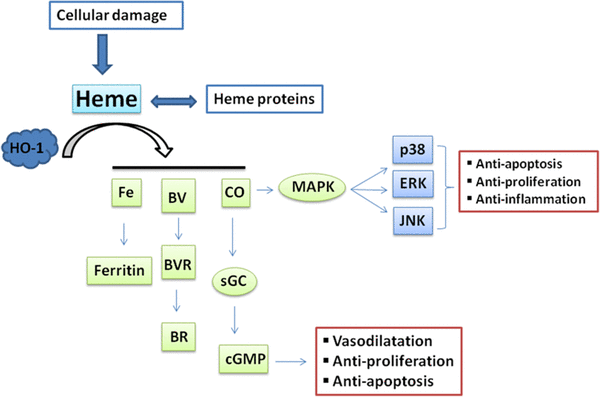
| + | [[קובץ:4HO-1.png|ממוזער|מרכז|600 פיקסלים|תרשים המראה את המנגנון המגן על התאים של HO-1 על ידי תוצרי הפירוק של ה-heme.]] | ||
| − | + | ==הוראות לביצוע הבדיקה== | |
| + | דם נלקח במבחנה כימית (פקק אדום או צהוב) ולאחר קרישתו וסרכוזו, הנסיוב משמש לבדיקת ELISA בערכה המקובלת, ImmunoSet TM HO-1 Elisa kit של חברת (Enzo (Framingdale. | ||
| + | ==ראו גם== | ||
| + | * [[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | ||
| + | * [[בדיקות ביוכימיות|בדיקות מעבדה - בדיקות ביוכימיות]] | ||
| − | + | {{ייחוס בן עמי}} | |
| − | + | [[קטגוריה:בדיקות מעבדה - בדיקות ביוכימיות]] | |
| − | + | [[קטגוריה:בדיקות מעבדה: כימיה בדם]] | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
גרסה אחרונה מ־03:12, 8 בדצמבר 2022
| מדריך בדיקות מעבדה | |
| הם אוקסידאז | |
|---|---|
| Heme oxidase | |
| שמות אחרים | HMOX, HO-1. Heme oxygenase, Haem oxidase |
| מעבדה | כימיה בדם |
| תחום | מולקולה אנזימטית המקטלזת את פירוק ה- heme והיא מעורבת בתהליכים מטבוליים רבים, בתהליכים סרטניים ובמחלות נוספות. |
| טווח ערכים תקין | 31.7 ננוגרם/מ"ל |
| יוצר הערך | פרופ' בן-עמי סלע |
ההיסטוריה של HMOX1
אנזים זה אופיין לראשונה על ידי Tenhunen ו-Scmidtftar שתיארו את היותו אחראי לקטליזה של הפיכת heme לבילירובין (Hupper וחב' ב-Nitric Oxide משנת 2021). מספר מעבדות ניסו להסביר את המהלך של התמרת heme ל-biliverdin, ואכן הופיעו מספר הסברים להפיכה לא-אנזימטית של ריאקציה זו. הראיה המוקדמת ביותר של ביו-טרנספורמציה זו פורסמה על ידי Plieninger ו- Fischer בשנת 1942. המוגלובין תואר לראשונה בשנות ה-40 של המאה ה-19, על ידי Hunefeld (Boor ב-General Physiology משנת 1930), וגרעין ה-heme שלו תואר לראשונה על ידי Teichmann ב-1853, אך רק כמעט 100 שנים מאוחר יותר, תיאר Irving London את היצירה של המוגלובין. חד תחמוצת הפחמן (CO) באוויר הננשף מהריאות זוהה בשנת 1869, כאשר von Fodor פיתח את המדידה הכמותית הראשונה של קרבוקסי-המוגלובין. הדיווח הראשון של זיהוי CO בדם אנושי היה בשנת 1923 על ידי Sayers וחב', אף על פי שחוקרים אלה התכחשו לתגליתם זו בהנחה שמדובר בטעות אקראית. בשנת 1933 אישר Gettler של-CO יש נוכחות נורמלית בדם, אך הוא פרש זאת לחשיפה בלתי נמנעת למזהמים סביבתיים, או שמקורו במיקרוביום האנושי (Hopper וחב' משנת 2020). רק בשנת 1952 הדגים Sjostrand שיצירת CO נובעת מתהליך הפירוק של המוגלובין.
Heme אוקסידאז
Heme oxidase (להלן HMOX) הוא אנזים המקטלז את הפירוק של heme ליצירה של יון ברזל דו-ערכי, biliverdin ו-CO (Ryter וחב' ב- Physiol Rev משנת 2006). ישנם אנזימים מפרקי heme רבים, אך רק אלה מהם המפרקים heme אארובי נחשבים ל-אנזימים דומי-HMOX בעוד שאנזימים אנארוביים אינם משתייכים למשפחת HMOX.
הגנום האנושי יכול לקודד לשלושה איזופורמים של HMOX. הפירוק של heme יוצר שלושה כרומוגנים, וריאקציה זו יכולה להתרחש בכל תא או תרומבוציט, כאשר הדוגמה הקלאסית היא תהליך הריפוי של חבלה, בה נוצרים שלושה כרומוגנים שונים בתהליך הריפוי: כרומוגן אדום, ההופך לירוק ביצירת biliverdin ההופך צהוב בהופעת בילירובין. אף על פי ש-HMOX מופיע בכל הגוף, הוא פעיל במיוחד בטחול בו הוא מסייע לפירוק של המוגלובין במהלך המחזור של אריתרוציטים. מלבד הטחול, ריכוזים גבוהים שלו מוצאים בכבד, ובכליות, וברמה התאית HMOX1 ממוקם בעיקר ברטיקולום האנדופלזמטי, וניתן לאתר אותו גם במיטוכונדריה, בגרעין התא, ובממברנה החיצונית של התא (Hopper וחב' ב-Curr Pharmaceut Design משנת 2018). HMOX יכול גם לשמש כחלבון chaperone, המעורב באינטראקציות בין חלבונים, וכן הוא יכול להיות מופרש אל תוך ציטופלזמת התא ולהשתתף בריאקציות שונות מעבר לתפקידו הקטליטי.
Heme oxydase 1: איזופורם זה, HMOX1, הוא חבר במשפחת ה-heat shock proteins המכונה גם HSP32.כיוון שמשקלו המולקולרי הוא 32,000 דלטון, והוא מכיל 288 חומצות אמינו, ומקודד על ידי הגן HMOX1 חלבון זה אינו hemoprotein כיוון שהוא אינו מכיל קבוצות פרוסטתיות של heme (Kikuchi וחב' ב-Biochem Biophys Res Commun משנת 2005). הפעילות של HMOX1 תלויה באנזים NADPH-cytochrome P450 reductase (Wang וחב' ב-J Biol Chem משנת 2003). HMOX1 הוא אנזים חיוני אך יש רק מצבים נדירים של חסר שלו מה מסתיים במוות. במחלות אחדות פעילותו של HMOX1 בעייתית. לדוגמה, חלבון זה מסוגל לפעול נגד פעילותם של תרופות כימותרפויטיות, ובכך הוא עלול לתרום לשגשוגם של תאים סרטניים (Schipper וחב' ב-Prog Neurobiol משנת 2019, Jozkowiicz וחב' ב-Antioxidants Redox Signaling משנת 2007, ו-Podkalicka וחב' ב-Contemp Oncol משנת 2018). HMOX1 מעוכב על ידי מספר פורפירינים כגון zinc protoporphyrin (Vreman וחב' ב-Canadian J Physiol Phermacol משנת 1996).
cDNA של HMOX1 שובט לראשונה מטחול של חולדה בשנת 1985 (Alam וחב' ב-J Biol Chem משנת 1989), ורצף חומצות האמינו גילה מקטע הידרופובי בקצה ה-C-טרמינלי, הדרוש לתאחיזה ברטיקולום האנדופלמטי. HMOX1 מבוטא במידה רבה באיברים האחראיים להרס של אריתרוציטים מזדקנים, וכן תאי טחול ותאים רטיקולו-אנדותליאליים בכבד ובמח העצם. אף על פי שהביטוי הבסיסי של HMOX1 נמוך ברקמות שאינן אחראיות ישירות במטבוליזם של המוגלובין, HMOX1 מבוטא בחוזקה בתאים הנחשפים לעקה על ידי מתכות כבדות, אנדוטוקסין, ציטוקינים, heme, היפוקסיה, NO ו-קרינת UV ( Keise וחב' ב-Mol Cell Biol משנת 1990, Lizzardini וחב' ב-Biochem J משנת 1993, Cantoni וחב' באותו כתב עת משנת 1991,ו- Lee וחב' ב-J Biol Chem משנת 1997).
Heme oxydas 2: איזופורם זה, HMOX2, הוא חלבון קונסטיטוטיבי המתבטא בתנאים הומאוסטטיים באשכים, במערכת העיכול, בתאי אנדותל, ובמוח (Munoz--Snschez ו-Chanes-Cardenaz ב-Oxidative Med Cell Longevity משנת 2014). איזופורם זה שמשקלו המולקולרי 36,000 דלטון מקודד על ידי הגן HMOX2 ויש לו זהות של 47% ברצף חומצות האמינו עם HMOX1. הוא שונה מ-HMOX1 בהכילו מקטע נוסף של 20 חומצות אמינו בקצה ה-N-טרמינלי, וכן בהיות HMOX2 הפופרוטאין בהכילו שיירי heme. בנוסף, בעוד ש-HMOX1 מושרה על ידי מספר משרנים, HMOX2 מושרה רק על ידי גלוקו-קורטיקואידים מהאדרנל, אם כי מספר מולקולות נוספות יכולות להגביר את מהירותו הקטליטית, ואילו אופיואידים יכולים לעכב את פעילותו.
Heme oxydase 3: איזופורם שנוי במחלוקת זה, אינו פעיל קטליטית, וההשערה היא שהוא מעורב בחישת heme או בדה-טוקסיפיקציה שלו. HMOX3 הוא בעל משקל מולקולרי של 33,000 דלטון, והנוכחות הגדולה ביותר שלו היא בכבד, בבלוטת הערמונית ובכליות.
Heme oxygenase מיקרוביאליים: האנזים heme oxygenase משומר פילוגנטית ביצורים מ-species מרוחקים (Li ו-Stocker ב-Redox Rep משנת 2009). המיקרוביום האנושי מכיל עשרות הומולוגים של HMOX מיקרוביאלי כגון HMX1 ממקור של Saccharomyces cerevisiae, ChuS ממקור של E.Coli, ו-HmuO ממקור של Corynebacterium diphtheriiae. התפקיד הקריטי של מערכות HMOX היפרוקריוטיות, הוא לסייע לקליטה של ברזל תזונתי מהפונדקאי האאוקריוטי (Frankenberg -Dinkel ב-Antioxidants Redox Signaling משנת 2004).
משרנים של HMOX1
HMOX1 מושרה על ידי מספר רב של מולקולות הכוללות מתכות כבדות, סטאטינים, paclitaxel, חד תחמוצת הפחמן, rapamycin, probucol, ,NO ,sildenafil ומספר פורפירינים (Ferrandiz ו-Deesa ב-Curr Pharmaceut Design משנת 2008). משרנים אנדוגניים כוללים ליפידים כגון lipoxin ו-epoxyeicosatrienoic acid, ופפטידים כגון adrenomedullin ו-apolipoprotein, וכן הוא מושרה על ידי hemin, hydroxycoumarin, genistein, חומצה ניטרואולאית, H2O2, succinykacetone ועוד (Ma ו-He ב-Pharmacol Rev משנת 2012).
התפקידים הפיזיולוגיים של HMOX
HMOX משתתף במספר תהליכים תאיים (Kim וחב' ב-Cell Mol Immunol משנת 2018, ו-Ryter וחב' ב-Cell Mol Biochem משנת 2002). היתרונות ההגנתיים התאיים של HMOX הגבירו את כמות המחקרים על פעילותיו הפרמוקולוגיות והשפעותיו הפוטנציאליות (Cheng ו-Rong ב-Curr Pharmceut Design משנת 2017).
חד תחמוצת הפחמן (CO) ו-HMOX
המרכיב העיקרי ביצירת CO אנדוגני הוא HMOX1 (Motterlini וחב' ב-Nat Rev Drug Discov משנת 2010), אף על פי שמולקולות נוספות תורמות באופן מופחת ליצירת CO. מולקולה זו מיוצרת בקצב של 16.4 מיקרומול/שעה בגוף האדם, כאשר 86% בערך מגיעים מפירוק Heme על ידי HMOX, ו-14% הנותרים מקורם ממקור שאינו heme, כולל פוטו-אוקסידציה, פראוסידציה של ליפידים ושל חומצות keto מהמיקרוביום או מקסנוביוטיקה (Hopper וחב' ב-Chem Rev משנת 2020). רמת קרבוקסי-המוגלובין (CO-Hb) הממוצעת בדם של לא-מעשנים היא בין 0.2 עד 0.85%, בעוד שרמתו בדמם של מעשנים יכולה להגיע ל-4 עד 10%. המִחְזוּר של אריתרוציטים בטחול הוא המקור של כ-80% של ה-CO ממקור ה-heme הנוצר אנדוגנית. יתר 20 האחוזים של יצירת CO ממקור heme מיוחסים לתהליכים קטבוליים של hemoproteins כגון מיוגלובין, ציטוכרומים, catalases, פראוקסידאזות, guanylate cyclase מסיס, והאנזים nitric synthase בכבד, וכן אריתרפויאזה בלתי יעילה במח העצם (Vreman וחב' ב-CRC Press משנת 2001). בנוסף להיות heme מקור של CO, ה-heme הוא גם מעביר איתותים קריטיים הקשורים בחישה של CO (Shimizu וחב' ב-Chem Rev משנת 2019). כגורם מאותת, CO קשור לתהליכים פיזיולוגיים נורמליים ויש לו יתרונות תרפויטיים בשיפור של מצבי דלקת והיפוקסיה (Motterlini ו-Foresti ב-Am J Physiol משנת 2017). עם זאת נשאלת השאלה באיזה מידה HMOX מעורב בהשפעה מגינה של כנגד היפוקסיה, שכן שלושה שווי-ערך של חמצן נדרשים כדי לייצר CO מתהליכי קטבוליזם של heme במקביל לאלה של רמת הזמינות של heme (Leung וחב' ב-Proc Natl Acad Sci USA משנת 2021), ובנוסף היצירה האיטית של heme שנמשכת מספר שעות (Pellacani וחב' ב-Circulation Res משנת 1998).
Biliverdin HMOX ו-Bilirubin
קיים תיעוד עתיק על הבילירובין הנוצר אנדוגנית בכתבי היפוקרטס (Watson בכינוס על הפיזיולוגיה של בילירובין משנת 1977). ברוב המקרים, HMOX מבקע את ה-heme של protoporphyrin IX בגשר α-methine, ליצירת הבילירובין. Biliverdin IXα עובר ביו-טרנספורמציה דרך biliverdin reductase ליצירה של bilirubin IXα (Wegiel ו-Otterbain ב-Front Pharmacol משנת 2012).ה-bilins משחקים תפקיד חשוב בממלכות הפילוגנטיות (Takemoto וחב' ב-Israel J Chem משנת 2019).
יון ferrous: יון הברזל הדו-ערכי המשתחרר מ-HMOX "נלכד" במהירות על ידי פריטין. עם זאת, יוני חמצן פעילים (ROS, המשתחררים בריאקציות Fenton או Haber-Weiss) מסוגלים לשגר איתותים תאיים (Sies ו-Jones ב-Nat Rev Mol Cell Biol משנת 2020, ו-NaveenKumar וחב' ב-ACS Cell Biol משנת 2018, ו- Frankenberg -Dinkel ב-Antioxidants Redox Signaling משנת 2004).
הריאקציה המקוטלזת על ידי HMOX1
ריאקציה זו יכולה להתרחש בכל תא. במושגים של מנגנונים מולקולריים, האנזים מסייע להידרוקסילציה של פחמן meso אחד במרכז ה-heme (Yoshida ו-Mikita ב-J Inorganic Chem משנת 2000). HMOX1 אחראי להגבלת הקצב של הקטבוליזם של heme התלוי ב-NADPH-cytochrome p450 reductase ובחמצן כדי לבקע את טבעת הפורפירין של heme בגשר של α-methene ליצירה של biliverdin. הריאקציה מתבצעת בשלושה שלבים (Evans וחב' ב-J Biol Chem משנת 2008):
Heme b3+ + O2 + NADPH + H+→ α-meso-hydroxyheme3+ + NADP++ H2O
α-meso-hydroxyheme3+ + H+ + O2 → verdoheme4+ + CO + H2O
verdoheme4+ + 7/2 NADPH + O2+ 3/2 H+ → biliverdin + Fe2+ + 7/2 NADP+ H2O
סך הריאקציות הללו הוא:
Heme b3+ + 3O2 + 9/2 NADPH + 7/2 H+ → biliverdin + Fe2+ + CO + 9/2 NADP++ 3H2O
ואם הברזל נמצא בתחילה דו-ערכי (ferrous), הריאקציה יכולה להיות:
Heme b2+ + 3O2 + 4 NADPH + 4 H+ → biliverdin + Fe2+ + CO + 4 NADP+ + 3H2O
ריאקציה זו יכולה להתרחש בכל תא. במושגים של מנגנונים מולקולריים, האנזים מסייע להידרוקסילציה של פחמן meso אחד במרכז ה-heme (Yoshida ו-Mikita ב-J Inorganic Chem משנת 2000).
הרלוונטיות הקלינית של HO-1 בשבץ-מוחי איסכמי
שבץ-מוחי הוא הגורם השני במעלה למוות בעולם האחראי ל-6 מיליון מקרי מוות בשנה וגורם חשוב לפגיעה ממושכת בתפקוד הגופני, ולנכות קבועה. (Mozaffarian ב-Circulation משנת 2000). עקה חמצונית היא גורם מרכזי באיסכמיה מוחית, הגורמת לנזק נוירונלי בלתי הפיך. אחד ממנגנוני ההגנה התאית הוא הציר Nfr2-HO-1. שבץ איסכמי הוא תרחיש של אי-תפקוד נוירונלי הנגרם על ידי אוטם מוחי, ספינלי או רטינלי (Sacco וחב' ב-Stroke משנת 2013). עקה חמצונית עם ROS הגורמת נזק למרכיבים תאיים כולל חלבונים, ליפידים וחומצות גרעין, משחקת תפקיד מרכזי במהלך איסכמיה מוחית, מה שמוביל לנזק לנוירונים עד כדי מותם (Chen וחב' ב-Brain Res משנת 2012, Yamauchi וחב' ב-Neuroscience משנת 2016, ו-Lv וחב' ב-Cell Physiol Biochem משנת 2017).
בין מודלים של שבץ מוחי בחיות חסימה של עורק המוח המרכזי נבחנה במספר רב של ניסויים על שבץ איסכמי (Howells וחב' ב-J Cereb Blood Flow Metab משנת 2010, ו-Fluri וחב' ב-Drug Des Devel Ther משנת 2015). מודל MCAO נחשב כמודל מתאים לחקות שבץ איסכמי באדם, עם מוות של נוירונים, דלקת מוחית ונזק למחסום דם-מוח. ניסוי מוקדם תוך שימוש ב- MACO בעכברים טרנסגניים הראה שביטוי-יתר של HO-1, הפחית משמעותית את נפח האוטם (Panahian וחב' ב-J Neurochem משנת 1999). לעומת זאת, בעכברי knockout ללא HO-1. נפח האוטם נמצא גדול יותר משמעותית בהשוואה לזן הבר שלהם. באדם, הביטוי של HO-1 מראה שונוּת רבה בגין promoter מאוד פולימורפי, שנכרך עם גורמי סיכון קרדיו-וסקולריים. הווריאנט הנחקר ביותר היה האורך של מקטע ה-(GT)n-repeat, שהיה כרוך באופן הופכי עם הביטוי של HO-1 (Chen וחב' ב-Hum Gen משנת 2002). בסקר אוכלוסייה פרוספקטיבי, נמצא שאלה עם repeats ארוכים יותר (מעל 32) על 2 האללים של HO-1 היו בעלי סיכון קרדיו-וסקולרי מוגבר, התפתחות מואצת של התהליך הטרשתי, ונטייה לרמות גבוהות יותר של פוספוליפידים מחומצנים על apolipoprotein B-100 (Pechlaner וחב' ב-Thromb Vasc Biol Arteriosclr משנת 2015). סקירה סיסטמטית עדכנית של הספרות האפידמיולוגית על פולימורפיזמים של HO-1(GT)n, מצאה שאלה עם repeats קצרים של הגנוטיפ SS (פחות מ-24–27) (דהיינו עם פעילות HO-1 מוגברת) נמצאו באחוז גבוה יותר באלה ללא מחלה קרדיו-וסקולרית ידועה.
HMOX ויתר לחץ-דם
הראיות על הקשר בין ביטוי HMOX1 ויתר לחץ-דם מגיעות מניסויים בחיות תוך שימוש בחולדות המפתחות באופן ספונטני לחץ-דם גבוה. כאשר מבצעים עירוי כרוני של angiotensin II לחולדות לחץ הדם הגבוה המושרה, מגביר את הביטוי של HMOX1 בוותין של החולדות (Ishizaka וחב' ב-Circulaion משנת 1997). יתרה מכך, כאשר מזריקים לחולדות אלו HMOX1 אנושי, מוצאים חחלשה של התפתחות יתר לחץ-דם, המיוחסת להרחבת כלי הדם על ידי CO (Sabaawy וחב' ב-Hypertension משנת 2001). ההשפעה המורידה לחץ-דם של טיפול למשך 3 חודשים עם olmesartan יוחסה בחלקה לעלייה בריכוז של ho-1 בפלזמה (Calò וחב' ב-Blood Press משנת 2011). בין המטבולים הקטבוליים של HO-1, הריכוזים של בילירובין נמצאו מופחתים משמעותית במטופלים עם יתר לחץ-דם בלתי מטופל, בעוד שריכוזי בילירובין לא השתנו באלה עם לחץ-דם נורמלי או במטופלים עם יתר לחץ-דם מטופלים כנגדו (Papadakis וחב' ב-Am J Hypertens משנת 1999). יתרה מכך, במעקב שנמשך 10 שנים בקוריאנים עם לחץ-דם תקין, רמות בילירובין בנסיוב ורמות מוגברות של לחץ-דם נמצאו עם מתאם שלילי (Chin וחב' ב-J Korean Med Sci משנת 2009). בנשים עם יתר לחץ-דם בהיריון, או באלו עם pre-eclampsia, רמות CO באוויר הנשאף היו נמוכות משמעותית בהשוואה לרמות אלה בנשים בריאות (Kreiser וחב' ב-J Perinatol משנת 2004).
HMOX וסוכרת
הביטוי של HO-1 בסוכרת נמצאו במתאם רציפרוקלי בניסויים בחיות, דהיינו ביטוי יתר של HO-1 היה כרוך בהתקדמות סוכרת בעכברי NOD, או השרייה של HO-1 בחולדות Zucker סוכרתיות, שפרה את הרגישות לאינסולין (Hu וחב' ב-Diabetes משנת 2007, ו-Nicolai וחב' ב-Hypertension משנת 2009). בבני-אדם הביטוי של HO-1 נמצא מופחת בדם ההיקפי בתאים מונו-נוקלאריים של חולי סוכרת (Song וחב' ב-Am J Epidemiol משנת 2009), בעוד שרמות ביטוי גבוהות של HO-1 בשלבי היריון מוקדמים, נכרכו עם סיכון מופחת של סוכרת הריונית (Qiu וחב' ב-One PLoS משנת 2012). יתרה מכך, ריכוזים מוגברים של HO-1 בפלזמה, היו קשורים עם סיכון מוגבר לפתח סוכרת type II (Bao וחב' ב-PLos One משנת 2010). המשרן של HO-1 ,Nrf2, נמצא בריכוז נמוך יותר במטופלים סוכרתיים וקדם-סוכרתיים, מה שמרמז שמנגנונים אנטי אוקסידנטים מוחלשים כתוצאה מירידה בריכוז Nrf2, עשויים להיות קשורים בהתפתחות של סוכרת (Jiménez-Osario וחב' ב-Int J Mol Sci משנת 2014). מטופלים עם רמות מוגברות של בילירובין בנסיוב, היו בסיכון מופחת לחלות בסוכרת (Cheriyath וחב' ב-J Clin Med Res משנת 2010). במטופלים עם תסמונת Gilbert וסוכרת, היפר-בילירובינמיה נכרכה על שכיחות מופחתת של אירועי סיבוכים וסקולריים, בהשוואה לאלה שהם סוכרתיים בלבד (Inoguchi וחב' ב-JAMA משנת 2007). בהתחשב בתוצאות הניסויים האחרונים היפר-בילירובינמיה מושרית ניסויית משך 3 ימים עם atazanavir בבני-אדם עם סוכרת type2 בניסוי כפול-סמיות ומבוקר כנגד פלצבו, נמצא גורם לשיפור משמעותי בתפקוד האנדותליאלי (Dekker וחב' ב- Atheriosclr Thromb Vasc biol משנת 2011).
בין גורמי השעתוק, Nrf2 (או nuclear factor erythroid 2-related factor 2) הוא בעל תפקיד מרכזי בהגנה מפני עקה חמצונית (Ishii וחב' ב-J Biol Chem משנת 2000). במצבים של חוסר איזון ב-redox, Nrf2 משפעל אנזימים אנטי-אוקסידנטים אחדים, כגון glutathione-S-trnsferase glutamyl cysteine synthetase ,γ, וריאקציה זו יכולה להתרחש בכל תא. במושגים של מנגנונים מולקולריים, האנזים מסייע להידרוקסילציה של פחמן meso אחד במרכז ה-heme (Yoshida ו-Mikita ב-J Inorganic Chem משנת 2000), ו-heme oxygenase או HO-1 על ידי התקשרות עם AREs (או antioxidant response elements) ועל ידי כך מושרה ביטוי גני (Kobayashi וחב' ב-Meth Enzymol משנת 2004). בין אנזימים אלה, HO-1 דווח כאנזים המכיל את הכי הרבה AREs על הפרומוטר שלו (Chumboutong וחב' ב-Neurochem Int משנת 2017), מה שהופך אותו ליעד תרפויטי מבטיח כנגד נזק מוחי בעת יצירת אוטם מוחי. HO-1 יכול להיות משופעל על ידי גירויים שונים כגון אינפקציות, מתכות כבדות, קרינת UV, חום, ציטוקינים דלקתיים ו-LDL מחומצן (Ameriso וחב' ב-Stroke משנת 2005). HO-1 מקטלז פירוק heme ליצירה של כמויות אקווי-מולריות של ברזל (Fe2+) חד תחמוצת הפחמן (CO) ו-biliverdin-IX. הברזל המשתחרר משרה ביטוי של פריטין, הגורם להַפְקָעָה של Fe2+ והגבלת הנזק לתאים המתווך על ידי ברזל (Balla וחב' ב-J Biol Chem משנת 1992, ו-Balla וחב' ב-Antioxid Redox Signal משנת 2007). תוצר אחר של פעילות HO-1 הוא CO הידוע כבעל תכונות מרחיבות כלי-דם, אנטי-דלקתיות ואנטי-אפופטוטיות (Motterlini ו-Otterbeiun ב- Nat Rev Drug Discoc משנת 2010), בעוד ש-biliverdin ו-bilirubin ידועים כמולקולות אנדוגניות פוטנטיות אנטיאוסידנטיות ואנטי-דלקתיות. גם פריטין נמצא בעל השפעה אנטי-דלקתית (Bolisetti וחב' ב-Kidney Int משנת 2015).
בנוסף, HO-1 מגביר את האנגיוגניות של תאים סרטניים על ידי שהוא משרה את הביטוי של גורמים אנגיוגניים כגון VEGF(Miyake וחב' ב-Oncol Rep משנת 2011). יש ראיות מתגברות המדגימות את המעורבות של שפעול שעתוקי בתיווך Nfr2 של גנים נוגדי חמצון מה שמסייע להתמרת תאים והפיכתם לטומורוגניים (DeNicola וחב' ב-Nature משנת 2011). מוטציות ב-Nfr2 ובמעכב שלו, KEAP1, זוהו בסוגי סרטן שונים באדם (Geismann וחב' ב-Onco Targets Ther משנת 2014). כיוון ש-HO-1 מהגנים המווסתים על ידי Nfr2, נראה שהתגובה נוגדת החמצון בתיווך של HO-1 תורמת לפחות חלקית לתהליך הסרטני על ידי רמת HO-1 מוגברת.
HO-1 ו-atherosclerosis
LDL מחומצן ביחד עם ROS משחקים תפקיד מרכזי ביצירת טרשת עורקית (Anwar וחב' ב-Free Radic Biol Med משנת 2005). התפקיד של HO-1 בהגנה של דופן כלי הדם מפני טרשת, התגלתה במקרה המדווח הראשון של מטופל ללא HO-1 שניתוח לאחר המוות גילה אצלו רצועות שומן ורבדים סיביים בוותין כבר בגיל 6 שנים (Yachie וחב' ב-J Clin Invest משנת 1999). הנוכחות של HO-1 נמצאה ברבדים טרשתיים של אנשים, בעוד שלא נמצא ביטוי של HO-1 באלה עם עורקים נורמליים (Wang וחב' ב-Am J Pathol משנת 1998). תוך עיבוי של עובי הרובד ומציאות של תאי שריר חלק וסקולרי (Cheng וחב' ב-Circulation משנת 2009). בעורקים כליליים שהתקבלו מניתוחים לאחר המוות באוכלוסייה היפנית, השכיחות של HO-1 גדלה ככל שהייתה התקדמות בגודל הנגע הטרשתי ודרגת היצרות כלי הדם (stenosis) והייתה משמעותית גבוהה יותר במטופלים סוכרתיים (Song וחב' ב-Atherosclerosis משנת 2009). כמו כן, הביטוי של HO-1 גדל עם חומרת הטרשת (Morsi וחב' ב-Clin Biochem משנת 2006). השרייה של HO-1 התבררה כגורם מייצב של רובדי טרשת על ידי הפחתה של הצטברות שומנים בתוך הרובד, תוך עיבוי של עובי הרובד ומציאות של תאי שריר חלק וסקולריים (Cheng וחב' ב-Circulation משנת 2009).
סקירה סיסטמטית עדכנית של הספרות האפידמיולוגית על פולימורפיזמים של HO-1(GT)n מצאה שאלה עם repeats קצרים של הגנוטיפ SS (פחות מ-24–27) (דהיינו עם פעילות HO-1 מוגברת) היו שכיחים באחוז גבוה יותר באלה ללא מחלה קרדיו-וסקולרית ידועה. לעומת זאת, אלה עם repeats ארוכים יותר (מעל 32) על 2 האללים של HO-1 היו בעלי סיכון קרדיו-וסקולרי מוגבר, התפתחות מואצת של התהליך הטרשתי, ונטייה לרמות גבוהות יותר של פוספוליפידים מחומצנים על apolipoprotein B-100 (Pechlaner וחב' ב-Arteriosclr Thromb Vasc Biol משנת 2015).
הרגולציה של ביטוי HO-1 בתאי סרטן
תאי סרטן מפגינים עקה חמצונית מוגברת בגין הקצב המטבולי הגבוה שלהם. יתרה מכך, תאי סרטן מוקפים על ידי מיקרו-סביבה מורכבת, ומושפעים משמעותית עם מרכיבי סטרומה, ובעיקר על ידי הסננה של תאי דלקת (Quail ו-Joyce ב-Nat Med משנת 2013). משערים שהעקה החמצונית והגירוי על ידי מספר גורמי גדילה וציטוקינים המופרשים מתאי סטרומה, מסוגלים להשרות שעתוק של הגן של HO-1 בתאי הסרטן, על ידי שפעול של מסלולים מאותתים וגורמי שעתוק כגון Nrf-2 ,NF-κB ,AP2 ואחרים (Kappas ו-Abraham ב-Proc Natl Acad Sci USA משנת 1994. גם היפוקסיה נמצאה משרה ביטוי של HO-1. יתרה מכך, ביטוי הגן של HO-1 משודרג על ידי אונקוגנים כגון BCR/ABL kinase(Mayerhofer וחב' ב-Cancer Res משנת 2004).
ההשפעות ההמטופויאטיות של HO-1 על התהליך הסרטני
נמצא ש-HO-1 יכול לאפנן (modulate) תפקודים חיסוניים רגולטוריים של תאים מיאלואידים על ידי דיכוי של ביטוי ציטוקינים מחישי-דלקת, כגון TNF-α, אך באותה מידה זירוז הביטוי של ציטוקינים מדכאי-חיסון, כגון IL-10. ידוע ש-HO-1 מעודד אנגיוגניות על ידי שדרוג הביטוי של VEGF במקרופאגים. נראה ש-HO-1 יכול להשפיע על התפתחות הסרטן בדרכים שונות. HO-1 אמנם מספק הגנה כנגד התהליך הסרטני בשלבי קרצינוגנזה מוקדמים, אך הוא מעודד את ההישרדות של תאים סרטניים, את שגשוגם וגם את התהליך הגרורתי בשלבים מתקדמים של המחלה.
בנוסף לתפקידו הראשי בקטבוליזם של heme, HMOX1 הוא בעל תכונות נוגדות חמצון ונוגדות דלקת דרך הפעילויות של biliverdin ו-CO, בהתאמה. HMOX1 מושרה במידה רבה במחלות שונות כולל סרטן. מספר ראיות תומכות במעורבות של מולקולה זו בקרצינוגניות ובהתפתחות סרטן, כאשר חסר שלו בתאים נורמליים מגביר את הנזק ל-DNA ולקרצינוגנזה, ואילו ביטוי-יתר שלו בתאים סרטניים מגביר את שגשוגם ואת הישרדותם. יתרה מכך, HMOX1 משרה אנגיוגניות. אף על פי ש-HMOX1 הוא חלבון הממוקם ברטיקולום האנדופלזמטי, מוצאים אותו בגרעין של תאים סרטניים, והוא משפיע על התקדמות התהליך הסרטני על ידי מודולציה של המיקרו-סביבה של הגדול הסרטני.
מספר מחקרים נערכו על מנת לאשש את הקשר בין הפולימורפיזם של הגן ל-HO-1 והסיכון לחלות בסרטן הפה (Chang וחב' ב-Br J Cancer משנת 2004), אדנוקרצינומה של הריאה (Kikuchi וחב' ב-Hum Genet משנת 2005), מלנומה (Okamoto וחב' ב-Int J Cancer משנת 2006), אדנוקרצינומה של הקיבה (Lo וחב' ב-Ann Surg Oncol משנת 2007), סרטן השד (Hong וחב' ב-Cancer Epidemiol Biomarkers Prev משנת 2007), אדנומה קשקשית של הוושט (Hu וחב' ב-Neoplasma משנת 2010), סרטן הלבלב (Vashist וחב' ב-J Surg Oncol משנת 2011), ומזותליומה (Muraklami וחב' ב-Lung משנת 2012). ביטוי-יתר של HO-1 נמצא באופן כללי במספר סוגי סרטן באדם כולל סרטן הערמונית (Maines ו-Abrahamsson ב-Urology משנת 1996), סרטן הכליות (Proc Soc Exp Biol Med משנת 2007), סרטן הקיבה (Yin וחב' ב-Exp Biol Med משנת 2012), סרטן המעי הגס (Yin וחב' ב-BMC Cancer משנת 2014), סרטן הריאות (Degese וחב' ב-Lung Cancer משנת 2012), סרטן התירואיד (Wang וחב' ב-Histopathology משנת 2014), סרטן שלפוחית השתן (Miyata וחב' ב-Transl Res משנת 2014), סרטן השד (Noh וחב' ב-BMC Cancer משנת 2013), סרטן הפה (Tsuji וחב' ב-Cancer Lett משנת 1999), וגליומה (Gandini וחב' ב-Tumor Biol משנת 2014). יתרה מכך, רמת הביטוי של HO-1 נמצאה במתאם חיובי עם שלב המחלה ועם הפרוגנוזה שלה. מספר מחקרים הראו ש-HO-1 התגלה לא רק בציטופלזמה, אלא גם בגרעין של תאי סרטן הערמונית (Sacca וחב' ב-Br J Cancer משנת 2007), סרטן ריאות (Hsu וחב' ב-Oncogene משנת 2014) וסרטן הפה (Gandini וחב' ב-Exp Mol Pathol משנת 2012). דרגת הנוכחות של HO-1 בגרעין התאים הסרטניים, הייתה כרוכה עם דרגת המחלה המתקדמת ופרוגנוזה גרועה, במטופלים עם סרטן הערמונית (Weigel וחב' ב-Cancer Res משנת 2013), ובאלה עם קרצינומה של הפה (Gandini וחב' ב-Exp Mol Pathol משנת 2012).
תפקודים פרדוקסליים של HO-1 בטומורוגניות
נזק ל-DNA הנגרם על ידי מולקולות עתירות חמצן (ROS) הוא גורם משמעותי למוטציות. בהפחתת ביטוי של HO-1 יש הגדלה ברמת ROS וממילא נזק ל-DNA בתאים. זאת ועוד, CO משפר את הישרדות התאים על ידי שהוא משרה תיקון בנזקי DNA (Otterbein וחב' ב-Proc Natl Acad Sci USA משנת 2011). לפיכך הגברת הביטוי של HO-1 מונעת נזק ל-DNA ואתחול התהליך הטומורוגני בתאים נורמלים. עם זאת, בשלב מאוחר של טומורוגנזה, ביטוי-יתר של HO-1 מגביר את הפרוליפרציה של תאי הסרטן ואת היכולת שלהם לייצר גרורות (Sunamura וחב' ב-Angiogenesis משנת 2003, Chen וחב' ב-J Cell Biochem משנת 2004, ו-Was וחב' ב-Am J Pathol משנת 2006). HO-1 מגן על תאים סרטניים מפני apoptosis שגורמים חומרים כימו-טוקסיים או קרינה, מה שמרמז על מעורבות HO-1 בעמידות תאים סרטניים לטיפולים תרפויטיים שונים (Liu וחב' ב-Oncogene משנת 2004, Berberat וחב' ב-Clin Cancer Res משנת 2005, Kweon וחב' ב-J Biol Chem משנת 2006, Kocanova וחב' ב-Apoptosis משנת 2007, Furfaro וחב' ב-Biochim Biophys Acta משנת 2014, Kongpetch וחב' ב-PLos One משנת 2012).
השפעול של Nfr2
הפעילות כנגד HO-1 מצטיירת כגישה יעילה לפחות בסרטן הערמונית העמיד לטיפול הורמונלי (Sporn ו-Liby ב-Nat Rev Cancer משנת 2012), והיא גם מתגברת על העמידות ל-imatinib ב-CML (Alaoui-Jamali וחב' ב-Cancer Res משנת 2009). פעילות זו של HO-1 גם מגבירה את הרגישות של הפאטומה, ושל סרטני הערמונית ומערכת השתן לכימותרפיה (Mayerhofer וחב' ב-Blood משנת 2008). המיקום של HO-1 בתוך גרעין התא, מעודד את הגידול הסרטני ואת הגרורתיות שלו, באופן בלתי-תלוי בפעילותו האנזימטית.
הוראות לביצוע הבדיקה
דם נלקח במבחנה כימית (פקק אדום או צהוב) ולאחר קרישתו וסרכוזו, הנסיוב משמש לבדיקת ELISA בערכה המקובלת, ImmunoSet TM HO-1 Elisa kit של חברת (Enzo (Framingdale.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק