הבדלים בין גרסאות בדף "חומצה סיאלית - Sialic acid"
| (7 גרסאות ביניים של אותו משתמש אינן מוצגות) | |||
| שורה 8: | שורה 8: | ||
|תחום=מדידת חומצה סיאלית בשתן מומלצת כבדיקת סקר המיועדת למטופלים הנחשדים כמאובחנים עם מחלת אגירה של חומצה סיאלית, עם sialidosis או עם galactosialidosis. | |תחום=מדידת חומצה סיאלית בשתן מומלצת כבדיקת סקר המיועדת למטופלים הנחשדים כמאובחנים עם מחלת אגירה של חומצה סיאלית, עם sialidosis או עם galactosialidosis. | ||
|יחידות מדידה= | |יחידות מדידה= | ||
| − | |טווח ערכים תקין=חומצה סיאלית חופשית-בגיל הצעיר מ-4 שבועות 208 mmol/mol | + | |טווח ערכים תקין=חומצה סיאלית חופשית-בגיל הצעיר מ-4 שבועות 208 mmol/mol creatinine או פחות; בגיל 5 שבועות עד שנה- 104 mmol/mol creatinine או פחות; בגיל 13 חודשים עד 18 שנים שנים- 100 mmol/mol creatinine או פחות; בגיל 19 שנים ומעלה - 38 mmol/mol creatinine או פחות.{{ש}} |
סך חומצה סיאלית: בגיל הצעיר מ-4 שבועות - 852 mmol/mol creatinine או פחות; בגיל 5 שבועות עד 12 חודשים - 656 mmol/mol creatinine או פחות; בגיל 13 חודשים עד 18 שנים - 335 mmol/mol creatinine או פחות; בגיל 19 שנים ומעלה -262 mmol/mol creatinine או פחות.{{ש}} | סך חומצה סיאלית: בגיל הצעיר מ-4 שבועות - 852 mmol/mol creatinine או פחות; בגיל 5 שבועות עד 12 חודשים - 656 mmol/mol creatinine או פחות; בגיל 13 חודשים עד 18 שנים - 335 mmol/mol creatinine או פחות; בגיל 19 שנים ומעלה -262 mmol/mol creatinine או פחות.{{ש}} | ||
היחס בין סך חומצה פולית לחומצה סיאלת חופשית: בגיל 4 שבועות או פחות - 1.94-18.68; בגיל 5 שבועות עד 12 חודשים - 2.34-13.85; בגיל 13 חודשים עד 18 שנים - 2.63-9.18; בגיל 19 שנים ומעלה - 3.35-15.81. | היחס בין סך חומצה פולית לחומצה סיאלת חופשית: בגיל 4 שבועות או פחות - 1.94-18.68; בגיל 5 שבועות עד 12 חודשים - 2.34-13.85; בגיל 13 חודשים עד 18 שנים - 2.63-9.18; בגיל 19 שנים ומעלה - 3.35-15.81. | ||
| שורה 15: | שורה 15: | ||
}} | }} | ||
==פיזיולוגיה של חומצה סיאלית== | ==פיזיולוגיה של חומצה סיאלית== | ||
| − | חומצות סיאליות הן מולקולות חשובות מגוונות באופן מבני. הן מצויות בבעלי חוליות | + | חומצות סיאליות הן מולקולות חשובות מגוונות באופן מבני. הן מצויות בבעלי חוליות ובבעלי חיים אחרים כגון פלטיהלמינטים, צפלופודה וקרסטצה. צמחים חסרים חומצה סיאלית., אך היא מופיעה בנגיפים, בחיידקים, בפרוטוזואה ובשמרים. חומצה נוירמינית שעברה דה-אמינציה נמצאת בשפע בבעלי חוליות נמוכים. חומצות סיאליות ממוקמות בקצוות הטרמינליים של גליקופרוטאינים וגליקוליפים, בפוליסכרידים של דופן חיידקים. חומצה סיאלית משחקת תפקידים חשובים בפיזיולוגיה של האדם, באינטראקציה בין תאים, באיתות בין-תאי, באינטראקציה בין חלבונים וקרבוהידרטים, בצימות תאים, בתהליכי התפתחות, בריאקציות של מערכת החיסון, ברפרודוקציה, בשגשוג תאי [[סרטן]] ויצירת גרורות, בביולוגיה של המיקרוביום, ובפתולוגיה. נמצא שחומצה סיאלית משחקת תפקיד בתרפויטיקה. אף על פי שחלבונים, חומצות גרעין, ליפידים ומולקולות קטנות יוצרים את המרכיבים העיקריים של תאי אדם, התרחשה התקדמות ניכרת במחקר על גליקנים על פני תאי אדם ותפקידם במגוון תפקודים תאיים (Varki ב-Trends Mol Med משנת 2008, Carter ו-Martin ב-J Cluin Pathol משנת 1962). שינויים בגליקוזילציה ובסיאלילציה כרוכים במספר מחלות באדם כולל סרטן. |
| + | |||
| + | חומצות סיאליות הן קבוצה מגוונת של מונו-סכרידים עם 9 פחמנים, וממוקמות בקצה השרשראות הקרבוהידרטיות בקשרי N ו-O ביונקים. מספר סוגי חיידקים יכולים לסנתז de novo חומצות סיאליות, אך כמה מהם יכולים להשיג חומצות סיאליות מהמאחסן (Haines-Menges וחב' ב-microbiol Spectr משנת 2015, ו־Vimr וחב' ב־Microbiol Mol Biol Rev משנת 2004). המטען השלילי והתכונות ההידרופיליות של חומצה סיאלית, מאפשרים לה תפקיד בתהליכים פיזיולוגיים נורמליים ופתולוגיים, בהיותם משמשים נקודות תאחיזה לפתוגנים ולטוקסינים, וכך הם מסוגלים להתחמק ממערכת החיסון (Mahajan ו-Pillai ב-Immunol Rev משנת 2016, ו־Gowthaman ו-Eswarakumar ב־Adv Nutr משנת 2012). תכולת חומצה סיאלית במוח האנושי היא הגבוהה ביותר בהשוואה לבעלי חיים אחרים, מה שעשוי להיות קשור עם היתרון האבולוציוני של האדם (Rademacher ב־Annu Rev Biochem משנת 1988, Varki וחב' ב־Essentials of glycobiology משנת 1999, Drickamer ו-Taylor ב־Introduction to glycobiology משנת 2006, Shauer ב-Glycoconj J משנת 2000, ו-Angata ו-Varki ב-Chem Rev משנת 2002). | ||
| − | |||
| − | |||
==תפקודים של חומצה סיאלית== | ==תפקודים של חומצה סיאלית== | ||
| − | חומצות סיאליות משפיעות על המבנה והתפקוד של גליקו-קוניוגטים ופועלות כליגנדים ללקטינים, לנוגדנים, ולאנזימים. הן משחקות תפקיד חיוני בייצוב של אריתרוציטים ובמניעת צימות של מרכיבי דם על ידי מטענם החשמלי השלילי, וכן על ידי ההידרופיליות שלהן. חומצות סיאליות ידועות בשל השפעתן על היציבות והתפקוד של הורמונים ושל אנזימים. הן משחקות תפקיד משמעותי | + | חומצות סיאליות משפיעות על המבנה והתפקוד של גליקו-קוניוגטים ופועלות כליגנדים ללקטינים, לנוגדנים, ולאנזימים. הן משחקות תפקיד חיוני בייצוב של אריתרוציטים ובמניעת צימות של מרכיבי דם על ידי מטענם החשמלי השלילי, וכן על ידי ההידרופיליות שלהן. חומצות סיאליות ידועות בשל השפעתן על היציבות והתפקוד של הורמונים ושל אנזימים. הן משחקות תפקיד משמעותי ברבייה, בהתפתחות ובסיאלילציה של FSH ושל hCG, ותורמות ליציבות ולתפקוד של הורמונים אלה (Leung וחב' ב-J Virol משנת 2012, ו-Nizet וחב' ב-Essentials of Microbiol משנת 2017). |
[[קובץ:Sialic1.jpg|מרכז|600px]] | [[קובץ:Sialic1.jpg|מרכז|600px]] | ||
==זמינות ותפקוד של חומצה סיאלית== | ==זמינות ותפקוד של חומצה סיאלית== | ||
| − | חומצות סיאליות מופיעות בתרכובות סוכריות גם בנגיפים, בחיידקים, בשמרים ובפרוטוזואה, בהם הן מופיעות כחלק מגליקופרוטאינים וגנגליוזידים, וכן בגליקוזאמינוגליקנים ביונקים ובבעלי חוליות (Schnaar וחב' ב-Physiol Rev משנת 2014), שם הם משמשים ליגנדים או קולטנים לקשר בינתאי, ולאינטראקציה בין טפילים למאחסן שלהם. דווח שחומצה סיאלית מופיעה בדרוזופילה ובחרקים אחרים (Roth וחב' ב-Science משנת 1992, ו-Ghosh ב-Glycoconj J משנת 2018), כמו גם ברכיכות מסוג Arion (לל Staudacher וחב' ב-Glycoconj J משנת 1999). תכולת החומצה הסיאלית בחרקים וברכיכות נמוכה (Zhukova וחב' ב-Biochim Biophys Acta משנת 1973, Kim ב-J Glycomics Lipidomics משנת 2014, ו-Chou ב-Proc Natl Acad Sci USA משנת 1998), וחסרה לחלוטין בצמחים. | + | חומצות סיאליות מופיעות בתרכובות סוכריות גם בנגיפים, בחיידקים, בשמרים ובפרוטוזואה, בהם הן מופיעות כחלק מגליקופרוטאינים וגנגליוזידים, וכן בגליקוזאמינוגליקנים ביונקים ובבעלי חוליות (Schnaar וחב' ב-Physiol Rev משנת 2014), שם הם משמשים ליגנדים או קולטנים לקשר בינתאי, ולאינטראקציה בין טפילים למאחסן שלהם. דווח שחומצה סיאלית מופיעה בדרוזופילה ובחרקים אחרים (Roth וחב' ב-Science משנת 1992, ו-Ghosh ב-Glycoconj J משנת 2018), כמו גם ברכיכות מסוג Arion (לל Staudacher וחב' ב-Glycoconj J משנת 1999). תכולת החומצה הסיאלית בחרקים וברכיכות נמוכה (Zhukova וחב' ב-Biochim Biophys Acta משנת 1973, Kim ב-J Glycomics Lipidomics משנת 2014, ו-Chou ב-Proc Natl Acad Sci USA משנת 1998), וחסרה לחלוטין בצמחים. |
==פתוגנים הנקשרים לחומצות סיאליות על פני תאי אדם== | ==פתוגנים הנקשרים לחומצות סיאליות על פני תאי אדם== | ||
{| class="wikitable" | {| class="wikitable" | ||
| − | ! | + | ! פתוגן!!חלבון ההתקשרות!!רצף המבנים של חומצה סיאלית |
|- | |- | ||
|Human Influenza A||Hemagglutinin||Siaα2–6Gal(NAc) | |Human Influenza A||Hemagglutinin||Siaα2–6Gal(NAc) | ||
| שורה 48: | שורה 48: | ||
==סיאלילציה ותחלואה== | ==סיאלילציה ותחלואה== | ||
| − | + | אף על פי שחומצות סיאליות ממוקמות בקצות גליקנים בכל סוגי התאים, במצבי מחלה כגון סרטן, פרופיל הסיאלילציה של תאים ברקמות הנגועות מבטאים ביטוי-יתר של מבנים גליקניים מסוימים (Varki וחב' ב-Essentials glycobiol משנת 2009). סיאלילציה משובשת של סעיפי אוליגוסכרידים של N-glycans (כגון הסתעפות של β1,6-GlcNAc) או סיאלילציה טרם-עת של יחידות סכרידיות קטומות (truncated), מדווחות להתרחש בגין ביטוי אנזימטי שעבר שינויים. ב-rheumatoid arthritis, גליקוזילציה בלתי מושלמת של גלקטוז ושל חומצה סיאלית גורמת למחדל חיסוני (Dekkers וחב' ב-Front Immunol משנת 2018). אך פעילות מוגברת של סאליל-טרנספרזות כגון ST3Gal-I מופיעה בתאי [[סרטן שד]] (Picco וחב' ב-Glycobiology משנת 2010) ופעילות מוגברת של האנזים ST6Gal-I, מדווחת בתאי סרטן שד ו[[סרטן המעי הגס]]. ביטוי-יתר של גנגליוזידים בסרטן דווח כ-GD3 ספציפי ב-CNS ברקמות סרטניות (Groux-Degroote ב-Chembiochem משנת 2017) כמו כן יש דיווחים על ביטוי-יתר של 9-O-acetylated sialic acid בסרטן שד (Cavdarli וחב' ב-Glycoconj J משנת 2019), וב-[[ALL]] בילדים (Ghosh ב-Glycoconj J משנת 2007, Pal וחב' ב-Glycobiology משנת 2004, Ghosh וחב' ב-Ann Hematol משנת 2005). השינויים בסיאלילציה תאית בסרטן משפיעה על האינטראקציה של תאי סרטן עם תאים אחרים ועל הספיחה, הנדידה, והגרורות הסרטניות (Zhang וחב' ב-Cancer משנת 2018, Häuselmann ו-Borsig ב-Front Oncol משנת 2014). סיאלילציה משפיעה על הטוקסיות של תאים ממיתים חיסוניים (NK) (Van Rinsum וחב' ב-Int J Cancer משנת 1986). | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | ==מחלות הקשורות לחומצה סיאלית== | |
| + | מחלת אגירה של חומצה סיאלית חופשית (להלן FSASD) היא מפגע נדיר של אגירה ליזוזומלית הנגרמת על ידי פגם ב-sialin שהוא אקספורטר של חומצה סיאלית ממברנלית, הידוע גם כ-SLC17A5. פגם זה גורם לאגירה מוגברת של חומצה סיאלית בליזוזומים. אלה עם FSASD סובלים מהיפוטוניה, באטקסיה של המוחון, בקומה נמוכה, ובפגיעה קוגניטיבית. בדיקות הדמיה יכולות להראות היפו-מייאלינציה צנטרלית, אטרופיה של המוחון, וקורפוס קלוסום דק. תינוקות וילדים עם מחלה חמורה יותר, הם בעלי תווי פנים גסים, ו-organomegaly, כגון כבד ולב מוגדלים. צורה מולדת של המחלה דווחה במטופלים עם hydrops fetalis לא חיסוני. Hydrops fetalis הוא תרחיש של בצקת כללית של העובר במנגנון חיסוני או בלתי חיסוני המופיע ב-75% מהמקרים. זהו מצב בו מצטברים נוזלים במדורים שונים בגוף, כגון בית החזה, בטן, תת-העור וכן השליה עצמה. היסטורית, FSASD חולק למספר מצבים בהתאם לגיל הופעת התסמינים וחומרתם: מחלת אגירה של חומצה סיאלית חופשית אינפנטילית, מחלת Salla חמורה לגיל הביניים, ומחלת Salla. כרגע לא קיימים טיפולים מאושרים ל-FSASD. רמת חומצה סיאלית בשתן תראה מוגברות של חומצה סיאלית חופשית, ויחס גבוה בין חומצה סיאלית חופשית לסך חומצה סיאלית במטופלים עם FSASD שהוא מפגע אוטוזומלי-רצסיבי הנגרם על ידי וריאנט פתוגני דו-אללי בגן SLC17A5. ישנם עוד שני מפגעים המאופיינים על ידי חומצה סיאלית חופשית מוגברת: Sialuria ו-N-acetylneuraminate pyruvate lyase (להלן NPL) deficiency. {כ}}Sialura היא מפגע אוטוזומלי רצסיבי הנגרם על ידי וריאנט פתוגני בגן GNE הבא לביטוי ב-organomegaly ובהתפתחות איטית בילדות. חסר של NPL גם כן מורש בגישה אוטוזומלית רצסיבית כתוצאה מווריאנט פתוגני בגן NPL. אלה עם חסר NPL מפתחים קרדיומיופתיה מתקדמת ומיופתיה שלדית מתונהבילדות. לא קיימות מאושרות לשני מצבים אלה והטיפול הוא רק מסייע. | ||
| − | + | Sialidosis נגרמת על ידי חסר באנזים neuraminidase מה שגורם להצטברות של sialyloligosaccharide בליזוזומים. אלה עם sialidosis מתאפיינים עם מפגעים קליניים חמורים יותר (type II) או מתונים יותר (type I). מאפיינים קליניים אלה נעים בין התפתחות מוקדמת איטית, קומה נמוכה, dysostosis multiplex (מחלה נדירה קונגניטלית המאופיינת על ידי שינויים שלדיים כונדרודיסטרופיים ושקיעה של חומר דמוי-ליפיד ברקמות רבות בגוף. התמונה האופיינית היא של גמדות עם דפורמציה של גפיים והגדלת הכבד והטחול) עד התפתחות מאוחרת של תסמונת מיוקלונית עם כתם אדום בוהק. (מחלה זו היא הנדירה ביותר מכלל המחלות הגורמות לאפילפסיות מיוקלוניות פרוגרסיביות, והוא מתחלק לשתי התבטאויות פנוטיפיות דומות המבטאות לכאורה פגיעות שונות בגנים סמוכים על אותו כרומוזום. Type I-גיל הופעת הסימפטומים, בזמן הילדות המאוחרת עם התבטאות הכוללת מיוקלונוס (לרוב בצורה קשה), הפרעה פרוגרסיבית בראייה, פרכוסים טוניים-קלוניים, אטקסיה וכתם אדום בוהק בפונדוסקופיה. ניתן למצוא עכירות ניכרת של העדשה בעין ופגיעה נוירולוגית פריפרית עם תחושה של שריפה בגפיים התחתונות. במחלה זו לא מתפתחת דמנציה. Type II- ההתבטאות דומה לזו שב Type I אבל המחלה מופיעה בגיל ההתבגרות, כשלהתבטאות הקלינית נוספים פגיעה במבנה הפנים, הפרעה בשמיעה וירידה איטית באינטלקט. האבחנה היא קלינית, על ידי מציאת כתם אדום בוהק בפונדוסקופיה. זאת לאחר התחלת ההתבטאות הקלינית של המחלה. האבחנה הסופית נעשית על ידי מציאת רמה גבוהה של Siolyloligosaccharides בשתן וחוסר ב Cayalabile αN- acetylneuroaminidase בלויקוציטים ובתרביות פיברובלסטים. | |
| − | |||
| − | |||
| − | |||
| − | + | בנוסף, עלולים להופיע פרכוסים ושיגשון, היפר-רפלקסיה בלמעלה מ-50% מהלוקים במחלה בשלב חיים מאוחר יותר. אנליזה של חומצה סיאלית בשתן, מגלה יחס נמוך של חומצה סיאלית חופשית לסך חומצה סיאלית במטופלים עם sialidosis. מומלץ גם לבצע אנליזה של [[אוליגוסכרידים בשתן]], במטופלים החשודים ל-sialidosis מצב הנגרם על ידי פתוגניות דו-אללית של וריאנטים בגן NEU1. מפגע נוסף ידוע כ-galactosialidosis בו רוב המאובחנים הם בעלי תסמינים מתונים יותר של אטקסיה, מיוקלונוס, אנגיוקרטומה, ודעיכה נוירולוגית וקוגניטיבית. גלקטוסיאלידוזיס הוא מפע אוטוזומלי-רצסיבי הנגרם על ידי וריאנט פתוגני דו-אללי של הגן CTSA. | |
| − | |||
| − | + | ==אינטרפרטציה== | |
| − | + | תוצאה מוגברת של היחס בין סך חומצה סיאלית לחומצה סיאלית חופשית יכולה לשמש אינדיקציה למצבים של sialidosis או של galactosialidosis{{כ}} (Annunziata וחב' ב־Expert Opin Orphan Drugs משנת 2017. לעומת זאת תוצאה מופחת של יחס זה יכולה לשמש אינדיקציה למחלת אגירה של חומצה סיאלית. עליה קלה בוחמצה סיאלית חופשית בשתן יכולה להופיע גם מסיבות אחרות הכוללות ספסיס, מחלת כליות, תסמונת המוליטית-אורמית וסוכרת type 2 . | |
| − | + | ==Selectins== | |
| − | + | סלקטינים הם מבנים התלויים בסידן, טרנס-ממברנליים type I, הנקשרים למולקולות קרבוהידרטיות המכילות fucose שעברו סיאלילציה, המתפקדים בספיחה וסקולרית, ומשחקים תפקיד מפתח בתהליכי דלקת, חיסון, המוסטאזיס, והתקדמות התהליך הסרטני. הליגנד של selectin מבטא ביטוי-יתר בתאי סרטן מה שמבגביר את התהליך הגרורתי, את הפרוגנוזה הגרועה, את יכולת הספיחה של תאי סרטן, ומשפעל את הקסקדה האיתותית של תאים אלה. סלקטינים משחקים תפקיד חיוני בתהליך ה-homing של לויקוציטים, והקישור של L-selecin לליגנדים על פני לויקוציטים משפעל תאים אלה. סלקטינים מאפשרים אינטראקציה עם טסיות ועם תאי אנדותל. | |
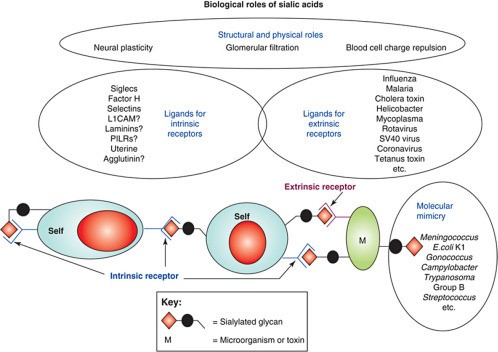
| − | + | [[קובץ:Sialic2.jpg|ממוזער|מרכז|600 פיקסלים|'''תפקידים ביולוגיים ופתולוגיים של חומצות סיאליות: הן משמשות אתרי קישור של פתוגנים וטקסינים, ופועלות כליגנדים עבור קולטנים כגוןSiglecs ופקטור H. חומצות סיאליות מאפשרות "דמיון מולקולרי" דרכו פתוגנים מיקרוביאליים משלבים חומצות סיאליות של המאחסן, ומתחמקים מתגובות מערכת החיסון של המאחסן. L1CAM-,L1 cell adhesion molecule PILR -paired immunoglobulin-like receptor.]] | |
| − | |||
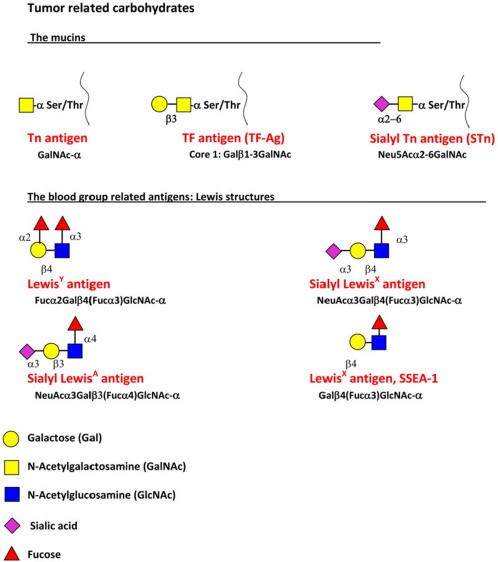
| − | + | [[קובץ:Sialic 3.jpg|ממוזער|מרכז|600 פיקסלים|'''מבנים של אנטיגנים קרבוהידרטיים מוציניים Tn, Sialyl Tn ו-TF, וקבוצת הדם Lewis. מבנים של גליקוספינגוליפידים מסדרות Globo H ו-SSEA-3, והגנגליוזידים GM1 ,GM2, GD2, GD3 ו .Fucosyl GM1''']] | |
| + | ==הוראות לביצוע הבדיקה== | ||
| + | יש לאסוף דגימת שתן אקראית רצוי של שעות הבוקר המוקדמות. יציבות דגימת השתן בקירור (דגימה מועדפת) 90 יום, וזה גם פרק הזמן של יציבות דגימת השתן הקפואה. יש לצרף לדגימה את גיל הנבדק. המדידה מתבצעת בשיטת Liquid Chromatography Tandem Mass Spectrometry (LC-MS/MS)). | ||
| + | ==ראו גם== | ||
| + | * [[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | ||
| + | * [[מדדי פוריות ורבייה|בדיקות מעבדה - מדדי פוריות ורבייה]] | ||
| + | * [[מפגעי מערכת העצבים והמוח|בדיקות מעבדה - מפגעי מערכת העצבים והמוח]] | ||
| + | {{שש}} | ||
| + | {{ייחוס בן עמי}} | ||
| − | + | [[קטגוריה:בדיקות מעבדה: כימיה בשתן]] | |
| − | + | [[קטגוריה:בדיקות מעבדה - מדדי פוריות ורבייה]] | |
| + | [[קטגוריה:בדיקות מעבדה - מפגעי מערכת העצבים והמוח]] | ||
גרסה אחרונה מ־06:00, 20 באפריל 2025
| מדריך בדיקות מעבדה | |
| חומצה סיאלית | |
|---|---|
| Sialic acid | |
| שמות אחרים | N-acetylneuraminic acid, Neu5Ac |
| מעבדה | כימיה בשתן |
| תחום | מדידת חומצה סיאלית בשתן מומלצת כבדיקת סקר המיועדת למטופלים הנחשדים כמאובחנים עם מחלת אגירה של חומצה סיאלית, עם sialidosis או עם galactosialidosis. |
| טווח ערכים תקין | חומצה סיאלית חופשית-בגיל הצעיר מ-4 שבועות 208 mmol/mol creatinine או פחות; בגיל 5 שבועות עד שנה- 104 mmol/mol creatinine או פחות; בגיל 13 חודשים עד 18 שנים שנים- 100 mmol/mol creatinine או פחות; בגיל 19 שנים ומעלה - 38 mmol/mol creatinine או פחות. סך חומצה סיאלית: בגיל הצעיר מ-4 שבועות - 852 mmol/mol creatinine או פחות; בגיל 5 שבועות עד 12 חודשים - 656 mmol/mol creatinine או פחות; בגיל 13 חודשים עד 18 שנים - 335 mmol/mol creatinine או פחות; בגיל 19 שנים ומעלה -262 mmol/mol creatinine או פחות. |
| יוצר הערך | פרופ' בן-עמי סלע |
פיזיולוגיה של חומצה סיאלית
חומצות סיאליות הן מולקולות חשובות מגוונות באופן מבני. הן מצויות בבעלי חוליות ובבעלי חיים אחרים כגון פלטיהלמינטים, צפלופודה וקרסטצה. צמחים חסרים חומצה סיאלית., אך היא מופיעה בנגיפים, בחיידקים, בפרוטוזואה ובשמרים. חומצה נוירמינית שעברה דה-אמינציה נמצאת בשפע בבעלי חוליות נמוכים. חומצות סיאליות ממוקמות בקצוות הטרמינליים של גליקופרוטאינים וגליקוליפים, בפוליסכרידים של דופן חיידקים. חומצה סיאלית משחקת תפקידים חשובים בפיזיולוגיה של האדם, באינטראקציה בין תאים, באיתות בין-תאי, באינטראקציה בין חלבונים וקרבוהידרטים, בצימות תאים, בתהליכי התפתחות, בריאקציות של מערכת החיסון, ברפרודוקציה, בשגשוג תאי סרטן ויצירת גרורות, בביולוגיה של המיקרוביום, ובפתולוגיה. נמצא שחומצה סיאלית משחקת תפקיד בתרפויטיקה. אף על פי שחלבונים, חומצות גרעין, ליפידים ומולקולות קטנות יוצרים את המרכיבים העיקריים של תאי אדם, התרחשה התקדמות ניכרת במחקר על גליקנים על פני תאי אדם ותפקידם במגוון תפקודים תאיים (Varki ב-Trends Mol Med משנת 2008, Carter ו-Martin ב-J Cluin Pathol משנת 1962). שינויים בגליקוזילציה ובסיאלילציה כרוכים במספר מחלות באדם כולל סרטן.
חומצות סיאליות הן קבוצה מגוונת של מונו-סכרידים עם 9 פחמנים, וממוקמות בקצה השרשראות הקרבוהידרטיות בקשרי N ו-O ביונקים. מספר סוגי חיידקים יכולים לסנתז de novo חומצות סיאליות, אך כמה מהם יכולים להשיג חומצות סיאליות מהמאחסן (Haines-Menges וחב' ב-microbiol Spectr משנת 2015, ו־Vimr וחב' ב־Microbiol Mol Biol Rev משנת 2004). המטען השלילי והתכונות ההידרופיליות של חומצה סיאלית, מאפשרים לה תפקיד בתהליכים פיזיולוגיים נורמליים ופתולוגיים, בהיותם משמשים נקודות תאחיזה לפתוגנים ולטוקסינים, וכך הם מסוגלים להתחמק ממערכת החיסון (Mahajan ו-Pillai ב-Immunol Rev משנת 2016, ו־Gowthaman ו-Eswarakumar ב־Adv Nutr משנת 2012). תכולת חומצה סיאלית במוח האנושי היא הגבוהה ביותר בהשוואה לבעלי חיים אחרים, מה שעשוי להיות קשור עם היתרון האבולוציוני של האדם (Rademacher ב־Annu Rev Biochem משנת 1988, Varki וחב' ב־Essentials of glycobiology משנת 1999, Drickamer ו-Taylor ב־Introduction to glycobiology משנת 2006, Shauer ב-Glycoconj J משנת 2000, ו-Angata ו-Varki ב-Chem Rev משנת 2002).
תפקודים של חומצה סיאלית
חומצות סיאליות משפיעות על המבנה והתפקוד של גליקו-קוניוגטים ופועלות כליגנדים ללקטינים, לנוגדנים, ולאנזימים. הן משחקות תפקיד חיוני בייצוב של אריתרוציטים ובמניעת צימות של מרכיבי דם על ידי מטענם החשמלי השלילי, וכן על ידי ההידרופיליות שלהן. חומצות סיאליות ידועות בשל השפעתן על היציבות והתפקוד של הורמונים ושל אנזימים. הן משחקות תפקיד משמעותי ברבייה, בהתפתחות ובסיאלילציה של FSH ושל hCG, ותורמות ליציבות ולתפקוד של הורמונים אלה (Leung וחב' ב-J Virol משנת 2012, ו-Nizet וחב' ב-Essentials of Microbiol משנת 2017).
זמינות ותפקוד של חומצה סיאלית
חומצות סיאליות מופיעות בתרכובות סוכריות גם בנגיפים, בחיידקים, בשמרים ובפרוטוזואה, בהם הן מופיעות כחלק מגליקופרוטאינים וגנגליוזידים, וכן בגליקוזאמינוגליקנים ביונקים ובבעלי חוליות (Schnaar וחב' ב-Physiol Rev משנת 2014), שם הם משמשים ליגנדים או קולטנים לקשר בינתאי, ולאינטראקציה בין טפילים למאחסן שלהם. דווח שחומצה סיאלית מופיעה בדרוזופילה ובחרקים אחרים (Roth וחב' ב-Science משנת 1992, ו-Ghosh ב-Glycoconj J משנת 2018), כמו גם ברכיכות מסוג Arion (לל Staudacher וחב' ב-Glycoconj J משנת 1999). תכולת החומצה הסיאלית בחרקים וברכיכות נמוכה (Zhukova וחב' ב-Biochim Biophys Acta משנת 1973, Kim ב-J Glycomics Lipidomics משנת 2014, ו-Chou ב-Proc Natl Acad Sci USA משנת 1998), וחסרה לחלוטין בצמחים.
פתוגנים הנקשרים לחומצות סיאליות על פני תאי אדם
| פתוגן | חלבון ההתקשרות | רצף המבנים של חומצה סיאלית |
|---|---|---|
| Human Influenza A | Hemagglutinin | Siaα2–6Gal(NAc) |
| Avian Influenza A | Hemagglutinin | Siaα2–3Galβ1- |
| Human Influenza C | Hemagglutinin-esterase | 9-O-Ac-Siaα2- |
| Vibrio cholera | Toxin | Galβ1–3GalNAcβ1,4(Siaα2–3)Lac-Cer |
| Plasmodium falciparum | EBA-175 | Siaα2–3Galβ1–3(Siaα2–6)GalNAc-O |
| Clostridium botulinum | Toxin | Polysialogangliosides |
| Helicobacter pylori | SabA | Siaα2–3Gal on gangliosides |
סיאלילציה ותחלואה
אף על פי שחומצות סיאליות ממוקמות בקצות גליקנים בכל סוגי התאים, במצבי מחלה כגון סרטן, פרופיל הסיאלילציה של תאים ברקמות הנגועות מבטאים ביטוי-יתר של מבנים גליקניים מסוימים (Varki וחב' ב-Essentials glycobiol משנת 2009). סיאלילציה משובשת של סעיפי אוליגוסכרידים של N-glycans (כגון הסתעפות של β1,6-GlcNAc) או סיאלילציה טרם-עת של יחידות סכרידיות קטומות (truncated), מדווחות להתרחש בגין ביטוי אנזימטי שעבר שינויים. ב-rheumatoid arthritis, גליקוזילציה בלתי מושלמת של גלקטוז ושל חומצה סיאלית גורמת למחדל חיסוני (Dekkers וחב' ב-Front Immunol משנת 2018). אך פעילות מוגברת של סאליל-טרנספרזות כגון ST3Gal-I מופיעה בתאי סרטן שד (Picco וחב' ב-Glycobiology משנת 2010) ופעילות מוגברת של האנזים ST6Gal-I, מדווחת בתאי סרטן שד וסרטן המעי הגס. ביטוי-יתר של גנגליוזידים בסרטן דווח כ-GD3 ספציפי ב-CNS ברקמות סרטניות (Groux-Degroote ב-Chembiochem משנת 2017) כמו כן יש דיווחים על ביטוי-יתר של 9-O-acetylated sialic acid בסרטן שד (Cavdarli וחב' ב-Glycoconj J משנת 2019), וב-ALL בילדים (Ghosh ב-Glycoconj J משנת 2007, Pal וחב' ב-Glycobiology משנת 2004, Ghosh וחב' ב-Ann Hematol משנת 2005). השינויים בסיאלילציה תאית בסרטן משפיעה על האינטראקציה של תאי סרטן עם תאים אחרים ועל הספיחה, הנדידה, והגרורות הסרטניות (Zhang וחב' ב-Cancer משנת 2018, Häuselmann ו-Borsig ב-Front Oncol משנת 2014). סיאלילציה משפיעה על הטוקסיות של תאים ממיתים חיסוניים (NK) (Van Rinsum וחב' ב-Int J Cancer משנת 1986).
מחלות הקשורות לחומצה סיאלית
מחלת אגירה של חומצה סיאלית חופשית (להלן FSASD) היא מפגע נדיר של אגירה ליזוזומלית הנגרמת על ידי פגם ב-sialin שהוא אקספורטר של חומצה סיאלית ממברנלית, הידוע גם כ-SLC17A5. פגם זה גורם לאגירה מוגברת של חומצה סיאלית בליזוזומים. אלה עם FSASD סובלים מהיפוטוניה, באטקסיה של המוחון, בקומה נמוכה, ובפגיעה קוגניטיבית. בדיקות הדמיה יכולות להראות היפו-מייאלינציה צנטרלית, אטרופיה של המוחון, וקורפוס קלוסום דק. תינוקות וילדים עם מחלה חמורה יותר, הם בעלי תווי פנים גסים, ו-organomegaly, כגון כבד ולב מוגדלים. צורה מולדת של המחלה דווחה במטופלים עם hydrops fetalis לא חיסוני. Hydrops fetalis הוא תרחיש של בצקת כללית של העובר במנגנון חיסוני או בלתי חיסוני המופיע ב-75% מהמקרים. זהו מצב בו מצטברים נוזלים במדורים שונים בגוף, כגון בית החזה, בטן, תת-העור וכן השליה עצמה. היסטורית, FSASD חולק למספר מצבים בהתאם לגיל הופעת התסמינים וחומרתם: מחלת אגירה של חומצה סיאלית חופשית אינפנטילית, מחלת Salla חמורה לגיל הביניים, ומחלת Salla. כרגע לא קיימים טיפולים מאושרים ל-FSASD. רמת חומצה סיאלית בשתן תראה מוגברות של חומצה סיאלית חופשית, ויחס גבוה בין חומצה סיאלית חופשית לסך חומצה סיאלית במטופלים עם FSASD שהוא מפגע אוטוזומלי-רצסיבי הנגרם על ידי וריאנט פתוגני דו-אללי בגן SLC17A5. ישנם עוד שני מפגעים המאופיינים על ידי חומצה סיאלית חופשית מוגברת: Sialuria ו-N-acetylneuraminate pyruvate lyase (להלן NPL) deficiency. {כ}}Sialura היא מפגע אוטוזומלי רצסיבי הנגרם על ידי וריאנט פתוגני בגן GNE הבא לביטוי ב-organomegaly ובהתפתחות איטית בילדות. חסר של NPL גם כן מורש בגישה אוטוזומלית רצסיבית כתוצאה מווריאנט פתוגני בגן NPL. אלה עם חסר NPL מפתחים קרדיומיופתיה מתקדמת ומיופתיה שלדית מתונהבילדות. לא קיימות מאושרות לשני מצבים אלה והטיפול הוא רק מסייע.
Sialidosis נגרמת על ידי חסר באנזים neuraminidase מה שגורם להצטברות של sialyloligosaccharide בליזוזומים. אלה עם sialidosis מתאפיינים עם מפגעים קליניים חמורים יותר (type II) או מתונים יותר (type I). מאפיינים קליניים אלה נעים בין התפתחות מוקדמת איטית, קומה נמוכה, dysostosis multiplex (מחלה נדירה קונגניטלית המאופיינת על ידי שינויים שלדיים כונדרודיסטרופיים ושקיעה של חומר דמוי-ליפיד ברקמות רבות בגוף. התמונה האופיינית היא של גמדות עם דפורמציה של גפיים והגדלת הכבד והטחול) עד התפתחות מאוחרת של תסמונת מיוקלונית עם כתם אדום בוהק. (מחלה זו היא הנדירה ביותר מכלל המחלות הגורמות לאפילפסיות מיוקלוניות פרוגרסיביות, והוא מתחלק לשתי התבטאויות פנוטיפיות דומות המבטאות לכאורה פגיעות שונות בגנים סמוכים על אותו כרומוזום. Type I-גיל הופעת הסימפטומים, בזמן הילדות המאוחרת עם התבטאות הכוללת מיוקלונוס (לרוב בצורה קשה), הפרעה פרוגרסיבית בראייה, פרכוסים טוניים-קלוניים, אטקסיה וכתם אדום בוהק בפונדוסקופיה. ניתן למצוא עכירות ניכרת של העדשה בעין ופגיעה נוירולוגית פריפרית עם תחושה של שריפה בגפיים התחתונות. במחלה זו לא מתפתחת דמנציה. Type II- ההתבטאות דומה לזו שב Type I אבל המחלה מופיעה בגיל ההתבגרות, כשלהתבטאות הקלינית נוספים פגיעה במבנה הפנים, הפרעה בשמיעה וירידה איטית באינטלקט. האבחנה היא קלינית, על ידי מציאת כתם אדום בוהק בפונדוסקופיה. זאת לאחר התחלת ההתבטאות הקלינית של המחלה. האבחנה הסופית נעשית על ידי מציאת רמה גבוהה של Siolyloligosaccharides בשתן וחוסר ב Cayalabile αN- acetylneuroaminidase בלויקוציטים ובתרביות פיברובלסטים.
בנוסף, עלולים להופיע פרכוסים ושיגשון, היפר-רפלקסיה בלמעלה מ-50% מהלוקים במחלה בשלב חיים מאוחר יותר. אנליזה של חומצה סיאלית בשתן, מגלה יחס נמוך של חומצה סיאלית חופשית לסך חומצה סיאלית במטופלים עם sialidosis. מומלץ גם לבצע אנליזה של אוליגוסכרידים בשתן, במטופלים החשודים ל-sialidosis מצב הנגרם על ידי פתוגניות דו-אללית של וריאנטים בגן NEU1. מפגע נוסף ידוע כ-galactosialidosis בו רוב המאובחנים הם בעלי תסמינים מתונים יותר של אטקסיה, מיוקלונוס, אנגיוקרטומה, ודעיכה נוירולוגית וקוגניטיבית. גלקטוסיאלידוזיס הוא מפע אוטוזומלי-רצסיבי הנגרם על ידי וריאנט פתוגני דו-אללי של הגן CTSA.
אינטרפרטציה
תוצאה מוגברת של היחס בין סך חומצה סיאלית לחומצה סיאלית חופשית יכולה לשמש אינדיקציה למצבים של sialidosis או של galactosialidosis (Annunziata וחב' ב־Expert Opin Orphan Drugs משנת 2017. לעומת זאת תוצאה מופחת של יחס זה יכולה לשמש אינדיקציה למחלת אגירה של חומצה סיאלית. עליה קלה בוחמצה סיאלית חופשית בשתן יכולה להופיע גם מסיבות אחרות הכוללות ספסיס, מחלת כליות, תסמונת המוליטית-אורמית וסוכרת type 2 .
Selectins
סלקטינים הם מבנים התלויים בסידן, טרנס-ממברנליים type I, הנקשרים למולקולות קרבוהידרטיות המכילות fucose שעברו סיאלילציה, המתפקדים בספיחה וסקולרית, ומשחקים תפקיד מפתח בתהליכי דלקת, חיסון, המוסטאזיס, והתקדמות התהליך הסרטני. הליגנד של selectin מבטא ביטוי-יתר בתאי סרטן מה שמבגביר את התהליך הגרורתי, את הפרוגנוזה הגרועה, את יכולת הספיחה של תאי סרטן, ומשפעל את הקסקדה האיתותית של תאים אלה. סלקטינים משחקים תפקיד חיוני בתהליך ה-homing של לויקוציטים, והקישור של L-selecin לליגנדים על פני לויקוציטים משפעל תאים אלה. סלקטינים מאפשרים אינטראקציה עם טסיות ועם תאי אנדותל.
הוראות לביצוע הבדיקה
יש לאסוף דגימת שתן אקראית רצוי של שעות הבוקר המוקדמות. יציבות דגימת השתן בקירור (דגימה מועדפת) 90 יום, וזה גם פרק הזמן של יציבות דגימת השתן הקפואה. יש לצרף לדגימה את גיל הנבדק. המדידה מתבצעת בשיטת Liquid Chromatography Tandem Mass Spectrometry (LC-MS/MS)).
ראו גם
- חזרה לדף מדריך בדיקות מעבדה
- בדיקות מעבדה - מדדי פוריות ורבייה
- בדיקות מעבדה - מפגעי מערכת העצבים והמוח
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק