הבדלים בין גרסאות בדף "פורפובילינוגן דמינאז - Porphobilinogen deaminase"
(יצירת דף עם התוכן "{{בדיקת מעבדה |שם עברי=פורפובילינוגן דמינאז |שם לועזי=Porphobilinogen deaminase |קיצור=hydroxymethylbilane synthas...") |
|||
| (7 גרסאות ביניים של אותו משתמש אינן מוצגות) | |||
| שורה 3: | שורה 3: | ||
|שם לועזי=Porphobilinogen deaminase | |שם לועזי=Porphobilinogen deaminase | ||
|קיצור=hydroxymethylbilane synthase (להלן HMBS), uroporphyrinogen I synthase, ו-PBD. | |קיצור=hydroxymethylbilane synthase (להלן HMBS), uroporphyrinogen I synthase, ו-PBD. | ||
| − | |תמונה= | + | |תמונה=[[קובץ:Porphobilinogen1.jpg|250ox]] |
| − | |כיתוב תמונה= | + | |כיתוב תמונה=Porphobilinogen |
|מעבדה=[[כימיה בדם]] ו[[כימיה בשתן]]. | |מעבדה=[[כימיה בדם]] ו[[כימיה בשתן]]. | ||
|תחום=[[פורפיריות]] | |תחום=[[פורפיריות]] | ||
|יחידות מדידה= | |יחידות מדידה= | ||
| − | |טווח ערכים תקין=ערכים אלה נקבעו רק לבני 16 שנים ומעלה, והם גבוהים או שווים ל-7 ננומול/ליטר/שניה. | + | |טווח ערכים תקין=ערכים אלה נקבעו רק לבני 16 שנים ומעלה, והם גבוהים או שווים ל-7 ננומול/ליטר/שניה. |
| − | ערכי ביניים הם 6.0-6.9 ננומול/ ליטר/שניה. | + | ערכי ביניים הם 6.0-6.9 ננומול/ ליטר/שניה. |
ערכים מופחתים הם פחות מ-6 ננומול/ליטר/שניה. | ערכים מופחתים הם פחות מ-6 ננומול/ליטר/שניה. | ||
| שורה 17: | שורה 17: | ||
}} | }} | ||
==מטרת הבדיקה== | ==מטרת הבדיקה== | ||
| − | בדיקה מדרגה ראשונה להערכה של חשד לפורפיריה חריפה, ל-AIP, לקופרופורפיריה תורשתית, ולפורפיריה וריאגטה. | + | בדיקה מדרגה ראשונה להערכה של חשד לפורפיריה חריפה, ל-AIP, לקופרופורפיריה תורשתית, ולפורפיריה וריאגטה. בתלות במפגע באנזים הספציפי המעורב, פורפיריות שונות והקודמנים שלהן מצטברים ליצירת סוגי הפורפיריה השונים. המתווים של הצטברות פורפירין באריתרוציטים ובפלזמה, והפרשת קודמנים של heme בשתן ובצואה, מאפשרים את הגילוי וההתמיינות של הפורפיריות. מפגעים אלה מסווגים ככאלה שמקורם באריתרוציטים ובכבד, תוך התבססות על המיקום הראשוני של המופע באנזים. יתרה מכך, הפורפיריה הכבדית יכולה להיות מסווגת ככרונית או כחריפה, על פי ההתייצגות הקלינית שלהן. |
| + | |||
| + | PBD הוא אנזים המקודד באדם על ידי הגן HMBS. אנזים זה כרוך בשלב השלישי של הביוסינתזה של ה-heme. האנזים מקטלז את דחיסת ראש לזנב של ארבע מולקולות porphobilinogen ליצירה ליניארית של hydroxymethylbilane, תוך שחרור מולקולות אמוניה. | ||
| + | |||
| + | ==מבנה ותפקוד== | ||
| + | מבחינה תפקודית PBD מקטלז את אובדן אמוניה מהמונומר הפורפובילינוגני בתהליך של דה-אמינציה, והפולימריזציה הבאה בעקבותיו ליצירת tetrapyrrole המשתחרר כ-hyroxymethylbilane. המבנה של PBD שמשקלו המולקולרי הוא 40–42 קילו-דלטון, שהוא אנזים משומר מאוד באורגניזמים השונים, ומורכב משלושה מקטעים (Lannfelt וחב' ב-Scand J Clin Lab Invest משנת 1989, Louie וחב' ב-Nature משנת 1992, Gill וחב' ב-Biochem J משנת 2009). מקטעים 1 ו-2 דומים ביותר: כל אחד מהם מורכב מחמישה β-sheets ושלושה α-helices באדם (Jordan ו-Warren ב-FEBS Lett משנת 1987). מקטע 3 ממוקם בי שני המקטעים הקודמים ויש לו גאומטריה שטוחה של β-sheet. | ||
| + | |||
| + | Dipyrrole, שהוא קו-פקטור של האנזים המורכב משני מולקולות פורפובילינוגן דחוסות, קשור קו-ולנטית למקטע 3 ומתמשך על לאתר הפעיל של האנזים, שהוא המגרעת בין מקטעים 1 ו-2. מספר שיירים טעונים של ארגינין נמצאו מייצבים את תפקודי carboxylate בשרשרת pyrrole הגדלה בהקשר של יצירת התוצר הסופי, hydroxymethylbilane (Lander וחב' ב-Biochem J משנת 1991). האנזים PBD מופיע כיחידות דימריות בציטופלזמה של התא. השלב הראשון כורך אלימינציה של E1 של אמוניה מהפורפובילינוגן, ליצירת תוצר ביניים קרבון-קטיוני (Pitchon וחב' ב-Tetrahedron משנת 1992). תוצר ביניים זה מותקף על ידי הקו-פקטור הדי-פירולי של PBD, אשר לאחר איבוד פרוטון יוצר טרימר הקשור קו-ולנטית ל-PBD. תוצר ביניים זה פתוח לריאקציה עם פורפובילינוגן. עם יצירת ה-hexamer, הידרוליזה מאשרת שחרור של hydroxymethylbilane כמו גם רגנרציה של הקו-פקטור (Leeper וחב' ב-Nature Prod Rep משנת 1989). התחום הרפואי הידוע ביותר הקשור לאנזים PBD, הוא acute intermittent porphyria, מפגע גנטי דומיננטי-רצסיבי בו מיוצרת כמות שאינה מספקת של hydroxymethylbimane, מה שגורם להצטברות של פורפובילינוגן בציטופלזמה. מצב זה נגרם על ידי מוטציה בגן, אשר ב-90% מהמקרים מפחיתה את כמויות האנזים. תוארו 115 מוטציות בגן הגורמות למחלה (Grandchamp וחב' ב-Nucleic Acid Res משנת 1989, ו-Asrrin ו-Desnick ב-Hum Mut משנת 1994). האנזים HMBS הוא מפתח לביוסינתזה של heme על ידי קטליזה של יצירת hydroxymethylbilane, הידוע גם כ-preuroporphyrinogen. ההליך הקטליטי מתחיל בהתכנסות של הקו-פקטור dipyrromethane, הנובע משתי מולקולות של פורפובילינוגן, או מ-preuroporphyrinogen על ידי apoenzyme. בשלב האחרון של הקטליזה, התוצר preuroporphyrinogen משתחרר תוך שהוא מותיר את הקו-פקטור השלם קשור ל-holodeaminase. | ||
| + | |||
| + | Acute intrrmittent porphyria (להלן AIP), הוא מפגע אוטוזומלי-רצסיבי נדיר, המתבטא לרוב עם כאבי בטן. המוטציות בגן סימפטומטיות ב-1–2 בני-אדם לכל 100,000. המוטציה מובילה לחסר של PBD. פורפובילינוגן ו-δ-aminolevulinic acid מצטברים ברקמות, וגורמים למשבר נוירו-ויסצרלי שמתבטא בכאבי בטן חריפים. התקפי כאבים אלה יכולים להתגבר על ידי גירוי של מערכת ציטוכרום 450 עם תרופות כגון rifampin, ברביטורטים וסולפונאמידים), אסטרוגנים או פרוגסטרון, עישון או צריכת אלכוהול. כאבי בטן מתרחשים גם כאשר יש השרייה של heme oxygenase על ידי עקות פיזיולוגיות כגון חום, צום, או זיהומים. | ||
| + | |||
| + | תוצאה נורמלית אינה שוללת AIP, שכן ב-5-10% מהמקרים של AIP מתקבלת פעילות נורמלית של PBD באריתרוציטים. בנוסף, פעילות האנזים יכולה להיות מוגברת בעת התקף חריף, לפיכך רמת האנזים צריכה להיקבע רק כאשר המטופל א-תסמיני. | ||
| + | |||
| + | הכאב נגרם על ידי נוירופתיה אוטונומית ויסצרלית המובילה לאזורי בטן פעילים ביתר. הכאבים עלולים להיות עקשים או עוויתיים, והם ממוקמים בדרך כלל בחלק התחתון של הבטן אך עלולים להופיע בגב או בצלעות הנמוכות. תסמינים נוספים כוללים חום, הקאות, עצירות, חולשה, התכווצויות שרירים, פרכוסים, הזיות ותלונות על תסמינים נוירו-פסיכיאטריים כולל דיכאון ודאגנות. ייתכן גם מצב של dysautonomia המאופיינת על ידי פגיעה במערכת העצבים האוטונומית. מצב זה עלול להשפיע על תקוד הלב, שלפוחית השתן, המעיים, בלוטות הזיעה וכלי הדם. למצב זה יש סיבות רבות, לא כולן נוירופתיות. ישנן מספר מחלות דיסאוטונומיות, בהן מחלת [[פרקינסון]], [[איידס]], ניוון רב מערכתי, כשל אוטונומי, תסמונת הטכיקרדיה התנוחתית, נוירופתיה אוטונומית. דיסאוטונומיה עלולה לגרום לתסמינים חוץ-בטניים כגון סומק, טכיקרדיה, דיאפורזיס (הֲזָעָת יתר), ויתר לחץ-דם או לחץ-דם נמוך. הפרכוסים נגרמים בדרך כלל כתוצאה מהיפונתרמיה, שיכולה להיות שניונית להקאות או לתסמונת של הפרשה לא ראויה של הורמון אנטי-דיורטי (ADH). נוירופתיה עלולה להיות מהירה וחמורה., שעלולה להוביל למעורבות רספירטורית מסכנת-חיים. הבטן בדרך כלל רך, עם רגישות קלה בלבד. האבחון מתבצע על ידי גילוי רמות מוגברות של פורפובילינוגן בשתן. התנהלות קצרת זמן של acute intermittent porphyria (להלן AIP) כוללת בקרת כאב, והערכה של תסמינים מסכני-חיים, כגון התפשרות נשימתית שמקורה בנוירופתיה סַרְעַפְתִּית או בהיפו-נתרמיה. | ||
| + | |||
| + | הפורפיריות הן קבוצה של של מפגעים העוברים בהורשה הנובעים מפגימות אנזימטיות במסלול הביוסינתזה של heme (Tortoelli ב-Biochem Mol Basi Pediatric Dis משנת 2003, Nuttall ו-Klee ב-Tietz Textbook Clin Chem משנת 2001, ו-Anderson וחב' ב-Am J Med Sci משנת 2021). ה-acute intermittent porphyria נובעת מירידה בפעילות האריתרוציטית של PBD. הופעת AIP מתחילה בגיל הבשלות המינית או מאוחר יותר, כאשר הלוקים במחלה חשים באפיזודות של תסמינים נוירופתיים. משברים בתסמינים עלולים להתגבר על ידי מגוון רחב של תרופות כגון ברביטורטים, תרופות סולפה ואלכוהול זיהומים, צום, מתכות כבדות ושינויים הורמונליים. אבחון מוקדם של AIP חיוני שכן המפגע עלול להיות קטלני. למעלה מ-80% מהמטופלים עם וריאנט חסר בגן HMBS, נותרים א-תסמיניים למשך כל חייהם. האבחון הביוכימי של AIP מתבצע על ידי הדגמה של הפרשה מוגברת של פורפובילינוגן בשתן, והיא מדויקת ביותר בעת אפיזודה חריפה. בנוסף, האבחון של AIP יכול להיות מדויק על ידי בדיקה כמותית של פעילות האנזים PBGD באריתרוציטים, אף על פי ש-5% עד 10% של המטופלים נמצאים עם פעילות נורמלית של PBGD באריתרוציטים. בנוסף לכך, אישור גנטי מולקולרי זמין על בסיס קליני, ועשוי להיות לעזר בזיהוי בני משפחה א-תסמיניים עם סיכון של תסמינים חריפים. | ||
| + | |||
| + | הפורפיריה הראשונית הכבדית החריפה, ה-AIP, הקופרופורפיריה התורשתית (להלן HCP), וה-variegate porphyria (להלן VP), כרוכים בתסמינים נוירו-ויסצרליים, שתחילתם בתקופת הבשלות המינית (pubery) או מאוחר יותר. רגישות לאור אינה כרוכה עם AIP, אך יכולה להיות רלוונטית במקרים של HCP ו-VP. הפורפובילינוגן בשתן מוגבר במהלך הפאזות החריפות של הפורפיריות הנוירולוגיות. אנליזה של פורפירינים בשתן או בצואה, צריכות להתבצע לאשרר את האבחון ולהבדיל בין HCP, AIP ו-VP. ויכולה לקבל אישור על ידי מדידת פורפיריות בצואה. Metachromatic leukodystrophy (צורות הבוגרים או הילדים), קשורה לדיס-פונקציה של הגן המקודד ל-arylsulphatase (להלן ARSA), הממוקם בעמדה 22q13, וכתוצאה מכך לחסר של ARSA ולאגירה אנורמלית ליזוזומלית של גלקטוזיל סולפטיד (להלן צרברוזיד סולפאט. חסר של saposin B, שהוא קו-פקטור של האנזים, גורם ל-metachromatic leukodystrophy (להלן MLD). מחלה זו מופיעה בשלוש צורות: וולדותי, ילדותי ו-ובוגר. אוליגודנדרוציטים רגישים במיוחד לאגירה הליזוזומלית | ||
| + | המוגזמת, מה שגורם לדה-מיאלינציה ולפגיעה בתפקוד הנוירולוגי. התסמינים הפיזיקליים כוללים שיגשון, שיתוק, אטרופיה אופטית, דיסטוניה, דיסארתריה (דיסארתריה, פגם בדיבור שנובע מנזק למערכת העצבים} היפו-רפלקסיה המתקדמת להיפר-רפלקסיה, דעיכה קוגניטיבית, שיטיון ומצב דה-צרברטיבי. מוצאים גם שינויי אישיות, דעיכה בהישגים בלימודים, עד כדי פסיכוזה. הדמיית MRI של המוח תראה שינויים בחומר הלבן כתוצאה של דה-מיאלינציה, והאבחון נעשה על ידי מדידת סולפטידים בשתן, וכן על ידי מציאת רמות נמוכות של האנזים בלויקוציטים בדם. | ||
| + | |||
| + | γ-אמינו-לבולינאט דהידרטאז (להלן ALAD) ידוע גם כ-porphobilinogen synthase או כ-porphobilinogen oxygenase, הוא אנזים המורכב מ-8 תת-יחידות זהות של 330 חומצות אמינו כל אחת. אנזים זה מקטלז את הדחיסה של שתי מולקולות של γ-אמינו-לבולינאט ליצירה של poyrrol porphobilinogen. אבץ חיוני לפעילות האנזימטית של ALAD, כאשר ALAD מעוכב על ידי עופרת. האנזים יוצר קשר Schiff-base עם המצע, והוא ממוקם בציטוזול. הפעילות של ALAD מושרית על ידי חסר חמצן. פעילות זו חוזרת לרמתה הנורמלית לאחר 4 ימים של התאוששות ממצב ה-hypoxia, מה שאינו מתרחש עם האנזים porphobilinogen deaminase. | ||
| + | |||
| + | [[קובץ:Heme1.png|מרכז|600px]] | ||
| + | |||
| + | ==פתו-ביולוגיה של פורפיריות== | ||
| + | קופרופורפיריה תורשתית (HCP) ו-פורפיריה וריאגטה (VP) נובעות מ-50% חסר של האנזים קופרופורפירינוגן אוקסידז (CPO), כמו גם חסר של האנזים פרוטפורפירינוגן אוקסידז (PPO). תוארו מוטציות שונות רבות בגנים המקודדים לאנזימים אלה. מוטציה ספציפית של הגן PPO (ללR59W), שכיחה בדרום אפריקה. ALA ו-PBG מוגברים בעת התקפים חריפים, בעוד שדרגת ומשך עליות אלו פחותות בדרך כלל מאשר ב-AIP. העליות ב-ALA וב-PBG מתרחשות כאשר ALA synthase (להלן ALAS1) ממקור כבדי מושרה על ידי גורמים כגון סטרואידים אנדוגניים, תרופות, ושינויי תזונה, וכיוון שהפעילות של PBG deaminase נמוכה כמעט כזו של ALAS1 אפילו בכבד נורמלי. | ||
| + | |||
| + | קופרופורפירינוגן III יכול להצטבר ב-VP בגלל קשר תפקודי בין CPO לבין חסר ב-PPO, במיטוכונדריה. יתרה מכך, קופרופורפירינוגן אובד מהר יותר מהכבד, בהשווה לפורפירינוגנים אחרים, והאובדן הזה גדל כאשר מתגברת הסינתזה של heme. צורה אחרת של HCP, הידועה כ-harderoporphyria, שהיא צורה של CPO שעברה שינוי, עם זיקה נמוכה יותר למצע, גורמת להצטברות של harderoporphyrin כמו גם של קופרופורפירינוגן. | ||
| + | |||
| + | ==Acute ntermittent porphyria== | ||
| + | חסר של האנזימים פורפובילינוגן דאמינז (PBG) ושל hydroxymethylbilane synthase (להלן HMBS) גורמים ל-AIP, הנגרם על ידי מוטציה בגן 11q23.3. תסמינים של AIP כוללים מתאפיינים על ידי התקפים נורו-ויסצרליים, של כאבי בטן, בחילות, הִתְנַפְּחוּת (distension), שלשולים, הקאות, עצירות ואי מתן שתן. תסמיני ה-CNS, כגון דאגנות, פסיכוזה, ישנוניות, סערת נפש והזיות. כמו כן ייתכנו תסמיני מערכת העצבים ההיקפית כגון נוירופתיה היקפית העלולה להתקדם לנזק עצבי קבוע. תסמינים עלולים להופיע על ידי צריכת תרופות המקובלות על ידי פסיכיאטרים כגון חומצה ולפרואית, [[carbamazepine]], [[benzodiazepine]], ו-TCA. | ||
| + | |||
| + | ==שיטת הבדיקה== | ||
| + | Liquid chromatography-Tandem Mass Spectrometry LC-MS/MS. נוזל הבדיקה: שתן חד פעמי אקראי. אין להכניס לשתן חומרים משמרים, אך ה-pH שלו חייב להיות מעל 5.0. השתן חייב להיכנס להקפאה מייד לאחר נטילתו. יש לשלוח את הדגימה למעבדה מוגנת מאור. יש לתעד את גיל הנבדק, ואת רשימת התרופות שהוא נוטל. הנבדק אמור להימנע משתיית אלכוהול 24 שעות לפני מתן השתן. זה חיוני כיוון שאתנול משרה פעילות של האנזים PBD. יש לפסול דגימות שתן מאוד המוליטיות. כאשר הבדיקה מתבצעת בדם יש לאחסן את הדם המלא בקירור (מועדף) שמשך יציבותו 8 ימים, או בטמפרטורת החדר שיציבותו 7 ימים. את הדם יש ליטול במבחנת הפארין (פקק ירוק) או במבחנת ספירת-דם (EDTA פקק סגלגל). | ||
| + | |||
| + | ==מדידת פורפובילינוגן בשתן== | ||
| + | יש ערכות מסחריות למדידת פורפובילינוגן בשתן (Hashim ב-Tutorials Clin Chem משנת 2024). ניתן להשתמש בריאגנט Ehrlich ויצירת amyl alcohol. ההופעה של צבע אדום בפאזה האורגנית העליונה (amyl alcohol) מצביעה על נוכחות urobilinogen, ומצביעה על כך שהדגימה שלילית לגבי פורפובילינוגן. עם זאת, הנוכחות של צבע אדום בפאזה המימית התחתונה מצביעה על נוכחות פורפובילינוגן. מגבלות של שיטה זו היא שבדגימות שתן "מרוכזות", urobilinogen בכמויות זעירות יכולות להימצא בפאזה האורגנית, שזו תופעה נורמלית. דגימות הנלקחות לזיהוי של acute intermittent porphyria חייבות להילקח במהלך התקף, שכן PBG יכול להיות שלילי במהלך שלבי ביניים. מחלת כבד עלולה להגדיל את coproporphyrin בשתן בגלל הפרשה מרתית, שהיא הגורם השכיח ביותר של פורפינוריה. בנוסף לזיהוי וטיפול בגורמי המחלה, טיפול עם אופיואידים, saline, דקסטרוז, chlorpromazine, ועירוי ורידי של hemin, מטרתם לעכב את 5ALAS I הפחתת רמות PBG בשתן, מצביעה על תגובה לטיפול. | ||
| + | |||
| + | ==ראו גם== | ||
| + | *[[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | ||
| + | * [[בדיקת מחלות מעי|בדיקות מעבדה - מחלות מעי]] | ||
| + | |||
| + | {{ייחוס בן עמי}} | ||
| + | |||
| + | [[קטגוריה:בדיקות מעבדה - מחלות מעי]] | ||
| + | [[קטגוריה:בדיקות מעבדה: כימיה בדם]] | ||
| + | [[קטגוריה:בדיקות מעבדה: כימיה בשתן]] | ||
גרסה אחרונה מ־05:03, 7 באוקטובר 2024
| מדריך בדיקות מעבדה | |
| פורפובילינוגן דמינאז | |
|---|---|
| Porphobilinogen deaminase | |
| שמות אחרים | hydroxymethylbilane synthase (להלן HMBS), uroporphyrinogen I synthase, ו-PBD. |
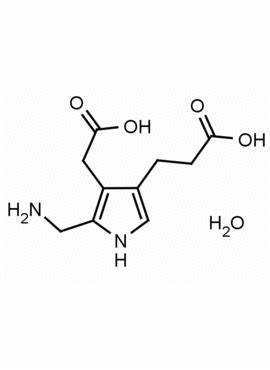
| |
Porphobilinogen
| |
| מעבדה | כימיה בדם וכימיה בשתן. |
| תחום | פורפיריות |
| טווח ערכים תקין | ערכים אלה נקבעו רק לבני 16 שנים ומעלה, והם גבוהים או שווים ל-7 ננומול/ליטר/שניה.
ערכי ביניים הם 6.0-6.9 ננומול/ ליטר/שניה. ערכים מופחתים הם פחות מ-6 ננומול/ליטר/שניה. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
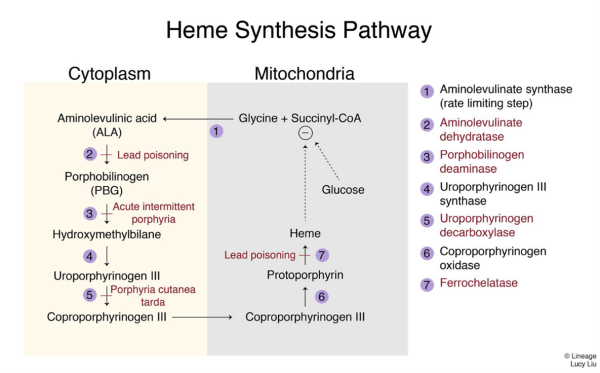
בדיקה מדרגה ראשונה להערכה של חשד לפורפיריה חריפה, ל-AIP, לקופרופורפיריה תורשתית, ולפורפיריה וריאגטה. בתלות במפגע באנזים הספציפי המעורב, פורפיריות שונות והקודמנים שלהן מצטברים ליצירת סוגי הפורפיריה השונים. המתווים של הצטברות פורפירין באריתרוציטים ובפלזמה, והפרשת קודמנים של heme בשתן ובצואה, מאפשרים את הגילוי וההתמיינות של הפורפיריות. מפגעים אלה מסווגים ככאלה שמקורם באריתרוציטים ובכבד, תוך התבססות על המיקום הראשוני של המופע באנזים. יתרה מכך, הפורפיריה הכבדית יכולה להיות מסווגת ככרונית או כחריפה, על פי ההתייצגות הקלינית שלהן.
PBD הוא אנזים המקודד באדם על ידי הגן HMBS. אנזים זה כרוך בשלב השלישי של הביוסינתזה של ה-heme. האנזים מקטלז את דחיסת ראש לזנב של ארבע מולקולות porphobilinogen ליצירה ליניארית של hydroxymethylbilane, תוך שחרור מולקולות אמוניה.
מבנה ותפקוד
מבחינה תפקודית PBD מקטלז את אובדן אמוניה מהמונומר הפורפובילינוגני בתהליך של דה-אמינציה, והפולימריזציה הבאה בעקבותיו ליצירת tetrapyrrole המשתחרר כ-hyroxymethylbilane. המבנה של PBD שמשקלו המולקולרי הוא 40–42 קילו-דלטון, שהוא אנזים משומר מאוד באורגניזמים השונים, ומורכב משלושה מקטעים (Lannfelt וחב' ב-Scand J Clin Lab Invest משנת 1989, Louie וחב' ב-Nature משנת 1992, Gill וחב' ב-Biochem J משנת 2009). מקטעים 1 ו-2 דומים ביותר: כל אחד מהם מורכב מחמישה β-sheets ושלושה α-helices באדם (Jordan ו-Warren ב-FEBS Lett משנת 1987). מקטע 3 ממוקם בי שני המקטעים הקודמים ויש לו גאומטריה שטוחה של β-sheet.
Dipyrrole, שהוא קו-פקטור של האנזים המורכב משני מולקולות פורפובילינוגן דחוסות, קשור קו-ולנטית למקטע 3 ומתמשך על לאתר הפעיל של האנזים, שהוא המגרעת בין מקטעים 1 ו-2. מספר שיירים טעונים של ארגינין נמצאו מייצבים את תפקודי carboxylate בשרשרת pyrrole הגדלה בהקשר של יצירת התוצר הסופי, hydroxymethylbilane (Lander וחב' ב-Biochem J משנת 1991). האנזים PBD מופיע כיחידות דימריות בציטופלזמה של התא. השלב הראשון כורך אלימינציה של E1 של אמוניה מהפורפובילינוגן, ליצירת תוצר ביניים קרבון-קטיוני (Pitchon וחב' ב-Tetrahedron משנת 1992). תוצר ביניים זה מותקף על ידי הקו-פקטור הדי-פירולי של PBD, אשר לאחר איבוד פרוטון יוצר טרימר הקשור קו-ולנטית ל-PBD. תוצר ביניים זה פתוח לריאקציה עם פורפובילינוגן. עם יצירת ה-hexamer, הידרוליזה מאשרת שחרור של hydroxymethylbilane כמו גם רגנרציה של הקו-פקטור (Leeper וחב' ב-Nature Prod Rep משנת 1989). התחום הרפואי הידוע ביותר הקשור לאנזים PBD, הוא acute intermittent porphyria, מפגע גנטי דומיננטי-רצסיבי בו מיוצרת כמות שאינה מספקת של hydroxymethylbimane, מה שגורם להצטברות של פורפובילינוגן בציטופלזמה. מצב זה נגרם על ידי מוטציה בגן, אשר ב-90% מהמקרים מפחיתה את כמויות האנזים. תוארו 115 מוטציות בגן הגורמות למחלה (Grandchamp וחב' ב-Nucleic Acid Res משנת 1989, ו-Asrrin ו-Desnick ב-Hum Mut משנת 1994). האנזים HMBS הוא מפתח לביוסינתזה של heme על ידי קטליזה של יצירת hydroxymethylbilane, הידוע גם כ-preuroporphyrinogen. ההליך הקטליטי מתחיל בהתכנסות של הקו-פקטור dipyrromethane, הנובע משתי מולקולות של פורפובילינוגן, או מ-preuroporphyrinogen על ידי apoenzyme. בשלב האחרון של הקטליזה, התוצר preuroporphyrinogen משתחרר תוך שהוא מותיר את הקו-פקטור השלם קשור ל-holodeaminase.
Acute intrrmittent porphyria (להלן AIP), הוא מפגע אוטוזומלי-רצסיבי נדיר, המתבטא לרוב עם כאבי בטן. המוטציות בגן סימפטומטיות ב-1–2 בני-אדם לכל 100,000. המוטציה מובילה לחסר של PBD. פורפובילינוגן ו-δ-aminolevulinic acid מצטברים ברקמות, וגורמים למשבר נוירו-ויסצרלי שמתבטא בכאבי בטן חריפים. התקפי כאבים אלה יכולים להתגבר על ידי גירוי של מערכת ציטוכרום 450 עם תרופות כגון rifampin, ברביטורטים וסולפונאמידים), אסטרוגנים או פרוגסטרון, עישון או צריכת אלכוהול. כאבי בטן מתרחשים גם כאשר יש השרייה של heme oxygenase על ידי עקות פיזיולוגיות כגון חום, צום, או זיהומים.
תוצאה נורמלית אינה שוללת AIP, שכן ב-5-10% מהמקרים של AIP מתקבלת פעילות נורמלית של PBD באריתרוציטים. בנוסף, פעילות האנזים יכולה להיות מוגברת בעת התקף חריף, לפיכך רמת האנזים צריכה להיקבע רק כאשר המטופל א-תסמיני.
הכאב נגרם על ידי נוירופתיה אוטונומית ויסצרלית המובילה לאזורי בטן פעילים ביתר. הכאבים עלולים להיות עקשים או עוויתיים, והם ממוקמים בדרך כלל בחלק התחתון של הבטן אך עלולים להופיע בגב או בצלעות הנמוכות. תסמינים נוספים כוללים חום, הקאות, עצירות, חולשה, התכווצויות שרירים, פרכוסים, הזיות ותלונות על תסמינים נוירו-פסיכיאטריים כולל דיכאון ודאגנות. ייתכן גם מצב של dysautonomia המאופיינת על ידי פגיעה במערכת העצבים האוטונומית. מצב זה עלול להשפיע על תקוד הלב, שלפוחית השתן, המעיים, בלוטות הזיעה וכלי הדם. למצב זה יש סיבות רבות, לא כולן נוירופתיות. ישנן מספר מחלות דיסאוטונומיות, בהן מחלת פרקינסון, איידס, ניוון רב מערכתי, כשל אוטונומי, תסמונת הטכיקרדיה התנוחתית, נוירופתיה אוטונומית. דיסאוטונומיה עלולה לגרום לתסמינים חוץ-בטניים כגון סומק, טכיקרדיה, דיאפורזיס (הֲזָעָת יתר), ויתר לחץ-דם או לחץ-דם נמוך. הפרכוסים נגרמים בדרך כלל כתוצאה מהיפונתרמיה, שיכולה להיות שניונית להקאות או לתסמונת של הפרשה לא ראויה של הורמון אנטי-דיורטי (ADH). נוירופתיה עלולה להיות מהירה וחמורה., שעלולה להוביל למעורבות רספירטורית מסכנת-חיים. הבטן בדרך כלל רך, עם רגישות קלה בלבד. האבחון מתבצע על ידי גילוי רמות מוגברות של פורפובילינוגן בשתן. התנהלות קצרת זמן של acute intermittent porphyria (להלן AIP) כוללת בקרת כאב, והערכה של תסמינים מסכני-חיים, כגון התפשרות נשימתית שמקורה בנוירופתיה סַרְעַפְתִּית או בהיפו-נתרמיה.
הפורפיריות הן קבוצה של של מפגעים העוברים בהורשה הנובעים מפגימות אנזימטיות במסלול הביוסינתזה של heme (Tortoelli ב-Biochem Mol Basi Pediatric Dis משנת 2003, Nuttall ו-Klee ב-Tietz Textbook Clin Chem משנת 2001, ו-Anderson וחב' ב-Am J Med Sci משנת 2021). ה-acute intermittent porphyria נובעת מירידה בפעילות האריתרוציטית של PBD. הופעת AIP מתחילה בגיל הבשלות המינית או מאוחר יותר, כאשר הלוקים במחלה חשים באפיזודות של תסמינים נוירופתיים. משברים בתסמינים עלולים להתגבר על ידי מגוון רחב של תרופות כגון ברביטורטים, תרופות סולפה ואלכוהול זיהומים, צום, מתכות כבדות ושינויים הורמונליים. אבחון מוקדם של AIP חיוני שכן המפגע עלול להיות קטלני. למעלה מ-80% מהמטופלים עם וריאנט חסר בגן HMBS, נותרים א-תסמיניים למשך כל חייהם. האבחון הביוכימי של AIP מתבצע על ידי הדגמה של הפרשה מוגברת של פורפובילינוגן בשתן, והיא מדויקת ביותר בעת אפיזודה חריפה. בנוסף, האבחון של AIP יכול להיות מדויק על ידי בדיקה כמותית של פעילות האנזים PBGD באריתרוציטים, אף על פי ש-5% עד 10% של המטופלים נמצאים עם פעילות נורמלית של PBGD באריתרוציטים. בנוסף לכך, אישור גנטי מולקולרי זמין על בסיס קליני, ועשוי להיות לעזר בזיהוי בני משפחה א-תסמיניים עם סיכון של תסמינים חריפים.
הפורפיריה הראשונית הכבדית החריפה, ה-AIP, הקופרופורפיריה התורשתית (להלן HCP), וה-variegate porphyria (להלן VP), כרוכים בתסמינים נוירו-ויסצרליים, שתחילתם בתקופת הבשלות המינית (pubery) או מאוחר יותר. רגישות לאור אינה כרוכה עם AIP, אך יכולה להיות רלוונטית במקרים של HCP ו-VP. הפורפובילינוגן בשתן מוגבר במהלך הפאזות החריפות של הפורפיריות הנוירולוגיות. אנליזה של פורפירינים בשתן או בצואה, צריכות להתבצע לאשרר את האבחון ולהבדיל בין HCP, AIP ו-VP. ויכולה לקבל אישור על ידי מדידת פורפיריות בצואה. Metachromatic leukodystrophy (צורות הבוגרים או הילדים), קשורה לדיס-פונקציה של הגן המקודד ל-arylsulphatase (להלן ARSA), הממוקם בעמדה 22q13, וכתוצאה מכך לחסר של ARSA ולאגירה אנורמלית ליזוזומלית של גלקטוזיל סולפטיד (להלן צרברוזיד סולפאט. חסר של saposin B, שהוא קו-פקטור של האנזים, גורם ל-metachromatic leukodystrophy (להלן MLD). מחלה זו מופיעה בשלוש צורות: וולדותי, ילדותי ו-ובוגר. אוליגודנדרוציטים רגישים במיוחד לאגירה הליזוזומלית המוגזמת, מה שגורם לדה-מיאלינציה ולפגיעה בתפקוד הנוירולוגי. התסמינים הפיזיקליים כוללים שיגשון, שיתוק, אטרופיה אופטית, דיסטוניה, דיסארתריה (דיסארתריה, פגם בדיבור שנובע מנזק למערכת העצבים} היפו-רפלקסיה המתקדמת להיפר-רפלקסיה, דעיכה קוגניטיבית, שיטיון ומצב דה-צרברטיבי. מוצאים גם שינויי אישיות, דעיכה בהישגים בלימודים, עד כדי פסיכוזה. הדמיית MRI של המוח תראה שינויים בחומר הלבן כתוצאה של דה-מיאלינציה, והאבחון נעשה על ידי מדידת סולפטידים בשתן, וכן על ידי מציאת רמות נמוכות של האנזים בלויקוציטים בדם.
γ-אמינו-לבולינאט דהידרטאז (להלן ALAD) ידוע גם כ-porphobilinogen synthase או כ-porphobilinogen oxygenase, הוא אנזים המורכב מ-8 תת-יחידות זהות של 330 חומצות אמינו כל אחת. אנזים זה מקטלז את הדחיסה של שתי מולקולות של γ-אמינו-לבולינאט ליצירה של poyrrol porphobilinogen. אבץ חיוני לפעילות האנזימטית של ALAD, כאשר ALAD מעוכב על ידי עופרת. האנזים יוצר קשר Schiff-base עם המצע, והוא ממוקם בציטוזול. הפעילות של ALAD מושרית על ידי חסר חמצן. פעילות זו חוזרת לרמתה הנורמלית לאחר 4 ימים של התאוששות ממצב ה-hypoxia, מה שאינו מתרחש עם האנזים porphobilinogen deaminase.
פתו-ביולוגיה של פורפיריות
קופרופורפיריה תורשתית (HCP) ו-פורפיריה וריאגטה (VP) נובעות מ-50% חסר של האנזים קופרופורפירינוגן אוקסידז (CPO), כמו גם חסר של האנזים פרוטפורפירינוגן אוקסידז (PPO). תוארו מוטציות שונות רבות בגנים המקודדים לאנזימים אלה. מוטציה ספציפית של הגן PPO (ללR59W), שכיחה בדרום אפריקה. ALA ו-PBG מוגברים בעת התקפים חריפים, בעוד שדרגת ומשך עליות אלו פחותות בדרך כלל מאשר ב-AIP. העליות ב-ALA וב-PBG מתרחשות כאשר ALA synthase (להלן ALAS1) ממקור כבדי מושרה על ידי גורמים כגון סטרואידים אנדוגניים, תרופות, ושינויי תזונה, וכיוון שהפעילות של PBG deaminase נמוכה כמעט כזו של ALAS1 אפילו בכבד נורמלי.
קופרופורפירינוגן III יכול להצטבר ב-VP בגלל קשר תפקודי בין CPO לבין חסר ב-PPO, במיטוכונדריה. יתרה מכך, קופרופורפירינוגן אובד מהר יותר מהכבד, בהשווה לפורפירינוגנים אחרים, והאובדן הזה גדל כאשר מתגברת הסינתזה של heme. צורה אחרת של HCP, הידועה כ-harderoporphyria, שהיא צורה של CPO שעברה שינוי, עם זיקה נמוכה יותר למצע, גורמת להצטברות של harderoporphyrin כמו גם של קופרופורפירינוגן.
Acute ntermittent porphyria
חסר של האנזימים פורפובילינוגן דאמינז (PBG) ושל hydroxymethylbilane synthase (להלן HMBS) גורמים ל-AIP, הנגרם על ידי מוטציה בגן 11q23.3. תסמינים של AIP כוללים מתאפיינים על ידי התקפים נורו-ויסצרליים, של כאבי בטן, בחילות, הִתְנַפְּחוּת (distension), שלשולים, הקאות, עצירות ואי מתן שתן. תסמיני ה-CNS, כגון דאגנות, פסיכוזה, ישנוניות, סערת נפש והזיות. כמו כן ייתכנו תסמיני מערכת העצבים ההיקפית כגון נוירופתיה היקפית העלולה להתקדם לנזק עצבי קבוע. תסמינים עלולים להופיע על ידי צריכת תרופות המקובלות על ידי פסיכיאטרים כגון חומצה ולפרואית, carbamazepine, benzodiazepine, ו-TCA.
שיטת הבדיקה
Liquid chromatography-Tandem Mass Spectrometry LC-MS/MS. נוזל הבדיקה: שתן חד פעמי אקראי. אין להכניס לשתן חומרים משמרים, אך ה-pH שלו חייב להיות מעל 5.0. השתן חייב להיכנס להקפאה מייד לאחר נטילתו. יש לשלוח את הדגימה למעבדה מוגנת מאור. יש לתעד את גיל הנבדק, ואת רשימת התרופות שהוא נוטל. הנבדק אמור להימנע משתיית אלכוהול 24 שעות לפני מתן השתן. זה חיוני כיוון שאתנול משרה פעילות של האנזים PBD. יש לפסול דגימות שתן מאוד המוליטיות. כאשר הבדיקה מתבצעת בדם יש לאחסן את הדם המלא בקירור (מועדף) שמשך יציבותו 8 ימים, או בטמפרטורת החדר שיציבותו 7 ימים. את הדם יש ליטול במבחנת הפארין (פקק ירוק) או במבחנת ספירת-דם (EDTA פקק סגלגל).
מדידת פורפובילינוגן בשתן
יש ערכות מסחריות למדידת פורפובילינוגן בשתן (Hashim ב-Tutorials Clin Chem משנת 2024). ניתן להשתמש בריאגנט Ehrlich ויצירת amyl alcohol. ההופעה של צבע אדום בפאזה האורגנית העליונה (amyl alcohol) מצביעה על נוכחות urobilinogen, ומצביעה על כך שהדגימה שלילית לגבי פורפובילינוגן. עם זאת, הנוכחות של צבע אדום בפאזה המימית התחתונה מצביעה על נוכחות פורפובילינוגן. מגבלות של שיטה זו היא שבדגימות שתן "מרוכזות", urobilinogen בכמויות זעירות יכולות להימצא בפאזה האורגנית, שזו תופעה נורמלית. דגימות הנלקחות לזיהוי של acute intermittent porphyria חייבות להילקח במהלך התקף, שכן PBG יכול להיות שלילי במהלך שלבי ביניים. מחלת כבד עלולה להגדיל את coproporphyrin בשתן בגלל הפרשה מרתית, שהיא הגורם השכיח ביותר של פורפינוריה. בנוסף לזיהוי וטיפול בגורמי המחלה, טיפול עם אופיואידים, saline, דקסטרוז, chlorpromazine, ועירוי ורידי של hemin, מטרתם לעכב את 5ALAS I הפחתת רמות PBG בשתן, מצביעה על תגובה לטיפול.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק