הבדלים בין גרסאות בדף "מלטונין - Melatonin"
(←ראו גם) |
|||
| (4 גרסאות ביניים של 2 משתמשים אינן מוצגות) | |||
| שורה 5: | שורה 5: | ||
|תמונה= | |תמונה= | ||
|כיתוב תמונה= | |כיתוב תמונה= | ||
| − | |מעבדה=[[ | + | |מעבדה=[[אנדוקרינולוגיה בדם]] |
|תחום=פיקוח הורמונאלי על תהליכי השעון הביולוגי | |תחום=פיקוח הורמונאלי על תהליכי השעון הביולוגי | ||
|יחידות מדידה= | |יחידות מדידה= | ||
| שורה 41: | שורה 41: | ||
הפילוסוף הצרפתי רנה דקארט ייחס לבלוטה משמעות בהקשר הפסיכופיזי, וטען שבלוטה זו היא "מקום מושב הנפש". אך רק בתחילת המאה ה-20 היה זה היבנר שתרם להבנת חשיבות האצטרובל, לאחר שטיפל בילד עם שאת סרטנית בבלוטה שהגיע לבגרות מינית מוקדמת. | הפילוסוף הצרפתי רנה דקארט ייחס לבלוטה משמעות בהקשר הפסיכופיזי, וטען שבלוטה זו היא "מקום מושב הנפש". אך רק בתחילת המאה ה-20 היה זה היבנר שתרם להבנת חשיבות האצטרובל, לאחר שטיפל בילד עם שאת סרטנית בבלוטה שהגיע לבגרות מינית מוקדמת. | ||
| − | בשנת 1995 פרסמו Robinson ו-Reiter את הספר | + | בשנת 1995 פרסמו Robinson ו-Reiter את הספר [[t:Melatonin|Melatonin]] בו הם ייחסו להורמון זה תפקידים ביולוגיים רבים. על פי שני אלה, מלטונין מווסת תהליכי הזדקנות, משפיע על מחזורי הרבייה, מגרה את בלוטת ההיפופיזה (יותרת המוח) ליצירת הורמון הגדילה (growth hormone), מווסת שינויים בפיגמנטציה של העור, וכמובן משפיע על מצבי ערות ושינה. בנוסף, מאמינים שני מחברי הספר שיש למלטונין פעילות נוגדת תהליכים סרטניים במספר מנגנונים: הגברת פעילות מערכת החיסון נגד תאי סרטן, היותו נוגד תהליכים מחמצנים כיוון שהורמון זה מסיס במים ובשומן ומתאפשרת חדירתו הקלה לרקמות רבות בגוף ויכולתו להגן על DNA מנזקי חמצון, היותו מקטין לכאורה את תהליך האנגיוגנזה (יצירת כלי דם חדשים המזינים גידולים סרטניים ומקלים על שליחת גרורות ברחבי הגוף). |
הראשון שבודד ואפיין את המלטונין בשנת 1958 היה Aaron Lerner, והוא עשה זאת בהקשר הפיקנטי כמעט של פקטור הגורם להבהרת העור בדו-חיים. אך בתחום היותר רלבנטי של התפקיד הפיזיולוגי של מלטונין בבני אדם, ניתן להגדיר מספר תחומים בהם תיתכן חשיבות להורמון זה. מעבר לחשיבות מלטונין בתחום מצבי הרוח (mood) הקשורים למצבי "אור וחשיכה" "יום ולילה", יש המציינים את השפעתו על מערכת החיסון, פריון (שאפילו בא לביטוי בשיעור ההצלחה של הפריה חוץ-גופית), ובעיקר בתחום האונקולוגי. | הראשון שבודד ואפיין את המלטונין בשנת 1958 היה Aaron Lerner, והוא עשה זאת בהקשר הפיקנטי כמעט של פקטור הגורם להבהרת העור בדו-חיים. אך בתחום היותר רלבנטי של התפקיד הפיזיולוגי של מלטונין בבני אדם, ניתן להגדיר מספר תחומים בהם תיתכן חשיבות להורמון זה. מעבר לחשיבות מלטונין בתחום מצבי הרוח (mood) הקשורים למצבי "אור וחשיכה" "יום ולילה", יש המציינים את השפעתו על מערכת החיסון, פריון (שאפילו בא לביטוי בשיעור ההצלחה של הפריה חוץ-גופית), ובעיקר בתחום האונקולוגי. | ||
| שורה 52: | שורה 52: | ||
===מלטונין והפרעות שינה=== | ===מלטונין והפרעות שינה=== | ||
| − | + | אך נראה שבתודעה הציבורית ואף בזו של החוקרים, הקשר המיידי של מלטונין הוא זה הקשור להפרעות שינה, אופי השינה, והשראת שינה. למלטונין יש ערך טיפולי למניעת הפרעות שינה שנגרמות בגלל "יעפת" (jet lag), אך מחקרים אחדים אישרו את יעילותו כי ייתכן שהוא יעיל גם כטיפול בנדודי שינה. המלטונין משמש בעיקר לטיפול בתסמונת פאזת השינה הדחויה, מה שידוע כ-DSPS או delayed sleep phase syndrome, שמקורה הוא שעון ביולוגי דחוי. בשנת 2008 אושרה על ידי ה-FDA לשימוש תרופת המרשם [[t:סירקדין - Circadin|סירקדין]] (Circadin), מלטונין בשחרור מבוקר בישראל, באירופה ובארצות שונות בעולם, לטיפול בנדודי שינה. התרופה פותחה על ידי החברה הפרמצבטית הישראלית "נעורים" (Neurim Pharmaceuticals). | |
| − | אך נראה שבתודעה הציבורית ואף בזו של החוקרים, הקשר המיידי של מלטונין הוא זה הקשור להפרעות שינה, אופי השינה, והשראת שינה. למלטונין יש ערך טיפולי למניעת הפרעות שינה שנגרמות בגלל "יעפת" (jet lag), אך מחקרים אחדים אישרו את יעילותו כי ייתכן שהוא יעיל גם כטיפול בנדודי שינה. המלטונין משמש בעיקר לטיפול בתסמונת פאזת השינה הדחויה, מה שידוע כ-DSPS או delayed sleep phase syndrome, שמקורה הוא שעון ביולוגי דחוי. בשנת 2008 אושרה על ידי ה-FDA לשימוש תרופת המרשם סירקדין (Circadin), מלטונין בשחרור מבוקר בישראל, באירופה ובארצות שונות בעולם, לטיפול בנדודי שינה. התרופה פותחה על ידי החברה הפרמצבטית הישראלית "נעורים" (Neurim Pharmaceuticals). | ||
Circadin הוא תכשיר בשחרור מושהה של 2 מיליגרם מלטונין, שנוטלים לפני השינה וכך הוא מחקה את פרופיל השחרור הפיזיולוגי של מלטונין אנדוגני. הטיפול מומלץ לבני 55 שנה ומעלה הסובלים מנדודי שינה (insomnia) ראשונית הפוגעת באיכות השינה. מחקר מראה שסירקדין משפר לא רק את איכות השינה אלא גם את הערנות ביום המחרת, בלי שהוא פוגע בזיכרון, בכושר הקוגניטיבי או בתפקוד הפסיכו-מוטורי. יתרון אחר שלו בהיותו חומר לא ממכר, שהפסקת השימוש בו אינה גורמת לתסמיני גמילה. | Circadin הוא תכשיר בשחרור מושהה של 2 מיליגרם מלטונין, שנוטלים לפני השינה וכך הוא מחקה את פרופיל השחרור הפיזיולוגי של מלטונין אנדוגני. הטיפול מומלץ לבני 55 שנה ומעלה הסובלים מנדודי שינה (insomnia) ראשונית הפוגעת באיכות השינה. מחקר מראה שסירקדין משפר לא רק את איכות השינה אלא גם את הערנות ביום המחרת, בלי שהוא פוגע בזיכרון, בכושר הקוגניטיבי או בתפקוד הפסיכו-מוטורי. יתרון אחר שלו בהיותו חומר לא ממכר, שהפסקת השימוש בו אינה גורמת לתסמיני גמילה. | ||
| שורה 59: | שורה 58: | ||
למלטונין יוחסו במרוצת השנים תכונות ויתרונות שונים בתחום הרפואה, אם כי לא בכולם ברור המנגנון, והמשמעות הביולוגית והטיפולית, אם בכלל. כך לדוגמה היו דיווחים רבים על משמעותו של מלטונין כנוגד-חמצון, השפעתו על מערכת החיסון בהגברת ייצור ציטוקינים כמו IL-1 ו-IL-2, ויש אף מחקרים התומכים בפעילות להאטת תהליכי הזדקנות של מלטונין, אך הפעילות האחרונה הודגמה בעיקר במחקרים עם עכברים. מחקרים אחרים רומזים להשפעתו במצבי דיכאון עונתיים, או ליעילותו בטיפול בכאבי ראש ומיגרנות. | למלטונין יוחסו במרוצת השנים תכונות ויתרונות שונים בתחום הרפואה, אם כי לא בכולם ברור המנגנון, והמשמעות הביולוגית והטיפולית, אם בכלל. כך לדוגמה היו דיווחים רבים על משמעותו של מלטונין כנוגד-חמצון, השפעתו על מערכת החיסון בהגברת ייצור ציטוקינים כמו IL-1 ו-IL-2, ויש אף מחקרים התומכים בפעילות להאטת תהליכי הזדקנות של מלטונין, אך הפעילות האחרונה הודגמה בעיקר במחקרים עם עכברים. מחקרים אחרים רומזים להשפעתו במצבי דיכאון עונתיים, או ליעילותו בטיפול בכאבי ראש ומיגרנות. | ||
| − | מחקרים בחיות אך גם בבני אדם הצביעו על השפעה של מלטונין להגנה בפני קרינה מייננת. נראה שיכולת מלטונין לקלוט רדיקלים חופשים קשורה להשפעה זו כנגד קרינה. יש אף מספר מחקרים המצביעים על מלטונין כמשפר מצבי טנטון (tinnitus). | + | מחקרים בחיות אך גם בבני אדם הצביעו על השפעה של מלטונין להגנה בפני קרינה מייננת. נראה שיכולת מלטונין לקלוט רדיקלים חופשים קשורה להשפעה זו כנגד קרינה. יש אף מספר מחקרים המצביעים על מלטונין כמשפר מצבי [[טנטון]] (tinnitus). |
===אינטראקציות עם תרופות=== | ===אינטראקציות עם תרופות=== | ||
| − | + | '''תרופות המפחיתות רמת מלטונין''': [[חוסמי תעלות סידן]] כגון nifedipine,amlodipine ,verapamil ,diltiazem ,felodipine ,nisoldipine ,bepridil; חוסמי בטא כגון acebutolol ,atenolol ,bisoprolol ,carteolol ,metoprolol ,nadolol ,propranolol. | |
| − | '''תרופות המפחיתות רמת מלטונין''': חוסמי תעלות סידן כגון nifedipine,amlodipine ,verapamil ,diltiazem ,felodipine ,nisoldipine ,bepridil; חוסמי בטא כגון acebutolol ,atenolol ,bisoprolol ,carteolol ,metoprolol ,nadolol ,propranolol. | ||
תכשירים אחרים עליהם דווח שהם יכולים להפחית רמת מלטונין בדם הם fluoxetine, חלק מתכשירי NSAID כמו ibuprofen, קפאין, טבק ואלכוהול. | תכשירים אחרים עליהם דווח שהם יכולים להפחית רמת מלטונין בדם הם fluoxetine, חלק מתכשירי NSAID כמו ibuprofen, קפאין, טבק ואלכוהול. | ||
מלטונין יכול להפחית יעילותם של תכשירים להפחתת לחץ הדם כגון methoxamine ו-clonidine, וכן להפחית יעילותם של מדכאי מערכת החיסון כגון קורטיקו-סטרואידים. מלטונין עלול להגביר את סכנת הדימום בנטילת נוגדי קרישה כ-warfarin. | מלטונין יכול להפחית יעילותם של תכשירים להפחתת לחץ הדם כגון methoxamine ו-clonidine, וכן להפחית יעילותם של מדכאי מערכת החיסון כגון קורטיקו-סטרואידים. מלטונין עלול להגביר את סכנת הדימום בנטילת נוגדי קרישה כ-warfarin. | ||
| − | |||
| − | |||
| − | |||
==ראו גם== | ==ראו גם== | ||
* [[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | * [[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | ||
* [[מפגעים הורמונאליים|בדיקות מעבדה - מפגעים הורמונאליים]] | * [[מפגעים הורמונאליים|בדיקות מעבדה - מפגעים הורמונאליים]] | ||
| + | |||
| + | |||
| + | {{ייחוס בן עמי}} | ||
[[קטגוריה:בדיקות מעבדה - מפגעים הורמונאליים]] | [[קטגוריה:בדיקות מעבדה - מפגעים הורמונאליים]] | ||
[[קטגוריה:בדיקות מעבדה: אנדוקרינולוגיה]] | [[קטגוריה:בדיקות מעבדה: אנדוקרינולוגיה]] | ||
גרסה אחרונה מ־03:05, 6 באוגוסט 2019
| מדריך בדיקות מעבדה | |
| מלטונין | |
|---|---|
| Melatonin | |
| מעבדה | אנדוקרינולוגיה בדם |
| תחום | פיקוח הורמונאלי על תהליכי השעון הביולוגי |
| טווח ערכים תקין | בשעות הצהריים: 5-10 פיקוגרם למ"ל; בשעות הלילה (חצות עד 0500 לפנות בוקר): מעל 75 פיקוגרם למ"ל |
| יוצר הערך | פרופ' בן עמי סלע |
מטרת הבדיקה
מדידת מלטונין בדם, ברוק או בשתן נדרשת לעתים להערכת מקרים של הפרעות שינה כרוניות, אך גם תופעות הנכרכות בשיבוש המחזור הביולוגי היומי (circadian rhythm). רמת מלטונין משמעותית בבירור שיבוש בציר היפותלמוס-היפופיזה-בלוטות המין. יש במקרים מסוימים דרישה למדידת רמת מלטונין בנשים עם הפרעה בוויסות ועיתוי הפרשת הורמוני הרבייה שלהם. כמו כן קביעת רמת מלטונין יכולה להידרש כחלק מברור של הפרעות במחזור החודשי.
בסיס פיזיולוגי
מלטונין שנוסחתו N-acetyl-5-methoxytryptamine, מכונה "הורמון החושך" והוא מופרש מבלוטת האצטרובל (pineal gland) במוח, ותפקידו בעיקר לווסת הורמונים אחרים ולשמור על ה-circadian rhythm או השעון הביולוגי הקובע הין השאר את מחזורי שינה וערות. מלטונין גם מסייע לפקח ולווסת את הפרשת הורמוני הרבייה באישה. יש למלטונין תפקיד בעיתוי התחלת הווסת, אורך המחזורים החודשיים, וחידלון הווסת בגיל המעבר.
תאי בלוטת האצטרובל מסבים את חומצת האמינו טריפטופאן להורמונים סרוטונין ומלטונין, כאשר ייצורו והפרשתו של האחרון, מבוקרת על ידי השעון הביולוגי של היממה הממוקם בגרעינים העל-כיאזמטיים שמעל צומת עצבי הראייה, בהיפּוֹתלמוּס. הפרשת מלטונין תלויה במחזוריות של אור וחושך, כאשר נתונים אלה מגיעים אל הגרעינים ההיפותלמיים מרשתית העין, ומועברים בהמשך למערכת הרטיקולארית במוח, וגם לגנגליון הידוע כ-SCG או superior cervical ganglion. מן הגנגליון נמשכים סיבים של תאי עצב סימפתטיים לבלוטת האצטרובל. תאי העצב האחרונים מפרישים נור-אדרנלין לתוך האצטרובל, באופן שטריפטופאן הופך לסרוטונין, המותמר ל-N-acetylserotonin, וזה מותמר למלטונין.
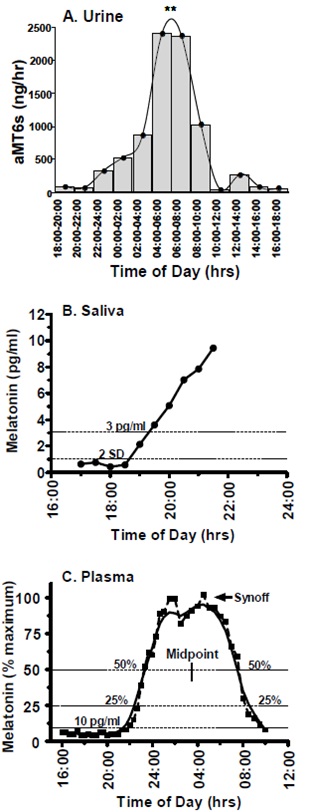
מטבע הדברים, רמת מלטונין בדם מגיעה לשיאה בשעות הלילה, ולמעשה בין חצות לשעות 3-4 לפנות בוקר, שהן שעות השינה וקליטת האור הנמוכה ביותר. באיורים לדוגמה, הפרשת מלטונין מגיעה דווקא לשיאה בשעות היום. לקראת הבוקר יורדת רמת מלטונין בדם לרמה נמוכה ביותר. סדרת התרשימים למטה מדגימה שבשיאה בשעות הלילה המאוחרות מגיעה רמת מלטונין בדם לריכוז של כ-100 פיקוגרם למ"ל, אם כי בשעות האור רמה זו דועכת עד כדי כ-5 פיקוגרם למ"ל. שיא רמת מלטונין בשתן הוא בשעות 6-8 בבוקר, כצפוי מספר שעות לאחר שיאו של הורמון זה בדם.
חשיפה של אנשים לאור מלאכותי בעוצמה גבוהה בשעות הלילה מביאה לדיכוי של הפרשת מלטונין, אם כי כאשר אדם מוכנס בשעות היום לשהייה בחדר חשוך, אין הדבר גורם בהכרח להגברת הפרשת ההורמון הזה. נתון מעניין נוסף, שבתקופת החורף עם התארכות שעות החשיכה, כמות המלטונין המופרשת על פני היממה היא משמעותית גבוהה יותר מאשר בתקופת הקיץ. תרחישים אחדים כגון יעפת (jet lag), עבודה במשמרות ליליות, וראיה פגומה יכולים לגרום לשינויים במחזורי הפרשת מלטונין.
נמצא שביונקים עם דפוסי התרבות עונתית, כלומר עם תקופות של פריון מוגבר או נמוך, יש למלטונין השפעה לדיכוי הפרשת הורמוני המין, הגונדוטרופינים. בחורף, מלטונין מופרש יותר ובכך מדוכאת הפרשת הורמוני המין מבלוטת יותרת המוח, ההיפופיזה, מה שגורם לדעיכת הפעילות המינית. היפוכו של דבר בתקופת הקיץ. באוגרים בהם נכרתה בלוטת האצטרובל הפעילות המינית הפכה קבועה בשתי תקופות השנה הללו, אך עם הזרקת מלטונין הופסקה תופעה זו.
הנתונים בבני אדם מבחינת הקשר בין מלטונין והורמוני המין אינם ברורים כמו אלה ביונקים אחרים. בעוד שביונקים מתן מלטונין מדכא פעילות מינית, בגין דיכוי הפרשת LH-RH מההיפותלמוס, התוצאות באדם פחות ברורות. כאשר נבדקו ילדים משני המינים בהם נצפתה בגרות מינית מוקדמת, נמצאו בהם רמות מלטונין נמוכות, ולעומת זאת בנערים עם איחור בהתבגרות המינית נמצאו רמות מלטונין הגבוהות פי-3 מרמתו בקבוצת ביקורת תקינה.
המלטונין משמש כסמן פיזיולוגי של חשיכה במוח ובאיברי הגוף. בהתאם לכך, מלטונין פועל ישירות על המוח להשריית שינה, אך גם לבקרה על מחזוריות ביולוגית של גורמים שונים המשתנים בין היום והלילה, כמו מחזור השינה, לחץ הדם, טמפרטורת הגוף, רמות גלוקוזה בדם, הורמונים שונים והלחץ התוך-עיני. מלטונין נמצא גם במעיים ומשפיע במנגנונים אחרים מאלה שמשפיע מלטונין המופרש מבלוטת האצטרובל. למלטונין שני סוגי קולטנים ספציפיים, MT1 ו-MT2, המצומדים לחלבוני G, ומפעילים מנגנוני פעולה על ידי העלאת רמת cAMP בתאי היעד. זמן מחצית החיים של מלטונין בדם קצר יחסית (כ-40 דקות), והוא נעלם מהר כתגובה לחשיפה לאור חזק. בכבד מלטונין מתחמצן ועובר צימוד לשייר סולפאט על ידי האנזים CYP1A2, ואמנם מעל 80% מההורמון הזה מופרש בשתן כתוצר מטבוליזם הידוע כ-6sulphatoximelatonin. אכן, מעכבים של האנזים CYP1A2 דוגמת התכשיר נוגד הדיכאון fluvoxamine, מעלים באופן ניכר את רמת מלטונין בדם.
בלוטת האצטרובל (pineal) תוארה לראשונה לפני כ-2,500 שנה על ידי הרופא האלכסנדרוני הירופוליס, שהגדיר אותה כ"שוער המווסת את זרימת המחשבה אל חדרי המוח". במאה ה-3 לספירה היה זה הרופא הרומי גלניוס שציין שהמבנה האנטומי של האצטרובל שונה משאר חלקי המוח, והוא אף השווה את פעולתה לזו של בלוטות הלימפה. האצטרובל היא בלוטה יחידה הממוקמת באמצע המוח מצידו האחורי, בין שני חצאי המוח (הֶמיספרות) והיא מופיעה בגובה העיניים. לנשים בלוטת אצטרובל גדולה מזו של הגברים, ועם ההזדקנות היא הולכת ומצטמקת עד כי בגיל 70 שנה היא מגיעה לכדי עשירית מגודלה המרבי.
הפילוסוף הצרפתי רנה דקארט ייחס לבלוטה משמעות בהקשר הפסיכופיזי, וטען שבלוטה זו היא "מקום מושב הנפש". אך רק בתחילת המאה ה-20 היה זה היבנר שתרם להבנת חשיבות האצטרובל, לאחר שטיפל בילד עם שאת סרטנית בבלוטה שהגיע לבגרות מינית מוקדמת.
בשנת 1995 פרסמו Robinson ו-Reiter את הספר Melatonin בו הם ייחסו להורמון זה תפקידים ביולוגיים רבים. על פי שני אלה, מלטונין מווסת תהליכי הזדקנות, משפיע על מחזורי הרבייה, מגרה את בלוטת ההיפופיזה (יותרת המוח) ליצירת הורמון הגדילה (growth hormone), מווסת שינויים בפיגמנטציה של העור, וכמובן משפיע על מצבי ערות ושינה. בנוסף, מאמינים שני מחברי הספר שיש למלטונין פעילות נוגדת תהליכים סרטניים במספר מנגנונים: הגברת פעילות מערכת החיסון נגד תאי סרטן, היותו נוגד תהליכים מחמצנים כיוון שהורמון זה מסיס במים ובשומן ומתאפשרת חדירתו הקלה לרקמות רבות בגוף ויכולתו להגן על DNA מנזקי חמצון, היותו מקטין לכאורה את תהליך האנגיוגנזה (יצירת כלי דם חדשים המזינים גידולים סרטניים ומקלים על שליחת גרורות ברחבי הגוף).
הראשון שבודד ואפיין את המלטונין בשנת 1958 היה Aaron Lerner, והוא עשה זאת בהקשר הפיקנטי כמעט של פקטור הגורם להבהרת העור בדו-חיים. אך בתחום היותר רלבנטי של התפקיד הפיזיולוגי של מלטונין בבני אדם, ניתן להגדיר מספר תחומים בהם תיתכן חשיבות להורמון זה. מעבר לחשיבות מלטונין בתחום מצבי הרוח (mood) הקשורים למצבי "אור וחשיכה" "יום ולילה", יש המציינים את השפעתו על מערכת החיסון, פריון (שאפילו בא לביטוי בשיעור ההצלחה של הפריה חוץ-גופית), ובעיקר בתחום האונקולוגי.
בסקירה המקיפה שלה משנת 2005 ב-Journal of Biological Rhythms, מקדישה Josephine Arendt פרק משמעותי להשפעות האונקו-סטטיות או מעכבות הסרטן של מלטונין. הוצעו מנגנונים אחדים לאפשרות שמלטונין מדכא תאי סרטן, כולל זה של Hill שהדגים בתרבית תאים שמלטונין יכול להתערב בקישור של אסטרוגנים לקולטנים שלו מסוג MT1 על פני תאי סרטן השד, ואילו Sauer פרסם ב-Biochemical Pharmacology על כך שמלטונין מדכא קליטת חומצות שומן רב- בלתי-רוויות על ידי תאי סרטן בתרבית, ובכך מעכב שגשוג תאים אלה. יש מספר פרסומים של Lissoni ואנשיו על יעילות גבוהה יותר של טיפול כימותרפי משולב במלטונין, ויש ראיות לכך שכריתה ניתוחית של בלוטת האצטרובל, תוך גרימת שינויים במחזוריות היומית של חושך-אור, משפיעה על גידולן של שאתות סרטניות.
מלטונין וסוכרת
יש מספר ראיות מחקריות לכך שמלטונין הוא בעל תפקיד במטבוליזם של גלוקוזה. הזנת חולדות מזן הנוטה לסוכרת במלטונין היא בעלת השפעה המגנה עליהן מפני המחלה. בעקבות פרויקט הגנום האנושי, הצטברו נתונים שבעקבות שינויים בקולטן האנושי MT2 של מלטונין, שינויים הידועים כ-SNPs או Single nucleotide polymorphisms, הגורמים להפחתה פעילות קולטן זה, יש שיעור גבוה יותר של מקרי סוכרת type 2. באפריל 2013 התפרסם בכתב העת JAMA מחקר משני מרכזים רפואיים של אוניברסיטת הרווארד בבוסטון, בניהול האפידמיולוג Eric Rimm, שבחן את הקשר בין הפרשת מלטונין לבין התרחשות סוכרת type 2 בנשים. מחקר זה התבסס על מדגם מחקר בריאות האחיות (Nurses’ Health Study), כאשר מ-18,500 מתוכן נלקחו דגימות דם ושתן בתחילת המחקר בשנת 2000 בהיותן בבריאות מלאה, כאשר ב-370 מהן אובחנה עד שנת 2012 סוכרת type 2. מסקנות מחקר זה שמדד בשתן את היחס בין 6sulfatoxymelatonin לקראטינין, שהנשים במחקר זה עם רמות נגזרת המלטונין הגבוהה ביותר בשתן היו בסיכון הנמוך פי 2.17 ללקות בסוכרת זו בהשוואה לנשים הנסקרות עם רמת מלטונין הנמוכה ביותר. זהו נתון אפידמיולוגי מרשים וראוי למחקרי המשך בהקשר לסוכרת type 2, תחלואה ששיעוריה באוכלוסיה העולמית עולים באופן משמעותי בעשרות השנים האחרונות.
מלטונין והפרעות שינה
אך נראה שבתודעה הציבורית ואף בזו של החוקרים, הקשר המיידי של מלטונין הוא זה הקשור להפרעות שינה, אופי השינה, והשראת שינה. למלטונין יש ערך טיפולי למניעת הפרעות שינה שנגרמות בגלל "יעפת" (jet lag), אך מחקרים אחדים אישרו את יעילותו כי ייתכן שהוא יעיל גם כטיפול בנדודי שינה. המלטונין משמש בעיקר לטיפול בתסמונת פאזת השינה הדחויה, מה שידוע כ-DSPS או delayed sleep phase syndrome, שמקורה הוא שעון ביולוגי דחוי. בשנת 2008 אושרה על ידי ה-FDA לשימוש תרופת המרשם סירקדין (Circadin), מלטונין בשחרור מבוקר בישראל, באירופה ובארצות שונות בעולם, לטיפול בנדודי שינה. התרופה פותחה על ידי החברה הפרמצבטית הישראלית "נעורים" (Neurim Pharmaceuticals).
Circadin הוא תכשיר בשחרור מושהה של 2 מיליגרם מלטונין, שנוטלים לפני השינה וכך הוא מחקה את פרופיל השחרור הפיזיולוגי של מלטונין אנדוגני. הטיפול מומלץ לבני 55 שנה ומעלה הסובלים מנדודי שינה (insomnia) ראשונית הפוגעת באיכות השינה. מחקר מראה שסירקדין משפר לא רק את איכות השינה אלא גם את הערנות ביום המחרת, בלי שהוא פוגע בזיכרון, בכושר הקוגניטיבי או בתפקוד הפסיכו-מוטורי. יתרון אחר שלו בהיותו חומר לא ממכר, שהפסקת השימוש בו אינה גורמת לתסמיני גמילה.
למלטונין יוחסו במרוצת השנים תכונות ויתרונות שונים בתחום הרפואה, אם כי לא בכולם ברור המנגנון, והמשמעות הביולוגית והטיפולית, אם בכלל. כך לדוגמה היו דיווחים רבים על משמעותו של מלטונין כנוגד-חמצון, השפעתו על מערכת החיסון בהגברת ייצור ציטוקינים כמו IL-1 ו-IL-2, ויש אף מחקרים התומכים בפעילות להאטת תהליכי הזדקנות של מלטונין, אך הפעילות האחרונה הודגמה בעיקר במחקרים עם עכברים. מחקרים אחרים רומזים להשפעתו במצבי דיכאון עונתיים, או ליעילותו בטיפול בכאבי ראש ומיגרנות.
מחקרים בחיות אך גם בבני אדם הצביעו על השפעה של מלטונין להגנה בפני קרינה מייננת. נראה שיכולת מלטונין לקלוט רדיקלים חופשים קשורה להשפעה זו כנגד קרינה. יש אף מספר מחקרים המצביעים על מלטונין כמשפר מצבי טנטון (tinnitus).
אינטראקציות עם תרופות
תרופות המפחיתות רמת מלטונין: חוסמי תעלות סידן כגון nifedipine,amlodipine ,verapamil ,diltiazem ,felodipine ,nisoldipine ,bepridil; חוסמי בטא כגון acebutolol ,atenolol ,bisoprolol ,carteolol ,metoprolol ,nadolol ,propranolol.
תכשירים אחרים עליהם דווח שהם יכולים להפחית רמת מלטונין בדם הם fluoxetine, חלק מתכשירי NSAID כמו ibuprofen, קפאין, טבק ואלכוהול.
מלטונין יכול להפחית יעילותם של תכשירים להפחתת לחץ הדם כגון methoxamine ו-clonidine, וכן להפחית יעילותם של מדכאי מערכת החיסון כגון קורטיקו-סטרואידים. מלטונין עלול להגביר את סכנת הדימום בנטילת נוגדי קרישה כ-warfarin.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק