הבדלים בין גרסאות בדף "Chromogenic factor X"
(יצירת דף עם התוכן "{{בדיקת מעבדה |שם עברי= |שם לועזי= |קיצור= |תמונה= |כיתוב תמונה= |מעבדה= |תחום= |יחידות מדידה= |ט...") |
|||
| שורה 93: | שורה 93: | ||
יש לפסול דגימות קרושות, מאוד המוליטיות או ליפמיות, אם כי ניתן לקבל דגימות עם המוליזה או ליפמיה מתונות. הדגימות יציבות בהקפאה למשך 14 יום, ואין לקבל כלל דגימות בטמפרטורת החדר או דגימות מקוררות מעבר ל-3 שעות לאחר לקיחת הדם. כמו כן יש לפסות דגימות מזוהמות בהפארין. | יש לפסול דגימות קרושות, מאוד המוליטיות או ליפמיות, אם כי ניתן לקבל דגימות עם המוליזה או ליפמיה מתונות. הדגימות יציבות בהקפאה למשך 14 יום, ואין לקבל כלל דגימות בטמפרטורת החדר או דגימות מקוררות מעבר ל-3 שעות לאחר לקיחת הדם. כמו כן יש לפסות דגימות מזוהמות בהפארין. | ||
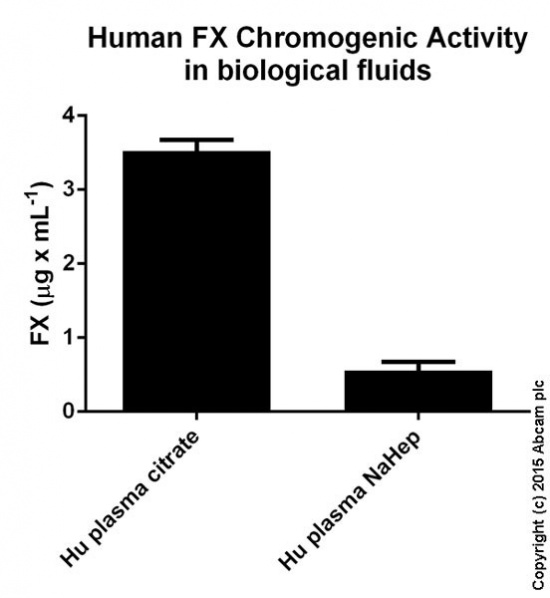
| − | השוואה בין | + | [[קובץ:Factor10.jpg|ממוזער|מרכז|550 פיקסלים|השוואה בין פעילות CFX כאשר היא נמדדת במבחנת סודיום ציטראט, לעומת מבחנת סודיום הפארין.{{ש}}(נלקח מפרסום של חברת Abcam משנת 2015).]] |
| − | (נלקח מפרסום של חברת Abcam משנת 2015). | ||
גרסה מ־21:56, 11 בדצמבר 2016
| מדריך בדיקות מעבדה | |
| ' | |
|---|---|
| ' | |
| יוצר הערך | פרופ' בן-עמי סלע |
Chromogenic Factor X
כינויים נוספים: CFX, Chromogenic Factor 10 . מעבדה: המטולוגיה בדם. תחום: ניטור של טיפול נוגד-קרישה, בעיקר במטופלים שבנסיוב שלהם יש אנטי-קואגולנטים, והם מטופלים עם argatroban. טווח ערכים תקין: 66-148%. יוצר הערך: פרופ' בן-עמי סלע. מטרת הבדיקה: ניטור של טיפול נוגד קרישה פּומי, בעיקר במטופלים שהפלזמה שלהם כוללת lupus anticoagulants או במטופלים המקבלים מעכבי תרומבין ישירים כמו Argatroban, hirudin, dabigatran או bivalirudin. בדיקת chromogenic factor X:
בדיקה זו היא מדידה אנזימטית של פקטור X, אחד מגורמי הקרישה שרמתו פוחתת בשעת טיפול בקומאדין. בדיקה זו אינה מושפעת על ידי LA. בהגדרה, לפלזמה נורמאלית יש 100% פעילות של פקטור X, ובכל הנבדקים הנורמאליים יש למצוא ערכי פעילות שמעל 70%. מעבדת Allina השייכת לקונצרן Abbott Northwestrn קובעת לדוגמה ש-INR של 2.5 תואם ערך CFX של בערך 28%, וכן ש-INR בתחום של 2.0-3.0 תואם CFX של 20-40%, מה שתואם את נתוני הספרות שהתפרסמו.
המתאם של CFX ו-INR בנבדקים ללא לופוס אנטיקואגולנט: ______________________________________________________________
CFX (ב-%): 60 50 40 30 20 15 10
INR (יח' מוחלטות) 1.6 1.8 2.0 2.4 3.3 4.1 5.7 _________________________________________________________________
מטופלים עם טיפול כרוני בקומאדין יכולים לעבור תקופתית בדיקת CFX ועל פי תוצאותיה ניתן להעלות או לפחית את המינון של קומאדין, שימוש בתחום של 20-40%, המקביל כאמור לתוצאות INR של 2.0-3.0. אם מתקבלת תוצאת CFX נמוכה מהתחום האמור, יש את מינון קומאדין , ואילו אם תוצאות CFX מתקבלות גבוהות מ-20-40%, יש להעלות את מינון קומאדין. יש לקחת בחשבון שמחלת כבד כרונית או חסר בוויטמין K יכולים להפחית את רמות CFX המתקבלות בבדיקה (Robert וחב' ב-Thromb Haemost משנת 1998).
מידע קליני:
ההשפעה נוגדת הקרישה של אנטגוניסטים של ויטמין K (כגון קומאדין) מתֻווכת על ידי הפחתת הפעילות בפלזמה של פרו-קואגולנטים כגורמי הקרישה II (פרותרומבין) ו-,X התלויים בוויטמין K לפעילותם. עוצמת המינון של טיפול בנוגדי קרישה עם אנטגוניסטים אלה, חייבים להיות מנוטרים ומותאמים לטווח תרפויטי צר יחסית, שכן מינון יתר שלהם מגביר את סיכוני הדימום, בעוד שמינון חסר שלהם לא ימנע אירועי פקקת בעתיד. ניטור זה מושג על ידי מערכת היחס של PT/INR.
Lupus anticoagulants(להלן LAC):
לופוס אנטי-קואגולנט הוא מרכיב אחד בתסמונת הנוגדנים האנטי-פוספוליפידים, ויכול להימצא במטופלים עם SLE, ממאירות, הדבקה ב-HIV, מחלות נוספות ואף באנשים בריאים ללא כל תסמיני מחלה. הנוכחות של LA יכולה לחשוף מטופלים לפקקת ורידית או עורקית, וכתוצאה מכך לטיפול כרוני בקומאדין.
LCA הם נוגדנים-עצמיים המפריעים במבדקי קרישה התלויים בפוספולידים, בעיקר על ידי הארכת משך ה-APTT אוactivated partial thromboplastin time. כידוע LAC יכול להיות קשור עם המפגע הפּרוֹ-תרומבוטי הידוע כתסמונת אנטי-פוספוליפידית, ועלול לגרום להארכת משך PT הבסיסי, ולשבש את תוצאת INR המשמש לניטור מידת היעילות של תכשירים נוגדי-קרישה פומיים. ההארכה של PT נצפית בעיקר עם גורמי רקמה ריקומביננטיים אנושיים thromboplastins)), עם ISI או International sensitivity indexes נמוך כמו Innovin (עם ISI=1.0). כאמור מדידת CFX אינה מושפעת על ידי LAC כיוון שה-endpoint של הבדיקה אינו זמן קרישה התלוי בפוספוליפידים.
במספר מטופלים עם LAC ה-INR עלול כאמור להתקבל מוגבר באופן כזוב, וכתוצאה מכך לחשוף את המטופל לתת-טיפול בקומאדין. נתונים מניסויים קליניים אחדים, מראים שבערך 10-20% מהמטופלים עם LA כרוני, אמנם מתקבלות תוצאות כּזובות מוגברות של INR (על פי Rosborough ו-Shepherd ב-Phamacotherapy משנת 2004).
Argatroban הוא מעכב ישיר של תרומבין הנלקח באופן לא-פומי שאושר לשימוש במקרים של HIT או heparin-induced thrombocytopenia טיפול ב-Argatroban מאריך את משך PT מה שהופך את בדיקת INR לבלתי מדויקת לניטור השפעת קומאדין במעבר מטיפול ב-Argatroban לטיפול בנוגד קרישה פומי. בדיקת CFX עשויה להוות תחליף למדידת INR לניטור והתאמת מינון קומאדין במעבר מנוגד הקרישה הלא-פומי לטיפול בנוגד הקרישה הפומי.
Argatroban הוא תכשיר מעכב תרומבין סינתטי המאושר למטרת פרופילקסיה או טיפול בפקקת במטופלים עם heparin-induced thrombocytopenia או HIT שהוא מפגע פרותרומבוטי המתֻווך על ידי נוגדן, או במטופלים עם HIT & thrombosis syndrome או HITTS (מסמך של GlaxoSmithKlein משנת 2003). נמצא ש-argatroban מאריך משמעותית את PT כמו גם את aPTT (על פי Walenga וחב' ב-Sem Thromb Hemost משנת 1999). מסיבות לא ברורות, argatroban משפיע על PT באופן דיספרופורציונאלי יותר מאשר מעכבי תרומבין ישירים אחרים כמו hirudin או bivalirudin (על פי Gosslin וחב' ב-Am J Clin Pathol משנת 2004). בנוסף, הנוכחות של argatroban מעלה באופן סינרגיסטי את תוצאות PT באלה המטופלים בקומאדין, מה שמסבך במקצת את המעבר מטיפול לקומאדין במטופלים ב-argatroban בגלל ההתייחסות לממצאי INR הבלתי מהימנים.
פקטור X הוא זימוגן בפלזמה של serine protease המשחק תפקיד ב-cascade הקרישה. פקטור X מנוקה מהפלזמה כחלבון בעל 2 שרשרות, האחת כבדה בעלת משקל מולקולארי של 45 אלף דלטון, והשנייה שרשרת קלה בעלת משקל מולקולארי של 17 אלף דלטון. השרשרת הכבדה של פקטור X מבוקעת במהלך הקרישה על ידי מספר פרוטאזות שונות, כולל ה-intrinsic Xase complex, האנזים המשפעל את פקטור X מ-Russell's viper venom או RVV, וכן על ידי טריפסין כמו גם על ידי ה-extrinsic pathway (הכולל את tissue factor /פקטור VIIa) ליצירת האנזים הפעיל פקטור Xa, המשמש כמשפעל של פרותרומבין ומהווה מרכיב מרכזי בנקודת המפגש בין המסלולים הפנימי והחיצוני של מהלך הקרישה. אינטרפרטציה: פעילות של CFX של בערך 20-35% תואמת את הטווח התרפויטי הרגיל של קומאדין שבא לביטוי ב-INR של 2.0-3.0. מטופלים בהם מוצאים lupus anticoagulants הכרוכים עם פקקת ורידים נשנית, מקבלים לעתים קרובות טיפול אנטי-קואגולנטי פומי ארוך טווח, אך קיימת אי תמימות-דעים לגבי המינון והעוצמה של טיפול זה על מנת שיהיה אופטימאלי. מספר איגודים רפואיים ממליצים שה-INR אליו צריכים להתכוונן מטופלים אלה צריך להיות מעל 3.0, ואילו אחרים ממליצים על INR בתחום של 2.0-3.0 כיעד ראוי למניעת אירועי פקקת חוזרים. נושא אחד התורם לאי ההסכמה לגבי תחום INR אופטימאלי בקבוצת מטופלים זו נובע מהראיות העדכניות המצביעות על כך ש-lupus anticoagulants יכולים לגרום להארכה בעלת אופי וריאבילי של PT, מה שעלול לגרום לתוצאה מוגברת כזובה (falsely elevated) של ה-INR, שאינה משקפת במדויק את הרמה האמיתית של האנטי-קואגולציה. Moll ו-Ortel במחקרם משנת 1997 ב-Ann Intern Med, היו הראשונים שדווחו על השפעת LAC על תוצאות INR המתקבלות תוך שימוש בתרומבופלסטינים שונים, כאשר בדרך כלל מתקבלת תוצאת INR מוגברת כזובה. במחקרם, זמני פרותרומבין (PT) נקבעו על ידי שימוש במספר תרומבופלסטינים, וערכי INR נקבעו במטופלים בקומאדין. רמות factor II, רמות CFX וזמני פרותרומבין-פרוקונברטין נקבעו במטופלים בקומאדין. התוצאות הצביעו על כך שבמטופלים עם lupus anticoagulants שלא טופלו בקומאדין, ערכי PT היו לעתים קרובות מוארכים ונמצאו משתנים מהותית עם תרומבופלסטינים שונים, שכן האחרונים מראים רגישות שונה לנוכחות של LA. לעומת זאת, במטופלים בקומאדין, ערכי INR שהתקבלו תוך שימוש בתרומבופלסטינים שונים הראו שונות רבה, ולרוב נתנו הערכת-יתר של מידת האנטי-קואגולציה.
השוואה בין chromogenic factor X לבין INR לתרפיה נוגדת קרישה:
McGlasson במחקר משנת 2008 ב-Blood Coagulation & Fibrinolysis השווה את בדיקות INR ו-CFX במטופלים עם תכשירים נוגדי-קרישה פומיים תוך שימוש בשיטת DiaPharma CFX על אנלייזר קרישה מסוג STA-R. שני מדדים אלה הושוו לצורך קביעת תחומי טיפול נורמאליים, תת-תרפויטיים, תרפויטיים ועל-תרפויטיים במטופלים אלה, שקובצו ב-3 קבוצות" אלה עם INR נמוך מ-2.0, או אלה עם INR שבין 2.0-3.0 וכן אלה עם INR גבוה מ-3.0. בניסוי השתתפו 390 מטופלים בנוגדי קרישה פומיים, בהם נמצא תחום של INR שבין 0.92-12.76, ותחום CFX של 9-132%. נמצא ש-CFX היה במתאם הפוך ל-INR עם R של 0.964, במשמעות סטטיסטית גבוהה, p<0.0001. התוצאות על בסיס 3 הקבוצות הללו כדלקמן: ב-INR נורמאלי (30 נבדקים) תחום CFX היה 72-131%, רמה ממוצעת של CFX הייתה 96%; ב-INR נמוך מ-2.0 (נכללו 70 נבדקים) ונמצא תחום CFX של 32-132% ורמה ממוצעת של 53%, באלה עם INR של 2.0-3.0 (נכללו 135 נבדקים) תחום CFX היה 18-48% עם רמה ממוצעת של 28%; ב-104 נבדקים עם INR שמעל 3.0 תחום CFX נקבע כ-9-46% עם רמה ממוצעת של 21%. כללית, יש יחס רציפרוקאלי בין INR ל-CFX, באופן בו כאשר האחד עולה, האחר יורד.
ברמת CFX של 35.5% הרגישות והספציפיות של מבדק זה היו זהים, 91.7% ו-91.9%, בהתאמה, כדי להבדיל בינו לבין INR של לפחות 2.0. השטח מתחת לעקומה (AUC) תוך שימוש ב-INR היה 0.984 (עם p<0.001). במדגם זה שנבחר באקראי של מטופלים בנוגדי קרישה ואנשים בריאים ברמות שונות של אנטי-קואגולציה, CFX תאם היטב עם INR כפי שנקבע על ידי R=0.964. נתונים אלה מרמזים ש-CFX עשוי להיות כלי שימושי לניטור טיפול אנטי-קואגולציה פומית, באוכלוסיות מטופלים בהם ערפלנים (confounders) של INR עלולים להימצא.
ניטור הטיפול בקומאדין במטופלים חיוביים ללופוס אנטי-קואגולנט:
1. אם מטופל חיובי ל-LA הנמצא בטיפול במינון קבוע של קומאדין, וה-INR שלו נשמר בין 2.0-3.0, כאשר בדיקה אקראית של CFX מתקבלת בין 20-40%, ההתייחסות אל תוצאת ה-INR צריכה להיות כאל תוצאה מדויקת וניתן להמשיך לנטר את המטופל בבדיקת INR בלבד. 2. אם מטופל חיובי ל-LA הנמצא בטיפול יציב של קומאדין, נמצא בתחום INR של 2.0-3.0 אך עם ערכי CFX גבוהים מ-40%, יש לבדוק את רמת CFX שלו בתכיפות גדולה יותר. יש אפשרות שמטופל עם רמה גבוהה כזובה של INR, מראה תוצאות CFX בתחום התרפויטי של 20-40%, ובמטופל זה מומלץ לבצע מספר מדידות סדרתיות של INR ו-CFX בו זמנית, כדי לקבוע את היחס בין 2 מדדים אלה במטופל הספציפי הזה. ייתכן שבחולה זה ש-INR של 4.5 יהיה תואם ערך CFX של 30%.
השימוש ב-CFX לצורך התייחסות לתוצאות INR במטופלים עם קומאדין:
בשנת 2009 סיכם Sanfelippo ב-Clin Med Res מקרה אופייני של מטופלת בקומאדין בה התקבלו תוצאות מוגברות באופן בלתי צפוי של INR, כאשר מדידה חוזרת של ה-INR שלה ב-2 מעבדות נתנה תוצאות סותרות. במקרה זה נקטו במדידת CFX לקבוע מהו ערך INR הנכון. למטופלת נמצאו תוצאות מעבדה המתאימות למקרה של dysfibrinogenemia, מה שמנע שימוש במערכת מדידה פוטו-אופטית. מקרה זה מתאים למדידת CFX כיוון שה-INR אינו יכול להיקבע במדויק כתוצאה מהפרעה ל-endpoint של פיברין במבחן INR.
המדובר במטופלת בת 79 שנה עם רקע של פרפור פרוזדורים שהייתה מטופלת בקומאדין משך 7 חודשים עם תוצאות INR בתחום התרפויטי, ללא סיבוכים. באחת הבדיקות התקבלה אצלה תוצאת INR חריגה של 11.0, והערכה של מעבדת הקרישה בהקשר של תרופות אחרות שנטלה, מצב בריאותה, הדיאטה ופעילותה הגופנית לא הניבו פתרון סביר לתוצאת ה-INR החריגה המתוארת. כאשר נמדד ערך INR שלה ב-2 מעבדות שונות, התקבלו תוצאות סותרות.
זמן פרותרומבין (PT) נקבע בשיטה הסטנדרטית במכשיר Sysmex 1500, עם ריאגנט Innovin של Dade, במעבדות א' וג', כאשר מעבדה ב' השתמשה במכשיר ACL model 7000. בדיקת CFX התבצעה במכשיר Dade BSC (על פי Sanfelippo וחב' ב-World Med J משנת 2000). תוצאות INR של נבדקת זו במעבדה א' בזמנים שונים היו בתחום שבין 1.6-2.4; תוצאות INR שלה במעבדה ב' ב- 5 מדידות בזמנים שונים התקבלו תמיד כ-INR שווה ל-11.0; תוצאות INR שלה במעבדה ג' התקבלו בתחום שבין 1.2-2.4. ערך PT שלה נקבע כ-21.4 שניות (תחום נורמה: 16.4-20.7 שניות); זמן reptilase שלה נקבע כ-16.1 שניות (תחום נורמה: 15.5-19. שניות); פעילות פיברינוגן שלה נמצא ברמה של 642 מיליגרם/ד"ל (תחום נורמה: 174-442 מיליגרם/ד"ל); רמת פיברינוגן נקבעה כ-50 מיליגרם/ד"ל (תחום נורמה: 180-310 מיליגרם/ד"ל).
כאשר הוחלט לבצע מדידות CFX במטופלת זו, התקבל ערך של 79% שתאם את ערך INR של 1.3 שהתקבל במעבדה ג'. אם לעומת זאת, הערך של INR=11.0 שהתקבל בעקביות ממעבדה ב' היה נכון, היינו מצפים לתוצאת CFX הנמוכה מ-10%. המשך הבירורים רמז שמטופלת זו היא בעלת מצב בלתי נורמאלי של פיברינוגן, או dysfibrinogenemia. מצב זה נרמז על ידי ערך PT שהיה מוארך באופן קל, אך בפירוש על ידי רמת פיברינוגן נמוכה משמעותית. ידוע שמספר צורות של dysfibrinogenemia עלולות להתבטא בנטייה לדימומים, אם כי גם בנטייה הפוכה ליצירת פקקת (Hayes ב-Arch Pathol Lab משנת 2002). יחד עם זאת, רוב הדיס-פיברינוגנמיות הן א-תסמיניות כפי שהיה עם המטופלת במקרה זה.
הקושי בגילוי קריש דם על ידי מספר מכשירים דווח במספר מקרים של dysfibrinogenemia. בעיה זו מתעוררת עם מכשור המתבסס באופן בלעדי על endpoint פוטו-אופטי. פיברינוגן Longmont צורת דיס-פיברינוגנמיה הגורמת להחמצת endpoints של פיברין במבחני קרישה המתבצעים עם מכשור מערכות גילוי פוטו-אופּטיוּת (Lefkowitz וחב' ב-Am J Hematol משנת 2000). במקרה שלפנינו היה כנראה פיברינוגן Longmont, והמכשור בעבדה ב' בה התקבלו תוצאות INR של 11.0, התבסס על גילוי פוטו-אופטי. נראה שדגמים שונים של מכשור מעבדה הם פחות אידיאליים לגילוי endpoint של פיברין, כאשר קיים פגם בשחרור של הפיברינו-פפטיד או בפּילמור של מונומרים של פיברין שעלול להתרחש במקרי דיס-פיברינוגנמיה.
מדידות של פיברינוגן, PT ו-reptilase time במטופלת שלפנינו, התבצעו במכשיר Sysmex 1500 המסוגל לגלות את ה-endpoint של פיברין במדידות אלו, ובכך להסביר מדוע ערך PT שלה היה מוגבר באופן קל, כאשר ערכי פיברינוגן וזמן reptilase נמצאו בתחומי הנורמה שלהם. ממצאים אלה נמצאו במקרים של נבדקים עם פיברינוגן Longmont, ויש לציין שכאשר מדידות PT ו-reptilase time התבצעו במכשור ACL 3000, התגלו לגבי 2 מדדים אלה ערכים מוגברים משמעותית. למרבה המזל, מקרים של דיס-פיברינוגנמיה אינם מאוד שכיחים, אך כאשר אנו פוגשים בהם הם גורמים לתוצאות מוגברות כזובות של INR במטופלים עם קומאדין. במקרים אלה מדידת CFX יעילה בניטור מטופלים אלה ובקביעת התקפות של תוצאת INR.
השימוש במבדק CFX לנבא תוצאות INR במטופלים מאושפזים העוברים מטיפול ב-Argatroban לקומאדין:
במחקר פרוספקטיבי-תצפיתי של Arpino וחב' ב-Pharmacotherapy משנת 2005, השתתפו 62 מאושפזים עם אינדיקציות לטיפול נוגד קרישה בהם נבדקו ערכי CFX לצורך הסבתם מטיפול ב-Argatroban לטיפול בקומאדין. כאשר ערכי CFX היו משביעי-רצון, הופסק הטיפול ב-argatroban במעבר לקומאדין תוך שימוש במדד INR. על מנת לקבוע את היכולת של קביעת רמת FCX לנבא את ערך INR המשוחרר מהשפעת argatroban, חושבו הרגישות והספציפיות של מבדק CFX עם סף ייחוס (cutoff) של 45% או למטה מכך לגבי רמת CFX, כאשר רמות CFX שמעל 45% תואמות ל-INR הגבוה מ-2.0. נעשה שימוש בעקומת ROC-receiver operating characteristic, לגבי ערכי סף שונים של CFX. מתוך 162 מטופלים שנסקרו, ל-62 היו נתונים המתאימים לקריטריונים לאנליזה במחקר זה.
בממוצע קיבלו 62 הנבדקים 6 טיפולי קומאדין לפני התחלת מדידת CFX, ובממוצע חלפו 9 שעות עד לקבלת הממצאים המאשרים מרגע מדידת CFX. השימוש במדד CFX ברמות של 45% או למטה מזה לנבא רמת INR מעל 2.0 ללא השפעת argatroban היה בעל רגישות של 93%, ובעל ספציפיות של 78%, ודרגת דיוק של 89%. השטח מתחת AOC נקבע כ-0.91.
עיקרון המדידה של CFX:
העֶרכּה למדידת chromogenic Human factor X activity, מודדת את השפעול של zymogen factor X לפקטור Xa על ידי Russell Viper Venom. הפעילות האמידוליטית של פקטור Xa ניתנת לכימות על יד שימוש במצע ספציפי מאוד של פקטור Xa המשחרר צבע צהוב של הכרומופור pNA או paranitroaniline. השינוי בבליעה של pNA באורך גל 405 ננומטר פרופורציוני באופן ישיר לפעילות פקטור Xa. פעילות גבוהה של פקטור X היא בתחום שבין 0.125-8 מיקרוגרם/מ"ל, ואילו פעילות נמוכה שלו היא בתחום שבין 0.0156-1 מיקרוגרם/מ"ל. הוראות לביצוע הבדיקה: דגימת הדם צריכה להילקח במבחנת סודיום ציטראט (פקק בצבע תכלת), כאשר הפלזמה הנשלחת למעבדה צריכה להיות דלה בטסיות-דם. לאחר הסרכוז הראשון והפרדת הפלזמה מתאי הדם, יש צורך להעביר את הפלזמה למבחנת פוליפרופילן ולסרכז פעם שנייה על מנת להמעיט בזיהום של טסיות דם העלולות להשפיע על תוצאת הבדיקה. לאחר הסרכוז יש להקפיא מיד את הפלזמה דלת-הטסיות ורצוי במקפיא בטמפרטורה של מינוס 40 מעלות ומטה, במידת האפשר. יש לפסול דגימות קרושות, מאוד המוליטיות או ליפמיות, אם כי ניתן לקבל דגימות עם המוליזה או ליפמיה מתונות. הדגימות יציבות בהקפאה למשך 14 יום, ואין לקבל כלל דגימות בטמפרטורת החדר או דגימות מקוררות מעבר ל-3 שעות לאחר לקיחת הדם. כמו כן יש לפסות דגימות מזוהמות בהפארין.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק