הבדלים בין גרסאות בדף "Kidney injury molecule-1"
| שורה 32: | שורה 32: | ||
תהליך ה- dedifferntiation הוא ביטוי מאוד מוקדם של תגובת תאי האפיתל לפגיעה (Bonventre וחב' ב- J Am Soc Nephrol משנת 2003). הגליקופרוטאין KIM-1 מבוטא גם בלימפוציטים אם כי ברמות נמוכות בהרבה, ולכן קרוי גם T-cell immunoglobulin mucin (TIM)-1. דווח גם ש-KIM-1 מבוטא גם בשבלול האוזן (cochlea) בתגובה לנזק הנגרם מטיפול בציספלטין (Mukherjea וחב' ב-Neuroscience משנת 2006). משפחת KIM/TIM מורכבת מ-8 חברים בעכברים, ששה בחולדות ו-3 באדם (Kuchroo וחב' ב-Adv Immunol משנת 2006). על ידי שימוש באנליזות סטנדרטיות כגון western blot או northern blot כמו גם אימונו-ציטוכימיה, הגן Kim-1 או ביטויו, אינם ניתנים לגילוי בכליה הנורמאלית. לאחר נזק כלייתי מופיע במהירות KIM-1 mRNA וחלה עלייה ניכרת ברמת החלבון KIM-1 הממוקם בריכוזים גבוהים בממברנה האפיקלית של האבוביות הקריבניות באזור בו האבוביות נפגעו באופן הניכר ביותר. במקרה של השרייה ניסויית של איסכמיה במכרסמים, ביטויו של Kim-1 הוא בעיקר בקטע S3 של האבובית הקריבנית. בבני-אדם, איסכמיה או נזק טוקסי הגורם לפגיעה כלייתית חריפה (AKI), ביטויו של KIM-1 הוא בשלושת הקטעים של האבובית הקריבנית. | תהליך ה- dedifferntiation הוא ביטוי מאוד מוקדם של תגובת תאי האפיתל לפגיעה (Bonventre וחב' ב- J Am Soc Nephrol משנת 2003). הגליקופרוטאין KIM-1 מבוטא גם בלימפוציטים אם כי ברמות נמוכות בהרבה, ולכן קרוי גם T-cell immunoglobulin mucin (TIM)-1. דווח גם ש-KIM-1 מבוטא גם בשבלול האוזן (cochlea) בתגובה לנזק הנגרם מטיפול בציספלטין (Mukherjea וחב' ב-Neuroscience משנת 2006). משפחת KIM/TIM מורכבת מ-8 חברים בעכברים, ששה בחולדות ו-3 באדם (Kuchroo וחב' ב-Adv Immunol משנת 2006). על ידי שימוש באנליזות סטנדרטיות כגון western blot או northern blot כמו גם אימונו-ציטוכימיה, הגן Kim-1 או ביטויו, אינם ניתנים לגילוי בכליה הנורמאלית. לאחר נזק כלייתי מופיע במהירות KIM-1 mRNA וחלה עלייה ניכרת ברמת החלבון KIM-1 הממוקם בריכוזים גבוהים בממברנה האפיקלית של האבוביות הקריבניות באזור בו האבוביות נפגעו באופן הניכר ביותר. במקרה של השרייה ניסויית של איסכמיה במכרסמים, ביטויו של Kim-1 הוא בעיקר בקטע S3 של האבובית הקריבנית. בבני-אדם, איסכמיה או נזק טוקסי הגורם לפגיעה כלייתית חריפה (AKI), ביטויו של KIM-1 הוא בשלושת הקטעים של האבובית הקריבנית. | ||
| + | |||
| + | המבנה של חלבון זה הביא את Bonventre ואנשיו למחשבה שיש לו תכונות של מולקולת ספיחה (adhesion) כפי שפרסמו Bailly וחב' ב-J Biol Chem משנת 2002. לאחר מכן מצאו Han וחב' (J Am Soc Nephrol משנת 2005) ש-KIM-1 מבוטא גם בריכוזים גבוהים במטופלים עם renal cell carcinoma מסוג תאי Clear, שגם בהם הנזק כרוך בדה-דיפרנציאציה של תאים האבובית הקריבנית. | ||
| + | |||
| + | כעת מתחילים להעריך את תפקודו של KIM-1 בכליה. חלבון זה מעניק לתאי האפיתל את היכולת לזהות ולבלוע בתהליך של פגוציטוזה תאים מתים המופיעים לאחר טראומה כלייתית, אשר גורמים לחסימה של נהור (lumen) האבוביות, מהמאפיינים של AKI. כמו כן, KIM-1 הוא קולטן של phosphatidylserine המזהה תאים אפופטוטים ומכוון אותם לליזוזומים. בנוסף, KIM-1 משמש קולטן לליפופרוטאינים מחומצנים ולכן הוא מתאים לזיהוי של איתותי "השמד אותי" של תאים אפופטוטים. לנוכח סגולות אלו נראה ש-KIM-1 ייחודי בהיותו הקולטן הראשון הלא-מילואידי של phosphatidylserine המתמיר תאי אפיתל לתאים עם פנוטיפ פגוציטי (Ichimura וחב' ב-J Clin Invest משנת 2008). בנוסף לסיוע שלו לפינוי של פסולת אפופטוטית מהנהור האבובי, KIM-1 עשוי לשחק תפקיד בהגבלת התגובה האוטו-אימונית לנזק כלייתי, כיוון שידוע במערכות רבות שפגוציטוזה של גופים אפופטוטים הוא מנגנון המגביל את התגובה הדלקתית. עם זאת, תגובת ההגנה האקוטית, אינה אמורה בהכרח להיות מתורגמת להשפעות הכרוניות של ביטוי KIM-1, כיוון שמטופלים רבים עם אי-ספיקה כלייתית כרונית, מבטאים את KIM-1 באבוביות הקריבניות שלהם (Vaidya וחב' ב-Clin Trans Sci משנת 2008, ו- van Timmeren ב-J Pathol משנת 2007). | ||
גרסה מ־10:56, 10 בינואר 2017
| מדריך בדיקות מעבדה | |
| Kidney Injury Molecule 1 | |
|---|---|
| שמות אחרים | TIM-1 או T cell immunoglobulin & mucin domain 1 , וכן Hepatitis A virus cellular receptor 1 (HAVcr-1) , ו-KIM-1, כמו גם CD365. |
| מעבדה | כימיה בשתן |
| תחום | נזק כלייתי כרוני וחריף |
| טווח ערכים תקין | פחות מ-1 ננוגרם/מ"ל |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
רמות מוגברות בשתן של KIM-1, עשויות לסיוע באבחון נזק כלייתי בעיקר לאבוביות הקריבניות (פרוקסימליות). בדיקה זו יכולה לתת הערכה פרוגנוסטית מוקדמת לגבי מטופלים עם אי-ספיקת כליות חריפה (להלן AKI), ויכולה לסייע לקלינאי לנקוט צעדים מוקדמים להאטה של ההתדרדרות הכלייתית לאחר AKI.
המבנה של KIM-1
מולקולת KIM-1 מכילה 339 חומצות אמינו, כאשר הקצה ה-N טרמינאלי שלה הוא הקצה המשתרבב מפני התא החוצה, וחלק חיצוני זה מורכב 272 חומצות אמינו המכילים את המקטע דמוי-אימונוגלובולין וכן את מקטע ה-mucin. המקטע החיצוני (ectodomain) יכול להיות מופרש לשתן במצבי פגיעה איסכמית וניתן לגילוי בעזרת נוגדנים ספציפיים. מכאן ששיטות גילוי אימונולוגיות הן השיטות המקובלות לגילוי ולכימות שלו בשגרת המעבדה הקלינית.
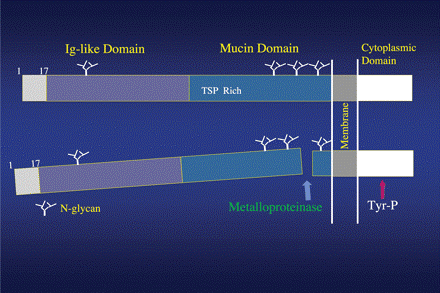
KIM-1 הוא גליקופרוטאין ממברנלי type 1, המכיל בחלק החוץ-תאי שלו מקטע חדש המכיל 6 שיירי ציסטאין דמוי-אימונוגלובולין, שני אתרי N-גליקוזילציה וכן מקטע עשיר ב- Thr/Ser/Pro האופייני לחלבונים עם אתרי O-גליקוזילציה. KIM-1 מכיל כמובן מקטע תוך-או טרנס-ממברנלי, וכן מקטע תוך-תאי קצר יחסית עם tyrosine phosphorylation signalling motif בתאי הכליה שסימונו KIM-1b.
אנליזה של רצף חומצות האמינו קבעה ש-339 חומצות האמינו של KIM-1, היו בעלי זהות של 79% בין הגליקופרוטאין האנושי וזה של קופים. חלבון זה מכיל רצף איתות (signal sequence), מקטע N-טרמינאלי של 109 חומצות אמינו עשיר בציסטאין המכיל רק אתר אחד של N-גליקוזילציה (בצבע אפור), מקטע mucin של 163 חומצות אמינו העשיר ברצף Thr/Ser/Pro המכיל 3 אתרי O-גליקוזילציה (בצבע כחול), ומקטע תוך תאי בן 48 חומצות אמינו (צבוע בלבן).
רקע פיזיולוגי
KIM-1 הידוע גם כ-TIM-1 וכן כ-HAVcr-1, הוא גליקופרוטאין טרנס-ממברנלי המכיל mucin חוץ-תאי וכן מקטעים (domains) של אימונוגלובולין (Chimura וחב' ב-J Biol Chem משנת 1998). הוא מבוטא במידה מעטה ביותר בתאי אפיתל של כליות בריאות, אך הביטוי שלו מתגבר משמעותית בעקבות נזק בתר-איסכמי באבוביות הקריבניות (proximal tubules). המקטע החוץ-תאי של KIM-1 מופיע בשתן זמן קצר לאחר הופעת הנזק האיסכמי המתואר וניתן לגלותו באופן איכותי בבדיקת סקר על ידי טבילת מקלון (dipstick) מתאים בשתן, מה שהופך את KIM-1 לסמן נוח וניתן לגילוי ולהערכה איכותית של נזק כלייתי חריף (להלן AKI).
ה-mRNA של הגליקופרוטאין הידוע כ-kidney injury molecule-1 המסומן במכרסמים כ-kim-1 ובבני-אדם כ-KIM-1, זוהה בשיטה המבוססת על PCR הידועה כ- representational difference analysis של cDNA שפותחה על ידי Hubank ו-Schatz ופורסמה בשנת 1994 ב-Nucl Acid Res. היה זה Joseph Bonventre במעבדתו ב-Harvard Med School בשיתוף פעולה עם Ichimura שהשתמשו לראשונה ב-1998 ב-J Biol Chem תוך שימוש בשיטה המתוארת כאן לחפש גנים שהביטוי שלהם התגבר מאוד 24-48 שעות לאחר איסכמיה בחולדות, ומצאו שביטוי הגן Kim-1 עלה באופן הבולט ביותר. אוטולוגים של KIM-1 נמצאים במינים רבים כולל דגי Zebra, קופים וכלבים.
תאגיד פרמצבטי גדול נקט בשיטה גנומית להעריך גנים המתבטאים-ביתר לאחר טיפול בציספלטין הידוע כמשרה נזק נפרוטוקסי, ואכן מצאו שהגן Kim-1 הגדיל את ביטויו יותר מכל אחד מגנים אחרים שנסרקו (Amin וחב' ב-Environ Health Perspect משנת 2004). מספר גדול של מחקרים בחיות הראו יצירה ניכרת של החלבון Kim-1 באזורים מושפעים של האבוביות הקריבניות כל אימת שרעלן או תרחיש פתו-פיזיולוגי גרם לפגיעה בהתמיינות (dedifferntiation) של אפיתל הכליה (Ichimura וחב' ב-Am J Physiol Renal Physiol משנת 2004, Vaidya וחב' באותו כתב עת משנת 2006, ו-Zhou וחב' ב-Toxicol Sci משנת 2009).
תהליך ה- dedifferntiation הוא ביטוי מאוד מוקדם של תגובת תאי האפיתל לפגיעה (Bonventre וחב' ב- J Am Soc Nephrol משנת 2003). הגליקופרוטאין KIM-1 מבוטא גם בלימפוציטים אם כי ברמות נמוכות בהרבה, ולכן קרוי גם T-cell immunoglobulin mucin (TIM)-1. דווח גם ש-KIM-1 מבוטא גם בשבלול האוזן (cochlea) בתגובה לנזק הנגרם מטיפול בציספלטין (Mukherjea וחב' ב-Neuroscience משנת 2006). משפחת KIM/TIM מורכבת מ-8 חברים בעכברים, ששה בחולדות ו-3 באדם (Kuchroo וחב' ב-Adv Immunol משנת 2006). על ידי שימוש באנליזות סטנדרטיות כגון western blot או northern blot כמו גם אימונו-ציטוכימיה, הגן Kim-1 או ביטויו, אינם ניתנים לגילוי בכליה הנורמאלית. לאחר נזק כלייתי מופיע במהירות KIM-1 mRNA וחלה עלייה ניכרת ברמת החלבון KIM-1 הממוקם בריכוזים גבוהים בממברנה האפיקלית של האבוביות הקריבניות באזור בו האבוביות נפגעו באופן הניכר ביותר. במקרה של השרייה ניסויית של איסכמיה במכרסמים, ביטויו של Kim-1 הוא בעיקר בקטע S3 של האבובית הקריבנית. בבני-אדם, איסכמיה או נזק טוקסי הגורם לפגיעה כלייתית חריפה (AKI), ביטויו של KIM-1 הוא בשלושת הקטעים של האבובית הקריבנית.
המבנה של חלבון זה הביא את Bonventre ואנשיו למחשבה שיש לו תכונות של מולקולת ספיחה (adhesion) כפי שפרסמו Bailly וחב' ב-J Biol Chem משנת 2002. לאחר מכן מצאו Han וחב' (J Am Soc Nephrol משנת 2005) ש-KIM-1 מבוטא גם בריכוזים גבוהים במטופלים עם renal cell carcinoma מסוג תאי Clear, שגם בהם הנזק כרוך בדה-דיפרנציאציה של תאים האבובית הקריבנית.
כעת מתחילים להעריך את תפקודו של KIM-1 בכליה. חלבון זה מעניק לתאי האפיתל את היכולת לזהות ולבלוע בתהליך של פגוציטוזה תאים מתים המופיעים לאחר טראומה כלייתית, אשר גורמים לחסימה של נהור (lumen) האבוביות, מהמאפיינים של AKI. כמו כן, KIM-1 הוא קולטן של phosphatidylserine המזהה תאים אפופטוטים ומכוון אותם לליזוזומים. בנוסף, KIM-1 משמש קולטן לליפופרוטאינים מחומצנים ולכן הוא מתאים לזיהוי של איתותי "השמד אותי" של תאים אפופטוטים. לנוכח סגולות אלו נראה ש-KIM-1 ייחודי בהיותו הקולטן הראשון הלא-מילואידי של phosphatidylserine המתמיר תאי אפיתל לתאים עם פנוטיפ פגוציטי (Ichimura וחב' ב-J Clin Invest משנת 2008). בנוסף לסיוע שלו לפינוי של פסולת אפופטוטית מהנהור האבובי, KIM-1 עשוי לשחק תפקיד בהגבלת התגובה האוטו-אימונית לנזק כלייתי, כיוון שידוע במערכות רבות שפגוציטוזה של גופים אפופטוטים הוא מנגנון המגביל את התגובה הדלקתית. עם זאת, תגובת ההגנה האקוטית, אינה אמורה בהכרח להיות מתורגמת להשפעות הכרוניות של ביטוי KIM-1, כיוון שמטופלים רבים עם אי-ספיקה כלייתית כרונית, מבטאים את KIM-1 באבוביות הקריבניות שלהם (Vaidya וחב' ב-Clin Trans Sci משנת 2008, ו- van Timmeren ב-J Pathol משנת 2007).


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק