הבדלים בין גרסאות בדף "פסוריאזיס - ספחת - טיפול במעכבי אינטרלויקין Psoriasis - treatment with interleukin 17A inhibitors - 17A"
גרסה מ־14:09, 25 באוקטובר 2021
| פסוריאזיס - טיפול במעכבי אינטרלויקין 17A | ||
|---|---|---|
| Psoriasis - treatment with interleukin 17A inhibitors | ||
| ||
| יוצר הערך | ד"ר מיכאל זיו | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – פסוריאזיס, סל תרופות 2016
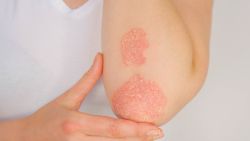
פסוריאזיס (ספחת) היא מחלת עור דלקתית כרונית הפוגעת ב-2–3 אחוזים מהאוכלוסייה. ההערכה היא כי התפתחות המחלה מקורה בגורמים גנטיים (Genetic) וסביבתיים אשר בתורם מביאים לשפעול תהליך דלקתי שסופו בשגשוג מואץ של תאי ה-Epidermis. הביטוי השכיח של המחלה הוא בהופעת נגעים אדומים מכוסי קשקשת כסופה, בפיזור סימטרי, בחלקים המישרים של הגפיים, גו ובמקרים רבים גם בקרקפת. צורת ביטוי זו מכונה Psoriasis Vulgaris. עם זאת יכולה המחלה לערב למעשה כל אזור בגוף, כולל כפות הידיים והרגליים, ציפורניים ואיבר המין.
בקרב חולי הספחת קיימת היארעות מוגברת של טרשת עורקים ומחלות קרדיווסקולריות (Cardiovascular), תסמונת מטבולית (Metabolic), דלקת מפרקים ודיכאון[1]. מכאן שלמחלה השלכות על תפקודם, איכות חייהם ובריאותם הכללית של החולים.
במרבית המקרים נקבעת האבחנה על ידי הקליניקה. שני הכלים עיקריים באמצעותם נקבעת חומרת המחלה הם:
- BSA (Body Surface Area) - בשיטה זו אחוז אחד של שטח הגוף נקבע על פי כף ידו של המטופל. על פי מדד זה מקובל לסווג את המחלה לשלוש דרגות חומרה (קלה- עד 3 אחוזים, בינונית-3–10 אחוזים וקשה - למעלה מ־10 אחוזים)
- מדד נוסף שבו מרבים להשתמש במחקרים קליניים הוא PASI (Psoriasis Area and Severity Index), כלי חישוב כמותי הכולל את המשתנים הבאים: דרגת האודם, עובי הרובד, עובי הקשקש, מידת פיזור הנגעים ומיקומם. הדירוג נע בין 0 (הפוגה מוחלטת) ל־72 (חומרה מרבית)
ברוב המחקרים הקליניים הבודקים יעילותה של תרופה נחשב '75 PASI' כמדד העיקרי להגדרת הצלחה טיפולית. כלומר, מספר המטופלים אצלם חל שיפור של 75 אחוזים ומעלה בתום תקופת המעקב בהשוואה למצבם בזמן הגיוס. מדד חשוב נוסף, המדרג את איכות חיי המטופל הוא DLQI (Dermatology Life Quality Index). הדירוג נע בין 0 (ללא כל פגיעה באיכות החיים) ל־30 (פגיעה מרבית באיכות החיים).
הטיפול בספחת
ככלל, הטיפול בספחת נקבע על פי חומרת המחלה ומיקום הפריחה. הטיפול במחלה מגוון וכולל את התכשירים הבאים:
- משחות - בעיקר על בסיס קורטיקוסטרואידי (Corticosteroid) (לבד או בשילוב עם Calcipotriol - נגזרת של Vitamin D). בשל החשש מספיגה מערכתית לאורך זמן וכן תופעות לוואי מקומיות, כגון אטרופיה (Atrophy) עורית, מוגבל השימוש בתכשירים אלה מבחינת משך והיקף שטח המריחה.
- תכשיר נוסף הוא עטרן (Coal tar) ולרוב נעשה בו שימוש במסגרת אשפוז או אשפוז יום ובשילוב עם קרינת UVB (Ultraviolet). שיטה זו של שילוב מכונה ״שיטת Goeckerman״
- פוטותרפיה (Phototherapy) - טיפול המבוסס על חשיפת החולה באופן מבוקר לאור על־סגול מסוג UVB) B) או A (UVA). האחרון נעשה בשילוב עם Psoralen, חומר פוטוטוקסי (Phototoxic) הניתן בכמוסות או בתמיסת השריה (באמבט). שילוב זה מכונה PUVA (Psoralen and ultraviolet A). משערים שהקרניים העל־סגוליות מעכבות את התהליך הדלקתי ואת שגשוג תאי ה-Epidermis. פוטותרפיה נחשבת לשיטת טיפול בטוחה ויעילה. עם זאת עלולות להתפתח תגובות לא רצויות הן בטווח הקצר (כגון כוויה) והן בטווח הארוך (כגון הזדקנות מואצת של העור וסיכון מוגבר להתפתחות סרטן עור)
- טיפול אקלימי בים המלח - מבוסס בעיקר על חשיפה מבוקרת לשמש
- טיפולים סיסטמיים ותיקים - Methotrexate, תרופה המשמשת לטיפול במגוון מחלות דלקתיות ופועלת בספחת על ידי עיכוב התהליך הדלקתי בעור
- Acitretin - Acitretin (Neotigason) - Retinoid -נגזרת של Vitamin A. אופן הפעולה המשוער של התרופה הוא השפעתה המיטיבה על התמיינות ושגשוג תאי ה-Epidermis והפעילות החיסונית
- Cyclosporine - Cyclosporine היא תרופה הפועלת באופן מהיר באמצעות דיכוי התהליך החיסוני בעור
- טיפול ביולוגי - בעשור האחרון אושרו לטיפול בספחת ארבע תרופות ביולוגיות:
- Etanercept (Enbrel)
- Infliximab (Remicade)
- Adalimumab (Humira)
שלושתן כנגד הציטוקין
- TNF-α (Tumor Necrosis Factor) ו-Stelara) Ustekinumab) המכוונת כנגד 12/23 IL (Interleukin)
הטיפול הביולוגי ניתן רק לאחר שלא הושגה הטבה מספקת עם הטיפולים האחרים שפורטו לעיל, ובהתאם להנחיות שנקבעו בסל התרופות. כל התרופות ניתנות בהזרקה תת-עורית, למעט Inliximab הניתנת בעירוי תוך ורידי.
ככלל, נחשבים טיפולים אלה כיעילים ובטוחים לטיפול בספחת. עם זאת, לא כל טיפול מביא להטבה הרצויה או שלאורך זמן ייתכן פיחות בהשפעתו המיטיבה. במקרים אלה נדרש מעבר בין טיפול ביולוגי אחד למשנהו. במחקרים אחדים נמצא שמעבר בין נוגדי TNF-α עשוי להיטיב עם המטופל[2], אולם מרבית המחקרים מצביעים על פגיעה ביעילות התגובה אצל אותם חולים לטיפול השני והשלישי בהשוואה למטופלים ״נאיבים״ בתכשיר מקבוצה זו[3]. כך הדבר גם במעבר מ-Etanercept ל- Ustekinumab[4].
נוגדי Interleukin-17A
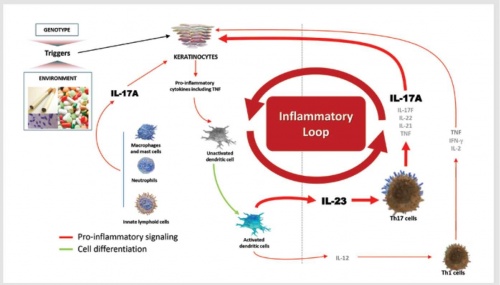
בשנת 2003 נתגלה ה-Cytokine IL-17A, כתוצר של שפעול שורת תאי T מסייעים חדשה על ידי 23-IL, שהוגדרה שנתיים מאוחר יותר כ־'Th17' (T helper). בנוסף, מיוצר IL-17A גם על ידי תאים אחרים, בהם נויטרופילים (Neutrophils) ותאי Mast. נמצא של-IL-17A תפקיד חשוב בפתוגנזה (Pathogenesis) של ספחת. תאי ה-Epidermis מהווים מטרה מרכזית ל-Cytokine זה. התקשרות IL-17A לקולטנים על פני תאי ה-Epidermis מביאה ליצירת כימוקינים (Chemokines) וציטוקנים (Cytokines) על ידם, בהם גם TNF-α, ועל ידי כך להגברת התהליך הדלקתי בתהליך מעגלי (תרשים מספר 1) ולשגשוגם המואץ של תאי ה-Epidermis[5].
בעקבות ממצאים אלה פותחו שני נוגדנים חד־שבטיים לעיכוב IL-17A:
האחרון אושר לטיפול בספחת בינונית-קשה בארצות הברית ובאירופה בינואר 2015, ובחודש אוגוסט 2015 אושר להתוויה זו גם בישראל.
Cosentyx היא נוגדן חד־שבטי ממקור אנושי המנטרל את פעילותו של IL-17A. במחקר קליני, פאזה III, שבו נבדקה יעילות התרופה במינון 300 מיליגרמים (הזרקה תת-עורית מדי שבוע ב־5 השבועות הראשונים ובהמשך כל 4 שבועות) בספחת בינונית עד קשה, הושגה הטבה של 75 אחוזים ומעלה (75 PASI) בקרב 81.6 אחוזים מהמטופלים לעומת 4.5 אחוזים מקרב מקבלי האינבו לאחר 12 שבועות טיפול. בתום תקופה זו נרשמו שיפור של 90 אחוזים (90 PASI) בקרב 59 אחוזים מהמטופלים והפוגה מוחלטת (100 PASI) בקרב 28.6 אחוזים מתוכם. ב-80.5 אחוזים נשמר 75 PASI לאורך 52 שבועות.
יעילות התרופה נבדקה גם מול שתי תרופות ביולוגיות המצויות בסל התרופות.
במחקר השוואתי שנערך מול Enbrel נמצאה Cosentyx יעילה יותר באופן משמעותי. בתום 52 שבועות נמדד 75 PASI של 84.3 אחוזים בקרב מטופלי Cosentyx לעומת 72.5 אחוזים ממטופלי Etanercept. לא נמצא הבדל מהותי בשיעור ובאופי תופעות הלוואי בין שני הטיפולים. תופעות הלוואי העיקריות היו קלות יחסית וכללו Nasopharyngitis כאב ראש ושלשול[6].
במחקר השוואתי שנערך מול Ustekinumab הושג, לאחר 16 שבועות, 90 PASI בקרב 79 אחוזים ממטופלי Cosentyx לעומת 57.6 אחוזים מהמטופלים ב-Ustekinumab. שיפור של 100 אחוזים, כלומר הפוגה מוחלטת, הושג ב־44.3 אחוזים מהמטופלים ב-Cosentyx לעומת 28.4 אחוזים במטופלי Ustekinumab. גם כאן לא נמצא הבדל מהותי בפרופיל הבטיחותי בין התרופות[7].
היבט נוסף שנבדק בשני המחקרים ההשוואתיים שלעיל היה מדד איכות החיים (DLQI). במחקר הראשון נמדד שיפור ממוצע של 10.4(-) (ירידה מדירוג ממוצע של 13.3-בתחילת המחקר ל־2.9 בתום 12 שבועות) בקרב מטופלי Cosentyx. במחקר השני ירד DLQ171 ל־0/1 בתום 16 שבועות בקרב 71.9 אחוזים מהמטופלים בתרופה. כלומר, חל שיפור משמעותי בקרב איכות חייהם של מרבית המטופלים.
Cosentyx היא תרופה ביולוגית חדשה ויעילה לטיפול ב-Psoriasis vulgaris, הפועלת במנגנון שונה מהתרופות הביולוגיות הקיימות, בעלת פרופיל בטיחות דומה ומהווה אפשרות טיפולית משמעותית נוספת במקרים שבהם מתקיימים הקריטריונים לטיפול ביולוגי. התרופה ניתנת בזריקות תת-עוריות במינון 300 מיליגרמים, מדי שבוע בחודש הראשון ובהמשך אחת ל־4 שבועות.
ביבליוגרפיה
- ↑ Richard MA, Barnetche T, Horreau C et al. Psoriasis, cardiovascular events, cancer risk and alcohol use: Evidence-based recommendations based on systematic review and expert opinion. J Eur Acad Dermatol Venereol 2013; suppl. 3, 2-11
- ↑ Bissonnette R, Bolduc C, Poulin Y et al. Efficacy and safety of Adalimumab in patients with plaque psoriasis who have shown unsatisfactory response to Etanercept. J Am Acad Dermatol 2010; 63:228-34
- ↑ Woolf RT, Smith CH, Robertson K et al. Switching to Adalimumab in patients with moderate to severe psoriasis who have failed on Etanercept: a retrospective case cohort study. Br J Dermatol 2010; 163: 889-892
- ↑ Griffith CEM, Strober BE, Kerkhof van de P et al. Comparison of Ustekinumab and Etanercept for moderate to severe psoriasis. N Eng J Med 2010; 362:118-128
- ↑ Lynde C, Poulin Y, Vender R et al. Interleukin 17A: Toward a new understanding of psoriasis pathogenesis. J Am Acad Dermatol 2014;71:141-150
- ↑ Langley R, Elewsky BE, Lebwohl M et al. Secukinumab in psoriasis-Results of two phase 3 trials. N Eng J Med 2014; 371: 326-38
- ↑ Thaci D, Blauvelt A, Reich K et al. Secukinumab is superior to ustekinumab in clearing skin of subjects with moderate to severe plaque psoriasis: CLEAR, a randomized controlled trial. J Am Acad Dermatol 2015; 73(3): 400-9
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר מיכאל זיו מרפאת פסוריאזיס, מחלקת עור, המרכז הרפואי העמק, עפולה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק