הבדלים בין גרסאות בדף "מבוא לתחלואה נלווית לא זיהומית במטופלים עם - Introduction to non-infectious comorbidiyty in HIV patients - HIV"
יאיר שוורץ (שיחה | תרומות) |
יאיר שוורץ (שיחה | תרומות) |
||
| שורה 93: | שורה 93: | ||
ב-CD4 מעל ל-500 ההנחיות הקליניות המקובלות בעולם אינן תמימות דעים. קהילת הרפואה והמחקר מצפה לקבל תשובה לשאלה חשובה זו בתוצאות מחקר ה- STRAT. | ב-CD4 מעל ל-500 ההנחיות הקליניות המקובלות בעולם אינן תמימות דעים. קהילת הרפואה והמחקר מצפה לקבל תשובה לשאלה חשובה זו בתוצאות מחקר ה- STRAT. | ||
| − | כדי לקבל מושג כללי לגבי הטיפול המשולב יפורט בקצרה על הנהוג לטיפול בקו ראשון:{{ש}}לטיפול קו ראשון לחולים שלא נחשפו לטיפול בעבר (נאיביים) כיום נהוג לשלב שתי תרופות ממשפחת ה-NRTI{{כ}} (Nucleoside | + | כדי לקבל מושג כללי לגבי הטיפול המשולב יפורט בקצרה על הנהוג לטיפול בקו ראשון:{{ש}}לטיפול קו ראשון לחולים שלא נחשפו לטיפול בעבר (נאיביים) כיום נהוג לשלב שתי תרופות ממשפחת ה-NRTI{{כ}} (Nucleoside reverse transcriptase inhibitor) (לרוב בטבלייה אחת) עם תרופה ממשפחת ה-NNRTI{{כ}} (Non-nucleoside reverse transcriptase inhibitor) או עם תרופה ממשפחת ה-PI{{כ}} (Protease inhibitors) (בשילוב PI במינון נמוך ritonavir כ-booster) או עם תרופה ממשפחת ITI{{כ}} (Integrase inhibitors). |
===תרופות ART לפי משפחות=== | ===תרופות ART לפי משפחות=== | ||
גרסה מ־21:09, 19 בדצמבר 2011
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| ' | ||
|---|---|---|
| ' | ||
| יוצר הערך | ד"ר ענב נוף | |
השימוש בטיפול אנטי-רטרווירלי משולב (ART) שינה באופן דרמטי את מהלך מחלתם של אנשים החיים עם HIV תוך הארכת תוחלת החיים, צמצום הזיהומים והגידולים האופורטוניסטיים, ושיפור איכות החיים (1,2). עם זאת, התמותה ותוחלת החיים הצפויה בקרב אנשים עם HIV שונה מהאוכלוסייה הבריאה, וכיום מתייחסים להדבקה ב-HIV תחת טיפול ב- ART כאל מחלה כרונית (1,2). יש שיאמרו כי מדובר בתהליך של הזדקנות מוקדמת, עם כל המשתמע מכך.
בין סיבות התמותה והתחלואה הבולטות באוכלוסיה זו בעידן ה- ART: מחלות קרדיווסקולריות, פגיעה כלייתית, מחלות מטבוליות כגון סוכרת ואוסטאופורוזיס, מחלות כבד, גידולים שאינם קשורים לאיידס כגון סרטן ריאה ולימפומות, פגיעה נוירוקוגנטיבית, פגיעה התפקוד המיני ותחלואה פסיכיאטרית (3,4,5,6).
הדעה המקובלת כיום בספרות המקצועית היא שהגורמים לשכיחות הגבוהה של מחלות ומצבים אלו באנשים החיים עם HIV הם שילוב של הארכת תוחלת החיים, תופעות לוואי של הטיפול האנטי-רטרוורלי, והפעלה של מערכת חיסון כתוצאה מהנגיף עצמו, אשר גורמת לדלקתיות וקרישתיות (9).
האמור לעיל ממחיש את האופי הכרוני של הדבקה ב-HIV, ולכן את ההכרח שבמעורבות רופא ראשוני בטיפול. עיקרי הצרכים המיוחדים לאוכלוסיית מטופלים זו הינם מצבים המוכרים היטב ברפואת המשפחה. חלקם הם אף "הלחם והמים" של הפרקטיקה היומיומית בטיפול במחלות כרוניות אחרות כגון סוכרת ומחלות לב איסכמיות, ואינם שונים בהרבה מטיפול במחלות אלו (7,8).
הספרות וההנחיות הקליניות המקובלות כיום בעולם לטיפול ב-HIV כוללות חלק נכבד על מניעה וטיפול בתחלואה צולבת שאינה זיהומית - "Non-infectious co-morbidities" (9).
אפידמיולוגיה
הערכת המחלקה לשחפת ואיידס של משרד הבריאות לקראת יום האיידס העולמי שנת 2011 (נכון ל- 2010) היא כי בישראל חיים 7,744 אנשים עם HIV. ההיארעות עלתה מ-382 מקרים חדשים לשנה בשנים 2006-2010 ל- 430 בשנת 2010.
בישראל אפשר למצוא HIV מכל מגוון האוכלוסייה, אך קיימות 3 אוכלוסיות עיקריות, כל אחת כשליש מהנשאים בארץ, בהם השכיחות גבוהה: גברים המקיימים יחסי מין עם גברים (MSM), יוצאי מדינות אנדמיות (בעיקר מהגרי עבודה ויוצאי אתיופיה), ומשתמשים בסמים בהזרקה (Intravenous drug abusers - IVUD). במהלך 2010 נרשמה עליה במספר הדיווחים על הדבקות בקרב MSM ובקרב מהגרים יוצאי מדינות אנדמיות שאינם אזרחי ישראל.
חשוב לציין כי בישראל בשנת 2010 עדיין נולדים ילדים עם HIV לאמהות שלא נבדקו לפני הלידה.
טיפול
HIV לאחר אבחנה
לאחר קבלת תשובה ראשונית חיובית לבדיקת HIV מופנה המטופל לאחד ממרכזי הטיפול ב-HIV בארץ: בי"ח רמב"ם, בי"ח הדסה עין כרם, בי"ח תל השומר, בי"ח איכילוב, בי"ח קפלן, בי"ח סורוקה, בי"ח מאיר. שם מבוצעת בדיקה נוספת וקבלת אבחנה סופית.
בפגישה הראשונה הוא מופנה לאחד הרופאים המומחים ל- HIV – בישראל כיום מטפלים ב- HIV רופאים מומחים למחלות זיהומיות או לאימונולוגיה. בנוסף עליו לבצע בדיקות שונות שישמשו כרמת בסיס (base line): רמת תאי ה- CD4 והעומס הנגיפי (Viral Load - VL), ספירת דם כללית, SMAC, פרופיל שומנים, צילום חזה, נוגדנים לטוקסופלזמה, CMV, דלקת כבד נגיפית מסוג A, B ו- C, VDRL ובדיקת מנטו.
על-פי תוצאות הבדיקות ניתנים החיסונים הרלוונטיים ומוחלט על טיפול רפואי, כולל טיפול ב- ART לפי הצורך (ראו בהמשך).
המעקב והטיפול במרכז האיידס כולל: בדיקת עמידות, מעקב אחר יעילות הטיפול בדיכוי ההתרבות (רפלקציה) של הנגיף ובשיפור מערכת החיסון, מעקב אחר תופעות לוואי מסוכנות, ושינוי ART לפי הצורך – אם בשל תופעות לוואי, אם בשל מחלות נלוות המחייבות שינוי תרופתי, ואם בשל כשלון טיפולי. החלק הנוסף של הטיפול באנשים עם HIV, הכולל טיפול כבכל אדם אחר, תוך התייחסות מיוחדת לתחלואה צולבת ולאיזון גורמי סיכון, נמצא בידי הרופא הראשוני בקהילה.
קיימת חשיבות ראשונה במעלה לתקשורת בין רופאי ה- HIV לרופאים הראשוניים, כפי שמתבצע בטיפול במחלות כרוניות אחרות כגון סוכרת.
המלצות כלליות להערכה ומעקב אחר גורמי סיכון ותחלואה נילווית במרפאה הראשונית
(9,10)
- אנמנזה:
- מלאה כולל הרגלים (תזונה, פעילות גופנית, עישון, אלכוהול, סמים, פעילות מינית, סטטוס בן הזוג, שימוש באמצעי מניעה, תרופות)
- הערכת סיכון קרדיווסקולארי
- הערכה של מצב מנטאלי ודיכאון בפרט
- בדיקה פיזיקאלית כולל אינדקס מסת גוף (BMI), מדידת לחץ דם
- 3 שאלות סקר נוירוקוגנטיבי (בהמשך)
- צילום חזה (לרוב יבוצע במרכז האיידס)
- אק"ג: גברים גיל >40, נשים גיל >50
- מעבדה: ספירת דם, תפקודי כבד, סידן ואלבומין, פוספט, גלוקוז, קראטינין, eGFR, פרופיל שומנים, שתן כללית (חלבון וסוכר), שתן לפרוטאין/קראטינין, ויטמין D
- הערכת סיכון למחלות המועברות במגע מיני (STD) אחרות ובדיקות מעבדה לפי הצורך
- PAP בנשים
- חיסון לדלקת כבד נגיפית מסוג A, B, פנאומוקוק (אחת ל-5 שנים), שפעת (אחת לשנה)
- הערכת סיכון לאוסטאופורוזיס ונפילות (FRAX למשל) במטופלים מגיל >40
- ייעוץ וטיפול להפסקת עישון, שמירה על משקל ופעילות גופנית
- ממוגרפיה בנשים מגיל 50
תחילת טיפול אנטי-רטרוויראלי ART
(Anti Retroviral Therapy) (9,10)
טיפול תרופתי ב- HIV גורם להתאוששות של המערכת החיסונית, המתבטאת מעבדתית בעלייה של כמות תאי ה- CD4 ואחוזם, ולירידה בעומס ה- RNA הנגיפי (VL) בדם. היעד הטיפולי המעבדתי המקובל כיום הוא עומס נגיפי (VL) שאינו ניתן למדידה בבדיקות חוזרות.
הטיפול ב-ART הוא טיפול לכל החיים. ההחלטה לגבי המועד המתאים לתחילת טיפול ART מורכבת, ונמצאת כיום במרכז המחקר והדיון בספרות העולמית בשל השלכות אפשרויות על האפידמיה העולמית כולה, ועל כן חשוב להרחיב בקצרה בנושא גם במסגרת הרפואה הראשונית.
מחד ברור כי הטיפול מביא לירידה דרמטית בתחלואה ובתמותה. מנגד הטיפול גורם לתופעות לוואי, בחלקן קשות, דורש היענות גבוהה ביותר כדי למנוע התפתחות עמידות, ועלותו הכלכלית כבדה.
כיום קיים שיקול נוסף לטובת תחילת טיפול מוקדם – הצטברות משמעותית של מחקרים ומאמרים לפיהם השיטה הטובה ביותר למניעת הדבקה היא על ידי טיפול באנשים עם HIV, כך שהעומס הנגיפי בדמם יהיה נמוך עד לא ניתן למדידה, ולכן למעשה לא יוכלו לדביק אחרים - טיפול כמניעה (Treatment as prevention) (11,12).
שאלה נוספת חשובה הנבדקת כעת במחקר גדול במעל ל-30 מדינות היא האם יש עדיפות קלינית לתחילת טיפול מוקדם יותר, שיביא למצב בו כמות תאי ה- CD4 תהיה גבוהה וקרובה יותר לכמותם באדם ללא HIV (Strategic timing of antiretroviral treatment - START) (13).
בשל מורכבת שאלת תחילת הטיפול נדונות ונכתבות מספר הנחיות קליניות המקובלות בעולם, המתעדכנות אחת לשנה, אך גם ההנחיות עצמן משאירות שיקול דעת משמעותי לרופא המומחה לHIV\איידס ולמטופל בהחלטה על מועד תחילת הטיפול.
גורמים רבים משפיעים על מועד התחלת הטיפול: תסמינים הקשורים להדבקה והתפתחות מחלות כשל חיסוני, מחלות נלוות וגורמי סיכון, גיל, גורמים היכולים להשפיע לרעה על היענות (כגון התמכרויות ומחלות פסיכיאטריות), התרופות הקיימות לרשות הרופא והמטופל, עלות כלכלית ועוד.
ההחלטה לגבי מועד תחילת הטיפול שמורה כיום לרופא המומחה ל- HIV\איידס, אך הרקע הביו-פסיכו-סוציאלי, הינו לעיתים קרובות קריטי בקבלת ההחלטה, כמו גם בהחלטה לגבי סוג הטיפול שיומלץ, וכאן שיתוף פעולה בין הרופא הראשוני לרופא ה- HIV חשוב מאין כמוהו.
על מנת להמחיש את מורכבות הנושא מובאות בקצרה ובהכללה ההנחיות הקליניות של הארגון האירופאי לאיידס EACS (The European AIDS Clinical Society) מאוקטובר 2011.
בהנחיות EACS ההמלצה היא להתחיל ART במקרים הבאים: מתקיימים מצבים רפואיים המגדירים "איידס" או תחלואה משמעותית כתוצאה מכשל חיסוני (לדוגמא בזיהומים אופורטוניסטים פעילים), ה- CD4 קטן מ-350, הריון, פגיעה כלייתית או נוירוקוגנטיבית כתוצאה מהנגיף, לימפומה מסוג הודג'קינס, סרטן הקשור לנגיף הפפילומה האנושי, דלקת כבד נגיפית מסוג B הדורשת טיפול, ודלקת כבד נגיפית מסוג C.
ברוב המצבים האחרים בהם ה- CD4 נע בין 350 ל- 500 התחלת טיפול ב-ART נתונה לשיקול הדעת של הרופא בשיתוף המטופל.
ב-CD4 מעל ל-500 ההנחיות הקליניות המקובלות בעולם אינן תמימות דעים. קהילת הרפואה והמחקר מצפה לקבל תשובה לשאלה חשובה זו בתוצאות מחקר ה- STRAT.
כדי לקבל מושג כללי לגבי הטיפול המשולב יפורט בקצרה על הנהוג לטיפול בקו ראשון:
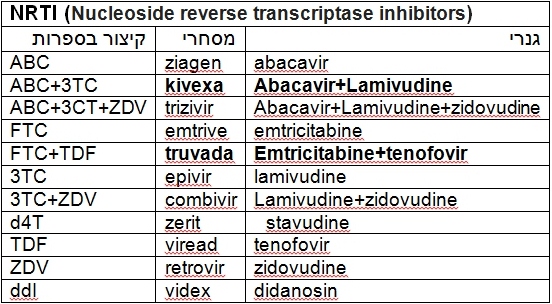
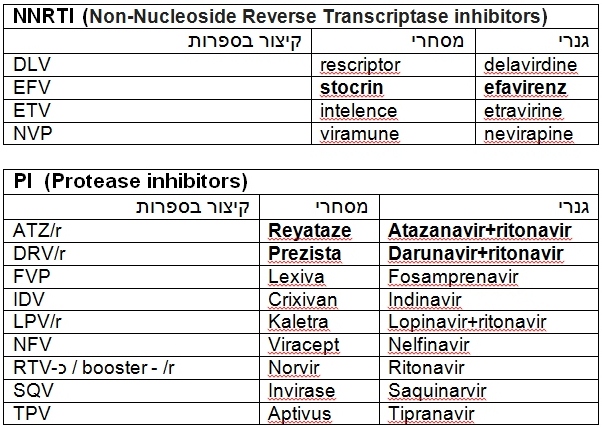
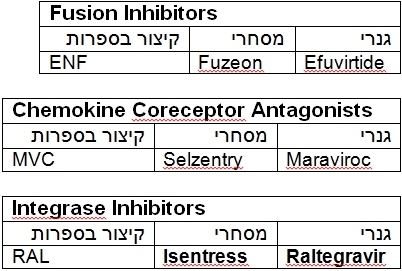
לטיפול קו ראשון לחולים שלא נחשפו לטיפול בעבר (נאיביים) כיום נהוג לשלב שתי תרופות ממשפחת ה-NRTI (Nucleoside reverse transcriptase inhibitor) (לרוב בטבלייה אחת) עם תרופה ממשפחת ה-NNRTI (Non-nucleoside reverse transcriptase inhibitor) או עם תרופה ממשפחת ה-PI (Protease inhibitors) (בשילוב PI במינון נמוך ritonavir כ-booster) או עם תרופה ממשפחת ITI (Integrase inhibitors).
תרופות ART לפי משפחות
שילובים בין הקבוצות:
Atripla = efarinent (NNRTI) + emtricitabine (NRTI)+ tenofovir (NRTI)
סיכום
HIV/איידס תחת טיפול ART נחשבת למחלה כרונית. ככזו, הטיפול בה הפך למורכב עוד יותר מבעבר, ומחייב התייחסות לתחלואה נלווית.
אופייה הכרוני של המחלה מחייב מעקב והתערבות של רופא המשפחה בכל שלבי המעקב והטיפול.
ביבליוגרפיה
- Kijpittayari S, Kasten MJ. Primary care of HIV-infected adults. J Med Liban. 2006; 54(2):65-73.
- Khalsa AM. Preventing, Counseling, Screening, and Therapy for the Patient with Newly Diagnosed HIV infection. Am Fam Physician. 2006; 73(2):271-80.
- Martinez E. et al. Incidence and causes of death in HIV-infected persons receiving highly active antiretroviral therapy compared with estimates for the general population of similar age and from the same geographical area. HIV Med. 2007; 8(4):251-58.
- Hooshyar D. et al. Trends in perimortal conditions and mortality rates among HIV-infected patients. AIDS 2007; 21(15):2093-100.
- Friis-Moller N. et al; DAD study group. Cardiovascular disease risk factors in HIV patients-association with antiretroviral therapy. Results from the DAD study. AIDS 2003; 17(8):1179-93.
- Israelski DM. et al. Psychiatric co-morbidity in vulnerable populations receiving primary care for HIV/AIDS. AIDS Care. 2007; 19(2):220-25.
- Mallison RK, Rajabiun S, Coleman S. The provider role client engagement in HIV care. AIDS Ptient Care STDS. 2007; 21 (Suppl 1): S77-84.
- Cohen DE, Mayer KH. Primary care issues for HIV-infected patients. Infec Dis Clin North Am. 2007; 21(1):49-70.
- The European Guidelines for treatment of HIV infected adults in Europe. October 2011.
- C.Hoffmann, J.K. Rockstroh. HIV 2011. www.hivbook.com. Medizin Fokus Verlag. 2011.
- Lima, V.D et al. Expanded access to highly active antiretroviral therapy: A potentially powerful strategy to curb the growth of the HIV epidemic. The Journal of Infectious Diseases. 2008:198:59-67.
- Granich, R.M et al. Universal voluntary HIV testing with immediate antiretroviral therapy as a strategy for elimination of HIV transmission: a mathematical model. The Lancet, 2009; 373: 48-57.
- Strategic Timing of Antiretroviral Treatment (START), http://clinicaltrials.gov/ct2/show/NCT00867048.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק