הבדלים בין גרסאות בדף "תלסמיה - Thalassemia"
מ |
|||
| שורה 20: | שורה 20: | ||
== אפידמיולוגיה == | == אפידמיולוגיה == | ||
| − | + | בדומה להמוגלובינופתיות (Hemoglobinopathies) אחרות, כמו [[אנמיה חרמשית]] (Sickle cell anemia), התלסמיות נפוצות מאוד באגן הים התיכון; שכיחותן גבוהה במדינות כמו יוון, איטליה, צפון אפריקה, ועוד. | |
תצפית מעניינת היא, שנשאות של תלסמיה ומחלות המוגלובין אחרות העניקו עמידות כנגד מחלת ה[[מלריה]] (Malaria) באזורים בהם הן נפוצות. | תצפית מעניינת היא, שנשאות של תלסמיה ומחלות המוגלובין אחרות העניקו עמידות כנגד מחלת ה[[מלריה]] (Malaria) באזורים בהם הן נפוצות. | ||
| שורה 26: | שורה 26: | ||
== אטיולוגיה == | == אטיולוגיה == | ||
| − | ההמוגלובין הוא מולקולה בעלת ארבעה חלקים | + | ההמוגלובין הוא מולקולה בעלת ארבעה חלקים, המורכבת מארבע שרשרות של החלבון גלובין (Globin) וממולקולת הם (Heme). מולקולת ההם היא פרוטופורפירין (Protoporphyrin) שבמרכזו ברזל. |
| − | באופן נורמלי, באדם המבוגר, שרשרות הגלובין מורכבות מזוג | + | באופן נורמלי, באדם המבוגר, שרשרות הגלובין מורכבות מזוג שרשרות אלפא וזוג שרשרות בטא. זהו '''המוגלובין A''' – המהווה כ-95% מההמוגלובין בתאי הדם האדומים. |
| − | המרכיב העיקרי של ההמוגלובין בעובר הוא ההמוגלובין העוברי, '''המוגלובין F''' - ובו שרשרת אלפא מתחברת עם שרשרת גאמא | + | המרכיב העיקרי של ההמוגלובין בעובר הוא ההמוגלובין העוברי, '''המוגלובין F''' - ובו שרשרת אלפא מתחברת עם שרשרת גאמא. ההמוגלובין העוברי הולך ופוחת לקראת הלידה, ובאדם הבוגר הוא מהווה מרכיב שולי (מינורי) של 2.5-3% מכלל ההמוגלובין. |
| − | מרכיב שולי נוסף במבוגר הוא '''המוגלובין A2''', הבנוי מצירוף של שרשרות אלפא עם שרשרות דלתא | + | מרכיב שולי נוסף במבוגר הוא '''המוגלובין A2''', הבנוי מצירוף של שרשרות אלפא עם שרשרות דלתא. המוגלובין זה מהווה 2.5% מההמוגלובין באדם בוגר. |
בתלסמיה ישנו ייצור מופחת של אחת משרשרות הגלובין: אלפא (אלפא תלסמיה) או בטא (בטא תלסמיה). ההפרעה היא כמותית - נוצר אמנם המוגלובין תקין, אבל בכמות מופחתת מהנורמה. | בתלסמיה ישנו ייצור מופחת של אחת משרשרות הגלובין: אלפא (אלפא תלסמיה) או בטא (בטא תלסמיה). ההפרעה היא כמותית - נוצר אמנם המוגלובין תקין, אבל בכמות מופחתת מהנורמה. | ||
| − | + | המנגנון המביא לביטויי המחלה, אם נתייחס כדוגמא לבטא טלסמיה, מתחיל מהפרעה בגן המייצר את שרשרות הבטא-גלובין. כתוצאה מכך, ישנם מעט מידי עותקים של שרשרות הבטא ביחס לשרשרות האלפא. שרשרות האלפא המיותרות שוקעות בתאי האב של הכדוריות האדומות, הנורמובלסטים (Normoblasts), במח העצם. שקיעה זו של שרשרות אלפא פוגעת בממברנות התאים וגורמת למותם. | |
חלק מתאי האב הללו יוצרים כדוריות אדומות המגיעות למחזור הדם, אך הן דלות בהמוגלובין ומעוותות בצורתן. כדוריות אדומות אלה נהרסות בעיקר בטחול, וגם במח העצם. כתוצאה מכך, יש מיעוט כדוריות אדומות, ותתכן אנמיה קשה. הרס זה גורם גם להגדלת הטחול. | חלק מתאי האב הללו יוצרים כדוריות אדומות המגיעות למחזור הדם, אך הן דלות בהמוגלובין ומעוותות בצורתן. כדוריות אדומות אלה נהרסות בעיקר בטחול, וגם במח העצם. כתוצאה מכך, יש מיעוט כדוריות אדומות, ותתכן אנמיה קשה. הרס זה גורם גם להגדלת הטחול. | ||
| שורה 43: | שורה 43: | ||
ב'''בטא תלסמיה''' ישנם 2 מצבי מחלה עיקריים: | ב'''בטא תלסמיה''' ישנם 2 מצבי מחלה עיקריים: | ||
| − | * נשאים לתלסמיה - אצלם רק אחד האללים (Alleles) הוא פתולוגי | + | * '''נשאים לתלסמיה''' - אצלם רק אחד האללים (Alleles) הוא פתולוגי. התסמינים הקליניים שלהם קלים. |
| − | * הומוזיגוטים | + | * '''הומוזיגוטים לתלסמיה''' - קיבלו גן פגום משני ההורים. אצלם ההסתמנות היא של בטא תלסמיה גדולה (Thalassemia major){{כ}}, הנקראת גם אנמיית קולי (Cooly's anemuia).{{כ}} <br/>מדובר במחלה קשה: ההרס המוגבר של הכדוריות האדומות גורם ל[[צהבת]], [[אבני מרה]], אנמיה קשה ו[[היפוקסיה]] (Hypoxia).{{כ}}<br/>גוף החולה מנסה ליצור פיצוי להיפוקסיה: בניסיון ליצור יותר תאי דם, ישנה גדילה של מח העצם ופלישה שלו לאזורים אחרים. הדבר מביא לשינויים בעצמות ויצירת דם חוץ-לשדית (Extramedullary hematopoiesis) - יצירת דם באיברים בהם בדרך כלל אין יצירת דם.<br/>החולים זקוקים לעירויי דם חוזרים כדי להתקיים; הדבר מביא לצבירת ברזל, השוקע באיברים שונים של הגוף (לב, כבד, לבלב), ובכך גורם לסיבוכים נוספים. |
===סיבוכים=== | ===סיבוכים=== | ||
גרסה מ־16:58, 9 באפריל 2012
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| טלסמיה | ||
|---|---|---|
| Thalassemia | ||
| ||
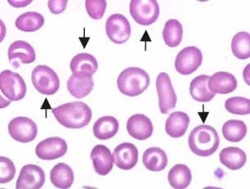
מראה כדוריות הדם האדומות בטלסמיה, חלקן נראות כ"תאי מטרה" עקב עלייה לא פרופורציונית של שטח הפנים של הכדוריות ביחס לנפחן- ממצא שכיח בטלסמיה.
| ||
| ICD-10 | Chapter D 56. | |
| ICD-9 | 282.4 | |
| MeSH | D013789 | |
| יוצר הערך | ד"ר מוטי חיימי | |
תלסמיה היא שם כללי לקבוצה של מחלות תורשתיות גנטיות של תאי הדם האדומים, אשר נובעות מפגם בשרשרות החלבון המרכיבות את ההמוגלובין (Hemoglobin).
מחלת התלסמיה גורמת לאנמיה בדרגות שונות. בצורתה הקשה, גורמת המחלה לאנמיה משמעותית, המצריכה מתן עירויי דם לכל החיים.
אפידמיולוגיה
בדומה להמוגלובינופתיות (Hemoglobinopathies) אחרות, כמו אנמיה חרמשית (Sickle cell anemia), התלסמיות נפוצות מאוד באגן הים התיכון; שכיחותן גבוהה במדינות כמו יוון, איטליה, צפון אפריקה, ועוד.
תצפית מעניינת היא, שנשאות של תלסמיה ומחלות המוגלובין אחרות העניקו עמידות כנגד מחלת המלריה (Malaria) באזורים בהם הן נפוצות.
אטיולוגיה
ההמוגלובין הוא מולקולה בעלת ארבעה חלקים, המורכבת מארבע שרשרות של החלבון גלובין (Globin) וממולקולת הם (Heme). מולקולת ההם היא פרוטופורפירין (Protoporphyrin) שבמרכזו ברזל.
באופן נורמלי, באדם המבוגר, שרשרות הגלובין מורכבות מזוג שרשרות אלפא וזוג שרשרות בטא. זהו המוגלובין A – המהווה כ-95% מההמוגלובין בתאי הדם האדומים.
המרכיב העיקרי של ההמוגלובין בעובר הוא ההמוגלובין העוברי, המוגלובין F - ובו שרשרת אלפא מתחברת עם שרשרת גאמא. ההמוגלובין העוברי הולך ופוחת לקראת הלידה, ובאדם הבוגר הוא מהווה מרכיב שולי (מינורי) של 2.5-3% מכלל ההמוגלובין.
מרכיב שולי נוסף במבוגר הוא המוגלובין A2, הבנוי מצירוף של שרשרות אלפא עם שרשרות דלתא. המוגלובין זה מהווה 2.5% מההמוגלובין באדם בוגר.
בתלסמיה ישנו ייצור מופחת של אחת משרשרות הגלובין: אלפא (אלפא תלסמיה) או בטא (בטא תלסמיה). ההפרעה היא כמותית - נוצר אמנם המוגלובין תקין, אבל בכמות מופחתת מהנורמה.
המנגנון המביא לביטויי המחלה, אם נתייחס כדוגמא לבטא טלסמיה, מתחיל מהפרעה בגן המייצר את שרשרות הבטא-גלובין. כתוצאה מכך, ישנם מעט מידי עותקים של שרשרות הבטא ביחס לשרשרות האלפא. שרשרות האלפא המיותרות שוקעות בתאי האב של הכדוריות האדומות, הנורמובלסטים (Normoblasts), במח העצם. שקיעה זו של שרשרות אלפא פוגעת בממברנות התאים וגורמת למותם.
חלק מתאי האב הללו יוצרים כדוריות אדומות המגיעות למחזור הדם, אך הן דלות בהמוגלובין ומעוותות בצורתן. כדוריות אדומות אלה נהרסות בעיקר בטחול, וגם במח העצם. כתוצאה מכך, יש מיעוט כדוריות אדומות, ותתכן אנמיה קשה. הרס זה גורם גם להגדלת הטחול.
קליניקה
בבטא תלסמיה ישנם 2 מצבי מחלה עיקריים:
- נשאים לתלסמיה - אצלם רק אחד האללים (Alleles) הוא פתולוגי. התסמינים הקליניים שלהם קלים.
- הומוזיגוטים לתלסמיה - קיבלו גן פגום משני ההורים. אצלם ההסתמנות היא של בטא תלסמיה גדולה (Thalassemia major), הנקראת גם אנמיית קולי (Cooly's anemuia).
מדובר במחלה קשה: ההרס המוגבר של הכדוריות האדומות גורם לצהבת, אבני מרה, אנמיה קשה והיפוקסיה (Hypoxia).
גוף החולה מנסה ליצור פיצוי להיפוקסיה: בניסיון ליצור יותר תאי דם, ישנה גדילה של מח העצם ופלישה שלו לאזורים אחרים. הדבר מביא לשינויים בעצמות ויצירת דם חוץ-לשדית (Extramedullary hematopoiesis) - יצירת דם באיברים בהם בדרך כלל אין יצירת דם.
החולים זקוקים לעירויי דם חוזרים כדי להתקיים; הדבר מביא לצבירת ברזל, השוקע באיברים שונים של הגוף (לב, כבד, לבלב), ובכך גורם לסיבוכים נוספים.
סיבוכים
סיבוכים מהמחלה עצמה:
- עקב נסיון לייצור תאי דם בעצמות שונות, כמו בגולגולת, מתפתח מראה טיפוסי: עצמות הלחיים והמצח מאוד בולטות. הדבר נגרם מכך שהלשד (Medulla) של עצם הגולגולת עובר גדילת-יתר (Hypertrophy) - ישנה התרחבות של מח העצם (Bone marrow expansion).
- הגדלת טחול וכבד (Hepatosplenomegaly), בגלל הרס דם מוגבר (hemolysis Increased) וייצור דם באיברים אלה.
סיבוכים מעירויי דם:
- סיכון להידבקות במחלות זיהומיות (דלקת כבד נגיפית, למשל).
- העמסת ברזל , המוכרומטוזיס (Hemochromatosis): בכל מנת דם ישנה כמות ברזל לא מבוטלת. עקב חוסר מנגנונים יעילים להיפטר מעודף הברזל, עודף הברזל שוקע באיברים שונים וגורם לנזק רב. שקיעה בכבד תביא לבסוף לשחמת הכבד (Cirrhosis).
הברזל שוקע גם בלב וגורם למחלת שריר לב (קרדיומיופתיה, Cardiomyopathy) קשה, המובילה לאי ספיקת לב, העלולה לגרום למוות.
הברזל שוקע גם באיברי הפרשה פנימית (Endocrine organs) כמו הלבלב, בלוטת התריס ויותרת בלוטת התריס (Parathyroid). בעקבות כך ייתכנו סוכרת, עיכוב בגדילה וצורך בטיפול הורמונלי חלופי (Hormone replacement therapy).
אבחנה
אבחון נשאים (הטרוזיגוטיים): לאבחון טלסמיה – נעזרים במדדים המתקבלים בספירת הדם מבחינת רמת ההמוגלובין, נפח הכדוריות האדומות וריכוזיותן. בנוסף לכך- נהוג לעשות בדיקה שנקראת המוגלובין אלקטרופורסיס-המודדת את תת הסוגים השונים של ההמוגלובין באותו אדם.
בבטא טלסמיה - גודל הכדוריות האדומות ומידת הריכוזיות שלהן - מופחתות (MCV ו-MCH נמוכים). בנוסף- ישנה רמה עודפת של ההמוגלובין A2 (באדם נורמלי הוא מהווה פחות מ-3.5% מכלל ההמוגלובין). דבר זה נובע מכך שעקב העודף היחסי בשרשרות האלפא גלובין, והן מתחברות לשרשרות דלתא (ליצירת אלפא2דלתא2= HbA2).
באלפא טלסמיה - הדבר היחידי שמחשיד לכך הוא נוכחות כדוריות דם קטנות - לפי מדדי ה-MCV – (הנמדד ביחידות נפח fL אם הוא מתחת ל-78 הממצא מחשיד), וה-MCH (mean corpuscular Hb - אם הוא מתחת ל-26 פיקוגראם -הממצא מחשיד). אין דרכים יותר מדויקות מלבד אנליזה גנטית של DNA.
אבחון הומוזיגוטיים אבחון בטא טלסמיה major יותר קל מאחר והמחלה מתבטאת באנמיה קשה, כבר בשלבי החיים הראשונים, והילדים נזקקים לעירויי דם בשלבים מוקדמים.
טיפול
בנשאים של טלסמיה מינור - יש צורך בעיקר במעקב, ייעוץ ואיבחון טרום לידתי. כמו כן תמיכה במצבים בהם יש ירידה נוספת בהמוגלובין, כמו הריון.
הדבר החשוב הוא לעשות איבחון טרום לידתי בהריון של שני הורים נשאים. במדינות בהן הטלסמיה שכיחה לא ניתן לקבל רישיון נישואין אם שני בני הזוג לא עברו בדיקת סקר לטלסמיה. אם 2 ההורים נשאים- ניתן לעשות איבחון טרום לידתי של העובר ובמקרה שהוא חולה- ניתן לבצע הפסקת הריון.
חולים בטלסמיה מאג'ור
יש צורך בטיפול בעירויי דם, אחת למספר שבועות, במשך כל החיים.
בנוסף לכך ניתן טיפול לספיחת הברזל העודף והוצאתו מהגוף (Iron chelation); בעבר הטיפול העיקרי היה על ידי מתן Desferal (Deferoxamine mesylate) בזריקות תת עוריות. במשך הזמן פותחו תכשירים פומיים, כמו ה-L1, הידוע גם בשם Deferiprone, שהיה הרבה יותר נוח לשימוש עבור המטופלים. לאחרונה פותח תכשיר בשם Exjade (Deferasirox), הניתן דרך הפה ונחשב מאד יעיל.
במהלך המעקב מטפלים גם בסיבוכי המחלה ובסיבוכי שקיעת הברזל, בהפרעות ההורמונליות (היפותירואידיזם והיפופאראתירואידיזם), בעיכוב בגדילה ובפגיעה בהתפתחות המינית.
הפיתרון הסופי היחיד הוא השתלת מח עצם.
פרוגנוזה
דגלים אדומים
ביבליוגרפיה
- Joly P, Lacan P, Garcia C, Couprie N, Francina A. Identification and molecular characterization of four new large deletions in the beta-globin gene cluster. Blood Cells Mol Dis. Mar 6 2009;[Medline].
- Nemeth E. Targeting the hepcidine-ferroportin axis in the diagnosis and treatment of anemias. Adv Hematol. 2010;[Medline].
- Deborah Chirnomas S, Geukes-Foppen M, Barry K, et al. Practical implications of liver and heart iron load assessment by T2*-MRI in children and adults with transfusion-dependent anemias. Am J Hematol. Oct 2008;83(10):781-3. [Medline].
- Hankins JS, McCarville MB, Loeffler RB, et al. R2* magnetic resonance imaging of the liver in patients with iron overload. Blood. Mar 4 2009;[Medline].
- Lucarelli G, Galimberti M, Polchi P, et al. Marrow transplantation in patients with thalassemia responsive to iron chelation therapy. N Engl J Med. Sep 16 1993;329(12):840-4. [Medline].
- Gharagozloo M, Bagherpour B, Tahanian M, et al. Premature senescence of T lymphocytes from patients with beta-thalassemia major. Immunol Lett. Jan 29 2009;122(1):84-8. [Medline].
- Ghaffari J, Vahidshahi K, Kosaryan M, Parvinnejad N, Mahdavi M, Karami H. Nitroblue tetrazolium test in patients with beta-thalassemia major. Saudi Med J. Nov 2008;29(11):1601-5. [Medline].
- Davison SM, Kelly DA. Management strategies for hepatitis C virus infection in children. Paediatr Drugs. 2008;10(6):357-65. [Medline].
- Finkenstedt A, Bianchi P, Theurl I, et al. Regulation of iron metabolism through GDF15 and hepcidin in pyruvate kinase deficiency. Br J Haematol. Mar 2009;144(5):789-93. [Medline].
- Cappellini MD. Long-term efficacy and safety of deferasirox. Blood Rev. Dec 2008;22 Suppl 2:S35-41. [Medline].
- Agarwal MB. Deferasirox: oral, once daily iron chelator--an expert opinion. Indian J Pediatr. Feb 2010;77(2):185-91. [Medline].
- Bauters T, Mondelaers V, Robays H, Hunninck K, de Moerloose B. Gastric ulcer in a child treated with deferasirox. Pharm World Sci. Apr 2010;32(2):112-3. [Medline].
- Marktel S, Napolitano S, Zino E, et al. Platelet transfusion refractoriness in highly immunized beta thalassemia children undergoing stem cell transplantation. Pediatr Transplant. Jan 7 2010;[Medline].
- Noe A, Cappelli B, Biffi A, et al. High incidence of severe cyclosporine neurotoxicity in children affected by haemoglobinopaties undergoing myeloablative haematopoietic stem cell transplantation: early diagnosis and prompt intervention ameliorates neurological outcome. Ital J Pediatr. Feb 6 2010;36(1):14. [Medline].
- Italia KY, Jijina FF, Merchant R, et al. Effect of hydroxyurea on the transfusion requirements in patients with severe HbE-beta-thalassaemia: a genotypic and phenotypic study. J Clin Pathol. Feb 2010;63(2):147-50. [Medline].
- Saewong T, Ounjaijean S, Mundee Y, et al. Effects of Green Tea on Iron Accumulation and Oxidative Stress in Livers of Iron-Challenged Thalassemic Mice. Med Chem. Mar 11 2010;[Medline].
- Koren A, Levin C, Dgany O, et al. Response to hydroxyurea therapy in beta-thalassemia. Am J Hematol. May 2008;83(5):366-70. [Medline].
- Karimi M, Borzouee M, Mehrabani A, Cohan N. Echocardiographic finding in beta-thalassemia intermedia and major: absence of pulmonary hypertension following hydroxyurea treatment in beta-thalassemia intermedia. Eur J Haematol. Mar 2009;82(3):213-8. [Medline].
- Geffner ME, Karlsson H. Use of recombinant human growth hormone in children with thalassemia. Horm Res. Jan 2009;71 Suppl 1:46-50. [Medline].
- [Guideline] Langlois S, Ford JC, Chitayat D, et al. Carrier screening for thalassemia and hemoglobinopathies in Canada. J Obstet Gynaecol Can. Oct 2008;30(10):950-71. [Medline].
- Cowan RS. Moving up the slippery slope: mandated genetic screening on Cyprus. Am J Med Genet C Semin Med Genet. Feb 15 2009;151C(1):95-103. [Medline].
- Srivorakun H, Fucharoen G, Sae-Ung N, Sanchaisuriya K, Ratanasiri T, Fucharoen S. Analysis of fetal blood using capillary electrophoresis system: a simple method for prenatal diagnosis of severe thalassemia diseases. Eur J Haematol. Feb 17 2009;[Medline].
- Winichagoon P, Svasti S, Munkongdee T, et al. Rapid diagnosis of thalassemias and other hemoglobinopathies by capillary electrophoresis system. Transl Res. Oct 2008;152(4):178-184. [Medline].
- Yi P, Chen Z, Yu L, et al. Development of a PCR/LDR/capillary electrophoresis assay with potential for the detection of a beta-thalassemia fetal mutation in maternal plasma. J Matern Fetal Neonatal Med. Feb 1 2010;[Medline].
- Barnett CF, Hsue PY, Machado RF. Pulmonary hypertension: an increasingly recognized complication of hereditary hemolytic anemias and HIV infection. JAMA. Jan 23 2008;299(3):324-31. [Medline].
- Morris CR, Gladwin MT, Kato GJ. Nitric oxide and arginine dysregulation: a novel pathway to pulmonary hypertension in hemolytic disorders. Curr Mol Med. Nov 2008;8(7):620-32. [Medline].
- El-Beshlawy A, Youssry I, El-Saidi S, et al. Pulmonary hypertension in beta-thalassemia major and the role of L-carnitine therapy. Pediatr Hematol Oncol. Dec 2008;25(8):734-43. [Medline].
- Metarugcheep P, Chanyawattiwongs S, Srisubat K, Pootrakul P. Clinical silent cerebral infarct (SCI) in patients with thalassemia diseases assessed by magnetic resonance imaging (MRI). J Med Assoc Thai. Jun 2008;91(6):889-94. [Medline].
- Parker TM, Ward LM, Johnston DL, Ventureya E, Klaassen RJ. A case of Moyamoya syndrome and hemoglobin E/beta-thalassemia. Pediatr Blood Cancer. Mar 2009;52(3):422-4. [Medline].
- Goldschmidt N, Spectre G, Brill A, et al. Increased platelet adhesion under flow conditions is induced by both thalassemic platelets and red blood cells. Thromb Haemost. Nov 2008;100(5):864-70. [Medline].
- Singer ST, Ataga KI. Hypercoagulability in sickle cell disease and beta-thalassemia. Curr Mol Med. Nov 2008;8(7):639-45. [Medline].
- Fung EB, Harmatz PR, Lee PD, et al. Increased prevalence of iron-overload associated endocrinopathy in thalassaemia versus sickle-cell disease. Br J Haematol. Nov 2006;135(4):574-82. [Medline].
- Delvecchio M, Cavallo L. Growth and endocrine function in thalassemia major in childhood and adolescence. J Endocrinol Invest. Jan 2010;33(1):61-8. [Medline].
- Poggi M, Pascucci C, Monti S, et al. Prevalence of Growth hormone (GH) Deficiency in Adult polytransfused betaThalassaemia patients (TM) and correlation with Transfusional and Chelation Parameters. J Endocrinol Invest. Feb 15 2010;[Medline].
- De Sanctis V, Borsari G, Brachi S, Govoni M, Carandina G. Spermatogenesis in young adult patients with beta-thalassaemia major long-term treated with desferrioxamine. Georgian Med News. Mar 2008;74-7. [Medline].
- Karabulut A, Balci Y, Demirlenk S, Semiz S. Gonadal dysfunction and pelvic sonographic findings in females with thalassaemia major. Gynecol Endocrinol. Apr 2010;26(4):307-10. [Medline].
- Atichartakarn V, Angchaisuksiri P, Aryurachai K, et al. In vivo platelet activation and hyperaggregation in hemoglobin E/beta-thalassemia: a consequence of splenectomy. Int J Hematol. Apr 2003;77(3):299-303. [Medline].
- Aypar E, Alehan D, Hazirolan T, Gumruk F. The efficacy of tissue Doppler imaging in predicting myocardial iron load in patients with beta-thalassemia major: correlation with T2* cardiovascular magnetic resonance. Int J Cardiovasc Imaging. Apr 2010;26(4):413-21. [Medline].
- Beutler E, Hoffbrand AV, Cook JD. Iron deficiency and overload. Hematology (Am Soc Hematol Educ Program). 2003;40-61. [Medline].
- Borgna-Pignatti C, Vergine G, Lombardo T, et al. Hepatocellular carcinoma in the thalassaemia syndromes. Br J Haematol. Jan 2004;124(1):114-7. [Medline].
- Cao A, Rosatelli C, Galanello R, et al. The prevention of thalassemia in Sardinia. Clin Genet. Nov 1989;36(5):277-85. [Medline].
- Cappellini MD, Cohen A, Piga A, et al. A phase 3 study of deferasirox (ICL670), a once-daily oral iron chelator, in patients with beta-thalassemia. Blood. May 1 2006;107(9):3455-62. [Medline].
- Cario H, Janka-Schaub G, Janssen G, et al. Recent developments in iron chelation therapy. Klin Padiatr. May-Jun 2007;219(3):158-65. [Medline].
- Centis F, Tabellini L, Lucarelli G, et al. The importance of erythroid expansion in determining the extent of apoptosis in erythroid precursors in patients with beta-thalassemia major. Blood. Nov 15 2000;96(10):3624-9. [Medline].
- Chakravarti A, Verma V, Kumaria R, Dubey AP. Anti HCV seropositivity among multi transfused patients with beta-thalassemia. J indian Med Assoc. 2005;103(2):64-66. [Medline].
- Christoforidis A, Haritandi A, Tsatra I, et al. Four-year evaluation of myocardial and liver iron assessed prospectively with serial MRI scans in young patients with beta-thalassaemia major: comparison between different chelation regimens. Eur J Haematol. Jan 2007;78(1):52-7. [Medline].
- Cunningham MJ, Macklin EA, Neufeld EJ, et al. Complications of beta-thalassemia major in North America. Blood. Jul 1 2004;104(1):34-9. [Medline].
- De Virgiliis S, Cossu P, Toccafondi C, et al. Effect of subcutaneous desferrioxamine on iron balance in young thalassemia major patients. Am J Pediatr Hematol Oncol. Spring 1983;5(1):73-7. [Medline].
- dos Santos CO, Costa FF. AHSP and beta-thalassemia: a possible genetic modifier. Hematology. 2005;10(2):57-61. [Medline].
- Economou M, Printza N, Teli A, et al. Renal dysfunction in patients with beta-thalassemia major receiving iron chelation therapy either with deferoxamine and deferiprone or with deferasirox. Acta Haematol. 2010;123(3):148-52. [Medline].
- Fucharoen S, Ketvichit P, Pootrakul P, et al. Clinical manifestation of beta-thalassemia/hemoglobin E disease. J Pediatr Hematol Oncol. Nov-Dec 2000;22(6):552-7. [Med Gardenghi S, Marongiu MF, Ramos P, et al. Ineffective erythropoiesis in beta-thalassemia is characterized by increased iron absorption mediated by down-regulation of hepcidin and up-regulation of ferroportin. Blood. Jun 1 2007;109(11):5027-35. [Medline].
- Gilman JG, Huisman TH, Abels J. Dutch beta 0-thalassaemia: a 10 kilobase DNA deletion associated with significant gamma-chain production. Br J Haematol. Feb 1984;56(2):339-48. [Medline].
- Haldane JBS. The rate of mutation of human genes. In: Proceedings of the VIII International Congress on Genetics and Heredity. 1949;267.
- Hershko C, Weatherall DJ. Iron-chelating therapy. Crit Rev Clin Lab Sci. 1988;26(4):303-45. [Medline].
- Kazazian HH Jr. The thalassemia syndromes: molecular basis and prenatal diagnosis in 1990. Semin Hematol. Jul 1990;27(3):209-28. [Medline].
- Kazazian HH Jr, Boehm CD. Molecular basis and prenatal diagnosis of beta-thalassemia. Blood. Oct 1988;72(4):1107-16. [Medline].
- Kontoghiorghes GJ. Deferasirox: uncertain future following renal failure fatalities, agranulocytosis and other toxicities. Expert Opin Drug Saf. May 2007;6(3):235-9. [Medline].
- Lilleyman JS, Hann IM, Blanchette V. The thalassemia. Pediatr Hematol. 2000;307-327.
- Lorey F. Asian immigration and public health in California: thalassemia in newborns in California. J Pediatr Hematol Oncol. Nov-Dec 2000;22(6):564-6. [Medline].
- Mentzer WC Jr. Differentiation of iron deficiency from thalassaemia trait. Lancet. Apr 21 1973;1(7808):882. [Medline].
- Mohkam M, Shamsian BS, Gharib A, Nariman S, Arzanian MT. Early markers of renal dysfunction in patients with beta-thalassemia major. Pediatr Nephrol. Jun 2008;23(6):971-6. [Medline].
- Nagel RL, Roth EF Jr. Malaria and RBC genetic defects. Blood. Sep 1989;74(4):1213-21. [Medline].
- Nathan DG, Gunn RB. Thalassemia: the consequences of unbalanced hemoglobin synthesis. Am J Med. Nov 1966;41(5):815-30. [Medline].
- Nathan DG, Oski FA. The thalassemia. In: Hematology of Infancy and Childhood. Vol 1. Philadelphia, Pa: WB Saunders Co;1998:783-879, 811-886.
- Nick H, Acklin P, Lattmann R, et al. Development of tridentate iron chelators: from desferrithiocin to ICL670. Curr Med Chem. Jun 2003;10(12):1065-76. [Medline].
- Olivieri NF, Brittenham GM, Matsui D, et al. Iron-chelation therapy with oral deferipronein patients with thalassemia major. N Engl J Med. Apr 6 1995;332(14):918-22. [Medline].
- Origa R, Galanello R, Ganz T, et al. Liver iron concentrations and urinary hepcidin in beta-thalassemia. Haematologica. May 2007;92(5):583-8. [Medline].
- Orkin SH, Kazazian HH Jr. The mutation and polymorphism of the human beta-globin gene and its surrounding DNA. Annu Rev Genet. 1984;18:131-71. [Medline].
- Pakbaz Z, Fischer R, Fung E, et al. Serum ferritin underestimates liver iron concentration in transfusion independent thalassemia patients as compared to regularly transfused thalassemia and sickle cell patients. Pediatr Blood Cancer. Sep 2007;49(3):329-32. [Medline].
- Pakpaz FR, Fung E, Harmatz P. Serum ferritin underestimates the liver iron concentration. Pediatric Blood and Cancer. 2004;42:497.
- Pan LL, Eng HL, Kuo CY, et al. Usefulness of brilliant cresyl blue staining as an auxiliary method of screening for alpha-thalassemia. J Lab Clin Med. Feb 2005;145(2):94-7. [Medline].
- Peters TJ, Raja KB, Simpson RJ, Snape S. Mechanisms and regulation of intestinal iron absorption. Ann N Y Acad Sci. 1988;526:141-7. [Medline].
- Piomelli S, Danoff SJ, Becker MH, et al. Prevention of bone malformations and cardiomegaly in Cooley's anemia by early hypertransfusion regimen. Ann N Y Acad Sci. Nov 20 1969;165(1):427-36. [Medline].
- Pippard MJ, Callender ST, Weatherall DJ. Intensive iron-chelation therapy with desferrioxamine in iron-loading anaemias. Clin Sci Mol Med. Jan 1978;54(1):99-106. [Medline].
- Premawardhena A, Fisher CA, Fathiu F, et al. Genetic determinants of jaundice and gallstones in haemoglobin E beta thalassaemia. Lancet. Jun 16 2001;357(9272):1945-6. [Medline].
- Reich S, Buhrer C, Henze G, et al. Oral isobutyramide reduces transfusion requirements in some patients with homozygous beta-thalassemia. Blood. Nov 15 2000;96(10):3357-63. [Medline].
- Ross J, Pizarro A. Human beta and delta globin messenger RNAs turn over at different rates. J Mol Biol. Jul 5 1983;167(3):607-17. [Medline].
- Roy CN, Enns CA. Iron homeostasis: new tales from the crypt. Blood. Dec 15 2000;96(13):4020-7. [Medline].
- Singer ST, Wu V, Mignacca R, et al. Alloimmunization and erythrocyte autoimmunization in transfusion- dependent thalassemia patients of predominantly asian descent. Blood. Nov 15 2000;96(10):3369-73. [Medline].
- Tanner MA, Galanello R, Dessi C, et al. A randomized, placebo-controlled, double-blind trial of the effect of combined therapy with deferoxamine and deferiprone on myocardial iron in thalassemia major using cardiovascular magnetic resonance. Circulation. Apr 10 2007;115(14):1876-84. [Medline].
- Thein SL. Dominant beta thalassaemia: molecular basis and pathophysiology. Br J Haematol. 1992;80(3):273-7. [Medline].
- Vichinsky EP. Reports of proceedings: 1999 international conference on E-Beta thalassemia. J Pediatr Hematol Oncol. 2000;22:6:550.
- Voskaridou E, Terpos E, Spina G, et al. Pamidronate is an effective treatment for osteoporosis in patients with beta-thalassaemia. Br J Haematol. Nov 2003;123(4):730-7. [Medline].
- Weatherall DJ. Thalassemia. In: Stamatoyannopoulos G et al, eds. The Molecular Basis of Blood Diseases. 1944:157-206.
- Weatherall DJ. Thalassemia. In: The Thalassemia Syndromes. 1981.
- Wintrobe MM, Mathews E. Familial hematopoietic disorder in Italian adolescents and adults resembling Mediterranean disease (thalassemia). JAMA. 1940;114:1530-4.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר מוטי חיימי, מומחה ברפואת ילדים, המטולוגיה ואונקולוגיה פדיאטרית, חבר באיגוד הישראלי להמטואונקולוגיה ילדים ועובד במרכז לבריאות הילד ארמון של הכללית בחיפה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק