הבדלים בין גרסאות בדף "הקומפלקס פירובט דהידרוגנאז - pyruvate dehydrogenase"
| שורה 112: | שורה 112: | ||
בדיקה זו אינה מתבצעת כבדיקה קדם-לידתית בעובר והדגימה הנדרשת היא רקמה הנלקחת בביופסיה. ניתן לבצע את הבדיקה באחד מהדגימות הבאות: | בדיקה זו אינה מתבצעת כבדיקה קדם-לידתית בעובר והדגימה הנדרשת היא רקמה הנלקחת בביופסיה. ניתן לבצע את הבדיקה באחד מהדגימות הבאות: | ||
*פיברובלסטים שגודלו בתרבית וממלאים במלואה צלוחית T-25 או T-75. עדיף שהצלוחית תגיע למעבדה בקירור, אך ניתן גם להעבירה בטמפרטורת החדר, תוך פחות מ-24 שעות. | *פיברובלסטים שגודלו בתרבית וממלאים במלואה צלוחית T-25 או T-75. עדיף שהצלוחית תגיע למעבדה בקירור, אך ניתן גם להעבירה בטמפרטורת החדר, תוך פחות מ-24 שעות. | ||
| − | *נטילת ביופסיה מהעור ( | + | *נטילת ביופסיה מהעור (mm punch{{כ}}-4) ולהעביר את הביופסיה בקירור (מועדף) או בטמפרטורת החדר במהירות האפשרית. |
כאשר מגדלים פיברובלסטים בתרבית ניתן להשתמש בכל מדיום סטנדרטי (Eagle's minimal essential media, RPMI 1640). המדיום צריך להכיל 1% פניצילין וסטרפטומיצין. שיטת הבדיקה אנזימטית קולורימטרית. | כאשר מגדלים פיברובלסטים בתרבית ניתן להשתמש בכל מדיום סטנדרטי (Eagle's minimal essential media, RPMI 1640). המדיום צריך להכיל 1% פניצילין וסטרפטומיצין. שיטת הבדיקה אנזימטית קולורימטרית. | ||
גרסה מ־13:26, 16 באפריל 2017
| מדריך בדיקות מעבדה | |
| הקומפלקס פירובט דהידרוגנאז | |
|---|---|
| pyruvate dehydrogenase | |
| שמות אחרים | PDC או Pyruvate Dehydrogenase Complex |
| |
| מעבדה | כימיה בדם |
| תחום | הערכה של חסר האנזים בתינוקות, ילדים ובוגרים עם חשד למפגע אנזימטי מטבולי. |
| טווח ערכים תקין | ערך תקין כאשר פעילות האנזים עולה על 25.0 nmol/min/g protein; רמה גבולית או רמת חסר קלה- 5.0-25.0nmol/min/g protein; רמת חסר של האנזים-פחות מ- 5/0nmol/min/g protein. רמות אלה מתייחסות לכל הגילים. |
| יוצר הערך | פרופ' בן-עמי סלע |
- מטרת הבדיקה
הערכה של נבדקים עם חשד קליני לחסר pyruvate dehydrogenase complex, או של מפגע במטבוליזם האנרגטי.
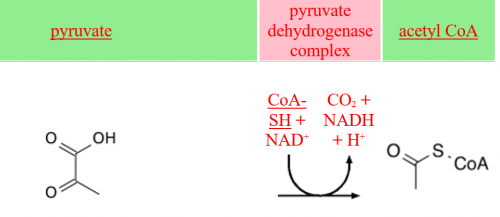
הקומפלקס פירובאט דהידרוגנאזה pyruvate dehydrogenase complex (להלן PDC) מקטלז את הדקרבוקסילציה החימצונית של פירובאט ל-acetyl-CoA, שהוא שלב קריטי ביצירת אנרגיה תאית. PDC הוא קומפלקס רב-אנזימי הממוקם בממברנה הפנימית של המיטוכונדריה, ומורכב מ-6 מרכיבים שונים: pyruvate decarboxylase שסימונו E1, והוא בנוי מ-2 תת יחידות α ו-2 תת-יחידות β; dihydrolipoic transacetylase שסימונו E2; האנזים dihydrolipoyl dehydrogenase שסימונו E3; שני אנזימים רגולטוריים (PDH kinase ו- PDH phosphatase) וכן חלבון קושר-E3 הידוע כ-E3BP. חסר של PDHC הוא מפגע מיטוכונדריאלי עם מגוון של תסמינים קליניים החל מ-lactic acidosis מולדת קטלנית וכלה בשיגשון (ataxia) או נירופתיה מתונים.
הקומפלקס של פירובאט דהידרוגנאזה מחבר בין הגליקוליזה למעגל TCA (הידוע כמעגל Krebs או מעגל חומצת הלימון). קומפלקס גדול זה מורכב מ-3 אנזימים הנתמכים על ידי 5 קו-פקטורים. תהליך החמצון של פירובאט מתרחש במיטוכונדריה לשם האחרון מגיע על ידי pyruvate translocase. האנזים E1 או Pyruvate dehydrogenase עושה שימוש ב-thiamine pyrophosphate (או TPP) כקבוצה הפרוסתטית שלו; האנזים E2 או dihydrolipoyl transacetylase עושה שימוש ב-lipoamide וב- coenzyme A כקבוצות הפרוסתטיות שלו; האנזים E3 או dihydrolipoyl dehydrogenase עושה שימוש ב-flavin adenine dinucleotide או +NAD כקו-פקטור שלו. קבוצה פרוסתטית היא מולקולה הקשורה קו-ולנטית לאנזים. נראה אם כן שהריאקציה המסבה פירובאט לאצטיל CoA ול- CO2 היא:
- 2pyruvate+2NAD++2coA→ 2acetyl coA+ 2NADH+2CO2
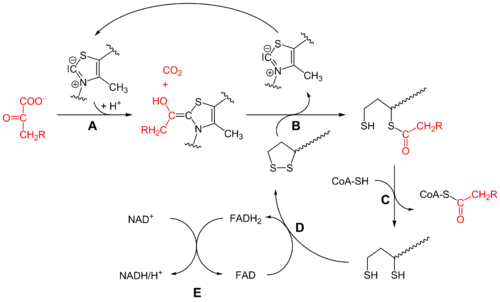
התהליך בכללותו הוא 5-שלבי:
- פירובאט עובר דקרבוקסילציה על ידי pyruvate dehydrogenase בעזרת TPP;
- הפחמן הפעיל בין N ו-S של הטבעת המחומשת של TPP מחומצן ומועבר כקבוצת אצטיל ל-lipoamide (המהווה קבוצה פרוסתטית של האנזים dihydrolipoyl transacetylase או E2. צעד זה יוצר תוצר ביניים של hydroxyethyl-TPP. נדרש כאן יון +H לתוצר הביניים לשחרר מולקולת CO2;
- dihydrolipoyl transacetylase והקופקטור lipoamide מחמצן hydroxyethyl לאצטיל, ואז מעביר אצטיל ל-CoA ליצירת acetyl-CoA;
- כיוון שהאנזים E2 עדיין קשור למולקולת acetyl-CoA, האנזים E3 או dihydrolipoyl dehydrogenase מחמצן את קבוצות ה-thiol של dihydrolipoamide בחזרה ל-lipoamide;
- כריאקציה צדדית, +NAD מחוזר והופך ל-NADH.
חסר של הקומפלקס של פירובאט דהידרוגנזאה
בתינוקות ובילדים עם חסר PDC, המאפיינים השכיחים ביותר הם פיגור התפתחותי והיפוטוניה. פרכוסים ואטקסיה גם כן תסמינים שכיחים, כאשר התבטאויות פחות שכיחות כוללת עיוותי מוח מולדים, בעיקר הרחבת חדרים (ventriculomegaly) או agenesis של הקורפוס קלוסום, או שינוים ניווניים הכוללים את תסמונת Leigh (Brown וחב' ב-Ann NY Acad Sci משנת 2003). בחלק קטן של אלה עם PDHC מוצאים תווי-פנים דיסמורפיים. חסר PDHC היא אחת הסיבות השכיחות לחמצת לקטית ראשונית בילדים, כאשר חומרת התקדמות המחלה קשורה לחומרה של החמצת הלקטית כמו גם לרמה השארית של הפעילות האנזימטית (Patel וחב' ב-Mol Genet Metab משנת 2012).
חסר PDC יכול להיגרם על ידי ליקויים בתת היחידות E1 α, E1 β, וכן E2 או E3. הסיבה השכיחה ביותר לחסר PDC הוא פגם בגן המקודד לתת היחידה E1 α, גן הממוקם על כרומוזום X. נקבות וזכרים עם המוטציה בגן E1 α, לוקים בחסר PDC, לכן הפגם מוגדר כ-X-linked dominant. הבדיקה האבחונית ההתחלתית החשובה ביותר היא המדידה בדם ובנוזל השדרה של רמות חומצה לקטית ופירובאט, וכן חישוב היחס לקטאט ל-פירובאט (L:P ratio), כאשר באופן אופייני מצביעה על רמות מוגברות של לקטאט ופירובאט, כאשר היחס בין השניים נורמאלי (Lib וחב' ב-Anal Chem משנת 2003). בנוסף, אנליזה כמותית של חומצות אמינו בפלזמה יכולה למצוא רמת אלנין מוגברת. האבחון של חסר PDC תלוי במדידה של פעילות הנזים בתאים או ברקמות, בעיקר בפיברובלסטים הלקוחים מהעור (Dahl ב-Am J Hum Genet משנת 1995).
חסר ב-pyruvate dehydrogenase מתאפיין בהצטברות של חומצת חלב ומגוון של בעיות נירולוגיות. סימנים ותסמינים של מצב זה בדרך כלל מופיעים מיד לאחר הלידה, בדרגות חומרה שונות. המאפיין השכיח ביותר הוא אמנם תרחיש של lactic acidosis שעלול אף לסכן חיים, שיכול לגרום לבחילה, הקאות, בעיות נשימה קשות וקצב-לב בלתי תקין. אלה עם חסר ב-pyruvate dehydrogenase, סובלים בדרך כלל מבעיות נירולוגיות, רובם סובלים מהתפתחות מעוכבת ביכולות המנטאליות ובכישורים מוטוריים כמו ישיבה והליכה. בעיות נירולוגיות נוספות הן ברמה האינטלקטואלית, פירכוסים, היפוטוניה, תנועות עיניים בלתי סדירות, קואורדינציה דלה, ובחלקם מוצאים מבנים מוחיים לא-נורמאליים כמו התפתחות דלה של ה-corpus callosum המחבר את חצאי המוח הימני והשמאלי, אטרופיה של החלק החיצוני של קליפת המוח, וכן נגעים של רקמה פגועה בחלקי מוח שונים.
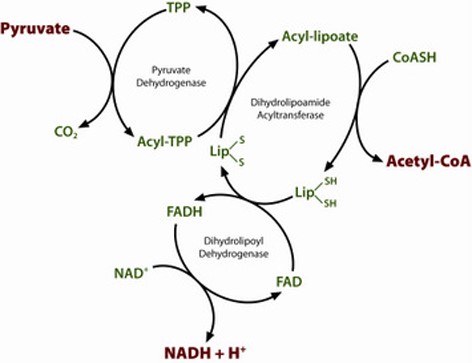
תהליך 5 השלבים של קומפלקס PDH
בתחילה, פירובאט ו-thiamine pyrophosphate או TPP, נקשרים על ידי תת היחידות של pyruvate dehydrogenase. טבעת ה-thiazolium של TPP נמצאת בצורה הצוויטריונית, והפחמן האניוני C2 מבצע התקפה נוקלאופילית על הקטון הקרבונילי C2 של פירובאט. תוצר הביניים ה-hemithioacetal עובר דקרבוקסילציה ליצירה של שווה-ערך של acyl anion, והאחרון תוקף את שייר S1 של lipoate מחומצן, הקשור לשייר lysine.
במנגנון של "פתיחת טבעת" דמוי SN2, שייר S2 מוחלף על ידי שיירי סולפיד או סולפהידריל. כתוצאה מכך ההתפרקות של ה-hemithioacetal הטטרהדראלי גורם לפליטת thiazole, לשחרור של הקו-פקטור TPP וליצירה של thioacetate על שייר S1 של lipoate. התהליך האנזימטי המקוטלז על ידי E1 הוא השלב ה-rate limiting של כל הקומפלקס של pyruvate dehydrogenase.
בשלב זה ה-lipoate-thioester מועבר לאתר הפעיל של dihydrolipoyl transacetylase או E2, שם ריאקציית טרנסאצילציה מעבירה שייר אצטיל ממולקולת lipoyl ל-thiol של קואנזים A. צעד זה יוצר אצטיל-CoA המשתחרר מהקומפלקס האנזימטי ונכנס למעגל חומצת הלימון. ניתן להתייחס ל-E2 כאל lipoamide reductase-transacetylase.
ה-dihydrolipoate שעדיין קשור לשייר הליזין של הקומפלקס, נודד אז לאתר הפעיל של E3 או dihydrolipoyl dehydrogenase שם הוא עובר חמצון בתיווך של flavin. בראשונה, FAD מחמצן dihydrolipoate בחזרה למצב המנוחה של ה-lipoate ומייצר FADH2. ואז, הקו-פקטור +NAD מחמצן FADH2 בחזרה למצב המנוחה של FAD, תוך שהוא מייצר NADH.
היבטים מבניים באאוקריוטים ובחיידקים גראם-חיוביים
באאוקריוטים, אך גם בחיידקים גראם-חיוביים (כמו Bacillus stearothermophilus) הגרעין המרכזי של PDC מכיל 60 מולקולות E2 המאורגנות ל-icosahedron (מבנה בעל 20 פאות). אאוקריוטים מכילים גם כן בגרעין של PDC עוד 12 עותקים של חלבון נוסף, E3BP או E3 binding protein. המיקום המדויק של החלבון האחרון אינו לגמרי ברור. באאוקריוטים, E1 נקשר באופן ספציפי על ידי E2, בעוד ש-E3 כרוך עם E3BP. יש סברה שעד 30 מולקולות E1 ו-6 מולקולות E3 נמצאות בקומפלקס של PD, אם כי המספר המדויק יכול להשתנות in vivo ולשקף את הדרישות המטבוליות של הרקמה הספציפית.
רגולציה של פעילות הקומפלקס
תפקוד ומבנה של PDH
הקומפלקס Pyruvate Dehydrogenase מקשר את מעגל חומצת הלימון ואת הזרחון החמצוני המלווה לגליקוליזה, לגלוקונאוגנזה ולמסלולי המטבוליזם של שומן וחומצות אמינו. PDH מקטלז את הדקרבוקסילציה החמצונית של פירובאט ליצירת אצטיל קואנזים A, וכן NADH ו-CO2. האנזים PDH מזרז את השימוש בפחמימות כדי לספק את הדרישות האנרגטיות, וכאשר המאגרים הפחמימניים מתדלדלים ביונקים, פעילות PDH עוברת down-regulation על מנת להגביל את השימוש בגלוקוזה על ידי oxidative phosphorylation. חומצות שומן או גופי קטו משמשים אז מקורות אנרגיה ברקמות דוגמת הלב ושרירי השלד.
קומפלקס האנזים PDH הוא בגודל של 9,500,000 דלטון המורכב מעותקים רבים של שלושת האנזימים pyruvate dehydrogenase או E1, וכן dihydrolipoamide transacetylase או E2, ו-dihydrolipoamide dehydrogenase או E3. תת-יחידה מבנית נוספת הידועה כ-E2/E3, נחוצה לסייע באינטראקציה בין תת היחידות E2 ו-E3.
וויסות הפעילות של PDH
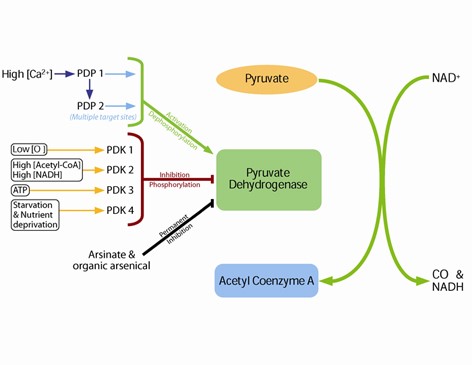
הפעילות של PDH מעוכבת על ידי זרחון הפיך של תת היחידה E1 α, בשיירים serine232, 293 serine ו-serine300. הזרחון של שיירים אלה מקוטלז על ידי ארבעת האיזופורמים של PDH kinases הידועים כ-PDK1-4. דפוספורילציה כדי לשחזר את פעילות PDH, מקוטלזת על ידי שני האנזימים PDH phosphatases המכונים PDP1 ו-PDP2. הקינאזות כמו גם הפוספטאזות באים לביטוי דיפרנציאלי ברקמות, והשעתוק שלהם מבוקר על ידי מגוון של אירועי עקה תאיים, כגון רעב, רמת חמצן נמוכה או ריכוז גבוה של NADH, אצטיל-CoA או סידן (תמונה למטה)
האנזים pyruvate dehydrogenase מעוכב כאשר אחד או יותר מהיחסים הבאים גדל: acetyl-CoA/CoA, NADH/NAD+ , ATP/ADP. באאוקריוטים PDC מבוקר באופן הדוק על ידי ה-pyruvate dehydrogenase kinase או PDK הספציפי שלו ועל ידי ה-pyruvate dehydrogenase phosphatase או PDP, המדכאים או משפעלים אותו, בהתאמה. ה-PDK מזרחן שלושה שיירי serine ספציפיים על E1 עם זיקות זרחון שונות. זרחון של כל אחד משיירים אלה הופך את E1 (ובעקבותיו את כל הקומפלקס) לבלתי פעיל. לעומת זאת, דפוספורילציה של E1 על ידי PDP משחזרת את פעילות הקומפלקס. תוצרים של הריאקציה פועלים כמעכבים אלוסטריים של PDC, שכן הם משפעלים את PDK. לעומת זאת, מצעים של הריאקציה מעכבים את PDK, וכך הם משפעלים מחדש את PDC.
בשעת צום, PDK גדל בכמותו ברוב הרקמות, כולל שריר השלד, על ידי הגברה של שעתוק גני. תחת אותם תנאים, כמות PDP ברקמות פוחתת. העיכוב הנובע מכך של PDC מונע מהשריר ומרקמות אחרות לפרק גלוקוזה וקודמנים של גלוקונאוגנזה. במצב זה מטבוליזם מופנה לכיוון של ניצול שומנים, בה בשעה שיש מזעור של פירוק חלבוני שריר השלד לספק קודמנים לגלוקונאוגנזה, ואילן הגלוקוזה הזמין נשמר לצריכה על ידי המוח. לסידן יש תפקיד ברגולציה של PDC ברקמת השריר, כיוון שהוא משפעל PDP, ומעודד גליקוליזה בהשתחררו לציטוזול בשעת התכווצות השריר.
פתו-פיזיולוגיה
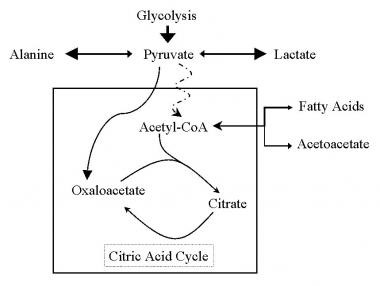
הקומפלקס pyruvate dehydrogenase מסב פירובאט לאצטיל CoA שהוא אחד משני המצעים החיוניים הנחוצים ליצירת חומצת לימון (תרשים למטה):
תרשים זה מראה את הגרסה הפשטנית של מעגל חומצת הלימון. הקו המרוסק מצביע על המסלול החסום המונע הפיכת פירובאט לאצטיל CoA. לפיכך פירובאט מופנה לשני מסלולים אחרים ליצירת לקטאט ואלנין. חסר אנזימטי זה מגביל את יצירת חומצת הלימון שהיא המצע הראשון במעגל חומצת הלימון, כך שמעגל זה נחסם. חסר רציני של קומפלקס PDH עלול לגרום לעיוותים מוחיים מולדים, כתוצאה ממחסור באנרגיה במהלך התפתחות העצבית בעובר, ולמעשה א-נורמליות מורפולוגית מתרחשת כבר לפני שבוע ההיריון ה-10. התפתחות מעוותת של ה-corpus callosum באלה עם PDC כבר בשלב העוברי.
ההתדרדרות הנירולוגית משתנה בקצב שלה ביילודים שמוחם בעת הלידה לכאורה בריא. תהליכים של תת-מיאלינציה, יצירת נגעים כיסיים במוח ותהליך של gliosis בקליפת המוח או במוחון, עם ניוון של החומר האפור או necrotizing encephalopathy, יכולים להתרחש בחלק מהלוקים ב-PDC, בה בשעה ש-gliosis של גזע המוח ושל ה-basal ganglia עם שגשוג קפילארי מתרחשים באלה עם תסמונת Leigh. ממצאים נירופתולוגיים אינם מופיעים בדרך כלל באלה עם התקף מאוחר יותר בחיים של PDC.
שכיחות PDC
השכיחות של PDC אינה ידועה, אך הסבירות היא שהיא קטנה מ-1:50,000. יחד עם זאת, השכיחות יכולה להיות גבוהה מהמשוער, כיוון שחסר אנזימטי זה אחראי באופן פוטנציאלי למקרים לא מוסברים של חמצת, פרכוסים, ועיכוב התפתחותי במקרים בהם לא מתבצע הבירור של מעורבות אפשרית של PDC, כמו גם במקרים לא מוסברים של תסמונת Leigh עם פתולוגיה של מערכת העצבים המרכזית. ידוע גם שמוטציות in-frame בגן E1 α הכרוך בכרומוזום X תוארו במקרים קלים רבים של PDC שלא נבחנו לאפשרות של החסר האחרון (Boyer ב-Concepts in Biochemistry משנת 2006).
תחלואה/תמותה
פרטים עם PDHC מהסוגים המאובחנים כיילודים או בתקופת הינקות, מתים בדרך כלל בשנות חייהם הראשונות. תחילת המחלה בשלבי ילדות מאוחרים יותר בדרך כלל כרוכה, אם כי לא תמיד, בהישרדות לתוך שנות הבגרות. כל הילדים הפגועים נולדים עם פעילות אנזים מוגבלת במידה מסוימת, כיוון שחסר מוחלט שלו אינה מאפשרת חיים כלל. אלה בגיל הינקות (infants) עם פעילות pyruvate dehydrogenase שהיא נמוכה מ-15% של פעילות האנזים התקינה אינם שורדים את תקופת הלידה. פעילות PDC הגבוהה מ-25% מערכי הנורמה כרוכה במחלה פחות חמורה ומאופיינים בדרך כלל עם ataxia, ועיכוב התפתחות פסיכו-מוטורי. מספר תרפיות עשויות להאריך את חיי אלה הלוקים בחסר רציני של PDC, אך האופי המתקדם של החסכים וההתדרדרות הנירולוגית באים לביטוי בתחלואה משמעותית.
זכרים נפגעים יותר במפגע מאשר נקבות, כיוון שהצורה השכיחה ביותר של PDC זו של האנזים E1 α היא X-linked, אם כי מספר נקבות נשאיות יכולות לסבול מתסמינים קלים. יש מגוון רחב של תסמינים צורות הרצסיביות של המחלה, אך רובם קלים יותר מאלה בצורת ה-X-linked. ל-PDC אין העדפה אתנית או גזעית. תסמונת West שכיחה יותר בקרב נקבות עם PDHC, ואילו חמצת לקטית חמורה ומוות מוקדם ותסמונת Leigh נפוצים יותר בקרב זכרים עם PDC.
אנליזה של פעילות PDH
שימוש בלתי מבוקר של גלוקוזה ושל חומצות שומן כמקורות אנרגיה נצפה לעתים קרובות בתסמונות מטבוליות כגון סוכרת והשמנת-יתר. בנוסף, תאי סרטן לרוב עוברים מתהליכי זירחון חמצוני (oxidative phosphorylation) למסלול הגליקוליזה ליצירת ATP. התפקיד המרכזי של PDH בפעילויות אלה הביא לעניין מתחדש בהבנת פעילות PDH.
כימות של רמת PDH אנדוגני ופעילות PDH מזורחן בתא ובתמציות של רקמות
המפתח למדידת פעילות PDH אנדוגני הוא לשמור על דרגת פוספורילציה in vivo. שיטת מיצוי הרקמות והשימוש בבופר מתאים לעכב אנזימי קינאזה ופוספטאזה ספציפיים ולא ספציפיים, על מנת למנוע שינויים לא-רצויים ב-PDH בתהליך הכנת פרפרט הדגימה. בשלב זה ניתן "ללכוד" את האנזים באופן אימונולוגי ולמדוד פעילותו על משטח סולידי ב- microplate עם 96 בארות, או בשיטת dipstick כאשר המקלון ספוח עם נוגדן ל-PDH. שיטות אימוניות אלו פשוטות יותר, מהירות ובטיחותיות יותר מאשר השיטה הקלאסית של שימוש ב-C]pyruvate14] ומדידת השתחררות התוצר של הקטליזה האנזימטית הלא הוא C]CO214].
פעילות PDH יכולה להיבחן בנוסף ex vivo לאחר ה-PDH immunocapture והרחקת קינאזות או פוספטאזות אנדוגניות. בשלב זה הדגימות עוברות זרחון עם אנזים PDK ריקומביננטי או עוברות דפוספורילציה עם אנזים PDP ריקומביננטי כדי לקבוע:
- פעילות שארית של PDH בצורתו המזורחנת במלואה;
- פעילות מרבית של PDH בצורתו נטולת הפוספאט במלואה;
- פעילות PDH אנדוגני ללא כל מודיפיקציה.
כימות של סך PDH ו-PDH מזורחן בתאים חיים ובתמצית רקמות
תת היחידה הרגולטורית העיקרית היא E1 α או PDH1, העוברת מודיפיקציה על ידי קינאזות הפועלות על שלושה שיירי serine כדי להפחית את פעילות האנזים. הכימות של סך פעילות תת היחידה E1 α של PDH וזו של המולקולה המזורחנת בשיירים Ser232, Ser293 ו-Ser300, יכול להתבצע בקלות על ידי שימוש במבחני sandwich ELISA. בשיטה זו ניתן למדוד את רמות החלבון והזרחון, באם הם אנדוגניים או כתוצאה מטיפול תרופתי.
מבחני ICE או In-cell ELISA יכולים לשמש למדידה של רמות האנזים לאחר מודיפקציות post-translational בתאים חיים בתרבית. היתרון של שיטת ICE הוא בכך שקיבוע מהיר של התאים בבארות של פלטת-96 בארות in situ מייצב את זרחון האנזים ומונע כל שינוי שיכול להתרחש במהלך הכנת הדגימה לבדיקה. אנליזה של תת יחידות של PDH בתאים חיים או בתמצית תאים ורקמות יכולה להתבצע על ידי Western Blot, אימונו-ציטוכימיה (ICC) או flow cytometry.
הוראות לביצוע הבדיקה:
בדיקה זו אינה מתבצעת כבדיקה קדם-לידתית בעובר והדגימה הנדרשת היא רקמה הנלקחת בביופסיה. ניתן לבצע את הבדיקה באחד מהדגימות הבאות:
- פיברובלסטים שגודלו בתרבית וממלאים במלואה צלוחית T-25 או T-75. עדיף שהצלוחית תגיע למעבדה בקירור, אך ניתן גם להעבירה בטמפרטורת החדר, תוך פחות מ-24 שעות.
- נטילת ביופסיה מהעור (mm punch-4) ולהעביר את הביופסיה בקירור (מועדף) או בטמפרטורת החדר במהירות האפשרית.
כאשר מגדלים פיברובלסטים בתרבית ניתן להשתמש בכל מדיום סטנדרטי (Eagle's minimal essential media, RPMI 1640). המדיום צריך להכיל 1% פניצילין וסטרפטומיצין. שיטת הבדיקה אנזימטית קולורימטרית.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק