הבדלים בין גרסאות בדף "טיפולים מכווני מטרה בסרטן מעי גס גרורתי"
| שורה 82: | שורה 82: | ||
יעילותן תלויה בביטוי תקין (wild-type) של חלבון KRAS, NRAS) RAS). חלבוני ^RAS הינם חלק משרשרת העברת הסיגנל שמופעל על ידי קשירת ליגנד ^EGFR. כאשר KRAS או NRAS מוטנטים (בכ-50% מהגידולים), המסלול מופעל באופן תמידי וללא תלות בקישור הליגנד לקולטן ^EGFR. לכן, בחולים בהם NRAS או KRAS מוטנטים, לא צפויה תגובה לתרופות הפועלות כנגד EGFR. | יעילותן תלויה בביטוי תקין (wild-type) של חלבון KRAS, NRAS) RAS). חלבוני ^RAS הינם חלק משרשרת העברת הסיגנל שמופעל על ידי קשירת ליגנד ^EGFR. כאשר KRAS או NRAS מוטנטים (בכ-50% מהגידולים), המסלול מופעל באופן תמידי וללא תלות בקישור הליגנד לקולטן ^EGFR. לכן, בחולים בהם NRAS או KRAS מוטנטים, לא צפויה תגובה לתרופות הפועלות כנגד EGFR. | ||
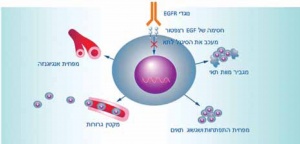
| − | + | [[קובץ:Angiogenesis2.jpg|ממוזער|מרכז|600 פקיסלים|איור מס' 2: מסלול העברת אותות Epidermal Growth Factor Receptors]] | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
גרסה מ־08:41, 14 ביוני 2018
טיפולים מכווני מטרה בסרטן מעי גס גרורתי ד״ר מיטל לברטובסקי, ד״ר עינת שחם-שמואלי המכון האונקולוגי, המרכז הרפואי שיבא, תל השומר
הטיפול הסיסטמי בסרטן המעי הגס הגרורתי מבוסס כיום על שילוב של טיפול כימי עם טיפולים מכווני מטרה שונים (targeted therapy). מאז שילוב הטיפולים המכוונים, אנו עדים לעלייה מתמדת בתוחלת החיים הממוצעת של החולה הסובל ממחלה גרורתית, אשר מגיעה כיום ל-30 חודשים בממוצע. את הטיפולים המכוונים ניתן לשלב בכל קו טיפולי, ולמעשה עם כל כימותרפיה הניתנת לסרטן המעי הגס. בניגוד לכימותרפיה, הפועלת על ידי פגיעה בחלוקת התא, הטיפול המכוון פוגע בתהליכי השגשוג של התא הסרטני עצמו או של הרקמות סביבו.
בסקירה זו נציג את הטיפולים המכוונים העיקריים הנמצאים בשימוש בסרטן מעי גס גרורתי. תרופות אלה פועלות באחד משני מישורים:
1. היווצרות כלי דם חדשים - אנגיוגנזה
Angiogenesis)).
2. פגיעה במסלולי העברת אותות של EGFR (Epidermal Growth Factor Receptors).
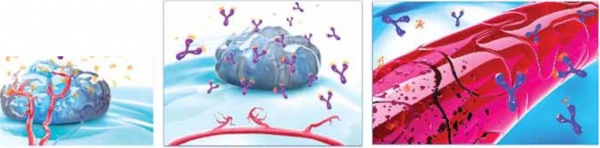
פגיעה באנגיוגנזה אנגיוגנזה - היווצרות כלי דם חדשים - הינו תהליך חשוב והכרחי בהתפתחות וקיום התהליך הסרטני. הגידול הסרטני ההולך וגדל נזקק לחומרים חיוניים שהוא מקבל דרך כלי דם חדשים הגדלים סביב הגידול. כלי הדם החדשים נוצרים בעקבות הפרשת VEGF Vascular Endothelial Growth Factor)) מהתא הגידולי וקשירתו אל קולטן VEGF receptor הנמצא על גבי תאי האנדותל. חיבור זה משפעל את תהליך האנגיוגנזה - יצירת כלי דם חדשים (איור 1). בנוכחות רמת VEGF גבוהה, כלי הדם החדשים הנוצרים הם בעלי נטייה רבה יותר לדלף מאחר שהאנדותל בהם אינו תקין והוא פרמאבילי יותר. התרופות המכוונות הפוגעות בקשירת הפקטור לקולטן גורמות למספר תהליכים: עיכוב היווצרות כלי דם חדשים, רגרסיה של כלי דם קיימים וכן נורמליזציה של תאי האנדותל בכלי הדם ומניעת דלף (איור 1).
איור מס' 1: מנגנוני פעולה של מעכבי אנגיוגנזה (Angiogenesis)
Anti-permeability of surviving vasculature
Regression of existing tumour vasculature
Inhibition of new vessel growth
מנגנונים אלו אחראים מצד אחד להקטנת אספקת הדם לגידול ומצד שני לנורמליזציה של זרימת הדם (והכימותרפיה). מנגנונים אלו מסבירים מדוע מתן נוגדן המכוון כנגד VEGF בשילוב עם כימותרפיה יעיל יותר מכימותרפיה בלבד.
התרופות העיקריות במשפחה זו:
בוואציזומאב - Bevacizumab
(אווסטין - ®Avastin)
נוגדן מונוקלונאלי המכוון כנגד הפקטור VEGF. זו התרופה המכוונת הראשונה אשר אושרה על ידי ^FDA בתחילת שנת 2004 לשימוש בחולי סרטן מעי גס גרורתי. ניתן לתת אותה בשילוב עם כימותרפיה מקו ראשון ואילך, ואף הוכח במחקר TML כי בחולים שהתקדמו בטיפול כימי עם בוואציזומאב בקו ראשון ניתן לשנות למשלב כימותרפי אחר בקו שני,
Inhibition of new vessel growth
Anti-permeability of surviving vasculature
במה | ביטאון לעובדי בריאות בנושא מחלת הסרטן והשלכותיה
לעומת כימותרפיה לבד, אך להמשיך מתן בוואציזומאב וכך להשיג שיפור בהישרדות של כחודש וחצי לעומת כימותרפיה בלבד. אסטרטגיה זו נקראת Bevacizumab beyond 1] progression! אפליברספט - Aflibercept (זלטראפ® - ®Zaltrap) תרופה שאינה נוגדן, אלא פועלת כ׳׳מלכודת" ^VEGF trap) VEGF). התרופה הינה חלבון רקומביננטי הבנוי מחיבור של החלק החוץ-תאי של הקולטן ^VEGF יחד עם החלק הקבוע של נוגדן IgG1 הומני. חלבון זה גורם ללכידת מולקולות VEGF ובכך מונע את חיבור הפקטור לקולטן על גבי תאי האנדותל. התרופה נבדקה במחקר 2] VELOUR], אשר כלל מטופלים שהתקדמו על משלב כימותרפיה שהכיל אוקסליפלטין - Oxaliplatin (אלוקסטין® - ®Eloxatin)*. מחצית מהחולים עברו לקו טיפול שני - FOLFIRI - מבוסס אירינוטקאן - Irinotecan (קאמפטו® - ®Campto)* והמחצית השנייה טופלה FOLFIRI-n עם אפליברספט. במחקר זה נצפתה הטבה בהישרדות של כחודש וחצי לתוספת אפליברספט. התרופה אינה מאושרת בסל ואינה בשימוש נרחב בישראל. תופעות הלוואי האופייניות לתרופות הנ״ל: 1. יתר לחץ דם - שכיחותו גבוהה אך הוא לרוב בדרגה לא חמורה וניתן לשליטה על ידי תרופות. נדיר (<1%) שיתפתח .Hypertensive crisis 2. איבוד חלבון בשתן (פרוטאינוריה) - גם כאן מדובר בתופעה המתרחשת בכרבע מהמטופלים, אשר משמעותה הקלינית לא ברורה, שכן רק אחוזים בודדים מפתחים איבוד כמויות משמעותיות של חלבון בשתן ותסמונת נפרוטית.
3. ניקוב של המעי (Perforation) - עלול להופיע בקרב 2-1.5% מהמטופלים. 4. הפרעה באיחוי פצע או חתך ניתוחי. 5. תופעות טרומבואמבוליות. רגוראפיניב - Regorafenib (סטיברגה® - ®Stivarga)* תרופה זו פועלת במנגנון של עיכוב תוך-תאי של הטירוזין קינאז של מספר קולטנים (FGF ,VEGF, PDGF). רגוראפיניב הינו מעכב טירוזין קינאז הראשון שנמצא יעיל בסרטן המעי הגס, והוא התרופה המכוונת הראשונה בסרטן המעי הגס שניתנת באופן פומי. במחקר 3] CORRECT] נבדקה התרופה מול טיפול תומך בחולי סרטן מעי גס גרורתי אשר מיצו את כל הטיפולים הסטנדרטיים, ונמצא שיפור בהישרדות של כחודש וחצי (6.4 חודשים בהשוואה ל-5 חודשים). התרופה לא מאושרת בסל התרופות בישראל. תופעות לוואי האופייניות לתרופה הינן שלשולים, יל"ד , קילוף ופריחה של כפות הידיים והרגלים (Hand and foot syndrome) ועייפות.
פגיעה במסלולי העברת סיגנל שלEGFR המסלול התוך-תאי המופעל כתוצאה מחיבור בין הקולטן EGFR לליגנדים שלו (אפירגולין, אמפירגולין) הינו מסלול חיוני בשגשוג והתמיינות התא הסרטני. הליגנד נקשר לקולטן החוץ-תאי ומפעיל שרשרת תהליכים תוך-תאיים המגיעים עד לגרעין התא (איור 2). התרופות העיקריות הפועלות בעיכוב המסלול הנ״ל הינן נוגדנים מונוקלונאליים המכוונים נגד החלק החוץ-תאי של הקולטן EGFR, אלה הן צטוקסימאב - Cetuximab (ארביטוקס® Erbitux® -)* ופניטומומאב -Panitumumab (וקטיביקס® - ®.[6-4] *(Vectibix יעילותן תלויה בביטוי תקין (wild-type) של חלבון KRAS, NRAS) RAS). חלבוני ^RAS הינם חלק משרשרת העברת הסיגנל שמופעל על ידי קשירת ליגנד ^EGFR. כאשר KRAS או NRAS מוטנטים (בכ-50% מהגידולים), המסלול מופעל באופן תמידי וללא תלות בקישור הליגנד לקולטן ^EGFR. לכן, בחולים בהם NRAS או KRAS מוטנטים, לא צפויה תגובה לתרופות הפועלות כנגד EGFR.
תופעות הלוואי האופייניות לתרופות הנ״ל:
1. פריחה דמוית אקנה, יובש עור, שינויים בתשעורת ובציפורניים.
2. היפומגנזמיה.
3. תגובות אלרגיות - תגובה אלרגית קשה ואנפילקסיס נדירות.
בחירת הטיפול מכוון המטרה
מספר מחקרים בחנו יעילות תשלובת כימית עם בוואציזומאב מול תשלובת כימית עם נוגד EGFR. במחקרים אלו (80405 CALGB ,FIRE-3, PEAK), אם בוחנים את כלל אוכלוסיית החולים, נצפו תוצאות דומות מאוד בכל קבוצות הטיפול מבחינת ההישרדות הכללית והזמן עד להתקדמות המחלה ברוב העבודות, פרט לעבודה FIRE3, בה נצפה יתרון הישרדותי לזרוע שקיבלה כימותרפיה FOLFIRI בתוספת צטוקסימאב, על פני הזרוע שטופלה בכימותרפיה עם בווציזומאב (28.7 מול 25 חודשים בהתאמה 017.=HR-0.77 P). עובדה מפתיעה שעלתה מעבודות אלה הצביעה על כך שאם מפלחים את החולים לפי מיקום הגידול הראשוני - מעי שמאל (המעי היורד, הסיגמואיד והרקטום) לעומת מעי גס ימין (הצקום והמעי עולה) אזי מתגלים הבדלים משמעותיים וחשובים. ראשית, ההישרדות הממוצעת של חולים עם גידולי מעי ימני פחותה משמעותית לעומת חולים עם גידולי מעי שמאל (טבלה מס' 1). שנית, בגידולים שמקורם בצדו השמאלי של המעי הגס, תרופות ממשפחת נוגדי ^EGFR משפרות
הישרדות ב-7 עד 11 חודשים לעומת בוואציזומאב. לעומת זאת, בגידולים שמקורם במעי הימני הודגם שיפור מתון בהישרדות במתן טיפול כימי עם בוואציזומאב לעומת נוגדי EGFR.
נתונים אלו שינו בשנה האחרונה את הגישה הטיפולית בבחירת הטיפול המכוון למטופלים עם סרטן מעי גס גרורתי. כעת משפיעים על ההחלטה לא רק נוכחות או היעדר מוטציות RAS, אלא גם מיקום הגידול הראשוני. במטופלים עם גידול שמקורו במעי השמאלי ואשר נשללו מוטציות KRAS או NRAS, נעדיף לרוב טיפול כימי עם מעכבי EGFR בקו ראשון.
תרופות מכוונות נוספות הנמצאות כעת בשלבים שונים של מחקר קליני:
תרופות נגד קולטן HER2
HER2 מבוטא ביתר בכ-4% מגידולי המעי הגס. במטופלים עם ביטוי יתר של רצפטורים HER2, נבדקה במסגרת מחקר HERACLES [10] יעילות שילוב של טרסטוזומאב Trastuzumab - (הרצפטין® - ®Herceptin)* ולפטיניב - Lapatinib (טיייקרב® - ®,*(Tykerb שהינן תרופות הנמצאות בשימוש נרחב בסרטן שד חיובי ^HER2. במחקר HERACLES נצפה כי בחולים אשר התקדמו על טיפול כימי בשילוב עם מעכבי ,EGFR השילוב לפטיניב עם טרסטוזומאב הביא לתגובה בקרב כ-30% מהחולים. תרופות אלו אינן נמצאות כרגע בשימוש בסרטן המעי הגס מחוץ למחקר הקליני.
מעכבי BRAF מוטציית BRAF V600E קיימת ב-9-5% מגידולי המעי הגס, ולרוב מנבאת פרוגנוזה עגומה. תרופות מעכבות BRAF נמצאו יעילות מאוד במלנומה עם מוטציית BRAF V600E, אך למרבה הצער יעילותן מוגבלת מאוד בסרטן מעי גס עם מוטציה זו. זאת כנראה עקב העובדה שעיכוב BRAF בסרטן מעי גס גורם לשפעול יתר של מסלולי EGFR ואחרים. במחקר אשר בחן שילוב של מעכב BRAF בשם דבראפיניב - Dabrafenib (טפינלאר® - ®Tafinlar)* עם מעכב MEK בשם טראמטיניב - Trametinib (מקיניסט® - ®Mekinist)* ועם מעכב EGFR (פניטומומאב), בחולים אשר קיבלו קווי טיפול קודמים, נצפתה תגובה ב-34% מהמטופלים, עם זמן חציוני עד התקדמות מחלה של 4.1 חודשים [11]. שילוב תרופות אלו אינו בשימוש בסרטן המעי הגס מחוץ למחקר הקליני. סיכום שילובן של התרופות המכוונות עם כימותרפיה הביאה לשיפור משמעותי בתוחלת החיים של מטופלים עם סרטן מעי גס גרורתי. תחום הטיפול מכוון המטרה הינו תחום מתפתח ומשתנה. ידוע כי נוכחות או היעדר מוטציות מסוימות משפיע על הסיכוי לתגובה לתרופות מכוונות. לאחרונה הדגימו תוצאות מפתיעות ממחקרים שונים כי גם למיקום הגידול הראשוני לאורך המעי השפעה ניכרת על התגובה לטיפולים השונים, והסיבות לכך עדיין לא ברורות דיין. אנו עדים לשינוי בתהליך קבלת ההחלטות לגבי האפשרויות הטיפוליות השונות. יש רק לקוות שבעתיד הקרוב ייכנסו תרופות נוספות לארסנל שיש באפשרותנו להציע למטופלינו, תרופות אשר ימשיכו להביא לעלייה מתמדת בתוחלת החיים של המטופלים.
1 Arnold D, Andre T, Bennouna J, et al. Bevacizumab (BEV) plus chemotherapy (CT) continued beyond first progression in patients with metastatic colorectal cancer (mCRC) previously treated with BEV plus CT: results of a randomized phase III intergroup study (TML study). J Clin Oncol. 2012;30(18) (suppl). [abstract]. Abstract CRA3503. 2. Van Cutsem E, et al. Intravenous aflibercept versus placebo in combination with irinotecan/5-FU (FOLFIRI) for second-line treatment of metastatic colorectal cancer (advanced cc): results of a multinational phase III trial (EFC10262-VELOUR). Ann Oncol. 2011;22(5). [abstract]. ESMO Abstract: O-0024. 3. Grothey, A, Sobrero AF, Siena S, et al. Results of a phase III randomized, double-blind, placebo- controlled, multicenter trial (CORRECT) of regorafenib plus best supportive care (BSC) versus placebo plus BSC in patients (pts) with metastatic colorectal cancer (mCRC) who have progressed after standard therapies. J Clin Oncol. 2012;30(4) (suppl). [abstract]. Abstract LBA385. 4. Peeters M, Price TJ, Cervantes A, et al. Randomized phase III study of panitumumab with fluorouracil, leucovorin, and irinotecan (FOLFIRI) compared with
FOLFIRI alone as second-line treatment in patients with metastatic colorectal cancer. J Clin Oncol. 2010 Nov;28(31):4706-13. 5. Douillard JY, Siena S, Cassidy J, et al. Randomized, phase III trial of panitumumab with infusional fluorouracil, leucovorin, and oxaliplatin (FOLFOX4) versus FOLFOX4 alone as first-line treatment in patients with previously untreated metastatic colorectal cancer: the PRIME study. J Clin Oncol. 2010 Nov;28(31):4697-705. 6. Van Cutsem E, Kohne CH, Lang I, et al. Cetuximab plus irinotecan, fluorouracil, and leucovorin as first-line treatment for metastatic colorectal cancer: updated analysis of overall survival according to tumor KRAS and BRAF mutation status. J Clin Oncol. 2011 May 20;29(15):2011-9. Epub 2011 Apr 18. 7. Venook AP, Niedzwiecki D, Lenz H-J, et al. CALGB/ SWOG 80405: phase III trial of irinotecan/5-FU/ leucovorin (FOLFIRI) or oxaliplatin/5-FU/leucovorin (mFOLFOX6) with bevacizumab (BV) or cetuximab (CET) for patients with KRAS wild-type untreated metastatic adenocarcinoma of the colon or rectum. J Clin Oncol. 2014;32(15) (suppl). [abstract]. ASCO Abstract LBA3.
8. Schwartzberg LS, Rivera F׳ Karthaus M, et al. PEAK: a randomized, multicenter phase II study of panitumumab plus modified fluorouracil, leucovorin, and oxaliplatin (mFOLFOX6) or bevacizumab plus mFOLFOX6 in patients with previously untreated, unresectable, wild- type KRAS exon 2 metastatic colorectal cancer. J Clin Oncol. 2014 Jul;32(21):2240-47. 9. Heinemann V, von Weikersthal LF, Decker T, et al. FOLFIRI plus cetuximab versus FOLFIRI plus bevacizumab as first-line treatment for patients with metastatic colorectal cancer (FIRE-3): a randomised, open-label, phase 3 trial. Lancet Oncol. 2014 Sep;15(10):1065-75. Epub 2014 Jul 31. 10. Siena S, Sartore-Bianchi A, Trusolino L, et al. Therapeutic dual inhibition of HER2 pathway for metastatic colorectal cancer (mCRC): the HERACLES trial. J Clin Oncol. 2015 Jan;33(3) (suppl). [abstract]. ASCO abstract 565. 11. Atreya CE, Van Cutsem E, Bendell JC, et al. Updated efficacy of the MEK inhibitor trametinib, BRAF inhibitor dabrafenib, and anti-EGFR antibody panitumumab in patients with BRAFV600E mutated metastatic colorectal cancer. J Clin Oncol. 2015 May 31;33(15) (suppl.) [abstract]. ASCO abstract 103.
1. Hurwitz H, et al. Bevacizumab plus Irinotecan, Fluorouracil, and Leucovorin for Metastatic Colorectal Cancer. N Engl J Med 2004;350:2335-42. 2. Giantonio et al. Bevacizumab in Combination With Oxaliplatin,Fluorouracil, and Leucovorin (FOLFOX4) for PreviouslyTreated Metastatic Colorectal Cancer ECOG study E3200. JCO 2007 3. Bennouna J, et al. Continuation of bevacizumab after first progression in metastatic colorectal cancer (ML18147): a randomised phase 3 trial Lancet Oncol 2013;14:29-37.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק