הבדלים בין גרסאות בדף "בילירובין - Bilirubin"
| שורה 60: | שורה 60: | ||
====תסמונת Crigler-Najjar==== | ====תסמונת Crigler-Najjar==== | ||
| − | תסמונת זו על שני סוגיה (I ו-II) מתאפיינת ברמת גבוהה של בילירובין לא ישיר בפלזמה, על רקע חסר פעילות של האנזים המצמד UGT. תסמונת CN הידועה גם כצהבת מולדת לא-המוליטית, היא מפגע אוטוסומאלי-המוליטי נדיר ביותר כאשר ב type 1 יש חסר מוחלט של פעילות האנזים בגלל שורה של מוטציות בגן המקודד לאנזים UGT1A1, ואילו ב-type 2 פעילות האנזים חלקית. תסמונת CN type 1 מתגלה בימי החיים הראשונים, ורב הלוקים בה מתים תוך חודשים אחדים, ורק בודדים מגיעים לגיל הבחרות. סיבת המוות היא אנצפאלופתיה חמורה הנגרמת מ-kernicterus. ב-type 1 רמת בילרובין בפלזמה יכולה להגיע עד לרמות שבין 20 ל-50 מיליגרם לדציליטר, ותסמינים יכולים לכלול הפרעות תנועה מהותיות, כגון [[chorea]], [[בליסמוס|בּליסמוּס]] ורעד, ומפגעי שמיעה עד חרשות, פגיעה בתנועת העיניים (gaze) כמו גם פיגור שכלי. הפגיעה המוחית נגרמת עקב מעבר בילירובין בלתי מצומד דרך מחסום דם-מוח, שעדיין אינו סגור הרמטית בגיל הרך, שקיעת חומר זה במוח ונזק שהוא גורם לגרעינים הבזאליים. טיפול ב[[פנוברביטל]] אינו יעיל כיוון שהאנזים UGT אינו קיים, ופוטותרפיה מפחיתה לא יותר מ-10 עד 20% מהבילירובין הלא מצומד בדם. | + | תסמונת זו על שני סוגיה (I ו-II) מתאפיינת ברמת גבוהה של בילירובין לא ישיר בפלזמה, על רקע חסר פעילות של האנזים המצמד UGT. תסמונת CN הידועה גם כצהבת מולדת לא-המוליטית, היא מפגע אוטוסומאלי-המוליטי נדיר ביותר כאשר ב type 1 יש חסר מוחלט של פעילות האנזים בגלל שורה של מוטציות בגן המקודד לאנזים UGT1A1, ואילו ב-type 2 פעילות האנזים חלקית. תסמונת CN type 1 מתגלה בימי החיים הראשונים, ורב הלוקים בה מתים תוך חודשים אחדים, ורק בודדים מגיעים לגיל הבחרות. סיבת המוות היא אנצפאלופתיה חמורה הנגרמת מ-kernicterus. ב-type 1 רמת בילרובין בפלזמה יכולה להגיע עד לרמות שבין 20 ל-50 מיליגרם לדציליטר, ותסמינים יכולים לכלול הפרעות תנועה מהותיות, כגון [[chorea]], [[בליסמוס|בּליסמוּס]] ורעד, ומפגעי שמיעה עד חרשות, פגיעה בתנועת העיניים (gaze) כמו גם [[פיגור שכלי]]. הפגיעה המוחית נגרמת עקב מעבר בילירובין בלתי מצומד דרך מחסום דם-מוח, שעדיין אינו סגור הרמטית בגיל הרך, שקיעת חומר זה במוח ונזק שהוא גורם לגרעינים הבזאליים. טיפול ב[[פנוברביטל]] אינו יעיל כיוון שהאנזים UGT אינו קיים, ופוטותרפיה מפחיתה לא יותר מ-10 עד 20% מהבילירובין הלא מצומד בדם. |
====תסמונת type 2 CJ==== | ====תסמונת type 2 CJ==== | ||
גרסה מ־12:03, 12 בדצמבר 2018
| מדריך בדיקות מעבדה | |
| בילירובין | |
|---|---|
| Bilirubin | |
| |
| מעבדה | כימיה בדם, כימיה בשתן, כימיה במי השפיר וכימיה בנוזל השדרה |
| תחום | הערכת תפקודי כבד הן במחלת כבד כרונית, בנזק חריף מזדמן כהרעלת פאראצטמול, נזק מסתימה בדרכי מרה, או מחלות תורשתיות המשפיעות על חילוף החומרים של בילירובין |
| יחידות מדידה | מיליגרם לדציליטר |
| טווח ערכים תקין | כיוון שבילירובין הוא תוצר הפרשה, ורמתו בדם משקפת את האיזון בין יצירת הפיגמנט והפרשתו מהגוף, מקורות שונים מספקים תחומי נורמה דומים אם כי לא זהים. בתינוקות עם נתוני לידה תקינים מעל גיל 7-30 ימים, וכן במבוגרים עד גיל 70 שנה מקובל תחום ריכוז תקין של 0.3-1.1 מיליגרם לדציליטר ל-total bilirubin, כאשר ריכוז בילירובין ישיר או מצומד (conjugated) נע בין 0.1-0.2 מיליגרם לדציליטר, ואילו רמת בילירובין בלתי-ישיר או בלתי-מצומד (unconjugated) נע בין 0.2-0.8 מיליגרם לדציליטר. רמת סך-בילירובין משקפת את סך רמת הבילירובין הישיר והבלתי-ישיר. בילירובין בלתי ישיר אינו נמדד ישירות, אלא מחושב על ידי החסרה של רמת הבילירובין הישיר מרמת סך-בילירובין. בדם חבל הטבור רמת סך בילירובין יכולה להגיע עד -2.52.0 מיליגרם לדציליטר, כאשר מייד לאחר הלידה בחלק גדול מוולדות מתרחשת המוליזה באופן שרמת סך-בילירובין יכולה להגיע ביום הראשון עד 6.0-8.0 מיליגרם לדציליטר בילדים שנולדו במועד, או אף עד 12.0 מיליגרם לדציליטר בפגים; בין הימים 3-5 לאחר הלידה רמת סך בילירובין בפג לא אמורה לעלות על 16 מיליגרם לדציליטר ובתינוקות שנולדו במועד רמת סך בילירובין נעה בין 1.5-12.9 מיליגרם לדציליטר. לפי גרסאות שונות, רמת בילירובין בתינוקות שנולדו במועד אמורה לחזור בין 7 ל-30 יום לערכי בילירובין במבוגרים. בשתן רמת בילירובין הנמדדת בעזרת מקלוני שתן היא שלילית במצבם תקינים. בנוזל מי השפיר רמת סך-בילירובין הנמדדת בשבוע ה-28 להיריון נמוכה מ-0.075 מיליגרם לדציליטר, ואילו בשבוע ה-40 להיריון רמת בילירובין נמוכה מ-0.025 מיליגרם לדציליטר. בנוזל שדרה (CSF) רמת בילירובין נמדדת על ידי סריקה ספקטרופוטומטרית באורכי גל שבין 300 ל-500 ננומטר, תוך חיפוש שיא בליעה באורך גל 454 ננומטר המתאים לבילירובין. בדרך כלל קובעים את היחס בין רמת הבליעה באורכי גל 418 ננומטר (בליעה מרבית של המוגלובין מחומצן) לבין זו באורך גל 454 ננומטר כאשר הנוזל קסנטוכרומי, לדומה במקרים של שטף דם תת-עכבישי (SAH) |
| יוצר הערך | פרופ' בן-עמי סלע |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – תפקודי כבד
מטרת הבדיקה
מדידת רמת בילירובין יכולה לשמש לבירור מגוון מפגעים, אם כי ברוב המקרים רמת בילירובין היא חלק בלתי נפרד מפרופיל של מדדי מעבדה שגרתיים, עם דגש על תפקודי כבד. בראש ובראשונה רמת בילירובין (total + direct) נמדדת במצבים בהם יש הצהבה של לובן העין או גוון העור המחשידים לצהבת. רמת בילירובין תעזור לברר האם מדובר בתמס-דם מסיבי מסיבות פיזיולוגיות או כתופעת לוואי של טיפול תרופתי. תוצאה של בילירובין לתת-סוגיו, תסייע לברר אם מדובר בחסימה של דרכי מרה כתוצאה מאבנים או אף מגידול בבלוטת הלבלב, תעזור בניטור של מחלת כבד כהפאטיטיס, צמקת הכבד, או מחלת כבד גדושה כתוצאה מאי-ספיקת לב גדושה. רמת בילירובין תסייע לעקוב אחר תוצאות טיפול במצבים האמורים, ולגלות נזקי טיפולים תרופתיים.
מדידת בילירובין תיתן מידי במקרים של תסמונות תורשתיות הקשורות לבילירובין כגון Rotor ,Dubin-Johnson ,Gilbert או מחלת Crigler-Najjar. המוליזה מוגברת במפגעים כמו אנמיה חרמשית, או חסר ב-G6PD צריכה להתברר בין השאר על ידי מדידה דיפרנציאלית של סוגי הבילירובין השונים. מחלה המוליטית של הילוד כתוצאה מאי התאמה של Rh, וכן ניטור צהבת פיזיולוגית בתינוקות בימיהם הראשונים מחייבת מדידת תכופה של רמת בילירובין.
בדיקת בילירובין נעשית לעתים מזומנות בנוסף ל"אנזימי כבד" כ-GPT, GOT , פוספטאזה בסיסית ו-Gamma GT, לבירור אי-סדירות בפעילות הכבד, מסיבות חריפות, כרוניות, ממאירות ראשונית של הכבד או במצבי גרורות לכבד. ברור נזקי אלכוהוליזם, הסיבות לשתן כהה, מצבי בחילה והקאות, כאבי בטן, כבד נמוש, עייפות ותסמיני חולי שהם פועל יוצא של מחלת כבד כרונית.
בסיס פיזיולוגי
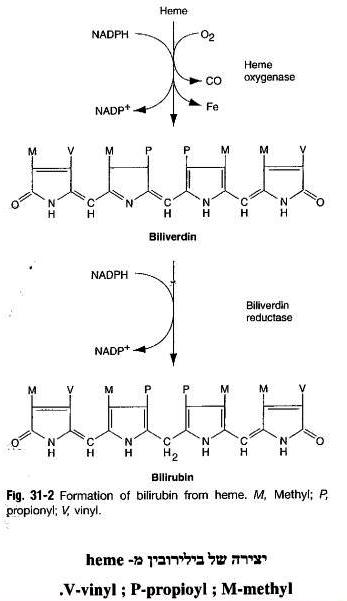
בילירובין בלתי-מצומד (בלתי-ישיר) הוא תוצר קטאבולי של מטבוליזם של ה-heme, שהוא בעל פוטנציאל רעלני לגוף, בפרט בהגיעו לריכוזים גבוהים. אדם מבוגר מייצר מדי יום 4 מיליגרם בילירובין לכל ק"ג משקל גוף, דהינו בסך הכול כ-250-400 מיליגרם בילירובין מדי יום. בערך 70-80% מכמות זו, מקורם בפרוק של Heme ממקור המוגלובין, ושאר 20-30 האחוזים מקורם מפרוק בכבד של המופרוטאינים אחרים כמו מיוגלובין, ציטוכרומים וקטלאזה. אחוז קטן של בילירובין הנוצר מדי יום, מקורו בהרס של כדוריות דם אדומות צעירות או כאלה בשלבי התפתחות מוקדמים.
הסיבה לכך שבילירובין מסיס מעט מאוד במים ב-pH הפיזיולוגי, נובעת מקשרי המימן התוך-מולקולאריים הרבים של בילירובין, שהמבנה מכונס שלו מוגדר כ-bilirubin IX-α-ZZ. קשרי מימן אלה ממסכים אתרים הידרופילים של מולקולת בילירובין, ומקנים לה אופי הידרופובי, וממילא מגבירים את הפוטנציאל לרעלנות. לבילירובין יש מבנה של שרשרת פתוחה המורכת מ-4 טבעות דמויות pyrrole, לעומת heme בו 4 הטבעות הפירוליות סגורות לטבעת פורפירינית.
לכן הפיכת מבנה IX-α של בילירובין לצורה מסיסה במים על ידי שיבוש קשרי המימן, חיונית לקליטת המולקולה בכבד, והפרשתה בהמשך בכליה. הדבר מושג על ידי צימוד החומצה הגלוקורונית לשרשרת הפרופיוניות הצדדיות בבילירובין, מה שפותח את המולקולה, חושף את קשרי המימן והופך אותה למסיסה במים, ומאפשר הפרשתה המהירה במרה. בילירובין מופרש בדם בעיקר כנגזרת diglucuronide, ואילו בילירובין בלתי-מצומד מהווה רק 14% מכלל הפיגמנט במרה במצב תקין.
מדידת בילירובין
בשנת 1913 היה van den Bergh הראשון שהדגים נוכחות בילרובין בנסיוב, בריאקציה עם ריאגנט אהרליך, בה מגיב diazotized sulfanilic acid עם פחמן שייר המתילן המרכזי של בילירובין וחותך את המולקולה ליצירת 2 מולקולות של אז-בילירובין, שניתן למדוד בספקטרופוטומטר. ון דן ברג נוכח לדעת שרוב הבילירובין בנסיוב אינו מגיב תוך דקה אחת עם ריאגנט דיאזו, אלא אם כן מוסיפים לתערובת הריאקציה "מאיץ" דוגמת urea או אתנול כדי לאפשר את התפתחות ריאקצית הצבע תוך 30-60 דקות ומאז הוגדר הבילירובין האחרון כ"בלתי ישיר", כאשר כיום ידוע שבילירובין בלתי ישיר הוא בילירובין בלתי מצומד שקשור לאלבומין, והוא בדרכו לכבד, והוספת האלכוהול להאצת ריאקצית הצבע נועדה להביא להמסתו. כיום, השיטה מקובלת למדידת סך בילירובין היא על ידי השימוש בריאגנט DPD או 2,5-dichlorophenyldiazonium, ואילו בילירובין ישיר או מצומד נמדד בשיטת Jendrassik ו-Grof.
בגלל האופי הלא-פולרי של הבילירובין הבלתי צמוד והזיקה הגבוהה שלו לאלבומין, לא ניתן למצוא אותו באופן נורמאלי בשתן, אלא בכמות זעירה ביותר. לעומת זאת, בילרובין מצומד לגלוקורונאט הוא פולארי, נמס בפלזמה ואינו קשור לחלבונים, לכן הוא מגיב באופן ישיר עם ריאגנט דיאזו ליצירת אזו-בילירובין. כאשר רמת הבילירובין המצומד "הישיר" גבוהה בדם, הוא יכול לעבור את פקעיות הכליה ולהיות מופרש בשתן.
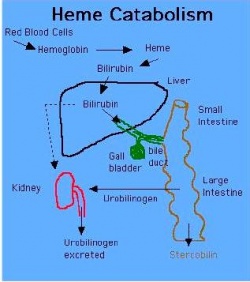
כאשר אריתרוציטים בני 120 יום או כאלה שניזוקו מסיבות שונות מפונים למערכת הרטיקולו-אנדותליאלית בטחול, בכבד ובמח העצם, הם משחררים שם את תכולת ההמוגלובין שלהם, המתפרק לגלובין, לברזל ולגרעין ה-heme, כאשר האחרון מתפרק בשלב הראשון במיקרוזומים של הכבד ליצירת billiverdin, פיגמנט ירוק בעל מבנה טטרה-פירולי טבעתי, וזאת בעזרת האנזים heme oxygenase. ה-billiverdin המסיס עובר לציטופלזמה, שם הוא מתחזר על ידי האנזים billiverdin reductase והופך לבילירובין בלתי ישיר, שהוא פיגמנט בגוון כתום-צהוב המסיס בשומן אך אינו מסיס במים, וזה נקשר לאלבומין ומובל כך לכבד עם אספקת הדם הוורידית מהווריד הפורטאלי. בהגיעו לצד הסינוסואידאלי של הכבד, עובר בילירובין הקשור לאלבומין לחלל ע"ש Diss, הממוקם בין האנדותל לממברנה של ההפאטוציט, שם הוא משתחרר מהאלבומין, ונכנס לתוך התאים ההפאטוציטים.
בשלב זה כשהוא נמצא בתוך הציטוזול המימי של ההפאטוציטים, הבילירובין עדיין בלתי מסיס במים, ואז הוא נקשר ל-2 חלבונים: האחד ידוע כ-cytosolic Y protein או ligandin והוא למעשה האנזים S transferase glutathione, והשני ידוע כ-cytosolic Z protein, ואלה מובילים את בילירובין ל-endoplasmic reticulum, שם הוא עובר צימוד עם חומצה גלוקורונית על ידי האנזים UDP glucuronyltransferase, מה שהופך אותו מסיס במים, ומאפשר את הפרשתו לכיס המרה, שהיא מדיום מימי. מעבר בילירובין לתוך מערכת המרה נעשה בצד הקניקולארי, והוא תהליך דורש אנרגיה בצורת ATP. התלוי בטרנספורטר הידוע כ-MRP2 או multidrug resistance protein, שמעביר את הבילירובין המצומד למרה. מערכת הצימוד האנזימטית יוצרת שני תוצרים, מונו-גלוקורוניד ודי-גלוקורוניד, כאשר רוב הבילירובין (85%) המצומד בדם הוא די-גלוקורוניד. מרה, המיוצרת על ידי תאי הכבד, זורמת ברשת של צינורות מרה המצויים בינות לתאי הכבד אל כיס המרה ומשם אל צינור המרה הראשי, המתחבר אל התריסריון, בקדמת המעי הדק.
חלק מהבילירובין המצומד נותר במעי הגס, ועובר של חילוף חומרים על ידי חיידקי המעי, ליצירת urobilinogen, וזה עובר מטבוליזם נוסף ליצירת stercobilinogen המתחמצן ליצירת stercobilin, החומר המקנה לצואה את הצבע החום האופייני. מדי יום כמות של 40-280 מיליגרם אורובילינוגן מופרשת בצואה. כ-20% מה-urobilinogen נספג מחדש במעי, חלקו נשאב למערכת הפורטלית וחוזר למרה במערכת האנטרו-הפטית, וחלקו מגיע מהפלזמה בסופו של תהליך ומופרש בשתן ביחד עם צורתו המחומצנת, urobilin, מה שמקנה לשתן את צבעו הצהוב.
עליה ברמת urobilinogen בשתן, מצביעה או על עליה ביצירת בילירובין והעברת הצורה המצומדת שלו למעיים, כפי שהדבר קורה במצבי תמס דם או סיבות אחרות לשחרור כמויות heme גדולות, או שהיא מצביעה על ירידה בפינוי על ידי כבד פגוע, כפי שרואים במצבי צמקת, אך גם בשלב התאוששות מנזק כבדי. מדידה של רמת urobilin או urobilinogen בשתן, מספקת מידע נוסף על מטופלים עם חשש למחלת כבד.
בילירובין דלתא (bilirubin δ)
רק בשנות ה-80 התגלה כמעט באקראי סוג נוסף של בילירובין-דלתא: מקטע זה של בילירובין הוא למעשה בילירובין בלתי מצומד הקשור בקשר קו-ולנטי לאלבומין, שהוא תולדה של ריאקציה לא אנזימטית בין שייר ליזין על פני אלבומין ומולקולת בילירובין לא מצומד. בילירובין דלתא התגלה כשחברת Kodak הכניסה את טכנולוגית של מדידת ערכי מעבדה על גבי שקפים במכשיר Ektachem. בילירובין דלתא מגיב כמו בילירובין מצומד, והוא נמצא בדם ברמות מאוד נמוכות. במצבים שרמת בילירובין בלתי מצומד עולה, כך גם עולה רמת בילירובין דלתא. מקטע זה אינו מגיב בריאקצית diazo, ורק שינויים בריכוז ריאגנט דיאזו ובמשך הריאקציה בטכנולוגיה של Kodak אפשרו את גילוי בילירובין דלתא.
במצבי כולסטאזיס של אבן התקועה בצינור המרה המשותף המונעת הפרשת מרה אל המעי, ויש הופעה של cholangitis, ובפרט אם מצב זה נמשך זמן רב כגון במקרים של קרצינומה של הלבלב, הבילירובין המצומד (בעיקר זה עם שייר גלוקורונאט בודד) יכול להגיע לפלזמה ולהיות מופרש בשתן. חלק מבילירובין מצומד זה שרמתו עולה במצבים אלה נקשר קו-ולנטית לאלבומין, וכל זמן שאלבומין שורד בדם (תקופת מחצית חיי החלבון 19 יום) מקטע דלתא זה יישאר גבוה. כלומר, למרות שתקופת מחצית החיים של בילירובין מצומד היא 24 שעות, כל עוד הוא קשור קו-ולנטית לאלבומין, הוא ישרוד בפלזמה, מה שעלול להתבטא אצל המתאוששים ממחלת כבד לרמה מוגברת של בילירובין מצומד בפלזמה, למשך זמן ארוך מהצפוי.
תרופות המגבירות את רמת בילירובין הנמדדת בדם או על ידי גרימת נזק לכבד, על ידי הפרעה לפעילות האנזים UGT על ידי הגברת המוליזה או על ידי הפרעה אנליטית היכולה להשפיע על מדידת רמת בילירובין, הן התרופות כדלקמן: allopurinol, סטרואידים ובעיקר סטרואידים אנאבוליים-אנדרוגניים וכן גלולות למניעת היריון, סוגי אנטיביוטיקה מסוימים (דוגמת פניצילין, novobiocin, rifampicin, gentamycin , clindamycin ואריתרומיצין), תרופות אנטי-מלריות, isoniazid, amphotericin B, ברביטוראטים, אפינפרין, פאראצטאמול, והלוטן.תרופות נוספות המגבירות רמת בילירובין הן azathioprine,phenytoin ,chlorpropamide ,labetalol, קודאין, methyldopa, מורפין, חומצה ניקוטינית, captopril ,indomethacin ,pyrazinaide ,sulfonamides ,quinidine, מעכבי האנזים מונואמין אוקסידאזה,diphenylhydantoin ,5aminosalicylic acid, תיאופילין, diazepam, flurazepam. גם תכשירים כולינרגיים יכולים להעלות רמת בילירובין, כמו גם תכשירים מְשַתנים, וכן meperidine ,tolbutamide ,procainamide ,methotrexate ו-phenothiazine.
תרופות שיכולות להפחית את רמת הבילירובין הנמדד כוללות קפאין, סליצילאטים כמו אספירין במינון גבוה, ויטמין C, וכן phenobarbital.
תסמונות גנטיות עם עליה בפלזמה של בילירובין בלתי ישיר
תסמונת Gilbert
ידועה גם כ-familial hyperbilirubinemia, משקפת מפגע תורשתי שפיר ושכיח יחסית של מטבוליזם של בילירובין ששכיחותה -4-9% מהאוכלוסייה, יותר בגברים מאשר בנשים. האבחון בדרך כלל בגיל שבין 10 ל-30 שנה, והוא מתאפיין בעלייה לסירוגין ברמת הבילירובין הבלתי ישיר, המתגלה לעתים קרובות בבדיקות שגרה ללא ממצאים קליניים. רמת סך בילירובין יכולה להגיע ל-4 מיליגרם לדציליטר, ורק לעתים נדירות עולה מעל 5 מיליגרם לדציליטר, כאשר רמת הבילירובין הישיר-מצומד היא בתחום התקין ומהווה בערך 20% מסך הבילירובין. תסמונת Gilbert היא אוטוסומאלית-רצסיבית, והעלייה ברמת הבילירובין מתרחשת בדרך כלל בעקבות צום, צריכת אלכוהול, פעילות גופנית בעצימות גבוהה, מחזור חודשי או תרחישי המוליזה אחרים, עקה, מחלה סיסטמית או זיהומית, או טיפול בחומצה ניקוטינית. בשעת ההתרחשות התלונות בדרך כלל על בחילות, כאבי-בטן ועייפות, אך ישנה גם דעה שתחושות אלה מקורן פסיכו-סומאטי יותר מאשר פיזיולוגי. אין סיבוכים ארוכי-טווח, אין צורך בטיפול פרטני והפרוגנוזה טובה.
בתסמונת Gilbert יש הבלים אתניים לגבי המוטציה באנזים UGT1A1. האזור השכיח למוטציה באוכלוסיה הלבנה הוא אלמנט TATAA ב-promoter הכרוך עם הגן המקודד לאנזים זה, והממוקם בכרומוזום 2, ולא בגן עצמו, מה שמוריד את פעילות האנזים הזה רק ב-30%. אמנם, אלה עם תסמונת Gilbert המטופלים ב-irinotecan לוקים בשלשולים קשים ובנויטרופניה חמורה, שכן תרופה זו העוברת מטבוליזם על ידי האנזים UGT1A1, מתחרה עם פעילות אנזים זה בצימוד בילרובין. גם טיפול במעכבי פרוטאזה כ-azatanavir ו-indinavir במחלות נגיפיות, עלול לפגוע חלקית בפעילות האנזים UGT מה שעלול להיות יותר משמעותי בתסמונת Gilbert. לעומת זאת, טיפול ב-phenobarbital המחזק פעילות אנזים זה, ידועה כטיפול יעיל המאובחנים עלם תסמונת זו , ומפחית באופן משמעותי את רמת הבילירובין הבלתי ישיר.
ב-94% מהמקרים של תסמונת Gilbert, שני אנזימים נוספים בעלי פעילות glucuronyltransferase נחלשים בפעילותם ואלה UGT1A6 (המאבד 50% מפעילותו) ו-UGT1A7 (המאבד 83% מפעילותו). מעניין לציין שמחקרים אפידמיולוגיים גדולים מצאו שתסמונת Gilbert מפחיתה משמעותית תחלואה קרדיו-וסקולארית, ונהוג לייחס השפעה חיובית זו לבילירובין IXa, הידוע כנוגד חמצון חזק.
תסמונת Crigler-Najjar
תסמונת זו על שני סוגיה (I ו-II) מתאפיינת ברמת גבוהה של בילירובין לא ישיר בפלזמה, על רקע חסר פעילות של האנזים המצמד UGT. תסמונת CN הידועה גם כצהבת מולדת לא-המוליטית, היא מפגע אוטוסומאלי-המוליטי נדיר ביותר כאשר ב type 1 יש חסר מוחלט של פעילות האנזים בגלל שורה של מוטציות בגן המקודד לאנזים UGT1A1, ואילו ב-type 2 פעילות האנזים חלקית. תסמונת CN type 1 מתגלה בימי החיים הראשונים, ורב הלוקים בה מתים תוך חודשים אחדים, ורק בודדים מגיעים לגיל הבחרות. סיבת המוות היא אנצפאלופתיה חמורה הנגרמת מ-kernicterus. ב-type 1 רמת בילרובין בפלזמה יכולה להגיע עד לרמות שבין 20 ל-50 מיליגרם לדציליטר, ותסמינים יכולים לכלול הפרעות תנועה מהותיות, כגון chorea, בּליסמוּס ורעד, ומפגעי שמיעה עד חרשות, פגיעה בתנועת העיניים (gaze) כמו גם פיגור שכלי. הפגיעה המוחית נגרמת עקב מעבר בילירובין בלתי מצומד דרך מחסום דם-מוח, שעדיין אינו סגור הרמטית בגיל הרך, שקיעת חומר זה במוח ונזק שהוא גורם לגרעינים הבזאליים. טיפול בפנוברביטל אינו יעיל כיוון שהאנזים UGT אינו קיים, ופוטותרפיה מפחיתה לא יותר מ-10 עד 20% מהבילירובין הלא מצומד בדם.
תסמונת type 2 CJ
מחלה קלה בהרבה עם רמת בילירובין לא-ישיר שאינה עולה על 20 מיליגרם לדציליטר. תוחלת החיים תקינה והאבחון נעשה בגיל מתקדם יותר אם בכלל. כיוון שהמוטציה היא היא מסוג של missence, בה הפגיעה בפעילות האנזים אינה מוחלטת. בסוג זה אינה יצירת קרניקטרוס, אם כי במצבים מזדמנים של עקה טראומה ניתוחית ואחרים, רמת בילירובין עלולה להיות גבוהה, עם הופעה של מפגע נוירולוגי. אינדוקציה עם פנוברביטל מפחיתה כ-30% מרמת הבילירובין הבלתי-ישיר בדם.
תסמונות גנטיות עם עליה בדם של בילירובין ישיר
תסמונת Dubin Johnson
תסמונת אוטוזומלית רצסיבית שגורמת לעליה של בילירובין מצומד (ללא עליה של אנזימי כבד- ALT, AST). תסמונת DJ שפירה כאשר רמת הבילירובין יכולה להגיע לעתים עד 7 מיליגרם לדציליטר, והיא קשורה לבעיה בהפרשה הקניקולארית של בילירובין מצומד מתאי הכבד למרה. לאחר הפיכת הבילירובין לבילירובין מצומד לחומצה גלוקורונית, הוא עובר אל מערכת המרה על ידי טרנספורטר פעיל הידוע כ- MRP2) multiple drug resistance protein 2). פגיעה בטרנספורטר זה גורמת להצטברות של בילירובין מצומד בתוך הכבד. לרוב אין בתסמונת זו סימנים קליניים, והיא מחלה זו שכיחה אצל יהודים ממוצא פרסי (1:1,300) ומתאפיינת במראה מאקרוסקופי שחור של הכבד, כתוצאה מהצטברות פיגמנט.
בתסמונת זו אין מחלה בעיה חסימתית של דרכי המרה. מלחי המרה המופרשים מהכבד אינם תלויים ככל הנראה בפעילותו של הטרנספורטר הפגוע, ולכן אין כולסטאזיס, ואין גרד האופייני לחולי כולסטאזיס. כמו כן, ניתן לאבחן תסמונת זו על בסיס היחס הבלתי רגיל של קופרופורפירינים, כאשר במצב נורמאלי, הקופרופורפירין הדומיננטי הוא 3, ואילו בתסמונת זו כמותו של קופרופורפירין 1 עולה מעבר ל-80%. אף על פי כן רמתם הכללית של הקופרופורפירינים בשתן נשמרת תקינה בתסמונת זו, שהיא המצב היחיד שבו עלייה בבילירובין-ישיר מלווה ברמת קופרופורפירין תקינה בשתן כשמעל 80% ממנו הוא קופרופורפירין 1.
בתסמונת DJ לא ניתן להדגים את כיס המרה בעזרת כולציסטוגרם פומי. אבחון נוסף של תסמונת זו על ידי שימוש בהזרקה תוך-ורידית של ברומו סולפו פטלאין-BSP, אשר עובר בדומה לבילירובין צימוד על ידי UGT ומופרש על ידי אותו הטרנספורטר-MRP2. במתן חומר זה לאדם בריא לאחר 30-45 דקות רמת החומר בנסיוב היא 5-15% מכמות החומר שהוזרק. לעומת זאת, בחולה עם תסמונת DJ, לאחר 30-40 דקות נרשמת ירידה ברמת BSP בנסיוב, אך לאחר 90 דקות הוא חוזר לרמתו המקורית. למעשה, BSP לא מצליח להיות מופרש על ידי MRP2, וחוזר לנסיוב מה שמעיד על הבעיה הקיימת בטרנספורטר.
תסמונת Rotor
תסמונת נדירה, אף היא אוטוסומאלית-רצסיבית אשר דומה קלינית לתסמונת DJ, הבעיה העיקרית הינה צבירה של בילירובין-מצומד בתוך התא. כאשר מזריקים BSP יש היעלמות מאד איטית ואין עלייה נוספת ברמתו, מאחר שהוא נצבר בתוך התאים ההפאטוציטים. פרופיל הקופרופורפירין שונה בתסמונת רוטור. כאשר רמת קופרופורפירין 1 היא כ-60%, אך עדיין רמתו גבוהה יותר מקופרופורפירין 3. בנוסף בתסמונת רוטור אין פיגמנט הפּאטי, והכבד לא משנה את צבעו. בתסמונת Rotor כן ניתן להדגים את כיס המרה על ידי כולציסטוגרם פומי. לרוב, מדובר בפרוגנוזה טובה, ואין צורך בטיפול היות שרוב החולים הינם אסימפטומטיים, פרט להופעת צהבת ללא גרד.
בילירובין נאו-נטאלי
במהלך היריון תקין רמת הבילירובין בנוזל מי השפיר מגיעה בסביבות השבוע ה-19 עד לשבוע ה-22 לשיא של 0.16-0.18 מיליגרם לדציליטר. תמס-דם תוך רחמי עלול לגרום לצהבת של העובר (erythroblastosis fetalis) מה שיכול להגביר באופן ניכר את רמת הבילירובין במי השפיר, שניתן למדוד אותה על ידי סריקה ספקטרופוטומטרית, המבוססת על כך שלבילירובין יש בליעה מרבית באורך גל 454 ננומטר. ייתכן יחד עם זאת, שאם לאישה ההרה יש היפרבילירובינמיה של בילירובין מצומד, הדבר עלול להביא לחדירת בילירובין מצומד ומסיס-מים זה למי השפיר, בהעדר מחלה המוליטית של העובר. בשנים האחרונות, מבחן חודרני זה הוחלף בשיטה רגישה יותר וספציפית של אולטרה-סאונד (Doppler) המודדת את שפיעת הדם בעורק המוח המרכזי, כמדד לאנמיה של העובר. גם במקרים של תמס דם מוגבר בעובר ויצירה מוגברת בילירובין כתוצאה מאי-התאמה באנטיגני הדם בין האם לעובר, הבילירובין בדם טבורי רק לעתים נדירות עולה מעל 5 מיליגרם לדציליטר. זאת כתוצאה ממעבר מהיר ויעיל של בילירובין דרך השליה והרחקתו על ידי דמה של האם.
רוב היילודים מפתחים מצב זמני וחולף של היפרבילירובינמיה בלתי-מצומדת עם צהבת, הנגרמת בדרך כלל על ידי יצירת בילירובין מוגברת כתוצאה מהרס מוגבר של כדוריות אדומות כתוצאה משחלוף דם בין האם לוולד, על ידי הפסקת מנגנון הרחקת בילרובין דרך השליה, והן בגלל אי הבשלות של אנזימי הכבד הקשורים לצימוד בילירובין וגלוקורונאט. פעילות זאת האנזים הכבדי UGT ביילוד היא רק כ 1% מפעילות אנזים זה במבוגרים. רמות גבוהות של בילירובין בילודים יכולות להיגרם בנוסף כתוצאה מפירוק תאי דם אדומים בגלל חוסר התאמה ברכיב ה- Rh בסוג הדם במקרים בהם לאם יש Rh שלילי, ולעובר יש Rh חיובי, או אף לעתים כאשר האם היא עם סוג דם O והעובר עם סוג דם A, B או AB, עלולה האם לפתח נוגדנים לתאי הדם האדומים של הילוד שיביאו להריסתם.
כיוון שיילודים חסרים בשלב זה את חיידקי המעיים, קטנה יכולתם לחזר במעיים בילירובין ל-urobilinogen. רמת הבילרובין הבלתי-מצומד גבוהה, גם כיוון שבעת הלידה, החיידק Bifidobacterium, המסייע בעיבוד הבילירובין, עדיין אינו נוכח במערכת העיכול. חיידק זה מגיע למערכת העיכול של הילוד תוך ימים ספורים באמצעות חלב אם, ואז בדרך כלל, יורדות רמות הבילירובין לתקנן. בנוסף, גדלה פעילות האנזים β-glucuronidase, מה שמגביר ביילודים את ההידרוליזה של בילירובין מצומד לבילירובין בלתי מצומד. רמה מוגברת זו של בילירובין בלתי מצומד במעי מגבירה ספיגה שלו במסלול של המעגל האנטרו-הפאטי, מה שמעלה רמת בילרובין בדם היילוד. חסר בהפרשת בילירובין מצומד ביילודים היא גם הסיבה לצבע החיוור יותר של צואה זו.
יש גם מרכיב של חוסר הבשלות של הטרנספורטר על פני ההפאטוציטים, ואי בשלות של מנגנון הרחקת בילירובין מהכבד לצואה ולשתן. בילודים לאחר היריון מלא, לא עולה רמת בילירובין בנסיוב מעל 12 מיליגרם לדציליטר, ואילו בפגים או ביילודים טרם עת, רמה זו יכולה לעלות על 15 מיליגרם לדציליטר. ביילודים בעיתם (full term) רמת הבילירובין נסוגה לערכים תקינים בדרך כלל תוך שבוע עד שבועיים, ואילו ביילודים עם רמות מוגברות באופן מתמיד יש לטפל בעזרת פוטותרפיה, פנוברביטל, או אף על ידי פלזמה-פרזיס, כל זאת במטרה למנוע מעבר מוגבר של בילירובין בלתי מצומד למוח, ותופעה חמורה של kernicterus. הטיפול הפוטותרפי בעזרת קרינת UV גורם לחלק מהקשרים הכפולים של בילירובין לעבור איזומריזציה, כאשר האיזומר Z,Z הפחות מסיס (צורת טרנס) הופך לאיזומר E,E מסיס יותר (צורת ציס) מה שיעודד הפרשתו בשתן וירידת רמת בילירובין בדם.
סיבה נוספת לרמה גבוה של בילירובין בלתי מצומד יכולה להיגרם על ידי חלב אם (breast milk jaundice), מה שמחייב הפסקת הנקה במקרים אלה. מפגע זה נגרם על ידי מרכיב בלתי מזוהה בחלב אם המגביר את ספיגת בילירובין במעי. מנגנון אפשרי ליתר-בילירובין באותם מקרים של תינוקות הניזונים מהנקה בהשוואה לתינוקות המקבלים מזון פורמולה, היא הרמה המוגברת של האנזים β glucuronidase בחלב האם, המפרק את הבילירובין המצומד, ומגדיל את ספיגת הבילירובין הלא-מצומד במסלול האנטרו-הפאטי.
צהבת מחלב אם משפיעה ב-0.5-2.4% מכלל הלידות, עם נטייה משפחתית למצב זה של 13.9%. התופעה מתחילה בדרך כלל 3-5 ימים מתחילת ההנקה, מגיעה לשיאה תוך שבועיים, ודועכת בהדרגה תוך 3-12 לערכי הנורמה של בילירובין. יש מקרים בסוג זה של צהבת ביילודים שרמת בילירובין בלתי מצומד עלולה אף להגיע ל-20 מיליגרם לדציליטר, מה שמחייב לא רק הפסקת הנקה מיידית , אלא אף טיפול פוטותרפי להפחתת רמה מסוכנת זו.
פענוח תוצאות הבדיקה
אנליזה של סוגי בילירובין בפלזמה מסייעת לבצע אבחנה מבדלת בין סוגי הצהבת השונים. צהבת קדם-כבדית (prehepaic) מביא לעליה משמעותית בבילרובין בלתי ישיר בגלל שחרור ומטבוליזם מוגבר של המוגלובין במצבי תמס-דם, המאטומות, או שטפי דם מסיבות שונות. לעומת זאת במפגעים קדם-כבדיים, בגלל המגבלה של טרנספורט של בילירובין בלתי-ישיר בכמויות גדולות אל תוך הכבד ליצירת בילרובין מצומד, יש רק עלייה קלה אם בכלל ברמת בילרובין מצומד במצבים אלה. ביילודים אנו עשויים למדוד רמות סך-בילרובין של עד 20 או אף יותר מיליגרם לדציליטר, כאשר מקטע בילירובין ישיר יהיה רק 2.5 עד 5.0 מיליגרם לדציליטר. במבוגרים במצבים של צהבת קדם-הפאטית ניתן למדוד בדם סך-בילירובין של 1.5-6.0 מיליגרם לדציליטר, כאשר רמת בילירובין מצומד לא תעלה על 0.1-0.6 מיליגרם לדציליטר. בנוסף, בגלל רמות מוגברות של בילרובין מצומד המופרשות מהכבד, רמת ה-urobilinogen בשתן, ורמת urobilin בצואה מוגברות, אך רמת בילירובין בשתן בצורתו המצומדת היא אפסית.
מפגעי צמקת מסיבות אלכוהוליות ואחרות, דלקת כבד על רקע נגיפי או על רקע רעלים אנדוגניים (נחושת במחלת וילסון, גליקוגן במחלות אגירת גליקוגן), רעלים אקסוגניים דוגמת אצטאמינופן ורעלים שמקורם בצמחים, וכן דלקת כבד אוטו-אימונית: כל התרחישים הללו פוגעים בתפקודי הכבד, ומתאפיינים על ידי הגברה ניכרת בבילירובין מצומד וכן בבילירובין דלתא בנסיוב. רמת סך-בילירובין בפלזמה בצהבת הפאטית היא בין 2ל-25 מיליגרם לדציליטר, כאשר רמת הבילירובין המצומד במפגעים האחרונים היא בין 1 ל-12 מיליגרם לדציליטר. במפגעים הפאטיים הצואה היא בצבע מעט בהיר יותר, ורמת בילירובין בשתן היא ++ עד ++++.
בצהבת חסימתית תוך-כבדית - חסימה של צינורות המרה הקטנים הנמצאים בתוך הכבד, דלקת כבד נגיפית ; דלקת כבד על רקע רעלים ותרופות, שחמת ראשונית של המרה (Primary Biliary Cirrhosis). חסימה תוך-כבדית על רקע מחלות חסימתיות של ורידי הכבד, על רקע הזנה ממושכת תוך-ורידית (TPN), או על רקע מחלת השתל-נגד-המאכסן (Graft-Versus-Host Disease).
חסימה חוץ-כבדית (post hepatic) - חסימה של צינורות המרה הגדולים או של צינור המרה, הנמצאים מחוץ לכבד על רקע של גידולים, או על רקע לא-גידולי כגון אבני מרה (סיבה שכיחה ביותר לחסימה חוץ-כבדית), דלקת לבלב כרונית, דלקת ראשונית צלקתית של דרכי מרה (Primary Sclerosing Cholangitis), או מחלה אוטו-אימונית, או נזק ניתוחי שנגרם להן, סך-בילירובין יכול להגיע בפלזמה לרמה של עד 25 מיליגרם לדציליטר, כאשר רמת בילירובין מצומד נעה בין 5 ל-12 מיליגרם לדציליטר. תרחישים פוסט-הפאטיים מתאיינים בגון בהיר של הצואה,ואילו רמת בילירובין בשתן היא ++++.
רמה מוגברת של בילירובין לא מצומד ניתן למצוא גם במצבים של תת-פעילות של בלוטת התריס, וב-infectious mononucleosis.גם במצבים של חסר ויטמין B12 וחומצה פולית, הגורמים לאריתרופויאזה יעילה באופן חלקי, תהיה הגברה ברמת בילירובין לא מצומד.
הוראות לביצוע הבדיקה
צריך להיות בצום של 4 שעות לפני נטילת הדם. צום ממושך לפני מתן בדיקה בדרך כלל מעלה את תוצאה הבילירובין הבלתי ישיר. הדם צריך להילקח במבחנה כימית (פקק אדום או צהוב) הדגימה חייבת להיות מוגנת מאור ומקוררת שכן בילירובין רגיש לאור ולחום. לקביעת סך-בילירובין (total bilirubin) בשיטת Malloy-Evelyn עם ריאגנט diazo המאוד מקובלת, יש להימנע מדגימה המוליטית כדי לא לקבל תוצאה נמוכה כזובה, ויש להעדיף נסיוב על פלזמה שכן הוספת אלכוהול במהלך ביצוע הבדיקה בשיטה האחרונה, יכולה להשקיע חלבונים מהפלזמה שמפריעים למהלך המדידה.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק