הבדלים בין גרסאות בדף "Muscle-specific kinase (MuSK) autoantibodies"
| שורה 13: | שורה 13: | ||
}} | }} | ||
==מטרת הבדיקה== | ==מטרת הבדיקה== | ||
| − | |||
אבחון וריאנט של MG על רקע נוגדנים עצמיים ל-MuSK, זאת כאשר מבחן הקו-הראשון של חיפוש אחר נוגדנים כנגד הקולטן לאצטילכולין מתקבל שלילי בנבדקים עם אבחנה קלינית ואלקטרו-פיזיולוגית של MG. קביעה כמותית של רמת בסיס של נוגדנים ל-MuSK המאפשרת השוואה עם רמת נוגדנים אלה בבדיקה עתידית אם יש החמרה בתסמיני החולשה. | אבחון וריאנט של MG על רקע נוגדנים עצמיים ל-MuSK, זאת כאשר מבחן הקו-הראשון של חיפוש אחר נוגדנים כנגד הקולטן לאצטילכולין מתקבל שלילי בנבדקים עם אבחנה קלינית ואלקטרו-פיזיולוגית של MG. קביעה כמותית של רמת בסיס של נוגדנים ל-MuSK המאפשרת השוואה עם רמת נוגדנים אלה בבדיקה עתידית אם יש החמרה בתסמיני החולשה. | ||
| − | ==בסיס פיזיולוגי של myasthenia gravis== | + | ==בסיס פיזיולוגי של myasthenia gravis== |
| − | |||
המחלה האוטואימונית myasthenia gravis (להלן MG), היא המפגע השכיח ביותר של הסינפסה הנוירו-מוסקולארית, הפוגעת ב-10-20 איש מתוך 100,000 (עפ"י Phillips ב-Ann NY Acad Sci משנת 2003). למעשה, רק ב-1960 הציע Simpson ב-Scott Med J שמדובר במחלה אוטואימונית, זאת על בסיס התצפיות שלו לפיהן אלה עם MG סבלו בשכיחות גבוהה יותר ממחלת בלוטת תריס אוטואימונית, מדלקת פרקים שגרונית, או מ-SLE. חלפו 16 שנים עד ש-Lindstrom וחב' אישרו במאמר ב-Neurology משנת 1976 את הבסיס האוטואימוני של MG, כאשר מצאו ש-85% מאלה עם MG הכילו נוגדנים עצמיים לקולטנים הניקוטיניים של אצטילכולין (להלן AChR). יחד עם זאת, חלפו עוד 25 שנה, עד ש-Hoch וחב' הדגימו ב-Nat Med משנת 2001, שב-70% מחולי MG שאינם מכילים נוגדנים ל-AChR ומוגדרים כ-seronegatives, ניתן למצוא בנסיוב נוגדנים ל-muscle-specific receptor tyrosine kinase (להלן MuSK-Ab). | המחלה האוטואימונית myasthenia gravis (להלן MG), היא המפגע השכיח ביותר של הסינפסה הנוירו-מוסקולארית, הפוגעת ב-10-20 איש מתוך 100,000 (עפ"י Phillips ב-Ann NY Acad Sci משנת 2003). למעשה, רק ב-1960 הציע Simpson ב-Scott Med J שמדובר במחלה אוטואימונית, זאת על בסיס התצפיות שלו לפיהן אלה עם MG סבלו בשכיחות גבוהה יותר ממחלת בלוטת תריס אוטואימונית, מדלקת פרקים שגרונית, או מ-SLE. חלפו 16 שנים עד ש-Lindstrom וחב' אישרו במאמר ב-Neurology משנת 1976 את הבסיס האוטואימוני של MG, כאשר מצאו ש-85% מאלה עם MG הכילו נוגדנים עצמיים לקולטנים הניקוטיניים של אצטילכולין (להלן AChR). יחד עם זאת, חלפו עוד 25 שנה, עד ש-Hoch וחב' הדגימו ב-Nat Med משנת 2001, שב-70% מחולי MG שאינם מכילים נוגדנים ל-AChR ומוגדרים כ-seronegatives, ניתן למצוא בנסיוב נוגדנים ל-muscle-specific receptor tyrosine kinase (להלן MuSK-Ab). | ||
===נתונים אפידמיולוגיים של MG=== | ===נתונים אפידמיולוגיים של MG=== | ||
| − | |||
לגבי הנתונים בארה"ב, השיעור השנתי של מקרים חדשים של MG אינו עולה על 2 מקרים לכל 100 אלף, ובהתאם מספר המאובחנים עם MG בארה"ב נע על פי הערכות שונות על 0.5-14.2 מקרים ל-100 אלף, אם כי יש נטייה לעליה בשיעורים אלה ב-20 השנים האחרונות בעקבות העלייה בתוחלת החיים, אך גם כתוצאה מאבחון מקרים בקבוצת הגיל הצעירה יותר. בערך 15-20% מהמאובחנים עם MG יחוו בשלב זה או אחר "משבר מיאסטיני", כאשר כ-75% מבין אלה יחוו משבר זה תוך שנתיים מאבחון המחלה אצלם. באשר לשיעורי המחלה בעולם כולו, נציין שבבריטניה מדובר על 15 מקרים לכל 100 אלף, בקרואטיה מדובר על 10 מקרים ל-100 אלף, ואילו בסרדיניה מספר מקרי MG טיפס מ-0.75 ל-100 אלף בשנת 1958, ל-4.5 מקרים לכל 100 אלף בשנת בשנת 1986. | לגבי הנתונים בארה"ב, השיעור השנתי של מקרים חדשים של MG אינו עולה על 2 מקרים לכל 100 אלף, ובהתאם מספר המאובחנים עם MG בארה"ב נע על פי הערכות שונות על 0.5-14.2 מקרים ל-100 אלף, אם כי יש נטייה לעליה בשיעורים אלה ב-20 השנים האחרונות בעקבות העלייה בתוחלת החיים, אך גם כתוצאה מאבחון מקרים בקבוצת הגיל הצעירה יותר. בערך 15-20% מהמאובחנים עם MG יחוו בשלב זה או אחר "משבר מיאסטיני", כאשר כ-75% מבין אלה יחוו משבר זה תוך שנתיים מאבחון המחלה אצלם. באשר לשיעורי המחלה בעולם כולו, נציין שבבריטניה מדובר על 15 מקרים לכל 100 אלף, בקרואטיה מדובר על 10 מקרים ל-100 אלף, ואילו בסרדיניה מספר מקרי MG טיפס מ-0.75 ל-100 אלף בשנת 1958, ל-4.5 מקרים לכל 100 אלף בשנת בשנת 1986. | ||
| שורה 29: | שורה 26: | ||
===מיאסתניה גראביס על רקע נוגדנים עצמיים ל-MuSK=== | ===מיאסתניה גראביס על רקע נוגדנים עצמיים ל-MuSK=== | ||
| − | |||
MuSK הוא טירוזין קינאזה טרנס-ממברנאלי בעל משקל מולקולארי מקורב של 100,000 דלטון. חלבון זה נוקה במקור מהגוף החשמלי העתיר בסינפסות של דג הסחוס Torpedo californica על ידי Jennings וחב' בשנת 1993 ופורסם ב-Proc Natl Acad Sci USA. בצומת (junction) עצב-שריר בבעלי-חוליות, מופרשים בקצוות האקסונים המוטוריים גופיפים (vesicles) המפרישים אצטילכולין הנקלט על ידי הקולטנים הבתר-סינפטיים של נוירוטרנסמיטור זה. וכך מתחיל תהליך כיווץ השריר. מעבר יעיל של הנוירוטרנמיטור תלוי במארז הדוק של של הקולטנים של אצטיל כולין לצברים (clusters) של קולטנים אלה, ומי שחיוני ליציבות של צברי קולטנים אלה הוא MuSK המהווה כמובן חלק מהקולטן וממוקם בקצה ה-C טרמינאלי שלו. (עפ"י DeChiara וחב' ב-Cell משנת 1996, וכן Kummer וחב' ב-Curr Opin Neurobiol משנת 2006 ו-Wu וחב' ב-Development משנת 2010). | MuSK הוא טירוזין קינאזה טרנס-ממברנאלי בעל משקל מולקולארי מקורב של 100,000 דלטון. חלבון זה נוקה במקור מהגוף החשמלי העתיר בסינפסות של דג הסחוס Torpedo californica על ידי Jennings וחב' בשנת 1993 ופורסם ב-Proc Natl Acad Sci USA. בצומת (junction) עצב-שריר בבעלי-חוליות, מופרשים בקצוות האקסונים המוטוריים גופיפים (vesicles) המפרישים אצטילכולין הנקלט על ידי הקולטנים הבתר-סינפטיים של נוירוטרנסמיטור זה. וכך מתחיל תהליך כיווץ השריר. מעבר יעיל של הנוירוטרנמיטור תלוי במארז הדוק של של הקולטנים של אצטיל כולין לצברים (clusters) של קולטנים אלה, ומי שחיוני ליציבות של צברי קולטנים אלה הוא MuSK המהווה כמובן חלק מהקולטן וממוקם בקצה ה-C טרמינאלי שלו. (עפ"י DeChiara וחב' ב-Cell משנת 1996, וכן Kummer וחב' ב-Curr Opin Neurobiol משנת 2006 ו-Wu וחב' ב-Development משנת 2010). | ||
| − | ===המבנה של MuSK ושל הקומפלקס של MuSK=== | + | ===המבנה של MuSK ושל הקומפלקס של MuSK=== |
| − | + | הגן MuSK ממוקם בעכבר בכרומוזום 4, אך באדם הוא ממוקם על כרומוזום 9. בגן 14 exons התורמים ליצירת של מספר שעתוקים (transcripts), שרובם מקודדים בשינויים קלים לפוליפפטיד השלם (100,000 דלטון) המהווה את המבנה הטרנס-ממברנאלי החוצה את ממברנת התא, כאשר הקצה ה-C טרינאלי של MuSK נמצא בציטפלזמה, והקצה ה-N טרמינאלי משתרבב מחוץ לתא. החלק החוץ-תאי של MuSK מורכב מ-4 מקטעים דמויי-אימונוגלובולין ([[IgG3]], [[IgG2]], [[IgG1]] ו-[[IgG4]]) וביניהם מקטע עתיר בציסטאין המוגדר כ-C6. המקטע של MuSK הממוקם בתוך הממברנה קרוי TM או transmembrane domain, והמקטע הציטופלזמטי הראשון של MuSK הסמוך לממברנה קרוי JM אוjuxtamembrane domain, ומיד אחריו ממוקם הקטע הקטליטי של tyrosine kinase. | |
| − | הגן MuSK ממוקם בעכבר בכרומוזום 4, אך באדם הוא ממוקם על כרומוזום 9. בגן 14 exons התורמים ליצירת של מספר שעתוקים (transcripts), שרובם מקודדים בשינויים קלים לפוליפפטיד השלם (100,000 דלטון) המהווה את המבנה הטרנס-ממברנאלי החוצה את ממברנת התא, כאשר הקצה ה-C טרינאלי של MuSK נמצא בציטפלזמה, והקצה ה-N טרמינאלי משתרבב מחוץ לתא. החלק החוץ-תאי של MuSK מורכב מ-4 מקטעים דמויי-אימונוגלובולין (IgG3, IgG2, IgG1 ו-IgG4) וביניהם מקטע עתיר בציסטאין המוגדר כ-C6. המקטע של MuSK הממוקם בתוך הממברנה קרוי TM או transmembrane domain, והמקטע הציטופלזמטי הראשון של MuSK הסמוך לממברנה קרוי JM אוjuxtamembrane domain, ומיד אחריו ממוקם הקטע הקטליטי של tyrosine kinase. | ||
| שורה 43: | שורה 38: | ||
===איתות דרך קולטן MuSK=== | ===איתות דרך קולטן MuSK=== | ||
| − | |||
הליגנד הנקשר ל-MuSK הוא פרוטאו-גליקן מסוג heparin-sulfate הידוע כ-agrin, המופרש מקצות תאי עצב מוטורי (עפ"י Mittaud וחב' ב-Mol Cell Biol משנת 2004), וכך MuSK יוצר את הליבה של קומפלקס איתות רב-חלבוני. הפרוטאוגליקן agrin אינו נקשר ישירות עם MuSK, אלא שהוא נקשר למרכיב בקומפלקס זה הידוע כ-LRP4 או low-density lipoprotein receptor-related protein 4 (עפ"י Kim וחב' ב-Cell משנת 2008 ו-Zhang וחב' ב-Neuron משנת 2008). שני החלבונים, LRP4 ו-MuSK, מגיבים ביניהם דרך המקטעים החוץ-תאיים שלהם. | הליגנד הנקשר ל-MuSK הוא פרוטאו-גליקן מסוג heparin-sulfate הידוע כ-agrin, המופרש מקצות תאי עצב מוטורי (עפ"י Mittaud וחב' ב-Mol Cell Biol משנת 2004), וכך MuSK יוצר את הליבה של קומפלקס איתות רב-חלבוני. הפרוטאוגליקן agrin אינו נקשר ישירות עם MuSK, אלא שהוא נקשר למרכיב בקומפלקס זה הידוע כ-LRP4 או low-density lipoprotein receptor-related protein 4 (עפ"י Kim וחב' ב-Cell משנת 2008 ו-Zhang וחב' ב-Neuron משנת 2008). שני החלבונים, LRP4 ו-MuSK, מגיבים ביניהם דרך המקטעים החוץ-תאיים שלהם. | ||
| שורה 53: | שורה 47: | ||
===התפקיד של MuSK ב-MG=== | ===התפקיד של MuSK ב-MG=== | ||
| − | |||
כאמור נוגדנים כנגד MuSK מוצאים בחולים עם MG להם אין נוגדנים כנגד הקולטן לאצטילכולין. בחולים אלה עדיין מוצאים אובדן אוטואימוני של פעילות הקולטנים לאצטילכולין (עפ"י Barrett-Jolley ב-Pflügers Archiv משנת 1994), אך צורת המחלה נראית שונה מ-MG קלאסית במספר פרמטרים: יותר שכיחה בנשים, פחות מעורבות של העיניים, יש יותר חולשה בצוואר, בשריר הסוגר העליון (oropharynx), בשרירי הכתף, ושכיחות גבוהה יותר בקרב אפרו-אמריקנים. (עפ"י Evoli וחב' ב-Brain משנת 2003 ו-Sanders וחב' בAnn Neurol משנת 1987). במודלים קדם-קליניים של MG מהסוג של נוגדנים עצמיים ל-MuSK, מתן 3,4diaminopyridine הגביר את ההפרשה של אצטילכולין והפחית את חולשת השרירים (עפ"י Morsch וחב' ב-J Physiol משנת 2013). | כאמור נוגדנים כנגד MuSK מוצאים בחולים עם MG להם אין נוגדנים כנגד הקולטן לאצטילכולין. בחולים אלה עדיין מוצאים אובדן אוטואימוני של פעילות הקולטנים לאצטילכולין (עפ"י Barrett-Jolley ב-Pflügers Archiv משנת 1994), אך צורת המחלה נראית שונה מ-MG קלאסית במספר פרמטרים: יותר שכיחה בנשים, פחות מעורבות של העיניים, יש יותר חולשה בצוואר, בשריר הסוגר העליון (oropharynx), בשרירי הכתף, ושכיחות גבוהה יותר בקרב אפרו-אמריקנים. (עפ"י Evoli וחב' ב-Brain משנת 2003 ו-Sanders וחב' בAnn Neurol משנת 1987). במודלים קדם-קליניים של MG מהסוג של נוגדנים עצמיים ל-MuSK, מתן 3,4diaminopyridine הגביר את ההפרשה של אצטילכולין והפחית את חולשת השרירים (עפ"י Morsch וחב' ב-J Physiol משנת 2013). | ||
| שורה 61: | שורה 54: | ||
===הפעילות הביולוגית של MuSK=== | ===הפעילות הביולוגית של MuSK=== | ||
| − | |||
נראה ש-MuSK משחק תפקיד קואורדינטיבי מרכזי ביצירת ה-neuromuscular junction או NMJ בעת התפתחות העוברית. עוברי עכברים החסרים MuSK נכשלים ביצירת NMJs יציבים, מה גורם להם לשיתוק ולמוות עוד בטרם הלידה. בשלב ההתפתחות העוברית, צברים של AChR נוצרים על פני סיבי שריר בלתי-בשלים לפני הבשלת תאי עצב מוטוריים (Harris וחב' ב-Philos Trans R Soc Lond B משנת 1981, ו-Lin וחב' ב-Nature משנת 2001). ואמנם, צברי AChR מוגבלים לחלק המרכזי של סיב השריר, אזור בו הביטוי של MuSK הוא הניכר ביותר. | נראה ש-MuSK משחק תפקיד קואורדינטיבי מרכזי ביצירת ה-neuromuscular junction או NMJ בעת התפתחות העוברית. עוברי עכברים החסרים MuSK נכשלים ביצירת NMJs יציבים, מה גורם להם לשיתוק ולמוות עוד בטרם הלידה. בשלב ההתפתחות העוברית, צברים של AChR נוצרים על פני סיבי שריר בלתי-בשלים לפני הבשלת תאי עצב מוטוריים (Harris וחב' ב-Philos Trans R Soc Lond B משנת 1981, ו-Lin וחב' ב-Nature משנת 2001). ואמנם, צברי AChR מוגבלים לחלק המרכזי של סיב השריר, אזור בו הביטוי של MuSK הוא הניכר ביותר. | ||
גרסה מ־13:51, 13 בדצמבר 2021
| מדריך בדיקות מעבדה | |
| Muscle-Specific Kinase (MuSK) autoantibodies | |
|---|---|
| מעבדה | כימיה בדם |
| תחום | הערכת התגובה האוטו-אימונית ב-myasthenia gravis |
| טווח ערכים תקין | נוגדנים כנגד MuSK בריכוז השווה או נמוך מ-0.02 ננומול'/ליטר |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
אבחון וריאנט של MG על רקע נוגדנים עצמיים ל-MuSK, זאת כאשר מבחן הקו-הראשון של חיפוש אחר נוגדנים כנגד הקולטן לאצטילכולין מתקבל שלילי בנבדקים עם אבחנה קלינית ואלקטרו-פיזיולוגית של MG. קביעה כמותית של רמת בסיס של נוגדנים ל-MuSK המאפשרת השוואה עם רמת נוגדנים אלה בבדיקה עתידית אם יש החמרה בתסמיני החולשה.
בסיס פיזיולוגי של myasthenia gravis
המחלה האוטואימונית myasthenia gravis (להלן MG), היא המפגע השכיח ביותר של הסינפסה הנוירו-מוסקולארית, הפוגעת ב-10-20 איש מתוך 100,000 (עפ"י Phillips ב-Ann NY Acad Sci משנת 2003). למעשה, רק ב-1960 הציע Simpson ב-Scott Med J שמדובר במחלה אוטואימונית, זאת על בסיס התצפיות שלו לפיהן אלה עם MG סבלו בשכיחות גבוהה יותר ממחלת בלוטת תריס אוטואימונית, מדלקת פרקים שגרונית, או מ-SLE. חלפו 16 שנים עד ש-Lindstrom וחב' אישרו במאמר ב-Neurology משנת 1976 את הבסיס האוטואימוני של MG, כאשר מצאו ש-85% מאלה עם MG הכילו נוגדנים עצמיים לקולטנים הניקוטיניים של אצטילכולין (להלן AChR). יחד עם זאת, חלפו עוד 25 שנה, עד ש-Hoch וחב' הדגימו ב-Nat Med משנת 2001, שב-70% מחולי MG שאינם מכילים נוגדנים ל-AChR ומוגדרים כ-seronegatives, ניתן למצוא בנסיוב נוגדנים ל-muscle-specific receptor tyrosine kinase (להלן MuSK-Ab).
נתונים אפידמיולוגיים של MG
לגבי הנתונים בארה"ב, השיעור השנתי של מקרים חדשים של MG אינו עולה על 2 מקרים לכל 100 אלף, ובהתאם מספר המאובחנים עם MG בארה"ב נע על פי הערכות שונות על 0.5-14.2 מקרים ל-100 אלף, אם כי יש נטייה לעליה בשיעורים אלה ב-20 השנים האחרונות בעקבות העלייה בתוחלת החיים, אך גם כתוצאה מאבחון מקרים בקבוצת הגיל הצעירה יותר. בערך 15-20% מהמאובחנים עם MG יחוו בשלב זה או אחר "משבר מיאסטיני", כאשר כ-75% מבין אלה יחוו משבר זה תוך שנתיים מאבחון המחלה אצלם. באשר לשיעורי המחלה בעולם כולו, נציין שבבריטניה מדובר על 15 מקרים לכל 100 אלף, בקרואטיה מדובר על 10 מקרים ל-100 אלף, ואילו בסרדיניה מספר מקרי MG טיפס מ-0.75 ל-100 אלף בשנת 1958, ל-4.5 מקרים לכל 100 אלף בשנת בשנת 1986.
MG יכולה להתרחש בכל גיל כאשר בין נשים השכיחות מגיעה לשיאה בעשור השלישי לחיים, בעוד שבין גברים המחלה מאובחנת בעיקר בעשורים ה-5 וה-6 לחיים. גיל האבחון הממוצע הוא 28 שנה בין נשים, ובין הגברים -42 שנה. מוכרת התופעה של MG חולפת ביילודים ותינוקות בגיל הרך אליהם הועברו נוגדנים כנגד AChR של האם שעברו לעובר דרך השליה. רוב התינוקות הנולדים לאימהות עם MG, מכילים נוגדנים אלה בשעת הלידה, אך 10-20%מתוכם מפתחים MG בגיל הרך, זאת כנראה כתוצאה מהפעולה המגינה של α-fetoprotein המעכב את קישורו של הנוגדן ל-AChR לקולטן זה. יש המציעים לבדוק את רמת נוגדנים אלה באישה ההרה הידועה כלוקה ב-MG, ואם רמתם גבוהה ביוחד, יש הגורסים שכדאי להפחית רמה זו על ידי plasmapheresis.
מקובל ששכיחות MG בנשים, ביחס לזו בגברים, היא 3:2, כאשר השכיחות בנשים דווקא גבוהה יותר באלו בנות 20-30 שנה, כאשר בין הגברים גיל האבחון גבוה ב-13-20 שנה. ההתבטאות העינית (ocular) של MG שכיחה יותר בקרב גברים. הופעת MG בקרב ילדים שכיחה יותר בקרב זכרים מאשר בנקבות ביחס של 5:1. MG בגיל הצעיר שכיחה מעט יותר בקרב אסיאתים מאשר בקבוצות אתניות אחרות.
מיאסתניה גראביס על רקע נוגדנים עצמיים ל-MuSK
MuSK הוא טירוזין קינאזה טרנס-ממברנאלי בעל משקל מולקולארי מקורב של 100,000 דלטון. חלבון זה נוקה במקור מהגוף החשמלי העתיר בסינפסות של דג הסחוס Torpedo californica על ידי Jennings וחב' בשנת 1993 ופורסם ב-Proc Natl Acad Sci USA. בצומת (junction) עצב-שריר בבעלי-חוליות, מופרשים בקצוות האקסונים המוטוריים גופיפים (vesicles) המפרישים אצטילכולין הנקלט על ידי הקולטנים הבתר-סינפטיים של נוירוטרנסמיטור זה. וכך מתחיל תהליך כיווץ השריר. מעבר יעיל של הנוירוטרנמיטור תלוי במארז הדוק של של הקולטנים של אצטיל כולין לצברים (clusters) של קולטנים אלה, ומי שחיוני ליציבות של צברי קולטנים אלה הוא MuSK המהווה כמובן חלק מהקולטן וממוקם בקצה ה-C טרמינאלי שלו. (עפ"י DeChiara וחב' ב-Cell משנת 1996, וכן Kummer וחב' ב-Curr Opin Neurobiol משנת 2006 ו-Wu וחב' ב-Development משנת 2010).
המבנה של MuSK ושל הקומפלקס של MuSK
הגן MuSK ממוקם בעכבר בכרומוזום 4, אך באדם הוא ממוקם על כרומוזום 9. בגן 14 exons התורמים ליצירת של מספר שעתוקים (transcripts), שרובם מקודדים בשינויים קלים לפוליפפטיד השלם (100,000 דלטון) המהווה את המבנה הטרנס-ממברנאלי החוצה את ממברנת התא, כאשר הקצה ה-C טרינאלי של MuSK נמצא בציטפלזמה, והקצה ה-N טרמינאלי משתרבב מחוץ לתא. החלק החוץ-תאי של MuSK מורכב מ-4 מקטעים דמויי-אימונוגלובולין (IgG3, IgG2, IgG1 ו-IgG4) וביניהם מקטע עתיר בציסטאין המוגדר כ-C6. המקטע של MuSK הממוקם בתוך הממברנה קרוי TM או transmembrane domain, והמקטע הציטופלזמטי הראשון של MuSK הסמוך לממברנה קרוי JM אוjuxtamembrane domain, ומיד אחריו ממוקם הקטע הקטליטי של tyrosine kinase.
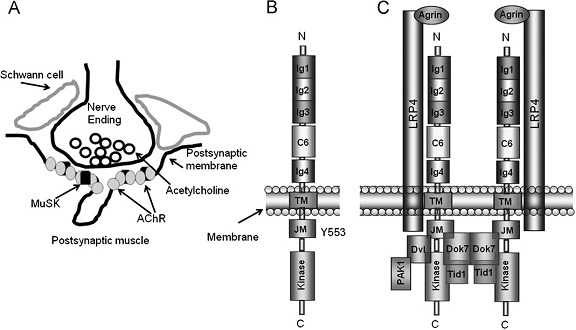
(A) בצומת הנוירו-מוסקולארית מיקומו של MuSK כחלק מהממברנה הבתר-סינפטית ובסמוך לקולטני אצטילכולין.
(B) מבנה החלבון MuSK שמשקלו המולקולארי כ-100 אלף דלטון כאשר הקצה ה-N טרמינאלי שלו הוא חוץ תאי, והקצה ה-N טרמינאלי הוא ציטופלזמטי.
(C) המבנה הדימרי השלם של MuSK.
להשלים את תמונת הקומפלקס של MuSK נתעכב על 3 מרכיבים נוספים: החלבון Tid1 או tumourous imaginal discs preotein, נקשר באופן מובנה (constitutive) לחלק הציטופלזמי של MuSK (עפ"י Linnoila וחב' ב-Neuron משנת 2008). חלבון נוסף Dvl או disheveled (חלבון סתור) נקשר למקטעי JM והקינאזה של MuSK, והוא שכורך את MuSK עם PAK1 או p21-activated kinase (עפ"י Luo וחב' ב-Neuron משנת 2002). כל המרכיבים הללו של קומפלקס האיתות של MuSK, נדרשים לתווך ביצירת צברי AChR בתגובה ל-agrin.
איתות דרך קולטן MuSK
הליגנד הנקשר ל-MuSK הוא פרוטאו-גליקן מסוג heparin-sulfate הידוע כ-agrin, המופרש מקצות תאי עצב מוטורי (עפ"י Mittaud וחב' ב-Mol Cell Biol משנת 2004), וכך MuSK יוצר את הליבה של קומפלקס איתות רב-חלבוני. הפרוטאוגליקן agrin אינו נקשר ישירות עם MuSK, אלא שהוא נקשר למרכיב בקומפלקס זה הידוע כ-LRP4 או low-density lipoprotein receptor-related protein 4 (עפ"י Kim וחב' ב-Cell משנת 2008 ו-Zhang וחב' ב-Neuron משנת 2008). שני החלבונים, LRP4 ו-MuSK, מגיבים ביניהם דרך המקטעים החוץ-תאיים שלהם.
בהיקשרו אל agrin ,MuSK שולח signal דרך רצף של 3 חלבונים :Casein kinase 2 או CK2 הגורם לפוספורילציה של שיירי serine ב-MuSK, מארגן את שלד ה-actin מה שמסייע לוויסות של תהליך האגרגציה של קולטני אצטילכולין (עפ"י Cheusova וחב' ב-Genes Develop משנת 2006; החלבון Dok-7(עפ"י Okada וחב' ב-Science משנת 2006)ו-rapsin שחשיבותו ביצירת צברי AChRs. החלבון המתאם DOK7 (או downstream-of-tyrosine-kinase-7) נקשר ל-motif של הטירוזין המזורחן במקטע JM של MuSK שכינויו NPXY553 (עפ"י Bergamin וחב' ב-Cell Mol משנת 2010). מעורבות של שלושת חלבונים אלה נדרשת להשרות יצירת צברים (clusters) של קולטני אצטילכולין. שני החלבונים CK2 ו-Dok-7, נחוצים ליצירת צומת (junction) נוירו-מוסקלארי תקינה, כיוון שעכברים החסרים Dok-7 נכשלו ביצור צברי קולטנים של אצטילכולין, וכמו כן הפחתה מושרית ביצירת CK2 פגעה בגיוס של AChR ליצירת הצברים האמורים.
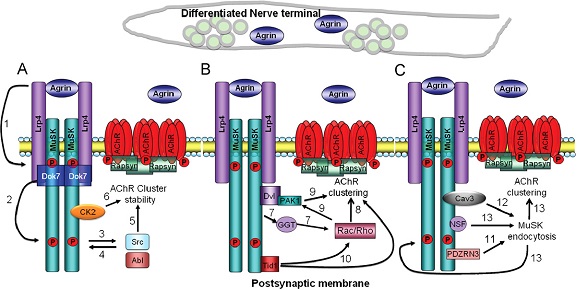
(A) קישור agrin לתלכיד Lrp4-MuSK (חץ 1), גורם לאוטו-פוספורילציה של טירוזין Y533, ועל ידי כך מגייס דימר של Dok7 (חץ 2). יצירת טטרמר יציב (2+2) של MuSK-Dok7 מעדיפה אוטו-פוספורילציה נוספת של שיירי טירוזין (חץ 3) מה שמשפעל טירוזין-קינאזות שאינם מהווים חלק מהקולטן, כגון Abl ו-Src (חץ 4). קינאזות אלו יכולות לשמש כמשוב חיובי לשפעול שלMuSK (חץ 5). הקינאזות Abl ו-Src חשובות לייצוב צברי AChR המתהווים. ייצוב זה כולל פוספורילציה של טירוזין בתת היחידה β של AChR. כאן מגויס rapsyn המסייע לקשור את AChR לשלד הציטוזולי. כעת מתרחשת פוספורילציה של שיירי serine על MuSK על ידיcasein kinase 2 או CK2, לייצוב צברי AChR (חץ 6).
(B) חלבון MuSK משפעל אתgeranylgeranyl I או GGT (חץ 7), והאחרון בתגובה משפעל את ה-GTPase הקטנים, Rou ו-Rac (חץ 8), כאשר 2 אלה מסייעים להגדלת צברי מיקרו שלAChR ליצירת צברים גדולים (חץ 9). מולקולות Rac משופעלות פועלות דרךPAK I kinase לסייע ברה-ארגון של actin ציטופלזמטי, וביצירת צברי AChR (חץ 10). בשלב זה Tid1 פועל דרך Rac להחיש יציר, צבריAChR (חץ 11).
(C) בשלב זה E3 ligase PDZRN3 גורם ל-MuSK תהליך שלubiquitination (חץ 12). ה-MuSK המשופעל נקשר ל-caveolin3, (חץ 13). החדרה (אינטרנליזציה) של MuSK אל תוך התא כרוכה עם שפעול מלא של MuSK ויצירת צברי AChR.
התפקיד של MuSK ב-MG
כאמור נוגדנים כנגד MuSK מוצאים בחולים עם MG להם אין נוגדנים כנגד הקולטן לאצטילכולין. בחולים אלה עדיין מוצאים אובדן אוטואימוני של פעילות הקולטנים לאצטילכולין (עפ"י Barrett-Jolley ב-Pflügers Archiv משנת 1994), אך צורת המחלה נראית שונה מ-MG קלאסית במספר פרמטרים: יותר שכיחה בנשים, פחות מעורבות של העיניים, יש יותר חולשה בצוואר, בשריר הסוגר העליון (oropharynx), בשרירי הכתף, ושכיחות גבוהה יותר בקרב אפרו-אמריקנים. (עפ"י Evoli וחב' ב-Brain משנת 2003 ו-Sanders וחב' בAnn Neurol משנת 1987). במודלים קדם-קליניים של MG מהסוג של נוגדנים עצמיים ל-MuSK, מתן 3,4diaminopyridine הגביר את ההפרשה של אצטילכולין והפחית את חולשת השרירים (עפ"י Morsch וחב' ב-J Physiol משנת 2013).
MG עם נוגדנים עצמיים כנגד MuSK היא תרחיש נדיר יחסית המהווה רק 5-8% מכלל מקרי MG. נתןנים אפידמיולוגיים פורמאליים באשר לשכיחות של MuSK-MG, קיימים רק לגבי שני אזורים באירופה, עם שכיחות של 2.9 מקרים לכל מיליון איש באוכלוסייה ביוון, ו-1.9 מקרים לכל מיליון בדרום הולנד (עפ"י Niks וחב' ב-J Neurol Neurosurg Psychiatry משנת 2007 ו-Carr וחב' ב- BMC Neurol משנת 2010). כאשר רק להמחשה עפ"י Carr השכיחות של AChR-MG גבוהה מהמצופה, עם 70-163 מקרים למיליון. מספר המאובחנים עם MuSK-MG המדווחים ממרכזים רפואיים אחדים של MG, מרמז על דעיכה במספר מרקרים ככל שנעים דרומה מצפון אירופה לדרומה.
ההשפעה יכולה להיות גנטית או סביבתית, שכן בעוד ש-AChR-MG כרוך עם HLA-B8DR3 (עפ"י Compston וחב' ב-Brain משנת 1980) וכן עם HLA-A02 ו-HLH-A25 (עפ"י Karmouch וחב' ב-Chem Biol Interact משנת 2012), הרי ש-MuSK-MG כרוך עם HLA-DR14-DQ5 (עפ"י Niks וחב' ב-Neurology משנת 2006), מה שמרמז על גורמים גנטיים שונים בהתפתחות כל אחת מ-2 הצורות של MG. בנוסף, המרכיב הגנטי הבא לביטוי בהתרחשות MG, בולט בעובדה ששכיחות מחלה זו גבוהה משמעותית בקרה אפרו-אמריקנים (Oh וחב' ב-Muscle Nerve משנת 2006, ו-Sanders וחב' ב-Neurology משנת 2003). כך על פי Oh באלבאמה לדוגמה, בשחורים במדינה זו בכ-50% מוצאים את צורת MuSK-MG בעוד שבין הלבנים באלאבמה רק ב-17% מוצאים סוג זה של MG. גם ממצאיהם של Burns וחב' ב-Neurology משנת 2008 תומכים בנתונים של Ho.
הפעילות הביולוגית של MuSK
נראה ש-MuSK משחק תפקיד קואורדינטיבי מרכזי ביצירת ה-neuromuscular junction או NMJ בעת התפתחות העוברית. עוברי עכברים החסרים MuSK נכשלים ביצירת NMJs יציבים, מה גורם להם לשיתוק ולמוות עוד בטרם הלידה. בשלב ההתפתחות העוברית, צברים של AChR נוצרים על פני סיבי שריר בלתי-בשלים לפני הבשלת תאי עצב מוטוריים (Harris וחב' ב-Philos Trans R Soc Lond B משנת 1981, ו-Lin וחב' ב-Nature משנת 2001). ואמנם, צברי AChR מוגבלים לחלק המרכזי של סיב השריר, אזור בו הביטוי של MuSK הוא הניכר ביותר.
יש ראיות לכך שהאיתות המתחיל במקור מאינטראקציה של agrin ו-MuSK, נחוץ לייצב את הסינפסות העובריות. כאשר השתמשו ב-promoter של actin לגרום אופן מלאכותי לרמות גבוהות של ביטוי MuSK לאורך סיב השריר העוברי, הופיעו צברי AChR באזורים יותר דיסטאלים של הסיב העצבי (Kim ו-Burden ב-Nat Neurosci משנת 2008). מחקרים בעוברים של דגי zebra, גם כן מצביעים על תפקידו של MuSK בהכוונה של אקסונים מוטוריים מתפתחים של תאי עצב.
הפרוטאו-גליקן agrin הוא כפי שידוע כיום המשפעל היעיל ביותר של MuSK. מחקרים עם החלק התוך-תאי המבודד של MuSK מצביעים על כך שהפוספורילציה העצמית של טירוזין בעמדה 533 (מה שמופיע כ-Y553) מקדימה את האוטו-פוספורילציה של 3 שיירי טירוזין אחרים (בעמדות 750, 754ו-755), הממוקמות בלולאת השפעול של מקטע הקינאזה (עפ"י Till וחב' ב-Structure משנת 2002). נראה שהזרחון של שלושת שיירי הטירוזין האחרונים חיוני להעברת MuSK לפאזה פעילה ויציבה. במכרסמים ובאדם הקצה הקרבוקסילי התוך-תאי של MuSK הידוע כ-VXV, מעודד את הקישור של PDZRN3, שהוא האנזים E3 ubiquitin ligase. כאשר תאי שריר נחשפים ל-agrin, הופך MuSK למצע לפעילות האנזים PDZRN3 (עפ"י Lu וחב' ב-J Cell Biol משנת 2007). ביטוי-יתר של PDZRN3 מפחית את הביטוי של MuSK על פני ממברנת תאי השריר, בעוד שביטוי-חסר של אנזים זה מגדיל את רמות MuSK על פני הממברנה. חוקרים אחרים הראו ש-NSF או N-ethylmalemide Sensitive Factor, נדרש לצורך השפעול של MuSK על ידי Agrin וההחדרה שלו אל תוך התא, שהם 2 תהליכים משולבים (Zhu וחב' ב-J Neurosci משנת 2008). במחקר של Hezel וחב' ב-Mol Biol Cell משנת 2010 הודגם שקישור agrin מעודד את קישור MuSK ל-caveolin-3, שידוע בפעילותו של יצירת צברי AChR ומעורבותו בפעילות הנוירו-מוסקלארית במתחם הסינפסה.
נראה שתהליך האיגור (aggregation) ויצירת הצברים של קולטני אצטילכולין דורש את פעילותם של 2 חלבוני G מאותתים, Rac ו-Rou, בעלי פעילות של האנזים GTPase שמשקלם המולקולארי 21,000 דלטון (Weston וחב' ב-J Biol Chem משנת 2003). כאשר מוסיפים agrin לתאי שריר, השפעול של MuSKוהזרחון של שיירי טירוזין של האנזים geranylgeranyl transferase I גורם לשפעול של Rac I וליצירה של מיקרו-צברים של AChR (עפ"י Lou וחב' ב-Neuron משנת 2013). השפעול של Rac מלווה על ידי שפעול של Rou, וזה פועל על פי הסברה דרך Pak I להגדיל את המיקרו-צברים של AChR והפיכתם לצברים גדולים (בקוטר של מעל 10 מיקרון) (Lou וחב' ב-Neuron משנת 2002).
שני ה-tyrosine kinases הציטופלזמטיים, Abl ו-Src, גם כן משופעלים על ידי MuSK. שתי קינאזות אלה חופפות בפעילותן, בתחזוק השפעול של MuSKתוך זרחון שייר טירוזין 390 בתת היחידה β של AChR. זרחון אחרון זה מגייס את החלבון המתאם rapsyn, ועל ידי כך מייצב את צברי AChR (עפ"י Borgers וחב' ב-J Neurosci משנת 2008). יש לציין שפעילות MuSK תלויה במנגנוני משוב חיוביים ושליליים: לדוגמה, Abl kinase פועל כמשוב לאחור לסייע בזרחון של MuSK, אך לעומת זאת מערכות אחרות דווקא פועלות למנוע את גידולם של צברי AChR. לדוגמה, השפעול של MuSK מאתחל מסלול של משוב שלילי בו מעורב האנזים tyrosine phosphatase, הידוע כ-Shp2 (עפ"י Qian וחב' ב-BMC Neurosci משנת 2008).
יתרה מכך, אצטילכולין המופרש על ידי קצוות העצבים המתהווים, פועל דרך האנזימים calpain ו-5cyclin-dependent kinase הפועלים במתחם הבתר-סינפטי, כדי לגרום לפירוק צברי AChR. כתגובה, מערכת ה-agrin-MuSK-rapsyn פועלת באופן מקומי כדי למנוע תהליך זה של פירוק צברי AChR, על ידי בידודו של rapsyn מיתר מרכיבי המערכת (Chen וחב' ב-Neuron משנת 2007).
MuSK מבוטא גם כן במוח ובתאי זרע של יונקים. כדי לבחון את המשמעות של MuSK בתאי עצב של ה-CNS, הוזרק להיפוקמפוס של מוח חולדות antisense oligonucleotide, על ידי Garcia-Osta וחב' ב-J Neurosci משנת 2006. דיכוי של ביטוי MuSK בהיפוקמפוס, גרם לאי-סדירות בתהליכי זיכרון. בחלקם המרכזי של תאי זרע יש ביטוי של הצורה המקוטעת (truncated) של MuSK המופיעה בסמוך ל-agrin, ל-rapsyn ולצורה הנוירונית של הקולטנים ל-AChR, צורת alfa7 בתאי זרע (עפ"י Kumar וחב' ב-Biochem Biophys Res Commun משנת 2006).
מחלות מולדות ואוטואימוניות הפועלות על מערכת MuSK
מספר תסמונות מיאסטיניות נדירות נגרמות על ידי מוטציות ב-rapsyn, ב-DOK7 או ב-MUSK. אנשים עם מוטציה ב-MuSK, מראים כצפוי חסכים ביצירת צברי AChR בתר-סינפטיים, כמו גם בהתמיינות (דיפרנציאציה) של קצות עצבים במתחם הקדם-סינפטי (Chevessier וחב' ב-Hum Mol Genet משנת 2004). מעט נדירים פחות (בערך מקרה אחד ל-100,000) הם המקרים של MG אוטואימונית הנגרמת על ידי נוגדנים כנגד MuSK. כאשר הזריקו לעכברים IgG שנלקח מאנשים שנמצאו חיוביים לנוכחות נוגדני אנטי-MuSK, הביא הדבר להיעלמות של MuSK מהממברנה הבתר-סינפטית (Cole וחב' ב-J Physiol (Lond) משנת 2010). פעולה זו גרמה לפירוק צברי AChR בתר-סינפטיים ולעייפות וחולשה בעכברים המטופלים. בניסוי נוסף של Cole וחב' שתואר ב-Ann Neurol משנת 2008, הוזרקו עכברים בני 6 שבועות מזני C57BL/6J ו-FVB/NJ עם IgG מנסיוב אנשים שאובחנו עם MG על רקע נוגדנים ל-MuSK. הזרקות תוך-צפקיות למשך 45 יום במינון יומי של 45 מיליגרם, הביאו לירידה משמעותית של עד 78% בצביעה הבתר-סינפטית של AChR , בהשוואה לעכברים שהוזרקו עם IgG של אנשים בריאים. העכברים המוזרקים עם IgG מאנשים עם נוגדנים עצמיים ל-MuSK איבדו ממשקלם ופיתחו חולשת שרירים.
נתונים קליניים
עייפות וחולשה כתוצאה משיבוש בהעברת איתותים ברמת ה-NMJ היא מאפיין של MG. האבחון מתבצע על ידי קריטריונים קליניים ובדיקת EMG. רוב המקרים הם על בסיס אוטו-אימוני כתוצאה מהופעת IgG עצמי המגיב עם הקולטן לאצטיכולין (Li וחב' ב-Cleve Clin J Med משנת 2013). התדירות של גילוי נוגדנים עצמיים ל-AChR היא הנמוכה ביותר במטופלים עם חולשה המוגבלת לשרירים extraocular (עפ"י Lennon ב-Neurology משנת 1997). בניסויים של חוקרי Mayo Clinic נמצאו נוגדנים עצמיים ל-AChR ב-92% מהמאובחנים עם MG, כאשר נוגדנים כנגד MuSK נתגלו ביותר משליש מאלה עם חולשה כללית כתוצאה מ-MG בהם לא נתגלו נוגדנים כנגד AChR (אלה המוגדרים כ-seronegative), כאשר האחרונים מהווים פחות מ-4% מכלל מקרי MG (עפ"י Chan וחב' ב-Muscle Nerve משנת 2007).
בכ-6% מהמטופלים הסובלים מ-MG ואשר מערכת החיסון שלהם אינה פגועה, אין מוצאים נוגדנים עצמיים כנגד AChR או כנגד MuSK, והם מוגדרים כ- double seronegative (או DSN). לאחרונה הופיעו מספר פרסומים לפיהם מטופלים עם MG ללא נוגדנים ל-AChR ול-MuSK מכילים נוגדנים כנגד LPR4 (עפ"י Motomura ו-Higuchi ב-Rinsho Shinkeigaku משנת 2012; Richman ב-Arch Neurol משנת 2012; Pevzner וחב' ב-J Neurol nab, 2012 ו-Zhang וחב' ב-Arch Neurol משנת 2012). יחד עם זאת נראה שישנם עדיין נוגדנים עצמיים נוספים שעדיין לא התגלו בהקשר זה. נשים בדרך כלל יותר נפגעות מהופעת נוגדנים עצמיים ל-MuSK ב-MG, כאשר התסמינים הקליניים עלולים להופיע בכל גיל. כיוון ש-MG על רקע נוגדנים ל-MuSK אינה מושפעת מאי תפקוד בלוטת הטימוס או מ-thymoma, טיפול על ידי כריתת בלוטה זו אינו מועיל. חולשות בשרירי הפנים ובמערכת הנשימה כמו גם של המערכת ה-bulbar, כן משמעותיות ב-MG על רקע נוגדנים ל-MuSK, כאשר משברים מיאסתניים בהחלט שכיחים (Skjei וחב' ב-Neuromuscul Disord משנת 2013).
מסתבר שיש ל-MuSK-MG שלושה פנוטיפים קליניים שונים :
- תרחיש קליני שאינו ניתן להבדלה מ-AChR-MG עם חולשת שרירית יותר כללית;
- תרחיש יותר מקומי עם חולשת שרירים בצוואר, בכתף ובמערכת הנשימה;
- צורה חמורה יותר עם חולשה ועייפות באזור הצוואר ושרירי הלסת מה שעלול לגרום לקשיי דיבור, לעיסה, בליעה, ואחיזת הראש במנח זקוף כל אלה המוגדרים ב-bulbar weakness על כך שהעצבים המעורבים מקורם מגזע המוח ומהמוח המוארך), כאשר צורת מפגע זה עלולה להיות מלווה עם משברי נשימה תכופים
- (Illa וחב' ב-Clin Med משנת 2005, Lee וחב' ב-J Clin Neurosci משנת 2006, Ohta וחב' ב-Eur J Neurol משנת 2007, Evoli וחב' ב-Ann NY Acad Sci משנת 2008, Chang וחב' ב-J Neurol Sci משנת 2009 ו-Guptill ו-Sanders ב-Curr Opin Neurol משנת 2010).
נוגדנים כנגד AChR הם בדרך כלל מסוג IgG1 והם הם גורמים לאיבוד של AChR מה-NMJ על ידי שלושה מנגנונים עיקריים: נזק המשופעל על ידי משלים (complement), מודולציה אנטיגנית כתוצאה מקישור דו-ולנטי של הנוגדנים, וחסימה ישירה של תפקוד הקולטן. לעומת זאת, הנוגדנים העיקריים בצורת MuSK של MG הם מסוג IgG4 שאינם משפעלים את המשלים, ולכן לא נגרם נזק על ידי האחרון ב-MuSK-MG (עפ"י McConville וחב' ב-Ann Neurol משנת 2004). ביופסיות שריר ומחקרים אלקטרופיזיולוגיים מרקמות שרירי צלעות (intercostal) מוחלשים במטופלים עם MuSK-MG לא הראו כל אובדן של AChR או שקיעה והתרבצות של משלים למרות שאובחנה בנבדקים אלה ירידה ב-MEPPs או miniature endplate potentials שהם תהליכי הדה-פולריזציה של סיבי שרירי שלד הנגרמים על ידי קישור של נוירוטרנסמיטורים דוגמת אצטילכולין לממברנה הבתר-סינפטית ב-NMJ (עפ"י Selcen וחב' ב-Neurology משנת 2004, ו-Shiraishi וחב' ב-Ann Neurol משנת 2005).
למרות ששרירי הצלעות ששימשו במחקר של Selcen היו מוחלשים באופן בולט, בדרך כלל שרירי הפנים מעורבים הרבה יותר ב-MuSK-MG, וניסויי העברת גירוי עצבי בשרירים אלה in vivo מצביעים על פגמים רבים יותר ב-MuSK-MG מאשר בשרירי הצלעות (Nemoto וחב' ב-J Neurol Neurosurg Psychaitryמשנת 2005 ו-Farrugia וחב' ב-Brain משנת 2006). אך מסיבות מובנות לא נוטלים ביופסיות משרירי הפנים בבני אדם, ולכן אופי הפגמים בשרירים אלה במאובחנים שם MuSK-MG לא יכול להיחקר.
למרות ש-70% עם-MG מטיפוס seronegative AChR באזור אוקספורד נמצאו כבעלי נוגדנים כנגד MuSK, מחקרים באזורים גיאוגרפיים אחרים הראו שכיחות ממוצעת של 37% בלבד של נוגדנים כנגד MuSK באלה שהם סרו-נגטיביים ל-AChR (עפ"י Wolfe ו-Wu ב-Ann NY Acad Sci משנת 2007). אכן בנורווגיה נרשם 0% (עפ"י Romi וחב' ב-Eur J Neurol משנת 2005), ובטורקיה נרשמו 49% (עפ"י Deymeer וחב' ב-Neurology משנת 2007). ראוי לציין שלעומת שיעור התחלואה היציב יחסית של AChR-MG בתוך כלל חולי MG שנע בתחום שבין 62-90% (בממוצע 77%) בעולם כולו, תופעת התנודות החדות בשיעורי התחלואה ב-MuSK-MG באזורים שונים ובקרב קבוצות אתניות שונות מאוד בהחלט בולטת. למרות שבאירופה קיים גרדיאנט של שיעורי תחלואה ב-SK-MG הפוחתים כל שמדרימים בקווי האורך הגיאוגרפיים, לא נמצאה מגמה דומה כאשר מדרימים בארה"ב או באסיה.
הפנוטיפ הקליני
החולשה המיאסתנית ב-MuSK-MG, נוטה להיות חמורה יותר ומגיבה פחות לטיפול בהשוואה למה שמקובל בצורות אחרות של MG. מחקרים אפידמיולוגיים של Padua וחב' ב-Eur J Neurol משנת 2006, קבעו שאחוז גבוה יותר של מאובחנים עם MuSK-MG, היו מוגדרים כמקרים חמורים בהתאם למדרג הקליני של ה-MG Foundation of America או MGFA, זאת בהשוואה למטופלים עם DSN-MG או double serum-negative-MG. גם Pasnoor וחב' ב-Muscle Nerve משנת 2009, קבעו מדרג III-IV של MGFA ב-55% מתוך 53 מאובחנים עם MUSK-MG. גם Stickler וחב' ב-Clin Neurophysiol משנת 2005 תוך עשיית שימוש ב-שיטת המדרג הקליני QMG או quantitative MG, מצאו דרגת תחלואה גבוהה יותר משמעותית ב-20 נבדקים עם MuSK-MG, בהשוואה ל-72 נבדקים עם AChR-MG. יחד עם זאת, סקירה של Oh מהמרכז הרפואי בבירמינגהם-אלאבמה שהופיעה בשנת 2009 ב-J Clin Neurol, מצאה גם כן שתסמינים הקליניים ב-MuSK-MG חמורים יותר מאשר ב-DSN-MG, אך לא חמורים יותר מאשר ב-AChR-MG.
Thymoma=== נמצאת בבסיס ההבדל בין AChR-MG לבין MuSK-MG===
ברוב המכריע של מאובחנים עם MuSK-MG, לא נמצאה מעורבות של thymoma. במחקרים של Lavrenic וחב' ב-J Neurol Neurosurg Psychiatry משנת 2005, נמצאה thymoma רק ב-2 בתוך 17 בלוטות טימוס שהתקבלו ב-thymectomy, ואילו Evoli וחב' במאמרם משנת 2008 ב-Ann NY Acad Sci, גילו טימומה נודולארית קטנה ב-1 מתוך 17 מאובחנים עם MuSK-MG שעברו thymectomy. נראה אם כן ש-thymoma הוא תרחיש נדיר בסוג האחרון של MG, לעומת מצב של שגשוג של הטימוס (lymphoid hyperplasia) שהתגלה ב-19 מתוך 73 מאובחנים עם MuSK-MG המהווים 26%. Oh בסקירתו ב-J Clin Neurol משנת 2009, מדווח על אי-מציאת thymoma באף לא מקרה אחד של MuSK-MG, בהשוואה ל-3 מקרים בהם נתגלתה thymoma באלה המוגדרים כ-DSN-MG וב-13 מקרים של מאובחנים עם AChR-MG.
בניגוד ל-AChR-MG, בלוטת הטימוס ב-MuSK-MG היא בדרך כלל תקינה, או שהיא מגלה שינויים מורפולוגיים קלים. כך למשל היפרפלזיה לימפואידית אינה שכיחה כפי שכבר צוין. שני מחקרים של Lauriola וחב' ב-Neurology משנת 2005, ו-Leite וחב' ב-Ann Neurol מאותה שנה, ביצעו בירור היסטולוגי מורפומטרי ואימונוהיסטוכימי, בו השוו מטופלים עם MuSK-MG, עם אלה עם AChR-MG ו-DSN-MG וכן עם ביקורת של אנשים בריאים. שני מחקרים אלה הדגישו את החסר של ליבה גרמינאלית או של הסננה לימפוציטית לבלוטת הטימוס במקרים של MuSK-MG בניגוד לשינויים טיפוסיים אלה שמוצאים ברוב המקרים של AChR-MG ובערך ב-50% מהמקרים של DSN-MG. ממצאים אלה מצביעים על הבדלים במנגנונים הפתולוגיים בין MuSK-MG לבין AChR-MG ומרמז לכך שהרחקת הטימוס אינה עשויה לסייע בקבוצת ה-MuSK-MG אך עשויה להיות בעלת ערך במקרים של DSN-MG.
מחקרים קליניים נלווים
ביופסית שריר של Sanders וחב' ב-Neurology משנת 2003 במקרי MuSK-MG הראתה בדרך כלל אטרופיה לא ספציפית, בדומה לממצאים של Padua וחב' ב- Eur J Neurol משנת 2006, שבנוסף לאטרופיה לא-ספציפית דיווח על שוֹנוּת מוגברת בקוטר הסיב ב-7 מתוך 11 ביופסיות של מטופלים עם MuSK-MG. השוואה יותר מפורטת בין ביופסיות שריר מ-6 מקרים של MuSK-MG של Martignago וחב' ב-Neuropathol Appl Neurobiol משנת 2009, וכן מ-7 מקרים של AChR-MG באוכלוסייה איטלקית. שינויים מיופתיים (כגון צברים מיטוכונדריאליים המוגדרים כ-ragged red fibres) היו שכיחים במקרי MuSK-MG, בעוד שאטרופיה הייתה שכיחה יותר במטופלים עם AChR-MG. לעומת זאת, Farrugia וחב' במחקרם ב-Brain משנת 2006, שכלל MRI של MuSK-MG כן מצאו אטרופיה של שרירי פנים עם מעורבות בולבארית במטופלים עם MuSK-MG כאשר אטרופיה כזו לא נמצאה במקרים של AChR-MG.
מחקר של Shirashi וחב' משנת 2005 ב-Ann Neurol באוכלוסייה ביפאן, ביצע ביופסיה של השריר הדו-ראשי (שריר הקִבּורֶת או ה-biceps) מ-8 מטופלים עם MuSK-MG, לא הצליח להראות ירידה משמעותית של AChR במתחם הבתר-סינפטי. בדומה לממצאים של Selcen וחב' ב-Neurology משנת 2004, התרבצות של אימונוגלובולינים ושל משלים הייתה דלה במתחם זה, מה שהביא את Selcen להצגת השאלה "האם נוגדנים ל-MuSK הם הגורמים העיקריים לתסמינים המיאסתניים"? ממצאים אלה מרמזים לאפשרות שהמנגנון הפתוגני של הפגם בהעברת האיתותים במתחם הנוירו-מוסקולארי ב-MuSK-MG, שונים מאלה ב-AChR-MG, ואין הם כרוכים בפגם ב-AChR בו יש מעורבות של משלים. ממצא זה יכול היה להיות צפוי לאור העובדה שהנוגדנים המעורבים ב-MuSK-MG הם מסוג IgG4 שאינו משפעל את המשלים (McConville וחב' ב-Ann Neurol משנת 2004).
הוראות לביצוע הבדיקה
הבדיקה מתבצעת בשיטת radioimmunoassay בנסיוב. יש לדגום דם במבחנה כימית (פקק אדום או צהוב) ולאחר סרכוז והפרדת התאים מהנסיוב, מועדף לאחסן את מבחנת הנסיוב המופרד בקירור רגיל. אין לפסול דגימת נסיוב גם היא המוליטית, ליפמית או איקטרית ברמה גבוהה. יציבות הדגימות היא של 72 שעות בטמפרטורת החדר, ו-28 יום בקירור או בהקפאה. יש לקחת בחשבון שבאנשים המקבלים טיפול בתרופות לדיכוי מערכת החיסון, עלולה להתקבל תוצאה שלילית כזובה (false negative) במדידה של נוגדנים בנסיוב כנגד MuSK. חשוב לכן לבצע את הבדיקה האמורה לפני שמתחילים בטיפול תרופתי לדיכוי מערכת החיסון.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק 