הבדלים בין גרסאות בדף "לייפת כיסתית - Cystic fibrosis"
(←קישורים חיצוניים: כל עוד אין קישורים, אין צורך בכותרת) |
|||
| שורה 174: | שורה 174: | ||
==ביבליוגרפיה== | ==ביבליוגרפיה== | ||
| − | |||
| − | |||
{{רישיון cc}} | {{רישיון cc}} | ||
| − | |||
[[קטגוריה:גנטיקה]] | [[קטגוריה:גנטיקה]] | ||
[[קטגוריה:פולמונולוגיה]] | [[קטגוריה:פולמונולוגיה]] | ||
[[קטגוריה:ערכים מומלצים]] | [[קטגוריה:ערכים מומלצים]] | ||
גרסה מ־21:48, 30 במאי 2022
| לייפת כיסתית | ||
|---|---|---|
| Cystic Fibrosis | ||
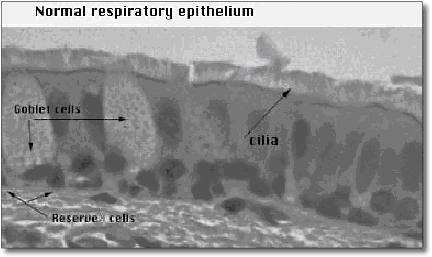
| 250px | ||
תרשים המדגים את הביטויים הקליניים של מחלת הלייפת הכיסתית
| ||
| שמות נוספים | סיסטיק פיברוזיס | |
| ICD-10 | Chapter E 84. | |
| ICD-9 | 277.0 | |
| MeSH | D003550 | |
| יוצר הערך | פרופ' איתן כרם | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – לייפת כיסתית
לייפת כיסתית (Cystic Fibrosis, CF) היא מחלה של המערכת ה-Exocrine - מערכת בלוטות ההפרשה החיצונית. המחלה נובעת מפגיעה בחלבון CFTR (Cystic Fibrosis Transmembrane Regulator), המהווה תעלת כלור (Chloride). המחלה פוגעת במערכת הנשימה [לרבות הסינוסים (Sinuses), הקנה, הסמפונות הגדולים והקטנים והריאות], מערכת העיכול (לרבות הלבלב, הכבד, המעי הדק והגס), מערכת המין הזכרית ומערכת הזיעה של החולים. עיקר הפגיעה נובעת מצמיגות יתר של ההפרשות, היוצרת Stasis ולחץ המובילים להצטברות חיידקים ולהרס רקמתי.
אפידמיולוגיה
שכיחות המחלה באוכלוסייה היהודית ובאוכלוסייה הערבית היא 1 ל-5000 לידות. עם זאת, השכיחות משתנה בין עדות שונות וכפרים שונים. האוכלוסייה הערבית כוללת חולים דרוזים, מוסלמים, נוצרים ובדואים. בשל השכיחות הגבוהה יחסית של נישואי קרובים, שכיחות המחלה גבוהה בקרב כפרים מסוימים, ונמוכה או אף חסרה באחרים. כמו כן, סוג המוטציה (Mutation) משתנה בין הכפרים והאוכלוסיות השונות.
אטיולוגיה
המחלה נגרמת כתוצאה מפגם בחלבון ה-CFTR. חלבון זה, הנמצא במעטפת התאים של איברים צינוריים, מהווה תעלה של כלור, ותפקידו לבקר את הפרשת המים אל התא ומחוצה לו.
במצב התקין, פתיחת תעלת הכלור גורמת להפרשה של כלור לחלל הצינור. הכלור טעון שלילית, ועל מנת לאזן את המטען החשמלי יוצא מן התא גם יון (Ion) נתרן בעל מטען חשמלי חיובי. שילוב של נתרן וכלור (המהווים יחד מלח בישול) סופח עמו גם מים, היוצאים מהתא לחלל הצינור.
על פני התאים נמצאות גם תעלות הסופגות נתרן, המצויות תחת בקרה שלילית של תעלת CFTR. כאשר תעלת CFTR מופעלת, יש דיכוי של פעולת תעלת הנתרן על פני התא, וכתוצאה מכך נוצר מצב בו יש מים בחלל הצינור. הפסקת פעולת תעלת CFTR מבטלת את העיכוב על תעלת הנתרן, מה שמוביל לכניסת מים לתוך התא. במערכת הנשימה נספגים ומופרשים מים באופן זה בכמות של קרוב לליטר.
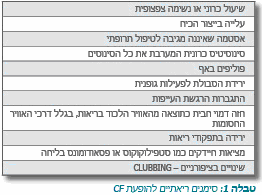
התאים במערכת הנשימה מצופים בריסים מיקרוסקופיים (Cilia), שתפקידם להגן על הסימפונות. הריסים פועלים בתוך סביבה מימית, אך קצותיהם מצופים על ידי שכבה שומנית דקה ביותר. השכבה השומנית מהווה מעין דבק שאליו נצמדים חיידקים, וירוסים וגרגירי אבק העלולים לגרום לדלקת במערכת הנשימה. הריסים פועלים בתיאום על מנת לדחוף את השכבה השומנית הדקה כלפי מעלה, לאזור הקנה וקצה מערכת הסימפונות, ובסופו של דבר אנו משתעלים אותה החוצה בצורה של ליחה.
בתוך הסביבה המימית שבה פועלים הריסים מתקיימים תהליכים פעילים להגנה של מערכת הנשימה. אותה סביבה מכילה נוגדנים, אנטיביוטיקות טבעיות וגורמים נוספים החיוניים להגנה על מערכת הנשימה. הנוזל הצמוד לתאים עם הריסים קרוי נוזל פרי-ציליארי (Peri-ciliar). אותו נוזל מהווה תוצר של פעילות משאבות מלחים – תעלת CFTR מעלה את ריכוז הכלור בנוזל, הסופח מולקולות נתרן ומים. במקביל, משאבות הנתרן האמורות לספוג את הנתרן בחזרה (ובעקבותיו גם מים וכלור) מעוכבות על ידי ה-CFTR, מה שמשאיר את המים והמלחים בנוזל הפרי-ציליארי.
הפגם במחלת CF נובע מחוסר תפקוד של תעלת CFTR, מה שמוביל להפחתה משמעותית בכמות המים המופרשים לנוזל הפרי-ציליארי. כלור אינו מופרש לנוזל, ומעט הנתרן המצוי בו נספג על ידי משאבות הנתרן שאינן מעוכבות על ידי CFTR. כתוצאה מכך, המים נספגים והשכבה הפרי-ציליארית מתייבשת. ללא הנוזל, הריסים אינם מסוגלים לנוע ולהוביל החוצה את הליחה ואת החיידקים המתיישבים עליה.
התוצאה הסופית היא פגיעה משמעותית ביכולת ההגנה של מערכת הנשימה. חיידקים ווירוסים מצליחים להתיישב באזור, ללא יכולת של הגוף לסלקם. עם הזמן מתפתחת דלקת מקומית ונזק באזור, המתבטאת בשלב הראשון כברונכיטיס (Bronchitis). בהמשך מתיישבים באזור גם חיידקים אלימים (כגון Staphylococcus aureus ו-Pseudomonas) המשחררים חומרים שגורמים להרס נרחב עוד יותר. מערכת ההגנה של הגוף שולחת לאזור תאים המשחררים חומרים המיועדים להילחם באותם חיידקים, אך בשל חוסר היכולת לסלק את אותם חיידקים אין אפשרות לעצור את הרס הרקמה הבריאה. התוצאה הסופית היא הרס של מערכת הנשימה, תוך איבוד הדרגתי של התפקוד הנשימתי עד להתפתחות אי ספיקה נשימתית.
הגן (Gene) הגורם למחלה יושב על כרומוזום (Chromosome) 7. גן זה זוהה בשנת 1989, וזיהויו היווה צעד גדול בהבנת גורם המחלה.
זוהו מוטציות רבות בגן המובילות למחלה. עם הזמן הסתבר כי בכל עדה בארץ יש כמה מוטציות שכיחות יותר המאפיינות אותה. כך, בדיקת 6 מוטציות מאפשרת לאבחן 97 אחוזים מהנשאים האשכנזים. לעומת זאת, אפשרות הגילוי בקרב בני עדות המזרח ויוצאי צפון אפריקה משתנה מעדה לעדה. לדוגמא, ניתן לגלות כ-85 אחוזים מהנשאים יוצאי מרוקו באמצעות בדיקת 3 מוטציות. לאור זאת, בדיקות הנשאות המוצעות כיום מבוצעות על פי המוצא העדתי.
קליניקה
מערכת הנשימה
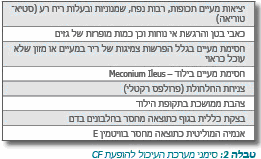
המחלה יכולה להתבטא בכל גיל, אולם במרבית החולים הסימנים הראשונים מופיעים כבר בחודשים הראשונים לחיים, והמחלה מאובחנת לפני גיל שנה. הביטויים הראשונים עשויים להתרחש כתוצאה מתחלואה במערכת הנשימה, וכוללים שיעול כרוני, זיהומים חוזרים בדרכי הנשימה, ברונכיטיס כרונית, תחלואה הדומה לאסתמה (Asthma) אך אינה מגיבה לטיפול המקובל באסתמה, צפצופים חוזרים ונשימה מהירה. בחלק מהמקרים יש צמיחה של חיידקים האופייניים למחלה (כגון Pseudomonas או Staphylococcus aureus) בתרבית ליחה.
הפגם בחלבון ה-CFTR בתאי האפיתל המצפים את דרכי הנשימה גורם לשינוי של הרכב המלחים בנוזל המצפה את דפנות דרכי האוויר. בעקבות אותו שינוי בריכוז יוני הכלור והנתרן והמחסור היחסי במים בחלל הצינורות, הריר בדרכי האוויר הופך סמיך ודביק, לוכד חיידקים ואינו מאפשר לריסים לנוע לעבר הלוע. שינוי זה מגביר את סיכויי החיידקים לשרוד ולהתרבות בדרכי הנשימה. כמו כן, הריר עצמו חוסם את מעברי הנשימה ומפריע לשחלוף הגזים.
מערכת העיכול
פגיעה בהפרשה התקינה של הלבלב מתרחשת בכ-80 אחוזים מהחולים. באותם חולים, בלוטות ההפרשה החיצוניות של הלבלב מייצרות הפרשות סמיכות מאוד, עד כדי כך שאנזימי העיכול נעצרים בתעלות הלבלב ואינם מצליחים להגיע לתריסריון. ללא אותם אנזימים, המזון אינו מתעכל כראוי וחלק גדול מהחלבונים והשומנים אינם נספגים.
ביטויים נוספים
לעיתים קרובות, ביטוי המחלה משותף לשתי המערכות. ישנם גם מקרים מסוימים בהם הביטוי שונה ובלתי אפייני, ולכן האבחון נעשה בגיל מבוגר יותר – לעתים אף מעבר לגיל 40.
ביטויים שאינם אופייניים למחלה כוללים:
- חסר מלחים בדם
- מחלת סינוסים כרונית
- פוליפים באף
- התאלות של קצות אצבעות הידיים והרגליים (Clubbing)
- דלקת לבלב כרונית
- מחלת כבד
- קומה נמוכה
- טעם מלוח של העור
תת תזונה
ללא התערבות מיוחדת, רוב החולים יגיעו למצב של תת-תזונה, הנובע ממספר גורמים:
- אי ספיקת לבלב - 85 אחוזים מהחולים סובלים מאי ספיקת לבלב. בחולי CF נוזלי הלבלב צמיגים וסמיכים, ועל כן הם סותמים את הצינוריות המובילות את אנזימי הלבלב למעי. נוכחות מזון במעי מעודדת יצירה והפרשה של אנזימים נוספים, המופרשים גם הם לצינורות הסתומים. כתוצאה מכך עולה הלחץ בצינורות, דפנות הצינורות נפגעות והאנזימים משתחררים בתוך רקמת הלבלב והורסים את הבלוטה. כתוצאה מכך נוצר חסר של אנזימי לבלב במעי, מה שפוגע קשות בספיגת המזון
- דלקת כרונית בריאות ומאמץ נשימתי מוגבר – כתוצאה מפגיעה בפינוי הליחה מצטברות במערכת הנשימה מושבות של חיידקים, שבתגובה להן נוצר תהליך של דלקת. מערכות ההגנה של הגוף לא מצליחות לסלק את החיידקים, והתהליך הדלקתי נמשך ללא סוף. תהליך זה צורך אנרגיה רבה. הפגיעה בדרכי הנשימה, היצרות הסימפונות והפגיעה באלסטיות (Elasticity) הריאה – מגבירות גם הן את המאמץ הכרוך בנשימה, ומעלות את הצריכה הקלורית
- חוסר תאבון – הדלקת הכרונית בדרכי הנשימה, הקושי בנשימה והשיעול הרב מובילים לחוסר תאבון. כמו כן, חלק מהחולים נותרים עם חוויה שלילית הקשורה באכילה, בשל כאבי הבטן והשלשולים שחוו בגיל צעיר. גם המאמץ הנשימתי תורם וגורם לעלייה בלחץ על הבטן המובילה לתחושת שובע מוקדמת
- הקאות – במידה ומופיע התקף שיעול כאשר הקיבה מלאה, השיעול יגרום לעלייה בלחץ הבטני ולהקאה
אבחנה
תבחין זיעה
ברוב המקרים, אבחנה של CF נעשית באמצעות תבחין זיעה בילדים הסובלים מהתופעות האופייניות. בדיקה זו כוללת מריחה של חומר המגרה הפרשת זיעה על היד, איסוף הזיעה באמצעות מכשיר עדין ומדידת תכולת המלחים שבה. אבחנה של CF נקבעת במידה וריכוז הכלור בזיעה עולה על 60 Milliequivalents לליטר.
ישנם מצבי ביניים בהם ריכוז הכלור הוא 60-40. מצבים אלו יכולים להתקיים בילדים חולים ב-CF, אך גם בילדים בריאים. כמו כן, תבחין הזיעה אינו יעיל לגילוי נשאים של המחלה. הנשאים אינם חולים, ולכן בלוטות הזיעה שלהן תקינות – כמו גם ריכוז המלחים בזיעה.
לעתים התבחין אינו יעיל בילודים, למרות שהפגם בבלוטות הזיעה קיים גם אצלם. חלק מהתינוקות אינם מסוגלים לייצר זיעה בכמות מספקת במשך החודש הראשון לחיים, ועל כן לא מתאפשרת בדיקה מהימנה.
תבחין הזיעה מהווה אמצעי פשוט, בלתי מכאיב, מהימן וזול לאבחנה. אין כל קשר בין רמת המלחים בזיעה לחומרת המחלה.
בדיקה גנטית
יש מוטציות שונות השכיחות בעדות ואוכלוסיות שונות, ולבצע את בדיקת הנשאות בהתאם. מומלץ להיוועץ במכון הגנטי (Genetic) בכל שאלה.
את הבדיקה הגנטית רצוי ומומלץ לבצע לפני הכניסה להריון, אולם ניתן לבצעה גם במהלך הריון. כדאי להיבדק מוקדם ככל האפשר, על מנת שניתן יהיה לבצע בדיקת סיסי שליה או מי שפיר במקרה הצורך. על כל מקרה, הבדיקה תבוצע רק בשלב הריון המוקדם מ-18 שבועות.
פוטנציאל רירית האף
בדיקה רגישה ויעילה המשמשת לאבחנה במצבים בהם תבחין הזיעה תקין או גבולי, ולא נמצאות מוטציות בגן ה-CFTR. הבדיקה כוללת מדידה של פוטנציאל הממברנה (Membrane potential) ברירית האף. היא מבוצעת באמצעות קטטר (Catheter) עדין המונח בקדמת האף ומחובר למכשיר המודד מתח. קצהו השני של המכשיר מחובר למחט קטנה הממוקמת באמה. פוטנציאל הממברנה באף הוא הבדל המתח החשמלי כפי שנמדד על ידי המכשיר. במצב התקין, הפוטנציאל הנמדד הוא פחות מ-30 MilliVolt. בחולי CF הפוטנציאל הנמדד גבוה יותר.
בשלב הבא מזליפים תמיסה של Amiloride, חומר המעכב את פעילות תעלת הנתרן. היות ותעלות הנתרן עובדות ביתר שאת בחולי CF, העיכוב שיודגם יהיה גדול יותר מאשר במצב התקין. בשלב הסופי מזליפים תמיסה של מים פיזיולוגיים (Physiological) שאינם מכילים כלור. היעדר הכלור גורם ליציאת כלור החוצה מהתא במצב התקין, פעולה הנמדדת על ידי מערכת המדידה. בחולי CF, בשל היעדר תעלות כלור מתפקדות, לא מודגמת תנועה של יוני כלור בזמן הזלפת התמיסה.
בדיקות נוספות
ImmunoReactive Trypsinogen (IRT) – בדיקת דם בה נמדדת רמת האנזים IRT המופרש מהלבלב. רמת אנזים (Enzyme) זה גבוהה בילודים ובתינוקות חולי CF. הבדיקה משמשת בארצות מסוימות לגילוי מוקדם של המחלה בתינוקות. במבוגרים, הבדיקה משמשת לאבחון פגיעה בתפקוד הלבלב.
טיפול
מרכזי טיפול ייעודיים
היות וטרם נמצא טיפול המרפא את הפגם הגנטי, הטיפול הניתן כיום מכוון לפגיעה במערכות השונות הנגרמת על ידי המחלה. הטיפול ניתן במרכז ייעודי המתמחה במתן טיפול ל-CF.
בארץ קיימים שישה מרכזים כאלו, שמיקומם:
- בית החולים תל השומר
- בית החולים שניידר
- בית החולים כרמל
- בית החולים רמב"ם
- בית החולים הדסה
- בית החולים סורוקה
כל חולה חייב להיות מופנה לטיפול באחד המרכזים הייעודיים. מחקרים רבים הראו שקבלת הטיפול במרכז ייעודי מעלה את תוחלת החיים בצורה משמעותית. מחקרים נוספים הדגימו כי מצבם הקליני של החולים המגיעים לביקורים סדירים במרכזים הייעודיים לפחות פעם בחודש טוב יותר מזה של החולים שאינם מגיעים למעקב מסודר.
הטיפול במרכז המתמחה ב-CF ניתן על ידי צוות רב-תחומי הכולל רופאים מומחים בתחום הפולמונולוגיה (Pulmonology), מומחים בתחום הגסטרואנטרולוגיה והתזונה, תזונאים, פיזיותרפיסטים, עובדים סוציאלים ופסיכולוגים. הטיפול מרוכז על ידי האחות האחראית במרכז.
הביקורים החודשיים כוללים מדידת גובה ומשקל, תפקודי ריאה, הערכה תזונתית, תרבית ליחה, בדיקות דם, צילום חזה ואולטרה-סאונד של הבטן. בדיקות אלו חיוניות להערכת מצב החולים, וברגע שמודגמת סטייה מהערכים שנמדדו בביקור הקודם – ננקטות הפעולות הנדרשות לטיפול וחזרה למצב הבסיסי.
עם התפתחות טיפולים למניעת הסיבוכים שאינם ריאתיים, נותרה המחלה הריאתית כגורם העיקרי לתחלואה ולתמותה בקרב חולי CF. אבחון וטיפול מוקדמים הם המפתח לתוחלת חיים ארוכה.
פיזיותרפיה
הטיפול במחלה כולל פיזיותרפיה לעידוד ניקוז ההפרשות בדרכי הנשימה. פיזיותרפיה נשימתית מתבצעת מדי יום, לפחות פעם ביום, ובמקרים הקשים אף יותר מפעם ביום למשך 45 דקות. את הטיפול יכול לבצע פיזיותרפיסט מומחה או מי שמאומן לכך. הפיזיותרפיה כוללת תרגילים לשחרור הליחה הצמיגה הנדבקת לדופן הסימפונות, במטרה לאפשר לחולים להשתעל אותה החוצה. לעתים נעזרים במכשירים הגורמים לרעד של בית החזה ובכך מסייעים לפינוי הליחה.
יש להתחיל את הטיפול הפיזיותרפי מייד עם האבחנה. הטיפול עצמו מותאם באופן אישי לחולה בהתאם לגיל, חומרת המחלה, שינויים מבניים בבית החזה וכו'. מטרתו להתגבר על הכיח הצמיג הגורם לחסימה מכנית של דרכי האוויר, ולמנוע זיהומים חריפים וכרוניים המובילים להרס רקמת הריאה.
עם הזמן, עבודת הנשימה המאומצת ומחלת הריאות החסימתית הכרונית יגרמו לשינויים מבניים בבית החזה, כגון פגיעה במבנה השלד, חוסר איזון באורך השרירים ופגיעה בטווח התנועה התקין של המפרקים. השינויים הללו מובילים ליצירת בית חזה חביתי ולכיפוף קדמי של עמוד השדרה החזי. קיבוע זה של בית החזה מגביל את יכולת התפשטות הריאה ומוביל להיווצרות Scoliosis, Kyphosis או שילוב של השניים.
טכניקות הטיפול הנשימתי
- Conventional Physiotherapy – שיטה הכוללת ניקוז תנוחתי והקשה על בית החזה. בעבר שימשה כטיפול הפיזיותרפיה הנשימתית העיקרי. העיקרון העומד בבסיסה הוא שהמטופל שוכב בתנוחה המאפשרת לכוח הכבידה לסייע בניקוז ההפרשות, מדרכי האוויר הקטנות דרך הסימפונות ובסופו של דבר לקנה. תנוחות הניקוז מבוססות על האנטומיה של עץ הסימפונות. חלקן מבוצעות כשבית החזה בשיפוע שלילי. היות ולאחרונה נמצא ששכיבה בשיפוע שלילי עלולה להגביר מעבר של חומצה מהקיבה לושט בחולי CF, הומלץ שלא להשתמש בשיטה זו עד לבירור מקיף של קיום התופעה אצל המטופל
- Clapping – הקשה על בית החזה. מאחר שהליחה של החולים צמיגה מאוד, היא נדבקת לדופן הסימפונות וקשה מאוד לשחרר אותה. טכניקה זו מבוססת על ההנחה שהקשה על בית החזה עוברת דרך בית החזה, מרטיטה את דרכי הנשימה ומסייעת בפינוי הליחה. תנועת ההקשה מתבצעת על ידי שורש כף ידו של המטפל, כאשר כף היד קמורה. המטפל מקיש על הצלעות על פי תנוחת הניקוז בה נמצא המטופל
- ויברציות (Vibrations) בנשיפה – בטכניקה זו, המטפל מרעיד את ידיו בזמן נשימת המטופל ליצירת תנודתיות של דפנות הסימפונות. הויברציות ניתנות לכל אורך הנשיפה לכיוון בית החזה בכל אחת מתנוחות הניקוז, תוך הפעלת לחץ על בית החזה. במשך הזמן פותחו מכשירים המייצרים תנודות אוויר וגורמים להיווצרות ויברציות. אותן ויברציות מועברות לתוך הסימפונות ומרעידות את דפנותיהן במטרה לשחרר את הריר הצמיג הנדבק לדופן. לאחרונה פותח מכשיר בצורת אפוד, הרוטט ומרעיד את בית החזה מבחוץ
- Active Cycle Breathing Technique – טכניקה המשמשת גם היא לשינוע הכיח מדפנות הסימפונות. טכניקה זו כוללת נשימות מבוקרות בנפח רגיל, המפעילות את הסרעפת בצורה משמעותית יותר תוך שימוש בבית החזה התחתון והרפיה של בית החזה העליון. נשימות אלו נקראות "נשימות בטן"
טיפול תרופתי
טיפול להורדת צמיגות הליחה=
- Pulmozyme (Recombinant Human Deoxyribonuclease) - תרופה המכילה אנזים המפרק DNA. מחקרים רבים הראו שהליחה של חולי CF מכילה כמות גדולה של DNA כתוצאה מהרס תאים ושחרור החומר הגרעיני. אותו DNA מגביר את צמיגות הליחה בצורה משמעותית. התרופה ניתנת באינהלציה (Inhalation) פעם ביום במטרה להפחית את צמיגות הליחה
- תמיסה היפרטונית (Hypertonic) – מים פיזיולוגיים בריכוז מלחים הגבוה מהריכוז בתאים. ריכוז המלח הגבוה גורם למים לצאת מהתאים ומעשיר את שכבת המים המצפה את מערכת הנשימה – מה שמשפר את פינוי הליחה. הטיפול בתמיסות מי מלח היפרטוניות ניתן באינהלציה מספר פעמים ביום, היות ומשך הפעולה שלו קצר. מטרתו לשפר את ניקוז הליחה מדרכי הנשימה וחלל האף. עד היום פורסמו עבודות רבות המצביעות על שיפור בתנועת הליחה מדרכי הנשימה, עלייה בכמות הליחה הנפלטת, ושיפור בתפקודי הריאה של החולים תחת טיפול זה
טיפול אנטיביוטי
מקרים של זיהומים בדרכי הנשימה מטופלים באנטיביוטיקה. החולים נזקקים לטיפולים אנטיביוטיים מרובים לאורך חייהם. ברוב המקרים הטיפול ניתן בצורה פומית, אך זיהומים קשים מצריכים טיפול תוך-ורידי למשך שבועיים
האנטיביוטיקה הניתנת מכוונת כנגד חיידקים במערכת הנשימה. החיידק השכיח ביותר הוא Pseudomonas, הגדל בתרביות ליחה ב-60-50 אחוזים מהחולים, ושכיחותו עולה עם הגיל. חיידקים נפוצים אחרים הם Staphylococcus, Haemophilus influenzae, Burkholderia cepacia ועוד.
במרבית החקרים, מרגע שחיידק צומח בדרכי הנשימה, קשה לסלקו. מטרת הטיפול למנוע צמיחת חיידקים או להפחית את כמותם. מספר מחקרים הראו שמתן אנטיביוטיקה באופן קבוע מדי 3 חודשים דרך הוריד מונע התפתחות של Pseudomonas במערכת הנשימה ומביא לתוחלת חיים ארוכה יותר.
מרבית החולים מקבלים טיפול אנטיביוטי קבוע באינהלציה. חסרונו העיקרי של הטיפול הוא התפתחות חיידקים עמידים לאנטיביוטיקה הקיימת – מה שיוצר קושי בהתאמת הטיפול האנטיביוטי לחולה. כמו כן, קיים חשש של העברת חיידקים מחולה לחולה. החולים והצוות הרפואי נקראים לשמור על כללים קפדניים למניעת הדבקה. מומלץ להימנע ממפגשים חברתיים בין החולים.
טיפול בנוגדי דלקת
חולי CF סובלים מתהליכים דלקתיים כרוניים במערכת הנשימה. התהליך הדלקתי גורם לנזק רקמתי, ועל כן מושקע מאמץ במטרה לשתקו. החולים מקבלים טיפול בתרופות נוגדות דלקת באופן קבוע. לאחרונה נמצא שתרופות ממשפחת ה-Macrolides גם הן מפחיתות את התהליך הדלקתי.
פעילות גופנית
פעילות גופנית הוכחה במחקרים רבים כבעלת חשיבות רבה בחיי היום-יום של חולי CF. יעילותה מתבטאת ב:
- שיפור סיבולת לב-ריאה
- שיפור פעולת שרירי הנשימה
- עלייה בזרימת האוויר בריאה
- סיוע בפינוי ההפרשות הצמיגות מדרכי הנשימה
- שיפור היציבה ושמירה על גמישות בית החזה
ענפי הספורט המומלצים: ריצה, שחייה, משחקי כדור, טניס, התעמלות מכשירים, רכיבה על סוסים, קפיצה על חבל, רכיבה על אופניים וכדומה.
תזונה והעשרה קלורית
חולי CF סובלים מאבדן קלורי (Caloric) במעי הנגרם מירידה בספיגה (כתוצאה מחסר אנזימי הלבלב), בשילוב עם הקאות ותיאבון מופחת. אותו אבדן קלורי עומד אל מול צורך גדול יותר בקלוריות לעומת אדם בריא באותו גיל. על כן, ההמלצה לחולי CF היא צריכה של 150-120 אחוזים מכמות הקלוריות המומלצת לבני גילם. הוכח כי החולים המצויים במצב תזונתי טוב סובלים פחות מהידרדרות המחלה הריאתית, ומתמודדים טוב יותר עם התלקחויות המחלה.
חמצן
חולים שמחלתם התקדמה וגרמה לפגיעה קשה בריאות נזקקים לחמצן באופן קבוע.
השתלת ריאות
אותם החולים הסובלים מפגיעה ריאתית קשה ונזקקים לחמצן באופן קבוע מופנים להשתלת ריאות. בניתוח יש להחליף את שתי הריאות החולות. המחלה אינה מתפתחת בריאות המושתלות, היות והן נושאות את המטען הגנטי של התורם. לעומת זאת, החולה ממשיך לסבול מהביטויים האחרים של המחלה, כגון הפגיעה בלבלב.
פרוגנוזה
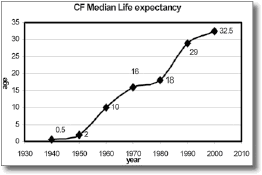
הודות להתקדמות בהבנת המחלה, שהביאה לפיתוח טיפולים טובים יותר, תוחלת החיים של חולי CF השתפרה מאוד עם השנים. כאשר המחלה תוארה לראשונה בשנות הארבעים של המאה הקודמת, הילדים היו נפטרים במהלך השנה הראשונה לחייהם. נכון לשנת 2011, 50 אחוזים מהחולים חיים מעבר לגיל 30, ואנו מניחים כי סיכויים של התינוקות הנולדים לעבור את גיל הארבעים הוא מעל 80 אחוזים.
חולים רבים המגיעים לבגרות מתפקדים בחברה באופן מלא. נשים רבות הרו, חלקן אף מספר פעמים. הגברים החולים עלולים לסבול מחסימה של צינור הזרע, מה שמוביל לחוסר פוריות. כיום יש טכניקות חדשות המאפשרות שאיבה של תאי זרע ישירות מהאשך, והפריית מבחנה המאפשרת להביא להריון ולידה. על כן, גם החולים הזכרים יכולים להיות אבות לילדים.
התקווה היא כי בעתיד יימצא פתרון למחלה בצורה של תיקון הפגם הגנטי או באמצעות תאי גזע עובריים שישמשו לבניית רקמות חדשות במקום אלו שנפגעו מהמחלה.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק