הבדלים בין גרסאות בדף "אוסטאופורוזיס - טיפול ברומוסוזומב"
| שורה 17: | שורה 17: | ||
כאשר נשקלת הכנסת תרופה מסוימת לסל שירותי הבריאות, נבדקים שני שיקולים עיקריים - יעילות התרופה ועלות התרופה. כלכלני בריאות מנסים לחשב כמה אלפי שקלים מוציאים בשנה כדי להרוויח שנת חיים נוספת וכך מציגים לוועדת הסל מדד של עלות־תועלת. נושא שאין להתעלם ממנו הוא איכות חיים, מדד סובייקטיבי שקשה מאוד להעריך, כי מי יכול להחליט אם כאב ראש קודם לכאב גב, לדוגמה. | כאשר נשקלת הכנסת תרופה מסוימת לסל שירותי הבריאות, נבדקים שני שיקולים עיקריים - יעילות התרופה ועלות התרופה. כלכלני בריאות מנסים לחשב כמה אלפי שקלים מוציאים בשנה כדי להרוויח שנת חיים נוספת וכך מציגים לוועדת הסל מדד של עלות־תועלת. נושא שאין להתעלם ממנו הוא איכות חיים, מדד סובייקטיבי שקשה מאוד להעריך, כי מי יכול להחליט אם כאב ראש קודם לכאב גב, לדוגמה. | ||
| − | מטרת הטיפול באוסטאופורוזיס היא מניעת שברים, מניעת תחלואה ותמותה | + | מטרת הטיפול באוסטאופורוזיס היא מניעת שברים, מניעת תחלואה ותמותה ומניעת סבל. |
==בניית עצם מהירה ויעילה למניעת שברים אוסטיאופורוטיים== | ==בניית עצם מהירה ויעילה למניעת שברים אוסטיאופורוטיים== | ||
| שורה 23: | שורה 23: | ||
קיימים תכשירים אנבולים, אנלוגים של הורמון הפרהתירואיד (PTH) שמעודדים יצירת עצם אך במקביל מעלים פירוק עצם (מגבירים את תהליך ה־Remodeling Bone, כך שיכולתם לבנות עצם למעשה מוגבלת). | קיימים תכשירים אנבולים, אנלוגים של הורמון הפרהתירואיד (PTH) שמעודדים יצירת עצם אך במקביל מעלים פירוק עצם (מגבירים את תהליך ה־Remodeling Bone, כך שיכולתם לבנות עצם למעשה מוגבלת). | ||
| − | *[[Romosozumab]] - נוגדן מונוקלונלי לסקלרוסטין - היא תרופה המעכבת סקלרוסטין ובכך מעודדת בנית עצם ומפחיתה פירוק עצם בו זמנית. התרופה ניתנת בהזרקה תת עורית פעם בחודש למשך שנה | + | *[[Romosozumab]] - נוגדן מונוקלונלי לסקלרוסטין - היא תרופה המעכבת סקלרוסטין ובכך מעודדת בנית עצם ומפחיתה פירוק עצם בו זמנית. התרופה ניתנת בהזרקה תת-עורית פעם בחודש למשך שנה |
| − | *[[Sclerostin]] - לאחר התגלית שחוסר בסקלרוסטין גורם למחלות גנטיות נדירות המתאפיינות במסת עצם גבוהה ועמידות בפני שברים{{הערה|שם=הערה3|Balemans W, Ebeling M, Patel N, et al. Increased bone density in sclerosteosis is due to the deficiency of a novel secreted protein (SOST). Hum Mol Genet 2001;10:537-543}}{{הערה|שם=הערה4|Brunkow ME, Gardner JC, Van Ness J, et al. Bone dysplasia sclerosteosis results from loss of the SOST gene product, a novel cystine knot-containing protein. Am J Hum Genet 2001;68:577-589}}, סלקרוסטין הפך מטרה למחקר ופיתוח לטיפול באוסיטאופורוזיס. סקלרוסטין מופרש על ידי תא האוסטאוציט | + | *[[Sclerostin]] - לאחר התגלית שחוסר בסקלרוסטין גורם למחלות גנטיות נדירות המתאפיינות במסת עצם גבוהה ועמידות בפני שברים{{הערה|שם=הערה3|Balemans W, Ebeling M, Patel N, et al. Increased bone density in sclerosteosis is due to the deficiency of a novel secreted protein (SOST). Hum Mol Genet 2001;10:537-543}}{{הערה|שם=הערה4|Brunkow ME, Gardner JC, Van Ness J, et al. Bone dysplasia sclerosteosis results from loss of the SOST gene product, a novel cystine knot-containing protein. Am J Hum Genet 2001;68:577-589}}, סלקרוסטין הפך מטרה למחקר ופיתוח לטיפול באוסיטאופורוזיס. סקלרוסטין מופרש על ידי תא האוסטאוציט והוא רגולטור שלילי של בניית עצם. סקלרוסטין מעכב את n־Wnt signaimg ומעכב בניית עצם דרך השפעתו על התפתחות ותפקוד תא האוסטאובלסט{{הערה|שם=הערה5|Li X, Zhang Y, Kang H, et al. Sclerostin binds to LRP5/6 and antagonizes canonical Wnt signaling. J Biol Chem 2005;280:19883-19887}} |
==מחקרים פרה-קליניים וקליניים== | ==מחקרים פרה-קליניים וקליניים== | ||
| שורה 37: | שורה 37: | ||
==בטיחות בטיפול== | ==בטיחות בטיפול== | ||
| − | במחקרים אלה הסבילות לטיפול ברומוסוזומב | + | במחקרים אלה הסבילות לטיפול ברומוסוזומב הייתה טובה, נרשמו מעט תגובות באזור הזרקת התרופה (כ־5% לעומת 3% בקבוצת הפלצבו). כל המשתתפות במחקרים קיבלו תוספים של סידן וויטמין D ונרשמו מעט אירועי היפוקלצמיה שהייתה קלה, חולפת ואסימפטומטית לרוב. כ־15% עד 20% מהמשתתפות פיתחו נוגדנים לרומוסוזומב אך לא נראה שלתופעה יש השלכה על יעילות הטיפול. |
ה-WNT signaling מעורב בתהליכי שגשוג תאי ברקמות רבות ולכן קיימת דאגה תאורטית לגבי התפתחות של תהליכים נאופלסטיים. לא נראה בשלב זה אף סיגנל, גם לא בנוגע להתפתחות גידולי עצם מסוג אוסטיאוסרקומה בחולדות כפי שנצפה עם אנלוגים של PTH{{כ}}{{הערה|שם=הערה12|McClung MR, Romosozumab for The Treatment of Osteoporosis. Osteoporosis and Sarcopenia 4 (2018) 11-15}}. | ה-WNT signaling מעורב בתהליכי שגשוג תאי ברקמות רבות ולכן קיימת דאגה תאורטית לגבי התפתחות של תהליכים נאופלסטיים. לא נראה בשלב זה אף סיגנל, גם לא בנוגע להתפתחות גידולי עצם מסוג אוסטיאוסרקומה בחולדות כפי שנצפה עם אנלוגים של PTH{{כ}}{{הערה|שם=הערה12|McClung MR, Romosozumab for The Treatment of Osteoporosis. Osteoporosis and Sarcopenia 4 (2018) 11-15}}. | ||
| שורה 46: | שורה 46: | ||
==סטטוס נוכחי (נכון ל-2023)== | ==סטטוס נוכחי (נכון ל-2023)== | ||
| − | רומוסוזומב קיבל את אישורי ה־FDA וה־EMEA ורשום בישראל לטיפול באוסטאופורוזיס בסיכון גבוה לשבר. התרופה כלולה בסל שירותי הבריאות כטיפול קו שני, לאחר | + | רומוסוזומב קיבל את אישורי ה־FDA וה־EMEA ורשום בישראל לטיפול באוסטאופורוזיס בסיכון גבוה לשבר. התרופה כלולה בסל שירותי הבריאות כטיפול קו שני, לאחר כישלון טיפול בתרופות קו ראשון (ירידה בצפיפות העצם ב־5% ומעלה או שבר אוסטיאופורוטי תחת טיפול) וגם כקו ראשון במטופלים עם אוסטאופורוזיס לפי צפיפות עצם + שבר אוסטיאופורוטי ובמקרים של קונטרה אינדיקציה מוחלטת לטיפול בטריפרטייד. |
סל שירותי הבריאות בישראל הוא מהמתקדמים בעולם ומאפשר טיפול לנשים ולגברים הסובלים מאוסטאופורוזיס, ובכל זאת יש מקום להרחבת הסל. | סל שירותי הבריאות בישראל הוא מהמתקדמים בעולם ומאפשר טיפול לנשים ולגברים הסובלים מאוסטאופורוזיס, ובכל זאת יש מקום להרחבת הסל. | ||
| שורה 57: | שורה 57: | ||
הרחבת הזכאות לחולות אוסטאופורוזיס לקבל טיפול בונה עצם (רומוסוזומב או טריפרטייד) יותר מפעם אחת במהלך המחלה. | הרחבת הזכאות לחולות אוסטאופורוזיס לקבל טיפול בונה עצם (רומוסוזומב או טריפרטייד) יותר מפעם אחת במהלך המחלה. | ||
| − | נתונים התומכים בבקשת ההרחבה: מחקרי עולם אמיתי שנערכו על יותר מ־500 חולים וחולות באוסטאופורוזיס בקו טיפולי ראשון ושני, הראו שאפקט הטיפול ברומוסוזומב על עלייה בצפיפות העצם בעמוד השדרה, עצם הירך וצוואר הירך הושפע ממתן טיפול קודם לאוסטאופורוזיס{{הערה|שם=הערה15|Ebina, K., Etani, Y., Tsuboi, H., Nagayama, Y., Kashii, M., Miyama, A., Kunugiza, Y., Hirao, M., Okamura, G., Noguchi, T., Takami, K., Goshima, A., Miura, T., Fukuda, Y., Kurihara, T., Okada, S., & Nakata, K. (2022). Effects of prior osteoporosis treatment on the treatment response of romosozumab followed by denosumab in patients with postmenopausal osteoporosis. Osteoporosis international : a journal established as result of cooperation between the European Foundation for Osteoporosis and the National Osteoporosis Foundation of the USA, 33(8), 1807-1813.}}{{הערה|שם=הערה16|Tominaga, A., Wada, K., Okazaki, K., Nishi, H., Terayama, Y., Kodama, Y., & Kato, Y. (2022). Effect of the duration of previous osteoporosis treatment on the effect of romosozumab treatment. Osteoporosis international : a journal established as result of cooperation between the European Foundation for Osteoporosis and the National Osteoporosis Foundation of the USA, 33(6), 1265-1273.}}{{הערה|שם=הערה17|Inose, H., Ariga, A., Motoyoshi, T., Fukushima, K., Tomizawa, S., Kato, T., Takahashi, K., Yoshii, T., & Okawa, A. (2022). The Real- World Effect of 12 Months of Romosozumab Treatment on Patients With Osteoporosis With a High Risk of Fracture and Factors Predicting the Rate of Bone Mass Increase: A Multicenter Retrospective Study. JBMR plus, 6(7), e10637. https://doi.org/10.1002/jbm4.10637.}}. מטופלים נאיביים שקיבלו טיפול ברומוסוזומב כקו טיפול ראשון הראו את התגובה הטיפולית הגבוהה ביותר בהשוואה לקבוצות האחרות, על פי מדד עלייה בצפיפות העצם. בנוסף, מטופלים שקיבלו טריפרטייד כקו ראשון וטופלו ברומוסוזומב, כטיפול בונה עצם נוסף, הראו את התגובה הטיפולית השנייה בעוצמתה מבחינת עלייה בצפיפות העצם. | + | נתונים התומכים בבקשת ההרחבה: מחקרי עולם אמיתי שנערכו על יותר מ־500 חולים וחולות באוסטאופורוזיס בקו טיפולי ראשון ושני, הראו שאפקט הטיפול ברומוסוזומב על עלייה בצפיפות העצם בעמוד השדרה, עצם הירך וצוואר הירך הושפע ממתן טיפול קודם לאוסטאופורוזיס{{הערה|שם=הערה15|Ebina, K., Etani, Y., Tsuboi, H., Nagayama, Y., Kashii, M., Miyama, A., Kunugiza, Y., Hirao, M., Okamura, G., Noguchi, T., Takami, K., Goshima, A., Miura, T., Fukuda, Y., Kurihara, T., Okada, S., & Nakata, K. (2022). Effects of prior osteoporosis treatment on the treatment response of romosozumab followed by denosumab in patients with postmenopausal osteoporosis. Osteoporosis international : a journal established as result of cooperation between the European Foundation for Osteoporosis and the National Osteoporosis Foundation of the USA, 33(8), 1807-1813.}}{{הערה|שם=הערה16|Tominaga, A., Wada, K., Okazaki, K., Nishi, H., Terayama, Y., Kodama, Y., & Kato, Y. (2022). Effect of the duration of previous osteoporosis treatment on the effect of romosozumab treatment. Osteoporosis international : a journal established as result of cooperation between the European Foundation for Osteoporosis and the National Osteoporosis Foundation of the USA, 33(6), 1265-1273.}}{{הערה|שם=הערה17|Inose, H., Ariga, A., Motoyoshi, T., Fukushima, K., Tomizawa, S., Kato, T., Takahashi, K., Yoshii, T., & Okawa, A. (2022). The Real- World Effect of 12 Months of Romosozumab Treatment on Patients With Osteoporosis With a High Risk of Fracture and Factors Predicting the Rate of Bone Mass Increase: A Multicenter Retrospective Study. JBMR plus, 6(7), e10637. https://doi.org/10.1002/jbm4.10637.}}. מטופלים נאיביים שקיבלו טיפול ברומוסוזומב כקו טיפול ראשון הראו את התגובה הטיפולית הגבוהה ביותר בהשוואה לקבוצות האחרות, על פי מדד עלייה בצפיפות העצם. בנוסף, מטופלים שקיבלו טריפרטייד כקו ראשון וטופלו ברומוסוזומב, כטיפול בונה עצם נוסף, הראו את התגובה הטיפולית השנייה בעוצמתה מבחינת עלייה בצפיפות העצם. |
==ביבליוגרפיה== | ==ביבליוגרפיה== | ||
| שורה 67: | שורה 67: | ||
'''הכתבה בחסות חברת מדיסון ללא מעורבות בתכנים ואינה מהווה תחליף לייעוץ רפואי.''' | '''הכתבה בחסות חברת מדיסון ללא מעורבות בתכנים ואינה מהווה תחליף לייעוץ רפואי.''' | ||
| − | |||
[[קטגוריה:אנדוקרינולוגיה וסוכרת]] | [[קטגוריה:אנדוקרינולוגיה וסוכרת]] | ||
גרסה מ־04:33, 29 בנובמבר 2024
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| אוסטאופורוזיס - טיפול ברומוסוזומב | ||
|---|---|---|
| ' | ||
| ||
| שמות נוספים | הרחבת הסל לטיפול באוסטאופורוזיס | |
| יוצר הערך | ד"ר רקפת בכרך | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – אוסטאופורוזיס#טיפול
ערך זה מעודכן לשנת 2024
כאשר נשקלת הכנסת תרופה מסוימת לסל שירותי הבריאות, נבדקים שני שיקולים עיקריים - יעילות התרופה ועלות התרופה. כלכלני בריאות מנסים לחשב כמה אלפי שקלים מוציאים בשנה כדי להרוויח שנת חיים נוספת וכך מציגים לוועדת הסל מדד של עלות־תועלת. נושא שאין להתעלם ממנו הוא איכות חיים, מדד סובייקטיבי שקשה מאוד להעריך, כי מי יכול להחליט אם כאב ראש קודם לכאב גב, לדוגמה.
מטרת הטיפול באוסטאופורוזיס היא מניעת שברים, מניעת תחלואה ותמותה ומניעת סבל.
בניית עצם מהירה ויעילה למניעת שברים אוסטיאופורוטיים
אוסטאופורוזיס היא מחלה המאופיינת בסיכון מוגבר לשברים ואיתם הסיכון לתחלואה ולתמותה[1]. בישראל, כל אישה שלישית וכל גבר חמישי יחוו שבר אוסטיאופורוטי במהלך חייהם ועלות הטיפול בשברים הללו למערכת הבריאות היא עצומה[2]. אוסטאופורוזיס מתאפיינת בירידה במסה ובאיכות העצם ודרושים טיפולים שמסוגלים לעודד בניית עצם חדשה ולשפר את איכות המבנה של העצם הפגומה. רוב התרופות הקיימות לטיפול באוסטאופורוזיס הן אנטי-רזורפטיביות, קרי עוצרות פירוק עצם, אך בו זמנית מפחיתות את יכולת הבנייה של העצם, כך שהן בעיקר עוצרות את תהליך דלדול העצם אבל אינן מסוגלות לשקם אותה.
קיימים תכשירים אנבולים, אנלוגים של הורמון הפרהתירואיד (PTH) שמעודדים יצירת עצם אך במקביל מעלים פירוק עצם (מגבירים את תהליך ה־Remodeling Bone, כך שיכולתם לבנות עצם למעשה מוגבלת).
- Romosozumab - נוגדן מונוקלונלי לסקלרוסטין - היא תרופה המעכבת סקלרוסטין ובכך מעודדת בנית עצם ומפחיתה פירוק עצם בו זמנית. התרופה ניתנת בהזרקה תת-עורית פעם בחודש למשך שנה
- Sclerostin - לאחר התגלית שחוסר בסקלרוסטין גורם למחלות גנטיות נדירות המתאפיינות במסת עצם גבוהה ועמידות בפני שברים[3][4], סלקרוסטין הפך מטרה למחקר ופיתוח לטיפול באוסיטאופורוזיס. סקלרוסטין מופרש על ידי תא האוסטאוציט והוא רגולטור שלילי של בניית עצם. סקלרוסטין מעכב את n־Wnt signaimg ומעכב בניית עצם דרך השפעתו על התפתחות ותפקוד תא האוסטאובלסט[5]
מחקרים פרה-קליניים וקליניים
במחקר פאזה 2, טיפול ברומוסוזומב בנשים פוסט-מנופאוזליות במשך שנה לווה בעלייה משמעותית בצפיפות העצם, עם עלייה בסמנים של בניית עצם שנמשכה כתשעה חודשים וכן הפחתה יציבה בסמני ספיגת עצם[6]. לאחר מכן, מחקרים קליניים פאזה 3 בחנו את היעילות ואת הבטיחות של הטיפול ברומוסוזומאב:
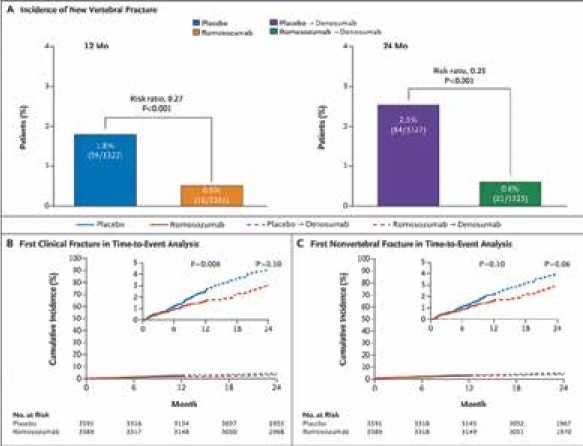
- מחקר ה-FRAME - מחקר אקראי מבוקר שבו 7,180 נשים פוסט-מנופאוזליות קיבלו רומוסוזומב או פלצבו למשך 12 חודשים ולאחר מכן דנוסומב לתקופה של 12 חודשים. הטיפול ברומוסוזומב לווה בעלייה משמעותית בצפיפות העצם ובהפחתה משמעותית (של 73%) בסיכון לשברים חדשים בעמוד השדרה ולשברים קליניים (ירידה של 36%) לעומת פלצבו לאחר 12 חודשי טיפול. התוצאות לגבי שברים מחוץ לעמוד השדרה לא הגיעו למובהקות סטטיסטית. המחברים הסבירו ששיעור נמוך מאוד של שברים אלה באזור אמריקה הלטינית השפיע על התוצאות, כאשר בשאר האזורים שנסקרו במחקר התוצאות היו מובהקות גם בהפחתת שברים מחוץ לעמוד השדרה[7]
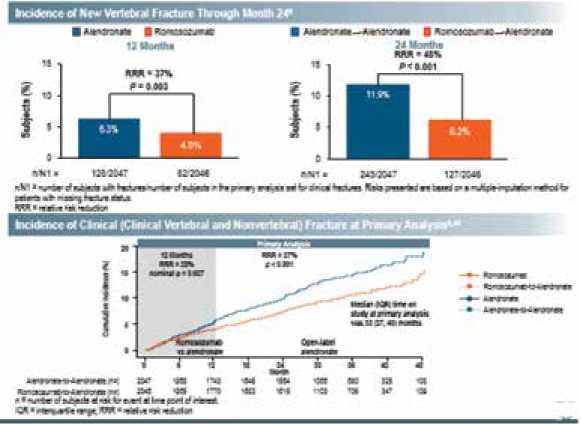
- מחקר ה-ARCH - מחקר שבו השתתפו 4,093 נשים פוסט מנופאוזליות עם אוסטאופורוזיס ושברים קודמים וחולקו באופן אקראי וסמוי לשתי קבוצות: רומוסוזומב או Alendronate לתקופה של 12 חודשים ולאחר מכן טיפול באלנדרונט לכל המשתתפות ל־24 חודשים נוספים. התוצאות אחרי 24 חודשי טיפול היו לטובת רומוסוזומב עם הפחתת שברים משמעותית יותר. למעשה, כבר אחרי 12 חודשי טיפול הודגמה הפחתה מובהקת בסיכון לשברים בעמוד השדרה, לשברים קליניים והן לשברים מאג'וריים מחוץ לעמוד השדרה[8]
- מחקר STRUCTURED - 436 נשים פוסט־מנפאוזליות עם טיפול קודם בביספוספונטים פומיים השתתפו במחקר זה וקיבלו באופן בלתי סמוי רומוסוזומב או טריפרטייד (PTH ANALOG) למשך 12 חודשים. הטיפול ברומוסוזומב לווה בעלייה משמעותית יותר בצפיפות העצם בהשוואה לטיפול בטריפרטייד. הבדל מובהק בין שתי הקבוצות בצפיפות עצם בעמוד השדרה, בירך ובצוואר הירך, נצפה אחרי שישה חודשי טיפול. במהלך ששת החודשים הללו נצפתה עלייה מובהקת של צפיפות עצם בירך ובצוואר הירך במטופלות ברומוסוזומב בהשוואה לקבוצת הטריפרטייד[9]. הערכות שבוצעו הצביעו על הבדל בין שתי הקבוצות בחוזק עצם הירך לטובת רומוסוזומב. התוצא במחקר זה היה שינוי בצפיפות העצם. שינוי בצפיפות העצם באתר הירך TOTAL HIP נחשב למנבא טוב למניעת שברים אבל אין ממחקר זה מידע על הסיכון לשברים[10][11]
בטיחות בטיפול
במחקרים אלה הסבילות לטיפול ברומוסוזומב הייתה טובה, נרשמו מעט תגובות באזור הזרקת התרופה (כ־5% לעומת 3% בקבוצת הפלצבו). כל המשתתפות במחקרים קיבלו תוספים של סידן וויטמין D ונרשמו מעט אירועי היפוקלצמיה שהייתה קלה, חולפת ואסימפטומטית לרוב. כ־15% עד 20% מהמשתתפות פיתחו נוגדנים לרומוסוזומב אך לא נראה שלתופעה יש השלכה על יעילות הטיפול.
ה-WNT signaling מעורב בתהליכי שגשוג תאי ברקמות רבות ולכן קיימת דאגה תאורטית לגבי התפתחות של תהליכים נאופלסטיים. לא נראה בשלב זה אף סיגנל, גם לא בנוגע להתפתחות גידולי עצם מסוג אוסטיאוסרקומה בחולדות כפי שנצפה עם אנלוגים של PTH[12].
בטיחות וסקולרית - לא נרשם סינגל במחקר FRAMED (רומוסוזומב מול פלצבו) אבל במחקר ה־ARCH נרשמו יותר אירועי MACE Major Adverse Cardiac Events: composite of cardiovascular death, nonfatal myocardial infarction and nonfatal stroke בקבוצת רומוסוזומב (2%) יחסית לקבוצת אלנדרונט (1.1%)[12][13].
המנגנון של אפקט וסקולרי אפשרי אינו ברור וקיימות השערות לגבי תפקידו של סקלרוסטין בטרשת עורקים. השערה נוספת היא שלאלנדרונט אפקט קרדיווסקולרי מגן כיוון שמול פלצבו לא נראה סיגנל כלל. נעשות אנליזות נוספות במחקרים קיימים על מנת לנסות לשפוך אור על סוגיה זו.
סטטוס נוכחי (נכון ל-2023)
רומוסוזומב קיבל את אישורי ה־FDA וה־EMEA ורשום בישראל לטיפול באוסטאופורוזיס בסיכון גבוה לשבר. התרופה כלולה בסל שירותי הבריאות כטיפול קו שני, לאחר כישלון טיפול בתרופות קו ראשון (ירידה בצפיפות העצם ב־5% ומעלה או שבר אוסטיאופורוטי תחת טיפול) וגם כקו ראשון במטופלים עם אוסטאופורוזיס לפי צפיפות עצם + שבר אוסטיאופורוטי ובמקרים של קונטרה אינדיקציה מוחלטת לטיפול בטריפרטייד.
סל שירותי הבריאות בישראל הוא מהמתקדמים בעולם ומאפשר טיפול לנשים ולגברים הסובלים מאוסטאופורוזיס, ובכל זאת יש מקום להרחבת הסל.
בקשת ההרחבה לסל שירותי הבריאות 2024
קו טיפול ראשון בחולות עם אוסטאופורוזיס בסיכון גבוה מאוד לשבר, ללא ההגבלה של קונטרה אינדיקציה למתן טריפרטייד.
נתונים התומכים בבקשת ההרחבה: מעבר לנתונים שהתקבלו בניסויים הקליניים של רומוסוזומב, FRAME, ARCH ו־STRUCTURE, נכללה גם מטא־אנאליזה, שהתפרסמה ב-2023 והשוותה את יעילות ובטיחות הטיפול ברומוסוזומב כקו טיפול ראשון ושני לעומת טריפרטייד, אלנדרונאט ופלצבו. האנליזה כללה תשעה מחקרים קליניים אקראיים מבוקרים עם יותר מ־12,000 מטופלות פוסט מנופאוזאליות[14]. התוצאות הראו שרומוסוזומב הורידה משמעותית שברים בחוליות, שברים לא חולייתיים ושברים קליניים (בהשוואה לאלנדרונאט או לפלצבו). כמו כן, הטיפול ברומוסוזומב העלה באופן משמעותי את צפיפות העצם בירך, בצוואר הירך ובעמוד השדרה המותני, בהשוואה לטריפרטייד, אלנדרונאט ופלצבו. לא היו הבדלים בשיעור תופעות הלוואי, כולל וסקולריות, למעט תגובתיות באתר ההזרקה שנצפתה יותר במטופלות שקיבלו רומוסוזומב.
הרחבת הזכאות לחולות אוסטאופורוזיס לקבל טיפול בונה עצם (רומוסוזומב או טריפרטייד) יותר מפעם אחת במהלך המחלה.
נתונים התומכים בבקשת ההרחבה: מחקרי עולם אמיתי שנערכו על יותר מ־500 חולים וחולות באוסטאופורוזיס בקו טיפולי ראשון ושני, הראו שאפקט הטיפול ברומוסוזומב על עלייה בצפיפות העצם בעמוד השדרה, עצם הירך וצוואר הירך הושפע ממתן טיפול קודם לאוסטאופורוזיס[15][16][17]. מטופלים נאיביים שקיבלו טיפול ברומוסוזומב כקו טיפול ראשון הראו את התגובה הטיפולית הגבוהה ביותר בהשוואה לקבוצות האחרות, על פי מדד עלייה בצפיפות העצם. בנוסף, מטופלים שקיבלו טריפרטייד כקו ראשון וטופלו ברומוסוזומב, כטיפול בונה עצם נוסף, הראו את התגובה הטיפולית השנייה בעוצמתה מבחינת עלייה בצפיפות העצם.
ביבליוגרפיה
- ↑ Cummings SR, Melton LJ. Epidemiology and outcomes of osteoporotic fractures. Lancet2002;359:1761-1767
- ↑ I. Goldshtein1,3, J. Chandler2, V. Shalev1,3, S. Ish -Shalom4, A.M. Nguyen2, V. Rouach5, G. Chodick1,3OSTEOPOROSIS IN THE COMMUNITY: FINDINGS FROM A NOVEL COMPUTERIZED REGISTRY IN A LARGE HEALTH ORGANIZATION IN ISRAEL. JARCP The Journal of Aging Research & Clinical Practice 2012.
- ↑ Balemans W, Ebeling M, Patel N, et al. Increased bone density in sclerosteosis is due to the deficiency of a novel secreted protein (SOST). Hum Mol Genet 2001;10:537-543
- ↑ Brunkow ME, Gardner JC, Van Ness J, et al. Bone dysplasia sclerosteosis results from loss of the SOST gene product, a novel cystine knot-containing protein. Am J Hum Genet 2001;68:577-589
- ↑ Li X, Zhang Y, Kang H, et al. Sclerostin binds to LRP5/6 and antagonizes canonical Wnt signaling. J Biol Chem 2005;280:19883-19887
- ↑ Ishibashi H,et al. Romosozumab increases bone mineral density in postmenopausal Japanese women with osteoporosis: a phase 2 study. Bone. 2017:103:209-215.
- ↑ Cosman F, et al. Romosozumab Treatment in Postmenopausal Women with Osteoporosis. N Engl J Med 375;16: 1533-43.
- ↑ Saag KG, et al. Romosozumab or Alendronate for Fracture Prevention in Women with Osteoporosis. N Engl J Med 2017;377:1417-27.
- ↑ Langdahl B, et al. Romosozumab versus Teriparatide in Postmenopausal Women with Osteoporosis Transitioning from Oral Bisphosphonate Therapy: a randomised, open¬label, phase 3 trial. Lancet 2017; 390: 1585-94
- ↑ J.P., Recknor C. Effects of romosozumab compared with teriparatide on bone density and mass at the spine and hip in postmenopausal women with low bone mass. J Bone Miner Res. 2017;32:181-187
- ↑ Keaveny T.M., Crittenden D.B., Bolognese M.A., Genant H.K., Engelke K., Oliveri B. Greater gains in spine and hip strength for romosozumab compared with teriparatide in postmenopausal women with low bone mass. J Bone Miner Res. 2017;32:1956-1962
- ↑ 12.0 12.1 McClung MR, Romosozumab for The Treatment of Osteoporosis. Osteoporosis and Sarcopenia 4 (2018) 11-15
- ↑ ROMOSUZUMAB FDA PI 2019
- ↑ Huang W, Nagao M, Yonemoto N, Guo S, Tanigawa T, Nishizaki Y. Evaluation of the efficacy and safety of romosozumab (evenity) for the treatment of osteoporotic vertebral compression fracture in postmenopausal women: A systematic review and meta-analysis of randomized controlled trials (CDM-J). Pharmacoepidemiol Drug Saf. 2023;32(6):671-684.
- ↑ Ebina, K., Etani, Y., Tsuboi, H., Nagayama, Y., Kashii, M., Miyama, A., Kunugiza, Y., Hirao, M., Okamura, G., Noguchi, T., Takami, K., Goshima, A., Miura, T., Fukuda, Y., Kurihara, T., Okada, S., & Nakata, K. (2022). Effects of prior osteoporosis treatment on the treatment response of romosozumab followed by denosumab in patients with postmenopausal osteoporosis. Osteoporosis international : a journal established as result of cooperation between the European Foundation for Osteoporosis and the National Osteoporosis Foundation of the USA, 33(8), 1807-1813.
- ↑ Tominaga, A., Wada, K., Okazaki, K., Nishi, H., Terayama, Y., Kodama, Y., & Kato, Y. (2022). Effect of the duration of previous osteoporosis treatment on the effect of romosozumab treatment. Osteoporosis international : a journal established as result of cooperation between the European Foundation for Osteoporosis and the National Osteoporosis Foundation of the USA, 33(6), 1265-1273.
- ↑ Inose, H., Ariga, A., Motoyoshi, T., Fukushima, K., Tomizawa, S., Kato, T., Takahashi, K., Yoshii, T., & Okawa, A. (2022). The Real- World Effect of 12 Months of Romosozumab Treatment on Patients With Osteoporosis With a High Risk of Fracture and Factors Predicting the Rate of Bone Mass Increase: A Multicenter Retrospective Study. JBMR plus, 6(7), e10637. https://doi.org/10.1002/jbm4.10637.
המידע שבדף זה נכתב על ידי ד"ר רקפת בכרך - מומחית ברפואת המשפחה, יו"ר עילא - העמותה הישראלית לאוסטאופורוזיס ומחלות עצם
הכתבה בחסות חברת מדיסון ללא מעורבות בתכנים ואינה מהווה תחליף לייעוץ רפואי.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק