הבדלים בין גרסאות בדף "Survivin"
| שורה 1: | שורה 1: | ||
{{בדיקת מעבדה | {{בדיקת מעבדה | ||
|שם עברי={{רווח קשיח}} | |שם עברי={{רווח קשיח}} | ||
| − | |שם לועזי=survivin | + | |שם לועזי=survivin |
|קיצור= | |קיצור= | ||
|תמונה= | |תמונה= | ||
| שורה 8: | שורה 8: | ||
|תחום=מחלות סרטניות. | |תחום=מחלות סרטניות. | ||
|יחידות מדידה= | |יחידות מדידה= | ||
| − | |טווח ערכים תקין=540-1,650 פיקוגרם/מ"ל עם SD של 843.5 פיקוגרם/מ"ל. | + | |טווח ערכים תקין=540-1,650 פיקוגרם/מ"ל עם SD של 843.5 פיקוגרם/מ"ל. |
|יוצר הערך=[[משתמש:בן עמי סלע|פרופ' בן-עמי סלע]] | |יוצר הערך=[[משתמש:בן עמי סלע|פרופ' בן-עמי סלע]] | ||
|אחראי הערך= | |אחראי הערך= | ||
}} | }} | ||
| − | '''Survivin''' ידוע גם | + | '''Survivin''' ידוע גם כ־baculoviral inhibitor of apoptosis repeat-containing 5 (להלן BIRC5) הוא חלבון אשר מקודד באדם על ידי הגן BIRC5 (Altieri ב-Biochemistry משנת 1994, ו-Sah וחב' ב-Cancer Lett משנת 2006). Survivin הוא חבר במשפחת מעכבי האפופטוזיס, והוא פועל כמעכב של שפעול caspase, ועל ידי כך הוא מווסת שלילית את האפופטוזיס או מות התאים המתוכנת בעיקר של תאים סרטניים. חלבון ה-survivin מבוטא בחוזקה ברוב סוגי הסרטן וברקמה העוברית, אך הוא חסר לחלוטין בתאים עם התמיינות (differentiation) (Olie וחב' ב-Cancer Res משנת 2000). נתונים אלה מצביעים על כך ש-survivin יכול להיות יעד לתרפיה של תאי סרטן על ידי דיסקרימינציה בין תאים נורמליים לבין תאים מותמרים. הביטוי של survivin מווסת גם על ידי מחזור התא, והוא מבוטא רק בפאזת G2-M . ידוע גם ש-survivin ממוקם בכישור המיטוטי על ידי אינטראקציה עם tubulin במהלך המיטוזה, ומסוגל לתרום לוויסות המיטוזה. הרגולציה על ידי survivin נראית כרוכה בחלבון p53, והוא גם גן יעד של מסלול Wnt, ועובר רגולציה על ידי β-catenin (Mirza וחב' ב-Oncogene משנת 2002). |
==איזופורמים== | ==איזופורמים== | ||
| − | הגן הבודד של | + | הגן הבודד של survivin יכול לקודד לארבעה טרנסקריפטים שעוברים splicing חלופי (Altiery ב-Biochemistry משנת 1994): |
#Survivin שהוא בעל מבנה של 3 introns ו-4 exons באדם ובעכבר | #Survivin שהוא בעל מבנה של 3 introns ו-4 exons באדם ובעכבר | ||
#Survivin-2B שהוא בעל החדרה של exon 2 חלופי | #Survivin-2B שהוא בעל החדרה של exon 2 חלופי | ||
| שורה 22: | שורה 22: | ||
==המבנה של surviving== | ==המבנה של surviving== | ||
| − | תכונה מבנית של כל החלבונים ממשפחת IAP היא שכולם מכילים לפחות מקטע אחד של baculoviral IAP repeat (להלן BIR) המאופיין על ידי מוטיף משומר של Cys/His הקשור לקואורדינציה של אבץ במחצית ה-N-טרמינלית של החלבון (Chantalat וחב' ב-Mol Cell משנת 2000). Survivin שונה מחברים אחרים במשפחת IAP בכך שיש בו רק מקטע BIR יחיד, כאשר מקטעי BIR באדם ובעכבר מאוד דומים מלבד שני הבדלים שיכולים להשפיע על התפקוד של החלבון. Survivin באדם מכיל גם סלילון (helix) מאורך של C-טרמינל המכיל 42 חומצות אמינו. Surivin הוא חלבון בגודל של 16.5 קילו-דלטון, והוא הקטן ביותר במשפחת חלבוני IAP. קריסטלוגרפיה בעזרת קרני X הראתה 2 מולקולות של החלבון היוצרות דימר עם צורת עֲנִיבַת פַּרְפַּר דרך האינטר-פאזה ההידרופובית. אזור זה כולל | + | תכונה מבנית של כל החלבונים ממשפחת IAP היא שכולם מכילים לפחות מקטע אחד של baculoviral IAP repeat (להלן BIR) המאופיין על ידי מוטיף משומר של Cys/His הקשור לקואורדינציה של אבץ במחצית ה-N-טרמינלית של החלבון (Chantalat וחב' ב-Mol Cell משנת 2000). Survivin שונה מחברים אחרים במשפחת IAP בכך שיש בו רק מקטע BIR יחיד, כאשר מקטעי BIR באדם ובעכבר מאוד דומים מלבד שני הבדלים שיכולים להשפיע על התפקוד של החלבון. Survivin באדם מכיל גם סלילון (helix) מאורך של C-טרמינל המכיל 42 חומצות אמינו. Surivin הוא חלבון בגודל של 16.5 קילו-דלטון, והוא הקטן ביותר במשפחת חלבוני IAP. קריסטלוגרפיה בעזרת קרני X הראתה 2 מולקולות של החלבון היוצרות דימר עם צורת עֲנִיבַת פַּרְפַּר דרך האינטר-פאזה ההידרופובית. אזור זה כולל 6–10 חומצות אמינו ממש לפני אזור BIR, ו-10 חומצות אמינו הקושרות את מקטע BIR עם הסליל ה-C טרמינלי. |
[[קובץ:Survivin1.png|מרכז|600px]] | [[קובץ:Survivin1.png|מרכז|600px]] | ||
===המסלול האקסטרינזי=== | ===המסלול האקסטרינזי=== | ||
| − | מאותחל על ידי ליגנדים אקסטרינזיים הנקשרים אל ה-death receptors על פני שטח הפנים של התא. כדוגמה לכך, היא הקישור של [[TNF-α]] | + | מאותחל על ידי ליגנדים אקסטרינזיים הנקשרים אל ה-death receptors על פני שטח הפנים של התא. כדוגמה לכך, היא הקישור של [[TNF-α]] לקולטן שלו. דוגמה של הקולטן ל-TNF הוא Fas או CD95, המגייס קספזות משפעלות כגון capase-8, לאחר קישור TNF על פני התא. השפעול של קספזה מאותחלת מפעיל קסקדה של האירועים המביאים להשריית effector caspases הפועלות במהלך האפופטוזיס (Shin וחב' ב-Biochemistry משנת 2001, ו-Ambrosini וחב' ב-Nature Med משנת 1997). |
===המסלול האינטרינסי=== | ===המסלול האינטרינסי=== | ||
| שורה 33: | שורה 33: | ||
==מנגנון הפעולה== | ==מנגנון הפעולה== | ||
| − | עיכוב של אפופטוזיס המושרה על ידי Bax ו-Fas:{{כ}} Tamm וחב' הראו ש-survivin מעכב את מסלולי האפופטוזיס המושרים על ידי Bax ו-Fas. הניסוי כלל טרנספקציה של תאי HEK 293 עם פלסמיד המקודד ל-Bax, שמגביר את תהליך האפופטוזיס פי-7 בערך כפי שנמדד על ידי צביעת DAPI. תאים אלה גרמו לטרנספקציה של תאי 293 עם פלסמידים המקודדים ל-Bax ול-survivin. החוקרים הבחינו בכך שהתאים שעברו טרנספקציה הראו ירידה משמעותית של פי-3 באפופטוזיס. תוצאה דומה נמצאה כאשר התאים עברו | + | עיכוב של אפופטוזיס המושרה על ידי Bax ו-Fas:{{כ}} Tamm וחב' הראו ש-survivin מעכב את מסלולי האפופטוזיס המושרים על ידי Bax ו-Fas. הניסוי כלל טרנספקציה של תאי HEK 293 עם פלסמיד המקודד ל-Bax, שמגביר את תהליך האפופטוזיס פי-7 בערך כפי שנמדד על ידי צביעת DAPI. תאים אלה גרמו לטרנספקציה של תאי 293 עם פלסמידים המקודדים ל-Bax ול-survivin. החוקרים הבחינו בכך שהתאים שעברו טרנספקציה הראו ירידה משמעותית של פי-3 באפופטוזיס. תוצאה דומה נמצאה כאשר התאים עברו טרנספקציה עם הפלסמיד המבטא Fax. |
==האינטראקציה של survivin עם קספזות 3 ו-7== | ==האינטראקציה של survivin עם קספזות 3 ו-7== | ||
| שורה 42: | שורה 42: | ||
==תפקיד survivin בסרטן== | ==תפקיד survivin בסרטן== | ||
| − | Survivin ידוע כבא לביטוי בשלב העוברי וברוב סוגי ה[[סרטן]], אך הוא מבוטא | + | Survivin ידוע כבא לביטוי בשלב העוברי וברוב סוגי ה[[סרטן]], אך הוא מבוטא לעיתים נדירות בתאים נורמליים (Castedo וחב' ב-Oncogene משנת 2004). נמצא ש-survivin מתבטא בכל 60 שורות תאים סרטניים באדם, עם הביטוי הגבוה ביותר בתאים סרטניים של ה[[סרטן ריאות|ריאות]] ו[[סרטן השד|השד]], והביטוי הנמוך היותר ב[[סרטן הכליה]] (Tamm וחב' ב-Cancer Res משנת 1998). Survivin יכול להיחשב כאונקוגן, שכן ביטוי היתר שלו ברוב תאי הסרטן, תורם לגירוי האפופטוטי ובכך מביא להשמדתם. |
==ביטוי בסרטן ככלי לתרפיה אנטי-סרטנית== | ==ביטוי בסרטן ככלי לתרפיה אנטי-סרטנית== | ||
| − | Survivin ידוע כמבוטא חזק ברוב סוגי הסרטן וחסר בתאים נורמליים, מה שהופך אותו ליעד טוב לתרפיה אנטי-סרטנית (Pennati וחב' ב-Carcinogenesis משנת 2007, Mita וחב' ב-Clin Cancer Res משנת 2008, Huynh וחב' ב-Biochem Biophys Res Commun משנת 2006, ו-Friedrichs וחב' ב-Leukem Lymphom משנת 2006). הניצול של הפרומוטר של survivin ברוב תאי הסרטן מאפשר את הטיפול התרפויטי רק של תאי סרטן ואי השפעתו על תאים נורמליים (Xiang וחב' ב-Cancer Res משנת 2005). siRNA או RNA התערבותי קטן (siRNA), המכונה לעיתים RNA התערבותי קצר או משתיק RNA הוא סוג של מולקולת RNA דו גדילי, 20-25 זוגות בסיסים באורכו. siRNA ממלא תפקידים רבים, אבל בולט ביותר במסלול ההפרעה ל-RNAi) RNA), שבו הוא מפריע לביטוי של גנים ספציפיים עם רצף נוקליאוטידים משלים. לפיכך השימוש ב-siRNA הוא בעל פוטנציאל גדול להיות בעל השפעה תרפויטית באדם, כיוון שהוא יכול להשתיק את הביטוי של כל חלבון. בעיה מתעוררת כאשר הביטוי של siRNA בתא, אינו יכול להיות מבוקר, מה שמאפשר לביטוי הקונסטיטוטיבי | + | Survivin ידוע כמבוטא חזק ברוב סוגי הסרטן וחסר בתאים נורמליים, מה שהופך אותו ליעד טוב לתרפיה אנטי-סרטנית (Pennati וחב' ב-Carcinogenesis משנת 2007, Mita וחב' ב-Clin Cancer Res משנת 2008, Huynh וחב' ב-Biochem Biophys Res Commun משנת 2006, ו-Friedrichs וחב' ב-Leukem Lymphom משנת 2006). הניצול של הפרומוטר של survivin ברוב תאי הסרטן מאפשר את הטיפול התרפויטי רק של תאי סרטן ואי השפעתו על תאים נורמליים (Xiang וחב' ב-Cancer Res משנת 2005). siRNA או RNA התערבותי קטן (siRNA), המכונה לעיתים RNA התערבותי קצר או משתיק RNA הוא סוג של מולקולת RNA דו גדילי, 20-25 זוגות בסיסים באורכו. siRNA ממלא תפקידים רבים, אבל בולט ביותר במסלול ההפרעה ל-RNAi) RNA), שבו הוא מפריע לביטוי של גנים ספציפיים עם רצף נוקליאוטידים משלים. לפיכך השימוש ב-siRNA הוא בעל פוטנציאל גדול להיות בעל השפעה תרפויטית באדם, כיוון שהוא יכול להשתיק את הביטוי של כל חלבון. בעיה מתעוררת כאשר הביטוי של siRNA בתא, אינו יכול להיות מבוקר, מה שמאפשר לביטוי הקונסטיטוטיבי לגרום לתופעות לוואי טוקסיות. בהקשר של הטיפול הפרקטי של סרטן, נדרש או להחדיר את siRNA באופן ספציפי לתוך תאי הסרטן, או לפקח על הביטוי של siRNA. |
==אי יציבות גנומית== | ==אי יציבות גנומית== | ||
| שורה 59: | שורה 59: | ||
==הוראות לביצוע הבדיקה== | ==הוראות לביצוע הבדיקה== | ||
| − | דגימת הדם | + | דגימת הדם נלקחה בקירור לתוך מבחנה כימית (פקק אדום או צהוב). לאחר סרכוז המתבצע בקירור, נאסף הנוזל העליון שהוא הנסיוב בדימות מהולות 1:10 והמדידה נעשית בשיטת sandwich enzyme-linked immunoassay המכילה נוגדנים אנטי-survivin בתוספת סטנדרט ריקומביננטי (DY647 R&D Systems, Minneapolis). סף הגילוי הוא 100 פיקוגרם/מ"ל. רמת ה-cutoff של חיוביות של surviving נקבעה כ-450 פיקוגרם/מ"ל על בסיס התוצאה של 104 מתנדבים בריאים (Andersson וחב' ב-PLoS One משנת 2012). |
==ראו גם== | ==ראו גם== | ||
* [[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | * [[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | ||
* [[סמנים סרטניים|בדיקות מעבדה - סמנים סרטניים]] | * [[סמנים סרטניים|בדיקות מעבדה - סמנים סרטניים]] | ||
| − | |||
{{ייחוס בן עמי}} | {{ייחוס בן עמי}} | ||
גרסה מ־06:04, 2 בדצמבר 2024
| מדריך בדיקות מעבדה | |
| survivin | |
|---|---|
| מעבדה | כימיה בדם |
| תחום | מחלות סרטניות. |
| טווח ערכים תקין | 540-1,650 פיקוגרם/מ"ל עם SD של 843.5 פיקוגרם/מ"ל. |
| יוצר הערך | פרופ' בן-עמי סלע |
Survivin ידוע גם כ־baculoviral inhibitor of apoptosis repeat-containing 5 (להלן BIRC5) הוא חלבון אשר מקודד באדם על ידי הגן BIRC5 (Altieri ב-Biochemistry משנת 1994, ו-Sah וחב' ב-Cancer Lett משנת 2006). Survivin הוא חבר במשפחת מעכבי האפופטוזיס, והוא פועל כמעכב של שפעול caspase, ועל ידי כך הוא מווסת שלילית את האפופטוזיס או מות התאים המתוכנת בעיקר של תאים סרטניים. חלבון ה-survivin מבוטא בחוזקה ברוב סוגי הסרטן וברקמה העוברית, אך הוא חסר לחלוטין בתאים עם התמיינות (differentiation) (Olie וחב' ב-Cancer Res משנת 2000). נתונים אלה מצביעים על כך ש-survivin יכול להיות יעד לתרפיה של תאי סרטן על ידי דיסקרימינציה בין תאים נורמליים לבין תאים מותמרים. הביטוי של survivin מווסת גם על ידי מחזור התא, והוא מבוטא רק בפאזת G2-M . ידוע גם ש-survivin ממוקם בכישור המיטוטי על ידי אינטראקציה עם tubulin במהלך המיטוזה, ומסוגל לתרום לוויסות המיטוזה. הרגולציה על ידי survivin נראית כרוכה בחלבון p53, והוא גם גן יעד של מסלול Wnt, ועובר רגולציה על ידי β-catenin (Mirza וחב' ב-Oncogene משנת 2002).
איזופורמים
הגן הבודד של survivin יכול לקודד לארבעה טרנסקריפטים שעוברים splicing חלופי (Altiery ב-Biochemistry משנת 1994):
- Survivin שהוא בעל מבנה של 3 introns ו-4 exons באדם ובעכבר
- Survivin-2B שהוא בעל החדרה של exon 2 חלופי
- Survivin-delta-Ex-3 בו exon-3 הוסר, מה שגורם לשינוי מסגרת היוצר טרמינל קרבוקסילי ייחודי עם תפקוד חדש. תפקוד זה עשוי להיות קשור לסיגנל גרעיני, וכן לסיגנל מיטוכונדריאלי
- Survivin-3B בו יש החדרה של exon 3 חלופי
המבנה של surviving
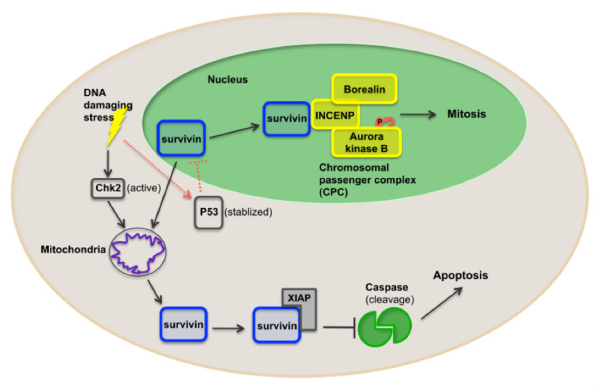
תכונה מבנית של כל החלבונים ממשפחת IAP היא שכולם מכילים לפחות מקטע אחד של baculoviral IAP repeat (להלן BIR) המאופיין על ידי מוטיף משומר של Cys/His הקשור לקואורדינציה של אבץ במחצית ה-N-טרמינלית של החלבון (Chantalat וחב' ב-Mol Cell משנת 2000). Survivin שונה מחברים אחרים במשפחת IAP בכך שיש בו רק מקטע BIR יחיד, כאשר מקטעי BIR באדם ובעכבר מאוד דומים מלבד שני הבדלים שיכולים להשפיע על התפקוד של החלבון. Survivin באדם מכיל גם סלילון (helix) מאורך של C-טרמינל המכיל 42 חומצות אמינו. Surivin הוא חלבון בגודל של 16.5 קילו-דלטון, והוא הקטן ביותר במשפחת חלבוני IAP. קריסטלוגרפיה בעזרת קרני X הראתה 2 מולקולות של החלבון היוצרות דימר עם צורת עֲנִיבַת פַּרְפַּר דרך האינטר-פאזה ההידרופובית. אזור זה כולל 6–10 חומצות אמינו ממש לפני אזור BIR, ו-10 חומצות אמינו הקושרות את מקטע BIR עם הסליל ה-C טרמינלי.
המסלול האקסטרינזי
מאותחל על ידי ליגנדים אקסטרינזיים הנקשרים אל ה-death receptors על פני שטח הפנים של התא. כדוגמה לכך, היא הקישור של TNF-α לקולטן שלו. דוגמה של הקולטן ל-TNF הוא Fas או CD95, המגייס קספזות משפעלות כגון capase-8, לאחר קישור TNF על פני התא. השפעול של קספזה מאותחלת מפעיל קסקדה של האירועים המביאים להשריית effector caspases הפועלות במהלך האפופטוזיס (Shin וחב' ב-Biochemistry משנת 2001, ו-Ambrosini וחב' ב-Nature Med משנת 1997).
המסלול האינטרינסי
מסלול זה מאותחל על ידי גירוי פנימי בתא. הוא ממוקד על ידי גילוי תפקוד לקוי של המיטוכונדריה בתא, וכתגובה משפעל את מסלולי האיתות לאובדן התא. החודרנות הממברנלית של המיטוכונדריה גדלה, וחלבונים ספציפיים מופרשים לתוך הציטופלזמה ומאפשרים את השפעול של קספזות. החלבון הפרטיקולרי המופרש מהמיטוכונדריה הוא ציטוכרום C, הנקשר ל-Apaf-1 בציטוזול וכתוצאה מכך משופעל caspase-9. שפעול זה מאתחל את הקסקדה של אירועים המסתיימים בהשריית effector caspases הפועלים באפופטוזיס. חלבוני IAP כגון survivin מעכבים את האפופטוזיס על ידי עיכוב התפקוד של קספזות.
מנגנון הפעולה
עיכוב של אפופטוזיס המושרה על ידי Bax ו-Fas: Tamm וחב' הראו ש-survivin מעכב את מסלולי האפופטוזיס המושרים על ידי Bax ו-Fas. הניסוי כלל טרנספקציה של תאי HEK 293 עם פלסמיד המקודד ל-Bax, שמגביר את תהליך האפופטוזיס פי-7 בערך כפי שנמדד על ידי צביעת DAPI. תאים אלה גרמו לטרנספקציה של תאי 293 עם פלסמידים המקודדים ל-Bax ול-survivin. החוקרים הבחינו בכך שהתאים שעברו טרנספקציה הראו ירידה משמעותית של פי-3 באפופטוזיס. תוצאה דומה נמצאה כאשר התאים עברו טרנספקציה עם הפלסמיד המבטא Fax.
האינטראקציה של survivin עם קספזות 3 ו-7
בשלב זה של הניסוי, Tamm וחב' ביצעו טרנספקציה של תאי 293 עם survivin וגרמו לתאים ליזיס, כאשר הליזטים שהתקבלו הודגרו עם צורות קספזה שונות, ו-survivin הושקע על ידי נוגדנים אנטי-survivin. המשקעים הללו הורצו בג'ל של SDS PAGE והג'ל עבר immunoblotting על גליונות ניטרו-צלולוז כדי לגלות את הקספזות שהושקעו. נמצא שקספזה-3 וקספזה-7 אמנם הושקעו על ידי survivin. נמצא גם ש-survivin אינו נקשר לקספזה-8. תוצאות אלה מדגימות את היכולת של survivin לקשור לקספזות מסוימות in vitro. באופן דומה, תוך התבוננות במסלול המיטוכונדריאלי של אפופטוזיס, ציטוכרום c נמצא מבוטא באופן בר-חלוף בתאי 293, וכן ש-survivin מעכב את השפעול של קספזות על ידי עיכוב ציטוכרום c. במהלך השלבים השונים של מיטוזה ניתן היה להיווכח ש-survivin ממוקם בעיקר בגרעין בשלבי ה-prophase וה-metaphase (Altieri ב-Nat Rev Cancer משנת 2003), כאשר בשלב ה-prophase כאשר הכרומטין נדחס באופן שניתן לראותו במיקרוסקופ, survivin מתחיל לנוע לכיוון הצנטרומרים. בשלב ה-prometaphase כאשר ממברנת הגרעין מתפרקת והמיקוטובולי של הכישור עוברים לאזור הגרעיני, נותר survivin צמוד לצנטרומרים.
ביטוי-יתר של survivin בגידולים סרטניים ובגרורות
Xiang וחב' (Xiang וחב' ב-Cancer Res משנת 2005) מצאו גישה חדשה לעכב שגשוג גידול סרטני על ידי התקפה סימולטנית של התגובה של תאי T ציטוטוקסיים (CTL) כנגד survivin, מה שגורם מאוחר יותר לשפעול של אפופטוזיס בתאים הסרטניים. הרעיון מאחורי טכניקה זו מתואר להלן: עכברים חוסנו באופן פומי ואז נחשפו לאתגרים סרטניים על ידי שהזריקו להם לחזה מספר מסוים של תאי סרטן. העכברים הוקרבו ושכבת האנדותל שלהם נצבעה עם חומר פלואורסצנטי שסייע בכימות של הנאו-וסקולריזציה תוך שימוש בבדיקת matrigel. בדיקה זו תופסת מקום בסיטואציות דומות: Matrigel מופק מ-Engelbreth-Holm-Swarm (להלן EHS) של סארקומה בעכבר, גידול עשיר בחלבונים של משתית חוץ-תאית (ECM). החומר matrigel מורכב בעיקר מ-laminin (בערך 60%), מקולאגן IV (בערך 30%), ומ-nidogen-1/entactin (בערך 8%), וכן הוא מכיל פרוטאוגליקנים כהפארן סולפאט, מ-perlecan, ומחלבוני ECM אחרים, וכן גורמי גדילה הקשורים ל-ECM. Matrigel מחקה את התכונות הפיזיולוגיות של משתית התא, והוא מהווה את המצע המשתיתי הנפוץ ביותר ללימוד של אנגיוגניות in vitro ו-in vivo.
תפקיד survivin בסרטן
Survivin ידוע כבא לביטוי בשלב העוברי וברוב סוגי הסרטן, אך הוא מבוטא לעיתים נדירות בתאים נורמליים (Castedo וחב' ב-Oncogene משנת 2004). נמצא ש-survivin מתבטא בכל 60 שורות תאים סרטניים באדם, עם הביטוי הגבוה ביותר בתאים סרטניים של הריאות והשד, והביטוי הנמוך היותר בסרטן הכליה (Tamm וחב' ב-Cancer Res משנת 1998). Survivin יכול להיחשב כאונקוגן, שכן ביטוי היתר שלו ברוב תאי הסרטן, תורם לגירוי האפופטוטי ובכך מביא להשמדתם.
ביטוי בסרטן ככלי לתרפיה אנטי-סרטנית
Survivin ידוע כמבוטא חזק ברוב סוגי הסרטן וחסר בתאים נורמליים, מה שהופך אותו ליעד טוב לתרפיה אנטי-סרטנית (Pennati וחב' ב-Carcinogenesis משנת 2007, Mita וחב' ב-Clin Cancer Res משנת 2008, Huynh וחב' ב-Biochem Biophys Res Commun משנת 2006, ו-Friedrichs וחב' ב-Leukem Lymphom משנת 2006). הניצול של הפרומוטר של survivin ברוב תאי הסרטן מאפשר את הטיפול התרפויטי רק של תאי סרטן ואי השפעתו על תאים נורמליים (Xiang וחב' ב-Cancer Res משנת 2005). siRNA או RNA התערבותי קטן (siRNA), המכונה לעיתים RNA התערבותי קצר או משתיק RNA הוא סוג של מולקולת RNA דו גדילי, 20-25 זוגות בסיסים באורכו. siRNA ממלא תפקידים רבים, אבל בולט ביותר במסלול ההפרעה ל-RNAi) RNA), שבו הוא מפריע לביטוי של גנים ספציפיים עם רצף נוקליאוטידים משלים. לפיכך השימוש ב-siRNA הוא בעל פוטנציאל גדול להיות בעל השפעה תרפויטית באדם, כיוון שהוא יכול להשתיק את הביטוי של כל חלבון. בעיה מתעוררת כאשר הביטוי של siRNA בתא, אינו יכול להיות מבוקר, מה שמאפשר לביטוי הקונסטיטוטיבי לגרום לתופעות לוואי טוקסיות. בהקשר של הטיפול הפרקטי של סרטן, נדרש או להחדיר את siRNA באופן ספציפי לתוך תאי הסרטן, או לפקח על הביטוי של siRNA.
אי יציבות גנומית
רוב סוגי הסרטן באדם נמצאו מכילים תוספות או חסכים של כרומוזומים בגלל chromosomal instability (להלן CIN), הנגרמת כתוצאה של אינאקטיבציה של גנים המפקחים על סגרגציה ראויה של אחיות כרומטידיות במהלך המיטוזה. ידוע ש-survivin כרוך עם מיקרוטובולי של הכישור המיטוטי בתחילת המיטוזה. הספרות מדווחת על כך שפגיעה ב-survivin בתאי סרטן פוגעת ביצירת מיקרוטובולי וגורמת ל-polyploidy וכן לאפופטוזיס מסיבי. הודגם גם שתאים בהם survivin נפגע, יוצאים מהמיטוזה ללא השגת מַעֲרָךְ כרומוזומלי מה שגורם ליצירת גרעינים טטרפלואידיים. ראיות מאוחרות מראות ש-survivin נדרש לעצירה מיטוטית כאשר הוא נוכח בבעיות במיטוזה.
Survivin נמצא מווסת על ידי מחזור חיי התא, שכן הביטוי שלו נמצא דומיננטי רק בפאזה G2/M (Sampath וחב' ב-Cell משנת 2004). ויסות זה קיים ברמת השעתוק, שכן יש ראיות לכך ש-suvrvivin עובר ubiquinilation ונהרס על ידי פרוטאזומים בשלב האינטר-פאזה של מחזור חיי התא. יתרה מכך, נמצא ש-survivin ממוקם בכישור המיטוטי בשלבי ה-anaphase וה-metaphase של המיטוזה. בנוסף, קשר פיזיקלי נמצא in vitro בין polymerized tubulin ו-survivin. הודגם גם כן שמודיפיקציה בתר-שעתוקית של survivin, כרוכה בזרחון של שייר thr34 המוביל לייצוב החלבון בפאזת G2/M של מחזור חיי התא. כן נמצא ש-p53 פועל באופן שאינו קשור במחזור חיי התא לעכב את הביטוי של survivin (Mirza וחב' ב-Oncogene משנת 2002).
אימונותרפיה של סרטן
כיוון ש-survivin הוא אנטיגן המבוטא בעיקר בתאי סרטן וחסר בתאים נורמליים, הוא הפך למרכז של עניין רב בתחום האימונותרפיה של סרטן. יש ראיות רבות המראות ש-survivin הוא אנטיגן המשפעל בחוזקה תאי-T, וניסויים קליניים החלו להוכיח את התועלת שלו (Friedrichs וחב' ב-Leuk Lympom משנת 2006).
סרטן הערמונית
נמצא שההתפתחות של עמידות הורמונלית בסרטן הערמונית עשויה להיות בעקבות השדרוג של גנים אנטי-אפופטוטיים שאחד מהם הוא survivin (Zhang וחב' ב-Oncogene משנת 2005). על פי חוקרים אלה, אם survivin הוא תורם משמעותי להתפתחות של עמידות לתרפיה הורמונלית של תאי סרטן הערמונית, התמקדות בחלבון זה תחיש את ההשפעה של תרפיה אנטי-אנדרוגנית. תרפיה זו עושה שימוש בתרופות שנועדו להרחיק את הנוכחות של אנדרוגנים בתא ובסביבתו, שכן אנדרוגנים אלה ידועים כמחזקים את האלמותיות של תאי סרטן הערמונית. Zhang חב' קבעו בהתחלה את רמת ביטויו של survivin בתאי LNCaP (שהם תאי סרטן הערמונית התלויים באנדרוגן ומכילים את הקולטנים לאנדרוגן), תוך אנליזת Western, ומצאו ביטוי ניכר של survivin בתאים אלה. תאים שנחשפו ל-dihydrotestosterone (להלן DHT) היו בעלי ביטוי מוגבר רק של survivin ולא של חברים אחרים במשפחת מעכבי אפופטוזיס. ממצא זה מצביע על כך שאנדרוגנים יכולים לשדרג את survivin, התורם לעמידות לאפופטוזיס שמוצאים בתאי סרטן רבים. בשלב הבא, עם הוספה לתאים של התכשיר האנטי-אנדרוגני flutamide, רמת survivin פחתה משמעותית. מאידך גיסא, ביטוי יתר של wild-type survivin, נמצא מפחית משמעותית את רמות האפופטוזיס כתוצאה מטיפול עם flutamide, בהשוואה לטיפול יחידני עם flutamide. לפיכך, תוצאות אלו תומכות בהשערה ש-survivin משחק תפקיד בתכונה האנטי-אפופטוטית של תאי LNCaP, ושעיכוב של survivin בתאי סרטן הערמונית מגביר את ההשפעה התרפויטית של flutamide.
הוראות לביצוע הבדיקה
דגימת הדם נלקחה בקירור לתוך מבחנה כימית (פקק אדום או צהוב). לאחר סרכוז המתבצע בקירור, נאסף הנוזל העליון שהוא הנסיוב בדימות מהולות 1:10 והמדידה נעשית בשיטת sandwich enzyme-linked immunoassay המכילה נוגדנים אנטי-survivin בתוספת סטנדרט ריקומביננטי (DY647 R&D Systems, Minneapolis). סף הגילוי הוא 100 פיקוגרם/מ"ל. רמת ה-cutoff של חיוביות של surviving נקבעה כ-450 פיקוגרם/מ"ל על בסיס התוצאה של 104 מתנדבים בריאים (Andersson וחב' ב-PLoS One משנת 2012).
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק