הבדלים בין גרסאות בדף "נוגדן עצמי ציטופלזמי כנגד תאי פורקינייה סוג 1 - Cytoplasmic autoantibody against purkinje type 1 cells"
| שורה 39: | שורה 39: | ||
==ממצאים מבדיקות אימונו-פלואורסצנטיות ובדיקות תספיג חלבון== | ==ממצאים מבדיקות אימונו-פלואורסצנטיות ובדיקות תספיג חלבון== | ||
Purkinje cell cytoplasmic autoantibody type 1 IgG התגלה בדגימות נסיוב של 81 מטופלות (98%) ובדגימות CSF של 18 מטופלות (22%); מבין 18 המטופלות שה-CSF שלהן נמצא חיובי ל-PCA-1 IgG, שתיים מתוכן (11%) היו בעלות דגימות נסיוב שנמצאו שליליות ל-PCA-1 IgG. החיוביות של purkinje cell cytoplasmic autoantibody type 1, אושרה בכל המקרים תוך שימוש בתספיג חלבון (Western blot) עם אנטיגן מסיס במים שעבר מיצוי מקליפת המוחון של חולדה בוגרת (Yu וחב' ב-Ann Neurol משנת 2001). כאשר הנסיוב וה-CSF נמצאו חיוביים ל-PCA-1 IgG, הטיטרים של הנסיוב נעו בין 480 ל-983,040 (עם חציון של 15,360, כאשר הטווח הנורמלי נמוך מ-120), ואילו הטיטרים ב-CSF נעו בין 128 ל-32,768 (עם חציון של 512). הטיטר בנסיוב ניבא במתינות את הטיטר ב-CSF של מטופלות אלו (R2 = 0.466). כל דגימות הנסיוב קיימו את הקריטריונים האימונו-היסטוכימיים של PCA-1 IgG, והיו גם קשורים לאלמנטים הציטופלזמטיים בנוירונים של ההיפוקמפוס, בנוירונים של חוט השדרה, בגנגליון של השורש הדורסלי, ובתאי Schwan בעצב ההיקפי. | Purkinje cell cytoplasmic autoantibody type 1 IgG התגלה בדגימות נסיוב של 81 מטופלות (98%) ובדגימות CSF של 18 מטופלות (22%); מבין 18 המטופלות שה-CSF שלהן נמצא חיובי ל-PCA-1 IgG, שתיים מתוכן (11%) היו בעלות דגימות נסיוב שנמצאו שליליות ל-PCA-1 IgG. החיוביות של purkinje cell cytoplasmic autoantibody type 1, אושרה בכל המקרים תוך שימוש בתספיג חלבון (Western blot) עם אנטיגן מסיס במים שעבר מיצוי מקליפת המוחון של חולדה בוגרת (Yu וחב' ב-Ann Neurol משנת 2001). כאשר הנסיוב וה-CSF נמצאו חיוביים ל-PCA-1 IgG, הטיטרים של הנסיוב נעו בין 480 ל-983,040 (עם חציון של 15,360, כאשר הטווח הנורמלי נמוך מ-120), ואילו הטיטרים ב-CSF נעו בין 128 ל-32,768 (עם חציון של 512). הטיטר בנסיוב ניבא במתינות את הטיטר ב-CSF של מטופלות אלו (R2 = 0.466). כל דגימות הנסיוב קיימו את הקריטריונים האימונו-היסטוכימיים של PCA-1 IgG, והיו גם קשורים לאלמנטים הציטופלזמטיים בנוירונים של ההיפוקמפוס, בנוירונים של חוט השדרה, בגנגליון של השורש הדורסלי, ובתאי Schwan בעצב ההיקפי. | ||
| + | |||
| + | == ממצאים נוירופתולוגיים== | ||
| + | הרקמות הנוירליות של שתי מטופלות שעברו אוטופסיה, עברו הערכה היסטופתולוגית. כאשר שתי מטופלות אללו היו בחיים, בשתיהן נמצאו סימנים קליניים של פגיעה במוחון ובמסלול הפירמידלי. המוחון, גזע המוח חוט השדרה והגנגליונים בשורש הדורסלי, הראו דלקת פרי-וסקולרית מפושטת, שפעול של המיקרוגליה, קשרירים במיקרוגליה, אובדן נוירונלי מפוזר וגליוזיס. אימונו-פנו-טייפינג של לימפוציטים גילה פרה-דומיננטיות של תאי CD8+ T פרי-וסקולריים ופרנכימליים. התוצאות של בחינה מיקרוסקופית של ההמיספרות המוחיות היו נורמליות בשתי המטופלות האמורות. פרק הזמן הופעת התסמינים ועד לביצוע האוטופסיה היה 17 חודשים לאחת מהן, ו-4 חודשים לשנייה. | ||
| + | |||
| + | ==קישורים נוירולוגיים== | ||
| + | סרטן התגלה ב-73 מטופלות (88%) עם סרטן שד או סרטן müllerian ב-69 מתוך 73 המטופלים (95%). ב-67 מתוך 73 המטופלים (92%), הסרטן היה מוגבל לאתר אנטומי יחיד, וב-6 מתוך 73 המטופלים (8%) הסרטן היה מפושט מקומית או גרורתי. במטופלת אחת אובחנה קרצינומה של השחלה. שתי מטופלות אובחנו עם גידולים חדשים רבים (קרצינומות של השחלה או של החצוצרות באחת מהן, ובשנייה התגלו סרטן השד או של הפריטונאום. בשלוש מתוך ארבע מטופלות בהן הסרטן החדש שהתגלה לא היה סרטן ה- müllerian או קרצינומה של השד, נמצאו גרורות של אדנו-קרצינומה ממקור לא ידוע, ו-4 מטופלות אובחנו על לימפומה. | ||
| + | |||
| + | [[קובץ:Purkinje 3.png|מרכז|600px]] | ||
| + | |||
| + | כאשר גידול סרטני ראשוני או גרורתי לא זוהה בתחילה על ידי הדמייה שגרתית אולטרה-סונוגרפיה או על ידי CT, גילוי ישיר על ידי לפרטומיה ב-4 מטופלות, או על ידי לפרוסקופיה במטופלת אחת, זיהה את האתר הראשוני של סרטן השחלה ב-4 מטופלות, או בחצוצרה במטופלת אחת. ב-4 מטופלות עם אדנו-קרצינומה ראשונית בפריטונאום, הגידול זוהה בעזרת CT, במהלך חסימה של ה-cecum ובהמשך על ידי שימוש לפרטומיה במטופלת אחת, או על ידי שימוש בציטולגיה של נוזל המיימת בחלל הבטן במטופלת אחת. ב-40 מתוך 83 המטופלות (48%), המפגע הנוירולוגי הקדים את אבחון הסרטן. זיהוי של PCA-1 IgG הקדים את אבחון של סרטן ב-37 מטופלות (45%). | ||
| + | |||
| + | ==אנומליות אחרות ב-CSF== | ||
| + | אנומליות אחרות ב-CSF: | ||
| + | |||
| + | דגימות CSF של 50 מטופלות נבדקו, ואנומליות נמצאו ב-38 מתוך 50 מטופלות (76%) (ראו טבלה):. | ||
| + | |||
| + | [[קובץ:Purkinje 4.png|מרכז|600px]] | ||
| + | |||
| + | ==טיפול ותוצאים== | ||
| + | מידע בדבר טיפול ותוצאים היה זמין עבור 67 מטופלים (Vernino וחב' ב-Neuro Oncol משנת 2012). הרופאים המטפלים דיווחו על יציבות נוירולוגית או אף על שיפור מתון ב-10 מתוך 67 המטופלים (15%): חמישה מטופלים קיבלו כימותרפיה ואימונותרפיה: שלושה מטופלים טופלו עם cyclophosphamide, שלושה מטופלים עברו שחלוף פלזמה, שלושה מטופלים טופלו עם קורטיקו-סטרואידים, ומטופל אחד קיבל עירוי של אימונו-גלובולין. שיפורים נוירולוגיים לאחר כימותרפיה או אימונו-תרפיה היו מתונים וברי-חלוף ב-14 מטופלי אחרים (17%). טיפולים נוירולוגיים לא היו במתאם משמעותי עם משל התסמינים לפני הטיפול או עם סוג הסרטן. מוות דווח ב-40 מטופלים עם הישרדות ממוצעת של 24 חודשים מרגע התחלת התסמינים הנוירולוגיים; שלושה מתוך 67 המטופלים (9%) שרדו לפחות 5 שנים. מידע באשר סיבת המוות היה זמין עבור 11 מהמטופלים: כשל נשימתי מתוך סיבוך של מפגעים נוירולוגיים פארא-נאופלסטיים (7 מטופלים), סרטן גרורתי (3 מטופלים) ושבץ איסכמי (מטופל אחד). | ||
| + | |||
| + | ==הוראות לביצוע הבדיקה== | ||
| + | את הדם יש להעביר למבחנה כימית (פקק אדום או צהוב), ולאחר סרכוז יש להעביר את הנסיוב למבחנת פלסטיק לצורך העברה למעבדה. יציבות הדגימה כאשר היא מועברת בקירור (מועדף) היא 28 יום, כדגימה מוקפאת - 28 מיום, ובטמפרטורת החדר - 72 שעות. הבדיקה מתבצעת בשיטת IFA (או Indirect Immunofluorescence Assay). | ||
גרסה מ־09:47, 13 במרץ 2026
| מדריך בדיקות מעבדה | |
| אוטו-נוגדן ציטופלזמי כנגד תאי 1 Purkinje type | |
|---|---|
| Cytoplasmic autoantibody against purkinje type 1 cells | |
| שמות אחרים | Anti Yo, PCA-1. |
| 250px | |
Drawing of Purkinje cells (A) and granule cells (B) from pigeon cerebellum by Santiago Ramón y Cajal, 1899. Instituto Santiago Ramón y Cajal, Madrid, Spain.
| |
| מעבדה | אימונולוגיה בדם |
| תחום | מפגעים במוחון. |
| טווח ערכים תקין | פחות מ-1:240. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
זיהוי מטופלות בהן ניוון תת-חריף של המוחון, או נוירופתיה היקפית נגרמת מהשפעה אוטו-אימונית של קרצינומה גינקולוגית או מקרצינומה של השד.
כללי
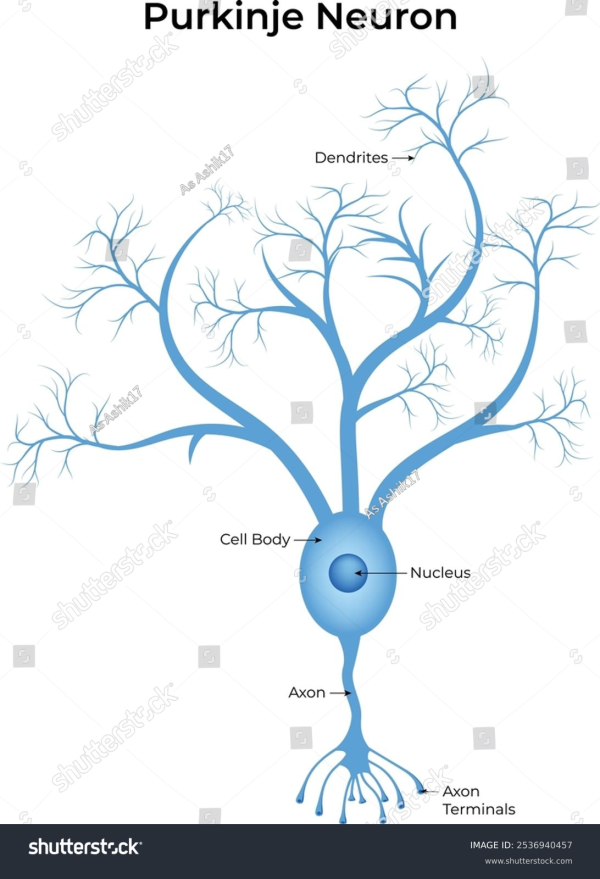
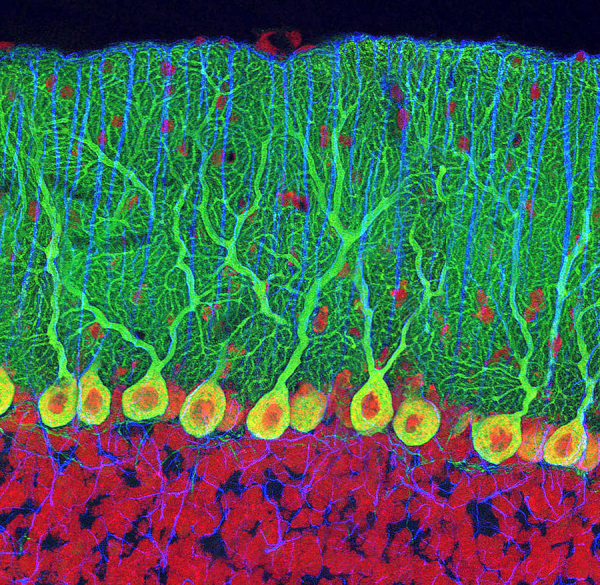
תא פורקינייה, הוא תא עצב (נוירון) גדול עם הסתעפויות רבות הבולטות ממנו הנמצא בקורטקס של המוחון במוח, ומשחק תפקיד משמעותי בבקרה של התנועה מוטורית. תאים אלה התגלו לראשונה בשנת 1837 על ידי הפיזיולוג הצ'כי יאן אוונגליסטה פורקינייה (Jan Evangelista Purkinje). תאי Purkinje מאופייינים על ידי גופי תא שצורתם כבַּקְבּוּקוֹן, על ידי מספר דנדריטים מסועפים, ועל ידי אקסון ארוך בודד. רוב תאי Purkinje מפרישים את הנוירוטרנסמיטר GABA (להלן gamma-aminobutyric acid), שהוא בעל פעולה מעכבת על נוירונים מסוימים, ולכן מפחית את ההעברה של איתותים עצביים. פעילויות מעכבות אלו מאפשרים לתאי Purkinje לווסת ולשמש קואורדינטורים של תנועות מוטוריות. הקורטקס של המוחון מורכב משלוש שכבות: שכבה חיצונית סינפטית (הידועה גם כשכבה המולקולרית), שכבת ביניים (הידועה גם כשכבת Purkinje) ושכבה פנימית גרנולרית. קלט סנסורי מכל מיני קולטנים, מועבר לאזורים ספציפיים של השכבה הרצפטיבית, המורכבת ממספרים גדולים של נוירונים קטנים (ומכאן הביטוי גרנולרי) "היורים" אקסונים לתוך השכנה הסינפטית. שם האקסונים מגרים דנדריטים של תאי Purkinje, שבתגובה "יורים" אקסונים לחלקים של ארבעת הגרעינים האינטרינזיים היוצרים את הגרעין הוסטיבולרי בתוך החדר הרביעי של גזע המוח. כיוון שרוב תאי Purkinje הם GABAergic ולפיכך משרים השפעות מעכבות חזקות על תאים המקבלים את קצות תאי Purkinje, כל ההשפעה הסנסורית במוחון גורמת לאימפולסים מעכבים בגרעינים העמוקים במוחון ובחלקים של הגרעין הוסטיבולרי. האובדן או הנזק לתאי Purkinje עלול לגרום למספר מחלות נוירולוגיות. במהלך הגדילה האמבריונית, תאי Purkinje עלולים להיות מושמדים באופן קבוע על ידי חשיפה לאלכוהול, מה שתורם להתפתחות של fetal alcohol syndrome. האובדן של תאי Purkinje נראה בילדים עם אוטיזם, ובמבוגרים עם מחלת Niemann-Pick type C, שהיא מפגע מטבולי העובר בהורשה.
התבטאות נוירולוגית ראשונית
המצג הנוירולוגי היה תת-חריף בכל המטופלות, ורב-מקומי ב-50 מתוכן (60%). אטקסיה של המוחון היוותה מצג דומיננטי ב-64 מטופלות (77%). תשע-עשרה (3%) מטופלות היו בעלות מצג של אחד או יותר מהמפגעים הבאים: מפגע של גזע המוח (פגיעה בתנועת העיניים ב-5 מתוכן, hyperacusis (שהיא רגישות יתר לרעשים חיצוניים או חוסר סבילות לרעש, הקיימת אצל כ- 10% מהאנשים). חלק גדול מהם סובלים גם מציפצופים באוזניים (טינטון), במטופלת אחת, ורטיגו במטופלת אחת, דעיכה קוגניטיבית מתונה במטופלת אחת, מיאללופתיה ב-4 מטופלות, הקאות בלתי נשלטות במטופלת אחת, נוירופתיה היקפית ב-8 מטופלות, pseudobulbar palsy במטופלת אחת, ונוירופתיה טריגמינלית דו-צדדית במטופלת אחת. במהלך חציוני של חודשיים, 19 מטופלות (53%) הראו סימני אטקסיה של המוחון.
ספקטרום של מצגים נוירולוגיים
מפגעים של ה-CNS: אטקסיה של המוחון התפתחה ב-74 מטופלות (89%) שהייתה הבעייה הפוגעת ביותר. עשרים וחמש מטופלות (30%) הראו סימנים של אי-תפקוד של המסלול הקורטיקו-ספינלי: שלוש עשרה מתוכן היו בעלות סימן Babinski, בעשר מתוכן נמצאה דיסארטריה (הפרעת דיבור הנגרמת כתוצאה מפגיעה בשרירים האחראים להפקת דיבור. ההפרעה מתבטאת בקושי בשליטה על השרירים של הפה, הלשון, הגרון או מיתרי הקול) אטקסית-ספסטית. ב-11 מטופלות (13%) נרשמו אנומליות של גזע המוח שכללו supranuclear gaze palsy (ב-2 מטופלות), שיתוק חד צדדי של העצב השישי (ב-2 מטופלות), שיתוק דו-צדדי של העצב השישי (ב-2 מטופלות), שיתוקים של העצב הרביעי ושל העצב השביעי הדו-צדדי במטופלת אחת, נוירופתיות טריגמינליות דו-צדדיות במטופלת אחת, ocular bobbing (שהיא סוג של תנועת עיניים לא נורמלית בה יש עֲווִית פתאומית כלפי מטה של העיניים) במטופלת אחת, וצניחת עפעפיים חד-צדדית במטופלת אחת. ממצאים נוירולוגיים נוספים כללו פגיעה קוגניטיבית או שינוי בהתנהגות נמצאו ב-4 מטופלות (5%), רעד במהלך מנוחה בשתי מטופלות (2%) ודיסטוניה (התכווצות ספונטנית של שרירי כפות הידיים ושורשי כפות הידיים, באופן שעושה את התנועות לבלתי אפשריות כמעט) ב-2 מטופלות (2%).
נוירופתיה היקפית
ב-8 מטופלות (10%) נרשמה נוירופתיה היקפית סומטית, או נוירופתיה מוטורית נמוכה המיוחסת לסיבות חלופיות. ממצאים אלה נמצאו בהתאמה עם תסמיני מוחון ב-4 מטופלות, והיו ההתבטאויות האקסקלוסיביות בשתי מטופלות. המצג הקליני היה חולשה, ורדימות של קצות הגפיים העליות והתחתונות (ב-2 מטופלות), חולשה ואובדן סנסורי בקצות הגפיים העליונות (ב-2 מטופלות), חולשה פרוגרסיבית של קצות הגפיים העליונות והתחתונות ונימול ברגליים במטופלת אחת, ואובדן סנסורי דו-צדדי בקצות הידיים והפנים במטופלת אחת.
דיסאוטונומיה
דיסאוטונומיה מקומית (שהיא אי-מוטיליות של המעי) דווחה בשתי מטופלות: אחת עם פסבדו-חסימה של המעי הדק, והשניה עם גסטרופרזיס שהיא התרוקנות קיבה איטית או שיתוק קיבה, מדובר במצב רפואי שבו יש שיתוק מוטורי חלקי או מלא של הקיבה. במצב זה המזון נותר בקיבה לזמן רב מעל הנורמה. אצל אנשים רגילים, הקיבה מתכווצת על מנת להעביר את המזון להמשך תהליך העיכול במעי הדק, והעצב התועה אחראי על התכווצויות אלו. גסטרופרזיס מתרחש כאשר העצב התועה נהרס או נפגע ושרירי הקיבה אינם מתפקדים כראוי. במקרה זה, המזון נע לאט במערכת העיכול, אם בכלל. בשתי המטופלות נמצאה גם אטקסיה של המוחון.
הדמייה של ה-neuraxis
ה-neuraxis הוא הציר של ה-CNS. הוא משתרע מהמוח דרך עמוד השדרה וקובע את הציר עושה דרכו של ה-CNS באורגניזמים מתפתחים ובוגרים. האנומליות הבאות אובחנו ב-35 מתוך 75 המטופלות (47%) בהן נוירו-הדמיות של המוח היו זמינות: אטרופיה מבודדת של המוחון נמצאה ב-25 מטופלות, אטרופיה כללית מוחית ומוחונית נמצאה ב-7 מטופלות, אטרופיה בגשר המוח נמצאה במטופלת אחת, אנומליות דיפוזיות של העברת סיגנלים בגזע המוח נמצאו במטופלת אחת, והגברה של העצב הטריגמינלי נמצאה במטופלת אחת. MRI של חוט השדרה גילתה סיגנלים דיפוזיים אנומליים התגלתה במטופלת אחת.
ממצאים מבדיקות אימונו-פלואורסצנטיות ובדיקות תספיג חלבון
Purkinje cell cytoplasmic autoantibody type 1 IgG התגלה בדגימות נסיוב של 81 מטופלות (98%) ובדגימות CSF של 18 מטופלות (22%); מבין 18 המטופלות שה-CSF שלהן נמצא חיובי ל-PCA-1 IgG, שתיים מתוכן (11%) היו בעלות דגימות נסיוב שנמצאו שליליות ל-PCA-1 IgG. החיוביות של purkinje cell cytoplasmic autoantibody type 1, אושרה בכל המקרים תוך שימוש בתספיג חלבון (Western blot) עם אנטיגן מסיס במים שעבר מיצוי מקליפת המוחון של חולדה בוגרת (Yu וחב' ב-Ann Neurol משנת 2001). כאשר הנסיוב וה-CSF נמצאו חיוביים ל-PCA-1 IgG, הטיטרים של הנסיוב נעו בין 480 ל-983,040 (עם חציון של 15,360, כאשר הטווח הנורמלי נמוך מ-120), ואילו הטיטרים ב-CSF נעו בין 128 ל-32,768 (עם חציון של 512). הטיטר בנסיוב ניבא במתינות את הטיטר ב-CSF של מטופלות אלו (R2 = 0.466). כל דגימות הנסיוב קיימו את הקריטריונים האימונו-היסטוכימיים של PCA-1 IgG, והיו גם קשורים לאלמנטים הציטופלזמטיים בנוירונים של ההיפוקמפוס, בנוירונים של חוט השדרה, בגנגליון של השורש הדורסלי, ובתאי Schwan בעצב ההיקפי.
ממצאים נוירופתולוגיים
הרקמות הנוירליות של שתי מטופלות שעברו אוטופסיה, עברו הערכה היסטופתולוגית. כאשר שתי מטופלות אללו היו בחיים, בשתיהן נמצאו סימנים קליניים של פגיעה במוחון ובמסלול הפירמידלי. המוחון, גזע המוח חוט השדרה והגנגליונים בשורש הדורסלי, הראו דלקת פרי-וסקולרית מפושטת, שפעול של המיקרוגליה, קשרירים במיקרוגליה, אובדן נוירונלי מפוזר וגליוזיס. אימונו-פנו-טייפינג של לימפוציטים גילה פרה-דומיננטיות של תאי CD8+ T פרי-וסקולריים ופרנכימליים. התוצאות של בחינה מיקרוסקופית של ההמיספרות המוחיות היו נורמליות בשתי המטופלות האמורות. פרק הזמן הופעת התסמינים ועד לביצוע האוטופסיה היה 17 חודשים לאחת מהן, ו-4 חודשים לשנייה.
קישורים נוירולוגיים
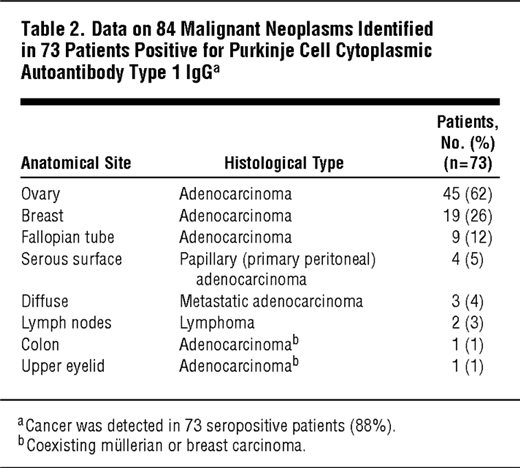
סרטן התגלה ב-73 מטופלות (88%) עם סרטן שד או סרטן müllerian ב-69 מתוך 73 המטופלים (95%). ב-67 מתוך 73 המטופלים (92%), הסרטן היה מוגבל לאתר אנטומי יחיד, וב-6 מתוך 73 המטופלים (8%) הסרטן היה מפושט מקומית או גרורתי. במטופלת אחת אובחנה קרצינומה של השחלה. שתי מטופלות אובחנו עם גידולים חדשים רבים (קרצינומות של השחלה או של החצוצרות באחת מהן, ובשנייה התגלו סרטן השד או של הפריטונאום. בשלוש מתוך ארבע מטופלות בהן הסרטן החדש שהתגלה לא היה סרטן ה- müllerian או קרצינומה של השד, נמצאו גרורות של אדנו-קרצינומה ממקור לא ידוע, ו-4 מטופלות אובחנו על לימפומה.
כאשר גידול סרטני ראשוני או גרורתי לא זוהה בתחילה על ידי הדמייה שגרתית אולטרה-סונוגרפיה או על ידי CT, גילוי ישיר על ידי לפרטומיה ב-4 מטופלות, או על ידי לפרוסקופיה במטופלת אחת, זיהה את האתר הראשוני של סרטן השחלה ב-4 מטופלות, או בחצוצרה במטופלת אחת. ב-4 מטופלות עם אדנו-קרצינומה ראשונית בפריטונאום, הגידול זוהה בעזרת CT, במהלך חסימה של ה-cecum ובהמשך על ידי שימוש לפרטומיה במטופלת אחת, או על ידי שימוש בציטולגיה של נוזל המיימת בחלל הבטן במטופלת אחת. ב-40 מתוך 83 המטופלות (48%), המפגע הנוירולוגי הקדים את אבחון הסרטן. זיהוי של PCA-1 IgG הקדים את אבחון של סרטן ב-37 מטופלות (45%).
אנומליות אחרות ב-CSF
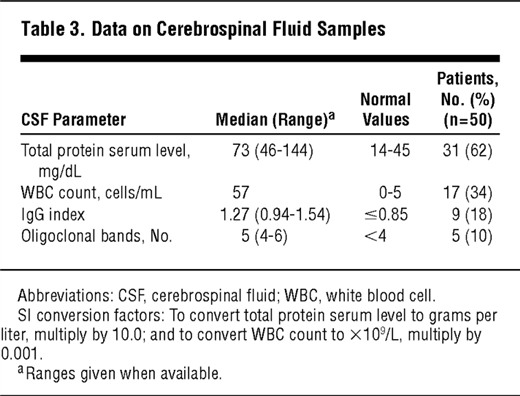
אנומליות אחרות ב-CSF:
דגימות CSF של 50 מטופלות נבדקו, ואנומליות נמצאו ב-38 מתוך 50 מטופלות (76%) (ראו טבלה):.
טיפול ותוצאים
מידע בדבר טיפול ותוצאים היה זמין עבור 67 מטופלים (Vernino וחב' ב-Neuro Oncol משנת 2012). הרופאים המטפלים דיווחו על יציבות נוירולוגית או אף על שיפור מתון ב-10 מתוך 67 המטופלים (15%): חמישה מטופלים קיבלו כימותרפיה ואימונותרפיה: שלושה מטופלים טופלו עם cyclophosphamide, שלושה מטופלים עברו שחלוף פלזמה, שלושה מטופלים טופלו עם קורטיקו-סטרואידים, ומטופל אחד קיבל עירוי של אימונו-גלובולין. שיפורים נוירולוגיים לאחר כימותרפיה או אימונו-תרפיה היו מתונים וברי-חלוף ב-14 מטופלי אחרים (17%). טיפולים נוירולוגיים לא היו במתאם משמעותי עם משל התסמינים לפני הטיפול או עם סוג הסרטן. מוות דווח ב-40 מטופלים עם הישרדות ממוצעת של 24 חודשים מרגע התחלת התסמינים הנוירולוגיים; שלושה מתוך 67 המטופלים (9%) שרדו לפחות 5 שנים. מידע באשר סיבת המוות היה זמין עבור 11 מהמטופלים: כשל נשימתי מתוך סיבוך של מפגעים נוירולוגיים פארא-נאופלסטיים (7 מטופלים), סרטן גרורתי (3 מטופלים) ושבץ איסכמי (מטופל אחד).
הוראות לביצוע הבדיקה
את הדם יש להעביר למבחנה כימית (פקק אדום או צהוב), ולאחר סרכוז יש להעביר את הנסיוב למבחנת פלסטיק לצורך העברה למעבדה. יציבות הדגימה כאשר היא מועברת בקירור (מועדף) היא 28 יום, כדגימה מוקפאת - 28 מיום, ובטמפרטורת החדר - 72 שעות. הבדיקה מתבצעת בשיטת IFA (או Indirect Immunofluorescence Assay).


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק