הבדלים בין גרסאות בדף "סכיזופרניה - טיפול בתכשירים המשפיעים על הקולטנים המטבוטרופיים לגלוטמט - Schizophrenia - treatment with drugs affecting metabotropic glutamate receptors"
| שורה 13: | שורה 13: | ||
|אחראי הערך= | |אחראי הערך= | ||
}} | }} | ||
| − | גלוטמט הוא | + | גלוטמט (Glutamate) הוא המוליך העצבי (Neurotransmitter) המעורר הנפוץ במערכת העצבים המרכזית. מקובל כיום לחשוב, כי חלק מהתהליך הנוירופתולוגי (Neuropathology) ב[[סכיזופרניה]], קשור בהפרעה במערכת הגלוטמט, בעיקר בתיווך הקולטן ל- NMDA {{כ}}(N-Methyl-D-aspartate). זאת בעקבות המידע על הופעת תופעות פסיכוטומימטיות (Psychotomimetic), לאחר חסימת הקולטן באמצעות תכשירים, כגון [[Sernyl]]{{כ}} (Phencyclidine){{כ}},[[Dizocilpine]] {{כ}}(MK801) או [[Ketamine]]. על כן, התאוריה המקובלת כיום גורסת, כי יש אפשרות של ירידה בפעילות הגלוטמט במוח בחולי סכיזופרניה {{הערה|שם=הערה1| Farber NB. The NMDA receptor hypofunction model of psychosis. Ann NY Acad Sci 2003;1003:119-130}}, לנוכח זאת פותחו תכניות טיפוליות המיועדות לשפעל את הקולטן ל-NMDA, כגון מתן המסייע-שותף (Co-agonist) לקולטן, [[גליצין]] (Glycine) או [[די-סרין]] (D-Serine) {{כ}}{{הערה|שם=הערה2| Heresco-Levy U, Ermilov M, Shimoni J, et al. Placebo-controlled trial of D-cycloserine added to conventional neuroleptics, olanzapine, or risperidone in schizophrenia. Am J Psychiatry 2002;159:480-482}}. ברם, מכיוון שמחלת הסכיזופרניה מתבטאת במספר מישורים, מעבר לממד הפסיכוטי, כגון: סימנים שליליים וליקוי הכרתי (Cognitive), נראה שהתמונה מורכבת יותר בכל הנוגע להשפעת גלוטמט. משפחת הקולטנים לגלוטמט {{הערה|שם=הערה3| Kew JN, Kemp JA. Ionotropic and metabotropic glutamate receptor structure and pharmacology. Psychopharmacology (Berl) 2005;179:4-29}} כוללת קולטנים אינוטרופיים (Inotropic){{כ}} (NMDA, {{כ}}AMPA{{כ}} (Alpha-amino-3-hydroxy-5-Methyl-4-isoxazole-Propionic Acid), {{כ}}Kainate) המשפעלים תעלות יוניות על גבי קרום התא, ומובילים לכניסה או ליציאה של יונים. קולטנים אלה הם בתר-מצמד (Post synapse) ומבוטאים על ידי כל תאי העצב. קישור של גלוטמט לקולטנים אלה, מוביל לעירור עצבי מהיר בכל המוח. על כן, התערבות תרופתית בפעילות קולטנים אלו, עלולה להתבטא בהשפעה מוחית כללית ותופעות לוואי משמעותיות. קבוצה שנייה היא הקולטנים המטבוטרופיים (Metabotropic) לגלוטמט (mGluRs), כאלה שבהפעלתם, משופעלת תגובה תוך-תאית באמצעות שליח משני (Second messenger). עדויות הנוגעות למעורבות הקולטנים המטבוטרופיים לגלוטמט בסכיזופרניה, {{הערה|שם=הערה4| Krivoy A, Fischel T, Weizman A. The possible involvement of metabotropic glutamate receptors in schizophrenia. Eur Neuropsychopharmacol 2008;18:395-405}} או הפרעות פסיכיאטריות אחרות, מתחילות להצטבר ולהוביל לפיתוח תכשירים, לטיפול דרך הפעלה או חסימה של קולטנים אלה. |
== הקולטנים המטבוטרופיים לגלוטמט (קמ"ג)== | == הקולטנים המטבוטרופיים לגלוטמט (קמ"ג)== | ||
| − | קבוצה זו כוללת, נכון להיום, שמונה קולטנים (ציור 1) המקובצים בשלוש קבוצות: 1 ו-5 נקראים קבוצה I; 2 ו-3 מכונים קבוצה II; ו-4, 6, 7 ו-8 הם קבוצה III. כל קבוצה מאופיינת במבנה ראשוני שונה, שליח משני שונה ופרופיל פרמקולוגי ייחודי{{הערה|שם=הערה5|Conn PJ, Pin JP. Pharmacology and functions of metabotropic glutamate receptors. Annu Rev Pharmacol Toxicol 1997;37:205-237}}. כל הקולטנים שובטו והמיקומים של הגנים שלהם זוהו. השליח המשני מופעל בקבוצה I באמצעות חלבוני Go/G11 והפעלת פוספוליפאזה C. השליח המשני בקבוצות II ו-III מופעל באמצעות חלבוני Gi/Gq ומוביל לעיכוב האנזים Adenylyl Cycalse. ככלל, תפקידם של קולטנים אלה הוא יותר מודולטורי בפעילות החשמלית של מערכת העצבים, בפלסטיות עצבית ובהולכה עצבית. | + | קבוצה זו כוללת, נכון להיום, שמונה קולטנים (ציור 1) המקובצים בשלוש קבוצות: 1 ו-5 נקראים קבוצה I; 2 ו-3 מכונים קבוצה II; ו-4, 6, 7 ו-8 הם קבוצה III. כל קבוצה מאופיינת במבנה ראשוני שונה, שליח משני שונה ופרופיל פרמקולוגי ייחודי{{הערה|שם=הערה5|Conn PJ, Pin JP. Pharmacology and functions of metabotropic glutamate receptors. Annu Rev Pharmacol Toxicol 1997;37:205-237}}. כל הקולטנים שובטו והמיקומים של הגנים שלהם זוהו. השליח המשני מופעל בקבוצה I באמצעות חלבוני Go/G11 והפעלת פוספוליפאזה C. השליח המשני בקבוצות II ו-III מופעל באמצעות חלבוני Gi/Gq ומוביל לעיכוב האנזים Adenylyl Cycalse. ככלל, תפקידם של קולטנים אלה הוא יותר מודולטורי בפעילות החשמלית של מערכת העצבים, בפלסטיות עצבית ובהולכה עצבית. הקולטנים המטבוטרופיים לגלוטמט נמצאים כולם, למעט הקולטנים המטבוטרופיים לגלוטמט 6 שנמצא ברשתית בלבד, על תאי עצב וגליה בפיזור אופייני לכל קבוצה. קבוצה I נמצאת בד"כ בקצה פוסט-סינפטי באזורים סומטודנדריטיים ואילו הקולטנים המטבוטרופיים לגלוטמט מקבוצה II ו-III לרוב פרה-סינפטיים, בקצות אקסונים, שם הם מעורבים בהסדרת המוליכות העצבית. באשר למיקומם של הקולטנים המטבוטרופיים לגלוטמטבמוח: קבוצה I נפוצה יותר בהיפוקמפוס, אמיגדלה, תלמוס, סטריאטום ונטרלי, קורטקס פרה-פרונטלי (הקולטנים המטבוטרופיים לגלוטמט 1), נוקלאוס אקומבנס, טוברקל אולפקטורי (הקולטנים המטבוטרופיים לגלוטמט 5). קבוצה II נפוצה בעיקר בקורטקס ודנטט גירוס (הקולטנים המטבוטרופיים לגלוטמט 2), תלמוס, סטריאטום, אמיגדלה, היפוקמפוס ותאי גליה (הקולטנים המטבוטרופיים לגלוטמט 3). קבוצה III נפוצה בעיקר בתלמוס וברשתית (הקולטנים המטבוטרופיים לגלוטמט 6). Gupta וחבריו {{הערה|שם=הערה6|Gupta DS, McCullumsmith RE, Beneyto M, et al. Metabotropic gluta- mate receptor protein expression in the prefrontal cortex and striatum in schizophrenia. Synapse 2005;57:123-131}} מצאו כי בקורטקס הפרה-פרונטלי (אזורי ברודמן 9, 11, 32, 46) יש עלייה משמעותית בביטוי של הקולטנים המטבוטרופיים לגלוטמט 1, 2 ו-3, אך לא של 4 ו-5. |
[[קובץ: Schizophrenia06.jpg|center|]] | [[קובץ: Schizophrenia06.jpg|center|]] | ||
| − | ==מעורבות | + | ==מעורבות הקולטנים המטבוטרופיים לגלוטמט בהולכת גלוטמט (ציור 1)== |
| − | + | הקולטנים המטבוטרופיים לגלוטמט 1 ו-5 (קבוצה I) ממוקמים בקצה הפרה-סינפטי והפוסט-סינפטי. פעולתם המשוערת היא שפעול הקולטן ל-NMDA, אך יש להם גם השפעה על קולטני AMPA. הקולטנים המטבוטרופיים לגלוטמט 2 ו-3 (קבוצה II) ממוקמים בקצה הפרה-סינפטי והפעלתם מעכבת את שחרור הגלוטמט. ההיפותזה היא שתת-פעילות של קולטני ה-NMDA מובילה להפחתה בהפרשת GABA מתאי עצב. תאי עצב אלה נקשרים דרך סינפסה לתאים מפרישי גלוטמט. משערים שהקולטנים המטבוטרופיים לגלוטמט 2/3 ממוקמים בקצה הפרה-סינפטי של תאי עצב אלה, והפעלתם מפחיתה את שחרור הגלוטמט העודף הנוירוטוקסי. קבוצה III היא הפחות נחקרת מבין הקולטנים המטבוטרופיים לגלוטמט. הקולטנים המטבוטרופיים לגלוטמט 6 ממוקמים בעיקר ברשתית, כאמור, ולכן מעורבותם בסכיזופרניה היא מועטה. לקולטנים המטבוטרופיים לגלוטמט 7 יש רגישות מעטה מאוד לגלוטמט ולאגוניסטים נוספים. | |
| − | ==מחקרים בתכשירים המשפיעים על | + | ==מחקרים בתכשירים המשפיעים על הקולטנים המטבוטרופיים לגלוטמט== |
| − | רוב המידע הקיים כיום על קולטנים אלו מגיע מניסויים בבעלי חיים. שיטות המחקר כוללות עכברים טרנס-גניים שעברו הסרה של גנים | + | רוב המידע הקיים כיום על קולטנים אלו מגיע מניסויים בבעלי חיים. שיטות המחקר כוללות עכברים טרנס-גניים שעברו הסרה של גנים לקולטנים המטבוטרופיים לגלוטמט השונים, מחקרים גנטיים שבהם נבדקת שכיחות אללים מועמדים (של גנים לקולטנים המטבוטרופיים לגלוטמט) באוכלוסייה רגילה לעומת חולי סכיזופרניה ופרדיגמות התנהגותיות המדמות רכיבים שונים של סכיזופרניה בכלל ובעיקר את המצב הפסיכוטי. "עיכוב של קדם פולס" IPP {{כ}} (Pre-Pulse Inhibition) משמעו בחינה של התגובה לטון לאחר שמיעה קודמת של אותו טון. חיה לקויה (וגם חולי סכיזופרניה) תגיב בצורה שונה לעומת חיה תקינה. במודל השני נבדקת התנועתיות של החולדה (Locomotion) שנמצאה מוגברת בדומה לחולי סכיזופרניה. במודל השלישי נבחנות תנועות סטראוטיפיות המאפיינות מצב פסיכוטי, המתבטאות בחולדה בהתנהגויות, כגון: תנועה מעגלית אופיינית ותנועות ראש. ניתן להשרות ליקוי כזה באמצעות תכשירים מעכבי NMDA, כגון: קטמין, PCP או MK801, ולבדוק את השפעתם של תכשירים שונים המשפיעים על הקולטנים המטבוטרופיים לגלוטמט. תכשירים אלו מוגדרים כאורטוסטריים אם אתר הקישור שלהם הוא ישירות באתר הפעיל של הליגנד או אלוסטריים אם אתר הקישור שלהם מרוחק מהאתר הפעיל, אך בכל זאת משפיע עליו. לתכשירים אלוסטריים יתרון בכך שהשפעתם מתונה יותר וכן מובילים להרבה פחות ויסות כלפי מעלה או מטה של הקולטנים. למרבית הקולטנים המטבוטרופיים לגלוטמט סונתזו תכשירים מעכבים או משפעלים. |
==תוצאות מחקרים בבעלי חיים== | ==תוצאות מחקרים בבעלי חיים== | ||
| − | === | + | === הקולטנים המטבוטרופיים לגלוטמט 1=== |
| − | משערים כי | + | משערים כי לקולטנים המטבוטרופיים לגלוטמט 1 יש תפקיד בשפעול הקולטן ל-NMDA. בעכברים ללא הגן לקולטנים המטבוטרופיים לגלוטמט 1 נראתה הפרעה בתפיסה החושית, כפי שהתבטאה ב-PPI לא תקין, תוצאה שלא הוחמרה בתוספת PCP{{כ}}{{הערה|שם=הערה7| Brody SA, Conquet F, Geyer MA. Disruption of prepulse inhibition in mice lackingmGluR1. Eur J Neurosci 2003;18:3361-3366}}. על אף זאת, מתן תכשירים אנטגוניסטיים לקולטנים המטבוטרופיים לגלוטמט 1 לא הובילו לתמונה דומה ב-PPI, גם לא לתיקון PPI לקוי בחיות שקיבלו לפני כן PCP או MK801{{כ}}{{הערה|שם=הערה8| De VJ, Horvath E, Schreiber R. Neuroprotective and behavioral effects of the selective metabotropic glutamate mGlu (1) receptor antagonist BAY 36-7620. Eur J Pharmacol 2001;428:203-214}}. מעכב הקולטנים המטבוטרופיים לגלוטמט 1 הוביל לשיפור בתנועות הסטראוטיפיות בחיות שטופלו לפני כן ב-MK801. בבחינת ההשפעה של מעכבי הקולטנים המטבוטרופיים לגלוטמט 1 על התנועתיות נראתה אפילו השפעה ממתנת בחיות לקויות. |
| − | === | + | ===הקולטנים המטבוטרופיים לגלוטמט 5=== |
| − | בעכברים ללא הגן | + | בעכברים ללא הגן לקולטנים המטבוטרופיים לגלוטמט 5 נראתה תגובה לקויה ב-PPI{{כ}}{{הערה|שם=הערה9| Kinney GG, Burno M, Campbell UC, et al. Metabotropic glutamate subtype 5 receptors modulate locomotor activity and sensorimotor gating in rodents. J Pharmacol Exp Ther 2003;306:116-123}}. משערים שפעילות הקולטנים המטבוטרופיים לגלוטמט 5 משפעלת את הקולטן ל-NMDA, בעיקר באזורי מוח הקשורים לסכיזופרניה. מעכבי הקולטנים המטבוטרופיים לגלוטמט אינם מובילים להפרעה בתנועתיות או להופעת תנועות סטראוטיפיות. מתן מעכב הקולטנים המטבוטרופיים לגלוטמט 5 הוביל להגברה בהפרעה ב-PPI לאחר מתן PCP, כמו גם להחמרה בשאר במדדים כגון תנועתיות וסטראוטיפיות. על כן,משערים כי אגוניסט לקולטנים המטבוטרופיים לגלוטמט 5 עשוי להיות בעל סגולות אנטיפסיכוטיות בחולדות. ואכן, מחקרים ראשונים מראים כי תכשיר משפעל הקולטנים המטבוטרופיים לגלוטמט 5 הוביל לשיפור בתנועתיות וב-PPI בחולדות שטופלו לפני כן באמפטמינים, השיפור שהתקבל היה בצורה תלוית מינון {{הערה|שם=הערה10| Kinney GG, O'Brien JA, Lemaire W, et al. A novel selective positive allosteric modulator of metabotropic glutamate receptor subtype 5 has in vivo activity and antipsychotic-like effects in rat behavioral models. J Pharmacol Exp Ther 2005;313:199-206}}. |
| − | ===אגוניסטים לקבוצה II ( | + | ===אגוניסטים לקבוצה II (הקולטנים המטבוטרופיים לגלוטמט 2/3)=== |
משערים כי קולטנים אלה, הממוקמים בקצה הקדם-סינפטי, מעכבים שחרור גלוטמט מקצה העצב לסינפסה ובכך משתתפים בבקרה על כמות הגלוטמט הסינפטית{{הערה|שם=הערה11| Schoepp DD, Jane DE, Monn JA. Pharmacological agents acting at subtypes of metabotropic glutamate receptors. Neuropharmacology 1999;38:1431-1476}}. תאי העצב המבטאים את הקולטנים הללו הם GABA Interneurons, כלומר תאים מתווכים, שבהפעלתם (בקישור לקולטן ל-GABA) יש ירידה בהפרשת גלוטמט בסינפסה. מחקרי חיות הראו השפעה מהפכת של מתן תכשירים אגוניסטים אורטוסטריים לקבוצה II על ליקוי כתוצאה ממתן PCP או אמפטמינים. נוסף על כך, נראתה ירידה בשחרור גלוטמט בקורטקס הקדם-פרונטלי וכן שיפור בזיכרון עבודה. | משערים כי קולטנים אלה, הממוקמים בקצה הקדם-סינפטי, מעכבים שחרור גלוטמט מקצה העצב לסינפסה ובכך משתתפים בבקרה על כמות הגלוטמט הסינפטית{{הערה|שם=הערה11| Schoepp DD, Jane DE, Monn JA. Pharmacological agents acting at subtypes of metabotropic glutamate receptors. Neuropharmacology 1999;38:1431-1476}}. תאי העצב המבטאים את הקולטנים הללו הם GABA Interneurons, כלומר תאים מתווכים, שבהפעלתם (בקישור לקולטן ל-GABA) יש ירידה בהפרשת גלוטמט בסינפסה. מחקרי חיות הראו השפעה מהפכת של מתן תכשירים אגוניסטים אורטוסטריים לקבוצה II על ליקוי כתוצאה ממתן PCP או אמפטמינים. נוסף על כך, נראתה ירידה בשחרור גלוטמט בקורטקס הקדם-פרונטלי וכן שיפור בזיכרון עבודה. | ||
| − | === | + | ===הקולטנים המטבוטרופיים לגלוטמט 2=== |
| − | נראה כי לאגוניסטים של | + | נראה כי לאגוניסטים של הקולטנים המטבוטרופיים לגלוטמט 2 יש השפעה דומה כמו לאגוניסטים של הקולטנים המטבוטרופיים לגלוטמט 2/3, דבר שמוביל להשערה כי עיקר השפעתם של האחרונים היא דרך הקולטנים המטבוטרופיים לגלוטמט 2. התכשיר LY487379 בעל השפעה אלוסטרית חיובית על הקולטנים המטבוטרופיים לגלוטמט 2 באופן ספציפי. לתכשיר יכולת לשפר הפרעה בתנועתיות בעכברים שטופלו |
| − | ב-PCP ואמפטמינים לפני כן, אך במידה פחותה מאגוניסטים | + | ב-PCP ואמפטמינים לפני כן, אך במידה פחותה מאגוניסטים לקולטנים המטבוטרופיים לגלוטמט 2/3 {{הערה|שם=הערה12| Johnson MP, Barda D, Britton TC, et al. Metabotropic glutamate 2 receptor potentiators: receptor modulation, frequency-dependent synaptic activity, and efficacy in preclinical anxiety and psychosis model(s). Psychopharmacology (Berl) 2005;179:271-283}}. עם זאת, לתכשיר זמן פעילות קצר דבר שלא מאפשר מחקר יישומי איתו. תכשיר חדש, BINA - אגוניסט לקולטנים המטבוטרופיים לגלוטמט 2 {{כ}}{{הערה|שם=הערה13| Galici R, Jones CK, Hemstapat K, et al. Biphenyl-indanone A, a positive allosteric modulator of the metabotropic glutamate receptor subtype 2, has antipsychotic- and anxiolytic-like effects in mice. J Pharmacol Exp Ther 2006;318:173-185}}, הראה שיפור בתנועתיות וב-PPI בחיות שטופלו ב-PCP, אך לא באמפטמינים. לתכשיר זה אף נצפה זמן פעולה ארוך של עד 8 שעות. |
| − | === | + | ===הקולטנים המטבוטרופיים לגלוטמט 3=== |
| − | לא סונתזו תכשירים המשפיעים על | + | לא סונתזו תכשירים המשפיעים על הקולטנים המטבוטרופיים לגלוטמט זה. אולם, יש בגוף ליגנד טבעי לקולטן: NAAG {{כ}} (N-Acetyl-Aspartate-Glutamate). החומר הוא אגוניסט/אנטגוניסט חלקי, כלומר, בריכוז נמוך הוא מעכב את הקולטן ל-NMDA ובריכוזים גבוהים מפעיל את הקולטן ל-NMDA. נוסף על כך, החומר מעכב אוטו-קולטנים מסוג הקולטנים המטבוטרופיים לגלוטמט 3 האחראים על שחרור גלוטמט מהסינפסה. בהתאם, הוצעה תאוריה לסכיזופרניה {{הערה|שם=הערה14| Tsai SJ. Central N-acetyl aspartylglutamate deficit: a possible pathogenesis of schizophrenia. Med Sci Monit 2005;11:39-45}} שבה מעורבת רמה נמוכה של NAAG, המובילה לעודף בהפרשת גלוטמט עקב ההשפעה על האוטוקולטנים. Olszewki וחבריו {{הערה|שם=הערה15| Olszewski RT, Bukhari N, Zhou J, et al. NAAG peptidase inhibition reduces locomotor activity and some stereotypes in the PCP model of schizophrenia via group II mGluR. J Neurochem 2004;89:876-885}} דיווחו על תכשיר שכונה ZJ43, מעכב חזק של האנזים Glutamate Carboxypeptidase II & III. אנזים האחראי על ניטרול NAAG לאחר שחרורו לסינפסה. התכשיר ZJ43 אינו מגיב ישירות עם הקולטן ל-NMDA או עם הקולטנים המטבוטרופיים לגלוטמט. ואכן, מתן התכשיר, שיפר הפרעה בתנועתיות בחולדה שקיבלה PCP. |
| − | == מחקרי אנוש בתכשירים אגוניסטיים | + | == מחקרי אנוש בתכשירים אגוניסטיים לקולטנים המטבוטרופיים לגלוטמט== |
| − | התכשיר LY354740 שהינו אגוניסט | + | התכשיר LY354740 שהינו אגוניסט לקולטנים המטבוטרופיים לגלוטמט 2/3 (לא מבדיל בין הקולטנים) נבדק בניסויי אנוש, כקדם-טיפול במתנדבים שנטלו [[קטמין]]. לא נמצאה השפעה של התכשיר על תסמיני הסכיזופרניה כפי שנבדו במבחן PANSS, עם זאת, כן נמצא שיפור מה בזיכרון עבודה {{הערה|שם=הערה16| Krystal JH, bi-Saab W, Perry E, et al. Preliminary evidence of attenuation of the disruptive effects of the NMDA glutamate receptor antagonist, ketamine, on working memory by pretreatment with the group II metabotropic glutamate receptor agonist, LY354740, in healthy human subjects. Psychopharmacology (Berl) 2005;179:303-309}}. לעומת זאת, Patyl וחבריו {{הערה|שם=הערה17| Patil ST, Zhang L, Martenyi F, et al. Activation of mGlu2/3 receptors as a new approach to treat schizophrenia: a randomized Phase 2 clinical trial. Nature Med 2007;13:1102-1107}} בדקו את התכשיר LY404039, גם הוא אגוניסט לקולטנים המטבוטרופיים לגלוטמט 2/3, כטיפול יחידי בחולי סכיזופרניה כרוניים. הם מצאו שיפור משמעותי בכל מדדי ה-PANSS לעומת אינבו. עוצמת השיפור הייתה דומה לזו שהתקבלה בקבוצה שטופלה באולנזפין. יתר על כן, התכשיר לא גרם לעלייה במשקל ורמת פרולקטין (בשונה מאולנזפין) או לתופעות לוואי אקסטרה-פירמידליות. |
==סיכום== | ==סיכום== | ||
| − | נראה כי לתכשירים המשפיעים על פעילות | + | נראה כי לתכשירים המשפיעים על פעילות הקולטנים המטבוטרופיים לגלוטמט יש תפקיד באפנון של הפעילות הגלוטמטרגית במוח. משמעותם הקלינית של תכשירים המשפיעים על ויסות הפרשת הגלוטמט עוד צריכה להתברר בניסויי אנוש רחבים המתוכננים עם תכשירים המשפיעים על הקולטנים המטבוטרופיים לגלוטמט בחולי סכיזופרניה. עם זאת, כבר כעת ניתן להניח כי השפעתם של קולטנים אלה עשויה להיות על כל קשת התסמינים בסכיזופרניה, ובכללם הממד הפסיכוטי, הסימנים השליליים והליקוי הקוגניטיבי. יש לצפות כי בעתיד נראה דיווחים על תכשירים המשפיעים על הקולטנים המטבוטרופיים לגלוטמט שנבחנו בניסויים קליניים בחולי סכיזופרניה. |
==דגלים אדומים== | ==דגלים אדומים== | ||
| שורה 75: | שורה 75: | ||
==קישורים חיצוניים== | ==קישורים חיצוניים== | ||
| − | * [http://www.medicalmedia.co.il/publications/ArticleDetails.aspx?artid=1948&sheetid=129 תכשירים המשפיעים על פעילות | + | * [http://www.medicalmedia.co.il/publications/ArticleDetails.aspx?artid=1948&sheetid=129 תכשירים המשפיעים על פעילות הקולטנים המטבוטרופיים לגלוטמט כטיפול בסכיזופרניה], מדיקל מדיה |
גרסה מ־16:32, 29 בינואר 2013
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
גלוטמט (Glutamate) הוא המוליך העצבי (Neurotransmitter) המעורר הנפוץ במערכת העצבים המרכזית. מקובל כיום לחשוב, כי חלק מהתהליך הנוירופתולוגי (Neuropathology) בסכיזופרניה, קשור בהפרעה במערכת הגלוטמט, בעיקר בתיווך הקולטן ל- NMDA (N-Methyl-D-aspartate). זאת בעקבות המידע על הופעת תופעות פסיכוטומימטיות (Psychotomimetic), לאחר חסימת הקולטן באמצעות תכשירים, כגון Sernyl (Phencyclidine),Dizocilpine (MK801) או Ketamine. על כן, התאוריה המקובלת כיום גורסת, כי יש אפשרות של ירידה בפעילות הגלוטמט במוח בחולי סכיזופרניה [1], לנוכח זאת פותחו תכניות טיפוליות המיועדות לשפעל את הקולטן ל-NMDA, כגון מתן המסייע-שותף (Co-agonist) לקולטן, גליצין (Glycine) או די-סרין (D-Serine) [2]. ברם, מכיוון שמחלת הסכיזופרניה מתבטאת במספר מישורים, מעבר לממד הפסיכוטי, כגון: סימנים שליליים וליקוי הכרתי (Cognitive), נראה שהתמונה מורכבת יותר בכל הנוגע להשפעת גלוטמט. משפחת הקולטנים לגלוטמט [3] כוללת קולטנים אינוטרופיים (Inotropic) (NMDA, AMPA (Alpha-amino-3-hydroxy-5-Methyl-4-isoxazole-Propionic Acid), Kainate) המשפעלים תעלות יוניות על גבי קרום התא, ומובילים לכניסה או ליציאה של יונים. קולטנים אלה הם בתר-מצמד (Post synapse) ומבוטאים על ידי כל תאי העצב. קישור של גלוטמט לקולטנים אלה, מוביל לעירור עצבי מהיר בכל המוח. על כן, התערבות תרופתית בפעילות קולטנים אלו, עלולה להתבטא בהשפעה מוחית כללית ותופעות לוואי משמעותיות. קבוצה שנייה היא הקולטנים המטבוטרופיים (Metabotropic) לגלוטמט (mGluRs), כאלה שבהפעלתם, משופעלת תגובה תוך-תאית באמצעות שליח משני (Second messenger). עדויות הנוגעות למעורבות הקולטנים המטבוטרופיים לגלוטמט בסכיזופרניה, [4] או הפרעות פסיכיאטריות אחרות, מתחילות להצטבר ולהוביל לפיתוח תכשירים, לטיפול דרך הפעלה או חסימה של קולטנים אלה.
הקולטנים המטבוטרופיים לגלוטמט (קמ"ג)
קבוצה זו כוללת, נכון להיום, שמונה קולטנים (ציור 1) המקובצים בשלוש קבוצות: 1 ו-5 נקראים קבוצה I; 2 ו-3 מכונים קבוצה II; ו-4, 6, 7 ו-8 הם קבוצה III. כל קבוצה מאופיינת במבנה ראשוני שונה, שליח משני שונה ופרופיל פרמקולוגי ייחודי[5]. כל הקולטנים שובטו והמיקומים של הגנים שלהם זוהו. השליח המשני מופעל בקבוצה I באמצעות חלבוני Go/G11 והפעלת פוספוליפאזה C. השליח המשני בקבוצות II ו-III מופעל באמצעות חלבוני Gi/Gq ומוביל לעיכוב האנזים Adenylyl Cycalse. ככלל, תפקידם של קולטנים אלה הוא יותר מודולטורי בפעילות החשמלית של מערכת העצבים, בפלסטיות עצבית ובהולכה עצבית. הקולטנים המטבוטרופיים לגלוטמט נמצאים כולם, למעט הקולטנים המטבוטרופיים לגלוטמט 6 שנמצא ברשתית בלבד, על תאי עצב וגליה בפיזור אופייני לכל קבוצה. קבוצה I נמצאת בד"כ בקצה פוסט-סינפטי באזורים סומטודנדריטיים ואילו הקולטנים המטבוטרופיים לגלוטמט מקבוצה II ו-III לרוב פרה-סינפטיים, בקצות אקסונים, שם הם מעורבים בהסדרת המוליכות העצבית. באשר למיקומם של הקולטנים המטבוטרופיים לגלוטמטבמוח: קבוצה I נפוצה יותר בהיפוקמפוס, אמיגדלה, תלמוס, סטריאטום ונטרלי, קורטקס פרה-פרונטלי (הקולטנים המטבוטרופיים לגלוטמט 1), נוקלאוס אקומבנס, טוברקל אולפקטורי (הקולטנים המטבוטרופיים לגלוטמט 5). קבוצה II נפוצה בעיקר בקורטקס ודנטט גירוס (הקולטנים המטבוטרופיים לגלוטמט 2), תלמוס, סטריאטום, אמיגדלה, היפוקמפוס ותאי גליה (הקולטנים המטבוטרופיים לגלוטמט 3). קבוצה III נפוצה בעיקר בתלמוס וברשתית (הקולטנים המטבוטרופיים לגלוטמט 6). Gupta וחבריו [6] מצאו כי בקורטקס הפרה-פרונטלי (אזורי ברודמן 9, 11, 32, 46) יש עלייה משמעותית בביטוי של הקולטנים המטבוטרופיים לגלוטמט 1, 2 ו-3, אך לא של 4 ו-5.
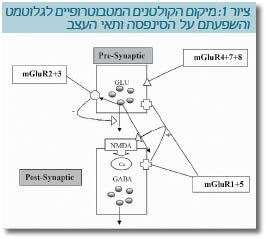
מעורבות הקולטנים המטבוטרופיים לגלוטמט בהולכת גלוטמט (ציור 1)
הקולטנים המטבוטרופיים לגלוטמט 1 ו-5 (קבוצה I) ממוקמים בקצה הפרה-סינפטי והפוסט-סינפטי. פעולתם המשוערת היא שפעול הקולטן ל-NMDA, אך יש להם גם השפעה על קולטני AMPA. הקולטנים המטבוטרופיים לגלוטמט 2 ו-3 (קבוצה II) ממוקמים בקצה הפרה-סינפטי והפעלתם מעכבת את שחרור הגלוטמט. ההיפותזה היא שתת-פעילות של קולטני ה-NMDA מובילה להפחתה בהפרשת GABA מתאי עצב. תאי עצב אלה נקשרים דרך סינפסה לתאים מפרישי גלוטמט. משערים שהקולטנים המטבוטרופיים לגלוטמט 2/3 ממוקמים בקצה הפרה-סינפטי של תאי עצב אלה, והפעלתם מפחיתה את שחרור הגלוטמט העודף הנוירוטוקסי. קבוצה III היא הפחות נחקרת מבין הקולטנים המטבוטרופיים לגלוטמט. הקולטנים המטבוטרופיים לגלוטמט 6 ממוקמים בעיקר ברשתית, כאמור, ולכן מעורבותם בסכיזופרניה היא מועטה. לקולטנים המטבוטרופיים לגלוטמט 7 יש רגישות מעטה מאוד לגלוטמט ולאגוניסטים נוספים.
מחקרים בתכשירים המשפיעים על הקולטנים המטבוטרופיים לגלוטמט
רוב המידע הקיים כיום על קולטנים אלו מגיע מניסויים בבעלי חיים. שיטות המחקר כוללות עכברים טרנס-גניים שעברו הסרה של גנים לקולטנים המטבוטרופיים לגלוטמט השונים, מחקרים גנטיים שבהם נבדקת שכיחות אללים מועמדים (של גנים לקולטנים המטבוטרופיים לגלוטמט) באוכלוסייה רגילה לעומת חולי סכיזופרניה ופרדיגמות התנהגותיות המדמות רכיבים שונים של סכיזופרניה בכלל ובעיקר את המצב הפסיכוטי. "עיכוב של קדם פולס" IPP (Pre-Pulse Inhibition) משמעו בחינה של התגובה לטון לאחר שמיעה קודמת של אותו טון. חיה לקויה (וגם חולי סכיזופרניה) תגיב בצורה שונה לעומת חיה תקינה. במודל השני נבדקת התנועתיות של החולדה (Locomotion) שנמצאה מוגברת בדומה לחולי סכיזופרניה. במודל השלישי נבחנות תנועות סטראוטיפיות המאפיינות מצב פסיכוטי, המתבטאות בחולדה בהתנהגויות, כגון: תנועה מעגלית אופיינית ותנועות ראש. ניתן להשרות ליקוי כזה באמצעות תכשירים מעכבי NMDA, כגון: קטמין, PCP או MK801, ולבדוק את השפעתם של תכשירים שונים המשפיעים על הקולטנים המטבוטרופיים לגלוטמט. תכשירים אלו מוגדרים כאורטוסטריים אם אתר הקישור שלהם הוא ישירות באתר הפעיל של הליגנד או אלוסטריים אם אתר הקישור שלהם מרוחק מהאתר הפעיל, אך בכל זאת משפיע עליו. לתכשירים אלוסטריים יתרון בכך שהשפעתם מתונה יותר וכן מובילים להרבה פחות ויסות כלפי מעלה או מטה של הקולטנים. למרבית הקולטנים המטבוטרופיים לגלוטמט סונתזו תכשירים מעכבים או משפעלים.
תוצאות מחקרים בבעלי חיים
הקולטנים המטבוטרופיים לגלוטמט 1
משערים כי לקולטנים המטבוטרופיים לגלוטמט 1 יש תפקיד בשפעול הקולטן ל-NMDA. בעכברים ללא הגן לקולטנים המטבוטרופיים לגלוטמט 1 נראתה הפרעה בתפיסה החושית, כפי שהתבטאה ב-PPI לא תקין, תוצאה שלא הוחמרה בתוספת PCP[7]. על אף זאת, מתן תכשירים אנטגוניסטיים לקולטנים המטבוטרופיים לגלוטמט 1 לא הובילו לתמונה דומה ב-PPI, גם לא לתיקון PPI לקוי בחיות שקיבלו לפני כן PCP או MK801[8]. מעכב הקולטנים המטבוטרופיים לגלוטמט 1 הוביל לשיפור בתנועות הסטראוטיפיות בחיות שטופלו לפני כן ב-MK801. בבחינת ההשפעה של מעכבי הקולטנים המטבוטרופיים לגלוטמט 1 על התנועתיות נראתה אפילו השפעה ממתנת בחיות לקויות.
הקולטנים המטבוטרופיים לגלוטמט 5
בעכברים ללא הגן לקולטנים המטבוטרופיים לגלוטמט 5 נראתה תגובה לקויה ב-PPI[9]. משערים שפעילות הקולטנים המטבוטרופיים לגלוטמט 5 משפעלת את הקולטן ל-NMDA, בעיקר באזורי מוח הקשורים לסכיזופרניה. מעכבי הקולטנים המטבוטרופיים לגלוטמט אינם מובילים להפרעה בתנועתיות או להופעת תנועות סטראוטיפיות. מתן מעכב הקולטנים המטבוטרופיים לגלוטמט 5 הוביל להגברה בהפרעה ב-PPI לאחר מתן PCP, כמו גם להחמרה בשאר במדדים כגון תנועתיות וסטראוטיפיות. על כן,משערים כי אגוניסט לקולטנים המטבוטרופיים לגלוטמט 5 עשוי להיות בעל סגולות אנטיפסיכוטיות בחולדות. ואכן, מחקרים ראשונים מראים כי תכשיר משפעל הקולטנים המטבוטרופיים לגלוטמט 5 הוביל לשיפור בתנועתיות וב-PPI בחולדות שטופלו לפני כן באמפטמינים, השיפור שהתקבל היה בצורה תלוית מינון [10].
אגוניסטים לקבוצה II (הקולטנים המטבוטרופיים לגלוטמט 2/3)
משערים כי קולטנים אלה, הממוקמים בקצה הקדם-סינפטי, מעכבים שחרור גלוטמט מקצה העצב לסינפסה ובכך משתתפים בבקרה על כמות הגלוטמט הסינפטית[11]. תאי העצב המבטאים את הקולטנים הללו הם GABA Interneurons, כלומר תאים מתווכים, שבהפעלתם (בקישור לקולטן ל-GABA) יש ירידה בהפרשת גלוטמט בסינפסה. מחקרי חיות הראו השפעה מהפכת של מתן תכשירים אגוניסטים אורטוסטריים לקבוצה II על ליקוי כתוצאה ממתן PCP או אמפטמינים. נוסף על כך, נראתה ירידה בשחרור גלוטמט בקורטקס הקדם-פרונטלי וכן שיפור בזיכרון עבודה.
הקולטנים המטבוטרופיים לגלוטמט 2
נראה כי לאגוניסטים של הקולטנים המטבוטרופיים לגלוטמט 2 יש השפעה דומה כמו לאגוניסטים של הקולטנים המטבוטרופיים לגלוטמט 2/3, דבר שמוביל להשערה כי עיקר השפעתם של האחרונים היא דרך הקולטנים המטבוטרופיים לגלוטמט 2. התכשיר LY487379 בעל השפעה אלוסטרית חיובית על הקולטנים המטבוטרופיים לגלוטמט 2 באופן ספציפי. לתכשיר יכולת לשפר הפרעה בתנועתיות בעכברים שטופלו ב-PCP ואמפטמינים לפני כן, אך במידה פחותה מאגוניסטים לקולטנים המטבוטרופיים לגלוטמט 2/3 [12]. עם זאת, לתכשיר זמן פעילות קצר דבר שלא מאפשר מחקר יישומי איתו. תכשיר חדש, BINA - אגוניסט לקולטנים המטבוטרופיים לגלוטמט 2 [13], הראה שיפור בתנועתיות וב-PPI בחיות שטופלו ב-PCP, אך לא באמפטמינים. לתכשיר זה אף נצפה זמן פעולה ארוך של עד 8 שעות.
הקולטנים המטבוטרופיים לגלוטמט 3
לא סונתזו תכשירים המשפיעים על הקולטנים המטבוטרופיים לגלוטמט זה. אולם, יש בגוף ליגנד טבעי לקולטן: NAAG (N-Acetyl-Aspartate-Glutamate). החומר הוא אגוניסט/אנטגוניסט חלקי, כלומר, בריכוז נמוך הוא מעכב את הקולטן ל-NMDA ובריכוזים גבוהים מפעיל את הקולטן ל-NMDA. נוסף על כך, החומר מעכב אוטו-קולטנים מסוג הקולטנים המטבוטרופיים לגלוטמט 3 האחראים על שחרור גלוטמט מהסינפסה. בהתאם, הוצעה תאוריה לסכיזופרניה [14] שבה מעורבת רמה נמוכה של NAAG, המובילה לעודף בהפרשת גלוטמט עקב ההשפעה על האוטוקולטנים. Olszewki וחבריו [15] דיווחו על תכשיר שכונה ZJ43, מעכב חזק של האנזים Glutamate Carboxypeptidase II & III. אנזים האחראי על ניטרול NAAG לאחר שחרורו לסינפסה. התכשיר ZJ43 אינו מגיב ישירות עם הקולטן ל-NMDA או עם הקולטנים המטבוטרופיים לגלוטמט. ואכן, מתן התכשיר, שיפר הפרעה בתנועתיות בחולדה שקיבלה PCP.
מחקרי אנוש בתכשירים אגוניסטיים לקולטנים המטבוטרופיים לגלוטמט
התכשיר LY354740 שהינו אגוניסט לקולטנים המטבוטרופיים לגלוטמט 2/3 (לא מבדיל בין הקולטנים) נבדק בניסויי אנוש, כקדם-טיפול במתנדבים שנטלו קטמין. לא נמצאה השפעה של התכשיר על תסמיני הסכיזופרניה כפי שנבדו במבחן PANSS, עם זאת, כן נמצא שיפור מה בזיכרון עבודה [16]. לעומת זאת, Patyl וחבריו [17] בדקו את התכשיר LY404039, גם הוא אגוניסט לקולטנים המטבוטרופיים לגלוטמט 2/3, כטיפול יחידי בחולי סכיזופרניה כרוניים. הם מצאו שיפור משמעותי בכל מדדי ה-PANSS לעומת אינבו. עוצמת השיפור הייתה דומה לזו שהתקבלה בקבוצה שטופלה באולנזפין. יתר על כן, התכשיר לא גרם לעלייה במשקל ורמת פרולקטין (בשונה מאולנזפין) או לתופעות לוואי אקסטרה-פירמידליות.
סיכום
נראה כי לתכשירים המשפיעים על פעילות הקולטנים המטבוטרופיים לגלוטמט יש תפקיד באפנון של הפעילות הגלוטמטרגית במוח. משמעותם הקלינית של תכשירים המשפיעים על ויסות הפרשת הגלוטמט עוד צריכה להתברר בניסויי אנוש רחבים המתוכננים עם תכשירים המשפיעים על הקולטנים המטבוטרופיים לגלוטמט בחולי סכיזופרניה. עם זאת, כבר כעת ניתן להניח כי השפעתם של קולטנים אלה עשויה להיות על כל קשת התסמינים בסכיזופרניה, ובכללם הממד הפסיכוטי, הסימנים השליליים והליקוי הקוגניטיבי. יש לצפות כי בעתיד נראה דיווחים על תכשירים המשפיעים על הקולטנים המטבוטרופיים לגלוטמט שנבחנו בניסויים קליניים בחולי סכיזופרניה.
דגלים אדומים
ביבליוגרפיה
- ↑ Farber NB. The NMDA receptor hypofunction model of psychosis. Ann NY Acad Sci 2003;1003:119-130
- ↑ Heresco-Levy U, Ermilov M, Shimoni J, et al. Placebo-controlled trial of D-cycloserine added to conventional neuroleptics, olanzapine, or risperidone in schizophrenia. Am J Psychiatry 2002;159:480-482
- ↑ Kew JN, Kemp JA. Ionotropic and metabotropic glutamate receptor structure and pharmacology. Psychopharmacology (Berl) 2005;179:4-29
- ↑ Krivoy A, Fischel T, Weizman A. The possible involvement of metabotropic glutamate receptors in schizophrenia. Eur Neuropsychopharmacol 2008;18:395-405
- ↑ Conn PJ, Pin JP. Pharmacology and functions of metabotropic glutamate receptors. Annu Rev Pharmacol Toxicol 1997;37:205-237
- ↑ Gupta DS, McCullumsmith RE, Beneyto M, et al. Metabotropic gluta- mate receptor protein expression in the prefrontal cortex and striatum in schizophrenia. Synapse 2005;57:123-131
- ↑ Brody SA, Conquet F, Geyer MA. Disruption of prepulse inhibition in mice lackingmGluR1. Eur J Neurosci 2003;18:3361-3366
- ↑ De VJ, Horvath E, Schreiber R. Neuroprotective and behavioral effects of the selective metabotropic glutamate mGlu (1) receptor antagonist BAY 36-7620. Eur J Pharmacol 2001;428:203-214
- ↑ Kinney GG, Burno M, Campbell UC, et al. Metabotropic glutamate subtype 5 receptors modulate locomotor activity and sensorimotor gating in rodents. J Pharmacol Exp Ther 2003;306:116-123
- ↑ Kinney GG, O'Brien JA, Lemaire W, et al. A novel selective positive allosteric modulator of metabotropic glutamate receptor subtype 5 has in vivo activity and antipsychotic-like effects in rat behavioral models. J Pharmacol Exp Ther 2005;313:199-206
- ↑ Schoepp DD, Jane DE, Monn JA. Pharmacological agents acting at subtypes of metabotropic glutamate receptors. Neuropharmacology 1999;38:1431-1476
- ↑ Johnson MP, Barda D, Britton TC, et al. Metabotropic glutamate 2 receptor potentiators: receptor modulation, frequency-dependent synaptic activity, and efficacy in preclinical anxiety and psychosis model(s). Psychopharmacology (Berl) 2005;179:271-283
- ↑ Galici R, Jones CK, Hemstapat K, et al. Biphenyl-indanone A, a positive allosteric modulator of the metabotropic glutamate receptor subtype 2, has antipsychotic- and anxiolytic-like effects in mice. J Pharmacol Exp Ther 2006;318:173-185
- ↑ Tsai SJ. Central N-acetyl aspartylglutamate deficit: a possible pathogenesis of schizophrenia. Med Sci Monit 2005;11:39-45
- ↑ Olszewski RT, Bukhari N, Zhou J, et al. NAAG peptidase inhibition reduces locomotor activity and some stereotypes in the PCP model of schizophrenia via group II mGluR. J Neurochem 2004;89:876-885
- ↑ Krystal JH, bi-Saab W, Perry E, et al. Preliminary evidence of attenuation of the disruptive effects of the NMDA glutamate receptor antagonist, ketamine, on working memory by pretreatment with the group II metabotropic glutamate receptor agonist, LY354740, in healthy human subjects. Psychopharmacology (Berl) 2005;179:303-309
- ↑ Patil ST, Zhang L, Martenyi F, et al. Activation of mGlu2/3 receptors as a new approach to treat schizophrenia: a randomized Phase 2 clinical trial. Nature Med 2007;13:1102-1107
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר אמיר קריבוי - מתמחה, המרכז לבריאות הנפש גהה, פתח תקווה, ד"ר צבי פישל - מ"מ מנהל מחלקה ג, המרכז לבריאות הנפש גהה, פתח תקווה, פרופ' אברהם ויצמן - מנהל יחידת המחקר, המרכז לבריאות הנפש גהה, פתח תקווה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק