הבדלים בין גרסאות בדף "טיפול פליאטיבי בחולה עם מחלת כליות סופנית המטופל בהמודיאליזה - Palliative care for patients with end-stage kidney disease undergoing hemodialysis"
| שורה 10: | שורה 10: | ||
|ICD-9= | |ICD-9= | ||
|MeSH= | |MeSH= | ||
| − | |יוצר הערך= טליה פליישמן ו[[משתמש:פסח שורצמן|פרופ' פסח | + | |יוצר הערך= טליה פליישמן ו[[משתמש:פסח שורצמן|פרופ' פסח שורצמן]] {{ש}}[[קובץ:TopLogoR.jpg|80px]] |
|אחראי הערך= | |אחראי הערך= | ||
}} | }} | ||
גרסה מ־08:21, 15 בפברואר 2013
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| טיפול פליאטיבי בחולה עם מחלת כליות סופנית המטופל בהמודיאליזה | ||
|---|---|---|
| Palliative care for patients with end-stage kidney disease undergoing hemodialysis | ||
| יוצר הערך | טליה פליישמן ופרופ' פסח שורצמן 
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – טיפול פליאטיבי, אי ספיקת כליות
בעשרים השנים האחרונות אנו עדים לשינויים דמוגרפיים ואפידמיולוגיים שחלו באוכלוסיית חולי אי ספיקת כליות סופנית המטופלים בדיאליזה. שינויים אלה הם ביטוי לתהליכים גלובליים המתרחשים במערכת הבריאות בכלל, ובתחום הנפרולוגי בפרט, כמו: עלייה בתוחלת החיים, עלייה בשכיחותן של מחלות חברת השפע בעולם (סוכרת ויתר לחץ דם), עלייה במודעות אנשי הבריאות והאוכלוסייה הכללית בתחום קידום הבריאות ואבחון המוקדם, נגישות גבוהה לשירותים הרפואיים והתפתחויות טכנולוגיות בתחום הטיפול הדיאליטי.
עם זאת, הטיפול בדיאליזה אינו תחליף אופטימלי לתפקוד הכלייתי, ועם הגידול בוותק הטיפול הדיאליטי, המטופל מתמודד עם עומס סימפטומים הולך ומתגבר.
איזון הסימפטומים הוא משימה אפשרית, וזאת תוך ביצוע שינוי תפיסתי בהתייחסות למחלת כליות סופנית המטופלת בדיאליזה כמחלה המקצרת את חיי המטופל והלא ניתנת לריפוי מלא.
במאמר זה נסקור ספרות מקצועית המתייחסת לאפידמיולוגיה של מחלת כליות סופנית, אפידמיולוגיה של חלק מהסימפטומים, יוצג כלי לגילוי עומס הסימפטומים וגם גישת טיפול תמיכתי במחלת כליות סופנית המטופלת בהמודיאליזה.
מבוא
מחלת כליות סופנית ESRD (End Stage Renal Disease), המטופלת באמצעות טיפולי כליה חלופיים RTT (Renal Replacement Therapy) שהשכיח מביניהם הוא המודיאליזה HD (Hemodialysis), היא בעיה עולמית בעלת שכיחות הולכת וגדלה. גם גיל המטופלים ב-HD נמצא במגמת עלייה מתמדת[1][2]. ע"פ נתוני ה-ISN (International Society of Nephrology) וה-IFKF (International Federation of Kidney Foundations), מספר החולים ב-ESRD בעולם עולה בקצב של כ-10%-7% בכל שנה, ומספרם של מטופלי הדיאליזה מגיע היום ל-1.5 מיליון[3]. שיעור התמותה השנתי בחולים הללו הוא 24%, והוא גבוה משיעורי התמותה של רוב סוגי הסרטן[4]. בארה"ב חיים כיום כ-470,000 חולי ESRD, כ-100,000 חולי ESRD חדשים מאובחנים כל שנה[5][6], וכ-336,000 אמריקאים מטופלים היום בדיאליזה[7]. באוסטרליה 7,952 חולים מטופלים באמצעות דיאליזה[1], ומאות אחדות של אוסטרלים נמצאים בסכנה לפתח מחלת כליות כרונית בעוד כעשר שנים [2]. באנגליה מספר החולים המטופלים ב-RTT עלה מ-20 איש למיליון איש באוכלוסייה בשנת 1982 ל-96 איש למיליון איש באוכלוסייה ב-1998. מתוכם 33% מטופלים ב-HD [1]. מנתוני המרכז הישראלי לדיאליזה ולהשתלת כליה עולה, שבעשור האחרון נרשם גידול של 35% בשיעור החולים הסובלים ממחלות כליה כרוניות (CKD): מ-48 חולים לכל 100,000 איש ב-1998 לכדי 65 חולים ב-2005. בישראל חיים כיום כ-700 אלף חולי כליה, המהווים כ-10% מכלל האוכלוסייה. על פי נתוני המרכז לדיאליזה ולהשתלות כליה במשרד הבריאות, מספר חולי הדיאליזה בישראל עלה בשמונה השנים האחרונות כמעט ב-60% אחוזים: מ-2,913 חולים בשנת 1998 לכ-5,000 חולים בשנת 2006. בשנים 2004 ו-2005 נפטרו 860 חולים, ובשנת 2006 נפטרו בישראל 910 חולי דיאליזה. רוב החולים נפטרים בעת שהם ממתינים להשתלת כליה (פרק הזמן הממוצע לקבלתה עומד על כ-5 שנים)[8].
תחלואה ותחלואה נלווית
ESRD מלווה בתחלואה קשה, כגון: סוכרת DM (Diabetes Mellitus), יתר לחץ דם HIT (Hypertension), מחלות לב וכלי דם CVD (Cardio-Vascular Diseases), חרדה (Anxiety) ודיכאון (Depression). התחלואה הנלווית מחמירה עם העלייה בגיל ובוותק הטיפול הדיאליטי[6]. על פי נתוני הסקר שנערך באנגליה בשנים 2004-1999, 32.6% ממטופלי הדיאליזה בגילים 65 ומעלה סובלים מ-CVD, יותר מ-18% מהם עוברים אוטם בשריר הלב MI (Myocardial Infarction), 14.7% סובלים ממחלת כלי דם במוח Cerebrovascular Disease, 17% סובלים ממחלת כלי דם פריפרית PVD (Peripheral Vascular Disease), 3.1% מפתחים כיבים איסכמיים בגפיים, 1.7% עוברים קטיעה וכ-27% סובלים מ-DM [9]. כ-28%-20% ממטופלי הדיאליזה סובלים דיכאון וכ-40% מחולי ESRD סובלים מחרדה, וזאת לעומת 13% הסובלים מחרדה באוכלוסייה הכללית[10][11].
נוסף על כך, חולי ESRD סובלים מסימפטומים קשים ומטרידים, כגון: כאב, בחילות, הקאות, חוסר תיאבון, גרד, קוצר נשימה, צימאון, יובש בפה, עצירות, הפרעות שינה, התכווצויות ברגליים, עייפות ועוד [11][12] מספר הסימפטומים הקשים אצל חולי ESRD דומה לזה של חולי סרטן[7].
הטיפול ב-ESRD ע"י ה-HD נחשב לטיפול פליאטיבי שמשמר חיים ומאפשר שליטה בסימפטומים אורמיים. עם זאת, הטיפול ב-HD אינו מונע את המשך התקדמותה של מחלת הכליות הבסיסית, המחלות הנלוות והתסמינים הקליניים הקשורים לאי ספיקת כליות והטיפול בה. עם העלייה בגיל ובוותק הטיפול ב-HD, הכמות והעוצמה של הסימפטומים הולכים ומחמירים [13].
תסמינים
כאב
כאב הוא אחד הסימפטומים השכיחים והמטרידים ביותר שאיתם מתמודד המטופל ב-HD. 50%-37% מהמטופלים ב-HD סובלים מכאבים, ו-82% מהם סובלים מכאבים קשים [7]. הסיבות לכאבים אצל חולי ה-ESRD הן מגוונות: הכאב עלול להיגרם ע"י המחלה הראשונית, כגון Polycystic Kidney Disease, או שעל ידי המחלה הנלווית, כמו: DM ו-PVD אשר מתבטאות בגפיים איסכמיות ונוירופתיה היקפית PN (Peripheral Neuropathy) . בחולי ESRD הקשישים שכיח כאב מוסקולוסקלטאלי הנובע מדלקת מפרקים (Arthritis). הכאב עלול להופיע גם בעקבות הטיפול ב-HD, לדוגמה: זיהום העירוי המרכזי או הגישה לכלי דם פריפריים שגרמו ל-Osteomyelitis או ל-Discitis. כאבים חוזרים עלולים להתנהג אצלם ככאב כרוני, לדוגמה: בעקבות הדקירות החוזרות ונשנות לגישה לכלי דם, סינדרום הגנבה (Steal Syndrome), התכווצויות שרירים (Muscle Cramps) וכאבי ראש במהלך הדיאליזה[14]. נוסף על כך, עלולים להופיע ולהחמיר עם העלייה בוותק הטיפולים הדיאליטי תסמיני כאב ייחודיים לחולי ה-ESRD, כגון: DRA (Dialysis Related Amiloidosis), NSF (Nephrogenic Sclerosing Fibrosis), Calciphylaxis, RO (Renal Osteodystrophy)[7].
במחקר של קבוצת חוקרים ישראלים מהמרכז הרפואי מאיר, כפר סבא, נמצא כי 51% מהמטופלים סבלו מכאב כרוני, ומתוכם 19.6% דיווחו על כאב חמור. לרוב היו הכאבים ממקור מוסקולוסקלטלי, נוירופתי או כאבי ראש. נמצא קשר מובהק בין הכאב לקיום הפרעה באיזון הורמון ה-Parathyroid (ה-PTH) עם עלייה ברמת הסידן בדם [15].
לכאב השפעה קשה על איכות החיים תלוית מחלה HRQOL (Health-Related Quality of Life). במחקרה של Davison (2002) , 62% מהמטופלים ב-HD דיווחו על פגיעה בפעילות הפנאי, 51% דיווחו על סבל קשה, ו-41% חשבו על הפסקת הדיאליזה בעקבות הכאבים. בעבודות שונות נמצא קשר חיובי בין כאב לדיכאון בקרב מטופלי הדיאליזה. הכאב מעלה את רמת החרדה ומשבש את התפקידים החברתיים ויכולת המטופל להמשיך לעבוד. כאב עלול להיות סיבה לפרישה מהדיאליזה [16].
גרד
סימפטום מטריד נוסף הוא גרד (Itching) שמלווה בהופעת פריחה (Uremic Pruritis). הסיבות לגרד ב-ESRD לא ברורות דיין, אך בדרך כלל מייחסים אותו לשקיעת מלחי סידן-זרחן בעור בעקבות ה-Secondary Hyperparathyroidism [17].
בשנים 1996-2001 נערך מחקר גדול, המכונה DOPPS I, שבו השתתפו 6,137 חולי ESRD מ-200 יחידות דיאליזה שנבחרו באופן אקראי בשבע מדינות: צרפת, גרמניה, איטליה, יפן, ספרד, אנגליה וארה"ב. נמצא כי חולים בכל היחידות שנבחרו סבלו מגרד, אך במידה שונה - 5% עד 75%. 46% מהחולים בממוצע התלוננו על גרד בינוני עד קשה, והממצאים במדינות היו כדלקמן: צרפת (38%), יפן וארה"ב (45%), ספרד (46%), אנגליה (48%), גרמניה (49%) ואיטליה (55%).
גברים התלוננו על גרד יותר מנשים (AOR¼ 1.10; p<0.05), בעלי ותק טיפול בדיאליזה נמוך מ-3 חודשים התלוננו פחות משאר המטופלים על גרד (AOR¼ 0.80; p<0.0003). חולים עם ערכי סידן גבוהים (Albumin-Corrected Calcium>10.2mg/dl), ערכי זרחן גבוהים (Phosphorus>5.5mg/dl) ו/או תוצר סידן-זרחן גבוה בדם (Calcium Phosphorous Product Concentrations >70mg2/dl2) התלוננו יותר משאר המטופלים על הגרד והפריחה. נמצא כי לגרד נטייה להחמיר בלילה, והוא פוגע באופן מובהק באיכות השינה אצל מטופלי ה-HD (1.5–4.1 Odds; p<0.002). חולים עם גרד קשה דיווחו על עייפות עד לתחושה של היות סחוט, מותש (2.3–5.2 Odds; p<0.0001) וכן רמת הדיכאון אצלם הייתה גבוהה יותר (1.3–1.7 Odds; p<0.01, p<0.0001). גרד קשה נמצא קשור לתמותה גבוהה ב-15% לעומת החולים ללא גרד (p<0.008) [18]. במחקר אחר נמצא קשר לנוכחות נוירופתיה פריפרית PN (Peripheral Neuropathy) וגרד. המטופלים עם PN התלוננו יותר על גרד (63.8%) לעומת המטופלים ללא נוירופתיה (42.1%) (pv=0.006)[19].
עייפות
עוד תלונה שכיחה ומטרידה היא עייפות (Fatigue). מדיווחי הספרות עולה, כי שיעור העייפות בקרב חולי ה-ESRD הוא 77% עד 91% [11]. לרוב, מופיעה עייפות לאחר הדיאליזה, אך עלולה להפוך לקבועה עם פגיעה ביכולת החולה לספק את צרכיו הבסיסיים, תלות באחרים ובעיות פסיכו-סוציאליות נוספות[16][17]. נמצא קשר בין עייפות קשה להפרעות שינה, חרדה, דיכאון, חולשת שרירים וכאבי מפרקים. נמצא קשר שלילי חלש בין עייפות לבין התפקוד היום-יומי (Physical Functioning). נשים דיווחו על עייפות רבה יותר ועל תפקוד פיזי טוב פחות, לעומת הגברים (r=-0.369; p=0.007). נמצא קשר חזק בין העלייה בגיל לבין הירידה הכללית בתפקוד היום-יומי והעייפות[20][21] (r=-0.339; p=0.021). ניתן לחלק את תחושת העייפות לארבע קטגוריות: עייפות כללית (General Fatigue), עייפות גופנית (Physical Fatigue), ירידה בפעילות (Reduced Activity) ירידה בהנעה (Reduced Motivation) ועייפות נפשית (Mental Fatigue). אצל חולי ESRD נמצאה עלייה בכל סוגי העייפות, אך במיוחד בעייפות הכללית (Cronbach’s Alpha=0.74) וירידה בפעילות (Cronbach’s Alpha=0.823) [22].
אומדן תסמינים
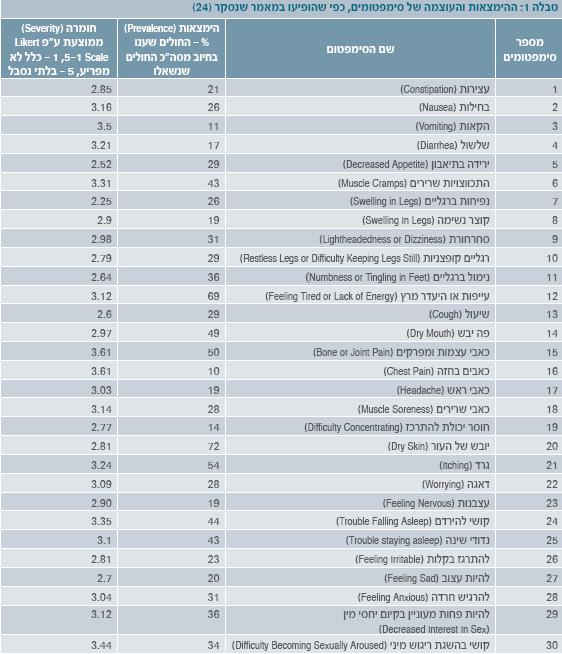
משום ריבוי הסימפטומים המטרידים, פיתחו קבוצת חוקרים מאוניברסיטת פיטסבורג, ארה"ב, מדד להערכת עומס הסימפטומים הגופניים והרגשיים באוכלוסיית המטופלים בהמודיאליזה כרונית, הקרוי DSI (The Dialysis Symptom Index) [22][23]. הכלי עבר בדיקת תוקף ומהימנות, והוא כולל 30 סימפטומים בעלי שכיחות והשפעה הגבוהים ביותר אצל המטופל ב-HD כרונית. במחקרם הנוסף של החוקרים, נבדקו ההימצאות והחומרה של הסימפטומים ע"פ DSI בקרב 162 מטופלי HD שמתוכם 62% היו גברים ו-48% היו חולי סוכרת. במחקרם נעשה שימוש ב-IEQ (Illness Effects Questionnaire) לבחינת איכות החיים וב-BDI (Beck Depression Inventory) לאבחון הדיכאון. המספר הממוצע של סימפטומים במטופלי HD מהמדגם היה 9, ועוצמתם הייתה מ-6 עד 13. עור יבש, עייפות, גרד וכאבי עצמות ומפרקים נמצאו כסימפטומים השכיחים ביותר אצל יותר מ-50% מאוכלוסיית המדגם[24].
ההתמודדות עם הסימפטומים, לרבות הכאב והתחלואה הנלווית, גורמת לסבל ופוגעת בכל האספקטים השונים של חיי המטופל ב-HD: במישור הגופני, הנפשי, הרוחני והחברתי. ההתמודדות עם הסימפטומים פוגעת באיכות חיי התא המשפחתי. HD אינה פוטרת את המטופל מהתמודדות עם הסימפטומים. ההפך הוא הנכון, העוצמה ומספרם של הסימפטומים המטרידים עולה עם העלייה בוותק הטיפול הדיאליטי, וזאת משום שהטיפול הדיאליטי אינו מונע את המשך ההתקדמות של מחלת הכליות הבסיסית, המחלות הנלוות והתסמינים הקליניים הקשורים לאי ספיקת כליות ולטיפול בה. לכן, HD נחשב כטיפול פליאטיבי (Palliative Care) במחלת כליות סופנית (End Stage Renal Disease) שלא ניתנת לריפוי באמצעים הקיימים היום. מטרתו של הטיפול הדיאליטי הוא לשמר חיים ולאפשר שליטה מרבית בסימפטומים האורמיים[13][25].
טיפול פליאטיבי (תמיכתי) בחולה עם אי ספיקת כליות המטופל בדיאליזה
מטופל בהמודיאליזה HD (Hemodialysis) ומשפחתו נדרשים להתמודד עם תסמיני המחלה והטיפול בה. התמודדות זו דורשת מהם ידע וכלים לאיזון הסימפטומים, וכן קיום מערכת תמיכה מקצועית שתסייע למטופל ולקרוביו המשמעותיים בהתמודדותם עם מלחמת הישרדות מתמדת זו. לצורך כך, אומצה בעשור האחרון במדינות המפותחות, כגון: ארה"ב [25][26], אנגליה[9] וקנדה[27], שיטת הטיפול הפליאטיבי ב-ESRD, הידועה כנותנת מענה לטיפול בחולים הסובלים ממחלות קשות וחשוכות מרפא.
על פי הגדרת ארגון הבריאות העולמי (WHO) מ-1992, מוגדר הטיפול הפליאטיבי/תמיכתי (Palliative/Supportive Care) כגישה טיפולית שמשפרת את איכות החיים של חולים ובני משפחותיהם, המתמודדים עם מחלות כרוניות קשות, על ידי מניעה והקלה של הסבל באמצעות זיהוי והערכה קפדנית של הסימפטומים, טיפול בכאב ובבעיות אחרות: גופניות, נפשיות ורוחניות.
באנגליה קונספט הטיפול התמיכתי במחלת כליות סופנית (ESRD) היא חלק ממדיניות הטיפול על פי NSF (National Service Framework for Renal Services Part 2, February 2005). הוא מתייחס לצורך לתת מענה אופטימלי לצורכי החולה ב-ESRD הנמצא בשלבים המתקדמים של מחלתו לקראת המוות, בייחוד גוף הידע שהצטבר בתחום הטיפול הפליאטיבי והנפרולוגי יחד. קבוצת חוקרים מאנגליה[28] ביצעה מטה-אנליזה של המושג "טיפול תמיכתי" (Supportive Care) אצל חולי ESRD בספרות העדכנית, וזיהו מספר אבני ייסוד לטיפול זה:
- נגישות מעת קביעת המחלה ועד המוות, תוך מתן דגש על כנות ואמינות בנוגע לפרוגנוזה ולהשלכות של מחלת כליות סופנית.
- קבלת המושג "מוות טוב" (Good Death)
- מטרות הטיפול דומות לאלה של מחלת הסרטן, עם הבדל אחד משמעותי והוא שמחלת הסרטן במקרים רבים ניתנת לריפוי, ואילו ESRD מקצרת משמעותית את תוחלת החיים, למרות הטיפול ב-RTT.
- שינויים דמוגרפיים של אוכלוסיית מטופלי הדיאליזה הכוללים עלייה במספר מטופלים קשישים מאוד וחולים מאוד, גורם להחמרת הפרוגנוזה.
- התקשורת ביחידת הדיאליזה אמורה להיות פתוחה, כך שהמטופל יבין שמדובר במחלה המקצרת את חייו (Life Limiting Disease).
- המטופל יהפוך לשותף פעיל בטיפולו ובתהליך קבלת ההחלטות, כולל האופציה שלא להתחיל ו/או להמשיך בטיפול הדיאליטי, שאמורה להיות פתוחה ונידונה עם המטופל ומשפחתו.
- גישת הטיפול הרב מקצועי (Interdisciplinary Approach to Care).
- על הצוות הנפרולוגי לאמץ שיטות של הטיפול התמיכתי או להיעזר במומחים מתחום הפליאטיבי.
- תפיסת הטיפול הפליאטיבי דורשת שינוי בתפיסת העולם של יחידת הדיאליזה.
- השינוי התפיסתי אמור להתחיל לא רק בשיטות העבודה הרב מקצועיות, אלא ראשית בתוך כל אחד מהמקצועות: רפואה נפרולוגית, סיעוד נפרולוגי, עבודה סוציאלית וכו'.
- לאחר שמקבלים שינוי בתפיסת המחלה כמקצרת חיים, ניתן להתייחס לצורכי המטופל מזווית אחרת, ולבדוק איתו איך ניתן להעביר את שארית חייו במינימום סבל ותוך מיצוי אופטימלי של צרכיו הרגשיים והחברתיים.
- טיפול מחזק ומשקם (Restorative Care).
- ייחודיות הטיפול התמיכתי (Supportive Care) ב-ESRD בכך שהוא כולל מרכיבים טיפוליים (Curative Care) ושיקומיים (Restorative Care). הטיפול המשקם מופנה לטיפול במחלה עצמה ולביטוייה, ניסיון להחזיר את המצב לקדמותו מבחינת התהליך הפתופיזיולוגי המתרחש בו.
- עם התקדמות הטכנולוגיה בתחום הטיפול הדיאליטי, ניתן להשיג תוצאות טיפול טובות מאוד במטופלי HD, תוך עיכוב התקדמות הסימפטומים. לכן, הטיפול המשקם (Restorative Care) הוא חלק בלתי נפרד מהטיפול הפליאטיבי בחולה ESRD מעת גילוי המחלה, דרך הטיפול בדיאליזה ועד סוף חייו. מתן תמיכה למשפחה ולמטפלים המשמעותיים של המטופל.
- משפחת המטופל מתמודדת עם הפחד מפני המחלה, המוות ומפני הבלתי נודע.
- קרובי המטופל מתמודדים עם העובדה שללא הטיפול הדיאליטי, יקירם נידון למוות.
- המשפחה מתמודדת עם העובדה כי יקירם סובל מבעיות מטרידות, כגון עודף נוזלים, כאבים וכו'.
- המשפחה מתמודדת עם העובדה שיקירם אולי זקוק לעזרה פסיכולוגית ורוחנית.
- המשפחה עלולה להתמודד עם העובדה, כי החולה הוא כעת מרכז החיים, ושצורכי המשפחה, כביכול, פחות חשובים.
- קונספט הטיפול התמיכתי כולל התייחסות למשפחת המטופל ולצרכיה.
- תקשורת אפקטיבית וברורה לצורך קבלת החלטות קליניות משמעותיות.
- כאשר מצב המטופל מידרדר מאוד, יש לשוחח על המשך הטיפול בצל תופעות הלוואי של ה-HD (החמרת הסימפטומים).
- יש גם להתייחס לעובדה כי המשך הטיפול הדיאליטי כרוך בהעלאת התחלואה ובעלות טיפול גבוהה עם תועלת נמוכה.
חשוב לציין, כי טיפול תמיכתי במחלת כליות סופנית אינו בא להחליף או להפסיק את הטיפול הדיאליטי, מדובר בפילוסופיה של טיפול לפיה הטיפול התמיכתי ניתן תוך כדי ניסיון לספק טיפול משקם ומחזק למטופל המתמודד עם ההשלכות של מחלת כליות סופנית (ESRD) והטיפול בה, טיפול שלא נותן מענה אופטימלי לצרכיו הגופניים, הנפשים והחברתיים של החולה[28][29].
סיכום
מחלת כליות סופנית היא מחלה קשה שלא ניתנת לריפוי מלא באמצעות טיפולים מחליפי התפקוד הכלייתי הקיימים היום. חולה ESRD מתמודד עם עומס סימפטומים למרות הטיפול הדיאליטי. איזון הסימפטומים הוא משימה חשובה ואפשרית לשיפור איכות החיים ושביעות הרצון של המטופל ומשפחתו. Renal Supportive Care – היא גישת טיפול חדשה בתחום הנפרולוגי. זהו טיפול תמיכתי במטופל ובמשפחתו, המשלב את מרכיבי הטיפול המרפא והמשמר במרכיבי הטיפול הפליאטיבי. דוגמה ליישום טיפול כזה הקיים באנגליה הוצג במאמר זה.
דגלים אדומים
ביבליוגרפיה
- ↑ 1.0 1.1 1.2 Roderick P, Ansell D. Changing patterns of renal replacement therapy. In Chambers EJ, German M, Brown E. Supportive care for the renal patient. 1th Ed. Oxford University Press Inc, New York 2004
- ↑ 2.0 2.1 Williams A, Manias E. A structured literature review of pail assessment and management of patients with chronic kidney disease. Journal of Clinical Nursing 2008;17: 69-81
- ↑ Noble H, Kelly D, Rawlings-Anderson K, et al. A concept analysis of renal supportive care: the changing world of nephrology. Journal of Advanced Nursing 2007;59(6):644–653
- ↑ US Renal Data System. USRDS 2001 Annual Data Report. In: Weisbord, SD, Fried LF, Arnold RM, et al. Development of a symptom assessment instrument for chronic hemodialysis patients: The Dialysis Symptom Index. Journal of Pain & Symptom Management 2004;27(3):226-240
- ↑ Kring DL, Crane PB. Factors Affecting Quality of Life in Persons on Hemodialysis. Nephrology Nursing Journal 2009;36(1):15-25
- ↑ 6.0 6.1 Annual Data Report: Athlas of End-Stage Renal Disease in Unated States. In: Davison SN. The prevalence and Management of Chronic Pain in End-Stage Renal Disease. Journal of Palliative Medicine 2007;10(6):1277-1287
- ↑ 7.0 7.1 7.2 7.3 Davison SN. The prevalence and Management of Chronic Pain in End-Stage Renal Disease. Journal of Palliative Medicine 2007;10(6):1277-1287
- ↑ נתונים שהוצגו בכנס מודעות למחלות כליה ופורסמו ב-17/02/08באתר www.doctors.co.il
- ↑ 9.0 9.1 Brown EA. Epidemiology of Renal Palliative Care. Journal of Palliative Medicine 2007;10(6):1248-1252
- ↑ Ibrahim S, El Salamony O. Depression, Quality of Life and Malnutrition-Inflammation Scores in Hemodialysis Patients. American Journal of Nephrology 2008;28:784–791
- ↑ 11.0 11.1 11.2 Kring DL, Crane PB. Factors Affecting Quality of Life in Persons on Hemodialysis. Nephrology Nursing Journal 2009;36(1):15-25
- ↑ Wicks MN, Bolden L, Mynatt S, et al. INSIGHT Potentially Prevents and Treats Depressive and Anxiety Symptoms in Black Women Caring for Chronic Hemodialysis Recipients. Nephrology Nursing Journal 2007;34(6): 623-629
- ↑ 13.0 13.1 Sekkarie MA, Swartz R. Symptoms of renal disease: The treatment and palliation of symptoms due to co-morbidity in end-stage renal disease. In: Chambers EJ, German M, Brown E. Supportive care for the renal patients. Oxford University Press Inc, New York 2004;95-104
- ↑ Davison SN, Jhangri GS. The impact of chronic pain on depression, sleep, and the desire to withdraw from dialysis in hemodialysis patients. Journal of Pain and Symptom Management 2005;30:465-473
- ↑ Golan E, Hahhiag I, Os P, et al. Calcium, Parathyroid Hormone and Vitamin D: Major determinants of chronic pain in Hemodialysis Patients. Clinical Journal of American Society of Nephrology 2009;4:1374-1380
- ↑ 16.0 16.1 Ferro CJ, Chambers J, Davison SN. Management of pain in renal failure. In: Chambers EJ, German M, Brown E. Supportive care for the renal patients. Oxford University Press Inc, New York 2004;8:105-153
- ↑ 17.0 17.1 Germain M, McCarthy S. Symptoms of renal disease: dialysis related symptomps. In E.J.Chambers, M.German, & E.Brown. Supportive care for the renal patients. Oxford University Press Inc., New York 2004;7(Part 1):75-94
- ↑ Wikstrom B. Itchy skin - a clinical problem for haemodialysis patients. Nephrology Dialysis and Transplantation 2007;22(Suppl 5):3–7
- ↑ Akhyani M, Ganji MR, Samadi N, et al. Pruritus in hemodialysis patients. BMC Dermatology 2005;5:7
- ↑ O’Sullivan D, McCarthy G. Exploring the Symptom of Fatigue in Patients with End Stage Renal Disease. Nephrology Nursing Journal 2009;36(1): 37-39,47
- ↑ McCann K, Boore J. Fatigue in persons with renal failure who require maintenance haemodialysis. Journal of Advanced Nursing 2000;32:1132–1142
- ↑ 22.0 22.1 O’Sullivan D, McCarthy G. An exploration of the relationship between fatigue and physical functioning in patients with end stage renal disease receiving haemodialysis. Journal of Nursing and Healthcare of Chronic Illness in association with Journal of Clinical Nursing 2007;16(11): 276–284
- ↑ Weisbord SD, Fried LF, Arnold RM, et al. Development of a symptom assessment instrument for chronic hemodialysis patients: The Dialysis Symptom Index. Journal of Pain & Symptom Management 2004;27(3):226-240
- ↑ Weisbord SD, Fried LF, Arnold RM, et al. J Am Soc Nephrol 2005;16:2487-2494
- ↑ 25.0 25.1 Cohen LM, Moss AH, Weisbord SD, et al. Renal Palliative Care. Journal of Palliative Medicine 2006;9(4):977-992
- ↑ Jablonski A. The Multidimensional Characteristics of Symptoms Reported by Patients on Hemodialysis. Nephrology Nursing 2007;34(1): 29-37
- ↑ Fainsinger RL, Davison SN, Brenneis C. A supportive care model for dialysis patients, Palliative Medicine 2003;17:81-82
- ↑ 28.0 28.1 Noble H, Kelly D, Rawlings-Anderson K, et al. A concept analysis of renal supportive care: the changing world of nephrology. Journal of Advanced Nursing 2007;59(6):644–653
- ↑ Chambers EJ, German M, Brown E. Supportive care for the renal patient. 1th Ed. Oxford University Press Inc, New York 2004
קישורים חיצוניים
המידע שבדף זה נכתב על ידי טליה פליישמן RN, MA - מורה בביה"ס לסיעוד, מרכז רפואי מאיר, שירותי בריאות כללית; אחות בחברת נפרומור בע"מ, פרופ' פסח שוורצמן - מנהל שירות שיכוך כאב והמחלקה לרפואת משפחה, שירותי בריאות כללית, מחוז דרום; אוניברסיטת בן גוריון בנגב, באר שבע


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק