תת פעילות ראשונית של בלוטות יותרת התריס - טיפול בנטפרה - Primary hypoparathyrodism - treatment with natpara
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| פעילות יתר ראשונית של בלוטות יותרת-התריס - טיפול בנטפרה | ||
|---|---|---|
| Primary hyperparathyroidism - treatment with natpara | ||
| יוצר הערך | פרופ׳ צופיה איש-שלום | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – רמת סידן בדם ובלוטת יותרת התריס#הפרעות בפעילות יותרת התריס
מחלות אנדוקריניות משתייכות ל-3 קבוצות עיקריות:
- מצבי חסר הורמונלי
- מצבי עודף
- עמידות להורמון
הטיפול המתאים ביותר למצב חסר הורמונלי הוא מתן ההורמון החסר, באופן שמחקה את הפרשתו הפיזיולוגית. הדבר מתאפשר בד"כ באופן חלקי, אך בכל מצבי החסר המוכרים עד כה ניתן טיפול הורמונלי, מלבד ב- PHPT (PRIMARY HYPOPARATHYROIDISM).
PHPT היא "מחלה יתומה", כלומר מחלה שהחולים בה מעטים. בארה"ב דווח על כ-70,000 חולים[1]. לא נעשה מחקר אפידמיולוגי בנושא זה בישראל, אך ניתן להעריך שיש כמה מאות חולים בארץ. המחלה נובעת מחסר הורמון PTH (Parathyroid hormone). היות ומדובר בהורמון חיוני לבקרת משק הסידו והזרחן בגופנו, החסר יתבטא בהיפוקלצמיה, היפרפוספטמיה, רמה נמוכה של 0H)2D)1,25, רמה נמוכה או נמוכה יחסית לריכוז הסידן בדם, של הורמון PTH בבדיקת מעבדה.
ברוב המקרים מדובר במחלה נרכשת והסיבה השכיחה ביותר היא כריתה של בלוטות יותרת התריס בניתוחי צוואר[1], [2], [3], [4], [5]. ייתכן גם הרס עקב תהליך אוטואימוני, הקרנות, שקיעת ברזל או נחושת בתוך הבלוטה[4], [5]. לעתים נדירות מדובר במחלה גנטית כגון תסמונת DiGeorge velocardiofacial syndromes ואחרות.
הביטוי הקליני של המחלה הנובע מהיפוקלצמיה, נע בין התייצגות מתונה יחסית נימול, התכווצויות שרירים, "הרדמות" גפיים, עייפות וקשיי חשיבה וריכוז; לביטוי חמור של גירוי נוירומוסקולרי כגון טטניה, לרינגו-וברונטספאזם ומעורטת מערכת העצבים המרכזית: מצב בלבולי, פרכוסים ואבדן הכרה. תיתכן מעורבות לבבית כגון הארכת קטע QT ואי ספיקת לב[2], [4].
הטיפול בביטוי חמור וחריף של המחלה הוא מתן תוך ורידי של מלחי סיח ומטמליט פעיל של ויטמין D, באשפוז ותחת בקרה[2], [6].
הטיפול הכרוני כולל מתן פומי של תוסף סידן ומטבוליט פעיל של ויטמין D. יעדי הטיפול הם השגת הקלה בסימפטומי ההיפוקלצמיה ומניעת סיבוכים ארוכי טווח. מבחינה מעבדתית, השאיפה היא לשמור את ריכוז הסידן המתוקנן לאלבומין בין 8-8.5 מ"ג/ ד"ל, ריכוז הזרחן מתחת ל-6 מ"ג/ד"ל, מכפלת ריכוזי סידן זרחן בסדום מתחת ל-55 מ"ג2/ד"ל2 ולשמור על הפרשת הסידן בשתן בתחום התקין. היפרקלציאוריה ממושכת יכולה לגרום ל-nephrocalcinosis, nephrolithiasis ומחלת כליות כרונית עם ירירה בתפקוד הכלייתי. היפרפוספתמיה עלולה להוביל לשקיעת מלחי סידן זרחן ברקמות הרכות ובגרעינים הבזליים במוח. ההצלחה בהשגת יעדי הטיפול[1] והמינון הטיפולי של תוספי סידן והמטבוליט הפעיל של ויטמין D, שונה מאוד מאדם לאדם. לעתים למרות מתן מינונים גבוהים של תכשירי הטיפול לא מושגים יעדי הטיפול, החולים סובלים מפגיעה באיכות חיים[2], [7] ומאירועי היפוקלצמיה סימפטומטית המחייבים אשפוז, זאת למרות הקפדה על תזונה דלת זרחן, צריכת תבשיrhם קושרי זרחן ו-disothiazide. עבור חולים אלה נדרש פיתרון יעיל יותר - מתן (1-84)rhPTH, שיעילותו בטיפול ב-PHPT הוכחה.
מאפיינים פרמקודינמיים של (1-84)rhPTH
(1-84) rhPTH (Natpara) זהה במבנה למולקולת PTH אנדוגני, המכילה קצה N - טרמינלי (34 חומצות אמינו) וקצה c - טרמינלי המכיל 50 חומצות אמינו[8], [9]. ל-PTH תפקיד מכריע בבקרת משק הסידן. הפרשת PTH מווסתת על ידי ריכוז יוני הסידן בסרום. חיישני הסידן (calcium sensing receptors-caSRs), הממוקמים בדפנות תאי ארבע בלוטות יותרת התריס, מעבירים לתוך התא מסר בהתאם לריכוז יוני הסידן בסרום[10]. ירידה קלה בריכוז יוני הסידן גורמת להפרשה של PTH ובהמשך להגברה של יצור ההורמui בבלוטות אלה' ואילו לעלייה בריכוז יוני הסידן השפעה הפוכה. בכך נשמרת רמת יוני הסידן בסרום באדם הבריא בטווח קבוע ויציב בין 4.4-5.3mg/dL . הסידן היוני מהווה קצת פחות מ-50% מסך הסידן שנמדד בבדיקות שגרה מעבדתיות.
PTH יחד עם שני הורמונים נוספים: 0H)2D)1,25 (מטבוליט פעיל של ויטמין D) ו-23 FGF (23 fibroblast growths factor) מווסת את רמת הסידן והזרחן בסרום, על ידי השפעה ישירה ועקיפה על עצם, כליה ומעי [11].
PTH פועל בשני אופנים שונים. חשיפה רציפה להורמון גורמת להפרשה של הסידן והזרחן מהעצם על ידי הגברת פרוק העצם עקב עידוד התמיינות האוסטיאוקלסטים - תאים מפרקי עצם. חשיפה קצרה להורמון זה מעודדת התמיינות ושרירות של האוסטיאובלסטים, תאים בוני עצם. כך שמצד אחד ההורמון מסייע בגיוס מהיר של יוני הסידן מהמאגר בשלד (בגוף האדם מכיל השלד בין 1-1.5 ק"ג סידן, המהווה מאגר חרום של יוני הסידן) ומאידך מעודד את בניית העצם ואת התחדשותה[12].
בכליה PTH מעודד את הריאבסורבציה הטובולרית של יוני הסידן ומגביר את הפרשת יוני הזרחן. כמו כן הוא מעודד את יצירת המטבוליט הפעיל של ויטמין D 0H)2D)1,25 מ-250HD, המשפיע על ספיגת הסידן והזרחן במעי. ל-PTH ול- 0H)2D)1,25 תפקיד חשוב בהגברת יצור והפרשה של 23-FGF, הורמון פוספטורי. מכות פעולה זו נשמרת מכפלת ריכוז הסידן והזרחן בסרום בתחום פיזיולוגי קבוע, שמונע יצירת משקעי מלחי סידן זרחן ברקמות הגוף[4]. לאור מורכבות הפעילות הפיזיולוגית של PTH והקושי לחקותה במדויק, בוצעה שורה של מחקרים להערכת ההשפעה של (1-84)rhPTH על משק הסידן והזרחן בחולי PHPT.
במחקר פאזה I, בשבעה חולי PHPT, מתן (1-84)rhPTH בהזרקה תת עורית בירך גרם לעלייה בריכוז הסידן בסרום לערך שיא (peak) 12 שעות לאחר ההזרקה והריכוז נשמר מעל הערך שלפני ההזרקה, לאחר 24 שעות. התגובה הייתה גדולה יותר לאחר מתן 100 מק"ג, בהשוואה למתן 50 מק״ג. כמו כן נצפתה ירידה בהפרשת הסידן בשתן[13], [14]. הזמינות הביולוגית של (1-84)rhPTH לאחר הזרקה תת עורית היא 53%[13]. התרופה מתפנה בעיקר באמצעות הכבד ובמידה פחותה דרך הכליה[13].
יעילות הטיפול ב- Natpara ((1-84)rhPTH) ב-PHPT
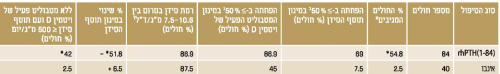
א. הכוונה למטופלים שבהם הושגו כל שלושת היעדים העיקריים של המחקר:
1. הפחתה ב-> 50% במינון תוסף הסידן
2. הפחתה ב-> 50% במינון המטבוליט הפעיל של ויטמין D.
3. רמת הסידן בסרום, המתוקננת לאלבומין בין 7.5 ל-10.6 מ״ג/ד"ל
ב, ג,ד. התייחסות ליעדים 1,2,3 בנפרד
*0.001>p לעומת אינבו
- מחקרים קליניים פאזה III
הפיתוח הקליני של הטיפול ב-Natpara ב-PHPT, כלל ארבעה מחקרי פאזה III:
- (RACE (NCT01297309
- (REPLACE (NCT00732615
- (RELAY (NCT01268098
- (REPEAT (NCT01455181
התרופה אושרה על ידי ה-FDA לטיפול ב-PHPT על סמך ממצאי מחקר REPLACE[8], [15].
במחקר זה, מחקר כפול סמיות, מבוקר אינבו, נבדקה יעילות ובטיחות של טיפול ב-Natpara (1-84)rhPTH בחולים עם PHPT. במחקר נכללו חולים עם PHPT מוכח במשך 18 חודשים לפחות, בגילאי 18 עד 85 (גיל ממוצע 47), 79% היו נשים. חולים שסבלו ממוטציות ב-CaSR או מ-Pseudohypoparathyroidism לא נכללו במחקר. לפני תחילת המחקר החולים עברו תקופת "הכשרה". בתקופה זו, שנמשכה 2-16 שבועות, תוקנו חסרים במגנזיום וויטמק D והופסק הטיפול ב-disothiazide[8], [15], [16]. רמת הסידן בסרום אוזנה בין 8-9 מ"ג/ד"ל על ידי מתן סדיר של תוסף סידן ומטבוליט פעיל של ויטמין D 0H)2D)1,25- או alfacaicidol. חולים ששמרו על איזון יציב של
במחקר. לפני תחילת המחקר החולים עברו תקופת ׳׳הכשרה׳׳. בתקופה זו, שנמשכה 2-16 p שטעות, תוקנו חסתם במגנזיום וויטמק ס והופסק הטיפול ^9•16•17disothiazide. רמת הסיק בסתם אחנה p 8-9 מ׳׳ג/ד׳׳ל על ית מתן סתר של תוסף סיק ומטמליט פעיל של ויטמק 1,25(0H)2D - D או alfacaicidol. חולים ששמרו על איזון יציב של רמת הסידן בתחום היעד עברו רנדומחציה לקמצת טיפול או אישו מחס 2 ל-84.1 חולים נכללו בסיום המחקר בקמצת הטיפול ו-40 בקמצת האישו. משתתפי קמצת הטיפול קבלו 50 מק׳׳ג Natpara, בהזרקה תת עורית מרך פעם ביום, באמצעות מזרק - multidose. טיפול זה ניתן תוך הורדה הדרגתית במינון תוסף הסיק 1-1,25(0H)2D. בחולים שלא השיגו את יעד הטיפול: הפחתה של מינון תוסף הסיק ל-500 מ׳׳ג /יום והפסקת מתן 1,25(0H)2D, ניתן היה להעלות את המינון הטיפולי של Natpara לפי שיקול דעת החוקר, ל-75 ולאחר מכן ל-100 מקג׳/יום לאחר שמעיים ו-4 שבועות מתחילת הטיפול. לאחר 5 שמעות לא ניתן תה לבצע העלאה של המינון הטיפולי של(1-84)rhPTH, אך ניתן היה לבצע הפחתה, עד למינון של 50 מק׳׳ג/יום17. כמו כן ניתן היה לבצע התאמה של מינון תוסף הסידן והמטמליט הפעיל של ויטמק D במטרה למנוע היפרקלציאוריה ולמנוע עלייה מרבי מכפלת רימזי הסיק הזרחן בסרום מעבר לתחום היעד. תוצאות המחקר סוכמו בטבלה מס׳ 1. נצפתה ירידה משמעותית במינון תוסף הסיק בקמצת הטיפול. כמו p היה הבדל משמעותי ב-% החולים שהפסיקו את השימוש במטמליט הפעיל של ויטמק ס והפחיתו במידה ניכרת את מינון תוסף הסידן, ל-<500 מ״ג/יום (42% בקבוצת הטיפול לעומת 2.5% בקמצת האישו)(ראה טבלה 1). בשתי הקמצות נצפתה יתדה בהפרשת הסיק בשתן: (79.4-) מ״ג/24 שעות בקםצת (1-84)rhPTH לעומת (91-) מ״ג/24 שעות בקמצת האישו16. בעת הכללה למחקר חולה אחד בכל אחת מקמצות המחקר התייצג עם מכפלת תכחי סיק זרחן בסדום מעל לתקין 0 55 מ׳׳ג^׳׳ל2), לאחר 24 שבועות טיפול, רק חולה אחד בקמצת האישו הציג ערך זה17׳9. כמו כן נצפתה ירידה ברימז הזרחן בסדום ב-0.48 - מ׳׳ג/ד׳׳ל בממוצע בקמצת הטיפול לעומת 0.04 - מ״גלד״ל בקמצת האישו. לאחר 24 שטעות טיפול נצפתה עלייה בכל מדדי שחלוף
ביבליוגרפיה
- ↑ 1.0 1.1 1.2 Powers J, Joy K, Ruscio A, et al. Prevalence and incidence of hypoparathyroidism in the United States using a large claims database. J Bone Miner Res. 2013;28(12):2570-6.
- ↑ 2.0 2.1 2.2 2.3 Bilezikian JP, Khan A, Potts JT Jr, et al. Hypoparathyroidism in the adult: epide¬miology, diagnosis, pathophysiology, target-organ involvement, treatment, and challenges for future research. J Bone Miner Res. 2011;26(10):2317-37.
- ↑ Pajevic PD, Wein MN, Kronenberg HM. Parathyroid hormone actions on bone and kidney. In: Brand[ ML, Brown EM,editors. Hypoparathyroidism. Milan:Springer; 2015. p. 99-109.
- ↑ 4.0 4.1 4.2 4.3 Shoback D. Clinical practice. Hypoparathyroidism. N Engl J Med. 2008;359(4):391-403.
- ↑ 5.0 5.1 Clarke BL. Epidemiology of hypoparathyroidism. In: Brandi ML, Brown EM, editors, hypoparathyroidism. Milan: Springer; 2015. p. 139-54.
- ↑ Horwitz MJ, Stewart AF. Hypoparathyroidism: is it time for replacement therapy? J Clin Endocrinol Metab. 2008;93(9): 3307-9.
- ↑ Arlt W, Fremerey C, Callies F, et al. Well-being, mood and calcium homeostasis in patients with hypoparathyroidism receiving standard treatment with calcium and vitamin D. Eur J Endocrinol. 2002;146(2):215-22.
- ↑ 8.0 8.1 8.2 8.3 US FDA. FDA briefing document for the September 12,2014 meeting of the Endocrine logic and Metabolic Drugs Advisory Committee. 2014. ttp://www.fda.gov/,
- ↑ D'Amour P. Circulating PTH molecular forms: what we know and what we dont. Kidney Int Suppl. 2006;70(Suppl 102s):S29-33.
- ↑ Isaia G, Marchetti M. PTH and PTH-related peptides. In: Brandi ML, Brown EM, editors. Hypoparathyroidism. Milan: Springer;2015. p. 19-24.
- ↑ Goltzman D, Kara pi is AC. The PTH/vitaminD/FGF23 axis. In: Brandi ML, Brown EM, editors. Hypoparathyroidism. Milan: Springer; 2015. p. 69-79.
- ↑ Goltzman D, Kara pi is AC. The PTH/vitaminD/FGF23 axis. In: Brandi ML, Brown EM, editors. Hypoparathyroidism. Milan: Springer; 2015. p. 69-79.
- ↑ 13.0 13.1 13.2 US FDA. Natpara_ (parathyroid hormone) for injection: US prescribing informa¬tion. 2015. http://www.fda.gov/. Accessed 22 June 2015.
- ↑ Clarke BL, Kay Berg J, Fox J, et al. Pharmacokinetics and pharmacodynamics of subcutaneous recombinant parathyroid hormone (1-84) in patients with hypopara-thyroidism: an openlabel, single-dose, phase I study. Clin Ther. 2014;36(5):722-36
- ↑ 15.0 15.1 15.2 US FDA. Natpara (parathyroid hormone) medical review. 2015.
- ↑ 17. Mannstadt M, Clarke BL, Vokes T, et al. Efficacy and safety of recombinant human parathyroid hormone (1-84) in hypoparathyroidism (REPLACE): a double-blind, placebo-controlled, randomised, phase 3 study. Lancet Diabetes Endocri-nol.2013;1(4):275-B3.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק