מערכת החיסון - Immune system
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| חיסונים בגיל ילדות | ||
|---|---|---|
| ' | ||
| יוצר הערך | ד"ר מיכאל דובלין | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – חיסונים
מהי מערכת החיסון
הקדמה
מערכת חיסון בריאה מסייעת לאדם להגיב במצבי פלישה של מיקרואורגניזמים אלימים שמקורם בדרך כלל מחוץ לגוף, או כאשר קיימת פעילות של תאים סרטניים המיוצרים מדי יום בגוף האדם.
גוף האדם מכיל כ־60 טריליארד תאים, מתוכם 20 מיליארד תאים הם תאי מערכת החיסון.
המערכת החיסונית מוגדרת לעיתים כ"חוש השישי": היא מזהה נגיפים וחיידקים שהמוח אינו מזהה והופכת את המידע למסרים ספציפיים המגיעים למוח ומפעילים את התהליך החיסוני. מערכת החיסון עובדת בשיתוף פעולה עם מערכות הגנה אחרות בגוף. למשל, העור משמש מחסום פיזי בפני חומרים זרים ומערכת הנשימה משתמשת בסילייה (ריסים),ריר ושיעול כדי להיפטר ממזהמים שונים שנשאפו לגוף במהלך הנשימה.
מערכת החיסון היא מכלול מורכב של איברים, תאים ומולקולות, אשר התפתחו במהלך האבולוציה של בעלי-החוליות במטרה להגן על גופם מפני פלישה של מיקרואורגניזמים פתוגניים, כגון חיידקים, נגיפים, פטריות וטפילים שונים, וכן מפני התפתחות סרטן. בין מרכיביה השונים של מערכת החיסון קיימים יחסי גומלין ענפים, המאפשרים להם לפעול בהתאמה נגד פולשים זרים מהם נשקפת סכנה לגוף.
חומר זר או פתוגן המסוגל לעורר את מערכת החיסון, מכונה: אימונוגן. חשיפה של מערכת החיסון לאימונוגן עשויה לגרום לסוגים שונים של תגובה חיסונית, בהתאם למאפייניו הביוכימיים של האימונוגן, אופן חדירתו לגוף וכמותו.
התגובה החיסונית נחלקת לשני שלבים עיקריים, הקשורים זה בזה בקשר הדוק: שלב הכרה ושלב תגובה. ראשיתה של התגובה החיסונית בהכרה, אשר משמעותה זיהוי הפתוגן על ידי מערכת החיסון. מערכת החיסון מסוגלת לזהות באופן ספציפי ומדויק מגוון עצום, כמעט אינסופי, של פתגונים שונים, והיא מצטיינת בכושר הבחנה דק להבדלים מזעריים בין פתוגן אחד למשנהו. לאחר שמערכת החיסון מזהה גורם זר כגון מיקרואורגניזם או פתוגן אחר, בשלב התגובה, היא מפעילה כנגדו תגובה חיסונית תוך גיוס מגוון רחב של תאים ומולקולות, הפועלים יחד במטרה לנטרל את הפולש הזר או לסלקו. תגובה חיסונית זו שבאמצעותה מערכת החיסון מנטרלת או מסלקת את הפתוגן מכונה "תגובה אפקטורית" Effector Response. מערכת החיסון עושה שימוש במנגנונים אפקטוריים רבים ומגוונים, אשר כל אחד מהם מותאם לטיפול בסוג אחר של פתוגן.
מערכת החיסון מסוגלת להבחין בין "עצמי" ל-"זר", כלומר בין מולקולות ותאים השייכים לגוף עצמו לבין מולקולות ותאים ממקור זר, באופן אשר מבטיח כי התגובה החיסונית תופעל אך ורק כנגד גורמים שהם זרים לגוף. הבחנה זו בין "עצמי" ל-"זר" מכונה סבילות חיסונית Immunotolerance, והיא מהווה מנגנון חיוני שתפקידו למנוע גרימת נזק עצמי לגוף. כאשר קיים פגם או ליקוי במנגנון הסבילות החיסונית עלולות להתפתח מחלות אוטואימוניות, בהן מערכת החיסון תוקפת מרכיבים עצמיים של הגוף.
אחד המאפיינים הבולטים והחשובים של מערכת החיסון, לצד יכולתה לזהות במדויק מספר עצום של פתוגנים, הוא הזיכרון החיסוני. חשיפה של מערכת החיסון לגורם זר או לפתוגן עימו היא התמודדה בעבר, מעוררת תגובת זיכרון Memory Response, מתאפיינת במהירות תגובה גבוהה ובעוצמה חזקה לכל פלישה חוזרת של פתוגן. תגובת הזיכרון מאפשרת למערכת החיסון לפעול ביתר נמרצות כנגד הפתוגן, לסלקו ביעילות ולמנוע התפתחות מחלה.
חיסון מולד וחיסון נרכש
מערכת החיסון נחלקת לשתי מערכות משנה: מערכת החיסון המולדת, המכונה גם: חיסון מולד / חסינות מולדת Innate Immunity, ומערכת החיסון הנרכשת, המכונה גם: חיסון נרכש / חסינות נרכשת Acquired Immunity ,Adaptive Immunity. שתי המערכות שונות זו מזו במהותן, אך הן שלובות זו בזו ופועלות בשיתוף פעולה ובתיאום. כל אחת משתי המערכות מפעילה מנגנונים שונים אשר מעוררים, מגבירים ומייעלים את התגובה של המערכת השנייה; יתרה מכך, שתי המערכות תלויות זו בזו: רכיבים שונים של מערכת החיסון המולדת נחוצים לצורך תפקודה היעיל של מערכת החיסון הנרכשת, ולהפך. שילוב זה בין שתי המערכות מאפשרת הגנה מיטבית לגוף מפני פתוגנים.
ניתן לומר כי מערכת החיסון המולדת מהווה את קו ההגנה הראשון של הגוף מפני פתוגנים, מרגע החשיפה לפתוגן ועד שמערכת החיסון הנרכשת נכנסת לפעולה. מנגנוני ההגנה הבלתי-ספציפיים של המערכת המולדת מצליחים, בדרך כלל, לסלק בכוחות עצמם את המיקרואורגניזמים והפולשים הזרים האחרים. מנגנוני החיסון הנרכש נחוצים לייעול התגובה החיסונית, בפרט כאשר מנגנוני ההגנה המולדים אינם אפקטיביים או כאשר פתוגנים מצליחים לחמוק מהם, וכן לצורך יצירת זיכרון חיסוני.
מערכת החיסון המולדת
מערכת החיסון המולדת קיימת באורגניזם החל מן הלידה, ולמעשה אף לפני הלידה, במהלך ההתפתחות העוברית. ככלל, מערכת זו מתאפיינת בכך שרכיביה השונים פועלים באופן בלתי-ספציפי, כלומר כל תא או מולקולה השייכים אליה פועלים כנגד מגוון רחב של פתוגנים, רק על בסיס ההבחנה בין "עצמי" ל-"זר". כמו כן, מערכת החיסון המולדת היא חסרת זיכרון.
- מערכת החיסון המולדת כוללת ארבעה מנגנוני הגנה עיקריים
- מחסומים אנטומיים ופיזיולוגיים המונעים או מעכבים את כניסת הפתוגנים לגוף והתרבותם בתוכו. מחסומים אלה כוללים, בין היתר, את העור והרקמות הריריות שבדרכי הנשימה, מערכת העיכול, אברי המין והעיניים; טמפרטורת הגוף; רמת החומציות הגבוהה בקיבה ובעור (תנאי pH נמוך)
- גורמים ביוכימיים מסיסים, כגון:
- ליזוזים - אנזים הידרוליטי המבקע את שכבת הפפטידוגליקאן Peptidoglycan בדופן התא של חיידקים
- אינטרפרונים - חלבונים ממשפחת הציטוקינים המיוצרים ומופרשים על ידי תאים שהודבקו בנגיף, נקלטים על ידי תאים בריאים הנמצאים בקרבתם, ומשרים בהם מצב אנטי-ויראלי המסייע להם להתגונן מפני הדבקה בנגיף
- מערכת "המשלים" – קבוצה של חלבוני סרום אשר מנטרלים פתוגנים שונים ומסייעים בסילוקם וכן מעורבים בהתפתחות של תגובה דלקתית
- תאים בולעניים (פגוציטים) ותאי הרג טבעיים. הפגוציטים, כדוגמת המקרופאג'ים והנויטרופילים הם תאים המתמחים בבליעה, הרג ועיכול של מיקרואורגניזמים שונים. תאי ההרג הטבעיים הם לימפוציטים גדולים ומגורגרים (granular), הממלאים תפקיד חשוב בהגנה מפני תאים סרטניים ומפני נגיפים מסוימים
- דלקת - תגובה חיסונית מורכבת הנגרמת עקב זיהום או נזק לרקמה, ואשר כרוכה בגיוס מגוון תאים ומולקולות של מערכת החיסון אל אתר הזיהום
מערכת החיסון הנרכשת
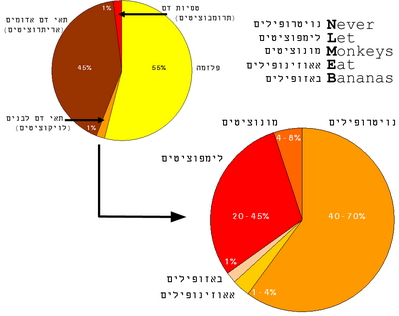
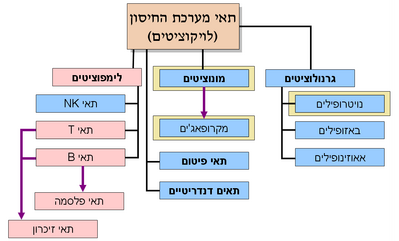
תא דם לבן או לויקוציט הוא תא דם השייך למערכת החיסון, כלומר רכיב בדם המשתתף - באופן פעיל או סביל - בהגנת גופנו מפני פולשים ומזיקים (פתוגנים). המערכת מורכבת מתאי דם לבנים המתפלגים למספר קבוצות על פי תפקיד מוגדר של כל תא דם לבן. המערכת מתפתחת עם שנות חיינו ומתאימה את עצמה לחשיפות שונות לחיידקים ווירוסים באמצעים שיפורטו בהמשך. בליטר דם של מבוגר בריא יש 4x109 עד 11x109 תאי דם לבנים. תאי דם לבנים נמצאים גם במערכת הלימפה וברקמות מיוחדות.
- מערכת החיסון המולדת (Innate immune system)
- גרנולציטים המכילים אברונים מגורגרים בציטופלסמה שלהם. שלושה סוגי תאים בקבוצה זו:
- נויטרופילים
- אאוזינופילים
- באזופילים
- מונוציטים המתמיינים ל:
- מאקרופאג'ים
- מערכת החיסון הלומדת (Adaptive immune system)
מערכת החיסון הנרכשת מתפתחת במהלך חיי האורגניזם עקב חשיפתו לפתוגנים, והיא מיוחדת בכך שרכיביה פועלים באופן בררני וספציפי: כל תא או מולקולה המשתייכים אליה מסוגלים לפעול כנגד פתוגן מסוים אחד ויחיד. לכן, בניגוד לתגובה החיסונית המולדת, שהיא זהה באופן עקרוני בקרב כל הפרטים המשתייכים למין מסוים, התגובה החיסונית הנרכשת משתנה מפרט אחד באוכלוסייה למשנהו בהתאם לניסיון האישי שרכש, כלומר בהתאם לפתגונים אליהם נחשף במהלך חייו. מאפיין מרכזי נוסף המייחד את מערכת החיסון הנרכשת הוא היכולת לייצר זיכרון חיסוני. מערכת החיסון הנרכשת כוללת את הלימפוציטים מהסוגים B ו-T ואת הנוגדנים.
- הזרועות האפקטוריות של מערכת החיסון
נהוג לחלק את מנגנוני התגובה החיסונית, כלומר המנגנונים האפקטוריים, לשתי זרועות: זרוע הוּמורָאלית וזרוע תאית. כל אחת משתי הזרועות כוללת הן מרכיבים במערכת החיסון המולדת (בלתי-ספציפיים) והן מרכיבים במערכת החיסון הנרכשת (ספציפיים). שתי הזרועות פועלות בשיתוף פעולה ובוויסות הדדי. א. הזרוע ההומוראלית - The Humoral Branch (הומוראלי = של נוזלי הגוף) מכונה גם תגובה הומוראלית Humoral Response או חסינות הומוראלית Humoral Immunity מקנה הגנה בעיקר מפני מיקרואורגניזמים ופתוגנים חוץ-תאיים, אשר גדלים ומתרבים מחוץ לתאי המאכסן, בנוזלי הגוף. הזרוע ההומוראלית כוללת שני מרכיבים עיקריים:
- נוגדנים - גליקופרוטאינים המופרשים על ידי תאי פלסמה, שמוצאם בהתמיינות לימפוציטים מסוג B. הנוגדנים מזהים מרכיב ספציפי על גבי אנטיגן, נקשרים אליו ומסייעים בנטרולו ובסילוקו.
- מערכת "המשלים".
ב. הזרוע התאית - The Cellular Branch : המכונה גם תגובה תאית Cell-Mediated Response או חסינות תאית Cellular Immunity, מספקת הגנה בעיקר מפני מיקרואורגניזמים ופתוגנים תוך- תאיים, אשר פולשים לתוך תאי המאכסן ומתרבים בתוכם, כגון: נגיפים (וירוסים), חיידקים תוך-תאיים, פרוטוזואה וכיוצא בזה. כמו כן היא פועלת לחיסול תאים סרטניים ותאים שמקורם ברקמת שתל זרה. תפקיד מרכזי נוסף של הזרוע התאית הוא להפעיל ולווסת את התגובה ההומוראלית, ובפרט לשפעל לימפוציטים מסוג B שבאו במגע עם אנטיגן, ולגרום להם להתחלק ולהתמיין לתאי פלסמה מפרישי נוגדנים אשר מתאימים באופן ספציפי לאנטיגן זה. הזרוע התאית כוללת מספר מרכיבים:
- לימפוציטים מסוג T, אשר נחלקים לשני סוגים עיקריים:
1. תאי T מסייעים, המסומנים בראשי תיבות: Th. 2. תאי T רעילי-תא או תאי T ציטוטוקסיים, המסומנים בראשי תיבות: Tc או CTL.
- תאי הרג טבעיים (ר' לעיל).
- תאים בולעניים (פגוציטים) מסוגים שונים, ובתוכם: מונוציטים, מקרופאג'ים, נויטרופילים ואאוזינופילים.
- באזופילים ותאי פיטום.
תאי T
תת אוכלוסיות של תאי T ישנם מספר סוגים של תאי T בוגרים:
- תאי T ציטוטוקסיים או ציטוליטיים (מסומנים CTL או +CD8). תאים אלו הורגים תאי גוף הנגועים בנגיף או תאים שעברו התמרה סרטנית. תאי המטרה מזוהים בזכות קומפלקס MHC מסוג 1 שהם מציגים. כתוצאה מהאינטראקציה שבין קומפלקס MHC לקולטן תאי T מחדירים תאי T ציטוטוקסיים, לתא הנגוע חומרים רעילים כגון פרפורין (Perforin) וגרנזים (Granzyme B). תאי ה CD8 בגופנו מתחלקים לשתי אוכלוסיות עיקריות - תאים נאיביים ותאי זיכרון. התאים הנאיביים הם אלו אשר טרם נתקלו באנטיגן, נגדו הם אמורים להגיב, ותאי הזיכרון הם התאים אשר נתקלו כבר בעבר פעם אחת או יותר באנטיגן נגדו הם מכוונים. קיימים חלבונים ממברנליים וציטופלסמטיים אשר מאפשרים להבחין בין שתי אוכלוסיות אלו, הנבדלות במידת הטוקסיות שלהן ובמיקומן בגוף.
- תאי T מסייעים (Helper T cells, מסומנים +CD4). תאים אלו מפרישים ציטוקינים הגורמים לגיוס אלמנטים שונים למאבק בפתוגן. תאים אלו מופעלים כתוצאה מאינטראקציה עם תאים מציגי אנטיגן מקצועיים כגון תאי B, מקרופאג'ים ותאים דנטריטיים. האינטראקציה נוצרת כתוצאה ממגע בין קומפלקס MHC מסוג 2, הנמצא על התאים המציגים, לבין קולטן תאי T הנמצא על תאי T.
תאי T מסייעים:
תא T מתקשר עם חלבוני MHC מסוג II תא T מתקשר עם חלבוני MHC מסוג I
ישנם שני סוגים של תאי T מסייעים:
- תאי T מסוג 1 (Th1)- אחראיים בעיקר לתגובה החיסונית התאית, כלומר מכוונת את מערכת החיסון כנגד נגיפים ותאים סרטניים. כתוצאה או באמצעות מהפרשת הציטוקינים כגון Il-2, אינטרפרון גמא, וTNF מתרבים ומופעלים תאי T ציטוטוקסיים, מקרופאג'ים ונויטרופילים, כמו כן מופרשים מתאי B נוגדנים מסוג IgG2a.
- תאי T מסוג 2 (Th2)- אחראיים בעיקר לתגובה ההומורלית (הקשורה לדם), כלומר מכוונת נגד זיהום של חיידקים, רעלנים או טפילים שחדרו למערכת הדם או לנוזל הבין-תאי. כתוצאה מהפרשת ציטוקינים כגון Il-2, Il-5, Il-6 iL10, ו-TGF בטא מתרבים ומופעלים תאי B המייצרים נוגדנים מסוג IgA, IgE, IgM וIgG-1. מתרבים ומופעלים תאי דם מסוג אאוזינופילים ותאי פיטום.
תאי NK תאי NK (ראשי תיבות של Natural Killer, "מחסל טבעי", באנגלית) הם תאים השייכים למערכת החיסון, אשר תפקידם העיקרי הוא חיסול תאי גוף שנדבקו בנגיפים או שהתפתחו לתאים סרטניים. בניגוד לחלק מתאי הדם הלבנים האחרים, תאי NK אינם נלחמים, אם כן, ישירות נגד פתוגנים. תאי NK נחשבים ללימפוציטים, אך בניגוד לתאי B ותאי T הם אינם משתייכים למערכת החיסון הלומדת (או הנרכשת), אלא למערכת החיסון המולדת. פירוש הדבר הוא שלתאי NK אין יכולת להילחם בפתוגנים ספציפיים (או בתאים שנדבקו בפתוגנים ספציפיים); הם תוקפים ללא הבחנה כל תא שהודבק בנגיף או שהפך לתא סרטני. הסיבה להיותם משויכים ללימפוציטים היא מוצאם - לתאי NK, תאי T ותאי B תא-הורה משותף במח העצם. תאי NK נודדים למקום הזיהום בשל משיכה כימית ( כימוטקטי )- הם קולטים חלבונים קטנים הנקראים ציטוקינים והמופרשים על ידי מקרופאג'ים לאחר היתקלות בפתוגנים. תאי NK נצמדים לתאי גוף הנגועים בנגיף ומפרישים אנזימים מעכלים וחלבונים אחרים - במיוחד פרפורין (Perforin, מהמילה האנגלית Perforate, "לעשות חור"), אשר מנקב חורים בממברנת התא וגורם בכך למותו המהיר של התא.
תאים בלעניים (פגוציטים) פגוציט (בעברית: תא בלען) הוא תא הקולט לתוך הציטופלסמה שלו חלקיקים מסביבתו. פגוציטוזה היא צורה של אנדוציטוזה, שבה החלקיק החודר לתא הוא גדול במיוחד. כך נקרא התהליך שבו אמבות ויצורים חד-תאיים אחרים בולעים חלקיקי מזון שאינם מסוגלים לעבור דרך ממברנת התא הבררנית, וכן התהליך שבו הפגוציטים, המשתייכים למערכת החיסון, בולעים פתוגנים וגורמים מזהמים. במערכת החיסון של האדם ישנם שלושה סוגים של תאי דם לבנים המשמשים כפגוציטים:
- מונוציטים: נמצאים בעיקר בדם.
- מקרופאג'ים: אלו הם מונוציטים שעברו התמיינות קלה; הם נמצאים בעיקר ברקמות.
- נויטרופילים: גרנולוציטים המהווים את חלק הארי של תאי הדם הלבנים.
למרות שגם תאים דנדריטיים בולעים פתוגנים, הם אינם נחשבים בדרך-כלל לפגוציטים. בליעת פתוגנים על ידי פגוציטים, וכן בליעת מזון על ידי אמבות, מתרחשת באופן הבא:
- הפגוציט שולח שלוחות ציטופלסמיות אל עבר הפתוגן (אותו הוא מזהה באמצעות מולקולות סוכר הנמצאות על-גבי ממברנת תא הפתוגן).
- השלוחות נדבקות אל הפתוגן ומושכות אותו לעבר תא הפגוציט.
- ציטופלסמת הפגוציט סוגרת אט-אט על הפתוגן ועוטפת אותו מכל הכיוונים. נוצרת בועית, המכילה את הפתוגן בתוכה והנקראה פגוזום.
- ליזוזום הנמצא בציטופלסמת הפגוציט מתלכד עם הפגוזום ליצירת פגוליזוזום.
- הליזוזום משחרר את תוכנו: אנזימים מעכלים הגורמים להרס ופירוק הפתוגן.
- שרידי הפתוגן נפלטים מהפגוציט באמצעות אקסוציטוזה (התלכדות הדרגתית של הבועית המכילה את השרידים עם ממברנת התא, עד להשתלבות מלאה של הבועית בממברנה ופליטת תוכנה אל מחוץ לתא).
שתי מערכות החיסון, המולדת והנרכשת, עושות שימוש ברכיבים מן הזרוע ההומוראלית ומן הזרוע התאית. כך, המערכת המולדת כוללת את הפגוציטים השונים, תאי ההרג הטבעיים וכן את מערכת "המשלים". המערכת הנרכשת כוללת את הנוגדנים ואת הלימפוציטים מסוגים B ו-T. יצוין כי תאי ההרג הטבעיים, מערכת "המשלים" וחלק מהפאגוציטים, אשר משתייכים באופן עקרוני למערכת המולדת, הבלתי-ספציפית, פועלים לעיתים באופן ספציפי במנגנון מיוחד אשר נקרא: "הרעלת תאים תלויית נוגדנים" Antibody-Dependent Cell-Mediated Cytotoxicity, ובר"ת ADCC. במנגנון זה נוגדנים מזהים באופן ספציפי תאי מטרה, ומסמנים אותם כיעד לחיסול בידי תאי הרג טבעיים, מערכת "המשלים" ופגוציטים מסוימים.
תיאום התגובה החיסונית הפעלת תגובה חיסונית אפקטיבית, המשלבת תאים ומרכיבים רבים ושונים מצריכה תיאום מורכב בין מערכת החיסון המולדת למערכת הנרכשת, ובין הזרוע ההומוראלית לזרוע התאית. תיאום זה מתבצע בעיקר בידי קבוצה של חלבונים המכונים: ציטוקינים. הציטוקינים הם חלבונים בעלי משקל מולקולארי נמוך, המופרשים על ידי תאי דם לבנים (לויקוציטים) ותאים אחרים בגוף בתגובה לגירויים שונים. הם משמשים כמעין שליחים המעבירים מסרים בין תאיה השונים של מערכת החיסון וכן בין מערכת החיסון ליתר תאי הגוף, ובכך הם מסייעים לויסות התגובה החיסונית ולהסדרתה. מערכת החיסון המולדת מעוררת ומכווינה את תגובות מערכת החיסון הנרכשת בעיקר על ידי הפרשת ציטוקינים מתאימים והצגת אנטיגנים Antigen Presentation לתאי T מסייעים (Th) על ידי תאים מציגי-אנטיגן. תאים מציגי-אנטיגן (תאים דנדריטיים, מקרופאג'ים ולימפוציטים מסוג B) בולעים אנטיגן בתהליך של אנדוציטוזה או פגוציטוזה, ולאחר מכן מציגים על שטח פני הממברנה שלהם מקטעים פפטידיים של האנטיגן על-גבי על מולקולות MHC מטיפוס II. תאי T-המסייעים מזהים באמצעות קולטן תא ה-T שלהם (TCR) קומפלקסים אלה של אנטיגן הנישא על-גבי מולקולת MHC מטיפוס II, ובאמצעות סיגנל מעורר נוסף הניתן על ידי התא מציג-האנטיגן, הם עוברים שפעול ומסוגלים להתרבות ולגייס מגוון של תאים ומולקולות לתגובה חיסונית כנגד האנטיגן.
מערכת החיסון הנרכשת מייצרת אף היא מסרים אשר מעוררים ומגבירים את יעילות התגובה המולדת. כך, למשל, לאחר שתאי T מסייעים מזהים אנטיגן המוצג על-גבי מולקולת MHC מטיפוס II, הם מייצרים ומפרישים ציטוקינים אשר משפרים את יכולתם של המקרופג'ים לבלוע ולהרוג אנטיגנים, ובנוסף לכך הם מגבירים את ביטוי מולקולות ה-MHC מטיפוס II על פני הממברנות של המקרופג'ים, ובכך הופכים אותם לתאים מציגי-אנטיגן יעילים יותר. דוגמה נוספת היא הגיוס וההפעלה של מערכת "המשלים" על ידי נוגדנים: נוגדנים שיוצרו והופרשו על ידי תאי פלסמה כנגד פתוגן מסוים, נקשרים אל הפתוגן ומצפים אותו, ובכך מסמנים אותו כמטרה להתקפה מצד מערכת "המשלים". B יוצרי הנוגדנים והזיכרון החיסוני – תאי ה
תא לימפוציט
B מסוג
תאי T (בכחול) תוקפים תא חשוד
הנגיפים נגיף (בלועזית: וירוס, Virus; מלטינית: "רעל") הוא גופיף הפולש לתאים אחרים ואשר לעיתים קרובות גורם למחלות. הנגיף הוא טפיל אובליגטורי שאינו יכול להתרבות ללא נשא חי. הנגיפים היו ידועים עוד לפני המצאת מיקרוסקופ האלקטרונים אך מדענים חשבו אותם לרעלן שיוצרים החיידקים, ומכאן שמם. במאה ה-20 החלו להצטבר עדויות לכך שנגיפים אינם חלק מחיידקים אלא יכולים להתקיפם, להתרבות בתוכם ואף לגרום למות החיידק. נגיפים מהסוג התוקף חיידקים כונו בקטריופאג'ים. למעשה נגיף איננו חי אלא חלקיק שעשוי כולו חומצת גרעין DNA או RNA, עטוף במעטפת חלבונית או במעטפת של שומנים. גודלם של הוירוסים הוא בין 0.00001 מ"מ ל 0.00005 מ"מ. צורתם של הנגיפים איננה אחידה, חלקם מקלוניים, כדוריים, סגלגלים או בעלי פאות. הנגיפים נטפלים ומזיקים לאדם, חיות, צמחים ואף לחיידקים. הנגיף איננו פעיל כל עוד איננו צמוד לתא חי או צומח. מרגע שנצמד לתא כזה הוא פורץ לתוכו דרך הדופן או לפחות מחדיר לתוכו את חומצת הגרעין שלו. בשלב זה משתלט הנגיף על מנגנון ההתרבות של התא ומשדר וגורם לו לייצר חומצת גרעין וחלבון זהים לאלו של הנגיף, וכך נוצרים נגיפים חדשים הפורצים החוצה מן התא, תוך שהם הורסים אותו, ונצמדים לתאים נוספים. ניתן להשמיד נגיפים על ידי חימום לטמפרטורה של 60 מעלות בלבד, וכן על ידי חשיפתם לחומרים כמו פורמלין או כלור, אך עם זאת הם עמידים לחלוטין בפני אנטיביוטיקה. כשהם מוקפאים הם בעלי יכולת בלתי מוגבלת להמשיך להתקיים עד להפשרתם.
בפני מפתחי תרופות נגד נגיפים ניצב הקושי להשמיד את הנגיף בלי לפגוע בתא החי עצמו, בשל החיבור הסימביוטי בין הנגיף לבין מערכת ההתרבות של התא שיוצר מעין ישות חיה חדשה.
ברוב המקרים חשיפה לזיהום נגיפי והחלמה ממנו יוצרת חיסון נגד אותו סוג נגיף. הבעיה היא שהנגיף משנה את תכונותיו על ידי מוטציות רבות ומהירות, מולן אין החיסון הקיים מספק.
וויריון הוא חלק או שבר של נגיף המסוגל אף הוא להדביק באופן עצמאי תאים אחרים. יש נגיפים של צמחים כדוגמת נגיף מוזיאקת הטבק. ישנם גם נגיפים הפוגעים בבעלי חיים, היותר מוכרים לאדם כמחוללי מחלות השפעת, אבעבועות רוח ועוד. כל נגיף שאינו מצוי בתא חי, צמחי או חיידקי, נחשב כחלקיק דומם חסר תכונות המוגדרות כחיים - יכולת התרבות, צריכת אנרגיה ויצירתה, תנועה, גדילה או תגובה. גם בעלי חיים סובלים ממחלות הנגרמות על ידי נגיפים, למשל מחלת הפה והטלפיים, כלבת, איידס של חתולים ועוד. לנגיף, כאמור, אין יכולת תנועה משלו, רק התנגשות מקרית עם קרום תא חי (ממברנה) מאפשרת את ספיחת הנגיף וחדירתו לתא. מכאן ואילך מתחיל הנגיף בפעולות דמויות חיים של סינתוז חלבונים מיוחדים ומרכיבי נגיפים חדשים, המתחברים בסוף התהליך ליצירת נגיפים חדשים המכונים ויריונים. הנגיף הופך את התא המודבק למעין "מפעל יצור", הפועל בעיקר לשם יצירת ויריונים חדשים, ומשתמש בחומר הגנטי של התא המודבק ותרכובות המצויות בתוכו ליצירתם.
הנגיפים בנויים ברובם מחומצת גרעין - דנ"א או רנ"א - שמוקפת מעטפת חלבונית בשם קפסיד עליה מצויים חלבונים המאפשרים הצמדות לקרום התא. חומצת הגרעין בתוך הקפסיד יכולה להופיע כמעגלית או קווית. הנגיף הוא היצור היחיד המוכר למדע שיכול להכיל רנ"א במקום דנ"א בתור חומר גנטי, מה שהופך אותו לרטרו וירוס - נגיף ה-HIV הגורם לאיידס הוא אחד הידועים לשמצה מסוג הוירוסים הללו.
לרוב הנגיפים קיימת יכולת מעניינת ביצירת אינטרפרון במאכסן - דבר הגורם לבסוף למות הווירוס ולהעלמות המחלה זאת אומרת שמרוב המחלות שנגרמות מנגיפים - נרפאים לבד ללא כל טיפול. קיימות מחלות ילדים רבות כמו אדמת המאופיינות בכך שלאחר שנדבקים בהן הגוף מתחסן ובדרך כלל אין נדבקים בהן שנית משום שהגוף מפתח נוגדנים שמקנים חסינות. היום מחסנים את התינוקות כנגד רוב מחלות הילדים הנגרמות מנגיפים כי בגיל מבוגר מחלות הילדים עלולות להיות הרבה יותר חריפות ועלולות לגרום לסיבוכים. כ־30 אחוזים מהילדים הנדבקים ממחלות ילדים נגיפיות אינם מראים כל סימני מחלה אבל הם מתחסנים. את התרכיבים מכינים מנגיף מוחלש או מנגיף מומת. חלק מהמחלות הנגרמות על ידי נגיפים הן מחלות עונתיות. לדוגמה, בחורף נפוצים נגיפים של מערכת הנשימה כמו שפעת RSV נגיף הפארהאינפלואנזה ועוד. בקיץ, למשל, נפוצים נגיפי המעיים שעלולים לגרום לדלקת קרום המוח הנגיפית. גם כנגד מחלות אלו מחסנים את רוב האוכלוסייה וזאת בשל הסיבוכים המופיעים ממחלות אלו ובשל הנזק הכלכלי הגדול שמחלות אלו גוררות אחריהן.
המחלות הוויראליות אשר תוקפות את העובר האנושי כגון וירוס האדמת היו בראש סדר העדיפויות לחיסון כלל עולמי. רוב אוכלוסיית העולם מחוסנת כנגד ווירוס זה.
נגיף ההרפס (שלבקת) הוא הנגיף הראשון שבודד בתרביות רקמה והוא נגיף מעניין במיוחד כי הוא נמצא בגוף בצורה רדומה ומתפרץ אצל אנשים שונים כל פעם מחדש - במיוחד אחרי מחלת חום כלשהי, חשיפה לשמש, וסת אצל נשים ואפילו מועקה נפשית. הרפס זוסטר שהוא אחד מבני משפחת ההרפס אחראי למחלת אבעבועות רוח. מנסים לחסן את כל אוכלוסיית הילדים בפני וירוס זה.
החיידקים
חיידקים (Bacteria) הם יצורים חד-תאיים המהווים ממלכת-על בפרוקריוטיים, לצד ממלכת החיידקים הקדומים.
בעבר נקראו ממלכות החיידקים האמיתיים והחיידקים הקדומים בשם הכולל מוֹנֵרָה או מונירה, (Monera). עד לפני כמה עשרות שנים סווג חלק מהחיידקים כצמחים, חלק כפטריות וחלק כאצות, וממלכת החיידקים לא הייתה קיימת.
התגלית שהביאה לסיווגם של החיידקים כיצורים נפרדים מהווה את ההבדל הבסיסי ביותר בין חיידקים ובין שאר היצורים: כל החיידקים (אמיתיים וקדומים) הם פרוקריוטיים (חסרי גרעין), ואילו כל היצורים האחרים הם אוקריוטיים (בעלי גרעין).
רוב החיידקים מקיימים בעצמם תהליכי חיים עצמאיים ומתרבים על ידי חלוקה בינארית. הזמן שעובר בין רגע יצירת החיידק לרגע חלוקתו נקרא זמן דור. בתנאים מבחנה אופטימליים של חום ואנרגיה מתחלקים חיידקי מעיים מסוימים בכל 20 דקות. החיידקים ניזונים מהסביבה, מפרישים לסביבה ובדרך כלל, בניגוד לנגיפים, אינם זקוקים למאכסן, כך שאינם מתקיימים כטפילים).
בניגוד לדעה הרווחת שכל החיידקים גורמי מחלות, רק מיעוט מתוך מאות אלפי סוגי החיידקים הוא פתוגני הגורם מחלות וסוגים רבים של חיידקים אף מועילים וחיוניים לבריאות.
בניגוד לתאיהם של בעלי חיים ובדומה לתאים צמחיים, לתאיהם של רוב החיידקים יש דופן תא. החיידקים סווגו בעבר לשתי קבוצות לפי סוג הדופן שלהם. בשל קיום הדופן בחיידקים והיעדרה בתאי האדם, משמשת הדופן כמטרה של הרבה סוגי אנטיביוטיקה, כגון פניצילינים וצפלוספורינים.
החיידקים, שמספרם על-גבי כדור הארץ עולה על זה של כל שאר היצורים גם יחד, מגוונים וסתגלנים הרבה יותר ממה שמסוגל האדם להעלות על דעתו: החל מחיידקים החיים בים המלח, עבור בחיידקים העמידים לקרינה, וכלה בחיידקים אשר חיים בטמפרטורות גבוהות ביותר (למעלה מ-50 חיידקים חובבי חום, המכונים תרמופילים, נמצאו משגשגים בטמפרטורות גבוהות מאוד במקומות דוגמת מעיינות מים חמים או בזרמים תת-ימיים חמים. חלק ממינים אלה, המכונים היפרתרמופילים, מתרבים בצורה אידיאלית מעל 100 מעלות צלזיוס, ויכולים לשרוד בטמפרטורה של עד 121 מעלות צלזיוס). חיידקים הם יצורים מיקרוסקופים חד תאיים.
חיידקי סטרפטוקוקוקס
החיים בודדים או במושבות. חיידקים נמצאים בכל מקום על פני כדור הארץ בכמויות אדירות. בתוך גופנו הבריא היחס בין החיידקים לתאים הוא 9 ל - 1 לטובת החיידקים. אפשר למצוא חיידקים באוויר, במים, באדמה, במעיינות גפרית, במעיינות מים רותחים, אפילו בים המלח) נמצא חיידקים. החיידקים הם חלק מהמערכת האקולוגית בה אנו חיים. חיידקים הם שותפים חשובים בתהליכים המתרחשים במערכות אקולוגיות, ביניהם:
- חיידקים המפרקים תרכובות אורגניות. חיידקים הקושרים חנקן מהאוויר, חיידקים המייצרים ויטמינים בתוך גופנו, חיידקים המייצרים תרכובות אורגניות, ועוד…
מעט מהחיידקים שייכים לקבוצת קטנה של חיידקים המכונים פתוגנים (פגעניים), חיידקים אלו גורמים למחלות באדם וביצורים אחרים, ויכולים בהחלט לפגוע בשגרת חיינו, למשל חיידקי הדבר, השחפת או העגבת.
גידול חיידקים מהו גידול אצל חיידקים? חיידק קולט חומרים מהסביבה, משתמש בהם להפקת אנרגיה ולבנייה. הוא גדל בנפח ובמסה, ואז מכפיל את הדנ"א שלו ומתחלק לשני תאי חיידקים. כך גדלה אוכלוסיית החיידקים. לשם מה לגדל חיידקים במעבדה?
- כדי לאבחן איזה סוג חיידק גרם למחלה.
- כדי לאבחן איזה סוג חיידק חדר למים או לחומוס וזיהם אותם.
- כדי להשתמש בחיידקים לצורכי האדם (דישון בחקלאות, פירוק כתמי נפט בים, ייצור חלבונים בהנדסה גנטית).
- כדי לבדוק כיצד תרופות כמו אנטיביוטיקה וחומרים אחרים משפיעים על גידולם של החיידקים.
כדי לזהות חיידק יש לגדלו בתרבית.
כדי שהחיידק יגדל יש לספק לו את כל צרכיו. כאשר רוצים להרבות חיידק לצורכי מחקר או בתעשייה ביו טכנולוגית להפקת חומרים שונים (לדוגמה: ייצור יוגורט), צריך להכיר את צרכיו ולספק לו את כולם בצורה מיטבית, כך מפיקים את מרב התוצרים מהחיידק. עקום גידול חיידקים כדי ללמוד על גידול חיידקים נשתמש בחיידק E. coli. חיידק E.coli גדל, ומתחלק כל 20 דקות בתנאים מיטביים. כאשר נותנים לחיידק מסוג E.coli את התנאים המיטביים, סוגרים בכלי ומאפשרים לו להתרבות מתקבל עקום גידול אופייני לאוכלוסיות:
עקום גידול חיידקים
תרשים של עקום גידול החיידקים מסוג קולי.
בעקום הגידול ארבעה שלבים עיקרים: 1. שלב ההשהיה- החיידקים "מסתגלים" למצע, מסנתזים את החומרים, גדֵלים, אך עדיין לא מתרבים. 2. שלב הגידול הלוגרתמי (המאריכי) - קצב גידול מהיר, התנאים טובים, יש מזון, חמצן, עדיין אין כמויות גדולות של פסולת, ובכל 20 דקות מוכפלת האוכלוסייה. 3. שלב הגידול היציב - התנאים הולכים ומשתנים, נגמר מזון וחמצן. 4. שלב המוות - התנאים הופכים גרועים, המזון נגמר וכמות הפסולת עולה, קצב התמותה גדול מקצב ההתרבות. החיידקים מתים.
מחזור חומרים בטבע לחיידקים מקום חשוב ביותר במחזור חומרים. יש לזכור כי מלאי החומרים בכדור הארץ מוגבל, ואין כניסת חומרים חדשים (מלבד מטאורים). החיידקים הם חלק מקבוצת אורגניזמים שמאפשרים פירוק החומרים והפיכתם לחומרים זמינים לתהליכים אחרים. לדוגמה, מחזור החנקן: החנקן הוא גז שנמצא באטמוספירה בריכוז של כ־80%, הוא הכרחי לבניית חלבונים, ואולם החיידקים הם היחידים שיכולים להפוך חנקן אטמוספירי לחנקן זמין לצמחים לבניית חלבונים. (גם בתעשייה כימית אפשר ליצר תרכובות חנקן זמינות, דשנים, אך זהו ייצור יקר יחסית). פירוק אורגניזמים לאחר מותם נעשה בחלקו הגדול בידי חיידקים.
מתוך הספר פרקים באקולוגיה מאת רות אמיר. חיידקים בשירות האדם
- שימוש בחיידקים לפירוק פסולת ביוב באגני חמצון, בהכנת דשנים אורגנים, בדישון חנקני בשדות (מרבים חיידקים קושרי חנקן ומפזרים אותם בשדה להעשרת הקרקע) ואפילו בפירוק כתמי נפט בים.
- הכנת מזונות - בהכנת ירקות ופירות כבושים ("חמוצים"), מוצרי חלב, יין (פטריות חד תאיות- שמרים).
- בהנדסה גנטית- יצור חלבונים או הורמונים באמצעות החיידק.
- ייצור חומרים אנטיביוטים באמצעות חיידקים המפרישים אותם.
הפלורה הטבעית
- חיידקים החיים בגופנו מייצרים ומספקים לנו ויטמינים שונים. לדוגמה חיידקים
המייצרים ויטמין B או ויטמין K.
- חיידקים החיים במערכת העיכול של מעלי גֵרה, מפרקים את התאית לחד סוכר
ומאפשרים למעלי הגרה לנצל את האנרגיה הגלומה בה.
- חיידקים ה"גרים" בפתחי הגוף אינם גורמים לנזק, ואינם מאפשרים
למיקרואורגניזמים גורמי מחלות להתיישב בפתחים או לחדור לגופנו (לדוגמה בפה, בעור ובנרתיק האישה). חיידקים גורמי מחלות חיידקים גורמי מחלות יכולים להיות בעלי חלק (או כל) התכונות האלה:
- יכולת חדירה לגוף- דרך דרכי הנשימה, או עם המזון למערכת העיכול.
- תוספת מבנה – לדוגמה קופסית או יכולת הפיכה לנבג שמגינה בפני התאים הבלעניים.
- שוטונים או ריסים המאפשרים תנועה מהירה בנוזלים.
- חיידקים מפרישים אנזימים מפרקי חלבונים או מפרקי שומנים המאפשרים להם לפרק רקמות ולחדור לרקמות שונות בגוף, לדוגמה למחזור הדם.
- הפרשת רעלים - חיידקים המפרישים רעלים שונים וגורמים לנזקים קשים.
- החיסונים שעליהם יסופר בפרקים הבאים מטרתם להתמודד עם כל אותם חיידקים שפגיעתם קשה מאוד ולנסות ולמנוע מחלות באמצאות שימוש מושכל במערכת החיסון הנרכשת בשילוב עם טכנולוגיות חדישות שיבטיחו לנו מירב הגנה עם מינימום תופעות לוואי מהחיסון.
הצטננות והפצת הווירוסים
דרכי הפצת הנגיפים
דרכי הפצה והדבקה עי חיידקים ווירוסים דיירי לוע
פרק 2 : חיסונים
חיסון – הקדמה
החיסון הוא אמצעי ריפוי מונע, כלומר, מטפל בגורמים מזיקים לבריאות כמו נגיפים ומחלות שונות לפני שהם מספיקים לפגוע בגוף. בגוף האדם פועלת המערכת החיסונית, שלאורך חיי האדם נתקלת בגורמים שונים ולומדת "לזהות" אותם ולסווגם כמזיקים, או לא מזיקים. כשהגוף מזהה גורם מזיק הוא מפתח נוגדנים, אמצעי ביולוגי עם יכולת התמודדות עם מחלות. עבור כל גורם מיוצרים נוגדנים ספציפיים לטיפול בו. מרבית החיסונים פועלים באמצעות הכנסה של הגורם המזיק (אנטיגן) בגרסה מוחלשת, או מומתת, אל הגוף, מתוך כוונה שהמערכת החיסונית "תלמד" אותו ותייצר עבורו נוגדנים, תחסל אותו, ותייצר תאי זיכרון ייחודיים לו. הגרסה המוחלשת הזאת על פי רוב לא גורמת להופעת המחלה כלל, ולעיתים מופיעים רק סימפטומים מוחלשים שלא משתווים בנזקם לזה של התפרצות מלאה של המחלה. חיסון מסוג זה נקרא חיסון פעיל. בחיסון סביל, לעומת זאת, מחדירים אל הגוף נוגדנים באופן ישיר; חיסון כזה מתבצע כשיש צורך לטפל באופן מיידי בזיהום חמור; במצב כזה הזמן יקר ולא ניתן לחכות עד שהגוף ייצר בעצמו נוגדנים, כפי שמתרחש בחיסון פעיל.
חיסונים הם הדרך הבטוחה ביותר למנוע מחלות זיהומיות ואת נזקיהן. בישראל, כמו בכל העולם, נהוגה שגרת חיסונים הכוללת חיסונים נגד רוב המחלות המידבקות הרלוונטיות.
קיימים שני סוגי חיסונים: חיסון פעיל וחיסון סביל. בחיסון פעיל מזריקים (או נותנים דרך הפה) נגיף, חיידק או רעלן המיוצר על ידיהם, ומערכת החיסון מייצרת נוגדנים נגד החומר שניתן. לעיתים קרובות נותנים חיסון עם חיידקים או נגיפים חיים כשהם מוחלשים ואינם מסוגלים לגרום נזק בילד או במבוגר שאינם סובלים מדיכוי של מערכת החיסון. לדוגמה, חיסון נגד שיתוק ילדים מסוג Sabin הוא חיסון עם נגיף חי מוחלש הניתן דרך הפה. בחיסון נגד טטנוס נותנים את הרעלן שמייצר חיידק הקלוסטרידיום טטני ומערכת החיסון מייצרת נוגדנים נגד הרעלן. חלק מהחיסונים ניתן לתת פעם אחת, אך חלק גדול מהחיסונים יש לתת מספר פעמים כדי שמערכת החיסון תייצר חיסון יעיל.
בחיסון סביל אנו מזריקים לגוף את הנוגדנים הספציפיים כנגד אותה מחלה. החיסון הזה אינו מגרה את מערכת החיסון לתגובה חיסונית ארוכת טווח ויעילותו של חיסון זה פגה תוך תקופה קצרה יחסית – כ 120 יום
תגובת הגוף להזרקת חיסונים
מגיפות בראי ההיסטוריה - מבט מקוצר על 5000 שנים של תחלואה אנושית
הקדמה מה פירוש המילה מגפה - המילה העברית “מגפה” - שורש נ.ג.ף, שפירושו ליפול, לספוג מכה או פצע, להיתקל במכשול. ספר שמואל א’, פרק ז’, פסוק י’: “וירעם ה’ בקול גדול ביום ההוא על פלשתים ויהמם וינגפו לפני ישראל”. ספר שמואל ב’, פרק י”ח, פסוק ז’: “וינגפו שם עם ישראל לפני עבדי דוד ותהי שם המגפה גדולה ביום ההוא עשרים אלף”. המילה “epidemic”, באה מיוונית, ופירושה במקום בו יש בני אדם. אנחנו מכנים מחלה בשם מגפה כאשר:
- מחלה זיהומית מתפשטת אל מעבר לאוכלוסייה מקומית מוגדרת
- נמשכת לאורך זמן רב מהרגיל
- פוגעת באנשים בשטח גאוגרפי נרחב.
- כאשר המחלה פוגעת בקנה מידה עולמי, אנשי המקצוע מכנים זאת 'פָנְדֶמיה'.
מגיפות בעבר הרחוק בעבר הרחוק המגיפות נחשבו לעונש מן השמיים על מעשים לא ראויים - פעולות של כוחות האופל ונציגיהם.
- במשך אלפי שנים חשבו בני האדם שהאלים הם אלה שאחראים לפרוץ מגיפות בעולם.
- כתוצאה מכך, גם הטיפול בהן נטה לכיוון העל-טבעי - מקדשים, תפילות, הקרבת קורבנות, קסמים ולחשים.
- יש גל של חזרה לרפואה האלטרנטיבית, שהולכת ותופסת מקום נכבד כאלטרנטיבה לרפואה הקונבנציונאלית.
מגיפות בזמן התנ"ך הרבה מודעות למחלות מידבקות ומגיפות - ספר ויקרא מכיל הוראות לשמירה על הגינה ציבורית, אספקת מים תקינה, טיפול בביוב, וכו’.
- המגפה העיקרית - צרעת.
- הסימפטומים - “אדם כי יהיה בעור-בשרו שאת או ספחת או בהרת והיה בעור-בשרו לנגע צרעת” (ויקרא, פרק י”ג).
- הגורם למחלה - לפי התנ”ך אין מדובר במחלה גופנית, כי אם באקט משמעתי רוחני שמקורו באלוהים - אות אזהרה לעבריין.
- הטיפול - השמת החולה בהסגר למשך מספר רב של ימים.
לדוגמה: ספר במדבר, פרק י”ב:
- סיפור המעשה: “ותדבר מרים ואהרן במשה על אודות האישה הכושית אשר לקח”.
- הסיבה לעונש: הוצאת לשון הרע - רכילות...
- התגובה האלוהית: “וְהֶעָנָן, סָר מֵעַל הָאֹהֶל, וְהִנֵּה מִרְיָם, מְצֹרַעַת כַּשָּׁלֶג” (במדבר, פרק י”ב).
- הפתרון: מרים ואהרון מתנצלים, ומרים מושמת בבידוד מחוץ למחנה למשך שבוע.
מסקנה: מגיפות הן התגלמות פיזית של חטא רוחני אנטי-סוציאלי (שבועת שווא, גאוותנות, דיבה, או פעולות נגד עם ישראל…). דוגמאות בולטות נוספות:
- מכות מצרים (כינים, שחין ומגפת הדבר).
- מגפת הפלשתים.
מגיפות במצריים העתיקה הסיבות למגיפות - המצרים האשימו את האלים של אויביהם בהבאת המגיפות, והתפללו לאלים בס וסקמת. 3000 לפנה”ס - סקחתאנך, הרופא הראשון. 2600 לפנה”ס - אימחותפ, יועץ רפואי למלך. הטכנולוגיה - צמחים ועשבי מרפא, ניתוחים, קמעי - קסם (חלקם אפילו עבדו…) בכל מקרה, בסופו של דבר, הרפואה היא רק כעזר לאלים - כאשר המצב מסתבך פונים לאלים. והפתרון - 500 לפנה”ס - אימחותפ “הופך” לאל, נבנים מקדשים עבורו המשמשים לריפוי האוכלוסייה.
מגיפות ביוון העתיקה האזכורים הראשונים למגיפות הופיעו אצל היוונים: באיליאדה של הומרוס (המאה ה-8 לפנה”ס) - האל אפולו יורה חיצי מגפה אל עבר הצבא היווני בקרב מול טרויה, כי אגממנון העליב כוהנת שלו. הסימפטומים - מחלה מידבקת מאוד, חום גבוה, מתפרצת במהירות וקטלנית מאוד. המגפה - ככל הנראה סוג של דיזנטריה, שהפכה לחריפה בשל התנאים הקשים בשדה הקרב.
- 429-430 לפנה”ס - מגפה קטלנית תקפה את אתונה באמצע המלחמה הפלפונזית (לא ידוע הסוג הספציפי).
כתוצאה מכך, הפסידה יוון את המלחמה מול ספרטה.
- היה ידע על העברת מחלות - היוונים ידעו לקשר בין עכברים להתפשטות המגפה.
- אבל לא מספיק ידע - לא ידעו על המיקרואורגניזמים שעל הפשפשים שנמצאים על העכברים, שהם אלה שמעבירים את המחלות.
- הפתרון - לפנות לאפולו, האל שמשויך לעכברים כדי שיסיר את המגפה…
המסקנה - אומנם התחיל להתפתח ידע ברפואה, ואובחן הקשר בין מגיפות לבין הגורמים האחראים להן, אבל בסיכומו של דבר - האלים הם אלה שגורמים למגיפות, והם אלה שיכולים להסיר אותן.
מגיפות באימפריה הרומית לפני תחילת המגיפות מנתה אוכלוסיית האימפריה הרומית כ-54 מיליון איש.
- 165 לספירה - “מגפת גאלן” - אבעבועות. המגפה קטלה כ-1/3 מאוכלוסיית האימפריה, כולל שני קיסרים.
- 251 - מגפת חצבת. מעל 5000 הרוגים מדי יום ברומא בלבד, כולל הקיסר קלאודיוס. הביאה לגל של התנצרות.
- 542 - מגפת Justinian, על שם הקיסר הביזנטי.
תוצאות המגיפות - מיליוני הרוגים, איבוד יכולת הלחימה, נפילת האימפריה הרומית.
מגיפות במזרח הרחוק
- הרפואה הסינית מאמינה שמחלות נגרמות בשל פגיעה באיזון הפנימי של הגוף (yin and yang).
- הטיפול - אקופונקטורה בנקודות מסוימות בגוף על מנת לתקן את הפגיעה בזרימת האנרגיה.
- בגלל מחסור בידע באנטומיה, לא בוצעו ניתוחים, ואף נאסר על רופאים לבצע חתכים בגוף.
- סין - שורת מגיפות ב-162, 310 וב-742 לספירה, הביאה לצמצום עצום באוכלוסיית סין, מ-50 מיליון ל-8.9 מיליון.
- יפן - במאה ה-8 וה-9 היו התפרצויות חוזרות ונשנות של אבעבועות.
- המגפה ב-735–736 לספירה הרגה חלק ניכר מבני מהמשפחה השולטת (Fujiwara), מה שהביא להתלהבות דתית ולעליית הבודהיזם ביפן.
מגיפות בימי הביניים
- המגפה הבולטת ביותר בימי הביניים היא “המגפה השחורה “, מגפת הדבר.
- 1348-1350 היו השנים בהן התפרצות המחלה היא הקשה ביותר - שליש מאוכלוסיית אירופה ואסיה נכחדות- כ־25 מיליון אנשים בשנתיים!!!
- במשך 300 השנים הבאות תכה המגפה באנגליה ובצרפת מספר פעמים ותפיל אלפי חללים עד 1665.
גורמים
- הגורמים למגיפות נקראים “מיאסמות”- אדי רעל או רוחות רעות
- התאוריה הובילה להתקדמות אדירה בדאגה להיגיינה ולניקיון ובעצם לבריאות הציבור.
- גורם נוסף בעקבות התקדמות האסטרונומיה היה הסבר אסטרונומי על מצב הכוכבים בעת פרוץ המגפה.
- והאמונה כי אלוהים והשטן הם הגורמים למגיפות- תאוריה שצברה כוח משלטון הדת.
טיפול
- טיפולים מגוונים שאינם קשורים בגורמי המחלה עצמם:
- בתי מצורעים- לבידוד המצורעים מהחברה ללא טיפול.
- רופאי אליל.
- תרופות נפוצות- תחבושות, משחות, אבקות, כדורים ומשאפים שהכילו צמחי מרפא.
- ניתוחי כריתת איברים פגועים.
השפעות
- המגפה הגדולה במאה ה-14 השפיעה רבות על מבנה החברה המעמדית באירופה, קירבה את קץ המשטר הפיאודלי ותרמה למפנה התרבותי חברתי בשחר ימי הרנסאנס.
- עקב ירידה במספר הידיים העובדות החלו החקלאים להתמקח על שכר עבודתם ובכך שיפרו משמעותית את תנאי חייהם.
- להקות חוזרים בתשובה נדדו מעיר לעיר והטיפו מוסר, וגרמו פראות ומהומות עקב הסתה כנגד היהודים.
- במגפה הבאה במאה ה-16 נוצר מוסד הקרנטינה- בידוד בני אדם המגיעים ממקומות נגועים לארבעים יום- שלא היה יעיל במיוחד.
- הדבר השאיר אחריו רושם עמוק בספרות ובאומנות באירופה:
- 1348 : בוקצ’ו מתאר את המגפה שפגעה קשות בפירנצה.
- “דקאמרון”- אוסף סיפורים שנכתבה בידי קבוצת צעירים שניתקו מגע עם שאר האנושות כדי להימלט מהמגפה.
- שיקספיר מזכיר את הדבר פעמים רבות בכתביו.
- שירו של שאול טשרניחובסקי “ברוך ממגנצה” מדבר על הפרעות ביהודים בעקבות המגפה והתאבדות המונית בשריפה של 60 אלף יהודים במינץ, פולין.
מגיפות בתקופת הרנסאנס
- המגיפות העיקריות בתקופה זו היו עדיין התפרצויות הדבר, סיפיליס, אבעבועות, חצבת וכו’.
- המחקר והמדע מתקדמים מאד, המצאת המיקרוסקופ, ניתוחי גופות ללימוד אנטומיה מעשירים את הידע - אך עדיין לא מונעים את התפרצות והתפשטות המגיפות.
- עדיין קיימים רופאי אליל, גופות חולים נשרפות ולא נקברות.
תקופת המהפכה התעשייתית
- ההתפתחות הגדולה בימי המהפכה התעשייתית היא במחקר ובמציאת פתרונות רפואיים למגיפות והקטנת תפוצתן.
- בתקופה זו ויליאם רנטגן מגלה את קרני הרנטגן, לואי פסטר מגלה את החיידקים כגורמי מחלות, וקוך מגדיר את הפוסטולטים באותו עניין מחקרי.
- ב-1796 אדוארד ג’נר ממציא את החיסון האקטיבי הראשון ברפואה המודרנית, החיסון לאבעבועות.
- בניתוחים מתחילים להשתמש בחומרי חיטוי והרדמה.
התקופה המודרנית גם במאה העשרים הושפענו מכמה מגיפות קטלניות:
- 1894 - תחילת מגפת הפוליו בארה”ב. המגפה המשיכה להשתולל, (7000 הרוגים ב-1916, 4000 ב-1931), עד פיתוח החיסון של סאלק ב-1955.
- 1918 - מגפת השפעת (influenza) גרמה למות 20 מיליון בני אדם, ולהפסקת מלחמת העולם ה-I.
הבעיה - וירוס השפעת (כמו גם וירוס האיידס) עובר מוטציות במהירות רבה, ולכן לא ניתן לפתח חיסון יעיל כנגדו.
ישנם כמה גורמים שמשפיעים על הפיכת מחלה למגפה:
- אופן העברת המחלה מאדם לאדם - ישנן דרכים שונות להפצת מחלות: באמצעות רוק, דם, מגע גופני, או אפילו באמצעות בעלי חיים. דרכי ההפצה משפיעות על קלות התפשטות המחלה.
למשל - מחלה המועברת באמצעות רוק או התעטשות יכולה להיות מועברת בקלות במקומות הומי-אדם, כפי שקורה במחלת הסארס. דוגמה אחרת היא מחלה המועברת באמצעות בעלי חיים. מחלת המלריה וקדחת הנילוס המערבי מועברות באמצעות יתושים. במקום שבהם ישנם יתושים המחלה מועברת בקלות. כאשר משמידים את אוכלוסיית היתושים ממקומות אלה, נמנעת לחלוטין העברת המחלה.
- רגישות גורם המחלה לתרופות ולחיסונים הקיימים - כאשר ישנה תרופה זמינה, חיסון או אמצעי מניעה מפני המחלה, נמנעת התפשטות המחלה.
דוגמה לכך הייתה מגפת האיידס. בתחילה, עד למציאת התרופה, המחלה גרמה לתמותה עצומה. עם מציאת הפתרון התרופתי ושינוי הרגלי ההתנהגות כתוצאה ממבצעי הדרכה על דרכי המניעה - אחוזי התמותה ירדו באחוזים רבים (בעולם המערבי).
- הוירולנטיות (התוקפנות) של גורם המחלה - למרבה האירוניה, ככל שהמחלה קשה יותר ומשך זמן המחלה מהיר יותר, נמנעת הפצתה והפיכתה למגפה. במקרים אלה, החולים אינם 'מספיקים' להפיץ את המחלה לפני מותם המהיר. משום כך מחלות קשות, כמו מחלת האבולה, פוגעות באוכלוסיות קטנות ומוגדרות, גורמות לתמותה באחוזים מחרידים, אבל אינן מופצות באזורים גאוגרפיים נרחבים.
- עמידות גורם המחלה לתנאי הסביבה - ככל שגורם המחלה - החיידק, הנגיף או הטפיל - רגיש יותר לתנאי הסביבה ומפונק יותר, הסבירות שהמחלה תופץ ברבים היא נמוכה יותר.
ישנם חיידקים ונגיפים שיכולים לשרוד רק בטמפרטורת הגוף (37 מעלות בקירוב) ומשום כך לא ישרדו מחוץ לגוף. נגיף כזה הוא נגיף האיידס שאינו שורד מחוץ לנוזלי גוף. דוגמה הפוכה אפשר למצוא בנגיף הסארס. מחקרים מצביעים על כך שמדובר בנגיף 'חזק' במיוחד המסוגל לשרוד בטמפרטורת החדר במשך ימים אחדים.
- התנהגות בבני האדם, חברות ומדינות - בעולם המודרני אוכלוסיות שונות, גם אם הן מרוחקות מבחינה גאוגרפית יכולות ליצור קשר בקלות. הקשר מתקיים בעזרת אמצעי תחבורה מודרניים, באמצעות מסחר וגם כתוצאה ממלחמות. כל אלה הן הזדמנויות פז למחוללי מחלה להדביק אוכלוסיות גדולות ברחבי העולם.
התנהגות של חברות מסוימות, כגון שימוש במקורות מים מזוהמים, ריבוי בני זוג ביחסי מין, והזרקת סמים באמצעות מזרקים משותפים מגבירה את הסיכויים להפצת מחלות שאינן מופצות בחברות שבהן אין נוהגים כך. ולהפך - החלטות של יחידים, של חברות או של מדינות יכולות להביא למיגור מחלות. דוגמה לכך תמצאו בטיפול הרשויות במחלת הסארס. מיד עם היוודע דבר התפרצות המחלה ננקטו צעדים שהביאו למניעת התפשטות המחלה - סגירת בתי ספר ומקומות ציבוריים, חבישת מסיכות, הטלת הסגר על מקומות נגועים והימנעות מנסיעה למקומות שבהם התפרצה המגפה. גם צורת המגורים של האדם המודרני משפיעה על אופן הפצת המחלות. רוב אוכלוסיית העולם חיה בערים. המגורים באזורים עירוניים מביאה אנשים רבים למגע קרוב. בסביבה כזאת חיידקים נושאי-מחלות מועברים ביתר קלות מאדם אחד לאחר. בערים רבות בעולם, במיוחד בעולם השלישי הערים מתפתחות במהירות ומערכות הבריאות והתברואה אינן מסוגלות לתת שירות לכל התושבים. מצב זה של היעדר תנאים סניטאריים נאותים, היעדר גישה לתרופות, לחיסונים ולמידע רפואי חיוני, מסייע להפצת מחלות זיהומיות.
- שינוי תנאים סביבתיים - שינויים אקלימיים וסביבתיים תורמים אף הם להתפשטות מחלות זיהומיות על ידי כך שהם יוצרים תנאים שמגבירים את נוכחות הגורמים מחוללי המחלות ובעלי החיים שנושאים אותם.
בצורת או שיטפונות יכולים לגרום לשינוי אזורי המחיה ובכך לשנות את סוגי מיני האורגניזמים החיים באזור ואת מספרם. דוגמה לכך אפשר למצוא במגפות שהתפשטו בסודן בשנת 1998, כאשר בצורת ומלחמת אחים הביאה למותם של רבים ממלריה ומחלות אחרות. בעקבות אסונות טבע רבים נפגעים מקורות המים, לכן מחלות המופצות באמצעות מים מזוהמים, כגון כולרה, מתפשטות במהירות גבוהה. חוקרים מזהירים גם מפני עלייה במחלות הזיהומיות כתוצאה מהתחממות כדור הארץ וירידה בכמות המשקעים. דוגמה לגורם אקלימי שסייע להתפשטות מגפה היא מחלת הדבר בימי הביניים. ישנם חוקרים שטוענים שתקופת התקררות אקלימית שהתרחשה במאה ה-14 הביאה לירידה בבריאות הציבור בערים הצפופות, לירידה ביבול החקלאי בגלל השינויים האקלימיים וכך לירידה בתזונה. לעומת זאת העלייה בגודל אוכלוסיית המכרסמים שחיו בערים שימשה קרקע פורייה להתפשטות המחלה שהביאה למותם של מיליונים באירופה.
חששות לגבי העתיד מחלות קשות כגון האבולה ואחרות ממשיכות להתפרץ במקומות שונים בעולם ולהרוג קורבנות רבים. עם זה, הווירולנטיות (כלומר: התוקפנות הרבה) של המחלות מונעת את התפשטותם מעבר לגבולות גאוגרפיים מוגדרים. כל זה נכון במקומות מבודדים שאינם נגישים לאמצעי התחבורה המודרניים. בעידן של תחבורה קלה ומהירה קיים חשש שגם מחלות קשות כאלה יוכלו להיות מופצות ביתר קלות.
סכנה נוספת נמצאת באותם חיידקים ונגיפים שפיתחו מוטציות ועמידות בפני התרופות הקיימות. כבר היום ישנם חיידקים של מחלות 'פשוטות' למדי, שאינם רגישים עוד למגוון התרופות האנטיביוטיות המקובלות. למעשה יש מעין תחרות בין כושר פיתוח העמידות של החיידקים לבין יכולת פיתוח התרופות האנטיביוטיות והחומרים האנטי-נגיפיים שהאדם מסוגל לפתח.
ההיסטוריה של החיסונים – המגפות הגדולות אחד האסונות הגדולים ביותר שפגעו בעולם אי-פעם, לא היה מלחמה. גם לא מבול, רעידת אדמה או רעב אלא מגפת הדבר המכונה מגפת המוות-השחור, מגפה שאין דומה לה בכל ההיסטוריה. שיעור התמותה של הנדבקים במחלה התקרב למאה אחוזים(!), ואנשים שנדבקו בה מתו תוך יומיים שלושה. השם שניתן למחלה בימי הביניים מעיד על אופייה האיום: המוות השחור. היו גם מגפות רבות אחרות של דבר וגם של מחלות אחרות, לרבות אבעבועות שחורות, שהיו קטלניות והרסניות, אך כולן היו מצומצמות יותר בתפוצתן, מקומיות יותר, ופחות נוראות מאותה פלישה ראשונה של המוות השחור לאירופה של סוף ימי-הביניים.
סיפורו של "המוות השחור" במאה ה 14- היו לאירופים נתיבות מסודרים למדי, ששמרו על קשר עם המזרח (אסיה). אלה נוצלו היטב למסחר ענף. לאיטלקים היה מרכז מסחרי בעיר קאפא שבאוקראינה של היום, על חופי הים-השחור. הסוחרים האיטלקים היו משייטים לקאפא וסוחרים משם עם אסיה. בשנת 1346 הותקפה קאפא בידי טטרים - פולשים מונגולים ממרכז אסיה, שניסו לפרוץ את חומותיה. הסוחרים האיטלקים שבעיר, יחד עם תושביה, צפו את נפילתה הקרובה של עירם בידי הטטרים, שהיו רבים וחזקים מהם. למרבה הפלא, הרפו הטטרים מן המצור על העיר, ואנשי קאפא נשמו לרווחה. אך התושבים, שניצלו מזעם הטטרים, לא זכו לשמוח בהצלתם, כי הטטרים מוכי-החולי חלקו עמם את צרתם, והשליכו את גויות מתיהם מעבר לחומות אל תוך העיר. התושבים בעלי התושייה השליכו מיד את הפגרים בחזרה אל מחוץ לעיר, אל תוך הים, אך תושייתם לא עמדה להם להצילם, והמגפה הכתה בהם.
המוות השחור – ציור מימי הביניים היה זה, כנראה, המקרה הראשון של אירופים שנפגעו במחלת הדבר, בדרכו מערבה. דרכי מסחר חדשות נסללו מאסיה המזרחית לאירופה המערבית, ועליהן דהר גם הדבר. כל אירופה הייתה בתחום פגיעתו. ספינות סוחר איטלקיות נשאו את הדבר לקונסטנטינופול (איסטנבול של היום), ומשם לנמלי הים התיכון. וכך תואר במסמך מאותם הימים: "כמו היו מלווים ברוחות-רשע, הביאו המלחים את המוות, לכל מקום שאליו הגיעו, ולכל אדם שבו פגשו". על אף שאופן העברת המחלה לא היה ברור, הבינו האנשים, שקיים תהליך של הידבקות. במרסיי, עיר הנמל הצרפתית, למשל, מנעו מספינות איטלקיות להתקרב אל החוף במשך תקופת ההסגר.
קרנטינה (הסגר) המילה קרנטינה (הסגר) מקורה במילה ארבעים באיטלקית. אלה ארבעים הימים שהחזיקו בהם את הספינה מחוץ לנמל, כדי לוודא שאינה נגועה במגפה. המלחים שעל הספינות היו במצב בריאותי ירוד ביותר, ורובם מתו תוך תקופת ההסגר. וכך, ספינות עמוסות סחורות שייטו מול נמל מרסי ללא צוותים, נושאות את מתיהן בלבד. בכל זאת התפשטה המגפה במהירות רבה, ראשית למרסיי וממנה במעלה עמק הרון. ממדי התמותה הייתה עצומים ובערים הנגועות מתו כמחצית מהאוכלוסין. אנשים מוכי אימה ופחד נסו מערי הנמל אל פנים-הארץ. הנמלטים מפני המוות הם אלה שהפיצו את המחלה, ונשאו אותה אל פנים הארץ. מפת התפשטותה של מחלת הדבר דומה למפת דרכי המסחר הראשיות באותם הימים, הן ביבשה והן בים. המסלול מוביל מסין לאירופה, דרומה - לאפריקה, צפונה - לרוסיה, ומפיציה הם האנשים שנעו ממקום למקום, וגם יתושים וחולדות.
בגד הגנה בפני הדבר – ציור מימי הביניים איך מחלת הדבר מועברת מנשא לנשא? הדבר הבובוני (שסימניו דלקת-המפשעה או פצעים מוגלתיים), מועבר על ידי פרעושים נגועים, החיים על חולדות שחורות. הפרעושים עוקצים בני אדם רק, כשאין חולדות. בהתרבותם בדם האדם הנגוע, נגיפי הדבר מסוגלים לעבור מוטציה מוזרה, שבעקבותיה הם תוקפים את הריאות, ומחלה זאת - דבר-הריאה - מועברת בנשימה מאדם לאדם. דבר הריאה יכול להתפשט ללא תיווכם של פרעושים או חולדות.
הדבר הבובוני והריאתי התפשטו באירופה בו-זמנית, וכתוצאה מכך המחלה נפוצה במהירות רבה מאוד ובתמותה גבוהה ביותר.
מניחים שכשליש מאוכלוסיית העולם באותו זמן נכחדה במגפת הדבר. המחלה התפשטה באירופה במשך שנת 1348, ובקיץ של אותה שנה הגיעה לראשונה לאנגליה.
מגפת הדבר באנגליה חדירת המגפה לאנגליה הייתה, כנראה, בספינה שהגיעה מנמל קלה שבצרפת ועגנה באחד מנמלי החוף הדרומי בחודש אוגוסט. המגפה התפשטה במהירות מנמל לנמל וביבשה. ערים אחדות ניסו לסגור עצמן מפני המגפה, אך ללא הועיל. כך למשל ניסו תושבי גלוסטר לנתק מגע מבריסטול הסמוכה, כשנפוצה השמועה שזו נפגעה בדבר, אך המחלה הגיעה גם אליהם.
המגפה התפשטה במהירות באזורים צפופי-אוכלוסין, כמו אזוריה המזרחיים והדרומיים של אנגליה, שהישובים בהם קרובים זה לזה והדרכים בהן משופרות. לעומת זאת, היא נעה באטיות יחסית בצפון ובמערב, וייתכן אף שהיו כפרים קטנים, מבודדים, שלא נפגעו כלל.
בלונדון בחורף 1349 הגיע הדבר ללונדון. הסופר דניאל דפו, שחיבר בין היתר את רובינזון קרוזו, השתמש ברשומות מאותם הימים ותיאר את התפשטות המחלה בעיר ואת הפלצות, שאחזה בתושביה מפני המוות השחור.
בסקוטלנד הסקוטים, בשומעם על הרעה שפגעה באנגליה ובראותם את חולשתה, החליטו לנצל את ההזדמנות ולפלוש לאנגליה הצפונית. בחורף 1349 התקדם הצבא הסקוטי ההרפתקן לגבולה של אנגליה. כבר בדרכם פגע בהם הדבר והפלישה בוטלה. החיילים החולים נטשו את גדודיהם ופנו איש-איש לביתו, כשהם מפיצים את מגפת הדבר ברחבי סקוטלנד...
האם שינה הדבר את פני ההיסטוריה? מאנגליה הגיע הדבר לסקנדינביה, משם בספינה לגרינלנד, שם חיסלה המגפה את כל מושבות הוויקינגים הוותיקות. יש אומרים שלוויקינגים האלה היו קשרים עם האי ניו-פאונדלנד, ואולי גם עם קנדה היבשתית, קשרים שאבדו לעד כשהוויקינגים נושאי הקשר גוועו במגפה. ייתכן שלולא המגפה, היו קשרים אלה מתפתחים ופני ההיסטוריה באמריקה הצפונית היו שונות לחלוטין.
חיסונים עתיקים גם בעבר ניסו בני האדם לחסן מפני המחלה. חיסונים נגד אבעבועות היו נהוגים בסין כבר במאה ה10-: הסינים לקחו גלדי אבעבועות של אנשים שמתו מן המחלה, והחדירו אותם לנחיריים של אנשים בריאים. שיטות חיסון עממיות דומות היו נהוגות גם באפריקה ובמזרח התיכון, ומשם עברו לאירופה.
החיסון המודרני החיסון המודרני נוצר שנים רבות מאוחר יותר בבריטניה. כיצד זה קרה? - הרופא האנגלי הכפרי, אדוארד ג'נר, שחי בשלהי המאה ה-18-, עסק במחקר רפואי ובזואולוגיה. לאוזניו הגיעה שמועה, שנשים כפריות שעסקו בחליבת פרות, ואשר נדבקו באבעבועות הבקר, לא חלו מעולם באבעבועות שחורות.
התגלית של ג'נר ג'נר החליט לבחון את הדברים. במאי 1796 הוא לקח חומר משלפוחית שהייתה על זרועה של רפתנית שחלתה באבעבועות בקר, שהיא, כזכור, מחלה קלה יותר מ"קרובת משפחתה", מחלת האבעבועות השחורות. הוא טבל מחט בחומר ושרט את עורו של בנה של המשרתת שלו. שישה שבועות אחר כך שרט את עורו של הילד במחט, שנטבלה בחומר שנלקח משלפוחית שהייתה על עורו של חולה באבעבועות שחורות. הילד לא נדבק במחלה.
ג'נר חיסן בדרך זו עוד 23 אנשים, ואז פרסם את תגליתו. מכאן נסללה הדרך לגילוי חיסונים יעילים ובטוחים יותר נגד אבעבועות שחורות, כמו נגד מגיפות אחרות.
ג'נר מחסן בפעם הראשונה מאה אלף איש, על פי חישוב פשוט, חוסנו בעולם. מספר האנשים שנהנו מתועלת החיסון ברחבי אירופה ואזורים אחרים על פני הגלובוס לא ניתנים לחזות: ונעשה היום ברור מכדי להודות במחלוקת, שהכחדת אבעבועות שחורות, הפורענות הנוראה ביותר של המין האנושי, חייבת להיות המטרה הסופית של השימוש בחיסון. אדוארד ג'נר, 1801
מילים מלאות תקווה אלו של ג'נר חזו את הנולד, על אף שעברו עוד 200 שנה עד שנגיף האבעבועות השחורות הוכחד מין העולם. לפני מאה שנה, יותר מ 48000 איש נדבקו באבעבועות שחורות כל שנה בארצות הברית. היום, המחלה פסה מן העולם והנגיף שמור ונעול במספר מעבדות בעולם. בעקבות חיסון המוני, מחלות נוספות הקשורות בתחלואה ותמותה גבוהים כמעט שנעלמו מארצות הברית. בשנת 2001, היו רק שני מקרי דיפטריה, לא היה אף מקרה של פוליו, ודווחו 116 מקרי חצבת. לפני שפותחו החיסונים למחלות אלו, יותר מ 170,000 מקרי דיפטריה, 16,000 מקרי פוליו, ו 500,000 מקרי חצבת דווחו כל שנה בארצות הברית. חיסונים מונעים מחלות בילדים, מקטינים את הנטל הנגרם מהמחלות על האוכלוסייה הכללית, ויכולים לגרום לחיסון "עדר" (כאשר אלו שלא חוסנו נהנים מירידה בפיזור הנגיפים או החיידקים עקב ירידה בתחלואה, או עקב חיסון פסיבי כאשר הווירוס המוחלש עובר מהמחוסן לסביבתו) ולמנוע התפשטות של מחלות קטלניות. המטרה המוחלטת של הרפואה הציבורית היא להשיג באמצעות החיסון, חיסול של המחלה המידבקת, ובהמשך הצורך בחיסון נגדה. מטרה זו הושגה רק במקרה של אבעבועות שחורות.
לואי פסטר (27 בדצמבר 1822 - 28 בספטמבר 1895) היה מדען צרפתי; הוא נחשב לאבי המיקרוביולוגיה והיה זה שפיתח את חיסון הפעיל הראשון בעולם. את החיסון לכלבת פיתח לואי פסטר. בשנת 1880 מצא פסטר כי הגורם למחלה אינו חיידק. הוא החל עורך ניסויים בכלבים נגועים על ידי תרביות מוחלשות של הנגיף. בהתאם לאמצעים של אותם ימים, היה בודק פסטר את השפעת החיסון על ידי ארנבונים חיים שהיה מכניס לכלוב הכלב. באחת הפעמים הבחין כי הכלב בו טיפל מיאן לתקוף את הארנבת כהרגלו. פסטר הסיק מכך כי תרכיב החיסון, אחד מני רבים שהכין, הוא אשר לו נזקק. יעילותו של החיסון הוכחה כאשר בשנת 1884, הובא לביתו של פסטר ילד שננשך על ידי כלב משוטט בתשעה מקומות. בעוד פסטר מזריק לו את החיסון הניסיוני שלו, נאסף סביב הבית קהל זועם שהמטיר נאצות כלפי פסטר וגידף את ניסוייו, אולם כעבור ימים אחדים ניצלו חייו של הילד.
החיסונים בארץ המחלות נגדן מוצעים חיסונים לכל הילדים בארץ הן: אסכרה (קרמת/דיפתריה), צפדת (פלצת/טטנוס), שעלת, שיתוק ילדים (פוליו), המופילוס אינפלואנזה b, חצבת, חזרת, אדמת, דלקת כבד נגיפית A ודלקת כבד נגיפית B. לציבור הרחב מוצע חיסון כנגד אבעבועות רוח. למרות שהחיסון טוב ויעיל, הוא טרם הוכנס לשגרת החיסונים על ידי משרד הבריאות. כמו כן מוצע החיסון כנגד שפעת. לפגים קטנים ולתינוקות הסובלים ממחלת ראות כרונית. מוצע חיסון סביל כנגד RSV. חיסונים נוספים המוצעים לקבוצות סיכון הם חיסון כנגד חיידק הפנאומוקוקוס, חיסון כנגד חיידק המנינגוקוקוס ועוד. חיסונים ניתנים גם לפני נסיעה לחו"ל לאזורים בהם שכיחות מחלות קשות שניתן לחסן כנגדן. החיסונים זו הדרך היעילה והבטוחה ביותר למנוע מחלות קשות. החיסונים הניתנים על ידי המדינה ניתנים הטיפות החלב, ואלה המוצעים ניתנים במרפאות הילדים החיסונים הניתנים בארץ מקובלים בארצות המערב. אחוז הילדים המקבלים את חיסוני השגרה בישראל הוא מהגבוהים בעולם למרות שקבלת החיסון אינה חובה על פי חוק. שגרת החיסונים לילדים
פרק 3 חיסונים ואנחנו (פרק זה מיועד להורים) (הפרק מבוסס על מאמר של פרופ' יונה אמיתי ופרופ' שמואל רשפון – משרד הבריאות)
יצירת התגובה החיסונית חומר החיסון, ניתן לילד בהזרקה מלבד חיסון חי מוחלש נגד שיתוק ילדים הניתן בטיפות לפה. החיסון מורכב מחיידקים או מנגיפים, מוחלשים או מומתים או ממרכיבי של הוירוסים והחיידקים המשרים את התגובה החיסונית. החיסונים גורמים ליצירת נוגדנים בגוף המתחסן, בדומה למה שקורה בעקבות מחלה טבעית. הנוגדנים הם המעניקים לאדם את ההגנה בפני המחלה אשר מפניה חוסן. לכל מחלה יש חיסון משלה. חיסונים ניתנים במנות חוזרות כדי להבטיח הגנה למשך שנים רבות.
מועדי החיסון חשובים רצוי להקפיד על מועדי חיסון כפי שהם מופיעים בטבלת החיסונים. דחיית מתן חיסון למועד מאוחר יותר מהמומלץ עלולה לחשוף את הילדים לסיכון לחלות במחלה נגדה עדיין לא חוסנו. תגובות לחיסון מתן חיסון, כמו מתן כל תרופה, עלול לגרום לתופעות לוואי כמו: עליית חום, הרגשה כללית רעה, אודם ונפיחות במקום שבו ניתנה הזריקה. תופעות אלו הן בדרך כלל קלות וחולפות תוך זמן קצר, לרוב תוך יום יומיים. אם מופיעים אודם או נפיחות במקום ההזרקה, מומלץ לשים על המקום תחבושות ספוגות מים פושרים. אין לעסות את מקום ההזרקה. אם החום עולה, יש לתת לתינוק, בהתייעצות עם הרופא המטפל, תכשיר להורדת חום. לעיתים נדירות ביותר, עלולה להיגרם תגובה אלרגית חמורה שהיא תופעת לוואי קשה יותר. תופעה זו ניתנת לטיפול מיידי בעזרת ערכת טיפול יעילה הנמצאת בכל תחנת "טיפת חלב" ובכל מרפאה בה ניתנים חיסונים. תופעה נדירה נוספת היא פרכוסים עקב חום גבוה. תופעה זו ניתנת למניעה בעזרת תרופות מורידות חום. שתי התופעות חולפות לאחר הטיפול ואינן גורמות נזק קבוע.
טכנולוגיות חדשות מאפשרות לתת יותר חיסונים בו זמנית עם פחות תופעות לוואי. שילוב מספר חיסונים באותה זריקה מונע מתן מיותר של זריקות באותו יום, מוריד את שיעור תופעות הלוואי המקומיות ואינו מפחית את יעילות החיסון.
משרד הבריאות שואף לדאוג לרווחתם של ילדינו והגנתם מפני כמה שיותר מחלות קשות ומסוכנות. המטרה, לשלב מקסימום חיסונים להגנת הילד עם מינימום תופעות לוואי. יש לזכור כי הסיכון הנובע מהמחלות שבפניהן הילד מקבל חיסונים, גבוה בהרבה מהסיכון לתופעות לוואי אפשריות בעקבות קבלת החיסונים.
דחיית חיסונים אם הילד אינו חש בטוב צריך להודיע על כך לאחות בתחנה לבריאות המשפחה. מתן החיסון או דחייתו יישקלו על ידי הצוות הרפואי. בבואכם עם הילד לקבלת חיסונים, דווחו על מצב בריאותו, על המחלות שעבר על תופעות אלרגיות שהילד סובל מהן ועל רגישותו לתרופות, כולל אנטיביוטיקה. כמו כן, יש להסב את תשומת-לב האחות לתופעות חריגות או לתגובות שהופיעו אצל התינוק אחרי חיסונים קודמים. פנקס החיסונים
(שימו לב – קיימים פנקסים שונים)
יש לשמור היטב על פנקס זה כל חיסון של הילד נרשם בפנקס. עם קבלת החיסון הראשון מקבל ההורה את פנקס החיסונים. על ההורה לשמור פנקס זה לרישום המשך החיסונים. פנקס זה מהווה מסמן המאשר את החיסונים שקיבל בעל הפנקס. בכל מקרה של פציעה יש להציגו בפני הרופא כדי למנוע מתן חיסון מיותר. יש לדאוג, שבפנקס החיסונים יירשמו כל החיסונים, שאדם מקבל במשך חייו.
בטיחות בחיסונים
חיסונים – פעוטות ומערכת החיסון – האם יותר מידי חיסונים ?
בישראל מומלץ על 10 חיסוני שגרה של ילדים. הורים מודאגים מהשאלה האם ילדיהם הפעוטות יהיו מסוגלים להתמודד עם הזריקות והחיסונים הרבים האלו.
התשובה לשאלה היא שחיסונים הם רק חלק קטן ממה שהמערכת החיסונית של הפעוטות נדרשת להתמודד עמו מדי יום ביומו. מערכת החיסון של ילודים נחשפת לשפע של זיהומים סביבתיים. מהדקה הראשונה להיוולדם, אלפי חיידקים שונים מתיישבים וחיים על פני העור של הילוד ברירית שבנחיריו, בלוע שלו ובמעי שלו. תינוקות מונעים מחיידקים לפלוש לזרם הדם שלהם על ידי תגובה חיסונית מהירה לאותם זיהומים.
למעשה תינוקות מסוגלים להגיב למגוון של מיליוני נגיפים וחיידקים מכיוון שיש בגופם הרך מיליארדי תאים של מערכת החיסון אשר בשלים ומוכנים לפעולה. לכן, לסיכום, חיסונים הניתנים לילודים בשתי השנים הראשונות לחייהם הם למעשה טיפה בים לעומת האתגרים החיסוניים שמערכת החיסון של התינוק צריכה להתמודד עמם מדי יום ובאופן טבעי. למרות שהילדים היום מקבלים יותר חיסונים ממספר החיסונים שהם קיבלו לפני מאה שנים, (אז המליצו רק על חיסון אחד כחיסון שגרה למניעת מחלות – והוא החיסון כנגד אבעבועות שחורות), הרי שבזכות החיסונים המודרניים סך הכל מספר החלבונים והסוכרים שניתנים בחיסונים היום פחת מאוד לעומת מספר החלבונים שהיו בחיסון שקיבל ילוד לפני 100 שנים. החיסון הישן כנגד אבעבועות שחורות הכיל כ־200 חומרי חלבון שונים. ואילו היום אם נסכם את מספר החומרים החלבוניים והסוכרים אשר עשרת חיסוני השגרה שניתנים מכילים נקבל סך של כ 50. זאת הודות לטכנולוגיה המודרנית של חומרי החיסון : בחיסון כנגד דיפתריה רק חלבון אחד, בחיסון כנגד טטנוס חלבון אחד בלבד, בחיסון כנגד שעלת 2–5 חלבונים, פוליו (15), חצבת (10), חזרת (9), אדמת (5), המופילוס אינפולואנזה b (2) ודלקת כבד נגיפית B (1).
מדוע ניתן לומר כי – "החיסון בטוח"? ההגדרה הראשונה של בטוח היא "לא מזיק". הגדרה זו מרמזת לכך שכל השלכה או תוצאה שלילית של חיסונים תהפוך אותם ללא בטוחים. אם נשתמש בהגדרה הזו, אפשר לומר שלא קיים חיסון אשר בטיחותו תוגדר 100%. כמעט כל החיסונים עשויים לגרום לכאב מקומי, אודם מקומי או רגישות במקום ההזרקה. חיסונים מסוימים עשויים לגרום לתופעות לוואי יותר משמעותיות. לדוגמה – חיסון השעלת (Pertussis) יכול לעיתים נדירות לגרום לבכי ממושך בילד שחוסן או לחום גבוה. למרות שהתופעות הללו אינן גורמות לנזק קבוע, הן מפחידות מאוד את ההורים. מעט דברים בחיי היום יום שלנו יכולים לענות על ההגדרה של בטוח לחלוטין או לא מזיק. לדוגמה, מדי שנה בארצות הברית 350 אנשים נהרגים מתאונות שקשורות ברחצה באמבטיה ו- 200 אנשים נהרגים ממזון שנתקע בקנה הנשימה. אולם למרות זאת רק מעטים מאיתנו ישקלו בעקבות המידע הזה שלא לאכול מזון מוצק או להתרחץ. רובנו אינם מחשיבים את הפעילויות הללו כ"לא בטוחות", אנו פשוט שוקלים יתרונות של אותן פעולות לעומת החסרונות של הסיכון הפוטנציאלי שבהן. ההגדרה הנוספת למילה "בטוח" היא "הישמרות מפני סכנה ממשית". הגדרה זו מתייחסת לכך שחיסונים מקנים ביטחון והגנה. אם נשתמש בהגדרה הזו, הסכנה (או המחלה) צריכה להיות הרבה יותר משמעותית וחמורה מאשר הסיכונים של האמצעי שבאמצעותו אנחנו מתגוננים כנגדה (החיסון כנגד מחלה). במילים אחרות יתרונותיו של החיסון גוברים חד משמעית על חסרונותיו. כדי להבין יותר טוב את הגדרת המילה "בטוח" בהתייחס לחיסונים הבה נבחן חיסון אחד ביחס למחלה שהוא מונע.
האם החיסונים באמת יעילים הדוגמה הטובה ביותר ליעילותם היא קיומו של חיסון שמונע דלקות קרום המח (meningitis) אשר נגרמות מחיידק Haemophilus influenza מזן b : Hib. החיסון הקיים היום כנגד Hib הוצג לראשונה כחיסון חדש בעולם בשנת 1990. אז חיידק זה היה הגורם החיידקי השכיח ביותר לדלקות קרום המח בפעוטות. הוא גרם בכל שנה בארץ בערך ל־200 מקרי תחלואה, מתוכם כ־100 מקרי דלקת קרום המח וכ־100 ביטויים אחרים של מחלה קשה שגרמה בעיקר לתינוקות לדלקת ראות ואלח דם. מקרב החולים הנ"ל כ 2–3 תינוקות בישראל נפטרו מדי שנה ו- 15 נותרו עם סיבוכים נוירולוגיים קבועים, כמו חירשות, פיגור שכלי ונכות. לפני הכנסת החיסון לתוכנית חיסוני השגרה של גיל הילדות הייתה שכיחות התחלואה והתמותה ממחלה זו יציבה מדי שנה בכל העשורים. לאחר שהחלו להשתמש בחיסון Hib באופן שגרתי ירד מספר החולים בדלקת קרום המח מחיידק זה מ־200 ל־10 חולים בשנה בלבד. מספר זה נמוך בהרבה מאשר באירופה המערבית.
סיפורו של החיסון כנגד חיידק Hib מאפיין את תועלתם המטיבה של כל שאר החיסונים. ירידה דרמטית בשכיחות מחלות בעקבות הפעלת תוכנית חיסון שגרתית לילדים הופיעה גם לאחר הפעלת תוכניות חיסון נגד מחלות זיהומיות קשות אחרות כגון חצבת, חזרת, שיתוק ילדים, דיפתריה (קרמת), טטנוס (צפדת) ושעלת. לסיכום – לא זו בלבד שחיסונים הם יעילים, אלא שהם בטוחים מאוד.
האם החיסונים מחלישים את מערכת החיסון של התינוק ?
הדבקה טבעית עם נגיפים מסוימים עשויה באמת להחליש את מערכת החיסון. פירושו של דבר שילדים שיידבקו בזיהום מנגיף אחד לא יוכלו להלחם באותה יעילות עם נגיף אחר או חיידק תוקפים אותם זמן קצר לאחר מכן. התופעה הזו מתרחשת בצורה הבולטת ביותר במהלך הדבקה טבעית באבעבועות רוח או במחלת החצבת. ילדים הנדבקים במחלת אבעבועות רוח רגישים במיוחד להדבקות מזיהומים חיידקיים מסוימים כגון "החיידק הטורף". ילדים שנדבקו בחצבת נוטים לחלות בזיהומים חיידקיים בזרם הדם (אלח דם). אך החומרים שבחיסונים הם שונים ואינם גורמים לחולשה החיסונית הזו כפי שגורמים הנגיפים הטבעיים. בנגיפים החיים המוחלשים שמצויים בחיסונים כנגד אבעבועות רוח וחצבת שונים מאוד מנגיפי מחלות אלו, אשר כנגדם אנו מחסנים. הנגיפים שבחומר החיסון אינם יכולים להחליש את מערכת החיסון של התינוק.
לכן ילדים שחוסנו אינם מצויים בסיכון גבוה יותר לחלות במחלות מידבקות אחרות מאשר ילדים אשר לא קיבלו חיסונים אלו.
מדוע נראה כי כבר לא צריך חיסונים?
בהתייחס לטענה זו, במובן מסוים החיסונים הופכים להיות הקורבן של ההצלחה הגבוהה שלהם בהורדת התחלואה. ההורים של היום לא ראו אף פעם חולה בחצבת, חזרת שיתוק ילדים, דיפתריה, טטנוס או שעלת. כתוצאה מכך שאינם מכירים מחלות אלה הורים מסוימים שואלים עצמם בשביל מה צריך לתת את החיסונים כנגד מחלות אלו, אשר לכאורה כבר אינן קיימות. התשובה היא שיש להמשיך כי מחוללי מחלות אלו נמצאים עדיין בסביבתנו ומי שלא יחוסן נגדן, גבוה הסיכוי שיחלה בהן. בארצות הברית למשל, כאשר שיעורי המתחסנים כנגד חצבת ירדו בסוף שנות ה-1980 ותחילת שנות 1990, התוצאה הייתה 11,000 אשפוזים של ילדים חולים ויותר ממאה פטירות שנגרמו מחצבת. מחלות מסוימות נכחדו לגמרי מהעולם המערבי בזכות החיסונים, למשל שיתוק ילדים או דיפתריה. אך הן קורות באזורים אחרים בעולם. לאור השיעורים הגבוהים בימינו של ההגירה, תנועות אוכלוסין ונסיעות לחו"ל ברור כיצד עלולות המחלות לקרות גם אצלנו אם לא נהיה מחוסנים כנגדן.
האם קיימת אמת באמירה כי החיסונים גורמים לאוטיזם?
התפרסמו כתבות באמצעי תקשורת שונים אשר גרמו להורים מסוימים לחשוש מפני חיסון הקומבינציה כנגד חצבת-חזרת-אדמת (MMR) מכיוון, שלפי אותם סיפורים, החיסון הזה גרם לאוטיזם. טענה זו הדירה שינה מעיני הורים רבים אשר שבו ופקדו הן את התחנות לבריאות המשפחה והן את הרופא בקופת החולים לקבל אישור וחיזוק למתן החיסון. למרות שהשאלה כבר פתוחה כ 20 שנה הרי שרק ב 5 השנים האחרונות הוברר למעלה מכל ספק כי לא קיים כל קשר בן חיסון לאוטיזם. השאלה הגיעה לבסוף להכרעה בבית המשפט העליון שמינה ועדת חוקרים שאספה עדויות מכל העולם ואשרה את הנחת הבסיס של משרד הבריאות כי לא קיים קשר בין חיסונים ואוטיזם.
מחקרים המראים כי חיסון MMR אינו גורם לאוטיזם להלן תקציר ארבעה מחקרים אשר הפריכו את האפשרות ש- MMR גורם לאוטיזם. 1. בשנת 1999 החוקר ברנט טיילור Brent Taylor ועמיתיו ביצעו מחקר מבוקר היטב שבו בחנו את יחסי הגומלין בין קבלת חיסוני MMR והתפתחות אוטיזם. הם בחנו 498 רשומות של ילדים עם אוטיזם ועם הפרעות בעלות קווים אוטיסטיים (Autism like disorder). הילדים שנכללו במחקר נלקחו מרשומים על ילדים אוטיסטיים במחוז North Thames באנגליה מהתקופה שלפני 1988 (השנה בה הכניסו את השימוש בחיסון MMR למערכת השגרה) ולאחריה. החוקר טיילור בחן את שכיחות האוטיזם בכל קבוצה (אלו שקיבלו חיסון, אחרי 1988 ואלו שלא קיבלו אותו, לפני 1988). הוא בדק גם את גילו של הילד בעת האבחנה של האוטיזם. ממצאיו : א. אחוז הילדים שחוסנו היה דומה בילדים עם אוטיזם ובילדים בלא אוטיזם. ב. לא נמצא שוני בגיל האבחנה של אוטיזם בילדים שקיבלו את החיסון לבין אלו שלא קיבלו את החיסון. ג. פרק הזמן בין מועד התחלת התסמינים של אוטיזם ובין מועד מתן החיסון היה שונה ממקרה למקרה (כעבור שניים, ארבעה או ששה חודשים). ממצאים אלו זו אינם תומכים במנגנון של קשר ביולוגי בין החיסון לתחלואה. 2,3. מחקרים אחרים אשר פרסמה החוקרת נטלי סמית (Natalie Smith) בכתב העת המדעי– Journal of American Medical Association, והחוקר הרשל ג'יק Hershel Jick בעיתון British Medical Journal הראו שהעלייה בדיווחים על ילדים הסובלים מאוטיזם אינה קשורה בעלייה בשימוש בחיסוני MMR. 4. המחקר הגדול ביותר אשר חקר את קשרי הגומלין בין חיסוני MMR ובין אוטיזם דווח בעיתון היוקרתי האמריקאיthe New England Journal of Medicine בחודש נובמבר 2002. במחקר זה כללו 537,000 ילדים מדנמרק אשר חלקם קיבלו את החיסון וחלקם לא. הם נבדקו שש שנים אחרי קבלת החיסון. נמצא ששכיחות האוטיזם הייתה זהה בילדים שקיבלו חיסון MMR ובילדים שלא קיבלו חיסון זה.
האם קיים קשר בין חיסונים לסוכרת נעורים? נטען שתינוקות שקיבלו חיסון בגיל 14 חודשים במנה אחת של חיסון נגד Hib נוטים פחות לחלות בסוכרת מאשר תינוקות שקיבלו ארבע מנות מאותו חיסון. הוא הסיק מכך שניתן להפחית את הסיכון לחלות בסוכרת על ידי כך שלא יחסנו אותם בגילאים רכים מאוד. הורים מסוימים קראו את המידע הזה ובחרו להמתין עד שילדם יגיע לגיל שנתיים ואז יתנו לו את החיסון. התוצאה הזו מצערת מאוד, מכיוון שמחלות קשות מסוימות שחיסונים יכולים למנוע כגון Hib, פניאומוקוקים, ושעלת מדביקים את הפעוט בעיקר בחודשי חייו הראשונים. נמצא ששיטות ניתוח המידע של מחקר זה, היו מאוד מטעות. בנוסף מחקר שבדק פעוטות שהתחסנו בתקופות שונות של חייהם במשך 10 שנים הראה ששכיחות סוכרת נעורים הייתה זהה בקרב אלה שקיבלו חיסונים מאוד מוקדם בחייהם ובקרב אלו שקיבלו את החיסון מאוחר יותר. יתר על כן מחקר שנערך במרכז לבקרת מחלות בארצות הברית נמצא ששכיחות הסוכרת זהה בילדים שקיבלו חיסונים, ובקרב אלה שלא חוסנו כלל. כך שאין שום עדות מדעית שתתמוך במחשבה שמוטב לדחות מתן חיסונים לילד.
האם החיסון הטבעי ( לחלות המחלה) נותן לגוף הגנה יותר טובה מחיסון מלאכותי ? נכון הדבר שזיהום "טבעי" במחלה יוצר לרב חסינות טובה יותר של הגוף מאשר חיסון מלאכותי ( למעט שלושה חיסונים אשר מצליחים להעניק חסינות גבוהה יותר מזו שמקנה הדבקה טבעית: החיסון כנגד דלקת ריאה מפניאומוקוקים, החיסון כנגד צפדת (טטנוס) והחיסון כנגד Hib ). אולם בעוד שהתחלואה הטבעית מקנה הגנה חיסונית לאחר הדבקה אחת, חיסונים יצרו הגנה חיסונית בגוף רק לאחר מספר מנות אשר ניתנות על פני מספר שנים. לדוגמה החיסון "המשולש" DTaP (כנגד קרמת-צפדת-שעלת), החיסון IPV (נגד נגיף שיתוק ילדים - פוליו) והחיסון כנגד דלקת כבד נגיפית B, יחסנו היטב רק אם יינתנו בשלוש מנות לפחות. ההבדל שבין התחסנות על ידי חיסונים לבין הדבקה הטבעית במחלה הוא המחיר שהתינוק צריך לשלם כדי לקבל את החסינות הזו. המחיר שמשלמים ילדים שמקבלים חיסון הוא אי הנוחות שבקבלת מספר זריקות ומדי פעם כאב בזרוע. המחיר שמשלמים לעומת זאת בהדבקה בתחלואה טבעית הוא בדרך כלל מחלה קשה: שיתוק מהדבקה טבעית בנגיף הפוליו, פיגור שכלי כתוצאה מהדבקה בנגיף Hib, אי ספיקת כבד מזיהום טבעי בנגיף דלקת כבד נגיפית מסוג B, חירשות או עקרות כתוצאה מזיהום חזרת, או דלקת ריאות כתוצאה מהדבקה טבעית בנגיף אבעבועות רוח. כל אלו הם מחירים גבוהים יותר מדי למען השגת חסינות כנגד מחלה.
מדוע לא לחכות עד גיל שנתיים שהילדים יותר חזקים ואז לחסן ? אנו מחסנים ילדים מייד בחודשי חייהם הראשונים מכיוון שישנן מחלות מידבקות קשות מאוד אשר מדביקות תינוקות רכים מיד בתחילת חייהם. הגיל המסוכן ביותר לחלות בשעלת הוא חודשי החיים הראשונים. ילדים מתחת לגיל שנתיים נמצאים בסיכון גבוה פי 500 מבני כל גיל אחר להדבק בדלקת קרום המח כתוצאה מחיידק Hib אם גר בבית אדם עם זיהום בחיידק זה. כ־90% מהילודים אשר אמותיהם נושאות את נגיף דלקת כבד נגיפית מסוג B ידבקו בנגיף זה, יפתחו דלקת כבד אשר קרוב לודאי תהיה בהמשך למחלת כבד ממושכת (כרונית), שחמת הכבד ולבסוף עלולה להסתיים בסרטן הכבד. מסיבות אלו ונוספות, חשוב מאוד שתינוקות יהיו מחוסנים באופן מלא כנגד מחלות מסוימות כבר בינקותם ולא יאוחר מגיל חצי שנה. מערכת החיסון של תינוקות רכים מגיבה בצורה טובה מאוד ומפתחת חסינות טובה כנגד נגיפים וחיידקים. כ־95% מהפעוטות אשר יקבלו את החיסון המשולש כנגד שעלת, קרמת וצפדת (DTaP ), ילדים שיחוסנו כנגד Hib וכנגד דלקת כבד נגיפית B יהיו מחוסנים בצורה מלאה כנגד מחלות מסוכנות אלה בהגיעם לגיל שנתיים.
היסטוריית החיסונים במדינת ישראל
(נלקח מפרסום המחלקה לאפידמיולוגיה של משרד הבריאות)
פרק 4. חיסוני השגרה בישראל
שיתוק ילדים (פוליו) מחלת שיתוק ילדים הייתה אחת המחלות המאיימות, שהודברו כמעט לחלוטין, לאחר פיתוח חיסון נגד הנגיפים הגורמים אותה. בשנות החמישים והשישים של המאה הקודמת פגע הנגיף קשות במדינת ישראל וילדים רבים נפגעו במחלה קשה זו. שיעורי ההיארעות של המחלה בשנת 1951 הגיעו ל 69 מקרים לכל 100000 תושבים. בשנת 1957 הוחל במתן חיסון הזן המומת ובשנת 1961 הוחל במתן החיסון מהזן חי מוחלש. כשנה לאחר מתן החיסון שיעור ההיארעות במדינת ישראל ירד ל 8 חולים למיליון תושבים (בשנת 1962 ) בשנת 1979 נמצאו מספר מקרים בודדים בלבד (בילדים שלא חוסנו) משנת 1980 ואילך לא נרשמו בארץ ילדים חולים במחלת הפוליו. בשנת 1985 נמצא מקרה אחד במדינה הקשור לחיסון עצמו ולא להתפרצות של המחלה. הווירוס שייך לקבוצת האנטרו-וירוסים ומבחינים בשלושה זנים סרולוגיים שונים.
קליניקה – ביטויי המחלה בתקופה הטרום-חיסונית, הנגיף גרם בדרך כלל למחלה קלה, שהתבטאה בחום, בכאב ראש, בכאב גרון ובהקאות, ונמשכה עד 3 ימים. בשליש מהילדים שנפגעו בנגיף, הופיעה הישנות המחלה בחומרה רבה יותר לאחר הפוגה בת 1–7 ימים, שבה חשו בטוב. ההופעה החוזרת של המחלה התבטאה בכאבים ובנוקשות בצוואר, בגב וברגליים, ממצאים המרמזים על הדבקה בקרומי מוח השדרה - Meningitis. הממצא המאיים, שעלול להתפתח הוא שיתוק המלווה בכאבי שרירים. הפגיעה אינה סימטרית בדרך כלל, ומשתנה בחומרתה מפגיעה קלה בשרירי הנשימה ועד אי-ספיקה נשימתית - מפגיעה קלה מוחית ללא כל הפרעה תפקודית ועד לפגיעה בעצבי גזע המוח. כאשר החום יורד, נעצרת התקדמות השיתוק ועשוי לחול שיפור תוך תקופה של שנה עד שנה וחצי. יש לזכור כי רוב המקרים הקשים בשנות החמישים והשישים חייבו אשפוז מסובך במתקן המכונה ריאת ברזל – לשם חוברו הילדים במשך שנים עד התאוששות של שרירי הנשימה. רוב הפגועים נשארו משותקים בידיים או ברגליים.
בעולם השלישי – זו עדיין מחלה קשה ביותר
חיסון חשיבות החיסון ביכולתו למנוע את המחלה למעשה באופן מוחלט. מבחינים בשני סוגי חיסונים לפוליו: 1. IPV - תרכיב מומת משופר נגד שיתוק ילדים. 2. OPV - תרכיב חי מוחלש הניתן דרך הפה בטיפות. ילדים בארץ מקבלים 3 מנות חיסון מהתרכיב המומת ו-4 מנות מהתרכיב המוחלש:
- התרכיב המומת ניתן בגיל 2, 4, ו - 12 חודשים.
- התרכיב המוחלש ניתן בגיל - 4, 6, ו - 12 חודשים ומנת דחף בגיל 6 שנים.
צילום ממקרוסקופ אלקטרוני של וירוס פוליו
חיסון חי מוחלש - טיפות התרכיב המוחלש ניתן בטיפות דרך הפה. בארצות הברית תרכיב זה אינו נמצא יותר בשימוש שיגרתי למעט מקרים יוצאי דופן. התרכיב נפוץ בשימוש בהרבה מארצות העולם כולל ישראל. החיסון יעיל בהקניית חסינות לאוכלוסיות גדולות, למניעת התפרצויות פוליו.
נכון לחודש יוני 2005 – הוחלט על שינוי במדיניות החיסונים וחיסון זה יוצא מהשימוש בדומה לארצות הברית.
שני החיסונים מקנים חסינות למקבליהם. OPV - טוב יותר במניעת התפשטות המחלה. לכן בארצות שבהן שיעור הדברת הפוליו אינו דומה לזה של ארצות הברית, נפוץ עדיין השימוש בחיסון, אם כי בשילוב התרכיב מומת.
ילדים או מבוגרים שלא חוסנו מעודם כנגד פוליו ועומדים לנסוע לארץ אנדמית (ארץ בה קיימת המחלה), יקבלו תרכיב מוחלש דרך הפה 4 שבועות לפני נסיעתם. ילדים בעלי רגישות לסוגי האנטיביוטיקה- נאומיצין, סטרפטומיצין, או פולימיקסין הנמצאים בשיעורים זעירים בתרכיב המומת, או בעלי רגישות אחרת לתרכיב המומת, יקבלו תרכיב מוחלש.
תופעות לוואי בשכיחות נדירה ביותר, של 1 לכל 2.4 מיליון מנות, עלולים להופיע סימני שיתוק אצל מקבל החיסון או אצל בני המשפחה שבאו במגע עם הפרשות המחוסן. מצב זה נמנע על ידי מתן החיסון המומת (בזריקה) לפני החיסון החי-מוחלש (בטיפות). ב-1989, הוכנס לתוכנית השגרתית בארץ, מתן חיסון מומת לפני החיסון החי המוחלש ומאז לא אירע אף מקרה שיתוק בין מקבלי החיסון. אך נוכח הסיכון האפשר הוחלט על הוצאתו משגרת החיסונים. סיכונים התרכיב המוחלש עלול, אם כי לעיתים נדירות, לגרום לפוליו. נדירות ניתן למצוא תגובות אלרגיות קשות, לדוגמה: קשיי נשימה צרידות, פריחה או נפיחות צווארית. אם מופיע שיתוק, הוא יתרחש בין שבוע לחודש מקבלת החיסון. למי אסור החיסון?
- אנשים הנמצאים בטיפול ממושך בסטרואידים.
- אנשים המקבלים טיפול כימי אנטי-סרטני.
- חולי איידס או חולים בעלי מערכת חיסונית ירודה או משובשת.
- לחולים אלו אסור להחליף חיתולי תינוקות שחוסנו בתרכיב המוחלש החי שכן, הוירוס מופרש בצואה ועלול להדביקם.
- לחולים שהראו תגובה אלרגית לחיסון - אסור חיסון חוזר.
- חולים במחלה בינונית עד קשה, מנועים מקבלת חיסון עד לאחר החלמתם.
תרכיב מומת - זריקה חיסון התרכיב המומת הוא החיסון המרכזי בארצות הברית.
בארצות בהן יש עדיין התפשטות המחלה, משתמשים בשילוב שני סוגי החיסונים. בארצות הברית, שבה שיעור ההידבקות אפסי, הסיכון להיפגע מהחיסון המוחלש עולה על הסיכון להדבקות בדרך אחרת, ולכן החיסון המומת הוא השגרתי. החיסון ניתן ברגל או בזרוע בהתאם לגיל הילד/ה. החיסון יכול להינתן במקביל וביחד עם חיסונים אחרים. חיסון מבוגרים מבוגרים בדרך כלל אינם זקוקים לחיסון למעט:
- אלו הנוסעים לאזורים נגועים.
- עובדי מעבדה העוסקים בנגיף הפוליו.
- עובדי רפואה המטפלים בחולים חשודים לפוליו.
- מבוגרים אשר מעולם לא חוסנו, וילדיהם אמורים לקבל חיסון בתרכיב חי- מוחלש דרך הפה.
חולים בעלי מערכת חסינות ירודה או פגומה יכולים לקבל את החיסון המומת אם לא חוסנו בעבר. במצבים אלו בני משפחה אחרים, אשר אינם מחוסנים, אמורים אף הם לקבל את החיסון, אך רק בתכשיר המומת. קבוצות מבוגרים אלו אמורים לקבל מנה ראשונה בכל זמן. המנה השנייה 1–2 חודשים מאוחר יותר ומנה שלישית, 6-12 חודשים לאחר המנה השנייה. אלו שקיבלו זריקה אחת צריכים השלמה בשתי זריקות בלבד ללא קשר למועד החיסון הראשון. אסור לחסן :
- אנשים הסובלים מרגישות לתכשירים האנטיביוטיים: נאומיצין, סטרפטומיצין או פולימיקסין B. תכשירים אלו נמצאים בכמויות מזעריות בחיסון ועלולים לכן לגרום לתופעות אלרגיות.
- אנשים שפיתחו תגובה אלרגית להזרקה קודמת של חומר החיסון.
- חולים במחלה בינונית עד קשה, מנועים מקבלת חיסון עד לאחר החלמתם.
- נשים בהיריון, אינן אמורות לקבל חיסון כנגד מחלת הפוליו, למרות שלא תוארו כל תופעות לוואי למתן התכשיר המומת. אם מסיבה כלשהי, מתעורר צורך דחוף בחיסון אישה בהיריון, החיסון הרצוי הוא בתכשיר המומת.
מחלת חום קלה עד בינונית עקב זיהום בדרכי הנשימה, שלשול, החלמה ממחלת חום, הנקה, או קבלת אנטיביוטיקה, אינם מהווים עילה לאי קבלת החיסון במועדו. תופעות לוואי תופעות הלוואי, מלבד תגובה מקומית מכאיבה, נדירות ביותר.
גרף זה מציג את הירידה החדה בתחלואה ממחלת הפוליו בארצות הברית כתוצאה מחיסון של למעלה מ 90% מכלל האוכלוסייה. בישראל המצב עוד הרבה יותר טוב
התפתחויות בישראל במהלך בדיקה שגרתית באתר טיהור השפכים של גוש דן, נמצא נגיף פוליו שעבר שינוי משמעותי במבנה שלו. הנגיף החדש עלול להיות בעל פוטנציאל להדבקה.
נגיף פוליו (שיתוק ילדים) שעבר שינוי משמעותי במבנה שלו התגלה בסוף אפריל באתר טיהור הביוב של גוש דן (השפד"ן) בראשון לציון. הנגיף נמצא במהלך בדיקה שגרתית של משרד הביוב שתוצאותיה הגיעו שלשום למשרד הבריאות. ככל הנראה מדובר בנגיף שניתן לתינוק כחלק מחיסון, שעבר שינוי ואשר עלול להיות בעל פוטנציאל להדבקה. נגיף הפוליו עלול לגרום לשיתוק בילדים ובחלק מהמקרים מדובר בפגיעה בלתי הפיכה במערכות העצבים ועמוד השדרה.
הנגיף שנמצא במאגר השפד"ן הוא הראשון שנמצא בארץ שעבר שינוי משמעותי (השינוי בנגיף הוא בהיקף של 13%), מאז התפרצות המחלה בארץ ב-1988. נגיף הפוליו עובר במערכות הביוב וההדבקה מתרחשת בין אדם לאדם באמצעות בליעה.
פוליו בישראל – טבלה רב שנתית צהבת נגיפית מסוג A
מחלה הנגרמת על ידי נגיף שתוקף את הכבד ומועברת במזון ובמים מזוהמים ומאדם לאדם. המחלה מתבטאת בחום, חוסר תיאבון, בחילה, הקאה וצהבת. המחלה עלולה לגרום להרס מוחלט של הכבד ומוות. מחלה זו הייתה אנדמית (מגפתית ) באזורינו בשנות ה-50 ו ה 60. שיעורי ההיארעות הגיע עד 140 חולים לכל 100000 תושבים לשנה – בגלי התפרצות עונתיים. נמצא קשר ישיר בין רמת תברואה ירודה לרמת תחלואה גבוהה. חיסון מכוון לכל אוכלוסיית התינוקות החל בשנת 1999 ומאז שנה זו חלה ירידה דרמטית בשיעורי התחלואה ממחלה זו ל 12 חולים ל 100000 – ז"א כ 500 חולים בשנה בכל המדינה לעומת כ 6000 בשנה בשנות השישים והשבעים. מדובר בווירוס עמיד למדי ממשפחת ה PICORNAVIRIDIAE. הווירוס הנ"ל מועבר בדרך כלל במאגרי מים מזוהמים ומאוכל מזוהם. הווירוס שמתרבה בתאי הכבד גורם לדלקת ניכרת ולשיבוש בכל מערכות הגוף עקב ירידה ניכרת בתפקוד הכבד. המחלה מסתיימת בדרך כלל מעצמה לאחר תקופה של מספר חודשים אחרי יצירה של תגובה חיסונית של הגוף כנגד הווירוס. למעשה הגוף שלנו מסוגל להלחם בעצמו במחלה זו אך הפגיעה הממושכת והתחלואה הקשה יכולה להימנע עי החיסון. היות שהמחלה מתפשטת בדרך כלל עי הפרשות אנושיות הרי שמגפות פורצות בדרך כלל במקומות עם סניטציה ירודה עם צפיפות אוכלוסייה גבוהה. בישראל של שנות ה-50 עד השבעים לרוב אוכלוסיית הילדים עד גיל 17 – 18 ניתן למצוא כי עברו מחלה זו. הווירוס מרגע היכנסו לגוף האדם עובר למצב של דגירה הנמשכת בין 2 עד 6 שבועות. המחלה המתפרצת בסיום הדגירה ועד הופעת הסימפטומים שונה בהסתמנות בהתאם לגיל החולה. אצל ילדים בדרך כלל יש מחלה קלה הרבה יותר מאשר אצל מבוגרים או חולים כרוניים. לרוב הילדים הקטנים המחלה חולפת כשפעת קשה כמעט ללא כניסה לשלב הצהבת כך שכמעט לא ניתן לאתר אותם אלא על פי בדיקות דם לסרולוגייה בלבד. המבוגרים משלב הדגירה עוברים בדרך כלל לשלב הפעיל לאחר שבועיים של דגירה ובשלב הזה מופיעה שקיעה של בילירובין (חומר הצבע הצהוב) הנפלט מהתאים הפגועים ושוקע בעור ובלחמיות העיניים (זו הצהבת) בשלב זה ניתן לראות בבדיקות הדם שינויים בתפקודי כבד ובילירובין גבוה בדם. חלק מהחולים מדווחים על כאבי ראש קשים, כאבי מפרקים ופריחה בזמן הופעת השלב האקוטי של המחלה.
השתן בדרך כלל כהה מאוד בשל הפרשת בילירובין לשתן והצואה בדרך כלל בהירה מאוד. החלמה ממחלה זו יכולה להמשך עד חצי שנה. פגיעה בלתי הפיכה בכבד היא נדירה מאוד. מי שחלה במחלה ונחשף כבר לווירוס אינו זקוק לחיסון נוסף היות שהגוף ייצר את החיסון בעצמו. ניתן לחלות במחלה רק פעם אחת בחיים היות שהחיסון שיוצר עי הגוף מספיק לכל החיים.
ברגע שבן משפחה חלה במחלה זו חייבים לחסן את כל המחלה הן בחיסון סביל והן בחיסון פעיל לשם מניעה של התפשטות המחלה.
חיסון לצהבת נגיפית A תכשיר החיסון הנמצא בשימוש בארץ נקרא Havrix. ונמצא במינונים של 720 \ 1440 יחידות. ילדים שנולדו לאחר שנת 1999 מקבלים חיסון זה בשגרת החיסונים. ילדים שנולדו לפני שנה זו מחוסנים רק על ידי קופות החולים – עלות החיסון הגבוהה מכוסה בכל הקופות על ידי הביטוחים המשלימים.
קיימים שני סוגים שונים של חיסונים: סביל ופעיל.
חיסון סביל אם ידוע על כך שהילד בא במגע עם הנגיף, לדוגמה אם חבר בגן חולה בצהבת זיהומית, יש מקום לתת לו חיסון סביל: נוגדנים ממאגר המכיל נוגדנים ספציפיים נגד נגיף זה - Gammaglobulin. – זו תערובת של נוגדנים אשר מכינים אותה מסרום של מאות אנשים בריאים (מתוך מנות הדם). היות שרוב המבוגרים מחוסנים לצהבת נגיפית זו הרי שבתערובת נמצאים גם נוגדנים ספציפיים כנגד הצהבת יש לזכור שזהו חיסון זמני בלבד המקנה הגנה מוגבלת לתקופה של חודשים ספורים (כ 3 חודשים).חיסון זה נמצא בשימוש רב בצבא למניעה של התפרצות מגפות באזורים עם תחלופת חיילים גבוהה – כגון בסיס קליטה ומיון ובסיסי טירונות. לפני יציאה לאזור אנדמי לצהבת מסוג A מומלץ גם על מתן חיסון סביל וזאת כאשר מדובר בקבוצה גדולה של בני אדם ללא יכולת מיידית לביצוע בדיקות סרולוגיות לקביעת רמת הנוגדנים בגוף. חיסון פעיל החיסון הפעיל הוא באמצעות נגיף (וירוס) צהבת מטיפוס A מומת בפורמאלדהיד. יעילות החיסון: 94%. מינונים:
- מינון למבוגרים מכיל 1440 יחידות לכל מיליליטר.
- מינון לילדים ונוער (1–18) מכיל 720 יחידות לכל 0.5 מיליליטר.
מתי לחסן החיסון נגד צהבת נגיפית A הוכנס לשגרת החיסונים של מדינת ישראל וניתן בגילאים 18 חודשים ו-24 חודשים. פרט לתינוקות המחוסנים באופן שגרתי, מומלץ לקבל את החיסון לכל מי שאינו מחוסן, או שלא חלה בעבר, ובמיוחד בקבוצות הסיכון הבאות:
- נוסעים לארצות מתפתחות, רצוי להתחסן לפחות 4 שבועות לפני הנסיעה.
- אוכלוסיית ההומוסקסואליים.
- מכורים לסמים המזריקים לעצמם.
- חולים במחלות כבד כרוניות.
- חולים ללא נוגדנים לפני השתלת כבד.
בשל תופעות הלוואי המועטות של חיסון זה ויעילותו הרבה הרי שחיסון זה מומלץ למעשה לכל מי שלא חלה בצהבת זיהומית מסוג זה.
דרך מתן החיסון זריקה לתוך השריר. את מי לא לחסן לאנשים הרגישים למרכיבי החיסון (חומר החיסון קשור לאלומיניום הידרוקסיד, ומכיל נאומיצין וחומרי ייצוב), אין לתת את החיסון. אפשר לחסן בתכשיר, יחד עם חיסונים אחרים (במקומות הזרקה שונים). רצוי שלא לחסן בהיריון, אלא אם יש סיכון גבוה להדבקות. תופעות לוואי תופעות הלוואי נדירות יחסית חום, חולשה, כאבי ראש ובחילה בשיעורים נמוכים. נפיחות ורגישות באזור ההזרקה רגישות יתר - נדירה.
המספרים כאן מדברים בעד עצמם – מנתוני משרד הבריאות עולה כי משנת 1999 אז הוכנס החיסון לשימוש ישנה ירידה של למעלה מ 90% בתחלואה במדינת ישראל.
צהבת נגיפית מסוג B צהבת עלולה לגרום לפגיעה חמורה בכבד
דלקת כבד נגיפית (הידועה בשם צהבת) היא מחלה מידבקת, בעלת תפוצה גבוהה. בדרך כלל מופיעה המחלה בצורתה הקלה יחסית, אך במקרים מסוימים עלולה לגרום לפגיעה חמור ובלתי הפיכה בכבד. לאור זאת, ובעקבות המלצותיהם של איגודים מקצועיים ומומחים נוספים בנושא זה, פתחנו במבצע הסברה שמטרתו להבהיר את חשיבות החיסון כל בני המשפחה מפני המחלה. התחסנות תקטין את מספר מקרי ההידבקות בצהבת ואת כמות החולים והנזקקים להשתלת הכבד. ישנם מספר נגיפים, הנבדלים בדרכי ההעברה וברמת הסיבוך האפשרית של המחלה. הנפוצים ביותר הם A ו- B.
הקדמה
בישראל חיים מעל 210 אלף נשאים וחולים (כ- % 7- %2 מהאוכלוסייה). מאז 1992 מחסן משרד הבריאות כל תינוק שנולד. לאור זאת - הצורך בחיסון מפני צהבת B קיים רק לגבי בני משפחה שנולדו לפני שנה זו. המחלה עלולה לגרום לשחמת ולסרטן הכבד, ואף להתדרדר למצב המצריך השתלת כבד. נגיף צהבת B מועבר דרך דם ויחסי מין נגיף צהבת B עמיד יותר ואף נפוץ יותר מנגיף האיידס, ולכן הסיכון להידבקות גבוה הרבה יותר. %5 -10% מהנבדקים בנגיף צהבת B יישארו נשאים, כאשר בקרב הילדים האחוזים גבוהים אף יותר. אצל חלק מהנדבקים לא מופיעים סימפטומים קליניים, ולכן הם עלולים להדביק את סביבתם, מתוך חוסר ידיעה. שיעורי ההיארעות של הבת מסוג B בטרם החיסון בשנת 1992 היו כ 3 חולים ל 100000 תושבים בשנה. דבר שירד ל 1.2 לאחר התחלת החיסון.
דלקת כבד נגיפית B איננה מחלה חדשה; היא קיימת כבר מאות שנים והיא אחד הגורמים ל"מחלת צהבת" בלשון העם. הסיבה העיקרית שלא שמעת עליה, היא שלא ניתן היה לעשות מאומה בקשר אליה. ואם אי אפשר לטפל במחלה, למה לדבר עליה ? כל זה השתנה. דלקת כבד נגיפית B היא מחלה שעדיין איננה ניתנת לריפוי. לעיתים קרובות היא אף מחלה קשה, ולפעמים גורמת למוות. אך היא כבר איננה בלתי נמנעת, משום שכעת קיים תרכיב חיסון שיכול להגן עליך מהידבקות במחלה. באזורינו, מסתמנת עליה בשכיחות דלקת כבד נגיפית B. סכנת החשיפה למחלה מאימת על כולנו. יש צורך להדגיש כי קיימות קבוצות אשר בגלל עיסוקם, סגנון החיים שלהם או תנאי הקיום והסביבה שלהם נמצאות בסיכון גבוה במיוחד.
מהי דלקת כבד נגיפית B דלקת כבד נגיפית B היא מחלה נגיפית הפוגעת בכבד. בצורתה החריפה היא עלולה לגרום לסימפטומים קשים ורבים כגון: חולשה, עייפות, חום, הקאה וכן להופעת צבע צהוב בעור ובלובן העיניים (צהבת). למרות שהיא גורמת מוות לעיתים רחוקות, אלה שנתקפו בה בצורה חירפה מאושפזים לעיתים קרובות, ונזקקים לזמן רב, שבועות ואף חודשים של מנוחה והחלמה לפני שהם יכולים לשוב לחיים תקינים. תקופת הדגירה והמחלה עלולות להימשך שבועות או אפילו חודשים והחולה עלול, במשך תקופה זו להיות גורם מדבק ולהוות סכנה לכל מי שבא אתו במגע. המחלה החריפה עלולה להפוך לכרונית ב־10% - 5% מהנדבקים המבוגרים. בילדים, הסיכון להפוך לחולה כרוני עוד יותר גבוה. הצורה הכרונית של דלקת כבד נגיפית B היא מצב שונה לחלוטין, מסוכן הרבה יותר. בדלקת כבד נגיפית B כרונית הסימפטומים עלולים להיות חבויים במשל שנים, בלי שניתן יהיה להבחין בהם. נשא הנגיף איננו מרגיש דבר ואינו יודע שהוא חולה. אך במצב זה נגיף המחלה נמצא בגופו, והוא עלול להרוס את הכבד שלו בצורה איטית מאוד. דלקת כבד נגיפית B בצורתה הכרונית עלולה לגרום למוות עקב התפתחות שחמת (cirrhosis ) או סרטן הכבד. מרגע שהתהליך החל אי-אפשר לעצור אותו. המחלה איננה ניתנת לריפוי. נושא הנגיף עלול להוות סכנה נסתרת לכל הסובבים אותו. לא הוא ולא אף אחד אחר יכולים לדעת שהוא חולה בדלקת כבד נגיפית B, ואף על פי כן הוא עלול להיות גורם מסכן ושלא מתכוון הוא עלול להדביק אחרים במחלה. כיצד נדבקים?
כאמור, דלקת כבד נגיפית B היא מחלה מידבקת. הנגיף עלול לעבור מאדם לאדם למשל באמצעות דם מזוהם החודר לגוף דרך סדקים קטנים מאוד בעור, אפילו בלתי נראים לעין. לדוגמה, אם החולה בדלקת כבד נגיפית B נחתך, ואדם אחר חובש את פצעו, טיפה מדמו המזוהם של החולה עלולה לחדור לגוף המטפל דרך סדקים זעירים בעורו וכך גם הוא עלול להידבק במחלה. כדאי לדעת שכל מוצרי הדם במדינת ישראל נבדקים שגרתית. אך הדם אינו האמצעי היחיד העלול לגרום להידבקות. ידוע שנגיף עלול להימצא בכל נוזלי הגוף, כגון: רוק, זרע, הפרשות מהנרתיק. לכן אפשר להידבק במחלה גם תוך קיום יחסי מין, כמו במחלות מין; או כתוצאה משימוש במברשת שיניים, בסכין גילוח או במחט מזוהמת. כך נבדקים לעיתים קרובות אנשים החיים עם אדם הנושא את הנגיף, אנשים הקיימים יחסי מין עם יותר מבן זוג אחד, הומוסקסואלים, וצרכני סמים.
דרכי הדבקה השכיחות
- מגע הדוק עם נשא/חולה במשפחה (אחים).
- מגע עם דם מזוהם ומוצריו ומגע מיני עם אדם בריא המודבק בנגיף (נשא).
- ילוד עלול להידבק במהלך הלידה, כאשר אמו היא נשאית. סיכוייו להפוך לנשא הם כ-90% אם נדבק מאמו, לעומת פחות מ-10% בגיל מאוחר יותר. מכאן הצורך לחסן את התינוקות מיד לאחר הלידה.
האם ניתן למנוע את המחלה?
כן, בעזרת חיסון. תרכיבי חיסון גורמים למערכת החיסון הטבעית של הגוף לייצר חומרים מגינים הנקראים "נוגדנים". נוגדנים אלה מסוגלים לנטרל נגיפים וחיידקים הנכנסים לגוף ולמנוע גרימת נזק. הגוף זקוק לסוג מיוחד של נוגדנים שיגנו עליו מפני דלקת כבד נגיפית B, ונוגדנים אלה חייבים להיות בדמו לפני התקפת הנגיף. לכן יש לקבל את תרכיב החיסון לפני המגע עם הנגיף, ולא - עלול להיות מאוחר מדי. תרכיבי חיסון מונעים מחלות הם אינם מרפאים אותן. חיסון החיסון הוא חלק משגרת החיסונים בישראל. מומלץ לחסן כל תינוק, ולא רק החשופים להדבקה. יש להבדיל בין חיסון סביל לחיסון פעיל. חיסון סביל מושג על ידי מתן אימונוגלובולין ספציפי כנגד הוירוס (HEPATITIS B IMMUNE GLOBULIN). התכשירים בארץ הם: Bay-Hep ו-Hepatect. שני התכשירים מכילים 500 יחידות בינלאומיות לכל מ"ל. החיסון הסביל ניתן במשולב עם החיסון הפעיל במצבים הבאים:
- לילוד שאמו נשאית.
- לילודים שאימותיהם חולות.
- לעובדי מערכת הבריאות שנחשפו לוירוס.
חיסון פעיל חיסון פעיל, Engerix-B, הוא תוצר הנדסה גנטית ומכיל 20 מיקרוגרם של Hepatitis B Surface Antigen. המנה לילדים עד גיל 10 מכילה מחצית מכמות זו.
החיסון ניתן בשלוש מנות. בין המנה הראשונה לשנייה חודש הבדל, והשלישית ניתנת חמישה-ששה חודשים לאחר החיסון הראשון.
תינוקות מקבלים את המנה הראשונה בסמוך ללידה, השנייה בגיל חודש, והשלישית בגיל חצי שנה.
החיסון טוב לכל אחד, אך במיוחד רצוי לקבלו כאשר קיים סיכון מוגבר להדבקה (עובדי מערכת הבריאות, חולי דיאליזה, חולים המקבלים ערויי דם ומוצריו, מכורים לסמים, כל אילו החשופים למגע עם דם כולל מטפלים בנפטרים, המקיימים יחסי מין בלתי מוגנים עם פרטנרים מגוונים.) החיסון יכול להינתן במשולב עם חיסונים אחרים.
צורת החיסון
- זריקה לתוך השריר.
- תינוקות וילודים, בשריר הירך, ילדים גדולים ומבוגרים, בשריר הזרוע.
את מי לא לחסן
- רגישות לחומרי החיסון, כולל שמרים (בשל תהליך ההכנה בתאי שמר בשיטת ההנדסה הגנטית).
- תגובה חריפה למנת חיסון קודמת.
האם החיסון כנגד דלקת כבד נגיפית B הוא בטוח ? לחיסון כנגד דלקת כבד נגיפית מסוג B יש מספר תופעות לוואי. רק אחת מתופעות הלוואי היא חמורה. אחד מכל 600,000 מתחסנים במנות כנגד דלקת כבד נגיפית B יסבול מתגובה אלרגית קשה הנקראת "אנאפילאקסיס". התסמינים של אנאפילקסיס כוללים קושי בנשימה וירידה בלחץ הדם. למרות שעד היום אף אחד לא נפטר מחיסון כנגד דלקת כבד נגיפית B, הרי תסמיני תופעת אנאפילקסיס שנגרמה כתוצאה מהחיסון יכולים להיות מפחידים. הורים מסוימים עשויים לתהות לכן, האם זה באמת חיוני לחסן ילודים כנגד דלקת כבד נגיפית B. הם עשויים לשאול : איך תינוק יכול להדבק בדלקת כבד נגיפית B ? התשובה היא שלפני שהשתמשו בחיסון זה, מדי שנה נדבקו הילדים מאחד מהוריהם או מבן משפחה אחר. אחרים נדבקו מאדם שאינו גר איתם בבית ואשר בא במגע כלשהו עם התינוק (כמו מטפלת). בארץ יש כ־150,000 נשאי נגיף זה.
מכיוון שנגיף זה יכול לגרום להדבקה שקטה (הדבקה שלא תגרום לתסמינים ברורים), אנשים רבים שנדבקו בנגיף או שהם נשאים שלו אינם יודעים על כך כלל.
לא ניתן לראות מבחינה חיצונית מי מדבק ומי לא.
לפיכך תינוק עלול להדבק בחודשי חייו הראשונים מהוריו, מאחיו ומכל מי שבא עמו בקשר הדוק.
סיכום: מכיוון שיתרונותיו של החיסון כנגד דלקת כבד עולים בהרבה ובאופן ברור על הסיכונים הפוטנציאליים שלו, הרי שהחיסון הזה הוא בטוח.
יעילות החיסון לאורך שנים: Long-Term Persistence of Immunity to Hepatitis B after Vaccination during Infancy in a Country Where Endemicity Is Low
The Journal of Infectious Diseases 2004 190:1264-9 האם משהו תהה אי-פעם מה תהיה יעילותו של חיסון כגון צהבת נגיפית B 15 שנה ויותר לאחר שניתן, לאוכלוסייה שבה שכיחותו של הווירוס נמוכה. האם עדיין יהיו רמות מגינות של נוגדנים המחקר שלפנינו עוסק בשאלה זו בדיוק.
שיטות: במחקר נבדקו ילדים שנולדו לאמהות נושאת צהבת נגיפית B וחוסנו מיד לאחר הלידה. נבדקו רמות נוגדנים וכן האם הייתה הדבקה למרות החיסון. כמו כן נבדקה יעילותו של חיסון דחף באוכלוסייה זו. נבדקו 63 ילדים בהם נבדקה רמת הנוגדנים לאחר החיסון ו-52 אחים צעירים של ילדים אילו בהם רמת הנוגדנים לא נבדקה לאחר החיסון. תוצאות : בכל קבוצה נמצא אירוע בודד של הדבקה. בקבוצה הראשונה היו 32 (חצי) ילדים בעלי רמות נוגדנים כנגד צהבת נגיפית B בלתי מדידות. לאחר זריקת דחף לקבוצה הראשונה רק ב־11% מהילדים נותרו הרמות בלתי מדידות, רוב אילו שלא הגיבו לחיסון הדחף טופלו בלידתם ב-HBIG וייתכן ולעובדה זו משמעות בחוסר יצירת האפקט החיסוני. 5% הראו תגובה ראשונית לחיסון (נוגדנים מסוג IGM ) והשאר הראו רמות גבוהות של נוגדנים כנגד האנטיגן הוירלי HBSAG. האחים הצעירים הראו תוצאות דומות אך עם כייל נוגדנים מעט גבוה יותר. מסקנות: רוב הילדים שומרים על זיכרון חיסוני כנגד האנטיגן הוירלי (מדובר על תאי B כתאי זיכרון ) ומסוגלים לייצר תגובה גם 15 שנה לאחר החיסון.
צילום במיקרוסקופיה אלקטרונית של הוירוס
והנזק שנגרם לכבד
דלקת כבד נגיפית מסוג C ( הפטיטיס C) – עובד מאתר החברה הישראלית
לחקר הכבד.
מבוא נגיף ההפטיטיס C (HCV ) הוא מהגורמים העיקריים למחלת כבד כרונית בעולם המערבי. הנגיף אחראי לכ־20% ממקרי ההפטיטיס הנגיפי החריף (האקוטי), ל־70 עד 80% אחוז ממקרי ההפטיטיס הכרוני שמתוכם כ־20 אחוז יפתחו שחמת, מחלות כבד סופניות וכ־5% יפתחו סרטן בכבד. ניתן למצוא נוגדנים ל- HCV בכ־1.8% מאוכלוסיית ארצות הברית - כמעט 4 מיליון איש, עובדה המעידה ברוב המקרים על זיהום בנגיף בהווה ובחלק קטן בעבר. הפטיטיס C גורם ל - 8000 עד 10000 מקרי מוות בשנה בארצות הברית. אחד ממאפייניו המובהקים והמרכזיים של נגיף ההפטיטיס C הוא נטייתו לגרום למחלת כבד כרונית. מהלך המחלה בהפטיטיס C כרונית, כמו גם תוצאותיה, מגוונים מאוד. מצד אחד ניתן למצוא חולים ללא כל תסמינים של מחלת כבד, עם רמות תקינות של אנזימי כבד בנסיוב הדם. בביופסיה של הכבד בחולים אלה מתגלה, בדרך כלל, דרגה מסוימת של דלקת כבד כרונית, אך למרות שהם נושאים את הנגיף הפגיעה אינה קשה, והסיכויים לעתיד טובים. בקצה האחר נמצאים חולים עם הפטיטיס C קשה, מלווה תסמינים, ורמות גבוהות של אנזימי כבד בנסיוב ושינויים קשים בביופסיית כבד. במקרים אלה מתפתחות, בסופו של דבר, שחמת ומחלת כבד סופנית. רוב החולים נמצאים בין שני הקצוות, עם תסמינים מעטים או ללא תסמינים, עלייה מתונה באנזימי הכבד וסיכויים לעתיד לא ידועים. מעריכים, שכ־20% מהלוקים בהפטיטיס C כרונית מפתחים שחמת, בתהליך שנמשך בין 10 ל - 20 שנה. סרטן כבד מתפתח לאחר 20 עד 40 שנה, באחוז קטן יותר מהחולים הכרוניים. חשוב לזכור שצריכת אלכוהול, אף בכמות מעטה, מאיצה מאוד את מהלך המחלה. שחמת הכבד כתוצאה מהפטיטיס C כרונית היא אחת הסיבות השכיחות ביותר להשתלות כבד בארצות הברית, והפטיטיס C היא, קרוב לודאי, הסיבה השכיחה ביותר לסרטן כבד ראשוני בעולם המפותח. לפחות מחצית ממקרי סרטן הכבד בעולם קשורים, כנראה ל- HCV. גברים, אלכוהוליסטים, חולי שחמת, אנשים מעל גיל 40 ומי שנשאו את הנגיף בדמם למעלה מ - 20 שנה, נמצאים בסיכון גבוה יותר לפתח סרטן כבד הקשור ל HCV.
העברה וגורמי סיכון הנגיף מועבר בעיקר במגע עם דם או עם תוצרי דם הנגועים בנגיף. עירויי דם ושימוש במחטים ובמזרקים לא סטריליים היו הגורמים העיקריים להפצתו בארצות הברית. ב־1991 פותחה בדיקה שגרתית לאיתור דם המכיל נוגדני HCV, ובדיקה זו שופרה במחצית שנת 1992. מאז נבדקות כל מנות הדם באופן שגרתי, והעברת הפטיטיס C בעירויי דם חדלה לחלוטין. גורם סיכון נוסף להידבקות במחלה הוא הזרקת סמים. עם זאת, חולים רבים הלוקים בהפטיטיס C לא נחשפו לדם או לתוצריו ואינם משתמשים בסמים. קבוצת הסיכון העיקריות להפטיטיס C הן:
- מי שקיבלו עירויי דם לפני יוני 1992, מועד הכנסתן לשימוש של בדיקות רגישות להימצאות נוגדנים ל. HCV
- מי שנחשפים לעיתים קרובות לעירויי דם או לתוצרי דם. עם קבוצה זו נמנים חולי המופיליה, מושתלי איברים, חולי כליות כרוניים או חולי סרטן המטופלים בכימותרפיה.
- עובדי מערכת הבריאות שנדקרו בשוגג במחט מזרק.
- מזריקי סמים, ובכלל זה גם מי שעשו זאת לזמן קצר לפני שנים רבות.
- קבוצות אחרות הנמצאות בסיכון:
- מי שמקיימים יחסי מין המוגדרים כ"בסיכון גבוה", בעלי שותפים מיניים רבים, חולים
- במחלות המועברות במגע מיני.
- צרכני קוקאין, בייחוד בשאיפה דרך האף, המשתמשים בציוד משותף.
- ילדים להורים נשאי HCV.
העברה מאם לתינוק: שכיחות ההעברה מאם לתינוק אינה גבוהה. במרבית המחקרים נמצא כי רק 5% מהתינוקות שנולדו לנשים נגועות ב - HCV נדבקו במחלה. ביילודים, המחלה נוטה להיות קלה וללא תסמינים. סיכון ההידבקות לתינוק עולה ככל שכמות הנגיפים בדם האם גדולה יותר. לא נמצא קשר בין הנקה ובין העברת HCV. העברה ביחסי מין: לא הוכח באופן מוחלט שהדבקה בהפטיטיס C תיתכן במגע מיני, ובמחקרים התקבלו תוצאות סותרות. ממחקרים שבדקו בני זוג של חולי הפטיטיס C עלה, כי פחות מ־5 אחוזים מהם נגועים בנגיף, וכי ברבים מהם, מקור החשיפה לנגיף עלול להיות אחר. לאור מחקרים אלה, אין המלצה לחולים הקשורים לשותף מיני קבוע לשנות את הרגליהם המיניים. לאנשים בעלי שותפים מיניים רבים מומלץ לנקוט אמצעים לקיום מין בטוח, המספקים הגנה לא רק מפני הפטיטיס C, אלא גם מפני נגיפים אחרים, כמו הפטיטיס B ו HIV.
העברה מזדמנת: העברה מזדמנת של הנגיף מכונה כך כאשר מקור ההדבקה אינו ידוע. היא מתרחשת בכ־10% אחוזים ממקרי הזיהום החריף בהפטיטיס C, ובכ - 30% ממקרי ההפטיטיס C הכרונית. מקרים אלה מכונים גם זיהומים מזדמנים, או נרכשים - בקהילה. מקור החשיפה לנגיף עלול להיות חתכים, פצעים, זריקות או טיפולים רפואיים אחרים. נגיף ההפטיטיס C : HCV הוא נגיף קטן (קוטרו 40 עד 60 ננומטרים), המורכב מסליל RNA יחיד הנתון בתוך מעטפת. הנגיף עובר מוטציות (שינויים גנטיים) במהירות, והשינויים בחלבון המעטפת מסייעים לו לחמוק ממערכת החיסון. קיימים לפחות 6 גנוטיפים עיקריים ויותר מ־50 תת- סוגים של HCV. הגנוטיפים השונים נמצאים בפיזור גאוגרפי שונה. גנוטיפים la ו- lb הם השכיחים ביותר בארצות הברית ובישראל. גנוטיפים 2 ו- 3 נמצאים רק ב־10-20% מהחולים. לא קיים הבדל משמעותי בחומרת המחלה או בתוצאותיה בין הגנוטיפים השונים, אך נשאי נגיפים עם גנוטיפים 2 ו- 3 נוטים להגיב טוב יותר לטיפולים הקיימים.
תסמינים וסימנים קליניים רבים מהחולים בהפטיטיס C כרונית אינם מגלים כל תסמינים של מחלת כבד, ואם יש להם תסמינים, הרי הם קלים, לא ספציפיים ועל פי רוב לא רצופים. תסמינים אלה כוללים:
- עייפות.
- אי - נוחות או רגישות קלה בחלק הימני העליון של הבטן.
- בחילות.
- חוסר תיאבון.
- כאבי שרירים ומפרקים.
בדיקה גופנית תהיה, בדרך כלל, תקינה או תגלה רגישות או הגדלה קלה של הכבד. : בבדיקות מעבדה בדרך כלל:
- נמצא שינויים קלים בתפקודי כבד.
- עלייה מתונה ברמת בילירבין.
- עלייה קלה ברמת הכולסטרול.
דלקת כבד חריפה אבחון של הפטיטיס C חריפה נעשה על סמך שילוב של תסמינים:
- צהבת
- עייפות ובחילה,
- עלייה ניכרת ברמות ה- ALT בנסיוב (יותר מפי 10, בדרך כלל)
- נוכחות של נוגדנים, או הופעת נוגדנים תוך כדי התפתחות התסמינים.
- אבחון של מחלה חריפה עלול לקחת זמן, שכן, כאמור, הופעת הנוגדנים אינה מיידית. גם כאן, אפשר לבצע בדיקת PCR ל- RNA נגיפי, או לחזור על בדיקת הנוגדנים כחודש לאחר הופעת המחלה.
דלקת כבד כרונית: הפטיטיס C כרונית מאובחנת כאשר נמצאים נוגדנים ורמות האמינוטרנספראזות מוגברות בדם במשך למעלה מ - 6 חודשים. באמצעות בדיקת PCR ל- RNA נגיפי ניתן לאמת את האבחנה ולאשר וירמיה (נוכחות נגיף בדם). כמעט בכל החולים הכרוניים יתגלה הגנום הנגיפי בנסיוב באמצעות PCR. בחולים שאינם יכולים לייצר נוגדנים ל - HCV עקב דיכוי או הפרעה בתפקוד המערכת החיסונית תיתכן בעיה באיבחון. לכן מומלץ למושתלי איברים, למטופלים בדיאליזה, לנוטלים קורטיקוסטרואידים וללוקים באגמאגלובולינמיה לעבור בדיקת HCVRNA. קושי באבחנה ייתכן גם בחולים עם נוגדנים ל- HCV הסובלים ממחלת כבד נוספת כגון אלכוהוליזם, הצטברות יתר של ברזל או מחלה אוטואימונית, כשלא ברור מהו הגורם העיקרי לפגיעה בכבד. במצבים אלה, הימצאות נוגדנים ל - HCV עשויה לייצג תגובה חיובית כוזבת, זיהום קודם ב - HCV, או הפטיטיס C קלה בנוסף על בעיית כבד אחרת. בעזרת בדיקת RNA נגיפי ניתן, במצבים אלה, לאמת את תרומת ההפטיטיס C לבעיה בכבד. אבחנה מבדלת: אבחון שגוי של הפטיטיס C עלול להתקבל בעיקר במצבים אלה:
- הפטיטיס אוטואימונית.
- הפטיטיס B ו- D כרונית.
- הפטיטיס על רקע שתיית אלכוהול.
- סטאטוהפטיטיס (כבד שומני) שלא כתוצאה מאלכוהול NASH)).
Sclerosing cholangitis.
- מחלת וילסון.
- מחלת כבד על רקע חסר אלפא - 1 - אנטיטריפסין.
- מחלת כבד כתוצאה מנטילת תרופות מסוימות.
המאפיינים הקליניים של שחמת: בשחמת הכבד, ניתן למצוא תסמינים וסימנים בולטים יותר. אלה כוללים: חולשת שרירים, חוסר תיאבון, בחילות, ירידה במשקל, גרד, שתן כהה, אגירת נוזלים ונפיחות בבטן. הממצאים הגופניים בשחמת כוללים:
- כבד מוגדל או מוקטן.
- טחול מוגדל.
- צהבת.
- דלדול שרירים.
- מיימת.
- בצקת בקרסוליים.
תופעות חוץ כבדיות: ב־1-2% מהחולים בהפטיטיס C עלולים להופיע סיבוכים במערכות אחרות מלבד הכבד. הסיבוך השכיח ביותר הוא הופעת צמתני -קור בדם (cryoglobulinemia ), וסימניו הם:
- פריחה עורית מסוגים שונים כגון: vasculitis, purpura,, urticaria.
- כאבי שרירים ומפרקים.
- מחלת כליות.
- פגיעה עצבית (נוירופתיה).
- קריוגלובולינים, גורמים ראומטואידיים ורמות נמוכות של חלבוני משלים בסרום.
סיבוכים אחרים של הפטיטיס C כרונית הם: גלומרולונפריטיס: דלקת כרונית של פקעיות הכליה. - Porphyria cutanea tarda. מחלות שעדיין לא ברור אם יש להן קשר להפטיטיס C הן: Seronegative arthritis - Keratoconjuncivitis
sicca סינדרום( Sjogren ).
לימפומה של תאי - B לא מסוג הודג'קין. פיברומיאלגיה. Lichen planus.
איבחון: הפטיטיס C ניתנת לאבחון הנקל כאשר רמות האמינוטרנספראזות בנסיוב גבוהות ויש נוגדנים בנסיוב. הימצאות RNA נגיפי בנסיוב מאמתת את האבחנה. בדיקות נסיוב: EIA הבדיקה הראשונה לאיתור המחלה מאתרת נוגדנים לנגיף בנסיוב הדם. היא מבוססת על שיטות חיסוניות אנזימטיות Enzyme - Immuno - Assay (EIA ). בדיקות הדור השלישי (3 - EIA ) הנמצאות בשימוש הן רגישות וספציפיות יותר מקודמותיהן. אך עדיין, בדומה לכל הבדיקות המבוססות על EIA, קיימת בעיה של תוצאות חיוביות - כוזבות, ואם התשובה המתקבלת חיובית, עורכים בדיקות נוספות לאימות האבחנה. גם תוצאה שלילית של בדיקת נוגדנים ל- HCV אינה תמיד סוף פסוק. בחולים שמערכת החיסון שלהם מדוכאת, עלולה להתקבל תשובה שלילית, גם אם הם נגועים ב- HCV, שכן כמות הנוגדנים בנסיוב שלהם אינה מספיקה לגילוי ב- EIA. גם במקרים של הפטיטיס חריפה, תוצאת הבדיקה הראשונה עשויה להיות שלילית. במקרים כאלה, מבצעים בדיקה נוספת כעבור חודש שהוא פרק זמן מספיק, על פי רוב, להופעת נוגדנים. כמו כן, מבצעים לעיתים בדיקת PCR ל- RNA נגיפי שמופיע בסרום בשלב מוקדם יותר מהנוגדנים.
RNA - HCV הבדיקה הספציפית ביותר לזיהום היא RNA - HCV באמצעות שיטת הגברת PCR. בשיטה זו אפשר לאתר רמות נמוכות של RNA של נגיף הפטיטיס C בנסיוב הדם. יתרונה של בדיקה זו הוא בכך שהיא ישירה, כלומר מאתרת את הנגיף עצמו. נוכחות של RNA נגיפי בנסיוב הדם מעידה חד - משמעית על זיהום פעיל. בדיקת PCR לאיתור RNA נגיפי שימושית במיוחד כאשר רמת אנזימי הכבד מסוג טרנסאמינאזות תקינה או גבוהה רק במקצת, או כאשר לא נמצאו נוגדנים, או כאשר קיימות סיבות אפשריות אחרות למחלת הכבד. בשיטה זו ניתן לאבחן הפטיטיס C באנשים שמערכת החיסון שלהם מדוכאת, במושתלי איברים זה מקרוב, או בחולים במחלת כליות כרונית. הבעיה היא, שבדיקת PCR היא טכניקה יקרה ומועדת לטעויות, ויש להקפיד לבצעה במעבדה מאושרת עם בקרת איכות גבוהה. סמנים ביוכימיים לזיהום בנגיף הפטיטיס C : בהפטיטיס C כרונית, העלייה ברמת אנזימי הכבד אלנין אמינוטרנספראז (ALT ) ואספרטט אמינוטרנספראז (AST ) בנסיוב היא עד פי 20 (אך בדרך כלל פחות מפי 5 ) מגבול התקינות העליון.
רמות ה- ALT בנסיוב גבוהות, בדרך כלל, מרמות ה - AST, אך הממצא עלול להיות הפוך בחולים עם שחמת (בעיקר על רקע אלכוהולי).
רמות האלקלין פוספטאז והגמא גלוטמיל טרנספפטידאז (GGT ) בנסיוב תקינות, בדרך כלל. אם הן גבוהות מהתקין, הדבר עלול להצביע על שחמת.
גורם שיגרוני (Rheumatoid factor ) וספירה נמוכה של טסיות ושל תאי דם לבנים מופיעים בשכיחות גבוהה בחולים עם שחמת, ומסייעים לאיתור מחלה במצב מתקדם. רמת האלבומין וזמן הפרותרומבין (PT ) תקינים עד לשלבים מתקדמים מאוד של המחלה. רמות הברזל והפריטין עלולות להיות גבוהות במקצת.
משמעות כמות ה- RNA הנגיפי בנסיוב: רמת הנגיף בנסיוב משמשת אומדן עקיף של העומס הנגיפי וניתן למדוד אותה בכמה שיטות, בניהן PCR כמותי ובדיקת DNA מסתעף (bDNA ). לבדיקות אלה אין עדיין תקן סטנדרטי, ושיטות שונות במעבדות שונות, עלולות לתת תוצאות שונות לאותה הדגימה.
רמות ה - RNA הנגיפי בנסיוב עשויות להשתנות ספונטנית בין פי 3 לפי 10.
אין מתאם בין העומס הנגיפי וחומרת ההפטיטיס, ועומס מוגבר אינו מעיד בהכרח על סיכויים גרועים לעתיד (כפי שקורה בזיהום HIV ): אולם, קיים מתאם בין העומס הנגיפי ובין סיכויי התגובה לטיפול האנטי - נגיפי. שיעורי התגובה לטיפול באלפא אינטרפרון ובריבאווירין גבוהים יותר בחולים עם רמה נמוכה של RNA נגיפי. קיימות מספר הגדרות ל"רמה נמוכה" של RNA נגיפי, אך הערך המקובל הוא פחות מ־2 מיליון עותקים למיליליטר. ניטור העומס הנגיפי בשלבי הטיפול המוקדמים עשוי לספק מידע מוקדם על הסיכוי לתגובה. ואולם, עקב מגבלות הבדיקות הנהוגות לקביעת רמת ה- RNA הנגיפי, לא ניתן להשתמש בתוצאותיהן בצורה אמינה לצורך הנחיות לטיפול. נחוצות שיטות רגישות יותר לאמינות יותר לקביעת RNA נגיפי ועד שיהיו, אין מקום לבצע בדיקות אלה דרך שגרה. משמעות הגנוטיפ והסרוטיפ של HCV : קיימים 6 גנוטיפים ידועים ויותר מ־50 תת-סוגים של HCV (ניתן להסתייע בגנוטיפ של הנגיף בהגדרת האפידמיולוגיה של הפטיטיס C ). ידיעת הגנוטיפ או הסרוטיפ (נוגדנים ספציפיים לגנוטיפ) של HCV עשויה לסייע בטיפול. נמצא כי הסיכוי להגיב היטב לטיפול באלפא אינטרפרון או בשילוב של אלפא אינטרפרון וריבאווירין גבוה פי שלושה כמעט בחולים עם גנוטיפים 2 ו - 3. יתר על כן כאשר ניתן הטיפול המשולב, משך הטיפול המומלץ תלוי בגנוטיפ הנגיפי. לחולים עם גנוטיפים 2 ו - 3 מומלץ טיפול משולב למשך 24 שבועות, ולנושאי גנוטיפ 1 מומלץ טיפול בן 48 שבועות. לאחר זיהוי הגנוטיפ, אין צורך לשוב ולבדוק אותו שכן הגנוטיפים אינם משתנים במהלך המחלה.
ביופסיה של הכבד : ביופסיה של הכבד אינה הכרחית לאבחון, אך היא מועילה בדירוג חומרת המחלה ובקביעת דרגת הנזק לכבד. צביעות המאטוקסילין ואאוזין וצביעת מאסון תלת- צבעי משמשות לדירוג שיעור הנמק והדלקת, ולקביעת דרגת הפיברוזיס. ביופסיה של הכבד מסייעת גם לשלול גורמים אחרים למחלת הכבד, כגון נזקי אלכוהול או עומס יתר של ברזל. HCV גורם לשינויים הבאים ברקמת הכבד: נמק ודלקת סביב האזורים הפורטליים, מצב הקרוי "piecemeal necrosis ". נמק של הפטוציטים ודלקת מוקדית בפרנכימה של הכבד. שינויי שומניים. תאי דלקת באזורים הפורטליים (דלקת פורטלית). פיברוזיס, המוגבלת בשלבים המוקדמים לרווחים הפורטליים. בשלבי הביניים, הרווחים הפורטליים מורחבים ונוצר גישור בין האזורים הפורטליים לאזור המרכזי. בשלבים המאוחרים, מתפתחת שחמת המאופיינת על ידי הרס מבני של הכבד עם פיברוזיס ורגנרציה. קביעת הדרגה והשלב של הנזק מסייעת במעקב אחר חולים עם הפטיטיס כרונית. ההערכות הניתנות לדרגת הדלקת והנמק הן: העדר נזק, פגיעה מזערית, קלה, בינונית, או חמורה. באופן דומה ניתן להעריך גם את דרגת הפיברוזיס.
הטיפול ב HCV : שלוש שיטות טיפול שונות אושרו לשימוש כטיפול בהפטיטיס C:
- טיפול משולב באלפא אינטרפרון וריבאווירין
- טיפול חד תרופתי באלפא אינטרפרון.
- טיפול משולב עם פג אינטרפרון וריבאווירין (עדיין מחקרי)
שיעורי התגובה המתמשכת המתקבלים בטיפול המשולב גבוהים יותר משמעותית מאשר בטיפול החד תרופתי. הטיפול המשולב כרוך בעלייה קלה בשיעור תופעות לוואי, אך הוא יעיל יותר חד משמעית. הטיפול החד - תרופתי ניתן באינטרפרון אלפא, אך ורק בחולים שהטיפול בריבאווירין עלול להזיק להם.
קיימים כמה תכשירים של אלפא אינטרפרון (אלפא - 2a, אלפא 2b ואינטרפרון קונצנזוס.( תכשירי אינטרפרון אל הניתנים תת-- עורית שלוש פעמים בשבוע, במנות של 3 מיליון יחידות (MIU ), או, במקרה של אינטרפרון קונצנזוס, 9 מיקרוגרם להזרקה. ריבאווירין היא תרופה אנטי - נגיפית שניתנת דרך הפה פעמיים ביום, בכמוסות של 200 מיליגרם, במינון כולל של 1000 מיליגרם ליום לחולים שמשקלם מתחת ל - 75 קילוגרם, או 1200 מיליגרם למי שמשקלם מעל - 75 קילוגרם. בעקבות הטיפול החד - תרופתי או המשולב, חל שיפור מהיר ברמות ה - ALT בנסיוב ב־50 עד 75 אחוזים מהחולים, ורמת ה- RNA הנגיפי יורדת אל מתחת לסף הגילוי בנסיוב ב־30 עד 50 אחוז מהמקרים. ואולם, שיפור לטווח ארוך במחלת הכבד, חל בדרך כלל, רק אם ה- RNA הנגיפי נעלם במהלך הטיפול ואינו שב ומתגלה עם סיום הטיפול. תגובה נחשבת "מתמשכת" אם, במשך 6 חודשים או יותר מתום הטיפול, אין מוצאים RNA נגיפי בנסיוב. טיפול חד תרופתי באינטרפרון מביא להיעלמות RNA נגיפי ב־30 עד 35 אחוזים מהחולים, אך במחציתם כמעט יש נסיגה לאחר הפסקת הטיפול. שיעור התגובה המתמשכת נע אפוא בין 15 ל־20 אחוזים בלבד. הטיפול המשולב באינטרפרון וריבאווירין, לעומת זאת, מביא להיעלמות ה- RNA הנגיפי ב־50 עד 55 אחוז מהמקרים, ולאורך זמן, ב־35 עד 45 אחוזים מן המקרים. שיעור ההיעלמות של ה- RNA הנגיפי בטיפול המשולב אם כן, גדול יותר בזמן הטיפול, ושיעור הנסיגה לאחר הפסקת הטיפול נמוך יותר. משך הטיפול האופטימאלי משתנה על פי סוג הטיפול: טיפול משולב של אינטרפרון וריבאווירין או חד - תרופתי של אינטרפרון בלבד. כמו כן משתנה סוג הטיפול בהתאם לגנוטיפ של הווירוס.
המלצות הטיפול הינן: בטיפול החד - תרופתי מומלץ להמשיך 48 שבועות, ללא תלות בגנוטיפ. בטיפול המשולב, לעומת זאת, משך הטיפול המיטבי תלוי בגנוטיפ הנגיף. נושאי גנוטיפ 2 ו - 3 מגיבים בשיעור גבוה יותר לטיפול המשולב (60 עד 80 אחוזים), ודי ב־24 שבועות כדי להגיע לתוצאות השקולות לאלה של טיפול בן 48 שבועות. בנושאי גנוטיפ 1, לעומת זאת, שיעור התגובה נמוך יותר (25 עד 35 אחוזים), וטיפול של 48 שבועות משיג שיעור תגובה לטווח ארוך יותר במידה משמעותית. לאור התגובות המשתנות לטיפול, חשוב לבדוק את גנוטיפ ה - HCV לפני מתן טיפול משולב. במי מטפלים? הטיפול המשולב באלפא אינטרפרון וריבאווירין מוצע לחולים עם נוגדנים ל- HCV, עם RNA נגיפי בנסיוב, עם רמות גבוהות של אמינוטרנספראזות בנסיוב ועם סימנים להפטיטיס כרונית בביופסיה של הכבד ובהיעדר התוויות - נגד. ועדת הסכמה של מכוני הבריאות הלאומיים בארצות הברית, המליצה להגביל את מתן הטיפול בהפטיטיס C לחולים שבהם קיימות עדויות היסטולוגיות למחלה מתקדמת. הגדרה זו כוללת את החולים שבהם נמצאו פיברוזיס או דלקת מדרגה בינונית עד חמורה, ונמק בביופסיה של הכבד. לחולים עם מחלה היסטולוגית חמורה פחות מומלץ טיפול על בסיס אישי. מתן הטיפול אינו מתבסס על נוכחות או העדר של תסמינים, על אופן ההידבקות, על הגנוטיפ של הנגיף, או על רמות ה- RNA הנגיפי בנסיוב. לחולים שבהם נמצאה שחמת בביופסיה של הכבד מוצע טיפול אם אין להם סימנים של הפרעה קשה בתפקוד הכבד, כגון מיימת, צהבת, דימום מדליות בוושט או אנצפלופתיה כבדית. בחולים בני 65 ומעלה מטפלים על בסיס אישי, שכן התועלת שבטיפול בחולים אלה לא תועדה היטב, ונראה שתופעות הלוואי חמורות יותר בחולים מבוגרים יותר. מידע מועט יחסית נאסף בקשר ליעילות הטיפול באינטרפרון בילדים עם הפטיטיס C. כאשר החולה נושא גם HIV, הטיפול חייב לקחת בחשבון את התרופות הנלקחות במקביל ואת המצב הרפואי. אם ספירות ה-4CD תקינות או חריגות רק במקצת (400 (/ml < התגובות לטיפול דומות לאלה של חולים ללא. HIV בחולים עם ביטויים קליניים חוץ - כבדיים משמעותיים, כגון קריוגלובולינמיה וגלומרולונפריטיס, הטיפול באלפא אינטרפרון עשוי להביא להפוגה בתסמינים ובסימנים הקליניים. אולם, לעיתים קרובות חלה התלקחות מחודשת לאחר הפסקת הטיפול. במקרים מסוימים ניתן טיפול רציף באלפא אינטרפרון למרות התמדת ה-RNA הנגיפי בנסיוב אם התסמינים הקליניים נעלמים עם הטיפול.
מתי ובמי לא לטפל עם אינטרפרון לא מומלץ לתת את הטיפול, מלבד בניסויים מבוקרים, המקרים הבאים:
- חולים עם שחמת לא מאוזנת בגלל הפטיטיס C.
- חולים עם רמות תקינות של אנזימי כבד (אמינוטרנספראזות.(
- חולים שעברו השתלת כליה או לב.
- בחולים לאחר השתלת כבד, יש לטפל בזהירות רבה.
- חולים עם התוויות - נגד ספציפיות לטיפול החד - תרופתי או המשולב.
התוויות נגד לטיפול באלפא אינטרפרון כוללות דיכאון קשה או סינדרום נוירופסיכאטרי אחר, שימוש פעיל בסמים או באלכוהול, מחלה אוטואימונית ( כגון דלקת פרקים שגרונית, לופוס, או פסוריאזיס שאינה נשלטת כראוי, דיכוי מח העצם ואי- יכולת להבטיח מניעת היריון.
התוויות נגד לריבאווירין (וממילא לטיפול המשולב) כוללות אנמיה משמעותית, כשל בתפקוד הכלייתי, מחלת לב כלילית, או מחלת כלי דם מוחית וגם כאן, אי יכולת להבטיח מניעת היריון.
לאלפא איטנרפרון יש השפעות נוירופסיכאטריות רבות. טיפול ממושך עלול לגרום לעצבנות, לחרדה, לשנויי אישיות, לדיכאון, ואף לפסיכוזה חריפה ולמחשבות אובדניות. המועדים במיוחד לסבול מתופעות לוואי אלה הם חולים בעלי היסטוריה פסיכיאטרית חמורה או הלוקים במחלות נוירולוגיות.
נמצא קשר ישיר בין נסיגה בתגובה לאחר הפסקת הטיפול באינטרפרון ובין היסטוריה של צריכת סמים או אלכוהול. לפיכך, מומלצת גמילה של 6 חודשים לפחות מאלכוהול ומסמים לפני תחילת הטיפול באלפא אינטרפרון. כאשר יש בעיה נמשכת של אלכוהול או סמים, הטיפול נעשה בשיתוף פעולה עם מומחים או יועצים לענייני התמכרות. אפשר לטפל בהצלחה בחולים שלוקחים מתאדון. הטיפול באלפא אינטרפרון עלול לגרום להיווצרות נוגדנים עצמיים, ובטיפול הנמשך 6 עד 12 חודשים מתרחשת תגובה חיסונית עצמונית ב־2 אחוזים מהמטופלים, בפרט אם יש להם נטייה בסיסית לאוטואימוניות (הימצאות כייל גבוה של נוגדנים נגד מרכיבי גרעין או נוגדנים נגד בלוטת התריס). החרפה של מחלה אוטואימונית קיימת (כגון ראומטואידית ארתריטיס או פסוריאזיס) במהלך טיפול באינטרפרון היא תופעה שכיחה.
לאלפא אינטרפרון יש השפעה מדכאת על מח העצם. לכן עוקבים בתדירות גבוהה אחר ספירת התאים בחולים עם כשל או ציטופניות של מח העצם, כגון ספירת טסיות נמוכה (75000> תאים לממ"ק) או ירידה בספירת תאי הדם הלבנים (נויטרופניה) (1000> תאים לממ"ק). ריבאווירין עלול לגרום לתמס (המוליזה) של תאי דם אדומים בדרגה זו או אחרת כמעט בכל החולים. לכן אין מטפלים בריבאווירין בחולים עם המוליזה או עם אנמיה ידועה (11g/g1 > המוגלובין או 33% > המטוקריט). אין נותנים ריבאווירין גם לחולים עם מחלת לב של העורקים כליליים או מחלת כלי דם מוחיים, מאחר שהאנמיה הנובעת מהטיפול, עלולה לגרום לאיסכמיה משמעותית.
הריבאווירין מופרש בעיקר על ידי הכליות, וחולים במחלות כליה עלולים לפתח תמס דם חמור עד מסוכן. אין מטפלים בריבאווירין בחולים שרמת הקראטינין בדמם גבוהה מ־2.0 מ"ג לדציליטר.
ריבאווירין גורם למומים מולדים בבעלי חיים ואינו ניתן לנשים שאינן נוקטות אמצעים למניעת היריון. לנשים הרות אסור גם לקחת אלפא אינטרפרון, כי הוא פוגע באופן ישיר בגדילה ובהתרבות תאים. לבנות זוגן של גברים המטופלים בטיפול המשולב אלפא אינטרפרון וריבאווירין, אסור להרות במשך הטיפול ו- 6 חודשים לאחר סיומו. תופעות הלוואי של הטיפול:
תופעות לוואי שכיחות של טיפול באלפא אינטרפרון (ביותר מ־10 אחוזים מהחולים) כוללות:
- עייפות.
- כאבי שרירים.
- כאבי ראש.
- בחילות והקאות.
- גירוי של העור במקום ההזרקה.
- חום נמוך.
- ירידה במשקל.
- עצבנות.
- דיכאון.
- דיכוי קל של מח העצם.
- נשירת שיער (הפיכה.)
רוב תופעות הלוואי הללו קלות עד בינוניות בחומרתן, וניתן לשלוט בהן. הן גרועות יותר בשבועות הראשונים לטיפול, בייחוד לאחר ההזרקה הראשונה, ופוחתות בהמשך. נגד כאבי שרירים וחום נמוך נותנים פארצטמול (אקמול), והתופעות עשויות להציק פחות אם הטיפול באינטרפרון ניתן בערב. אם העייפות והדיכאון מציקים מאוד, מקטינים לפעמים את מנת האינטרפרון או מפסיקים את הטיפול. גם לריבאווירין יש תופעות לוואי, והתגובה לטיפול המשולב קשה, בדרך כלל, יותר מאשר לאינטרפרון לבדו. תופעות הלוואי השכיחות ביותר של הריבאוורין הן:
- אנמיה.
- עייפות ועצבנות.
- גרד.
- פריחה בעור.
- גודש באף, סינוסיטיס ושיעול.
ריבאווירין גורם לתמס תאי דם אדומים, בהתאם למינון: בטיפול המשולב, ההמוגלובין יורד בדרך כלל ב־2 עד 3 ג' לדציליטר, וההמטוקריט יורד ב־5 עד 10 אחוזים. שיעור הירידה בהמוגלובין משתנה מאוד. הירידה מתחילה בין השבוע הראשון לשבוע הרביעי של הטיפול, ולעיתים היא תלולה מאוד. בחלק מהחולים מופיעים תסמינים של אנמיה, וביניהם עייפות, קוצר נשימה, פלפיטציות (דפיקות לב מהירות) וכאבי ראש. עקב צניחה פתאומית בהמוגלובין, תיתכן תעוקת חזה ( אנגינה פקטוריס) בחולים בעלי נטייה לכך. דווח על מקרים של אוטם שריר הלב ושל שבץ מוחי בחולים שקיבלו טיפול משולב להפטיטיס C. משום כך, אין נותנים ריבאווירין לחולים שיש להם אנמיה קודמת או מחלה טרשתית משמעותית של הלב או המוח. במקרים אלו עדיף הטיפול החד - תרופתי באלפא אינטרפרון. ריבאווירין עלול לגרום גם לגירוד וגודש באף - תופעות לוואי דמויות היסטמין: הן מופיעות ב־10 עד 20 אחוזים מהחולים, ועל פי רוב, חומרתן קלה עד בינונית. ואולם, מקצת החולים סובלים מאוד מסינוסיטיס, מברונכיטיס חוזרת, או מתסימינים דמויי - קצרת (אסתמה). חשוב לדעת לשייך תסמינים אלה לריבאווירין, שכן לעיתים יש צורך לשנות את המינון ( ב־200 מ"ג ליום ), או להפסיק את הטיפול בטרם עת.
תופעות לוואי נדירות למדי ( בפחות מ־2 אחוזים מהמטופלים) של אלפא אינטרפרון ושל הטיפול המשולב הן:
- מחלה אוטואימונית (בייחוד מחלת בלוטת התריס).
- זיהומים חיידקיים קשים.
- ירידה משמעותית בספירת טסיות הדם (תרומבוציטופניה).
- פרכוסים.
- דיכאון ומחשבות אובדניות או ניסיונות התאבדות.
- דימומים זעירים ברשתית העין (רטינופתיה).
- איבוד שמיעה (וטיניטוס).
תופעות לוואי ייחודית ונדירה היא החמרה פרדוקסלית במחלת הכבד. אחת הסברות היא שהדבר נובע מהשראת הפטיטיס אוטואימונית, אך למעשה הסיבה אינה ידועה. עקב אפשרות זו, מנטרים את רמת האמינוטרנפראזות בנסיוב בזמן הטיפול. אם רמות ה- ALT עולות ליותר מפעמיים ערכיהן הבסיסיים, הטיפול מופסק והמטופל נשאר במעקב. חולים עם סיבוך זה מטופלים לעיתים בקורטיקוסטרואידים. אפשרויות טיפול לחולים שאינם מגיבים לטיפול המקובל: קיימות אפשרויות מעטות לטיפול בחולים שמחלתם אינה מגיבה לטיפול המקובל או שמגיבה בהתחלה ואחר כך נסוגה. כאשר הנסיגה חלה אחרי קורס חד - תרופתי של אינטרפרון, רצוי לתת 24 שבועות של טיפול משולב, בפרט אם ה- RNA הנגיפי נעלם במהלך הטיפול החד תרופתי ולא חזר. אפשרות אחרת היא לטפל באיטרפרון לטווח ארוך, או ברציפות, ניתן לעשות זאת רק אם הטיפול באינטרפרון נסבל היטב ויש לו השפעה ברורה על רמת האמינוטרנספראזות בנסיוב ועל ההיסטולוגיה של הכבד, גם אם ה- RNA הנגיפי לא נעלם.
תרופות חדשות: המאמץ לפתח תרופות חדשות וגישות חדשות לטיפול נמשך כל העת. הטיפול החדיש ביותר והמוביל בעולם הוא הטיפול בשילוב של פג - אינטרפרון וריבאווירין. פג- הוא אינטרפרון ארוך טווח בעל פעילות ממושכת. לפיכך ניתן להזריקו פעם בשבוע בלבד, בניגוד לאינטרפרון אלפא הרגיל הנעלם מן הגוף מהר יחסית ולכן יש צורך להזריקו מידי יומיים לפחות ע"מ להילחם בנגיף. הפג - אינטרפרון נלחם בנגיף במשך כל השבוע. כתוצאה מכך עולה יעילות הטיפול ב־50% בהשוואה לטיפול המקובל, וגם הטיפול המשולב עם ריבאווירין נותן תוצאות טובות יותר עם SUSTAINED RESPONSE של למעלה מ־50% מהמטופלים.
תרופות נסיוניות, כגון אינטרלאוקין 10 רקומביננטי (10 –( IL נבחנות עתה בניסויים מבוקרים. עוד נבחנים שימוש בציטוקינים אחרים ופיתוח של תרופות אנטי - נגיפיות חדשות, כגון מעכבי RNA פולימראז, הליקאז, או פרוטאז.
האם לספר על המחלה אין חובה לספר ולדווח על המחלה. ההחלטה היא אישית, וכן גם ההחלטה למי לספר. אנו ממליצים לספר: לבני המשפחה - חשוב מאד שבתקופת הטיפול תהיה תקשורת טובה ומערכת יחסים פתוחה ותומכת של בני המשפחה.
חברים ומקום העבודה - החלטה היא אישית ובהתאם למערכת היחסים ולאמון שיש איתם. עם זאת, יש לקחת בחשבון שתיתקל באנשים בעלי דעות קדומות. חוסר הידע לגבי המחלה הוא גדול ותיתכנה תגובות פוגעות.
בגלל אורך הטיפול והקושי שבתופעות הלוואי, יש צורך לבנות מערכת תמיכה במשפחה ומחוצה לה.
אנו ממליצים להשתתף בקבוצת תמיכה של החולים ובני/ות זוגם.
בקבוצה מעלים המשתתפים את הרגשות העוברים עליהם, הקשיים וההתמודדות עם הטיפול, ולומדים להיעזר אחד בשני ולתמוך אחד בשני. מתוך ניסיון למדנו כי קל יותר להמשיך בטיפול כאשר יש קבוצה תומכת. מה אני יכול לעשות למען עצמי בתקופת המחלה? לנוח הרבה. אין ל"הלחם" בעייפות, לאכול אוכל מאוזן ובריא. להימנע ממתחים למצוא ידידם עימם ניתן לשוחח על הרגשות הקשים. להיעזר בייעוץ מקצועי ובקבוצת תמיכה. למלא בדייקנות אחר הוראות הרופא בקשר לתרופות. לא לשתות אלכוהול. שמירה על מצב בריאותי פיזי ונפשי חזק חשובים על - מנת להתמודד עם המחלה והטיפול
מה אין צורך לשנות בחיי לאחר שנודע לי שאני חולה בהפטיטיס C ? הווירוס אינו עובר באוויר, דרך כלי אוכל, שירותים, במגע יד, חיבוק או נשיקה. הווירוס עובר במגע של דם עם דם נגוע.
אם אתה מקיים יחסי מין עם בן/בת זוג קבוע (ה) אין הכרח להשתמש בקונדום ולשנות את ההרגלים המיניים. אם אין בן/ת זוג קבוע (ה), הכרחי להשתמש בקונדום. אפשר להמשיך ולהתנהג במשפחה ובעבודה כרגיל. אין צורך בכלי אוכל או שירותים נפרדים, אפשר להתחבק ולהתנשק כמקובל במשפחה ובחברה. מה עלי לשנות ולעשות בחיי לאחר שנודע לי שאני חולה בהפטיטיס C ? לא להיכנס לפאניקה. רצוי לפנות למרפאה שתחום התמחותה כבד. לא לשתות אלכוהול בשום צורה, גם בכמויות קטנות, כי האלכוהול מחמיר את המחלה בצורה משמעותית. לא לתרום דם. להודיע לכל רופא שמטפל בכם (כולל חדר מיון אם אתם מגיעים לשם ), כי אובחנה אצלך הפטיטיס C. (גינקולוג, רופא שיניים וכו). לא לחלוק מברשת שיניים, סכין גילוח, מספרי גזיזת ציפורניים או מכונת גילוח חשמלית. רצוי מאד לקבל חיסון נגד הפטיטיס A ו B, אם אינך מחוסן כנגדן.
אבעבועות רוח והחיסון לאבעבועות
אבעבועות רוח היא מחלה נפוצה בעלת אחוזי הדבקה גבוהים בילדים ובמבוגרים לא מחוסנים. פרק זה ידון בסימני המחלה, דרכי ההדבקה בתופעות הלוואי ובחיסון הקיים היום.
הקדמה : אבעבועות רוח היא מחלת ילדים וירלית המתרחשת לרוב בשנים הראשונות לחיים. ברוב המקרים, מעבר לגרד ולתסכול שבמצב, המחלה קלה וחולפת במהירות. למרות זאת המחלה עלולה להיות לעיתים קשה בעלת סיבוכים משניים ולגרום לאשפוזים ואף לתמותה. כ-1 מכל 1,000 ילדים (בריאים שאינם חולים במחלה אחרת כלשהי) החולים במחלה יתאשפז בבי"ח. אחוז התמותה מהמחלה הוא אחד לכל 100,000 ילדים חולים. למעשה מדובר עד היום במחלת ילדות קלאסית שעדיין לא הודברה וזאת בשל אי כניסת החיסון לשגרת החיסונים (וזאת בניגוד לרוב מדינות אירופה, אמריקה הצפונית אוסטרליה ויפן שם החיסון הוא חובה כבר שנים רבות – בארצות הברית כ 12 שנים וביפן 36 שנים)
הווירוס: מדובר בווירוס המכיל DNA ונחשב לווירוס משוכלל יחסית וגדול. לוירוס זה שני שמות (בשל שתי מחלות שונות אותן הוא מחולל ) וריצלה ( (VZV-Varicalla-Zoster Virus. וירוס זה נמנה עם משפחת נגיפי ההרפס.
אפידמיולוגיה: הווירוס מדביק מאדם לאדם בהדבקה טיפתית. אזורי החדירה של הווירוס הם הריריות – כל אותן רקמות דקות ולחות של האף והלוע. כמו קיימת הדבקה דרך לחמיות העיניים. מגע ישיר מילד חולה אפשרית מאוד – הדבקה ממגע יד של ילד בריא בפצע של ילד חולים והחדרת הווירוס לפה או לעין.
התרבותו הראשונית של הווירוס מתבצעת בבלוטות לימפה אזוריות של הצוואר והלוע. ההתרבות הראשונית נמשכת כ 3 ימים. לאחר 3 ימים נוצרת וירמיה ראשונה עי פלישת הווירוס לזרם הדם והדבקת איברים שונים בגוף בעיקר כבד וטחול. התקופה הזו מכונה דגירה. לאחר דגירה של כשבועיים נוצרת וירמייה שנייה בה חל פיזור של הווירוס לעור ומופיעים הפצעים. ניתן להדבק במחלה בכל גיל – עובר ברחם יכול להדבק (מחלה קלה לעובר אם האם כבר חלתה במחלה). לאחר הלידה יכולים להדבק מלידה ועד גיל הזקנה. רוב הילדים נחשפים לווירוס לאחר גיל שנה בעיקר בזמן מגיפות – אז קיימת ירידה בכמות הנוגדנים הספציפיים שירשו מהאם והחשיפה לווירוס גדולה מאוד. עוצמת המחלה תלויה בדרך כלל ברמת הנוגדנים בגוף. בדרך כלל ילדים החולים מתחת לגיל שנה סובלים ממחלה קלה יותר אך היות שהתפתחות הנוגדנים שלהם עדיין חלשה ייתכן מאוד ויחלו במחלה פעם נוספת. רוב הילדים אכן נדבקים בין גיל 3 עד 6 שנים. מחלה מעל גיל 15 נדירה יחסית והיא מחלה קשה יותר ומסובכת יותר.
מה הם סימני המחלה ? חום, כאבי ראש וחולשה ניכרת מופיעים כ 24 ועד 36 שעות לפני הופעת הפריחה. הפריחה אופיינית מאוד ומתחילה על החזה או הבטן. ביום הראשון מוצאים בדרך כלל מספר קטן מאוד של נגעים שלפוחיתיים. ביום הבא התפרחת השלפוחיתית מתפשטת – לראש צוואר וגפיים. ביום השלישי ניתן לראות שלפוחיות בכל מקום בגוף כולל פה, אברי מין ועיניים. השלפוחיות בדרך כלל מתבקעות לאחר מספר שעות מהיווצרותן ולאחר יום- יומיים מתחיל תהליך של הגלדה והחלמה. היות שהשלפוחיות נוצרות באפידרמיס (החלק הדק והרחוק ביותר של העור) הרי שהנזק לעור קטן. אם לא יהיו זיהומים משניים הרי שלא יישארו כמעט הצטלקויות.
גרד הוא סימן חשוב במחלה וחשוב מאוד למנוע אותו. גירוד הנגעים יכול להעביר את הפצעים ממקום למקום (כולל עיניים) ויכול לגרום לזיהום משני ניכר.
מקובל מאוד טיפול כנגד הגרד עצמו על ידי תרופות אנטיהיסטמיניות. קיימות תרופות סבתא הכוללות אמבט עם קורנפלור, שמנים למיניהם (בעיקר מחיטה המכילים אומגה 6 ).
ריפוי הפצעים עד היוצרות גלד סגור אורך כ 10 ימים.
החום אמור לרדת לאחר 48 שעות מתחילת הופעת השלפוחיות. כל חום שמופיע לאחר תקופה זו (חום שלא היה קודם לכן או שנמשך מעבר ל 48 שעות מפרוץ המחלה) דורש בדיקת רופא. לא מקובל לבצע בדיקות מעבדה לשם קבלת זיהוי מעבדתי לאבעבועות רוח וזאת בשל הקליניקה הייחודית. בדיקות מעבדה מבוצעות אם חלים סיבוכים הדורשים בדיקות יותר מעמיקות (בעיקר בזיהומים משניים). נשים בהיריון או כאשר מתוכנן היריון ואין זוכרים באם הייתה מחלה מקובל לבצע בדיקת מעבדה לנוגדני הרפס. אם לא נמצאים נוגדנים מקובל לחסן.
סיבוכים משניים 1. זיהום משני בעיקר עם סטפילוקוק אריאוס או עם סטרפטוקוק. 2. מחלות בהן הגוף מגיב כנגד הנוגדנים של עצמו ופוגע בהם כאילו היו הווירוס – רוב הפגיעות במצב זה קשות. 3. הצטלקויות קשות (בחלק קטן של הנפגעים)
בזיהומים משניים מטפלים בדרך כלל במשחות אנטיביוטיות מקומיות – מקובל לשלב טיפול במשחה אנטיביוטית עם מעט סטרואידים לשם מניעת תגובת הצטלקות מקומית. בזיהומים קשים יותר מקובל לתת טיפול פומי אנטיביוטי או אפילו טיפול תוך ורידי כאשר מדובר הזיהום קשה יותר (חיידקים אלימים כגון סטרפטוקוק אלים המכונה "חיידק טורף") סיבוכים כאלה נדירים מאוד, אך אם נגרמים הרי שהמצב מסכן חיים ומחייב התערבות מיידית.
הסיבוך השני הנגרם מהיוצרות נוגדנים הפוגעים בגוף עצמו מופיע בשכיחות נמוכה והסתמנותו הקלינית מופיעה רק כ 3 שבועות מתום המחלה האקוטית. בדרך כלל המופע הקליני כולל פרכוסים, הפרעות בהליכה (שיווי משקל), הפרעות יציבה בשל קשיים בארגון מוטורי של תנועה, כאבי ראש, ישנוניות ואובדן הכרה. מצב זה דומה מעט לדלקת של המוח אך הוא נגרם למעשה מנזק למילין (תאי מעטפת העוטפים את תאי העצב ומשמשים למעשה כחומר מבודד בין העצבים). הנזק המוחי הוא רחב בדרך כלל ואם מתחילים טיפול מהיר ניתן עדיין לעצור אותו. הטיפול כולל מתן סטרואידים תוך ורידי, אימונו גלובולינים במינון גבוה, וזווירקס תוך ורידי.
את ההצטלקויות ניתן למנוע על ידי מתן טיפול בזווירקס בחולה בו רואים מיידית כי הפצעים שלו גדולים ועמוקים מאוד (קיימים מופעי מחלה קשים במיוחד בעיקר אצל חולים עם מערכת חיסון ירודה). טיפול מקומי במשחת זווירקס + אנטיביוטיקה + סטרואידים מקומי יכולים לעצור מעט את ההצטלקויות.
הטיפול בזווירקס (קיים גם בסירופ) יכול לקצר את משך המחלה במספר ימים אך אינו מונע סיבוכים משניים של המחלה עצמה.
מתי לחזור לרופא 1. כשהחום אינו יורד לאחר 48 שעות 2. חום גבוה מאוד מעל 40 מעלות הנמשך כבר 48 שעות 3. חום שנעלם והופיע שוב 4. כשהפריחה לא דומה לאבעבועות רוח 5. שינוי במצב ההכרה 6. כאבי ראש קשים, פרכוס (אפילו פרכוס חום פשוט). 7. הופעת נגעי אבעבועות בעין (מחייב הפנייה לרופא עיניים). 8. הופעת כאבי אוזניים או לוע קשים 9. זיהום מקומי של הנגעים
חיסון לאבעבועות רוח : חיסון יעיל הופק כבר בשנות השישים ביפן שם החלו לחסן לפני כ 30 שנה. חיסון זה מופק מווירוס מוחלש של הזן OKA – אותו זן בו מחסנים במדינת ישראל. ארצות הברית, קנדה ואוסטרליה החלו בחיסון המוני לילדים מגיל שנה משנת 1995. בארץ קיים החיסון מזן OKA. החיסון אינו חיסון שגרה והוא ניתן על ידי קופות החולים וממומן ברובו על ידי הביטוחים המשלימים למיניהם. החיסון מתבצע בהזרקה תת-עורית.
החיסון הנ"ל מזן OKA הקיים כבר בשימוש שנים (רבות) מונע את הופעת המחלה ב 70% מכלל המחוסנים. ל 30% מתפתחת מחלה אך בדרך כלל הרבה יותר קלה.
למרות השמועות כי החיסון יהיה יעיל רק ל 10 שנים הרי שחיסון בזן זה מראה יעילות מתמשכת ומיפן מדווחים על המשך יעילות של למעלה מ 30 שנים במחוסנים הוותיקים ביותר. תופעות הלוואי מהחיסון הן לרוב מקומיות - אודם וכאב במקום ההזרקה ולעיתים פריחה מקומית. בחלק קטן מהילדים יכולה להופיע פריחה על פני הגוף כתוצאה מהחיסון ניתן לחסן ילדים לאחר חשיפה למחלה תוך כדי 48 שעות מהחשיפה וכך למנוע את התפתחות המחלה. מבחינה כלכלית החיסון חוסך ימי מחלה רבים, עוגמת נפש ניכרת מהצטלקויות וחוסך לנו את המופע הבא של הווירוס – את שלב הזוסטר המתואר בפסקה הבאה.
שלבקת חוגרת : הרפס זוסטר (שלבקת חוגרת) היא מחלה שכיחה יחסית הנגרמת על ידי נגיף ומתבטאת בהופעת שלפוחיות לאורך עצב המלוות ובכאבים חזקים מאוד.
הרפס זוסטר נגרם על ידי נגיף הורצילה – זוסטר, אותו הנגיף שגורם בילדות לאבעבועות רוח ומופיע לכן רק אצל אנשים שחלו בילדותם במחלה זו או קבלו חיסון נגדה. לאחר חלוף אבעבועות הרוח נשאר הנגיף במצב רדום בתאי העצב. אצל חלק קטן מהאנשים תתפרץ המחלה – שלבקת חוגרת, בדרך זו: הנגיף הרדום בתאי העצב מתרבה וגורם לדלקת העצב וכתוצאה מכך לכאבים. בהמשך לכך מתפשט הנגיף אל העור וגורם להופעת פריחה שלפוחיתית. השכיחות למחלה זו עולה עם הגיל כשברוב המקרים מופיעה המחלה מעל גיל 50. עם דיכוי המערכת החיסונית השכיחות גבוהה יותר. מתח תשישות גופנית וטיפולים רפואיים שונים יכולים להגדיל את הסיכון להתפרצות המחלה. המחלה איננה מדבקת המחלה אינה מדבקת אך ילדים קטנים שלא חלו בעבר באבעבועות רוח ובאים במגע עם חולי הרפס עלולים להידבק באבעבועות רוח.
המחלה:
לאחר מספר ימים של כאבים לאורך העצב הנגוע מופיעה שם פריחה אופיינית המתבטאת בשלפוחיות בקבוצות על רקע עור אדמדם. הפריחה היא לא סימטרית, בצד אחד של הגוף ומופיעה לאורך אחד מעצבי העור. המקום הנפוץ ביותר הוא בחזה בצורת חגורה – מכאן השם "שלבקת חוגרת". מקום שני בשכיחותו הוא בעצב הפנים, בעיקר באזור המצח או אזור האף והלחי עם מעורבות לעיתים של העין. זיהום התקפי של הרפס זוסטר נמשך בין 2–3 שבועות.
סיבוכים:
הסבוך השכיח ביותר הוא כאבים באזור השלבקת החוגרת המופיע בחלק מהאנשים, בעיקר במבוגרים מעל גיל 60. הכאבים עלולים להמשך חודשים לאחר חלוף הפריחה בעור (POST HERPETIC NEURALGIAׂ). סבוך אחר הוא הרפס זוסטר מפושט בכל עור הגוף, המופיע באנשים עם מחלות קשות הגורמות לדיכוי המערכת החיסונית.
אבחנה: אבחנת המחלה היא בדרך כלל קלה על פי התמונה הקלינית והכאבים הטיפוסיים. ניתן בהחלט לקחת תרביות לווירוסים מהנגעים עצמם לשם קבלת אבחנה מעבדתית. ברוב המקרים ניתן להסתפק בקליניקה עצמה.
טיפול: מטרת הטיפול היא קיצור משך המחלה והפחתת הכאבים. הטיפול צריך להינתן מה שיותר מוקדם, ב־3-4 ימים הראשונים למחלה.
הטיפול הוא בתכשירים אנטי ויראליים ספציפיים נגד נגיף ההרפס, כמו כדורי זובירקס (אציקלווביר) או כדורי ולטרקס (ולציקלוביר) או כדורי פמביר (פמציקלוביר) הניתנים במינון גבוה. במקרים קלים ללא כאבים, ניתן להסתפק בטיפול מקומי בלבד הכולל תמיסות וקרמים לייבוש וחיטוי. במבוגרים - מנוחה וחמום מקומי יכולים לעזור במניעת הכאבים. זווירקס קיים גם בסירופ שניתן לתת אותו לילדים (במתן של 5 פעמים ביום ל 5 ימים). ילדים או מבוגרים להם קיימת פגיעה במערכת החיסון – מולדת או נרכשת חייבים בטיפול תרופתי.
במקרים של כאבים מתמשכים שכאמור יכולים להמשך גם לאחר חלוף הפריחה בעור יש צורך לטפל בכדורים נגד כאבים ולהיעזר בטיפול במרפאת כאב.קיימות בספרות עדויות שלחיסון מונע כנגד אבעבועות רוח יכולת להקטין את הסיכוי להופעת מצב זה בהמשך דרכו של הילד המחוסן.
לסיכום: למרות שעלולים לחלות באבעבועות גם לאחר קבלת החיסון הוא מקנה הגנה טובה מפני מחלה קשה ומקל על סבלם של הילדים. אין ספק כי מומלץ מאוד לחסן. החיסון בטוח וגם אם לא ימנע את המחלה הרי מניעת סיבוכים היא תוצאה חשובה לא פחות וזוהי התחלת הדרך שתוביל אולי להכחדתה של המחלה ביום מן הימים.
שאלות נפוצות לגבי חיסון זה שאלה האם מותר לחסן תינוקות מתחת לגיל שנה? תשובה החיסון כנגד אבעבועות רוח מאושר לשימוש החל מגיל שנה. שאלה לכמה זמן יעיל החיסון? תשובה עד כמה שידוע היום, החיסון יעיל לתקופה העולה על 10 שנים. יש לזכור שבמשך הזמן המחוסן בא בדרך כלל במגע עם נגיפי האבעבועות. חשיפה זאת מעוררת את מנגנון החיסון ומשפרת את הזיכרון האימונולוגי. אם ברבות השנים יתברר שהחסינות יורדת, יומלץ לתת מנה נוספת בגיל מאוחר יותר. גורם זה לא צריך להרתיע משמוש בחיסון. היות שמדינת ישראל משתמשת בזן שמקורו ביפן הרי שמידע המגיע מיפן קובע כי לאחר 37 שנות חיסון ביפן אין ירידה משמעותית ברמת הנוגדנים כלפי הווירוס. ייתכן מאוד שהשימוש בזן היפני יקנה לנו חיסון לכל החיים. שאלה האם נכון, כי מחלת האבעבועות לפני גיל שנה, אינה מחסנת, וניתן לחלות בה שוב? תשובה אין ביסוס לאמונה שמחלה בשנה הראשונה אינה מחסנת. נכון שאבעבועות רוח אצל המבוגר מסוכנת הרבה יותר מאשר כמחלת ילדים, אך הדבקה בילדות מקנה חיסון לכל החיים. שאלה האם ניתן לבדוק האם נוצרו נוגדנים למחלה בדם? תשובה כן, ניתן לבדוק את רמת הנוגדנים כנגד נגיף האבעבועות וזאת בבדיקת דם פשוטה בכל אחת מקופות החולים.
חיסון MMR – חצבת, חזרת ואדמת
חצבת חצבת היא מחלה וירלית הנחשבת למחלה אימתנית בעולם השלישי. מחלה זו תוארה לפני יותר מאלף שנים כאשר מהלך המחלה תואר בצורה מדויקת רק לפני כ 150 שנים. בשנת 1954 בודד הווירוס לראשונה ובשנת 1963 הומצא כנגדו חיסון פעיל שהיה יעיל מאוד. החיסון הוכנס לשימוש בארץ על ידי משרד הבריאות בשנת 1967.
המחלה כיסתה טרם החיסון את כל העולם. עד שנת 1963 כ 90% מכלל אוכלוסיית הילדים בעולם לקתה כבר במחלה זו.
שיעורי ההיארעות במדינת ישראל טרם החיסון עמדו על 77 ל 10000 תושבים (1967 ) בשנת 1979 ירדה ההיארעות ל 4 ל 100000. ובשנת 2001 שיעור ההיארעות ירד עד 3 למיליון תושבים. מחלת החצבת נחשבת עד היום כמחלה קטלנית במיוחד. לפי ארגון הבריאות העולמי כפי שנלקח מאתר ה CDC האמריקאי הרי שבעולם השלישי חולים כל שנה במחלה זו כ 30 מיליון בני אדם. הקף התמותה העולמי השנתי ממחלה זו נע סביב מיליון בני אדם.
וירוס החצבת : וירוס החצבת שייך למשפחת הפאראמיקסו-וירוסים הווירוס פשוט וקטן יחסית ומכיל גדיל בודד של סיב RNA. לווירוס זה זן אחד בלבד. הווירוס רגיש מאוד לתנאים חיצוניים של האקלים ואינו שורד בתנאי טמפרטורה קיצוניים. הוא נהרס על ידי או וחום כאשר משך העמידות שלו באוויר לא עולה על שעתיים.
גם וירוס זה הוא טיפול אובליגטורי של הגזע האנושי – הוא מתקיים ומתרבה אך ורק באמצעות הגוף האנושי ואין לו שום מאגר אחר בטבע.
האדם לא נושא את הווירוס ולא קיים מאגר של נשאים שאינם חולים. כל אדם שאינו מחוסן יכול להדבק בחשיפה לווירוס כאשר מקדם ההדבקה בין בני האדם מגיע כמעט ל 100 אחוז. ההדבקה טיפתית וכל התעטשות יכולה לשאת וירוס זה בקוטר הדבקה של כ 2 מטר. ולהישאר באוויר כשעתיים עד הגיע המארח הבא.
הווירוס חי בתחילת האביב בין החודשים מרץ למאי. קשה לנו לזכור את המצב בארץ לפני התחלת החיסון. בתקופה זו כל שנתיים לערך הייתה מתעוררת מגפה קשה שפגעה ברוב אוכלוסיית הילדים הלא מחוסנים. מאז תחילת החיסון בשנת 1967 חלה ירידה כמעט ב99 אחוז במקרי ההדבקה כך שהיום רק מספר ילדים בודד נדבק כל שנה.
התפתחות המחלה וקליניקה: וירוס החצבת הוא מהיר ומתרבה במספר שלבים ברורים הגוררים אחריהם סימפטומים גופניים אותם אנו מרגישים. מייד לאחר חדירת הווירוס דרך ריריות הפה והאף הוא מתחיל להתרבות באופן מקומי וזאת במשך יומיים. לאחר יומיים הוא פורץ לבלוטות לימפה אזוריות דרך מחזור הדם והלימפה (וירמיה ראשונה). לאחר 3 ימי דגירה בבלוטות הלימפה שם הוא מתרבה פורץ הווירוס שוב למערכת הדם ואז הוא מדביק את רוב מערכות הגוף (וירמיה שנייה).
מרגע כניסת הווירוס לגוף האדם והתחלת התרבות הווירוס ברקמות הלוע – אותו אדם מדביק – וזו הסיבה למהירות ההדבקה בין בני אדם שנראים בריאים לחלוטין.
מרגע ההדבקה ועד רגע הופעת הסימפטומים הקליניים של המחלה עוברים בדרך כלל כשבועיים שנקראים דגירה. לאחר כשבועיים מתחיל להופיע סימנים לא ספציפיים של מחלה המזכירה מאוד את מחלת השפעת – חום בלוטות לימפה צוואריות מוגדלות ונזלת. חלק מהחולים מפתחים אודם ניכר בעיניים שהוא אחד מהסימנים המאפיינים מחלה זו. בחלק קטן מהחולים ניתן להבחין בנקודות לבנות על הלחי הפנימית בקרבת השיניים הטוחנות – נקודות אילו מכונות נקודות קופליק. הסימן הזה מייחד את מחלת החצבת. הנקודות נעלמות מהר מאוד וקשה מאוד לאבחן אותן בשל מהירות היעלמותן – בדרך כלל נעלמות תוך פחות מיממה.
כל הסימנים הלא ספציפיים נמשכים כ 3 ימים אז מתחילה להופיע פריחה נקודתית אדומה המתחילה בקרקפת (רום הפנים) ויורדת לכיוון פנים, צוואר ומשם לידיים, גוף ורגליים. מהלך התפשטות הפריחה כ 3 ימים. במהלך ההתפשטות מופיעים משטחים רצופים בשל התחברות נקודות התפרחת. למעשה לאחר 3 ימים בדרך כלל לא רואים נקודות בודדות אלא משטחים אדומים מקובעים שאינם נעלמים בלחץ על העור.
הסימפטומים הנוספים כוללים – חום גבוה, כאבי ראש, כאבי בטן, שלשולים, שיעול ניכר, בלוטות לימפה מוגדלות. בשליש מהחולים ניתן למצוא גם מרכיבים נוספים למחלה התפתחות של דלקות אוזניים, דלקות ריאה (ראשוני של הווירוס או משני מהדבקה חיידקית מחיידק אופורטוניסט), ושלשולים ניכרים. רוב הסיבוכים נצפים במבוגרים מאוד ובתינוקות.
המרכיבים הנוספים שהוזכרו יכולים להיות קשים מאוד ואף לגרום למוות.
העלמות התפרחת מתקדמת כפי שהחלה מהראש כלפי מטה. לפני ההיעלמות ניתן לצפות בקילופי עור באזורים בהם היו רבדים גדולים וצברים של משטחים של תפרחת.
נוגדנים לחצבת ניתן למצוא בדם כ 3 ימים מהופעת הסימפטומים. בכל מקרה של חשד יש להמתין כ 3 ימים בטרם לקיחת בדיקת הדם לסרולוגייה.
סיבוכים הסיבוך הקשה ביותר במחלה זו והנדיר בין כל סיבוכיה הוא אנצפליטיס המופיעה באחד מכל 1000 חולים במחלה. סיבוך זה באם מופיע מתרחש כשבוע מפרוץ המחלה. המצב מאופיין בכאבי ראש קשים, חום, הקאות ישנוניות פרכוסים חוסר הכרה עד מוות. נזקים מוחיים מופיעים ברבע מהנפגעים. כ 15% מהנפגעים אינם שורדים מצב זה.
נתן לאבחן מצב זה בניקור מותני – מוצאים תאים וחלבון. כמו כן ב CT או MRI ניתן לראות את הנזקים. ב EEG רואים האטה כללית של הגלים המאפיינת זיהום מוחי.
סיבוך מאוחר ונדיר הוא סיבוך המכונה SSPE. מדובר בפגיעה דמוית אלצהיימר – דהיינו ספגת איטית ומתקדמת של המוח. הסינדרום מסתיים תוך תקופה לא ארוכה בהרס מוחי קשה, דמנציה מוחלטת ומוות. הסינדרום מתפתח בדרך כלל מספר שנים מסיום המחלה. לפני פיתוח החיסון ניתן היה לראות תופעות אילה באחד מכל 100.000 חולים. הסינדרום נדיר ביותר בעולם המערבי וניתן לראותו בעיקר באפריקה.
האם ניתן למות מחצבת : בהחלט כן !! אחד מכל 1000 חולים נפטר או מאי ספיקה ריאתית בשל דלקת ראות קשה או מפגיעה מוחית קשה. רוב הנפטרים הם תינוקות.
אני בהיריון וחליתי בחצבת מהם סיכויי העובר חצבת נחשבת לאחת המחלות שגורמות בשל המחלה הקשה ללידות מוקדמות או להפלות. המחלה עצמה לא פוגעת ישירות בעובר אך המחלה הקשה לאם פוגעת באופן עקיף לעובר. אין ספק כי לפני כל היריון מתוכנן יש לעבור בתחנה לבריאות המשפחה עם פנקס חיסונים בכדי לוודא כי קיבלת את כל החיסונים בייחוד את חיסוני הילדות (בייחוד לעולים חדשים שלא חוסנו בארץ)
החיסון לחצבת : החיסון הוא עם וירוס חי מוחלש הניתן כחיסון משולב בשם MMR. החיסון ניתן לכל הילדים בארץ בגיל שנה ובגיל 6 שנים. הבעיה הגדולה עם חיסון זה היא בריחה גדולה של אוכלוסיות שלמות מביצוע חיסון זה דבר הגורר אחריו הופעה של מגיפות ממוקדות באותה אוכלוסייה. באוכלוסיית מאה שערים בירושלים בה קיימת ירידה חדה בחיסון זה נצפתה הדנה מגפה נקודתית כאשר מספר המחוסנים ירד בצורה דרמטית. החיסון גורם למחלה תת-קלינית קלה מאוד היוצרת חיסון מלא ב 95% מכלל הילדים תוך מספר ימים. הזריקה השנייה המכונה בוסטר מכסה עוד 4% מהילדים אצלם החיסון לא תפס קודם לכן. חיסון בזמן דגירה של המחלה יכול בהחלט לעצור את התקדמות המחלה באותו ילד שנחשף.
זהו קטע שנלקח מעיתון מעריב ינואר - 2006 "ילד בן שבע וחצי מירושלים מת אתמול כתוצאה ממחלת החצבת. זו הפעם הראשונה זה עשור שאדם בישראל מת ממחלה זו. הילד, בן למשפחה חרדית המתגוררת בשכונת גבעת-שאול שבירושלים, אושפז לפני כעשרה ימים בבית החולים הדסה הר-הצופים כשהוא סובל מחום גבוה ומקשיי נשימה. לאחר שנבדק, התברר לרופאים כי הוא לקה בחצבת. בנוסף ציינו הרופאים, כי הילד לקה בגיל צעיר במחלה קשה. לשכת הבריאות המחוזית בירושלים קיימה בירור עם הוריו של הילד, ממנו עלה כי הוא ושתי אחיותיו לא חוסנו נגד המחלה. כתוצאה מהבירור, חוסנו שתי האחיות, אולם בינתיים הספיקו גם הן לפתח את סימני המחלה. בשלב זה מצבן הרפואי מוגדר כיציב, והן שוהות בבית תחת מעקב רפואי. כפי שפורסם במעריב, ביולי השנה אירעה התפרצות קשה של מחלת החצבת בשכונת מאה שערים שבירושלים. בעקבות התפרצות המגפה החל משרד הבריאות במבצע מהיר לאיתור ילדים שנדבקו במחלה.
על פי המידע שנאסף בלשכת הבריאות בירושלים, במהלך חודש אחד לקו 53 מתושבי העיר במחלה, מתוכם 46 שייכים לקהילת ברסלב, או מתגוררים ברחובות הסמוכים למאה שערים. "בחודש האחרון חיסנה טיפת חלב בשכונת מאה שערים ילדים רבים," סיפרה מנהלת לשכת הבריאות המחוזית בירושלים, ד"ר חן זמיר. "בנוסף, פתחנו במבצע לאיתור ילדים שלא חוסנו, במוסדות החינוך החרדיים."
זמיר הוסיפה כי "רוב החולים הם ילדים מתחת לגיל ,9 ובנוסף לקו במחלה גם 2 בחורות שנדבקו בה לאחר שטיפלו בילדים חולים. מצבם של כל החולים יציב ואף חולה לא אושפז, מלבד הילד שנפטר." לדבריה, משרד הבריאות פתח בחקירה שמטרתה לגלות אם קיים קשר בין משפחת הנפטר לקהילת ברסלב.
משרד הבריאות קרא אתמול להורים לחסן את ילדיהם על פי תוכנית החיסונים המומלצת בטיפות חלב. על פי התוכנית, חיסון נגד חצבת ניתן בכל טיפת חלב לפעוטות בגיל שנה, ומנת חיסון נוספת ניתנת בכיתה א.' "החיסון יעיל, בטוח ומונע את המחלה ואת סיבוכיה," הדגישו במשרד הבריאות."
מקריאת הקטע ברור כי המחלה קיימת והיא אלימה. אין ספק כי ירידה של רמת החיסון באוכלוסייה של חלתה מאז 1967. מעלה מאוד את הסיכון להתפרצות היות שהחיסון לא מגן על כולם. כאשר קיימת ירידה של רמת החיסון הכללית באוכלוסייה מתחת ל 70% מתחילים לראות את ההתפרצויות שראינו בירושלים.
תופעות לוואי מהחיסון : 1. תופעות לוואי מקומיות – תפרחת מקומית, גרד, נפיחות מקומית, אודם מקומי. 2. תופעות אלרגיות משמעותיות מיידיות – מרגישות לחלבון החיסון (רגישות הדומה לרגישות לאנטיביוטיקה) התופעות כוללות בצקת בדרכי הנשימה, ירידה בלחץ דם – המכונות אנפילקסיס. חולה שידוע כי רגיש לנאומיצין שהוא אחד ממרכיבי החיסון יחוסן רק תחת השגחה בחדר מיון בנוכחות רופא. 3. חום המופיע לאחר כ 10 ימים וזאת בשל מחלה תת-קלינית שיוצר הווירוס המוחלש. בחלק מהילדים ניתן לראות אפילו תפרחת קלה הנעלמת בדרך כלל תוך 24 שעות. 4. טרומבוציטופנייה ניכרת על רקע אימוני – תופעת לוואי נדירה החולפת לאחר מספר שבועות. בזמן הירידה בטסיות הדם ניתן לראות כתמים אדומים כחולים על עור הידיים והרגליים הדומים לחבורות ללא חבלה.
ילדכם קיבל חיסון - האם יש קשר בין התפתחות אוטיזם לחיסון ? לא !! הייתה שמועה כזו לפני מספר שנים שהופצה עי קבוצת חוקרים שבבסיס אמונתה היה כי החיסונים עצמם פוגעים בילדים. את השקפת עולמם זו גילמו בנתונים שקריים ובתוצאות מוטות ולא נכונות. בשל פרסום גלובאלי חסר פרופורציה נוצרה ירידה חדה במספר החיסונים לחצבת בארצות הברית דבר שגרר אחריו התפרצות קשה מאוד של חצבת. בבדיקה בכל העולם שבוצעה כלפי החיסון לא נמצא שום קשר לאוטיזם אצל מקבלי החיסון.
סיכום מדובר במחלת ילדים קשה מאוד שפגעה קשה בארצנו עד לפני כ 50 שנה. קשה לזכור את אותה תקופה היות שתיעוד מדיה אלקטרונית לא היה קיים. המחלה גורמת למוות וחשוב מאוד שכל האוכלוסייה תתחסן בכדי להגן על אילו שאינם מחוסנים. ירידה בחיסון תביא מיידית לאותן מגפות גדולות שראינו בעבר.
שני גרפים שונים שמקורם ממשרד הבריאות – החתכים משנים שונות ניתן לראות את הירידה החדה בשיעורי התחלואה מאז הוחל במתן החיסון.
חזרת זו אחת ממחלות הילדים המוכרות ביותר בעולם. בשנות השישים המחלה הייתה נפוצה מאוד עם שיעורי היארעות של כ 180 חולים ל 10,000 תושבים - זה אומר שבשנות השישים חלו בארץ במחלה זו (כל שנה) כ 10,000 ילדים. מאז הוכנס לשימוש בשנת 1967 חיסון יעיל כנגד מחלה זו הפכה המחלה לנדירה יחסית. שיעורי ההיארעות מגיעים ל חולה אחד על כל מיליון תושבים בשנה. למרות שהייתה מחלה נפוצה מאוד הרי שברור כי מדובר במחלה קשה (יחסית). למרות שחמישים שנה כמעט ולא ראינו חזרת הרי שבזיכרון הקולקטיבי של כולנו נשארה החזרת כמחלה שהיא קוריוז בלבד וכמעט אף אחד לא זוכר כמה קשה הייתה התקופה בה חלו ילדים במחלה זו. בעברית נקראת המחלה "חזרת" מכיוון שהיא יוצרת אצל החולה פנים נפוחות המזכירות את פני החזיר.
העיסוק המחודש במחלה נובע מהעובדה כי למחלה זו יש נטייה לחזור. היות שהאדם הוא המאחסן היחידי של הווירוס וברור כי ווירוס זה לא נעלם מהעולם הרי שכל ירידה ברמת החיסון במדינה כלשהי מעלה מייד את מספר הנדבקים במחלה.
מסתבר שבבריטניה למשל בה נפלו שיעורי חיסון הילדים מ-92% מהילדים בשנת 1995 לסביבות 80% מהילדים בשנים 4–2003. אין כלל ספק שהירידה הניכרת בהיענות לחיסון המשולש MMR בבריטניה תורמת שם להתפרצות המחלה בראשית 2005, ואמנם לאחר שמספר מקרי החזרת הנרשמים מדי שנה בבריטניה החל משנת 1995 עמד על כ-600 נצפתה עלייה תולה ברבעון האחרון של 2004 ונרשמו סך של 2,800 מקרים, וכאמור בינואר 2005 מעל 5,000 מקרים מה שבמבטא ממדים של מגפה.
ילד חולה בחזרת
הוירוס : נגיף החזרת הוא נגיף RNA חד-גדילי העטוף במעטפת והשייך למשפחת נגיפי פּאראמיקסוֹ, הגורם למחלה מידבקת חריפה, בעיקר בילדים בגיל 5 עד 15 שנה, אך גם במבוגרים צעירים, ואינה שכיחה בילדים מתחת גיל שנתיים. הפצתה על ידי שאיפת טיפות לחות בהן נמצא הנגיף, הנפלטות לחלל האוויר בשעת שיעול או עיטוש של אדם נגוע בנגיף, והאדם הוא המאחסן היחיד של נגיף זה. כל נוזלי הגוף נגועים בווירוס – רוק, דמעות, CSF, נוזלי זרע, מי שפיר. הווירוס רגיש מאוד לאור אולטראסגול, פורמלין וחומרי הרדמה כגון כלורופורם ואתר. רוב ההדבקות בסוף החורף ובתחילת האביב
המחלה יחסית מדבקת ומתפשטת מהר בקרב בני משפחה או אלה הנמצאים בקרבת החולה בה. מספר הנדבקים המשניים ממגע עם חולה הוא כ-10 עד 12, כאשר לשם השוואה מחלת החצבת הנחשבת ליותר מדבקת, עלולה להדביק 15 עד 17 נדבקים משניים. התרבות הווירוס מתבצעת ברקמות מערכת הנשימה ובבלוטות לימפה צוואריות אזוריות. הדגירה נמשכת כשבועיים עד שלושה ומשלב זה מתחילה חדירה של וירוס זה למחזור הדם. בשלב הווירמיה כל מערכות הגוף חשופות להדבקה כולל מערכת הרבייה, מוח וקרומיו בלוטות רוק ולבלב.
התחלת המחלה מתבטאת בסימנים לא ספציפיים המתאימים לכל מחלת חום ויראלית הכוללים, עייפות, ירידה בתיאבון וחום. 40-50% מההדבקות יסתיימו ללא אירועים נוספים ויראו כנזלת או מחלה וירלית קלה.רק לאחר תקופה זו מופיעים התסמינים המאפיינים את החזרת. הסימן השכיח ביותר המתרחש ב-30-40% מהחולים הוא דלקת של בלוטות הרוק. הדלקת יכולה להיות חד- או דו-צדדית, כאשר ב-90% מהם היא דו-צדדית. טמפרטורת הגוף עלולה להגיע עד 40 מעלות צלזיוס כאשר תפיחות הבלוטות מגיעה לשיאה ביום השני, והיא מופיעה ב-95% מהמקרים התסמינים של חזרת. לרוב הסימנים מופעיים ביומיים הראשונים של המחלה ולעיתים קודמים להם כאבי אוזניים או כאבים בזווית הלסת התחתונה. משך הדלקת לרוב 7–10 ימים והיא חולפת ללא סיבוכים מיוחדים המשפיעים על תפקוד בלוטות הרוק בהמשך.
ההנחיה בדרך כלל היא לילדים בגיל הגן או בית הספר, להימנע מחזרה למוסדות אלה למשך 5 ימים מהופעת בלוטות הרוק הנפוחות. לעיתים, רגישות מקומית וכן כאבי אוזניים מופיעים לפני נפיחות בלוטות הרוק. דלקת הבלוטות נובעת מהדבקה ישירה של האפיתל של צינוריות הרוק, ואז נמצא ערכים מוגברים של האנזים עמילאזה ממקור בלוטות הרוק בנסיוב.
שלושים אחוז מההדבקות בחזרת הן בעלות מהלך תת-קליני, כאשר במקרים אחדים חזרת מתרחשת ללא נפיחות בלוטות הרוק. למרות שהתסמינים דומים, המהלך הקליני של המחלה במבוגרים ובמתבדרים קשה יותר מאשר מהלכה בילדים. בנוכחות של דלקת בלוטות הרוק והתנפחותן במיוחד בעת של התפרצות ידועה של המחלה, אבחון חזרת הוא פשוט, אם כי גורמים אחרים להתנפחות דו- או חד צדדית של בלוטות הרוק ראויים להתייחסות. גורמים מדביקים אחרים כגון נגיפי קוקסאקי, parainfluenza ו-influenza A, נגיף אפשטיין-בר, אדנו-וירוס ואף הדבקה חיידקית הגורמת להצטברות מוגלה. סיבות אחרות להופעת נפיחות זו הם אבנים בבלוטות הרוק, שאתות מקומיות, תסמונת Sjögren, בליעת עמילן או תרופות תיאזידיות, או רגישות ליוד.
צילום של הווירוס במיקרוסקופ אלקטרוני סכימה של הווירוס סיבוכי מחלת החזרת:
ברוב המקרים הילדים הנדבקים בנגיף החזרת מחלימים לחלוטין, אם כי לעיתים נדירות תסמיני המחלה עלולים לחזור ולהחמיר תוך כשבועיים.
הסיבוכים שנצפו כוללים:
דלקת קרום המוח:
לפני שהוכנס החיסון המשולש, נגיף החזרת היווה את הגורם השכיח ביותר של דלקת נגיפית של קרום המוח-מנינגיטיס, וכן אחת הסיבות המובילות לאבדן שמיעה בילדים תחת גיל 15 שנה בבריטניה. על בסיס בחינה מיקרוסקופית של נוזל השדרה ומציאת ריבוי של תאי-דם לבנים (pleocytosis), נראה שבמחצית של כל ההידבקויות בנגיף החזרת יש מעורבות של מערכת העצבים המרכזית. סיבוכים נוירולוגיים בנוסף לדלקת קרום המוח, כוללים את דלקת המוח (אנצפאליטיס) באחוז זעיר (1:6,000) מהמקרים, יכולים אף להופיע במקרים רבים ללא תופעה של התנפחות בלוטות הרוק, ואז אף עלול להיגרם נזק עצבי קבוע כמו חֵרשות עצבית או שיתוק חד צדדי של עצבי הפנים.
דלקת של המוח: גברים צעירים הם בסיכון הגבוה ביותר לתופעות מנינגו-אנצפליטיות אלה. פרכוסים מתרחשים בילדים עם תופעות נוירולוגיות, למרות שמבחן EEG בהם בדרך כלל תקין. במקרים אלה עלולים להופיע תסמינים ככאבי-ראש, צוואר נוקשה, תרדמת או ישנוניות. אם כי כאמור המעורבות של מערכת העצבים המרכזית בהדברות בנגיף החזרת ברוב הקרים שפירה ללא נזק ארוך טווח, לעיתים נדירות נמצא מצבי הידרוצפאלוס חסימתי המביא להצטברות מים בחדרי המוח, כאמור התחרשות חד-צדדית, דלקת בנוזל השדרה (מיאליטיס), או מקרי איבוד של תיאום שרירים והליכה בלתי יציבה (שיגשון או ataxia).
סוכרת?? סיבוך מוכר אחר במקרי חזרת הוא התפתחות של דלקת הלבלב (פנקראטיטיס), שעלול להופיע עוד לקראת סוף השבוע הראשון של המחלה. מצב זה מתאפיין על ידי בחילות, הקאות וכאבים ברום הבטן וניתן לאבחנו על ידי עלייה ברמת אנזימים של בלוטת הלבלב כגון ליפאזה או עמילאזה פנקריאטית. דלקת הלבלב כתוצאה מחזרת בדרך כלל חולפת ללא סיבוכים מקץ שבוע.
דלקת באשכים:
הסיבוך היותר שכיח המתרחש ב-20% מבין הגברים הנדבקים בחזרת אחרי הגיעם לבגרות מינית, היא דלקת מכאיבה בדרך כלל באחד האשכים או ב-15-30% מהמקרים בשניהם (אוֹרְכיטיס), כאשר בעת ההחלמה עלולים האשכים להצטמק, ב-13% מהמקרים תהיה ירידה בפוריות ובמקרים נדירים אף תופיע עקרות.
הדבקת תאי הפּארֶנכימה באשך עלולה להביא לתהליך של אטרופיה באשך בכמחצית המקרים עם אורכיטיס.
דלקת בשחלות:
ל 5% מהנשים הנדבקות בנגיף החזרת בגיל שלאחר הבשלות המינית, עלולה להופיע דלקת באחת השחלות או בשתיהן (אוֹפוֹריטיס) המתבטא בכאב במורד הבטן, ואך במקרים נדירות לעקרות.
סיבוכים נדירים
חזרת עלולה לפגוע גם באיברים אחרים לעיתים נדירות: כך נרשמו מקרים שלך דלקת כליות, דלקת מפרקים (ארטריטיס), דלקת בבלוטת המגן (תירואידיטיס), דלקת שריר הלב (מיוקרדיטיס) ואף באופן נדיר ביותר דלקת הכבד (הפאטיטיס). יש נתונים על עליה בשיעורי הפלות בנשים הרות הנדבקות בנגיף החזרת בשליש הריונן הראשון.
מוות מחזרת : מוות עקב מחלת החזרת הוא נדיר. בארצות הברית מדווח בממוצע על מקרה מוות אחד לשנה עקב סיבוכים של מחלת החזרת. בעבר טרם החיסון היו מקרי מוות נפוצים יותר והשכיחות המדווחת הייתה של 1–3 לכל 10.000 חולים.
בדיקות המעבדה: חלק ממצאי המעבדה בהדבקות בנגיף החזרת כוללות לעיתים תמונה של ירידה בספירה של תאי דם לבנים (לוֹיקוֹפּניה) עם עליה יחסית במקטע הלימפוציטים בדם, ולעיתים אף בספירת נויטרופילים. ייתכן למצוא שקיעת דם מוחשת או עליה ברמת המדד לדלקת CRP. כבר כ-11 יום מהחשיפה לנגיף, וברוב המקרים בעת הופעת התופעות הקליניות, כבר ניתן לגלות בנסיוב נוגדנים מסוג IgM הספציפיים לנגיף החזרת, וניתן אף לגלות נוגדנים אלה בדגימות רוק. אם לא מתגלים נוגדנים יש המבצעים בדיקה מעבדתית מהירה כ-PCR לגילוי חומצת הגרעין (RNA) של הנגיף. את הנגיף עצמו ניתן לבודד אפילו מהשתן עד שבועיים לאחר תחילת הסימנים הקליניים. כאשר נגיף החזרת הוא הגורם למנינגו-אנצאפאליטיס נמצא בנוזל השדרה עודף לימפוציטים (בממוצע 250 תאים בממ"ק), עליה ברמת החלבון, וירידה ברמת גלוקוז עם לחץ פתיחה נורמאלי בדיקור מותני של נוזל השדרה. ב-96% מהמקרים עם תופעות מנינגו-אנצאפאליטיס ניתן לגלות חומצת גרעין של הנגיף בנוזל השדרה בשיטת PCR, עד שנתיים לאחר האירוע. נוגדני IgM ספציפיים לנגיף נמצאים במחצית הקרים, לעיתים עד שנה ממציאת ספירת תאים מוגברת בנוזל השדרה.
טיפול: אין טיפול רפואי מקובל או יעיל בעת התרחשות המחלה. כאשר חזרת מופיעה בתקופת היריון אין כל מידע על מומים מולדים בילוד. הידבקות אחת בנגיף החזרת מספקת בדרך כלל חיסון לכל החיים. על פי ארגון הבריאות העולמי (WHO) חיסון של כ-90% מהילדים בגיל שנתיים בתרכיב המשולש MMR או measles, mumps rubella, ימנע התפרצויות של מגפות חזרת באוכלוסייה.
החיסון לחזרת : בימים טרם התחלת החיסון בארצות הברית תועדו בה מעל 200.000 מקרי חזרת לשנה. בישראל הייתה שכיחות החזרת גבוהה מאוד כ 158 מקרים ל 100000תושבים. בשנת 1987 לפני החיסון הנוכחי חלו בישראל יותר מ 10000 תושבים. 90% מהחולים היו בני 15 ומטה. מאחז החיסון חלה בישראל ירידה חדה במספר החולים – 7 ל 100000 תושבים בשנת 1990 (385 חולים מדווחים). בשנת 1995 נרשמה ירידה נוספת ל 2 מקרים לכל 100000 תושבים ( 120 חולים). מאז התחלה של חיסון שני בכיתה א בשנת 1995 נרשמה ירידה חדה במספר חולים החזרת - בשנת 2001 נרשמה שכיחות של 1 למיליון תושבים (6 חולים באותה שנה) החיסון הניתן (כחלק מחיסון ה-MMR) הוכנס לשימוש בשנת 1977. החיסון מבוסס על וירוס חי מוחלש. חיסון בודד בוירוס זה מקנה חסינות כנגד הדבקה 90% מהמחוסנים. מי שמתחסן הרי שהחסינות היא לכל החיים. רוב הילדים שחוסנו בגיל שנה היו בעלי נוגדנים כנגד הדבקה בגיל 10.5 שנים (יעילות של כ 80% ). בשל היעילות שהייתה רק 80% לאחר חיסון ראשון בגיל שנה הוחלט לאחר מספר שנים לבצע חיסון נוסף בגיל 6 שנים דבר המעלה את יעילות החיסון ל 99%. תופעות לוואי מהחיסון נדירות מאוד. דלקת קרום המח מתוארת בתדירות של מקרה בודד לכל חצי מיליון מחוסנים.
את מי אסון לחסן 1. חולים עם פגיעה מולדת או נרכשת במערכת החיסון 2. נשים בהיריון (אסור לחסן 3 חודשים בטרם היריון מתוכנן) 3. העת רגישות מוכרת ומתועדת לנאומיצין או לגלטין
לסיכום : מדובר במחלת עבר שרוב הרופאים במדינת ישראל כבר לא ראו מימיהם וטוב שכך. מחלה זו יכולה ויודעת לחזור בכל ירידה ברמת החיסון הכללי באוכלוסייה וזאת ראינו כבר במדינה מפותחת כמו בריטניה בה חלו בשנת 2005 יותר מ 5000 בני אדם. השנה עדיין לא ברור כמה חלו בה. אין ספק כי מדובר בווירוס שפגיעתו רעה. שמירה על רמת חיסון גבוהה באוכלוסייה יכולה למנוע התפרצויות מחודשות של ווירוס זה. המצב בישראל -מגפת חזרת במזרח ירושלים
התגלו 23 תלמידי בי"ס שלקו במחלת החזרת. הסיבה: הרשות הפלסטינית מסרבת לאמץ את תוכנית החיסונים הישראלית. אחיות טיפת חלב של משרד הבריאות הישראלי הוזעקו לחסן מאות תלמידים פלסטיניים במזרח ירושלים, לאחר שהתגלו 23 מקרים של מחלת החזרת. התפרצות המחלות נבעה מכך שהרשות הפלסטינית מסרבת לאמץ את תוכנית החיסונים הישראלית, ומחסירה חיסונים רבים חיוניים המונעים מחלות קטלניות. לשכת הבריאות המחוזית בירושלים אשר קיבלה את ההודעה על מגפת החזרת, הורתה לאחיות טיפת חלב לחסן את תלמידי בתי הספר במזרח ירושלים. נכון למועד כתיבת מאמר זה חוסנו 400 תלמידים בבית הספר בו אובחנו המקרים. תלמידי שני בתי ספר נוספים יחוסנו בהמשך היום. סך הכול יחוסנו קרוב ל-900 תלמידים במזרח ירושלים.
(נלקח מאתר משרד הבריאות) אדמת – Rubella
הקדמה :
מדובר באחת ממחלות הילדות הקשות ביותר והמאיימות ביותר אשר השאירו את חותמן על בני הדור הקודם לשלנו.
בשנות השבעים המחלה הייתה אחת המחלות הויראליות הנפוצות ביותר ובשנת 1972 הגיע שיעור ההיארעות לשיא של 548 חולים 100000 תושבים (כ 30000 חולים בשנה זו). היות שכך מיד בשנת 1973 הוחל בחיסון כל הבנות שהגיעו לגיל 12. בשנה לאחר מכן שיעור ההיארעות ירד ל 31 ל 100000. בשנת 1978 שוב התפרצה המחלה הפעם בשיא אדיר של 960 מקרים לכל 100000 תושבים ( כ 500000 חולים בשנה ). מאז ישנה ירידה ניכרת בשיעורי ההיארעות והממוצע הוא 23 חולים ל 100000. משנת 1988 שונתה מדיניות החיסונים וחיסון זה ניתן לכל ילד שהגיע לגיל 15 חודשים (MMR ). בעקבות התפרצויות נוספות בשנים שבאו לאחר מכן שונה שוב בשנת 1994 לוח החיסונים והוסף חיסון בגיל 12 חודשים וחיסון שלישי בגיל 6 שנים. מאז השינוי שיעור ההיארעות ירד ל 1 למיליון תושבים בשנה (כ 5 חולים בשנה במדינת ישראל).
המחלה תוקפת בעיקר בחורף ובתחילת האביב. התחלואה הייתה מאופיינת במגיפות שהתרחשו כל 5–9 שנים.
היסטוריה : השם העברי אדמתתורגם מהשם הלטיני רובלה שמשמעו אדום וקטן. הפיצול של מחלה זו ממחלות החום יוצרות התפרחת האחרות – שנית וחצבת החל רק בשנת 1814 עד שנה זו נחשבה מחלת האדמת כסוג של שנית או חצבת. היות שההפרדה קרתה בגרמניה כונתה מחלה זו בכל העולם בשם "חצבת גרמנית". בשנת 1914 הוברר במחקרים שבוצעו במוחות של קופים כי מחלה זו מועברת על ידי וירוס.רק בשנת 1938 נמצאה ההוכחה כי וירוס זה פוגע גם באדם. הווירוס עצמו זוהה ובודד לראשונה בשנת 1962.
וירוס האדמת שייך למשפחת ה- togavirus, זהו וירוס מבוסס RNA העטוף במעטפת. הווירוס אינו יציב בסביבה החוץ תאית ונהרס בקלות על ידי גורמים שונים כגון חום או חומרים כימיים.
ההדבקה : ווירוס האדמת מועבר מאדם לאדם על ידי פיזור באוויר מהפרשות שמקורן במערכת הנשימה (שיעול, התעטשות – קוטר פיזור הווירוס בהתעטשות אחת עולה על מטר וחצי).וירוס זה נישא ומועבר על ידי המין האנושי בלבד ואין למצוא אותו במינים אחרים של בעלי חיים. הווירוס חודר למערכת הנשימה לאחר ביצוע החדירה הוא מתרבה ברקמות הלוע ובבלוטות הלימפה האזוריות. התרבות ראשונית זו נמשכת בין 5–7 ימים. לאחר ההתרבות הראשונית יוצא ווירוס זה למחזור הדם בתהליך המכונה וירמיה, ומתפשט בכל הגוף. הווירוס נעלם ממחזור הדם ברגע בו הופיעה פריחה שהיא אופיינית מאוד למחלה.
את הווירוס ניתן למצוא בצואה במשך כ 11 עד 12ימים –למעשה ניתן למצוא אותם כ 4 ימים טרם הפריחה ועד 4 ימים מסיומה. כמו כן ניתן למצוא את הוירוס בחלל הלוע כשבוע טרם הופעת הפריחה ועד כשבוע לאחר העלמה, דבר המצביע כי החולים במחלה מדבקים במשך כל זמן המצאות הווירוס בלוע ובצואה ולא רק בזמן הופעת הפריחה.
תקופת הדגירה של המחלה – זאת אומרת השלב בין ההדבקה ועד תחילת השלב הקליני של המחלה נע בין 12–23 יום, (בדרך כלל שבועיים). משך המחלה הקליני נע בין 5–7 ימים ומתחיל מרגע הופעת הפריחה.
כשבוע לאחר הופעת הפריחה חלה ירידה משמעותית בכמות הוירוסים בחלל ומשלב זה החולים אינם מדביקים. בזמן הפריחה החולים נחשבים למדביקים ביותר ובשלב הזה נוהגים לבודד חולים אילו מבתי הספר גני ילדים ומקומות עבודה.
מהלך המחלה : חשוב לציין כי בטרם היות החיסון ובזמן מגפות גדולות למעלה מ 50% מכלל הילדים שנדבקים במחלה אינם מפתחים סימפטומים כלשהם והם עוברים מחלה זו בלא ידיעת הוריהם. צורת הדבקה זו שאינה גוררת תחלואה ברורה יכולה לגרום להתפשטות המחלה על ידי ילדים חולים שאינם יודעים בכלל כי הם חולים. בילדים צעירים אשר מפתחים את תסמיני המחלה הרי שהתפרחת היא הסימפטום הראשוני ולפניו אין סימנים אחרים.
במבוגרים יותר או במבוגרים ניתן לפעמים למדוד חום שבין 37.5 ועד 38.5 וכן קיימת הרגשת חולשה, הגדלת בלוטות לימפה ונזלת 1–5 ימים טרם הופעת הפריחה (הפרודרום של המחלה = סימפטומים מקדימים). בחלק מהחולים ניתן לראות בלוע יום לפני הופעת הפריחה על הגוף, נקודות אדומות קטנות על החיך הרך.
הפריחה באדמת מאוד אופיינית ומופיעה לרוב באזור הפנים ומשם מתפשטת לכיוון הרגליים. הפריחה איננה מגרדת ולכן גרד יכול להצביע על אבחנות אחרות ולא אדמת. צבע הפריחה ורוד ומורכבת מנקודות קטנות לא מרשימות, צפופות מאוד שאינן מתחברות למשטחים על אזור הבטן יכולה צפיפות ניכרת של הנקודות להיראות כמשטח אך במבט בוחן ניתן לראות כי מדובר בנקודות נפרדות. משך הפריחה הוא כ-3 ימים. תחילת הפריחה מלווה בהופעתם של נוגדנים כנגד אדמת בדמו של החולה.
הסימנים הקלאסיים של המחלה – ז"א לאחר הופעת התפרחת היא הופעת של בלוטות לימפה נפוחות עורפיות או מאחורי האוזניים הבלוטות כואבות אך נעלמות בסוף המחלה התופעות הנוספות כוללות כאבי מפרקים – סימן זה מופיע בעיקר במבוגרים – מופיע ב 70% מהחולים מעל גיל 15. דלקת מפרקים אמיתית הכוללת נפיחות אודם והגבלת תנועה פחות שכיחה אך גם היא מופיעה ב 50% מכלל המבוגרים החולים. לרוב מדובר בדלקת של מפרקי אצבעות הידיים ושורש כף היד ובאחוז נמוך גם מפרק הברך. הדלקת מופיעה בזמן הופעת הפריחה. הכאבים חולפים תוך 4 שבועות מתחילת הדלקת. מהלך ארוך יותר הוא נדיר.
סיבוכים : הסיבוך הקשה ביותר של מחלה זו היא אנצפליטיס שהיא דלקת של רקמת המח. תהליך זה הוא נדיר ומתועד יותר במבוגרים בשכיחות של 1 לכל 7500 חולים קיימת שכיחות גדולה יותר אצל נשים ביחס של 1 ל 2. סיבוכים נוספים כוללים דלקת באשכים – בדרך כלל בבנים מתבגרים כאשר השכיחות גם כאן די נמוכה 1 לכל 3500 חולים. אירועים של דמם קשה – בעיקר דרך מערכת העיכול מדווח גם הוא בעיקר במבוגרים הנוטלים תרופות המונעות קרישה כגון אספירין או קומדין וזאת בשל ירידה זמנית במספר טסיות הדם בדומה למחלת ITP.
אדמת ונשים בהיריון \ תסמונת אדמת מולדת התיעוד הראשון על תסמונת האדמת המולדת הגיע מגרמניה משנת 1941. במחקר רטרוספקטיבי לבדיקת מספר לא סביר של פגיעות עיניים מולדות ( קטרקט ) באזור מצומצם במחוז אחד עלה כי שנה קודם לכן נדבקו כל אותן אמהות צעירות במחלת האדמת בזמן מגפה גדולה במחוז. נשים היו בשלבי היריון מוקדמים בזמן התפרצות המחלה ולחלקן אף לא הייתה אדמת קלאסית הכוללת תפרחת אלא מחלה תת-קלינית. זו הייתה העידות הראשונה כי לווירוס זה יכולת בזמן הווירמיה של המחלה לעבור שלייה ולגרום להדבקת העובר במחלה קשה. משנות הארבעים ועד סוף שנות השישים נצפו עשרות אלפי ילדים בארצות הברית שסבלו מתסמונת זו שהסתבר שגורמת גם לחירשות עצבית (בדרך כלל באוזן אחת). גם בישראל של שנות השישים נצפו מאות ילדים שנולדו עם תסמונת זו. מאז תחילת שנות השבעים של המאה הקודמת בהם הוחל לחסן כנגד המחלה חלה ירידה דרסטית בהופעה של אדמת מולדת כאשר בארץ תסמונת זו נעלמה לחלוטין בשנת 1994.
ידוע ממחקרים ארוכי טווח כי וירוס האדמת הוא אחד הוירוסים המזיקים ביותר לרקמותיו של העובר. הוא משפיע למעשה על כל הרקמות וגורם למומים מולדים רבים וכן למוות תוך רחמי של העובר, לידה מוקדמת או הפלה. גודל הנזק הנגרם לעובר תלוי בשלב ההיריון בו חלתה האם כשככל שההיריון צעיר יותר כך מידת הנזק גדולה יותר.
מידת החדירות של הווירוס לשלייה הוא גבוה מאוד ויותר מ 85% מהתינוקות שאימם סבלה מאדמת בשליש הראשון להיריון יסבלו מפגיעה של סינדרום האדמת המולדת. אם האם חלתה לאחר השליש השני להיריון הרי ההסתברות לפגיעה בעובר נמוכה מאוד.
פגיעות שנצפות בילדים: 5. קטרקט בעיניים 6. חירשות (ברוב המקרים באוזן אחת) 7. מומי לב (ASD, VSD, PS ) – פגיעות במחיצות ובמסתמים 8. פגיעה מוחית שגורמת לראש קטן ופיגור שכלי 9. דמם קשה של הילוד 10. צהבת מולדת קשה מאוד 11. הגדלת כבד וטחול 12. פגיעה במינרליזציה (בהתגבשות הסידן) של העצמות
אבחון: הבדיקה הטובה ביותר היא בדיקת נוגדנים המתפתחים מספר ימים מאז תחילת המחלה. הנוגדנים הספציפיים הראשונים המתפתחים הם מסוג IGM – זהו נוגדן גדול יחסית המתפתח מהר ותפקידו בהרס הווירוס. לאחר מספר שבועות רמת ה IGM יורדת והשארית שנשארת כזיכרון תמידי הוא נוגדן ספציפי מסוג IGG אשר מציאתו וכמותו מאשרים לנו חשיפה בעבר לווירוס או חיסון מלא. הנוגדן משייט באופן קבוע במחזור הדם ובכל חשיפה נוספת כמותו עולה במהירות ומשמידה כל וירוס פולש מסוג זה
החיסון לאדמת : החיסון הניתן אושר לשימוש החל בשנת 1979. מדובר בזן של וירוס חי מוחלש שאינו מכיל חלבונים מכל מקור אחר מלבד אנושי. הוירוס המדובר אינו מדבק אחרים למעט דרך חלב אם. ניתן לחסן עם וירוס זה כחיסון בודד או בשילוב עם חיסון כנגד חזרת או בשילוב משולש עם חיסון כנגד חזרת וחצבת (זהו השילוב המקובל בארץ בגיל שנה ובכיתה א, בנות מחוסנות פעם נוספת בתחילת התיכון. למעשה כל חיסון כנגד אדמת בארץ יינתן כחיסון משולב כנגד חצבת וחזרת יחד).
מתן החיסון בגיל שנה ומעלה מספק תגובה חיסונית ב-95% מהילדים. ב-90% מהמקרים מספק החיסון הנ"ל הגנה למשך 15 שנה לפחות אך בחלק גדול מהמקרים החיסון מספק כנראה הגנה לכל החיים.
בדיקות לרמה חיסונית בהיריון – האם לבדוק רמת נוגדנים ? לא. אין צורך לבדוק יותר את רמת הנוגדנים. היות שכל נערה מקבלת את החיסון פעמיים עד גיל הפוריות הרי שאין צורך בבדיקה של רמת הנוגדנים. מקובל לתת חיסון בטיפת חלב אחרי הלידה ולא לבדוק את רמת הנוגדנים. ההחלטה עדכנית לשנת 2006.
חיסון בזמן היריון – מותר ? לא. היות שמקור החיסון בווירוס חי מוחלש הרי שאין לחסן בזמן היריון. לפי הוראות משרד הבריאות אין להיכנס להיריון מתוכנן כחודש מקבלת חיסון זה. על פי החלטת האחות בתחנה לבריאות המשפחה ניתן לחסן נשים הרות מבוגרות שלא יודעות האם חוסנו או לא רק לאחר הלידה. ניתן לבצע בדיקת נוגדנים בחשד לחשיפה במשרד הבריאות בלבד. הבדיקה הוצאה מסל הבריאות בשנת 2006.
מהן תופעות לוואי מהחיסון ? תופעות הלוואי בילדים ותינוקות מינוריות אך קיימות ברוב המתחסנים וכוללות חום ואי שקט. במבוגרים תופעות הלוואי כוללות הגדלת בלוטות לימפה וכאבי פרקים הנמצאים ב 10-25% מכלל המתחסנים בחיסון זה. תופעות הלוואי יכולים להמשך עד 3 שבועות מהופעתם (כ 5 – 10 ימים מהחיסון
האם קיים טיפול למחלת האדמת ? הטיפול במחלת האדמת הוא טיפול תומך בלבד. המחלה עוברת מעצמה ללא צורך בטיפול מיוחד. יש צורך במעקב של סקירת מערכות מדוקדקת בכל אישה בהיריון שחלתה באדמת.
לסיכום : מחלה "קלה" זו ידעה בימיה הטובים בשנות השישים לגבות מחיר כבד מאוד בכול העולם. רק בארצות הברית נפגעו ממחלה זו בשנות השישים כ 50.000 ילדים בפגיעות כרוניות קשות. התחלת חיסון יעיל בשנות השבעים גרר אחריו ירידה חדה ולמעשה היעלמות של אדמת מולדת בכול העולם המערבי (כולל ישראל).
יש לשמור על רמה חיסונית טובה במחלה זו היות שאם הרמה החיסונית הכללית באוכלוסייה תרד מייד נזכה לחידוש התפרצויות האדמת שלא נכחדה מהעולם.
ניתן לראות כי מאז שנת 1995 אין אף מקרה של אדמת מולדת בישראל
חיסון DTP – דיפטריה שעלת וטטנוס
שעלת
הקדמה שכיחות המחלות המידבקות עולה מסיבות שונות, ובהן הגידול באוכלוסייה והצפיפות בערים, התפתחות זני חיידקים העמידים לאנטיביוטיקה והידרדרות בתוכניות לבריאות הציבור. בשנת 1996 ציין ארגון הבריאות העולמי את מחלת השעלת כאחת מעשר המחלות הקטלניות ביותר בעולם (לצד מחלות כגון איידס, שחפת, צהבת, קדחת ועוד). על-פי נתוני הארגון, בשנת 1995 אירעו ברחבי העולם כ-350,000 מקרי מוות משעלת. חלה עלייה חדה במספר החולים בשעלת בישראל. להלן יוצגו בתמציתיות מידע על מחלת השעלת, נתונים על שכיחותה בארץ וסקירה קצרה על היקף המחלה בעולם, על דרכי מניעתה והטיפול בה ועל המחלוקת סביב תופעות הלוואי של החיסון נגדה. השנה מתחוללת התפרצות קשה של מחלת השעלת בישראל: על-פי נתוני משרד הבריאות חלו במחלה מאז תחילת השנה יותר מ-1,000 איש, אולם מעריכים כי מספרם האמיתי של החולים מגיע לאלפים. לאור חומרת המצב פרסם מנהל המחלקה לאפידמיולוגיה, ד"ר פאול סלייטר, חוזר מיוחד, שבו מפורטות הקלות אחדות בחיסון נגד שעלת הניתן לתינוקות. זאת במטרה לבלום את התפשטות המחלה בישראל. בין היתר הוחלט להקדים את מתן החיסון הראשון נגד המחלה מגיל שמונה שבועות לשישה שבועות. עוד נקבע כי יש לצמצם את הרווח בין הזריקה הראשונה לשנייה ובין השנייה לשלישית לארבעה שבועות במקום שמונה, כמקובל היום. ועדת ההיגוי של המחלקה לאפידמיולוגיה במשרד הבריאות המליצה באחרונה להוסיף מנת חיסון נוספת נגד המחלה בכיתה א'.
התקפי שיעול שטפי דם סביב ובתוך העיניים חיידק השעלת – Bordetella Pertussis – גורם למחלה ממושכת בדרכי הנשימה, המופיעה בשכיחות גבוהה בעיקר בקרב תינוקות בני פחות משנה. משך תקופת הדגירה של החיידק הוא שבוע; לאחריו מופיע חום, מלווה בהפרשה מרובה מהאף, שנמשך 1–2 שבועות, ובהמשך מופיע שיעול המחמיר בהדרגה. שיעול זה מופיע בהתקפים שבסופם חרחור ("Whoop"). זהו השלב הקשה והמסוכן של המחלה, שבו החולה עלול לסבול ממצוקה נשימתית. שלב זה נמשך 3–6 שבועות, ולאחריו יש שלב החלמה, שבו השיעול פוחת בעוצמתו ובתדירותו, והוא נמשך 2–3 שבועות. המחלה עלולה לגרום סיבוכים קשים עד כדי סכנת מוות – כגון דלקת ריאות ודלקת קרום המוח – בעיקר בקרב תינוקות. ההידבקות בשעלת מתרחשת בעת מגע ישיר, פנים מול פנים, עם החולה, או במגע עם הפרשות החולה (כמו רוק). תיאור זה של התפתחות המחלה נכון בייחוד בקרב ילדים, ואילו בקרב מבוגרים התסמין העיקרי של המחלה הוא שיעול ממושך.
היסטוריה: לא נמצאו תיאורים של השעלת בעת העתיקה או בימי הביניים. נראה כי מחלה זו החלה להופיע רק בסוף ימי הביניים. השם פרטוסיס נקבע במאה ה 17 ומקורו בלטינית ופירושו שיעול קשה. בשנת 1906 בודד חיידק השעלת ונקבע בשם Bordetella Pertussis ורק 30 שנה מאוחר יותר בשנת 1935 נמצא חיידק נוסף ששמו Bordetella ParaPertussis האחראי על 5 אחוז מכלל ההדבקות במחלה זו. פיתוח והפצה של חיסון יעיל החלה בשנת 1947.
אפידמיולוגייה: מנתוני הלשכה המרכזית לסטטיסטיקה עולה כי מאז שנת 1999 חלה עלייה ניכרת במספר מקרי התחלואה בשעלת: בשנת 1999 עצמה נרשמו 311 מקרים, לעומת כ-100 מקרים בממוצע בכל שנה בשבע השנים שקדמו לה. בשנת 2003 דווח על 914 מקרים של שעלת, לעומת 546 מקרים בשנת 2002 (עלייה בשיעור 70% בקירוב). יתר על כן, בבחינת שיעור התחלואה במחלה זו בשנת 2004 (חודשים ינואר–אוגוסט) מתגלה עלייה של יותר מ-100% במספר המקרים בהשוואה לתקופה המקבילה בשנת 2003 (977 לעומת 478 מקרים בהתאמה). מפרסומי משרד הבריאות עולה כי המגמות שאובחנו בישראל בשיעורי השעלת ב-25 השנים האחרונות שונות מאלה שאובחנו באיחוד האירופי ודומות לאלה שאובחנו בארצות-הברית. בשנת 2001 אובחנו בישראל 8.9 מקרים של מחלת השעלת ל-100,000 תושבים. מההשוואה בין שיעור מקרי השעלת בישראל בשנה זו לבין שיעורם בכמה מדינות מערביות עולה כי שיעורי השעלת בישראל היו נמוכים פי 3–6 מהממוצע באיחוד האירופי, וגבוהים מהממוצע בארצות-הברית (2.7 מקרים ל-100,000 תושבים), ובמדינות כגון דנמרק (3.4 ל-100,000), בריטניה (1.8 ל-100,000) וספרד (1 ל-100,000). פתולוגיה: מדובר בחיידק קטן ועגול שאינו נצבע בצביעה המכונה צביעת גרם ומכאן תכונת הצבע שלו היא גרם שלילית. החיידק נעזר לשם התקדמותו והמשך קיומו ברעלנים רבים המופרשים ממנו. החיידק נעזר גם בחלבוני הצמדה המסייעים להיצמדותו לרקמות הרירית אליה הוא חייב לחדור. אלימותו הגדולה של החיידק נובעת מפעילות הרעלנים המסוגלים לגרום לשיבוש ניכר במערכת החיסון ( ולמעשה לקריסתה ולהופעת זיהומים משניים), ולפגיעה בריריות עצמן על ידי חומרי פירוק. קליניקה: את הקליניקה הקלאסית ניתן לראות בדרך כלל אצל ילדים הגדולים מגיל שנתיים. במבוגרים מגיל 60 שוב לא רואים את הקליניקה הקלאסית המתוארת בספרות. לאחר תקופת דגירה הנמשכת כשבועיים מתחילים להופיע סימפטומים קליניים כאשר המחלה מתוארת באופן קלאסי כבעלת שלושה שלבים נפרדים הנמשכים ביחד כחודש וחצי. 1. השלב הקטראלי – שלב הנזלת, שיעול ודמעת (שלב זה דומה מאוד להצטננות רגילה – אפילו ללא חום. הסימפטום הקלאסי שהוא השיעול הולך ומתגבר ואינו נפסק. 2. השלב השני מכונה השלב הפרוכסיסמאלי –שלב השיעול ההתקפי. בשלב זה מופיעים התקפים קשים מאוד של שיעול מאוד ייחודי בקולו היות שהוא מופיע בזמן מעבר אוויר דרך גלוטיס בצקתי מאוד (השיעול מכונה whooping ) בזמן שיעול זה יכולה להופיע הכחלה או האדמה של הפנים מהמאמץ. על פי רוב מופיעים סימנים לעלייה בלחץ בפנים בזמן השיעול הכוללים פקיעת נימי דם בפנים ובעיניים. חלק מהשיעולים ההתקפיים מסתיימים בריור רב או בהקאות. התקפי שיעול מופיעים הן ביום והן בלילה ומוחמרים בכל גירוי קל של בית הדיבור. בין ההתקפים אין שום קליניקה. 3. שלב ההחלמה – בו השיעולים מתחילים לסגת עד ריפוי מלא. חשוב להבין כי מזה שנים רבות לא רואים כבר את שלושת שלבי המחלה הקלאסיים והסיבות מגוונות וכוללות: חיסון שהוכנס ושינה את המחלה, שימוש מיידי במשאפים למיניהם, שימוש מהיר מאוד באנטיביוטיקה שלא היה זמין כל כך ומשנה את הקליניקה. ההגדרה היחידה לשעלת היא קליניקה של שיעול התקפי מעל 21 יום והמצאות הוכחה מעבדתית לשעלת (משטח לוע, נוגדנים או PCR חיובי). כל הוכחה מעבדתית חיובית עוד לפני 21 יום נחשבת לשעלת חיובית. במקרים בהם הקליניקה חיובית אך אין הוכחה מעבדתית אך יש קשר ישיר לחולה אחר עם הוכחה מעבדתית הרי שהמקרה חיובי מבחינה אפידמיולוגית. אצל מבוגרים מאוד התקפי השיעולים אינם מאפיינים ולכן יש לחפש הוכחה בכל מקרה של שיעול מעל 21 ימים. ובתינוקות מתחת לגיל שנה שם יכול להופיע מצב דמוי חנק או קוצר נשימה קשה דמוי התקף אסתמה.
שעלת בגילאים השונים: מהטבלה למטה שמקורה במשרד הבריאות ניתן לראות כי השכיחות הגדולה ביותר של מקרי שעלת חדשים לאורך כל השנים היה בקבוצת הגיל של תינוקות מתחת לגיל שנה האחראים על 50% מכלל התחלואה. ניתן לראות כי במשך השנים קבוצת הגיל הזו דעכה אך חזרה לאותה רמה והיא האחראית לגידול הניכר במספר חולי השעלת – דבר שגרם לשינוי במבנה החיסון. ניתן גם לראות בבירור תרומה הולכת וגוברת של ילדים מעל גיל 5 בתחלואה וזאת בכפולות של פי 2 כל עשור – דבר שהביא בשנת 2004 לחיסון נוסף חמישי בכיתה א'. קיים זיהוי טוב יותר של המחלה המציג לנו כי בין גיל 15 ל 45 קיימת אפשרות לחלות אך המספרים עדיין נמוכים. מספר חולי השעלת הקשישים הוא נמוך מאוד לכל אורך המעקב.יש לשים לב כי הנתונים עדכניים לשנת 2001 השנה בו נחתם הסקר אך אין עדיין נתונים חדשים של משרד הבריאות בנוגע לשנים האחרונות.
שכיחות לפי גיל ושנה (נתוני משרד הבריאות) אבחנה מעבדתית של שעלת: 1. משטח לוע 2. בדיקת נוגדנים ומציאת נוגדנים מסוג IGM – רק לאחר כשבועיים של מחלה 3. בדיקת PCR – בדיקה מדויקת מאוד להוכחה מהירה של קיום החיידק 4. בדיקה לא ספציפית – ספירת דם ומציאת לימפוציטוזיס ניכרת
השעלת בישראל: החיסון הוכנס לישראל בשנת 1957 וניתן כחלק מחיסון DTP ב 4 מנות בגיל חודשיים ארבעה שישה חודשים וגיל שנה. ברוב העולם המתועש מקובלת מנה נוספת בגיל 5 שנים – גיל כניסה לבית ספר (ארצות הברית – כיתת גן). מאז הוחל בחיסון נרשמה ירידה חדה במספר החולים וזאת עד שנת 2000. משנה זו החלה עלייה כלל עולמית (בעולם המערבי) במספר החולים במחלה זו. בעוד שעד שנת 2000 נרשמו לא יותר ממאה חולים בשנה הרי שבשנים 2003 - 2004 הגענו ל 1000 חולים ובשנת 2005 – 2006 ליותר מ 2000 חולים. חלק גדול מהעלייה המספרית מקורו בשיטות אבחון טובות יותר – PCR ולא רק משטחים וסרולוגייה דבר המאפשר אבחון יעיל יותר ומהיר יותר. כמו כן חלה עלייה ניכרת במודעות המערכת הרפואית דבר שגרם לשליחה של הרבה יותר דגימות לבדיקה. ייתכן ומספר כה גדול של חולים – 1000 השנה מתגמד ליד המספר האמיתי שהוא גבוה בהרבה ותלוי במספר הדגימות הנשלחות. בשל כל הנ"ל נוצר צורך כבר בשנת 2004 בהתערבות מהירה של משרד הבריאות. במהלך חודש ספטמבר 2004 הפיץ משרד הבריאות חוזר מיוחד במחלקות הילדים בכל בתי-החולים בארץ, ולפיו הוחלט לחסן תינוקות נגד שעלת כבר בגיל שישה שבועות, בעת הביקור בטיפת-חלב (עד מועד החלטה זו, ניתן החיסון לראשונה בגיל חודשיים). המלצת משרד הבריאות באה בעקבות העלייה החדה במספר החולים בשעלת בארץ. במשרד הוחלט לנסות לבלום את העלייה באמצעות תוכנית פעולה מיוחדת לאחר שהחיסונים האחרונים נגד שעלת לא הפחיתו את מספר החולים. הסיבה לעלייה היא, ככל הנראה, הירידה בעמידות הגוף לחיידק השעלת שנים אחדות לאחר קבלת החיסון. ועדת ההיגוי של המחלקה לאפידמיולוגיה המליצה כי הנהלת המשרד תשקול הוספת חיסון נגד שעלת בכיתה א' ועדכון מלאי התרופות לחולי השעלת בהוספת סוגים שונים של אנטיביוטיקה.
הטיפול בשעלת: הטיפול המחלת השעלת הוא טיפול אנטיביוטי. הטיפול חייב להיות מהיר ואגרסיבי. טיפול הבחירה הוא עם אזניל (אזיטרומיצין ) ל 5 ימים. קיימות אנטיביוטיקות נוספות שהן יעילות מאוד כנגד המחלה. משך הטיפול המקובל בתרופות אחרות הוא כשבועיים ימים. גם הטיפול במגעים קרובים הוא אנטיביוטי.
בתינוקות יש מקום לטיפול במרחיבי סמפונות בשל קוצר נשימה קשה היכול להתפתח. הטיפול אינו משנה את חומרת המחלה אך הוא עוצר אותה ומונע את הדבקת מגעים קרובים.
החיסון החיסון נגד שעלת ניתן בישראל מאז שנת 1957. מאז חודש מאי 2002 הוא ניתן במסגרת חיסון משולש (DTP): דיפתריה, טטנוס ושעלת. מדובר בגרסה חדשה יותר של החיסון הקודם, שלא נכלל בה החיידק המומת השלם, כפי שנעשה לפני כן, אלא רק חלבונים של החיידק. החיסון החדש מכונה חיסון א-סלולרי.
החיסון נמצא בשימוש בכמה מדינות מפותחות, ואפשר לשלבו בחיסון נגד מחלת הפוליו ודלקת קרום המוח (חיסון מחומש). הוא ניתן בכמה מנות – בגיל חודשיים, בגיל ארבעה חודשים, בגיל חצי שנה ובגיל שנה. החיסון בחיידק השעלת המומת עלול לגרום בין היתר לחום גבוה ולתופעות נוירולוגיות שונות, והדעות חלוקות בעניין האפשרות של נזק מוחי קבוע בעקבותיו, אולם כאמור לעיל, בשנת 2002 הוכנס לשימוש חיסון חדש נגד שעלת, המיוצר בטכנולוגיה מתקדמת, ובחיסון זה נכללים רק כמה מרכיבים חלבוניים של חיידק השעלת. לדברי פרופ' שמואל רשפון, ראש ועדת ההיגוי של המחלקה לאפידמיולוגיה במשרד הבריאות, שיעור המקרים של תופעות לוואי לחיסון החדש, כגון חום ואדמומיות, נמוך פי עשרה משיעורם בחיסון הרגיל. תופעות לוואי לאחר החיסון: תופעות לוואי מהחיסון הישן יותר היו קשות וכללו: 1. תופעות לוואי מקומיות: כאבים, נפיחות מקומית 2. חום – עד 40 מעלות 3. פרכוסי חום 4. פרכוסים ללא חום 5. הקאות 6. שיתוקים מפגיעה מוחית גלובאלית – אחד ל 750000 הזרקות 7. מוות בעריסה (לא ברורה השכיחות היות שהחיסון הוחלף) 8. מוות – אחד ל 5 מיליון הזרקות
פרכוסי חום ואף נזקים מוחיים קבועים. תופעות לוואי מקומיות שכללו חום ואפילו תופעות הלוואי מהחיסון החדש – א-סלולרי (DTPa) הן מינוריות ושכיחותן נמוכה פי 10 מהחיסון הקודם. בשל תביעות משפטיות שהגיעו לבית המשפט העליון בשבתו כבית משפט לערעורים, הגיעה תביעה של משפחה שילדם חוסן בחיסון DTP ולאחריו התפתחה אצלו פגיעה מוחית קשה מסוג סינדרום על שם ווסט (פרכוסים ופגיעה מוחית קשה) הנזקים ממחלה זו הם קשים מאוד וכוללים שיתוק מלא רפה ופיגור שכלי עמוק. בידי בית המשפט עמדו שתי דעות שונות האחת יוצגה על ידי משרד הבריאות ומומחיו שטענו כי שכיחות התופעות הנ"ל מאוד נמוכה וממולם עמדו מתנגדי החיסון (ארגון חוסן ונציגיו הרופאים) שטענו כי שכיחות התופעות הרבה יותר גבוהה ממה שאנו מודים. לאחר הקמת וועדת מומחים שדנה בנושא וקיבלה אף חוות דעת מכל העולם הגיע בית המשפע להחלטה ברורה וחד משמעית : שכיחות תופעות הלוואי הנ"ל 1 ל 500000 ילדים בחיסון הישן ואחד ל 5 מיליון בחיסון החדש. היות שטובת הכלל דוחה את טובת הפרט חיסון זה לא רק שלא ניפסל אלא הובררה יעילותו הרבה. אין אפשרות לתבוע את משרד הבריאות על תופעות לוואי מחיסונים לאחר פסיקה חד משמעית זו.
לסיכום : השעלת מחלה שכיחה מאוד שסימניה לא מתאימים תמיד למה שלומדים בספרות. היא הייתה וממשיכה להיות מזהם קשה של מערכת הנשימה. חזרתה של מחלה זו לאזורינו ושינוי ניכר בסימפטומים הקליניים שלה מצריכים ניסיונות אבחון מוקדמים בכל חולה עם שיעול התקפי ממושך ובלתי פוסק. השעלת שהייתה בעבר מחלת ילדות היא נחלתם של ילדים ומבוגרים כאחד. חיסוניות נמוכה של האוכלוסייה תורמת מאוד להתפרצות בכל שכבות הגילאים. במבוגרים המחלה קלה הרבה יותר מאשר בילדים ולכן קשה לאתרה. יש לבצע בכל מקרה חשוד משטח לוע, בדיקה סרולוגית ובדיקת PCR לאישור המחלה. חשוב מאוד לעדכן את משרד הבריאות בכל מקרה חדש של שעלת לשם חיסון וטיפול במגעים קרובים.
ניתן לראות כי משרד הבריאות נכנס להילוך גבוה בנושא השעלת היות שמשנת 2000 חלה עלייה חדה מאוד במספר החולים כל שנה דבר שיחייב הערכת מצב מחודשת של משרד הבריאות ופעולה מיידית ברמה לאומית.
שכיחות השפעת לפי שנה (נתוני משרד הבריאות)
מחלת הצפדת - טטנוס מחלת הטטנוס נגרמת על ידי החיידק Clostrdium Tetani. החיידק אנא אירובי ונוטה ליצור נבגים היציבים לחום, יובש ולחומרים מחטאים. הנבגים נפוצים ביותר בטבע ונמצאים בקרקע, אבק הבית, מעי בעלי חיים והפרשותיהם וכן בצואת האדם. החיידק החודר לגוף יכול להימצא בצורה רדומה זמן רב עד שנוצרים תנאים נאותים לגידולו: תנאי חוסר אויר (תנאים אנא אירוביים). הסכנה מהחיידק נובעת מהפרשות הרעלנים שלו: טטנוספזמין וטטנוליזין. רעלנים (טוקסינים) אלו מתפשטים לכיוון מערכת העצבים באמצעות המערכת הלימפתית ומחזור הדם. העצבים הנפגעים אינם מסוגלים לשחרר מתוכם חומרים כימיים-הנאורוטרנסמיטורים, הדרושים להפעלה השוטפת של העצבים והעברת גירויים ביניהם. גירוי תחושתי יגרום לכן להופעת תגובה מוטורית מתמדת, מהעדר הפרשת כימיקאלים לביטול הפעולה. תופיע התכווצות שרירים אגוניסטיים ואנטגוניסטיים בעת ובעונה אחת מה שקרוי תגובה טיטאנית. עיקר הפגיעה בשרירי הלסתות והצוואר ובהמשך התכווצות שרירים כללית. מרגע שהרעלן התיישב בקצות העצבים, הוא אינו ניתן לנטרול על ידי אנטי טוקסין. בשנת 1952 שיעורי ההיארעות בישראל היו 2.7 ל 100000 תושבים (כ 100 חולים בשנה ). החיסון הוחל בישראל לכלל התינוקות בשנת 1955 ומאז נרשמה ירידה חדה ביותר במספר החולים שירד בשנות השישים ל 1 למיליון תושבים (4 חולים בשנת 1965 ). משנה זו המחלה נדירה ביותר ועקב החיסון כמעט ולא נצפית באזורינו. טטנוס של ילודים שהייתה מחלה קשה ביותר שפגעה בשנת 1954 ב 50 תינוקות, נעלמה לחלוטין בשנת 1990 ומאז לא נצפתה בישראל.
טטנוס בילד טטנוס מולד
החיסון תפקיד החיסון למנוע את נזקי החיידק ורעליו. החיסון מבוסס על מתן טוקסואיד (הטוקסין שעבר טיפול כימי המנטרל את האפקט הטוקסי מבלי לפגוע ביכולתו לעורר תגובה חיסונית - יצירת נוגדנים). הטוקסואיד עובר ספיחה עם מלחי אלומיניום ע"מ להגביר את כושרו האימונולוגי. החיסון בטוקסואיד הוא חיסון פעיל. להשגת חסינות יש לתת בגיל הינקות את החיסון המשולב - דיפטריה, טטנוס ושעלת (DTP ). במבוגרים מעל גיל 7 שנים, ניתן חיסון בטוקסואיד הדיפטריה והטטנוס בלבד (ללא שעלת). חיסון פעיל הוא חיסון שניתן ב-3 מנות בנות 0.5 מ"ל. ההזרקה השנייה 6–8 שבועות לאחר הראשונה. השלישית, 6-12 חודשים לאחר השנייה. החיסון יעיל ל-10 שנים לפציעות קלות. בפציעות קשות- יש לתת מנת דחף לאחר 5 שנים. רצוי לשלב הזרקה זו עם חיסון סביל, (חיסון המכיל נוגדנים כנגד הטטנוס ושמקורם - הומני), לאנשים בלתי מחוסנים, וזאת על מנת לגשר על פער הזמנים שבין הופעת הנוגדנים עקב החיסון הפעיל ומועד הפציעה. תופעות לוואי מקומיות. נדירות: רגישות יתר או פגיעה עצבית.
דיפטריה - קרמת בניגוד לשעלת, שעדיין קיימת ותוקפת גם ילדים גדולים ומבוגרים, דיפטריה נדירה ביותר באזורנו עקב החיסון.
תמונה קלינית חיידק הדיפטריה מתיישב בלוע, ומתפשט באמצעות טיפות מהפרשות האף והלוע לסביבה. משך תקופת הדגירה נע בין יומיים לשבוע. החיידק גורם לדלקת בלוע תוך כדי יצירת קרום, אשר עלול לחסום את נתיבי האוויר, ולגרום חנק. נוסף לכך החיידק מפריש רעלן (טוקסין), אשר עלול לתקוף את שריר הלב ולגרום לדלקת של השריר (Myocarditis). סיבוך מאוחר יותר מהרעלן הוא פגיעה במערכת העצבים ושיתוק.
טיפול הטיפול במחלה הוא מניעה באמצעות חיסון. בזמן מחלה חריפה הטיפול הוא מתן אנטיטוקסין, כדי למנוע את השפעת הרעלן, ואנטיביוטיקה נגד החיידק עצמו.
חיסון החיסון נגד דיפטריה ניתן כחלק מהחיסון המשולש (ראה שעלת). החיסון הוא באמצעות רעלן (טוקסין) מוחלש בזריקה לשריר. החיסון ניתן נגד הטוקסין ולא נגד החיידק השלם שכן עיקר הסכנה במחלה היא בהפרשת הטוקסין והשפעתו המזיקה על שריר הלב.
מועדי החיסון החיסון ניתן בחודשים ה-2, 4, 6, ו-12 לחיים ומנת דחף נוספת בגיל 7 ו-13 (מנת דחף לא כוללת חיסון לשעלת).
מתי לא לחסן בזמן מחלת חום חריפה.
תופעות לוואי רוב תופעות הלוואי קשורות למרכיב החיסון כנגד שעלת הנמצא בחיסון המשולש. תופעות הלוואי כנגד דיפטריה –טטנוס טוקסואיד קשורות לעלית חום ותגובה מקומית באזור ההזרקה. תופעות של רגישות יתר כללית –נדירות.
מספר חולים לעומת שנה (מקור 2 הגרפים בנתוני משרד הבריאות) המופילוס אינפלואנזה B (גורם לדלקת קרום מוח, דלקות אוזניים קשות ופרכוסי חום) דלקת בקרום המוח מאופיינת בשלושה סימפטומים: כאבי ראש, הקאה חוזרת וחום גבוה. תינוק יכול לגלות מצב של אי-שקט או אפתיה. בהמשך חלה הידרדרות במצב ההכרה, עד כדי כך שהחולה אינו מגיב כצפוי לגירויים. בבדיקה מתגלים סימנים מנינגאליים כלומר, קשיון עורף וסימן על שם קרנינג וברוז'ינסקי: בהרמת העורף מתרוממות הרגליים, ובהרמת הרגליים חלה החמרה בכאב בעורף. הבדיקה הדחופה המתבקשת בשלב זה היא ניקור מותני. בבדיקה זו מחדירים מחט דקה בין שתי חוליות עמוד השדרה אל תוך חלל קטן הנמצא במעטפת השדרה. זוהי בדיקה קצרה ולא מסוכנת, ונדיר ביותר, אם בכלל, שיופיעו סיבוכים. הבדיקה אינפורמטיבית מאוד. אם יש זיהום חיידקי, ניתן בדרך כלל לראות נוזל עכור ולהתחיל מיד בטיפול אנטיביוטי ובטיפול תומך. הנוזל נשלח למעבדה לזיהוי החיידק ולספירת כדוריות דם לבנות (לויקוציטים), בדיקת הימצאות חלבון, בדיקת רמת הסוכר ועוד. מטרת הבדיקות, בין השאר, היא לנסות להבדיל בין גורם חיידקי לגורם נגיפי. שיעור ההיארעות בישראל בין השנים 1982- 1992 לתחלואה בדלקת קרום המוח מחיידק זה נעה בין 1.7 ל 2.4 לכל 100000 תושבים.
משנת 1994 בה הוחל מתן החיסון שיעור ההיארעות ירד מתחת ל 0.1 ל 100000 – דבר המעיד על הצלחה חסרת תקדים במתן חיסון זה.
גורמים הגורמים העיקריים לדלקת קרום המוח הם חיידקים ווירוסים. מבין החיידקים העיקרי הוא ההמופילוס אינפלואנזה.
המופילוס אינפלואנזה זן B (Hemophilus Influenza type B): גורם התחלואה השכיח ביותר בילדים מתחת לגיל 4. מתבגרים ומבוגרים מהווים לעיתים קרובות, נשאים של החיידק ואינם מראים את תמונת המחלה. החיידק נמצא בהפרשות האף והלוע ומועבר על ידי זיהום טיפתי (התעטשות, נשיקות ושעול).
תחלואה מלבד דלקת קרום המוח יכול חיידק ההמופילוס אינפלואנזה לגרום לדלקות ברקמות הרכות (צלוליטיס), דלקות במפרקים, אפיגלוטיטיס ודלקות בעצם (אוסטאומיאליטיס). דלקת קרום המוח בעידן הטרום ניתוחי היותה שני שלישים מכלל הזיהומים בחיידק. שעור התמותה נע בין 2%-5% למרות טיפול אנטיביוטי. הפרעות בשמיעה נמצאו ב־15%-30% לאחר המחלה.
תחלואה לפי גיל שעור ההדבקה הגבוה ביותר היה בין 6–7 חודשים לחיים. 60% מהחולים היו למטה מגיל שנה ו-90% פחות מגיל 5 שנים. חיסון החיסון מבוסס על יצירת נוגדנים כנגד הקופסית הרב סוכרתית (הפוליסכרידית) של החיידק הנמצאת בתאחיזה למרכיבי חלבון שאינם רעילים של רעלן הדיפטריה. בשוק יש מספר תכשירים ברי החלפה מבחינת יעילותם. החיסון ניתן לילדים עד גיל 5. מעבר לגיל זה ניתנת מנת חיסון אחת בלבד לאותם חולים המהווים קבוצת סיכון - ילדים שעברו כריתת טחול או מצבי אנמיה חרמשית. החיסון נמצא בשגרת החיסונים של מדינת ישראל. החיסון ניתן ב-4 מנות בגילאים: 2 חד', 4 חד', 6 חד' ו-12 חודשים לחיים. תינוק שהגיע לגיל 12 חודשים ולא קיבל את החיסון המלא מספיקות 2 מנות חיסון בהפרש של חודשיים להשגת חסינות. מעל גיל 15 חודש מספיקה מנת חיסון אחת להשגת חסינות. מאז תחילת מתן החיסון נגד החיידק המופילוס אינפלואנזה מסוג B, חלה ירידה חדה בשכיחות דלקת קרום המוח בכלל, ובמיוחד עקב מחולל זה, שהיה בעבר הלא רחוק הגורם העיקרי לדלקת קרום המוח אצל תינוקות וילדים רכים. נצפתה גם ירידה חדה בשיעורי ההיארעות של פרכוסי חום בישראל – כנראה מאז התחלת השימוש בחיסון
דרך מתן החיסון \ תופעות לוואי - זריקה לתוך השריר., לא נצפו תופעות ייחודיות.
טיפול בדלקת קרום המוח האנטיביוטיקה הנבחרת במקרה זה היא זו שתתן מענה לחיידקים האפשריים, תחדור לקרומי המוח ותפעל ביעילות ובמהירות. משפחת הצפלוספורינים מהדור השלישי היא התרופה העדיפה במצב זה. הטיפול נמשך בין עשרה ימים לשבועיים.
מאז תחילת מתן החיסון נגד החיידק המופילוס אינפלואנזה מסוג B, חלה ירידה חדה בשכיחות דלקת קרום המוח בכלל, ובמיוחד עקב מחולל זה, שהיה בעבר הלא רחוק הגורם העיקרי לדלקת קרום המוח אצל תינוקות וילדים רכים.
עדיין המנינגוקוקוס והפנוימוקוקוס עלולים לגרום למחלה, אך סך הכול השכיחות, כאמור, ירדה.
סיבוכים הסיבוך השכיח ביותר אחרי דלקת קרום המוח חיידקית הוא פגיעה בשמיעה, ולכן יש לערוך לילד בדיקת שמיעה לאחר חלוף המחלה. אחוז הפגיעה במערכת העצבים המרכזית (פגיעה בתהליכי החשיבה) לאחר דלקת קרום המוח אינו מבוטל, ולכן במקרה של חשד בדלקת קרום המוח יש הכרח להגיע לאבחנה במהירות האפשרית, ולהתחיל מיד בטיפול אנטיביוטי ובטיפול תומך אחר.
(מנתוני משרד הבריאות)
פרק 5. חיסונים שאינם בשגרת חיסונים בישראל מחלת השפעת
שפעת היא מחלה ויראלית מדבקת והיא אולי מחלת החורף הקשה ביותר. בין 10-20% מן ילדים בישראל חולים בשפעת מדי שנה. המחלה מערבת בעיקר את דרכי הנשימה העליונים (האף, ה"עץ" הברונכיאלי והריאות).
היסטוריה נגיפי השפעת מסוגים A, B עוברים באופן קבוע שינוי אנטיגני מסוג סחיפה. תהליך זה מתרחש באופן תדיר מעונה לעונה בה פורצת מחלת השפעת. שינוי אנטיגני מסוג העברה מתרחש באופן אקראי לחלוטין ובלתי צפוי שקשה להתכונן לו. וכאשר זה מתרחש, אוכלוסיות שלמות של אנשים, לעיתים מדובר בכלל האוכלוסייה ממש, נותרים ללא הגנה כל שהיא מול הנגיף, והתוצאות קטלניות. שינוי כזה מניב מגפה בסדר גודל עולמי הנקראת פנדמייה ולא אפידמייה. במהלך המאה הנוכחית, אירעו שלוש פנדמיות של נגיף השפעת בשנים 1918, 1957 ו- 1968. כל שנה כזאת גרמה לתמותה גבוהה עקב השפעת, ובפרט זאת של שנת 1918, שנה שבה התנהלה במקביל גם מלחמת העולם הראשונה שכל מספר חלליה לא מתקרב לזו של השפעת "הספרדית".
המגפה בשנת 1918 - בידוד
נתוני התמותה לפנדמיית השפעת מבהילים דיים. להלן הפירוט:
1918-19 "השפעת הספרדית" A(H1N1) גרמה למספר החללים הגבוה ביותר שגרם נגיף שפעת כלשהו. בערך חצי מיליון נספים בארצות הברית, וכ־20 מיליון בעולם כולו.
1957-58 "השפעת האסייתית".A(H2N2) 70,000 מתים בארצות הברית בלבד.
1968-69 "שפעת הונג קונג" A(H3N2). 34,000 מתים בארצות הברית בלבד.
התפרצותה של "שפעת הונג קונג" בשנים 69–1968 מציינת את תחילתו של עידן.A(H3N2) כאשר נגיף זה התגלה לראשונה, הוא אובחן על רקע השיפור שחל בתמותה החולים ביחס למוטציות הקודמות שלו. ישנם סיבות אפשריות העשויות להסביר את השיפור בהישרדות החולים. ראשית, הנגיף "האסייאתי" מסוג A(H2N2) עבר שינוי מסוג העברה והפך לנגיף המוכר לנו בשם שפעת הונג קונג" מסוג A(H3N2). השינוי כפי שניתן להיווכח התרחש רק בחלבון Hemagglutinin כאשר החלבון Neuramindase נותר ללא שינוי, ולכן ניתן היה להסביר שלגוף הייתה בכ"ז הגנה מסוימת מפני המוטציה החדשה. הסבר שני לשיפור בשרידות החולים הוא שמוטציית שפעת עם אותו מבנה Hemagglutinin גרמה לשפעת בין השנים 1890 ולאורך השנים הראשונות של המאה. במצב שכזה, חולים שהיו בני 60 ואילך בשנת 1968 היו בעלי חסינות כלשהי כנגד נגיף השפעת, חסינות שנרכשה כנראה בתקופת חייהם כצעירים בסביבת המוטציה הנוכחית של השפעת.
ישנן עובדות הקשורות לנגיף השפעת שאינן ברורות די הצורך. למרות יחסי התמותה המשופרים של נגיף הונג קונג A(H3N2), ממשיך נגיף זה להפיל חללים לאורך שנות פעילותו. במשך פעילותו של נגיף זה מאז שהתגלה, גרם A(H3N2) ל־400,000 מתים בארצות הברית בלבד, ו 90% מבין אלה שייכים לאוכלוסיות הבוגרות. ולכן מבחינת פוטנציאל הנזק של נגיף שפעת, A(H3N2) עדיין מהווה את המוקד לפגיעה חריפה ומסוכנת באוכלוסיות בוגרות או כרוניות.
מחלקה בבית חולים בזמן מגפת השפעת הספרדית
מגפת 1918 – תמונות מאותה תקופה
גם המוטציה A(H1N1) הקטלנית יש לה היסטוריה מעניינת. לאחר הפנדמייה של שנת 19–1918 היא עברה באופן קבוע שינוי מסוג דריפט (הזזה), ובאופן עקיב גרמה למגיפות שפעת אבל לא בהיקף המחריד של שנת 19–1918. כאשר צצה השפעת האסיאתית AH2N2 בשנת 1957, נעלם הנגיף מסוג AH1N1, ממש כמו שהוא עצמו נעלם כאשר התגלה נגיף "הונג קונג" AH3N2 בשנת 1968. בשנת 1977 שוב הופיע הנגיף AH1N1 שכונה "השפעת הרוסית" והתקשר לתוך AH3N2 בהתלכדות תמידית, בינתיים. ובכל זאת הייתה לו השפעה מיוחדת, כי הנגיף של שנת 1977 היה זהה במבנהו לנגיף AH1N1 שפעל בשנת 1950. לכן, רובם של האנשים שנולדו לפני שנת 1950 היו מחוסנים בפני הנגיף, והתפרצות השפעת מסוג AH1N1 פגעה דווקא בצעירים יותר, לאמור בגילאים של 25 ומטה. העובדה שדווקא הבוגרים יותר מגלים חסינות לנגיף השפעת "הספרדי" האימתני מסביר בהתאם גם את השיפור שנצפה בהישרדות החולים. שהרי ממילא האוכלוסייה הבוגרת גם פגיעה יותר, ואם דווקא לה יש חסינות, ממילא משתפרים סיכויי השרידות של כלל האוכלוסייה בצורה דרמטית
הידבקות המחלה נקשרת לקור וחורף, אולם אין לה קשר ישיר לקור. ישנם מספר תאוריות באשר לתפוצתה הרבה של המחלה בעונת החורף. הסבר אפשרי אחד לתפוצתה הרבה בחורף נובע מהטעם הפשוט של חוסר אוורור במקומות הומי אדם. הסבר אחר הוא שטמפרטורות נמוכות גורמות לאוויר יבש יותר שמקשה על הגוף להיפטר מריכוזי הנגיף. ייתכן שגם ריבוי טיולים וביקורי קרובים בעונת החורף (במדינות המערב) מעודד את ההתפשטות. הסבר נוסף הוא שקור מחליש את מערכת החיסון של הגוף.
העברת הנגיף
הנגיף גם מתקיים בקור לאורך זמן רב יותר על משטחים חשופים. ההידבקות עצמה במחלה נעשית באמצעות נגיפי המחלה המועברים בקלות רבה מאוד באמצעות האוויר, מה שהופך את המחלה למדבקת ביותר. ההידבקות בשפעת מתבצעת על ידי מעבר הנגיף אל דרכי הנשימה. שם הוא חודר לתוך תאי האפיתל שבדפנות דרכי הנשימה, לכל תא בנפרד. בתוך התאים משתכפל הנגיף בקצב מהיר ביותר ובתוך שעות אחדות נהרס התא, הנגיף מתפזר, חודר לתאים סמוכים וחוזר חלילה. התאים הנגועים מתים והמחלה מתקדמת עד שמערכת החיסון מדבירה את הנגיף או שהנגיף הורג את האדם מבנה הווירוס נגיף השפעת נראה כמו כדור העטוף ביתדות. היתדות עשויים מולקולות של החלבונים האנטיגנים Hemagglutinin ו- Neuraminidase. כאשר יתדות אלה הממוקמים ע"פ חזית הנגיף באים במגע עם התא הבריא אליו נצמד הנגיף, הוא מפריש מייד נוגדנים הנלחמים בנגיף הפולש. היות שלנגיף יש קומבינציות שונות של יתדות כאלה על פניו, מפרישה המערכת החיסונית חומרים כנגד כל סוג נגיף שהיא מאתרת. יתרה מכך, המערכת החיסונית "מתעדת" את הנגיף שהתקיף את התא כך במקרה של זיהוי חוזר של תוקף דומה תוכל המערכת החיסונית להגיב מיידית על הפלישה.
צילום במיקרוסקופ אלקטרוני של הווירוס
מוליקולת ההמאגלוטינין אינה יציבה ולכן היא משתנה כל הזמן ומחייבת גם את המערכת החיסונית להגיב על חותם הנגיף החדש. אבל כאמור כל עוד השינויים הם רק ביצירת עותקים זהים של המאגלוטינין מסוג הזזה קלה, עדיין שמורה למערכת החיסונית יכולת כלשהי להתגונן ורובם של נפגעי השפעת ישובו לאיתנם. אבל אם מתבצע שינוי בהמאגלוטינין גופו, שינוי מסוג תנועה והחלפת מקום, אזי המצב מחמיר ועובר לכלל מגפה עולמית המכונה פאנדמייה.
ישנם שלושה וירוסים שונים: אינפלואנזה A ,B ,C.
- הזנים A ו-B גורמים למחלה המערבת דרכי נשימה. הם מופיעים בכל חורף בדרגות משתנות.
זנים אלו גורמים לצורה הקשה יותר של שפעת והמאמצים לחסן ולמנוע מתמקדים בזנים אלו. עם זאת, לזנים אלו יש יכולת השתנות, כך שכמעט בכל שנה מופיעה ואריאציה מעט שונה של הווירוס ולא תמיד החיסון יעיל כנגד אותה צורה מתחדשת.
- הזן C גורם למחלה קלה בדרכי הנשימה או שהוא חולף בצורה נטולת סימפטומים. השפעתו על בריאות הציבור אינה כה רחבה והוא אינו מופיע בכל שנה.
וירוס השפעת משתנה בתדירות גבוהה (עובר מוטציות רבות) וכך הוא מתחמק הן מן הזיכרון לטווח ארוך של מערכת החיסון משנים קודמות ולעיתים גם מן החיסון המיועד לאותה שנה ונועד לעצור את הזן החדש. תהליך ההדבקה והתחלואה די מובנה:
- אדם שנדבק בשפעת מפתח נוגדנים כנגד הווירוס.
- הווירוס עובר מוטציה (שינוי צורה גדול או קטן ).
- הנוגדנים כנגד הווירוס הקודם אינם מספקים הגנה כנגד הווירוס החדש.
- מופיעה הדבקה מחדש בעונה הבאה.
לעיתים המוטציה אינה מלאה והנוגדנים כנגד הווירוס הקודם' מספקים הגנה כלשהי, מכיוון שהמוטציה אינה משנה את כל מרכיבי הווירוס המושפעים מהחיסון. כרגע קיימים בעולם שני זנים של קבוצה A וזן אחד של קבוצה B האחראיים לתחלואה בעולם. תת-הקבוצות של וירוס מסוג A מסווגות על בסיס שני חלבונים בוירוס הנקראים המאגלוטינין (H) ונוירואמינידאז (N). לכן בעולם המדע מוכרים הזנים הפעילים כעת בתור – H1N1 & H3N2. קליניקה סימני המחלה מופיעים אצל החולה כ – 48 שעות לאחר שנדבק מחולה שפעת אחר. היא מתחילה לרוב בצורה פתאומית על ידי צמרמורת, חום גבוה העולה עד 40 מעלות ואפילו יותר, כאבי ראש (מעל העיניים), שלשולים והקאות, כאבי גב ושרירים, בין הצלעות ובגפיים. הפנים אדומות והסומק מתפשט גם אל הצוואר והחזה. הפה יבש, הגרון כואב, האף בתחילה סתום, ולפעמים מדמם. קולו של החולה צרוד, בהתחלה מופיע שיעול קצר ויבש, ולאחר מכן הוא נעשה עוויתי – דמוי שיעול של שעלת. החם הגבוה נמשך 3 – 4 ימים. קורה שלאחר שהחם ירד ליום – יומיים, הוא שב ועולה ליומיים נוספים, מבלי שמהלך זה יבשר סיבוך במחלה. כאשר לחולה יש חם הוא עייף, רדום לעיתים, והעייפות והתשישות נמשכות כמה ימים לאחר תם המחלה, גם באותם מקרים שהשפעת עוברת בצורה קל
סימפטומים שכיחים:
- חום, שעלול להיות גבוה
- כאב שרירים
- הרגשה כללית רעה "בכל הגוף"
- כאבי ראש
- שיעול, לרוב יבש (לא פרודוקטיבי)
- כאבי גרון
- נזלת (בחלק מן המקרים)
- בחילה, לעיתים הקאה
- יציאות רכות
- חולשה ועייפות
משך המחלה הוא כשבוע במרבית האנשים, אבל החולשה והתשישות נמשכים עוד שבועות מספר. כמו שניתן לראות רשימת הסימפטומים אינה ספציפית לשפעת. רק רופא הילדים יוכל למצות את ממצאי הבדיקה הגופנית וההיסטוריה שתוארה בפניו ולאבחן את המחלה.
שפעת לעומת הצטננות אלו שתי מחלות שונות ונגרמות על ידי וירוסים שונים. ישנם כמה קווים משותפים אולם רב ההבדל על המשותף. גם להצטננות ייתכנו סיבוכים (דלקות אוזניים סינוסיטיס או דלקת ריאות) אולם כאשר היא מופיעה ללא סיבוכים הרי שזו מחלה קלה בהרבה. להלן מספר הבדלים:
שפעת הצטננות חום גבוה חום נמוך, או ללא חום כלל כמעט תמיד קיימים כאבי ראש כאבי ראש מופיעים לעיתים נזלת מופיעה רק לעיתים כמעט תמיד יש נזלת לרוב אין התעטשויות מתעטשים שיעול יבש הולך ומחמיר שיעול "נבחני" לרוב כאבי שרירים מעט כאבי שרירים חולשה ותשישות למשך שבועות מעט חולשה כאבי גרון רק לפעמים לרוב קיימים כאבי גרון תשישות, לעיתים קיצונית ירידה קלה ברמת האנרגיה הבסיסית
חיסון התרכיב המקובל הוא תרכיב מומת בזריקה. התרכיב מכיל 3 זנים של שפעת, שמשתנים קצת מדי שנה. בכל השנים יש: H1N1, H3,N2 ונציג של שפעת B. הזנים מגודלים בביצים ולכן מי שאלרגי לביצים לא מקבל את החיסון. מטפלים בנגיפים בפורמלין כדי להרוג אותם. התרכיב הזה נקרא whole vaccine. המרכיב השומני של התרכיב גורם לתופעות לוואי, בעיקר בילדים ולכן הוסיפו שלב נוסף ויצרו split vaccine שזה אותו התרכיב, אבל ללא השומנים, אלא רק עם החלבונים.
Subunit vaccine – תרכיב שמכיל חלקים בלבד של הנגיף. עד היום מתן של תרכיב כזה בריריות לא גרם להופעה של חיסון. יש שני מרכזים למערכת החיסון הרירית – peyer`s patches ואתר נוסף באף. המטרה היא ליצור תרכיב שיעורר תגובה של המרכז באף. אחת הסכנות בנגיף מוחלש – שחלוף גנטי עם נגיף רגיל. CAR- Cold Adapted Reassortment – פיתחו זן של הנגיף החי והמוחלש שמתרבה רק ב-32 מעלות. התרכיב הזה לא מגן נגד כל הסוגים. מכינים זנים רקומביננטיים שכל גני ההתרבות שלהם מוחלשים, אבל NA וHA- שלהם הוא השולט. זה עדיין ניסיוני וזה נקרא CAR או CR. קבוצת היעד לתרכיב הזה היא חולים כרוניים קשים, חולים ללא מערכת חיסון ולצוות מטפל.
FluMist חיסון דרך האף מנהל התרופות והמזון האמריקאי אישר חיסון הראשון לשפעת הניתן דרך האף. החיסון ישווק בארצות הברית בשם FluMist, והוא מכיל נגיפים מוחלשים של שפעת.
ה FluMist מאושר למניעת שפעת כתוצאה מנגיפים מסוג A ו B, והוא ניתן לגילאי 5 עד 49. אצל ילדים בגילאי 5 עד 8 אשר מקבלים את החיסון בפעם הראשונה, החיסון ניתן בשתי מנות בהפרש של 6 שבועות לפחות. במתבגרים ובמבוגרים בגילאי 9 עד 49, נדרשת מנה אחת בלבד. החיסון מכיל שלושה זנים ויראליים (שניים מסוג A, ואחד מסוג B) אשר הומלצו לעונת השפעת של שנת 2003–2004. הנגיפים בחיסון חיים, אולם הם שונו כך שאינם יכולים לצמוח בטמפרטורת הגוף.
במחקרים קליניים רחבי היקף, FluMist הראה יעילות של 87% במניעת שפעת בילדים, והפחית את הסיכון למחלה חמורה בליווי חום אצל מבוגרים.
החיסון אינו מתאים לשימוש במצבים הבאים: אנשים הסובלים מדיכוי מערכת החסון, חולי אסתמה או חולים אחרים עם בעיות במערכת הנשימה, גיל מתחת ל 5 או מעל 50, מחלות כרוניות אשר עלולות להגביר את הסיכון לשפעת חמורה, רגישות לביצים או לחיסון עצמו. תופעות הלוואי כתוצאה משימוש בחיסון כוללות: הצטננות, נזלת, כאב גרון, ושיעול. החיסון החדש מספק דרך נוספת למניעת שפעת, ומגביר את הזמינות של זריקות נגד שפעת המכילות נגיף מומת, עבור חולים הנמצאים בסיכון גבוה. יש לקוות שבקרוב יגיע חיסון זה גם לארץ.
את מי לחסן
- מבוגרים מעל גיל 65, אצלם סיבוכים יביאו לתחלואה משמעותי באם יחלו בשפעת.
- חולים החוסים במוסדות, או שיש להם מחלת רקע כרונית.
- כל ילד או מבוגר עם בעיית רקע ריאתית או לבבית ובכלל זה אסתמה, ציסטיק פיברוזיס, מחלת ריאות משנית לפגות (BPD).
- כל ילד או מבוגר עם מחלה כרונית מן הרשימה הבאה: החולים במחלות מטבוליות (כולל סוכרת), הפרעה כלייתית, דיכוי מערכת החיסון ( מולד, נרכש, או תרופתי), המוגלובינופתיה (אנמיות נרכשות או מולדות).
- ילדים בין הגילאים חצי שנה לגיל שמונה עשרה שנים הנוטלים אספירין באופן קבוע.
- תינוקות בריאים בני 6–23 חודשים
- נשים הרות או בתקופת ההחלמה לאחר לידה.
- עובדים בתחום הבריאות. - רופאים, אחיות ואחרים המטפלים בחולים בסיכון גבוה בבתי-חולים ובקהילה (כגון ביחידות לטיפול נמרץ), בבתי חולים ומוסדות לחולים כרוניים או לקשישים, עובדי בתי- מרקחת וחדרי מיון. כמו כן צוותי שעת חירום כגון: עובד בתחום הפרא- רפואי (פרמדיק) וטכנאי רפואי. צוות רפואי ושאר מטפלים ומתנדבים הנכנסים לביקורי בית אצל אנשים בסיכון גבוה, וכן בני משפחה של האנשים בסיכון.
- עובדים בבתי הבראה ועובדים הבאים במגע עם חולים בסיכון גבוה.
- בני ביתם של חולים במחלה כרונית (ובכלל זה אחים/ אחיות של ילדים הנוטלים טיפול כימותראפי).
- אנשים הממלאים תפקידי מפתח כלשהם או מועסקים בשירותים קהילתיים חיוניים וכתוצאה מתחלואה גבוהה בקבוצה זאת עלולים להיווצר שיבושים בתפקוד השירותים לאוכלוסייה
- תיירים אשר מבקרים בארצות טרופיות בכל חודשי השנה או תיירים אשר מבקרים בארצות שבחצי הכדור הדרומי בין אפריל לספטמבר.
- כל מי שמעוניין להפחית את הסיכון ללקות בשפעת.
עיתוי רצוי לחסן נגד שפעת כבר מתחילת חודש אוקטובר ומאוד מומלץ לא מאוחר מסוף נובמבר, אבל ניתן לחסן גם אחרי מועד זה. הערה: יש לתכנן שילדים אשר לא חוסנו בעבר וזקוקים לשתי מנות תרכיב ברווח זמן של חודש ביניהן, יקבלו את המנה השנייה עד סוף נובמבר.
מתן בו-זמני של תרכיב שפעת ותרכיבים אחרים.
ניתן לחסן בו-זמנית בתרכיב נגד שפעת עם חיסוני השיגרה בגיל הילדות או עם כל חיסון אחר (כגון נגד פנאומוקוקוס בקבוצות סיכון אשר לא קיבלו חיסון זה בעבר).
מקום ההזרקה
יש להזריק את התרכיב לתוך השריר: באזור הדלטואיד למבוגרים ובחלק הקדמי- צדדי של הירך לתינוקות וילדים קטנים. מינון
להלן לוח בו מצוין המינון לפי קבוצות גיל
גיל מינון* מספר מנות סוג התרכיב 6-35 חודש 1/2 מנה 1-2 ** מפוצל (split) *** בלבד 3-8 שנים 1 מנה 1-2 ** מפוצל (split) *** בלבד 9-12 שנים 1 מנה 1 מפוצל (split) *** בלבד 13 ש' ומעלה 1 מנה 1 רגיל או מפוצל
- הכמות למנה מפורטת בדף ההסבר המלווה את אריזת התרכיב. נמצאים בשוק מזרקים חד-מנתיים \לשימוש בילדים. כמו כן, על חלק מהמזרקים המיועדים למבוגרים קיים ציון חצי מנה.
- 2 מנות מומלצות לילדים אשר מתחסנים נגד שפעת בפעם הראשונה בחייהם. מומלץ על רווח זמן של 4 שבועות בין המנות.
- ילדים מתחת לגיל 13 שנים, ובמיוחד ילדים בגילאים 6 חודשים עד 3 שנים, עלולים להגיב בתופעות טוקסיות (לרבות התכווצויות מלוות חום) לתרכיב שפעת רגיל, המוכן מנגיף שפעת שלם. תרכיב השפעת מהטיפוס המפוצל (split) מלווה בפחות תופעות לואי מאשר תרכיב המוכן מנגיף שלם, לכן, בגילאים אלה מומלץ מתן תרכיב מפוצל, בהרכב ובמינון זהים למינון התרכיב הרגיל (ראה בעלון התרכיב). בתרכיב המפוצל, הנגיפים עברו טיפול כימי להקטנת רמת המרכיבים העלולים לגרום לחום. תרכיבים אלו מופיעים תחת שמות כגון:
- 2 מנות מומלצות לילדים אשר מתחסנים נגד שפעת בפעם הראשונה בחייהם. מומלץ על רווח זמן של 4 שבועות בין המנות.
“split" "subvirion” “purified-surface antigen” “sub-unit” “disrupted” תופעות לוואי וסיבוכים
מפני שתרכיב השפעת מכיל נגיפים מומתים, הוא אינו יכול לגרום לשפעת. הופעת זיהום נשימתי סמוך לקבלת החיסון פירושו שהתרכיב ניתן בתקופת הדגירה של השפעת, או שהמחלה נגרמה על ידי מחולל אחר. התגובות לאחר מתן תרכיב שפעת הן נדירות. תגובות מקומיות של אודם, נפיחות, רגישות במשך 1–2 ימים, מופיעות בפחות משליש ממקבלי החיסון. תופעות טוקסיות כגון חום, מצב כללי רע, כאבי שרירים ותופעות כלליות אחרות מופיעות 6- 12 שעות לאחר הזרקת התרכיב ונמשכות יום או יומיים. תופעות אלה שכיחות במיוחד אצל אלו שלא היו חשופים בעבר לאנטיגנים של זני השפעת אשר בתרכיב (כגון ילדים). על מנת להפחית החום אצל ילדים יש להשתמש בתרכיב מפוצל. תופעות אלרגיות המופיעות מיד לאחר הזרקת התרכיב הן נדירות ביותר: אורטיקריה, אנגיואדמה, קשיים נשימתיים, או הלם אנפילקטי. תופעות אלה נובעות מרגישות-יתר למרכיבים מסוימים בתרכיב, במיוחד לחלבון ביצה. אנשים הידועים כבעלי רגישות מטיפוס אימונוגלובולין E (IgE) לחלבון ביצה, כולל אנשים עם תופעות של אסתמה תעסוקתית או תופעות אלרגיות אחרות על רקע חשיפה תעסוקתית לחלבון ביצה, נמצאים בסיכון גבוה יותר לפתח תגובות לאחר חיסון נגד שפעת.התרכיבים נגד שפעת הנמצאים בשימוש, למרות היותם מוכנים על ביצים מופרות, הם מטוהרים מאוד, ולכן נדירות למדי תופעות אלרגיות לאחר קבלתם.
סיבוכים נוירולוגיים: מאז 1976 (כשניתן חיסון שפעת מזן החזירים), לא נרשמה עליה בשכיחות תסמונת Guillain-Barre' קשור למתן תרכיב שפעת מזנים אחרים.
הוראות נגד ואזהרות אין לתת את החיסון לאנשים אשר סובלים ממחלת חום בשלב החריף. אין לתת תרכיב נגד שפעת לאנשים עם סיפור של תגובה קודמת חמורה לתרכיב או עם תולדות של רגישות-יתר מטיפוס אנפילקטי לחלבון ביצה בלי להתייעץ עם רופא המטפל. בקבוצה זאת נכללים אלו אשר אחרי אכילת ביצה מפתחים נפיחות בשפתיים או בלשון, בצקת כללית, קשיים נשימתיים או אבוד הכרה. הטיפול התרופתי בשפעת:
השימוש בתרופות למניעה מומלץ במקרים הבאים:
- התפרצות שפעת בעיקר במוסד בו מתגוררים אנשים בסיכון גבוה, ובמיוחד כאשר יש ספק לגבי יעילות התרכיב עקב שינויים אנטיגניים בנגיף. יש להתחיל במתן הטיפול בהקדם האפשרי, כשיש חשד להתפרצות, לכל דיירי המוסד (כולל אלה שקיבלו חיסון נגד שפעת בעונה הקודמת) ולהמשיך בטיפול לאורך כל תקופת ההתפרצות ועוד שבוע אחד לאחר סיומה.
- אנשים בסיכון גבוה שחוסנו באיחור כאשר פעילות השפעת כבר החלה בקהילה. התרופות אינן מונעות יצירת נוגדנים לנגיף השפעת ומומלץ לתת במשך שבועיים נוספים לאחר מתן התרכיב (עד להתפתחות החסינות).
- השלמת ההגנה של אנשים אשר קיבלו חיסון נגד שפעת וידועים כמדוכאי חסינות. אין מידע על פעולות הדדיות עם תרופות נגד זיהום HIV.
- אנשים הידועים כרגישים לחלבון ביצה ועלולים לפתח תופעות אנפילקטיות לחיסון.
- ניתן להשתמש בתרופות הנ"ל גם לטיפול באנשים מבוגרים בריאים הלוקים במחלה החשודה לשפעת בעת פעילות שפעת בקהילה, במטרה למנוע אצלם את סיבוכי המחלה וצמצום משך המחלה. את התרופה יש לתת תוך 24–48 שעות מהתחלת המחלה ולהמשיך עוד 48 שעות לאחר העלמות סימניה.
הטיפול יקבע על ידי רופא הילדים בהתבסס על:
- גיל הילד/ה, מצב הבריאות הכללי וההיסטוריה הרפואית.
- מפושטות המחלה וחומרתה.
- מידת ההיענות והסבילות של הילד/ה לטיפול תרופתי.
- הצפי לגבי מהלך המחלה מעת המפגש במרפאה.
- העדפות המשפחה והילד/ה.
הטיפול יכלול לרוב:
- תרופות המפחיתות כאב ומורידות חום. (יש להימנע משימוש באספירין).
- טיפול נוגד גודש לאף במקרי נזלת.
- מנוחה.
- שתייה מרובה.
- טיפול ספציפי במקרים מיוחדים.
בארסנל חברות התרופות והממסד הרפואי בעולם נמצאות 4 תרופות לטיפול או למניעה (prophylaxis) של הדבקות בנגיף ה-influenza: שתי תרופות הוותיקות יותר שאושרו לשימוש עוד בשנת 1993, amantadine ו-rimantadine (שם מותג Flumadine), שייכות למשפחת תרופות המפריעות לנגיף שחדר לתא הפונדקאי בשלב העירום שלו, דהינו אותו שלב מאבד נגיף את המעטפת החיצונית שלו (uncoating) וחומצת הגרעין שלו מתחילה את תהליך שכפולה ליצירת נגיפי-בת רבים. שתי תרופות אלה יעילות רק כנגד הנגיף influenza A2, הזן ה"אסייתי", על ידי שהן נקשרות לחלבון הנגיפי M2, ובכך מפריעות להסרת מעטפת הנגיף לאחר חדירתו לתא. אך השימוש בשתי תרופות אלה מוגבל הן בשל מספר תופעות לוואי רעלניות ובפרט השפעתן על מערכת העצבים, וכן כיוון שהנגיפים המטופלים בתרופות אלה פיתחו עד מהרה עמידות כנגדן, והסתבר שהזנים העמידים שהם יציבים מבחינה גנטית ועלולים להיות מועברים בהדבקות מאדם לשני, והם פתוגניים באותה מידה כמו נגיף הבר, וגרוע מכך הם יכולים להמשיך והתרבות ולהיות מופרשים בנוזלי גוף של אותם מטופלים עם מערכת חיסונית פגומה או מוחלשת ובכך להפוך למקור מתמשך של הדבקות עם זן נגיפים עמיד לתרופות אלה. ההופעה של עמידות בנגיפים המטופלים בשתי תרופות ממשפחת ה-adamantanes, מגבילה אם כן את יעילות השימוש בהן. שתי התרופות האחרות העומדות היום בחזית המאבק בנגיף ה-influenza הן zanzmivir (שם מותג Relenza) ו-oseltamivir (שם מותג Tamiflu) פועלות למעשה כמעכבות את פעולת האנזים neuraminidase, ובכך מפריעות לשחרור נגיפי שפעת מהתאים המודבקים, ובכך נמנעת התפשטות הנגיף והמחלה בדרכי הריאות. כיוון שההתרבות של נגיף השפעת בצינור הנשימה מגיעה לשיאה בין 24 ל-72 שעות מהופעת המחלה, שתי התרופות האחרונות הפועלות בשלב התרבות הנגיף, צריכות להינתן מוקדם ככל האפשר. בניגוד לשתי תרופות הוותיקות, התרופות מהדור החדש שהן יקרות בהרבה מקודמותיהן, מעכבות neuraminidase, אינן גורמות לתופעות לוואי רעלניות ואינם מעודדות יצירת נגיפי-שפעת עמידים להן. אך החשוב מכל היא תכונת שתי התרופות האחרונות לגלות יעילות כנגד כל זני נגיף השפעת בכך שהן מעכבות פעילות אנזים העומדת ביסוד ההדבקה וההתפשטות של כל נגיפי influenza. תכשיר Relenza מגיע בצורת אבקה המוחדרת בעזרת משאף, ואילו Tamiflu כטבליות לבליעה. גם יעילות הטיפול בשתי תרופות אלה רבה יותר ככל שמקדימים בו. ניסוי משנת 2003 עם Tamiflu בקרב 1,426 חולי שפעת הראה שכאשר הטיפול החל 12 מתחילת התסמינים קיצר את מהלך המחלה ביותר משלושה ימים, ולעומתו טיפול באותה תרופה שהחל בין 36–48 מתחילת התסמינים הראה יעילות מופחתת בהרבה. מה יעילותן של שתי התרופות האחרונות בהפחתת סבל או אף תמותה בקרב קשישים? סקירה של ניסויים קליניים שנערכו לפני שנת 2002 בקרב קשישים מעל גיל 65 שנה או אלה עם מצבים קליניים כרוניים, הראו ש Relenza הפחיתה את פרק הזמן עד להיעלמות התסמינים ביומיים, אם כי Tamiflu היה יעיל פחות ובממוצע קיצר את הזמן מתחילת הטיפול בו עד להתפוגגות התסמינים בחצי יום בלבד. ומה באשר לילדים? כאן דווקא מתהפכות היוצרות לגבי יעילות שתי התרופות האמורות: ניסוי קליני ב-471 ילדים בני 5 עד 12 שנה בהם ניתן הטיפול ב-Relenza, בין 36 עד 48 שעות מתחילת התסמינים, נמצא שתרופה זו קצרה את משך התסמינים ביום אחד בממוצע. לעומתה, טיפול ב-695 ילדים בגיל 1 עד 12 שנה ב-Tamiflu שהחל באותו פרק זמן מתחילת התסמינים כמו במקרה של Relenza, הביא לקיצור מהלך המחלה ב-1.5 ימים בממוצע. מה שמרשים יותר, שהטיפול בילדים עם שפעת ב-Tamiflu הפחית ב-44% את התרחשות דלקת חריפה של האוזן התיכונה שהיא סיבוך שכיח בילדים עם שפעת.
מינונים המינון בטיפול מלא בשפעת: Amantadine – 100mg פעמיים ביום למשך 10 ימים. Rimantadine - 100mg פעמיים ביום למשך 10 ימים. Oseltamivir –75mg פעמיים ביום למשך 5 ימים.
נתונים על יעילות התרופות השונות ובטיחות השימוש בהן
קריטריון/תרופה Amantadine Rimantadine Oseltamivir יעילות נגד שפעת A 70%–90% 70%–90% 70%–90% יעילות נגד שפעת B אין אין 70%–90% התפתחות של עמידות הנגיף לתרופה מהירה מהירה אטית, אם בכלל הפסקת התרופה עקב תופעות לוואי 11% (חלקן קשות) 6% 2% חיי מדף 5 שנים 5 שנים 10 שנים השפעת הטיפול קיצור המחלה ביום קיצור המחלה ביום קיצור המחלה ביום הפחתת התחלואה – מניעה לפני חשיפה 63% 63% 71% הפחתת התחלואה – מניעה לאחר חשיפה 63% 63% 83%
אמצעי זהירות בשל מגוון תופעות הלואי של התרופות האנטי-נגיפיות, יש להתייעץ עם מומחה למחלות זיהומיות לפני השימוש, הן לגבי בחירת התרופה והן לגבי המינון, ובכל מקרה יש לעיין בעלון היצרן.
תופעות לואי של אמנטדין: בחילה, סחרחורת, חוסר שינה, עצבנות, קשיי ריכוז. תופעות אלו ואחרות עלולות להופיע במיוחד אצל בני-אדם אשר סובלים ממחלות כרוניות, במיוחד זקנים, לכן נחוץ מעקב מיוחד לגבי אנשים אלה.
תופעות לואי של oseltamivir: בחילות והקאות.
זהירות מיוחדת דרושה כאשר הטיפול ניתן לאנשים הסובלים מליקויים בתפקודי הכליות, הכבד, מהתקפים אפילפטיים או נלקח בו-זמנית עם תרופות הפועלות על מערכת העצבים המרכזית. במצבים אלה יש לשקול הקטנת המינון ולהפסיק את הטיפול מיד עם הופעת תגובות חריגות.
לא מומלץ לנשים בהיריון ולמניקות.
סיכום המלצת ארגון רופאי הילדים בישראל היא חד משמעית בעד חיסון כל ילד מגיל חצי שנה. אין ספק כי ככל שיהיו יותר ילדים מחוסנים הרי שהסיכוי להתפתחות מגפות כלל ארציות קטן יותר. לפי דעת הכותב יש לחייב כל ילד\ אדם הלומד במוסד חינוכי מפעוטון ועד אוניברסיטה להתחסן לשפעת בטרם כניסתו לכותלי המוסד הלימודי (כפי שמקובל בארצות הברית וקנדה).
שפעת העופות והקשר לשפעת שפעת העופות (Avian influenza) היא סוג של שפעת נגיפית התוקפת עופות. לשפעת העופות שני זנים עיקריים: זן שאינו אלים (H9N2) וזן אלים (H5N1).
התגלו כמה עשרות הידבקויות וגם תמותה של בני אדם במחלה בדרום מזרח אסיה. כמו כן התגלו מוטציות רבות של הנגיף (לא כאלו שמועברות לבני אדם). החשש הכבד הוא שהנגיף הקטלני יעבור מוטציה שתקנה לו כושר הדבקה מהיר, בדומה לנגיף השפעת האנושי הנפוץ, ובכך יביא למגפה עולמית. לנגיף זה לא נמצאה תרופה שהוכחה כיעילה. קיימת הערכה שהתרופה "תמיפלו", הנמצאת בשימוש כנגד שפעת רגילה, יכולה להפחית את נזקו של הנגיף על האדם, אם כי לא לחסן מפניו. הסיבות להתפרצות המגפה במזרח אסיה
- גידול בע"ח (עופות, חזירים) בערוב ובצמידות למגורי אדם.
- שווקי עופות חיים מפותחים.
- צמיחה מהירה בגידול העופות האינטנסיבי.
- יצוא מפותח (הברחה של עופות).
- שימוש בתרכיבים ברמת איכות נמוכה (סין, אינדונזיה).
- רמת דיווח וניטור נמוכה.
- הסתרת מידע מכוונת מטעם השלטונות (אירועים החלו במחצית הראשונה של 2003).
- חוסר ניסיון בטיפול באירועים דומים.
- מחסור באמצעים כלכליים ומערכות פיצוי לחקלאים.
מגורים עם העופות- סין – מחלה מקצועית של מגדלי ומוכרי עופות סין ידועה מזה שנים רבות, כמקור להפצת נגיף השפעת. נראה שמקור הנגיף הוא דרום סין בדיקות רצף של הנגיף שבודד מברווזים שהוברחו לטייוואן מסין ב – 22/01/03, מצאו התאמה לנגיף שבודד מחולים בוייטנאם: מרבית בני האדם שנדבקו היו במגע ישיר עם עופות חולים, אך ישנם גם דיווחים שלא הוכחו על בני משפחה שנדבקו זה מזה. שפעת העופות תוקפת בעיקר בני אדם צעירים; כ 70% מאלו שנדבקו במחלה היו מתחת לגיל 20.
התסמינים הקליניים של בני אדם שחלו בשפעת העופות (H5N1) דומים לאלו של בני האדם שחולים בשפעת האנושית הרגילה (H3N2). מתברר, כי הנגיף H5N1 הקטלני מעביר מטען גנטי בינו ובין אחד ממיני נגיף השפעת הרגילה, ויוצר מוטציה קטלנית הגורמת למוות בהדבקתו את האדם.
במחקרים שבוצעו על עכברים גילו החוקרים שזנים חדשים של שפעת העופות שהוזרקו לעכברים הפכו לקטלניים יותר.
נגיף שפעת העופות H5N1 התגלה לראשונה ב 1961 בדרום אפריקה. הפעם הראשונה שבה אובחנה הדבקה של בני אדם על ידי מוטציה של הנגיף הייתה ב 1997 בהונג קונג, כששמונה-עשר בני אדם נדבקו במחלה ושישה מהם מתו. בתחילת 2003 חלו בסין שלושה בני משפחה אחת ושניים מהם מתו. בהמשך התגלו סימני המחלה אצל בני אדם בטייוואן, וייטנאם, דרום קוריאה, יפן, תאילנד, קמבודיה, לאוס, אינדונזיה ופקיסטן. מתוך 120 בני אדם שחלו במחלה, מתו 60. בסוף 2005 התגלו בטורקיה רומניה, ורוסיה התפרצויות של שפעת העופות בעופות, בעקבות נדידת עופות מהמזרח הרחוק, בנוסף נפוצו ידיעות על התפשטות המחלה ליוון שהתבררו כלא נכונות, שלטונות הבריאות בעולם נערכו למניעת הידבקות המונית של בני אדם במחלה. התפשטות זו של המחלה הביאה את ללחץ חזק על חברת "רוש", יצרנית תרופת טמיפלו, להתיר ייצור של התרופה על ידי חברות אחרות וזאת על מנת להגדיל את הייצור לאחר שהחברה מסרה כי לא תוכל לטפל בכל ההזמנות שהוזמנו ברגע האחרון למרות שהחברה הציע לממשלות להזמין אותן באמצע שנות ה-90, החברה נכנעה לבסוף ללחץ ובסוף אוקטובר 2005 החלה במשא ומתן עם חברות תרופות אחרות בנושא. במקביל החלו להתעורר פקפוקים בנושא יעילות התרופה לגבי הזן שעלול לעבור מוטציה אולם המצב בנושא זה עדיין איננו ברור.
החשש בישראל הוא שעופות נודדים שחונים חניית ביניים בשמורת החולה ובמקומות אחרים עלולים להעביר את המחלה לישראל.
לא ברור לאן פניה של המגפה ואם נכונה לנו בעתיד מגפה עולמית או לא. בעד מגפה עולמית העובדה שמדובר בנגיף שטרם תקף בני אדם ועל כן מערכת החיסון שלנו עדיין לא למדה כיצד להתגונן מפני נגיף זה. נגד - העובדה שעד היום לא קרה דבר. החששות שהובעו על ידי ארגון הבריאות העולמית ממגפה קשה של שפעת העופות נובע מקרבה ניכרת בין שפעת העופות שתקפה בדרום אסיה לנגיף השפעת הספרדית. החשש הוא כי נגיף השפעת הספרדית שתקף גם את העופות יעבור שינוי גנטי וכך יתקוף בחזרה בני אדם אשר לא יהיו מחוסנים כלפי הנגיף "המשופר". ההסתברות הסטטיסטית ששינוי כזה בנגיף יקרה בתקופה הקרובה הוא די גבוה. ועל פי מודלים מתמטיים חושב כי אם לא תהייה הכנה מוקדמת כנגד הווירוס הנ"ל הרי שצפויים להיפגע כ 150 מיליון איש ברחבי העולם תוך שנה אחת.
ארגון הבריאות העולמי דרש מישראל להצטייד במלאי תרופות כנגד השפעת שיספיקו לטיפול בכל אוכלוסיית ישראל.
צילום במיקרוסקופ אלקטרוני של וירוס שפעת העופות
RSV – הגורם לברונכיוליטיס
ברונכיוליטיס היא מחלה של דרכי הנשימה העליונות והתחתונות. מדובר במחלה עונתית נגיפית מגפתית. הגורם המחולל השכיח ביותר למחלה הוא וירוס ה-RSV ( Respiratory Syncytial Virus). הגורמים הנוספים הם וירוס השפעת ווירוס הפראאינפלואנזה. רוב ילדי העולם נדבקים במחלה זו בשנות חייהם הראשונות. לרוב מדובר במחלה בינונית בחומרתה שביטוייה הם כשל שפעת הנמשכת כ שבוע ימים. לעיתים המחלה יכולה להתבטא בחומרה גדולה יותר ואז היא דומה יותר לשילוב שבין שפעת + אסתמה + דלקת ראות בגוף שגילו לא עולה בדרך כלל על גיל חצי שנה. במקרים כאילה מחלה זו יכולה להמשך בין 10 ימים לשבועיים ויכולה בהחלט לסכן חיים. בתצורתה הקשה מחלה זו יכולה לגרום לאי ספיקה נשימתית, הפסקות נשימה עד מוות.
כ 20% מכלל אשפוזי החורף בילדים מקורם בווירוס זה.
וירוס ה-RSV שייך למשפחת ה- Para-myxo-viridea. לווירוס שני חלבונים עקריים על הקופסית שלו האחד שמו F - חלבון הגורם לאיחוי והחדרת המטען הגנטי לתא המאחסן והשני G הגורם להצמדה לתא המאחסן. הווירוס גורם ליצירת תאי ענק מרובי גרעינים ברקמת תאי הרירית של הגוף המארח. קיימים שני תת-מינים של הווירוס A – שאחראי על הזיהומים החמורים יותר ו B האחראי על 80% מכלל ההדבקות והוא הזן הפחות אלים.
צילום במיקרוסקופ אלקטרוני של הווירוס בתאי ענק מרובי גרעינים
גוף האדם יודע ליצור נוגדנים כנגד החלבונים G ו F ומכאן החיסון הטבעי המתפתח לאחר הזיהום. התפתחות נוגדנים כנגד חלבון F מקנה חסינות מלאה בעוד שנוגדנים כנגד חלבון G מקנים לנו חסינות חלקית בלבד. החיסון הסביל שניתן לתינוקות הוא נוגדן ספציפי כנגד חלבון F דבר המקנה חסינות זמנית מלאה כנגד הווירוס.
ממי נידבק בווירוס ההדבקה מתבצעת על ידי מגע יד מזוהמת בהפרשות מתינוק אחר. לא מדובר על הדבקה טיפתית. שרשרת הדבקה זו הניתנת לעצירה על ידי שטיפת ידיים ובפגיות בארץ ובעולם מקובל שימוש בכפפות חד פעמיות ומגני פנים וחלוקים למניעת הדבקת הפגים.
הדגירה במחלה קצרה ונמשכת בדרך כלל כיומיים בלבד ומרגע זה התינוק כבר מדביק אחרים. הווירוס מדביק את התינוק מייד עם כניסתו לפה והוא מופרש מילד מודבק מכל נוזלי הגוף. הווירוס מופרש כ 5 ימים מרגע ההדבקה ועד 3 שבועות מתחילת המחלה. למעשה בגן ילדים שאליו הובא תינוק אחד עם RSV ידביק תוך כיממה אחת את רוב התינוקות בגן כאשר המטפלות הן הווקטור למחלה.
כמחצית מהצוות המטפל \ מורים \ גננות ידבקו באותה הדבקה. שליש מהילדים ומהצוות שנדבק יסבלו גם מזיהומים נוספים חיידקיים שהם סיבוך שכיח למחלה זו (בעיקר דלקות אוזניים וריאות)
אפידמיולוגיה : המגפות בווירוס זה הן רחבות תחלואה ונמשכות כ 3 חודשים. התחלואה עונתית ומתרחשת בין החודשים ינואר ועד אפריל. הפגיעה באוכלוסייה רחבה מאוד וכל שכבות הגילאים יכולות להיפגע. עד גיל שנתיים רוב האוכלוסייה כבר נפגעת מווירוס זה. רוב הפגיעות הקשות מתרחשות בתינוקות מתחת לגיל שנה והפגיעה הקשה ביותר היא בפגים.
בכל חורף כ 15–20 אחוז מכלל אשפוזי הילדים מתחת לגיל שנתיים מקורם בהדבקה בווירוס זה.
מבחינה סטטיסטית קיימת שונות מובהקת בין שכבות האוכלוסייה. בשכבות סוציואקונומיות נמוכות שיעור האשפוזים גבוה פי 5 מאשר בשכבות החזקות יותר. הנתון הזה נכון גם בישראל ומודגש הרבה יותר בארצות הברית שם שיעור האשפוזים בשכבות חלשות מגיע לפי 10 מאשר בשכבות החזקות (צפיפות דיור, מספר ילדים בבית ורמת הכנסה נמוכה היו המנבאים החזקים ביותר לאשפוז בשל RSV ).
בנים מאושפזים פי 2 מאשר בנות – למרות תחלואה זהה בחומרתה בשני המינים.
הגורמים האתיולוגיים לברונכיוליטיס 1. RSV – 75% 2. פראאינפלואנזה וירוס 7% 3. אינפלואנזה B 7-10% 4. אדנו וירוס – 3% 5. מיקופלסמה – 1-2% 6. פנאומווירוס – 1%
גורמי הסיכון לאשפוז משקל לידה נמוך – מתחת ל 2200 גרם פגות – מתחת ל 28 שבועות היריון שכבה סוציו-אקונומית נמוכה עישון של ההורים העדר יניקה ביקור במעון או גן ילדים בן פי 2 מבת
קליניקה המחלה מתחילה כהצטננות רגילה המלווה בשיעול נזלת וחום. לאחר כיומיים מתחילת המחלה מתחיל שיעול עמוק יותר ומתחילים להופיע צפצופים וחרחורים על פני הראות. מופיעים התקפי שיעולים הנשמעים כהתקפי אסתמה קשה. התינוקות מתקשים באכילה, שתייה ויניקה. חלק מהתינוקות מפתחים בזמן אכילה קוצר נשימה והכחלה סביב לפה. לעיתים מופיעים סימנים של מצוקה נשימתית מתגברת הכוללים פעילות שרירים מוגברת של בית החזה (רתיעות), נשימת כנפי אף ואף הפסקות נשימה בעיקר בשינה – דבר הצריך להדליק נורה אדומה אצל ההורים. המחלה מתרפית מעצמה וברוב המקרים הקלים יותר לאחר כ 7 עד 10 ימים של חום ושיעול מתחיל תהליך החלמה הדרגתי הכולל את ירידת החולים והפסקה הדרגתית של השיעולים. חלק מהילדים ימשיכו להשתעל עוד מספר חודשים לאחר תום המחלה ואצל חלקם תתפתח אסתמה כרונית.
מה קורה בריאות ? מקור הפגיעה הריאתית בבצקת המתפתחת בדפנות העץ הברונכיאלי וזאת בשל הסננת הווירוס לאזור. התאים הפגועים מהווירוס נושרים לתוך חלל העץ הברונכיאלי ומתווספים להפרשות הסמיכות המופרשות מהברונכים הפגועים. כל ההפרשות הנל הופכות להיות יותר ויותר סמיכות וצמיגות ומפריעות מאוד בנשימה. בשלב הזה מופעלת מערכת החיסון שלנו המושכת בצורה כימית כמות גדולה של לימפוציטים המוסיפים לבצקת הכללית.
הבצקות וההפרשות יוצרות חסימות חלקיות או מלאות של דרכי האוויר הקטנים בריאה ונוצרים חללי אוויר גדולים הלכודים בריאה והחלקה הריאה עוברת תמט בשל חוסר אוורור.
הריאה מאבדקת חלק גדול מהאלסטיות שלה ומיכולתה לשמש כמכשיר כהעברת חמצן לרקמות ולשחרור פחמן דו-חמצני – מכאן ההפוקסמיה (חוסר חמצן בקרמות).
המצב יכול להיות קל ולהסתדר על ידי מערכת החיסון של הגוף הפוגעת בווירוס ולאחר תקופה של מספר ימים מתקנת את הנזקים. המצב יכול להגיע לאי ספיקה נשימתית המצריכה הנשמה בלחץ חיובי לשם פתיחת דרכי הנשימה המוצרים והמודלקים.
אוכלוסיית הסובלים ממחלת ריאה בסיסית כגון: אסתמה קשה, מחלה היאלינית של פגות, חולי CF הם ילדים המועדים להיפגע קשות מווירוס זה.
ילדים הסובלים ממחלות לב קשותאו מחלות מטבוליות קשות גם כן מועדים להפגע קשה יותר מווירוס זה.
אבחנה : ברוב המקרים רואים בבדיקה תינוק קטן הסובל מחום גבוה וברוב המקרים גם ממצוקה נשימתית ניכרת. האבחון הוא קליני בדרך כלל ניתן לשמוע על פני הראות ציפצופים אקספירטוריים ואינספירטוריים – דהיינו הן בשאיפה והן בנשיפה. בחלק מהמקרים ניתן לשמוע חירחורים עדינים על פני בסיסי הריאות וכן קולות המזכירים נייר פרגמנט מקומט (קרפיטציות). ברוב המקרים מוצאים נשימה מהירה עם שימוש ניכר בשרירי בית החזה לנשימה וכן תנועה של כנפי האף המצביעים על מצוקה נשימתית. מצוקה נשימתית קשה יותר ניתן לראות על ידי כיחלון סביב השפתיים, כיחלון באצבעות ורתיעות בין צלעיות. כל הנ"ל יכולים להצביע על מעורבות של חלק גדול מהריאות בתהליך דלקתי רחב. בדיקת ריווי חמצן בדם שהיא בדיקה פשוטה מאוד בעזרת מתמר קטן המצוי בכל מרפאה יכולה לתת אינדיקצייה מיידית לגבי מצבו האמיתי של הילד\ תינוק. ריווי חמצן שיורד מ 92 אחוז משמעו פגיעה בינונית ברקמת הריאה ומתחת ל85–90 אחוז יש להפנות את התינוק באופן מיידי לבית חולים. בדיקות עזר העומדות לרשות הרופא: צילום חזה בו ניתן לראות תמונה אופיינית מאוד למחלה זו. בספירת דם ניתן לראות לעיתים עליה של מספר הכדוריות הלבנות - מצביע על תהליך דלקתי ממקור זיהומי. בבתי החולים בחדרי מיון קיימים תבחינים ספציפיים אותם מספק משרד הבריאות שנועדו לאיתור מהיר של הווירוס מהפרשות. התבחין אמין מאוד והתשובה מתקבלת מיידית. תבחינים אלה נמצאים רק במרכזים רפואיים ובחדרי מיון ולא במרפאות הקהילה (מחיר).
אסתמה לאחר ברונכיוליטיס : אין ספק כי קיים קשר סטטיסטי בין תחלואה ב RSV בגיל צעיר והופעת אסתמה. מאות מחקרים נכתבו על נושא זה ולא קיימת תמימות דעים לגבי הדרך בה נגרמת מחלת ריאות כרונית לאחר זיהום וויראלי זה.
לעיתים לאחר סיום המחלה יש צורך במתן טיפול מונע עם סטרואידים בשאיפה או עם חוסמי לויקוטריאנים לשם טיפול בהתקפי קוצר הנשימה.
טיפול : הטיפול בעיקרו הוא טיפול תומך וכולל מתן חמצן בשעת הצורך, אינהלציות של מרחיבי סימפונות, סטרואידים ואנטיביוטיקה בזמן הדבקה חיידקית משנית.
בתינוקות מתחת לגיל שנה מקובל לתת סטרואידים בשאיפה בעזרת מכשיר אינהלצייה. שני התכשירים המצויים בשוק בודיקורט רספיולס ופליקסוטייד נביולס. לתכשירים אילו השפעה יחסית קטנה על הקליניקה ורב הוויכוח על הצורך במתן טיפול בסטרואידים למחלה זו.
רוב התינוקות הקטנים מצריכים השגחה בבית חולים תחת ניטור של ריווי חמצן בדם.
הפסקות נשימה הן אחת הבעיות הקשות איתן חייבים להתמודד במהירות ולכן בדרך כלל נוטים לאשפז תינוקות קטנים החולים בברונכיוליטיס לשם ניטור אפניאות תחת השגחה רפואית בבית חולים.
חיסון למרות ניסיונות ארוכי שנים לייצר חיסון פעיל יעיל הרי שחיסון כזה עדיין לא קיים בשוק.
החיסון היחידי הקיים הוא חיסון סביל שהוא נוגדן ספציפי אותו ניתן לתת כמניעה בטרם מתחילה עונת המחלה.
על פי קריטריונים שנקבעו על ידי משרד הבריאות החיסון הסביל ניתן רק לקבוצות אוכלוסייה בסיכון גבוה מאוד – פגים קטנים שנולדו מתחת ל 28 שבועות היריון. זו קבוצת הגיל אותה מכסה סל הבריאות (מחירו העדכני של החיסון הוא כ 1900 ₪ לפג ).
ניתן לרכוש את החיסון באופן פרטי – מחירו באופן פרטי גבוה בהרבה ויכול להגיע ל 3000 דולר לילד.
החיסון, שאושר לשימוש ב-1999 ומשווק בישראל על ידי חברת אבוט, הוא חיסון סביל, המכיל נוגדנים בדומה לאלה שיילוד בשל מקבל באופן טבעי מאמו, ופעיל כ-30 יום. זיהומי ה-RSV מופיעים לרוב בתקופת החורף; מתן זריקה חודשית של החיסון בתקופה זו מפחית את הסיכון ללקות במחלה ב-80%-55%, ומפחית את הסיכון לאשפוז בשל הווירוס ב 60%. החיסון הוכנס לסל הבריאות בישראל ב-2001, אך בשל עלותו הגבוהה - כ-35 אלף שקל לפג לטיפול מלא - הוחלט לתת אותו רק לפגים שנולדו מהשבוע ה-28 ומטה, ושלא הגיעו לגיל שישה חודשים לפני מועד מתן החיסון הראשון. עוד מקבלים אותו פגים החולים במחלת ריאות כרונית ותינוקות עם מומי לב מולדים.
החל מממועד כתיבת מאמר זה (2006) הוחלט שהחיסון יינתן על ידי קופות החולים, ולא בבתי החולים, כפי שהיה נהוג.
אוכלוסיות הנמצאות בסיכון – התוויות לחיסון פגים ותינוקות עם מחלת ריאות כרונית חשופים יותר לזיהומים בדרכי הנשימה התחתונות, אשר עשויים להוביל לאשפוז. אוכלוסייה זו עשויה גם לסבול מהשפעות ארוכות טווח של התחלואה, כגון אסתמה. אצל פגים הריאות ומערכת החיסון אינן מפותחות. כמו כן, פגים אינם מקבלים מהאם נוגדנים כנגד RSV, שכן עיקר הנוגדנים עוברים מהשבוע ה-35 להיריון. מכאן שפגים נמצאים בקבוצת סיכון, והמחלה עלולה להסתבך אצלם, תוך כדי שהיא עוברת לדרכי הנשימה התחתונות, עד כדי אשפוז בטיפול נמרץ הכולל הנשמה מלאכותית ובמקרים קיצוניים גם למוות. וירוס RSV הוא הגורם הנפוץ ביותר לאשפוז חוזר של פגים.
אבו סינגיס הוא טיפול למניעת זיהום וירוס RSV. מדובר בחיסון סביל המכיל נוגדנים מוכנים. החיסון הוא תוצר של הנדסה גנטית מגורם אנושי ברובו. הטיפול נמצא בסל הבריאות ומיועד לפגים שנולדו עד שבוע 28, שהשתחררו מביה'ח וטרם מלאה להם חצי שנה. כמו כן, פגים עם מחלת ראות כרונית, עד גיל שנה או שנתיים אם הם תלויי חמצן, זכאים לקבל את הטיפול. בשנה שעברה חוסנו 330 פגים. הטיפול המניעתי ניתן בזריקה חודשית במשך 5 החודשים בהם הוירוס פעיל (נובמבר עד מרץ). בזריקה מוזרק נוגדן ספציפי לוירוס. על פי המלצות של האקדמיה האמריקאית לרפואת ילדים יש לחסן פגים שנולדו עד שבוע 28 וטרם מלאה להם שנה, פגים שנולדו בשבוע 29–32 וטרם מלאה להם חצי שנה ופגים שנולדו בשבוע 33–35 שטרם מלאה להם חצי שנה ויש להם 2 גורמי סיכון (כגון: אחים קטנים בבית, הורה מעשן ועוד). החיסון מפחית 55%-80% מהאשפוזים הקשורים ל-RSV אצל פגים ומפחית עד כ־57% שיעור האשפוזים במחלקה לטיפול נמרץ.
הגנה ביתית כנגד RSV ישנם מספר צעדים שהורים יכולים לנקוט כדי לעזור להפחית את הסיכון לזיהום בשל וירוס RSV:
- רחיצת ידיים תכופה של מי שבא במגע עם התינוק.
- העברת מוצרי היגיינה משומשים לפח סגור (קיימים פחים אטומים).
- ניקוי וחיטוי של צעצועי התינוק, במיוחד אם ילד אחר שיחק בהם.
- שימוש בחדרי שינה נפרדים לתינוקות וילדים בגיל ביה'ס במידת האפשר.
- הימנעות משהות במעון יום.
- שמירת מרחק בין התינוק לבין אדם עם סימפטומים של צינון.
- הימנעות משיעון בסביבת התינוק \ להימנע מעישון בבית.
- הימנעות משהות במקומות הומי אדם
לסיכום : מדובר במחלת ילדים הדומה מאוד בהתנהגותה לשפעת קשה שהמחולל העיקרי שלה הוא ה RSV. רוב הילדים עוברים מחלת חום זו ללא בעיות מיוחדות. הבעיות העקריות במחלה זו היא בשכבת הילדים מתחת לגיל שנה ובפגים. בשתי הקבוצות מחלה זו יכולה להיות קשה מאוד ואף קטלנית. מחלה זו אחראית לחלק לא מבוטל מאשפוזי התינוקות כל שנה בחודשי החורף. ניתן למנוע מחלה זו בקבוצות הגיל הבעייתיות על ידי חיסון סביל וזאת בזמן מגפות. מחירו של החיסון גבוה מאוד. עדיין אין בנמצא חיסון פעיל למחלה זו. מנינגוקוק – ("החיידק האלים") - Neisseria meningitides (- אינו בחיסוני השגרה)
הקדמה : התחלואה בחיידק זה חוזרת לכותרות מידי מספר שנים בשל התפרצויות מקומיות ותוצאתן ההרסנית באותו אזור. בשנות התשעים היינו עדים להתפרצויות קשות באזור הצפון אז נפגעו בו זמנית מספר רב של ילדים בבריכת שחייה באחד הקיבוצים בצפון, לאחר מכן התפשטה המחלה לעיר נהרייה ונמצאה גם במספר כפרים הסמוכים לעיר זו. אחוזי התמותה בשנים אלו עמד על למעלה מ 75% ב 24 השעות הראשונות לחשיפה לחיידק.
החיידק בודד וזוהה סופית בשנת 1887. מאותה תקופה מעמיד חיידק זה אתגר קשה בפני הרפואה המודרנית המצליחה לפגוע בחיידק זה רק לאחר חדירתו לגוף על ידי מתן תכשירים אנטיביוטיים יעילים אך לא קיים חיסון יעיל למחלה זו.
שמו המלא של החיידק הוא Neisseria meningitidesוהוא חיידק עגול וקטן שאינו נצבע בצביעה מיוחדת לחיידקים הנראית צביעת גרם (מכאן שהחיידק גרם שלילי). עד היום נמצאו 13 זנים שונים של חיידק זה המכונים על פי אותיות. הזנים נבדלים האחד מהשני על פי צורת המעטפת הרב סוכרתית משולבת החלבון שלהם (למעשה על פי חלקי המעטפת המוצגים כלפי חוץ). באימונולוגיה מודרנית אנו משתמשים בצורות הסוכרתיות הנ"ל לשם יצירת חיסונים ספציפיים כלפי אותם חיידקים.
הזן מסוג B הוא הקשה ביותר ל"טיפול אימונולוגי" וזאת בשל צורת מעטפת המקשה מאוד על יצירת חיסון. חיידק זה הוא החיידק התוקף ילדים בישראל ובחלק מהמקרים גורם למותם.
החיידק וגוף האדם: החיידק נמצא בבני אדם בלבד ולא בבעלי חיים – זאת אומרת שהאדם הוא המעביר היחידי של החיידק בטבע וגם בית הגידול היחידי של החיידק. מכך עולה כי חלק מהאוכלוסייה הבריאה חייבת לשאת את החיידק באופן קבוע אחרת החיידק היה נעלם מהעולם. אכן כ% 5 מכלל האוכלוסייה הבריאה נושאית חיידק זה בלוע (בתקופה ללא מגפות) ובתקופת מגפות גדולות שכיחות החיידק הנישא בלוע של ילד בריא לחלוטין יכול להגיע אפילו ל 30% מכלל הילדים עד גיל שנתיים. מעניין הוא כי רוב הנשאים הם בוגרים – דהיינו מעל גיל 18 שנים ורוב החולים הם תינוקות – מתחת לגיל שנתיים.
החיידק חודר אלינו דרך מערכת הנשימה בהדבקה טיפתית (בדומה לרוב החיידקים). החיידק מתיישב ומתרבה בלוע האדם. סיכויי החדירה של החיידק את רקמות הלוע בהם הוא יושב והגעה למחזור הדם הוא נמוך מאוד בשל היותו חיידק שהגוף מצליח ברוב המקרים לפגוע בו המהירות בכל ניסיון חדירה.
בחלק מאוד קטן מהילדים (אשר לנו כרופאים לא ברור מי מהילדים חשוף יותר ולמה) מתרחשת העברה לדם שם מייצר החיידק מחלה קשה מאוד ולמעשה הופך להיות אלים וטורף. לא ברור מדוע הופך החיידק לאלים אך ברור כי בזמן מגפות אלימותו משתנה בייחוד של זן B (האלים יותר) שהופך תוך שעות ממצב של נשא למצב של מחלה קשה המסכנת חיים. לכל שאר הילדים הנושאים את החיידק בלוע ולא מתפתחת מחלה פולשנית הרי שתוך מספר ימים יתחילו להיווצר נוגדנים כנגד החיידק ותוך מספר שבועות בודד יהיה הגוף מחוסן לחלוטין בפני החיידק. היות שרוב הנדבקים הם תינוקות עלתה השאלה מתי יורדת כמות הנוגדנים שקבלו מאמם והאם קיימת התאמה לכך במועד ההדבקה. אכן נמצא כי לרוב התינוקות שנולדים חיסון מלא כנגד החיידק שמועבר להם דרך השלייה או בהנקה. בין חצי שנה לגיל שנתיים מתחילה ירידה הדרגתית של החיסון האימהי ומתחילה להיווצר חסינות נרכשת (ראו ערך מערכת החיסון הנרכשת בתחילת הספר). החסינות הנרכשת מקורה בחשיפות אקראיות לחיידק שלא בזמן מגפה בזמן שאלימותו נמוכה יחסות ואז לגוף יש מספיק זמן לייצר נוגדנים המגנים עלינו בזמן הופעת המגפות. נראה כי לכל אותם ילדים שנפגעו מהחיידק בצורה אלימה כל כך לא היו מספיק נוגדנים שהיו אמורים להירכש מוקדם יותר או שמערכת החיסון של אותם ילדים הייתה ירודה יותר (מצב סוציואקונומי ירוד עם רמת תברואה נמוכה). חיידק זה יודע לפגוע לא רק בזמן מגיפות ואף יודע לפגוע סביב השנה באופן אקראי כאשר הוא פוגש מאכסן שלא מצליח לפתח נוגדנים כלפיו.
בשל התפתחות של רפואה מונעת יעילה מאוד דלקות של העוצבה (קרום המוח) הפכו לדבר נדיר ורוב התוקפים הם ווירוסים שלא גורמים נזק קבוע למוח. לחיידק זה (שאין דרך כרגע לחסן בפני זן B שלו מקום חשוב מאוד ביצירת נזקים קבועים במוח בשל גרימת מחלה פחות אלימה ממנינגוקוקסמיה (דלקת המועברת דרך הדם) והיא דלקת קרום המוח.
אפידמיולוגיה : בישראל, כ-1,500 איש מתדרדרים מדי שנה למצב של אלח דם חמור ומבין המקרים כ־30%-50% מסתיימים במוות (בארצות הברית כ-750,000 מדי שנה). מתוך קבוצה זו בין 40 – 60 סובלים מאלח דם על רקע פלישה של מנינגוקוק אלים וכל השאר מחיידקים אחרים.
אלח דם חמור הוא זיהום כללי אשר גורם לכשל מערכות וידוע בקרב רופאי היחידות לטיפול נמרץ כגורם העיקרי לתמותה של חולים המאושפזים במחלקות לטיפול נמרץ בבתי חולים.
מספר גורמים מהווים זרז להחמרת הזיהום עד למצב של אלח דם חמור: טראומה שלאחר ניתוחים וטיפולים חודרניים, עמידות של סוגי חיידקים לאנטיביוטיקה, כוויות, תאונות דרכים או מחלות כגון סרטן ודלקת ריאות, כל אלה מחלישים את מערכת
צילומים במיקרוסקופ אלקטרוני של החיידק
החיסון של הגוף. מהירות טיפול היא גורם מכריע בטיפול באלח דם חמור. ידועים מקרים רבים על קושי בזיהוי ואבחון המצב הקליני אשר מוביל למוות מהיר של המטופל. אמצעי הטיפול המקובלים כוללים טיפול בזיהום על ידי מתן אנטיביוטיקה וטיפול תומך לאיבר (מערכת) שנפגע.
המחלה פוגעת בכל חודשי השנה אך קיימת נטייה לתחלואת יתר בעיקר בחודשי האביב המוקדמים (אפריל – מאי). יותר מ 50% מכלל הנפגעים הם ילדים הקטנים מגיל שנתיים. גיל הנפגעים יורד מאוד בזמן מגפות גדולות כאשר אז הזנים הפחות אלימים דווקא שולטים (בעיקר זן A ). זן A היווה את הזן השולט במגפות הגדולות לפני מלחמת העולם השנייה אך כמעט נעלם לחלוטין לאחריה.
ההנחה האפידמיולוגית היא כי שינוי חד במצב הסוציואקונומי ושיפורו ב 50 השנים האחרונות עם שיפור ניכר במערכת התברואה בעולם המתועש תרמו במידה ניכרת לירידה ניכרת במספר המגפות.
כ 80% מכלל ההדבקות בעולם נגרמים על ידי 5 זנים A,B,C,Y,W135. באירופה שולטים הזנים B ו-C ואחראים לרוב ההדבקות. באסיה ואפריקה רוב ההדבקות מקורן בזנים A,C. בישראל הזנים השולטים הם B ו Y המהווים את רוב ההדבקות החדשות.
אפריקה היא האזור הגאוגרפי הסובל ביותר מחיידק המניגוקוק האזור המוכה מכונה "חגורת המנינגיטיס" ומשתרע מאתיופיה במזרח ועד לסנגל במערב. באזור זה שכיח הזן A. שכיחות התחלואה באזור זה גדולה פי 100 מאירופה וארצות הברית אחת ל 10 שנים לערך מתחוללת באפריקה מגפה שמעלה את שכיחות התחלואה ל 1000 מקרים לכל 100.000 תושבים. שכיחות התמותה מתחלואה בחיידק באזור זה עומדת על 20%.
סוג B פעיל יותר בחורף ואחראי על המקרים המפוזרים והתפרצויות קטנות. הסוג W135 נפוץ מאוד בעולי רגל המקיימים את מצוות החאג' וכל שנה מספר לא מבוטל של עולים לרגל נחשפים לחיידק זה ומתים בזמן החאג'. בישראל נהוג לחסן את כל עולי הרגל למכה.
קליניקה כפי שנכתב עוד קודם מקור הבעיה הוא במהפך של חיידק נוח ועדין להיות אלים ופולשני ומעבר שלו לתוך מערכת הדם תוך כדי חציית כל המחסומים בדרכו מהלוע. חיידק אלים כזה גורם למחלה קשה מאוד המכונה מנינגוקוקסמיה הגורמת לאלח דם וזריעה של החיידק לכל אברי הגוף. בשל זריעה מפושטת זו נפגעים רוב אברי הגוף בו זמנית : ראות, מוח, אוזניים, מפרקים, לב, מעי ובלוטות יותרת הכליה. אפילו שרירים ורקמות העור הם אברי מטרה. אין אבר בגוף שלא יכול להיפגע מהחיידק ולכן המחלה מאופיינת בקריסת מערכות מהירה ביותר.
אבחון מחלה זו בשלביה המוקדמים הוא קשה במיוחד ודורש ניסיון רב כיון שלמעשה היא אינה שונה בצורה משמעותית ממגוון מחלות אחרות כמו שפעת או הצטננות רגילה המלווה בחום. תחילה גורם המנינגוקוק לתסמינים שונים במערכת הנשימה העליונה: נזלת, שיעול קל המלווים בחום גבוה על אלה עשויה להתלוות פריחה כתמית אדומה-כחלחלה על פני העור, שאינה נעלמת בנגיעה קלה. המנינגוקוק עלול לגרום גם לפגיעה במערכת העצבים, עד לירידה במצב ההכרה ופרכוסים.
הנזק נוצר מפגיעה בכלי הדם דרכם הוא עובר – ביציאתו החוצה מכלי הדם הוא יוצר קרישי דם בשל נזק לתאים הנקראים תאי אנדותל המרכיבים את כלי הדם. פגיעה רב מערכתית כזו בשל ירידה באספקת הדם לרוב אברי הגוף גורמת לקריסה מהירה ולירידה חדה בלחץ הדם. מלה קשה זו מסתיימת במוות ב 15 – 50% מהחולים כתלות במדינה (במדינת ישראל כ 10% תמותה לעומת 50% בשנות השמונים). גם כאן חלק גדול מהחולים במנינגוקוקסמיה חובלים רק ממחלה קלה ורק לחלק קטן מחלה דרמטית וקשה מאוד. לאבחון מצב זה יש צורך בצפייה ישירה של החיידק בדם וזיהוי אנטיגני שלו בצביעות מיוחדות. הבדיקות מבוצעות דרך מחלקת טיפול נמרץ. מחלה קלה יותר יחסית נצפית אצל כל אלה שהסימפטום הראשון שלהם היה התפתחות של דלקת קרום המוח. בחולים אילו המחלה מתחילה בדרך כלל בצורה פתאומית עם כאבי ראש חום גבוה ובהמשך מופיעים סימני דלק קרום המח הכוללים קשיון עורף בבחילות והקאות. בילדים צעירים מאוד סימני דלקת קרום המח לא אופייניים וכוללים מרפס בולט ופועם, אי שקט ועצבנות, הכרה מעורפלת והתנהגות שאינה מאפיינת אותו. גם כאן ב 75% מהמקרים ניתן לבודד בתרבית דם חיידקים. בחולים אילו ניתן לזהות את החיידק בנוזל השדרה בבדיקה המכונה LP (ניקור נוזל השידרה). דלקת ריאות מתחוללת ב 20% מהחולים אך דלקת זו די מעטה בסימפטומים ממוקדים וקל מאוד לא לזהות אותה בתחילת המחלה למעשה הפעולות בחדר המיון די קבועות - בחדר המיון תעברו בדיקת רופא, לאחריה במידת הצורך יבוצע הליך הקרוי "בירור ספסיס מלא" הכולל בדיקות דם, בדיקת נוזל שתן, ובדיקת נוזל שדרה – על ידי ניקור מותני לשם איתור החיידקים. בחשד לזיהום בחיידק, לאחר מכן מועברים כל הילדים לאשפוז במחלקה בחדר מבודד או לטיפול נמרץ בזמן אבחון של מנינגוקוקסמייה, והילד יקבל טיפול אנטיביוטי לתוך הוריד למשך מספר ימים, עד לקבלת תשובה סופית מהמעבדה על סוג החיידק המדויק שצמח בתרבית שנלקחה.
זיהוי החיידק בחולים החשודים נלקחות תרביות הן מהדם והן מנוזל עמוד-השדרה. תרביות אילו מודגרות בתנאים הנוחים להתרבות החיידק ואם הוא אכן קיים בנוזלים הללו ניתן לזהות אותו בדגימות, לאחר כיומיים.
קיימות בדיקות ישירות לזיהוי הנקראות אימונופלורסצנטיות – בדיקות אילו מבוצעות מיידית לאחר צפייה ישירה בחיידקים בדם וזאת על מנת לקבל את סוגו המדויק של זן החיידק והערכת הטיפול על פי אלימות החיידק.
כמה קטלני החיידק ? בכל העולם המערבי אחוזי התמותה נעים סביב 10% - וזאת ב 10 השנים האחרונות. למרות שיפור ניכר בטכנולוגיה ובטיפול התרופתי הרי שלא חל שום שינוי באחוזי התמותה בעשור האחרון. נמצאו שינויים קלים בקשר בין גיל החולה לתמותה אך השינויים לא משמעותיים מבחינה סטטיסטית גלובאלית. סיבוכים מהמחלה נפוצים – כ 25% מכלל הנפגעים מסיימים עם חסר כלשהו – פגיעה בשמיעה, חסרי עור, נזקים לגפיים, שרירים ועצמות.
טיפול במגעים קרובים היות שהסיכוי ללקות במחלה לאנשים שבאו במגע קרוב עם חולה במנינגוקוקסמיה הוא פי 500 מאשר שאר האוכלוסייה הרי שמקובל לטפל בכל הנחשפים.
הטיפול כולל טיפול אנטיביוטי רחב טווח בזריקה לקטנים ובכדור לבוגרים. מקובל לחסן את כל המגעים הקרובים בחיסון פעיל (במקרה ומדובר במחנות צבא או בתי ספר גדולים).
מניעה וחיסון: עיקר תפקידו של משרד הבריאות הוא ביצירת סגר על אזור נגוע וטיפול אנטיביוטי לכל המגעים הקרובים של החולה. ניראה כי תברואה טובה ומצב בריאות טובה של כלל האוכלוסייה יכולים למנוע חלק ניכר מהמעבר המהיר של החיידק מאדם לאדם ולהקטין את הפיזור הארצי שלו (טיפול ברמה לאומית). תפקידו של משרד הבריאות בחיסון אוכלוסיות ספציפיות של חולים כרוניים הסובלים מהמחלות הבאות או במצבים מיוחדים:
- חולים שעברו כריתת טחול.
- חולים עם הפרעה בתפקוד הטחול כגון אנמיה חרמשית.
- אנשים חסרי טחול מלידה.
- חולים המיועדים לעבור כריתת טחול, מתן החיסון לפני כריתת הטחול.
- חולים עם חסרים מסוימים במרכיבי המשלים ). נקבע עי בדיקות אימונולוגיות מיוחדות במחלקה לאימונולוגיה).
- לחולים עם חסרים במערכת החיסון מסיבות שונות (מחלות של מערכת החיסון וחולי איידס).
- תיירים לארצות בהן המחלה אנדמית או בהתפרצות עונתית
- חיסון בזמן התפרצות נקודתית של אוכלוסייה בסיכון להדבקה ישירה (בית ספר לאחר הדבקה של אחד הילדים, מחנות צבא וכו' )
החיסונים הקיימים הארץ הם Mencevax AC, Mencevax ACWY. החיסונים ניתנים בזריקה תוך שרירית במינון של 0.5 מ"ל בכל הגילאים. אין הבדל במינון לעומת גיל.
החיסון אסור לחולים הידוע שרגישים לחיסונים, ולחלבון. החיסון מאושר למתן בהיריון רק כאשר שנה התוויה מיוחדת – סיכוי גבוה להדבקה. אישור לחיסון בהיריון חייב להגיע ממומחה בזיהומים או ממשרד הבריאות המחוזי.
תופעות הלוואי מהחיסון מעטות וכוללות נפיחות מקומית, כאב מקומי ואף חום שיכול להתפתח ב 24 השעות הראשונות לאחר החיסון. לא נצפו תופעות לוואי קשות יותר.
טיפול: הטיפול המיידי הוא אנטיביוטיקה תוך ורידית כאשר רוב זני המנינגוקוק מגיבים לרוצפין תוך ורידי (צפלוספורין דור III ). מתן סטרואידים תוך ורידי הוא חלק מאלגוריתם הטיפול במחלה.
כל החולים מאושפזים במחלקות טיפול נמרץ ללא קשר למצבם תוך כדי מתן נוזלים תוך ורידי וניטור קבוע אחר כל מערכות הגוף.
התרופה זיגריס, המאושרת על ידי משרד הבריאות בישראל, היא תרופה ראשונה מסוגה לטיפול באלח דם חמור, אולם עדיין איננה כלולה בסל התרופות ובשל מחירה הגבוה ניתנת רק במקרים מעטים, למרות היותה תרופה מצילת חיים.
מדובר בטיפול הניתן בהזרקה תוך וורידית למשך 96 שעות ומפחיתה את הסיכון למוות ב־30%. זיגריס, מהווה נקודת מפנה בטיפול. מדובר בטיפול חדשני ויחיד לטיפול באלח דם חמור. מדובר בפרוטאין C אקטיבי. התרופה פועלת על 3 מערכות בו זמנית ומיוצרת בטכנולוגיה של ביולוגיה מולקולארית והנדסה גנטית.
לסיכום: כל התסמינים זהים למחלת חום רגילה וחום כשלעצמו הוא תסמין שכיח אצל תינוקות וילדים, ולפיכך אין צורך בכל עליית חום בטיפול רפואי, שכן ברוב המקרים המדובר בדלקת נגיפית החולפת מאליה. אם בנוסף לחום הגבוה הילד ישנוני, מסרב לאכול, ומופיעה על פני העור תפרחת בצורת כתמים אדומים – כחלחלים שאינה נעלמת למשך שניות לאחר לחיצה קלה באצבעות על המקום, או במקרה של הופעת פרכוסים או חוסר הכרה, יש לפנות לרופא או לחדר מיון מיידית.
אכן יש לגלות ערנות לזיהוי הסימנים שהוצגו למעלה ולהחיש את החולה לקבלת טיפול רפואי.אך למרות ההד התקשורתי והפאניקה הרבה עדיין מדובר במחלה נדירה ובחיידק מוכר כך שהפחד מחיידק זה הוא ברוב המקרים מוגזם ונטול בסיס הגיוני.
(התרשימים נלקחו מנתוני משרד הבריאות)
מנתוני משרד הבריאות
נלקח מהרצאתו של פרופ' מנפרד גרין המרכז הלאומי לבקרת מחלות משרד הבריאות


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק