Programmed death-ligand 1
| מדריך בדיקות מעבדה | |
| Programmed death-ligand 1 | |
|---|---|
| שמות אחרים | PD-L1 , cluster of differentiation 274 (CD274), B7 homolog 1 (B7-H1, SP142; ISPDL1SP142IHC; GPPDL1SP142. |
| מעבדה | אימונולוגיה בדגימות ביופסיה |
| תחום | אימונותרפיה |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
זיהוי גידולים סרטניים המבטאים על פניהם את PL-L1.
היסטוריה
כבר לפני למעלה מ-120 שנה היו עדויות לכך שמערכת החיסון של הגוף מסוגלת לתקוף תאים סרטניים. בשנות ה-80 של המאה ה-19 הצביע האימונולוג פאול אהרליך על אפשרות זו, ובשנת 1896 פרסם הכירורג William Coley בכתב העת של בית החולים Johns Hopkins את האפשרות שניתן לגרות ולעורר את מערכת החיסון כנגד תאים סרטניים בגידולים סולידיים על ידי הזרקה של טוקסינים שהופרשו מחיידקים לגופם של 160 חולי סרטן, בהם טיפל.
חלפה עוד מחצית המאה עד שהאימונולוג האוסטרלי McFarlane Burnet טבע את המושג Cancer Immune Surveillance לפיו מערכת החיסון בגופנו מפקחת באופן מתמיד על התפתחות תאים סרטניים, ועל בסיס תאוריה זו פותחה בין השאר הגישה של גירוי המערכת החיסונית ל"תקיפות יתר" בהשמדת תאי סרטן שלפוחית השתן על ידי הזרקה תוך-עורית של תמצית המוכנה מחיידק המתג Bacillus Calmette–Guérin.
תאוריות וגישות טיפוליות אלו נולדו "טרם זמנן", במובן שבתקופה המוקדמת יחסית בה הן התפרסמו לא הייתה עדיין קיימת תשתית של ידע והבנה של המנגנונים התאיים והמולקולאריים בהם מערכת החיסון פועלת לניטור ונטרול תאי סרטן. זריקת עידוד לתאוריה המוקדמת של Burnet ניתנה בשנת 2001 במאמר מכונן ב-Nature של Robert Schreiber ו-Lloyd Old, בו הודגם שטיפול באינטרפרון-γ עשוי לעורר לימפוציטים לתגובה חיסונית כנגד תאי סרטן, ובשנת 2007 דיווחו אותם חוקרים על היכולת של מערכת החיסון לבלום תאי סרטן מהתפשטות ולשמור אותם בשיווי משקל תת-קליני סמוי.
גם Robert Weinberg איש MIT הציע בסקירה שלו שהתפרסמה בשנת 2011 ב-Cell, שגידול סרטני חייב להתחמק מעיניה הפקוחות של מערכת החיסון על מנת לשגשג ולהגיע לביטוי קליני בגוף. סודותיהם של תהליכים סרטניים, ו"סירובם" להיכנע להפגנת הידע המצוי בידנו בנקודת זמן זו בניסיונות להתגבר על תהליכים אלה, עדיין מהווים אתגר רב לעוסקים במחקר הרפואי. כך לדוגמה, הגישה שנהגה בדור האחרון במתן ציטוקינים כגון אינטרפרון-α או IL-2 על מנת לגרות ולעודד אימונותרפיה של סוגי סרטן שונים או אף בחיסון עם תמציות של תאי סרטן מומתים על מנת לעורר במערכת החיסון תגובה כנגד אנטיגנים המופיעים על שטח הפנים של תאי סרטן אלה, לא זכתה לעדנה רבה, או כפי שציין חוקר הסרטן Steve Rosenberg בסקירה משנת 2012, הייתה אפילו תחילת אכזבה מהתאוריה לפיה מערכת החיסון חיונית באופן מוחלט לדכא תהליכים סרטניים.
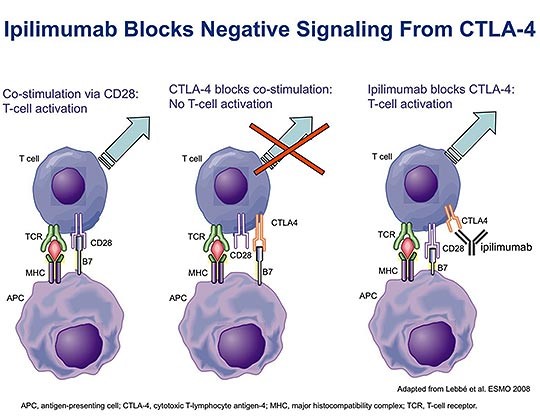
מחקריו החלוציים של Allison בעכברים בתחילת שנות ה-90 הדגישו את החשיבות של CLTA-4 כנקודת בקרה חיסונית (check point) החיונית לפעילות תאי T. Allison הראה שבתהליך השפעול של תאי T, רמת הקולטנים מסוג CTLA-4 עולה באופן ניכר על פני תאים אלה, וכן מצא Allison שהזיקה (affinity) של CTLA-4 ל-B7 הרבה יותר חזקה מזו של CD28, ולכן נוצר קשר מועדף בין CTLA-4 ו-B7, מה שגורם לשיגור אותות מעכבים אל תוך תא T, וממילא מפחית את רמת האיתותים המשפעלים שמעביר בדרך כלל הקולטן CD28 לתוך תאי T, זאת כיוון שרמת הקשירה של CD28 ו-B7 קטנה. אז כבר הבין Allison שכדי להשיג תגובה יעילה יותר של תאי T כנגד תאים סרטניים, יש צורך לחסום את CTLA-4.
כהמשך טבעי לתאוריה זו, הכין Allison נוגדנים חד-שבטיים כנגד CLTA-4 ובחן אותם במודל של עכברים, תוך שהוא הדגים שנוגדן זה חוסם אמנם את הקולטן CTLA-4 וניתן היה לגרום לצמצום שגשוגם של גידולים במודלים של מלנומה, וסרטן הערמונית וסרטן המעי הגס בעכברים. גישה זו של מודולציה של מערכת החיסון, והגברת פעילותה כנגד שאתות סרטניות שכנעה את החברה הפרמצבטית Medarex להירתם לנושא, על ידי הכנת נוגדן חד-שבטי כנגד CTLA-4, נוגדן שכונה בתחילה MDX-010 שהוכיח עצמו בניסויים בקופים, ובהמשך שונה שם הנוגדן ל-ipilimumab. אכן נמצא שנוגדן זה חסם את CTLA-4 וגרם לכך שיותר קולטני CD28 נקשרו ל-B7, מה שהביא לשפעול של תאי T במספר ניסויים בחיות ולאחר מכן באדם, והוכח כיעיל בסוגי סרטן שונים באדם (ראו תמונה).
הפיזיולוגיה של קולטנים ממברנליים המשמשים לתגובה החיסונית
כך גם עם הבנת הדרך בה פועלים ציטוקינים דוגמת אינטרפרון ו-IL-2 בגירוי מערכת החיסון נגד תאי הסרטן. התחושה עדיין שררה לפיה ציטוקינים אלה עשויים לדרבן את מערכת החיסון, אם כי תוצאות מעשיות הושגו רק ב-5-10% מהמטופלים חולי סרטן מאוד מסוימים כגון מלנומה וקרצינומה של תאי הכליה. בשנת 1992 הופיע ב-Nature מאמר פורץ-דרך של Allison בו דיווח על קולטן הממוקם על פני תאי T והידוע כ-CD28 דרכו עובר לתוך תאים אלה איתות (signal) המגרה אותם לפעילות, ומונע את "תרדמתם" ואת חוסר פעילותם כתאים מרכזיים של מנגנון החיסון. חלפו עוד שנתיים עד למאמרו המכונן של Allison ב-Science משנת 1994, בו תיאר לראשונה את המושג של חסימת קולטנים מסוג CTLA-4 על פני תאי T ועל ידי כך הגברת התהליך החיסוני כנגד תאי סרטן.
CD28 ו-CTLA-4 (הידוע גם כ Cytotoxic T lymphocyte antigen-4 וגם כ-CD152) הם חלבונים טרנס-ממברנליים המופיעים על פני תאי T. אך קיים הבדל מספרי ניכר בין שניהם: כמות קולטני CD28 המופיעים על פני תאי T גדולה בהרבה מזו של קולטני CTLA-4, אך מספר הקולטנים מסוג CTLA-4 עולה בתלילות על פני תאי T שעברו שפעול. בדומה לקולטן CD28 כן גם הקולטן CLTA-4 נקשרים בזיקה גבוהה למולקולות ממשפחת חלבוני B7 הכוללת 10 חלבונים שונים, אשר 2 מתוכם, B7-1 (הידוע כ-CD80) ו-B7-2 (הידוע כ-CD86), רלוונטיים למנגנון שיתואר להלן. שני חלבוני B7 אלה, מופיעים על פני תאים-מציגי-אנטיגן או APC כקיצור ל-antigen presenting cells, הידועים גם כתאים דנדריטים, המציגים לתאי T את קומפלקס MHC או major histocompatibility antigen, הקובע את זהותם האנטיגנית של תאים אלה כאשר קומפלקס MHC נקשר על פני תאי T לקולטן TCR או T cell receptor. אך הקישור של MHC כשלעצמו ל-TCR אינו מספיק לייצר תגובה של תאי T, ובהיעדר אותות מגרים נוספים ייכנסו תאי T לשלב של חוסר פעילות. לכן העזרה לגירוי מערכת האיתות התוך-תאי מגיעה אמנם מחלבוני B7 הנקשרים לקולטניהם על תאי T.
לחלבוני B7 יכולה להיות השפעה משפעלת או מעכבת על תאי T, וזאת בתלות בסוג הקולטנים אליהם הם נקשרים: כאשר B7 נקשר לקולטן CD28 הוא משפעל את תאי T, ואילו כאשר B7 נקשר לקולטני CTLA-4, הוא מעכב את פעילותם של תאי T והופך תאים אלה לאׇנרגיים. אמנם התפקיד של CTLA-4 בהיקשרו ל-B7 הוא תפקיד "חיובי" על מנת למנוע תגובת-יתר של המערכת החיסונית ועל ידי כך למנוע מחלות אוטואימוניות או תופעות אלרגיות. אך לפעולה זו של קולטני CTLA-4 יש גם מחיר בכך שהיא מעכבת את פעילות מערכת החיסון נגד התאים הסרטניים, וממילא מחישה את שגשוגם של התאים הסרטניים.
Ipilimumab הידוע בשם המותג שלו Yervoy, אושר לשימוש על ידי ה- FDA במרץ 2011 לטיפול במלנומה בשלביה המתקדמים, כאשר היא מפושטת ואינה ניתנת להסרה בניתוח. בפברואר 2012 ניתן אישור דומה בקנדה, ובנובמבר אותה שנה הצטרף למאשרים את הטיפול בנוגדן זה לאותה מטרה ה-EU האירופי. Allison זכה בשנת 2015 בפרס Lasker על פיתוח תכשיר זה, ובשנת 2018 אף זכה בפרס נובל ברפואה.
תוצאות ביניים של ניסויים קליניים עם ipilimumab
החל מתחילת העשור הראשון של המאה ה-20 נערכה סדרת ניסויים מקדימים עם נוגדן זה במטופלים עם מלנומה, קרצינומה של הכליה, סרטן הערמונית, קרצינומה של מערכת השתן וסרטן שחלות. תוצאות הביניים, כפי שניתן לשער בשלב מוקדם של לימוד השימוש בתרופה חדשה מבחינת המינונים, נראו מבטיחות אם כי בפירוש לא מרגשות. חברות Medarex וחברת Bristol-Myers Squibb שרכשה את זכויות ייצור התכשיר ושיווקו, על תוצאות של 3 ניסויים קליניים שבחנו את השפעות התרופה בסך של 487 מטופלים עם מלנומה בשלב מתקדם. אחד משלושת הניסויים הללו נכשל ביעד הראשוני שלו, דהיינו לגרום לכיווץ הגידול בלפחות 10 אחוז מבין 155 משתתפיו.
בשנת 2010 הוצגו תוצאות ניסוי אחר בו הושגה הישרדות ממוצעת של 10 חודשים במטופלים עם מלנומה מתקדמת שטופלו בתכשיר, לעומת הישרדות של 4 חודשים בתכשיר ניסיוני אחר (gp100), כאשר ההישרדות למשך שנה אחת הושגה ב-46 אחוז מהמטופלים עם ipilimumab ורק 25 אחוז מהמטופלים עם gp100.
גם לגבי סרטן הערמונית היו הודעות מוקדמות משנת 2009 של חברת Medarex על תוצאות ניסוי phase I/II במטופלים עם סרטן ערמונית גרורתי שלא הגיב לטיפולים הורמונליים. באחדים מהמטופלים דווח על כיווץ דרמטי בממדי השאת. אחת הביקורות על תכשיר זה היא שתופעות הלוואי שלו עלולות להיות משמעותיות והרות-אסון, שהרי מדובר כאן בתרופה שמעודדת אמנם את מערכת החיסון לפגוע בתאים סרטניים, אך אין אפשרות להעריך מה תהיה ההשפעה הזו על יכולתם של תאי T לגרום לתופעות לא רצויות של אוטו-אימוניות כנגד תאי הגוף הבריאים.
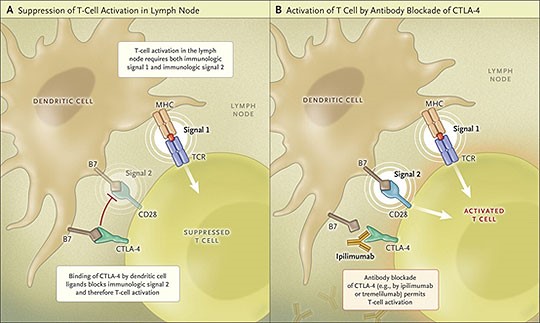
ההתייחסות אל הקולטן CTLA-4 היא כמו למולקולת בקרה אימונולוגית (check point) שתפקידה ל"רסן" את תאי T, כדי שאלה לא יהיו פעילים מדי ובכך עלולים לגרום תגובות אוטו-אימוניות שפוגעות בגוף. אכן, הרעיון של Allison היה לייצר נוגדן חד-שבטי שזכה לשם ipilimumab המגיב ספציפית עם הקולטן CTLA-4 על מנת לנטרל אותו, ולאפשר את האינטראקציה בין CD28 לבין B7 ליצור את signal 2 הדרוש לחבור ל-signal 1 הנוצר על ידי הקשר בין TCR ל-MHC, ובכך לאפשר את שפעול תאי T לפעול את פעולתם בפגיעה בתאים הסרטניים.
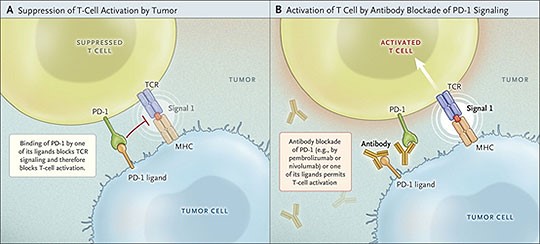
גישה זו של נטרול העכבות של תאי T ושל מערכת החיסון בכללותה, הובילה לאסטרטגיה של "שחרור" פעילותו של קולטן אחר על פני תאי T הידוע כ-PD-1 אוprogrammed cell death-1, קולטן שתאי הסרטן יודעים לנטרל על ידי החלבון המופיע על פניהם והידוע כ-PD-L1 או כ-PD-1 ligand-1 הקושר את PD-1 ועל ידי כך מנטרל אף הוא את תאי T, ומדכא את פעילותם האנטי-סרטנית. גם כאן נוסתה הגישה של נטרול immune checkpoint בדומה לזו שנוסתה עם הכנת נוגדנים כנגד CTLA-4 (ראו תמונה למטה).
הקולטן PD-1 (הידוע גם כ-CD274) מבוטא לא רק על תאי T, אלא גם על תאי pro-B-cells, והוא יכול להיקשר לשני ליגנדים, PD-L1 ו-PD-L2. ההשפעה המעכבת של PD-1 על מערכת החיסון, מושגת על ידי מנגנון כפול: בעת ובעונה אחת הוא מעודד את מותם המתוכנת (אפופטוזיס) של תאי T בקשרי לימפה, אך גם את הפחתת האפופטוזיס בתאי T מווסתים הידועים גם כ-suppressor T cells המדכאים את יכולתם החיסונית של תאי T (על פי Francisco וחב' ב-Immunological Reviews משנת 2010, ו-Fife ו-Pauken ב- Annals of the New York Academy of Sciences משנת 2011).
PD-L1 אופיין ב-Mayo Clinic כמולקולה רגולטורית של התגובה החיסונית, הידועה כ-B7-H1, ששמה הומר בהמשך ל-PD-L1, כיוון שהיא זוהתה כליגנד הנקשר ל-PD-1 (על פי Dong וחב' ב-Nature Med משנת 2002). מספר סוגי תאים סרטניים באדם, מבטאים רמות גבוהות של PD-L1, והחסימה של מולקולה זו הפחיתה את השגשוג של התאים הסרטניים, בנוכחות תאי חיסון. באותו זמן המסקנה הייתה ש-PD-L1 מסייע לתאים הסרטניים להתחמק מהתגובה החיסונית כנגד תאי הסרטן (Curiel וחב' ב-Nature Med משנת 2003). בשנת 2003 נמצא ש-PD-L1 מתבטא על פני תאים מיאלואידיים, כחלבון checkpoint, והוצע שחלבון זה ישמש כיעד פוטנציאלי באימונו-תרפיה של סרטן אנושי (Butte וחב' ב-Mol Immunol משנת 2008).
למעשה ניתן לראות ב-PD-1 בן משפחה של מווסתי פעילות תאי T, אליה שייכים גם הקולטנים CD28 ו- CTLA-4. הקולטן PD-1 מבוטא לא רק על תאי T משופעלים, ועל תאי pro-B, אלא גם על פני מקרופאגים, מה שמצביע על כך שיכולת ההשפעה המווסתת-מעכבת של PD-1 על התגובות החיסוניות רחבה יותר מזו של הקולטן CTLA-4 (על פי Agata וחב' ב-International Immunology משנת 1996). ל-PD-1 יש 2 ליגנדים אליהם הוא נקשר: PD-L1 ו-PD-L2, שהם חברים במשפחת B7 (Freeman וחב' ב-Journal of Experimental Medicine משנת 2000, ו-Latchman וחב' ב-Nature Immunology משנת 2001).
החלבון PD-L1 עובר שדרוג על פני מקרופאגים ותאים דנדריטים בתגובה לגירוי הנוצר כאשר מטפלים בתאים אלה עם ליפופוליסכריד (LPS) או עם פקטור הגירוי של גרנולוציטים ומקרופאגים (GM-CSF). כמו כן, משודרג PD-L1 על פני תאי T ו-B לאחר איתות של הקולטנים של תאי T (TCR), או של תאי B. הביטוי של PD-L2 מצומצם יותר ומופיע על פני תאי דנדריטים ומספר שורות של תאים סרטניים (Yamazaki וחב' ב-Journal of Immunology משנת 2002). ישנן ראיות אחדות המצביעות על התפקיד של PD-1 והליגנדים שלו בעיכוב של התגובה החיסונית. לדוגמה, עכברי knock out שהונדסו גנטית לחסר מוחלט ב-PD-1, פיתחו גלומרולו-נפריטיס וקרדיו-מיופתיה (Nishimura וחב' ב-Science משנת 2001).
בהקשר של חסימת PD-1 על ידי נוגדנים חד-שבטיים המכוונים כנגד חלבון זה, כדי לעודד תגובה חיסונית של תאי T כנגד תאים סרטניים, עורר נושא זה פעילות נמרצת (Tapalian וחב' ב-New England Journal of Medicine משנת 2012). הרבה סוגים של תאי סרטן מבטאים את הליגנד PD-L1, שכאשר הוא נקשר ל-PD-1 הוא מדכא את התגובה החיסונית על ידי מניעת השפעול של תאי T. לכן יצירת נוגדנים המונעים את הקישור בין PD-1 ל-PD-L1 עשויה לעודד את תגובות תאי T כנגד תאי סרטן.
חברת Bristol-Myers Squibb ייצרה את הנוגדן החד שבטי nivolumab (שם מותג Opdivo) המנטרל את PD-1, ובניסוי קליני בהשתתפות 296 חולים עם סרטן תאי כליה, מלנומה או סרטן ריאות מסוג non-small cell הושגו תגובות קליניות מלאות או חלקיות, אם כי בסרטנים של הערמונית ושל הלבלב לא הושגו כל תגובות. תוצאות אלו הביאו לאישור תרופה זו לטיפול במלנומה ממאירה ביפן ביולי 2014, וכן לאישור ה-DFA לאותה מטרה בדצמבר 2014.
נוגדן חד שבטי אחר, pembroliozumab (שם מותג Keytruda) יוצר על ידי חברת Merck, ואף הוא מכוון נגד PD-1. תכשיר זה אושר על ידי ה-FDA בספטמבר 2014 לטיפול במלנומה גרורתית. בניסויים קליניים נרשמה לו הצלחה מדודה, עם תופעות לוואי מועטות יחסית. ב-2 באוקטובר 2015 אושר תכשיר זה על ידי ה-FDA לטיפול ב-NSCLC גרורתי במטופלים שטיפולים אחרים לא הועילו להם. במועד כתיבת מאמר זה נמצאים בצנרת הפיתוח בשלבים מוקדמים תכשירים נוספים המכוונים נגד קולטני PD-1: חברת Cure Tech מפתחת את pidilizumab, חברת Bristol-Myers Squibb מייצרת את הנוגדן BMS936559, ואילו חברת Roche מייצרת את NPDL328OA.
הפיזיולוגיה של PD-L1
PD-L1 אופיין ב-Mayo Clinic כמולקולה רגולטורית של התגובה החיסונית, כיוון שהיא זוהתה כליגנד הנקשר ל-PD-1 (על פי Dong וחב' ב-Nature Med משנת 2002). מספר סוגי תאים סרטניים באדם, מבטאים רמות גבוהות של PD-L1, והחסימה של מולקולה זו הפחיתה את השגשוג של התאים הסרטניים, בנוכחות תאי חיסון. באותו זמן המסקנה הייתה ש-PD-L1 מסייע לתאים הסרטניים להתחמק מהתגובה החיסונית כנגד תאי הסרטן (Curiel וחב' ב-Nature Med משנת 2003). בשנת 2003 נמצא ש-PD-L1 מתבטא על פני תאים מיאלואידיים, כחלבון checkpoint, והוצע שחלבון זה ישמש כיעד פוטנציאלי באימונו-תרפיה של סרטן אנושי (Butte וחב' ב-Mol Immunol משנת 2008).
החלבון PD-L1 באדם מקודד על ידי הגן CD274 (Chemnitz וחב' ב-J Immunol משנת 2004). החלבון PD-L1 מכיל 290 חומצות אמינו הוא בעל משקל מולקולרי של 40,000 דלטון, והוא מוגדר כחלבון טרנס-ממברנלי type 1, שהוא בעל תפקיד מרכזי בדיכוי של מערכת החיסון במהלך אירועים כגון היריון, שתל של allografts, מחלה אוטו-אימונית.
קישור PD-L1 לקולטנו
PD-L1 נקשר לקולטן שלו, PD-1, הנמצא על פני תאי T ו-B משופעלים, ועל פני תאים מייאלואידיים, לגרום למודולציה של שפעול או עיכוב. הזיקה בין PD-L1 ו-PD-1, המוגדרת על ידי קבוע הדיסוסיאציה Kd, היא 770nM. ל- PD-L1 יש גם זיקה משמעותית למולקולת CD80, אך לא למולקולת CD-86 (Said וחב' ב-Nature Med משנת 2010). למולקולה הדומה PD-L2, אין זיקה דומה ל-CD80, אך גם היא יכולה להיקשר לקולטן PD-1, עם Kd של 140nM. נמצא שרמה מוגברת של קולטני PD-1 על פני תאי T משופעלים מסוג CD4, יכולה להביא לקישור קולטנים אלה ל-PD-L1 המבוטאים על פני מונוציטים, ומשרה יצירה של IL-10 על ידי המונוציטים הללו (Sheppard וחב' ב-FEBS let משנת 2004).
הקישור שלPD-L1 לקולטן שלו PD-1 על פני תאי T, משגר איתות המעכב את הייצור של IL-2 המתווך על ידי ה-T cell receptor, ומעכב את שגשוג תאי T. מנגנון האיתות האמור, כרוך בעיכוב של הפוספורילציה של ZPA70, ואת הקשר של האחרון עם CD3ζ (Karwzcz וחב' ב-EMBO Mol Med משנת 2011). הקישור של PD-L1 ל-PD-1 תורם גם ל- down-modulation של TCR במהלך הצגת האנטיגן לתאי T נאיביים, על ידי הגברת הפעילות של E3 ubiquitin ligase CBL-b (Flies ו-Chen ב-J Immunother משנת 2007).
הרגולציה של פעילות PD-L1
כתוצאה מסטימולציה של IFN-γ, PD-L1 מבוטא על פני תאי T, תאי NK, מקרופאגים, תאים מייאלואידים, תאי B, תאי אפיתל, ועל תאי אנדותל וסקולריים (Lee וחב' ב-FEBS let משנת 2006). באזור ה-promoter של הגן של PD-L1 קיים אלמנט תגובה ל-IRF-1, שהוא interferon regulatory factor (Yamazaki וחב' ב- J Immunol משנת 2002). אינטרפרון type I יכול גם להגביר ביטוי PD-L1 על פני הפאטוציטים, מונוציטים ותאי סרטן של עכברים (Loke ו-Allison ב-Proc Natl Acad Sci USA משנת 2003).
PD-L1 מבוטא על פני מקרופאגים. בעכבר, נמצא ששפעול של מקרופאגים (המושרה על ידי type I helper T cells או על ידי שילוב של LPS ואינטרפרון- γ) משדרג מאוד את ביטוי PD-L1 (Bianchini וחב' ב-Sci Immunol משנת 2019). באופן חלופי, מקרופאגים משופעלים על ידי IL-4, מגבירים מעט את הביטוי של PD-L1, אך מגבירים בהרבה את הביטוי של PD-L2. נמצא כמו כן ש-PD-L1 מבוטא באופן קונסטיטוטיבי על פני תאים מונוציטים לא-קלאסיים מסוג Ly6Clo (Gong וחב' ב-J Immunol משנת 2009).
המשמעות הקלינית
- סרטן: נראה ששדרוג הביטוי של PD-L1 יכול לאפשר לגידולים סרטניים להתחמק ממערכת החיסון של המאחסן. אנליזה של 196 דגימות של גידולים סרטניים ממטופלים עם קרצינומה של תאי סרטן כליות, מצאה שהגברת הביטוי של PD-L1 הביא להגברת האגרסיביות של הגידול, והגבירה את הסיכון למוות פי-4.5 (Thompson וחב' ב-Proc Natl Acad Sci USA משנת 2004). מעכבים רבים של PD-L1 נמצאים בשלבי פיתוח כחלק מתרפיה אימונו-אונקולוגית ונותנים תוצאים מבטיחות בניסויים קליניים (Vecheti וחב' ב- J Tech Methods Pathol משנת 2014). דוגמאות לתכשירים מעכבים אלה הם durvalumab, atezolizumab ו-avelumab
- אוטואימוניות: האינטראקציה בין PD-1/PD-L1 משחקת תפקיד באוטו-אימוניות בהתבסס על מספר ראיות. עכברי NOD, המשמשים מודל לאוטו-אימוניות הגורמת לרגישות להתפתחות ספונטנית של סוכרת type 1 ולמחלות אוטו-אימוניות אחרות, נמצאו מפתחים סוכרת מחסימת PD-1 או PD-L1 (אך לא מחסימת PD-L2) (Ansari וחב' ב-J Exp Med משנת 2003)
באדם, נמצא שהביטוי של PD-L1 עבר שינוי בילדים עם SLE. במחקר של peripheral blood mononuclear cells מילדים בריאים, נמצא ש- myeloid dendritic cells לא בשלים וכן מונוציטים מבטאים רק מעט PD-L1 בבידוד ראשוני, אך הביטוי שלהם עולה ספונטנית אחרי 24 שעות. לעומת זאת, גם תאים דנדריטים בשלים וכן מונוציטים של מטופלים עם SLE פעילה, נכשלו בהגברת הביטוי של PD-L1 במהלך 5 ימים לאחר בידודם, ומבטאים את החלבון הזה רק בעת רמיסיה של המחלה (Mozaffarian וחב' ב-Rheumatology משנת 2008).
במיקרו-סביבה ההיפוקסית של הגידול הסרטני מוגבר הביטוי של PD-L1 על פני Myeloid-derived suppressor cells (להלן MDSC), וניתן להשתמש בשינוי רמת PD-L1 להערכת היעילות של תרפיה היפר-אוקסית (Qian וחב' ב- Am J Cancer Res משנת 2019). כמו כן, Tumor-associated macrophages cells (להלן TAMs) המבטאים בעודף PD-L1 על פניהם, יכולים לדכא את התפקוד של תאי T ציטוטוקסיים. השערה נוספת עלתה, לפיה שלושת הקולטנים של תאי TAM, Tyro3, Axl ו-Mertk, יכולים להגביר את הביטוי של PD-L1 על פני שורת תאי סרטן שד (Kasikara וחב' ב- Mol Cancer Res משנת 2017). יתרה מכך, IFN-γ מסוגל להגביר את רמת PD-L1 המבוטא על פני exosomes המופרשים על ידי תאי מלנומה, והכרוך בקידום ההימלטות מתאי החיסון, וסיוע לתהליך הסרטני.
מחקרים אישרו שרמות PD-L1 המבוטאות על פני exosomes, אך לא PD-L1 מסיס, נמצאים במתאם עם התקדמות התהליך הסרטני של קרצינומת תאי קשקש של הראש והצוואר (להלן HNSCC) (Theodoraki וחב' ב-Clin Cancer Res משנת 2018). תוצאות מחקרים בשיטות flow cytometry ואימונו-פלואורסצנציה מצביעות על כך ש-PD-L1 נמצא לא רק על פני vesicles אלא גם בתוכם (Poggio וחב' ב-Cell משנת 2019).
מחקרים עדכניים הראו שביטוי גבוה של PD-L1 במטופלות עם סרטן שד (triple negative), כרוך בפרוגנוזה גרועה (Pan וחב' ב- Zhonghua Bing Li Xue Za Zhi משנת 2017). נמצא גם שתאי סרטן הם בעלי פוטנציאל לווסת את התהליך המולקולרי של הידרוליזה של PD-L1 בתוך הליזוזום, מה שמביא לעמידות בפני תגובה חיסונית. יתרה מכך, נמצא שאינטרפרון- γ המופרש על ידי תאי דלקת כמו מקרופאגים ותאי NK, יכול להגביר ביטוי של PD-L1 בתאי סרטן (Abiko וחב' ב-Br J Cancer משנת 2015, ו-Garcia-Diaz וחב' ב-Cell Rep משנת 2017). עם ביטוי מוגבר של PD-L1, תאי סרטן יכולים לתווך ביצירת עמידות אדפטיבית ל- IFN-γ המופרש על ידי לימפוציטים T ציטוטוקסיים, מה שמגביר את האגרסיביות וההחמרה של התהליך הסרטני. בסרטן הקיבה, מספר דיווחים הראו שהביטוי של PD-L1 יכול להימצא ב-25-65% מהתאים הסרטניים (Harada וחב' ב- Gastric Cancer משנת 2018). עוד נמצא שהסננת תאי חיסון למיקרו-סביבה של הגידול הסרטני, יכולה להיות כרוכה עם הנוכחות של PD-L1 על שטח פני התאים (Ruffell ו-Coussens ב-Cancer Cell משנת 2015).
במיקרו-סביבה ההיפוקסית של הגידול הסרטני מוגבר הביטוי של PD-L1 על פני Myeloid-derived suppressor cells (להלן MDSC), וניתן להשתמש בשינוי רמת PD-L1 להערכת היעילות של תרפיה היפר-אוקסית (Qian וחב' ב- Am J Cancer Res משנת 2019). כמו כן, Tumor-associated macrophages cells (להלן TAMs) המבטאים בעודף PD-L1 על פניהם, יכולים לדכא את התפקוד של תאי T ציטוטוקסיים. השערה נוספת עלתה, לפיה שלושת הקולטנים של תאי TAM, Tyro3, Axl ו- Mertk, יכולים להגביר את הביטוי של PD-L1 על פני שורת תאי סרטן שד (Kasikara וחב' ב- Mol Cancer Res משנת 2017). יתרה מכך, IFN-γ מסוגל להגביר את רמת PD-L1 המבוטא על פני exosomes המופרשים על ידי תאי מלנומה, והכרוך בקידום ההימלטות מתאי החיסון, וסיוע לתהליך הסרטני.
אינטרפרטציה של תוצאות הבדיקה
בדיקה זו מומלצת בעיקר לאלה עם מלנומה, גליובלסטומה, סרטן השד, סרטן כליות, סרטן שלפוחית השתן, לימפומה ע"ש הודג'קין, וסרטן מסוג NSCLC. מטרת הבדיקה היא לקבוע את רמת PD-L1 על פני תאים סרטניים אלה. אם רמת PD-L1 מתקבלת גבוהה, הרי שהמטופל עשוי להפיק תועלת מאימונו-תרפיה. היפוכו של דבר, אם מתקבלת תוצאה של רמת PD-L1 נמוכה על פני התאים הסרטניים, היעילות של אימונו-תרפיה עלולה להיות מוגבלת.
הוראות לביצוע הבדיקה
הבדיקה שהיא חצי כמותית מתבצעת בצביעה אימונו-היסטו-כימית. לאחר ביצוע של הגידול הסרטני, מכינים "בלוק" על ידי קיבוע בפורמלין ו-embedding בפרפין, וזכוכית נושא אחת בה החומר שנלקח בביופסיה נצבע על ידי hematoxylin & eosin . פרוסות הרקמה לצורך הצביעה והמיקרוסקופיה 4 מיקרון. הדגימה צריכה להישלח למעבדה בטמפרטורת החדר (מועדף), או בקירור. יש לפסול דגימות הנשלחות מוקפאות/רטובות, או כמשטחים ציטולוגיים, או כרקמות שלא עברו קיבוע בפורמלין, או embedding בפרפין.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק