אבחון מעקב וטיפול טרומבוציטופניה אלואימונית - נייר עמדה - Fetal and neonatal alloimmune thrombocytopenia (FNAIT)
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
|
| |
|---|---|
| קווים מנחים לאבחון מעקב וטיפול טרומבוציטופניה אלואימונית - Fetal and Neonatal Alloimmune thrombocytopenia (FNAIT) | |
| תחום | ??? |
| |
| האיגוד המפרסם |
|
| קישור | באתר הר"י |
| תאריך פרסום | פברואר 2023 |
| יוצר הערך |
|
| ניירות עמדה מתפרסמים ככלי עזר לרופא/ה ואינם באים במקום שיקול דעתו/ה בכל מצב נתון. כל הכתוב בלשון זכר מתייחס לשני המגדרים. | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – טרומבוציטופניה אלואימונית
רקע
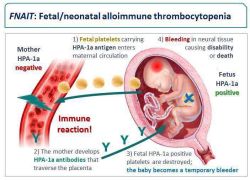
Fetal and neonatal alloimmune thrombocytopenia (FNAIT( מהווה את הסיבה השכיחה ביותר לטרומבוציטופניה בעובר וביילוד עם שיעור היארעות משוער של 1 ל- 1000. הטרומבוציטופניה נגרמת על ידי נוגדנים אימהיים כנגד אנטיגנים שעל פני טסיות העובר )HPAs Human platelets antigens(, בעקבות ריגוש אימהי לרוב, לאחר חשיפה לאנטיגנים ממקור אבהי שעל פני הטסיות של העובר. נוגדנים כנגד HPA-1a אחראים לכ- 80% מהמקרים של FNAIT באוכלוסייה הלבנה. הסיבוך הקשה העיקרי של FNAIT הינו דימום תוך מוחי בעובר או ביילוד, שעלול להוביל לתמותה או תחלואה נוירולוגית ארוכת טווח. 80% ממקרי הדמם התוך מוחי מתרחשים במהלך ההיריון ולפני הלידה. לאחר הלידה, הסיכון לדמם הינו מירבי ב- 96 השעות הראשונות לחיים. ללא טיפול, הטרומבוציטופניה של היילוד חולפת תוך 1-5 שבועות אחרי הלידה. המחלה מאובחנת לרוב בעקבות לידה של יילוד עם טרומבוציטופניה שנתגלתה בספירת דם מקרית, או בעקבות ביטויי דמם כגון: פטכיות עוריות או דימום מוחי. הטרומבוציטופניה תישנה ואף עלולה להחמיר במקרה של אי התאמה אנטיגנית בין האם לעובר בהיריונות הבאים; מכאן, חשיבותו של הבירור והאבחון המעבדתי. 1. האבחון המעבדתי ■ באילו מקרים לבצע בירור ל- FNAIT? יש לבדוק את האם והאב במקרים הבאים: א. יילוד עם טרומבוציטופניה מתחת ל-100K/ul בלידה או עד שבעה ימים לאחריה בהיעדר אטיולוגיה אחרת. ב. ליילוד/עובר עם דמם מוחי ללא אטיולוגיה ברורה אחרת. במידה ונלקחה ליילוד/לעובר ספירת דם שהצביעה על רמת טסיות תקינה בבדיקות חוזרות אין צורך בבירור. ג. אחות לאם ליילוד עם FNAIT . ד. בנוכחות אבחנה של ITP לאם - יש לשקול גם בירור ל-FNAIT במידה וליילוד סימני דמם ו/או טרומבוציטופניה קשה )מתחת ל- 50K/ul ). ה. מה לבדוק? יש לשלוח דגימת דם של ההורים והיילוד )אם ניתן( למעבדה מוסמכת בה ייבדקו: א. בדם האימהי ייבדקו נוגדנים כנגד HPA 1,2,3,4,5,9,15. בנוסף, ניתן לבדוק נוגדנים כנגד GPIV וכנגד אנטיגנים נדירים על פני הטסיות )ע”י MAIPA(. שיעור הגילוי של נוגדנים אימהיים עלול לרדת אחרי 6 שבועות מהלידה. ב. הצלבה בין טסיות טריות מהאב לבין סרום האם )לאיתור נוגדנים, כולל נדירים ומשפחתיים(. ג. מיפוי גנוטיפי של טסיות ההורים והיילוד )באם ניתן( לאנטיגנים 1,2,3,4,5,9,15 HPA. ד. המלצות למעקב בהיריון הבא ע״פ תוצאות בירור א. במקרה שנמצאה אי התאמה אנטיגנית בין ההורים )1,2,3,4,5,9,15 HPA( ונמצאו נוגדנים כנגד האנטיגן/אנטיגנים אלו האבחנה של FNAIT היא וודאית. ההמלצות במקרה זה הן: 1. במידה שהאב הומוזיגוט לשינוי האנטיגני, יש להמליץ על טיפול בכל ההיריונות הבאים. 2. במידה שהאב הטרוזיגוט לשינוי האנטיגני, או לא זמין לבדיקה, או לא ידוע - מומלץ, אבחון גנטי לעובר ממי שפיר או מדם אימהי Non invasive prenatal testing (NIPT) )באם קיים( והמשך ניהול המקרה בהתאם לממצאים: ■ אי התאמה בין טסיות העובר לטסיות האם - מומלץ טיפול בהיריון ■ התאמה בין טסיות העובר לטסיות האם - מומלץ לעקוב בדם האם אחרי התפתחות נוגדנים בשבוע 16 )רמת הבסיס( ובשבוע 24 בכדי לשלול תוצאה false negative באבחון העובר ■ במידה, שלא ניתן לקבוע את גנוטיפ העובר יש לטפל באבחנה משוערת של FNAIT 3. במקרים שהאב הטרוזיגוט ניתן להציע להורים לשקול אבחון גנטי טרום השרשתי )PGD), והחזרת עובר שהינו זהה לאם מבחינת האנטיגן שלגביו ישנה אי התאמה. ב. במקרה שנמצאה אי התאמה בין ההורים באנטיגן אחד או יותר מהאנטיגנים הנבדקים (1,2,3,4,5,9,15 HPA( ללא נוכחות נוגדנים - האבחנה של FNAIT איננה חד משמעית. יש לבצע מעקב נוגדנים באם במהלך ההיריון הבא בשבועות 16, 22 ו- 30. 1. במידה שנמצאו נוגדנים - אבחנה של FNAIT המצריכה טיפול בהיריון 2. במידה, שלא נמצאו נוגדנים וקיימת אי התאמה בין האם ליילוד - מומלץ לבדוק ליילוד ספירת טסיות, ולחזור על בדיקת נוגדנים לאם 2-6 שבועות לאחר הלידה וכן בשבוע 16 להיריון הבא 3. במקרה של אי התאמה ב- HPA1a כשגנוטיפ האם HPA1bb, מומלץ, לבדוק פנוטיפ 01:01*HLADRB3 באם. היעדר האנטיגן 01:01*DRB3 קשור לסיכוי נמוך מאוד ליצירת נוגדנים באם עם פנוטיפ HPA1bb שאין לה היסטוריה של FNAIT (Negative Predictive Value 96%-100%) ג. במקרה שלא נמצאה אי התאמה אנטיגנית (1,2,3,4,5,9,15 HPA( וללא נוכחות נוגדנים - האבחנה של FNAIT נשללה בסבירות גבוהה. עם זאת, בשל האפשרות של אנטיגנים נדירים שלא נבדקים ובמיוחד, אם יש היסטוריה של טרומבוציטופניה קשה ו/או דימום מוחי, יש לשקול לבצע מעקב נוגדנים באם בשבוע 22 ובשבוע 30. 1. במידה, שנמצאו נוגדנים - אבחנה של FNAIT המצריכה טיפול במהלך ההיריון. 2. במידה, שלא נמצאו נוגדנים וקיימת אי התאמה בין האם ליילוד - מומלץ, לחזור על בדיקת נוגדנים 2-6 שבועות לאחר הלידה וכן, בשבוע 16 להיריון הבא. 3. Antenatal recommendations .2 המלצות לטיפול בהיריון עם חשד FNAIT-ל הסיכון בהישנות של FNAIT בהיריונות הבאים במקרה של אי התאמה אנטיגנית הינו סביב 80%. המלצות להערכת סיכון ולטיפול: א. נשים עם היריון בסיכון ל- FNAIT צריכות להיות מטופלות במרכז עם מומחי אם-עובר, ניאונטולוגים והמטולוגים ילדים. ב. לצורך הערכת הסיכון בהיריון הבא במקרה שהאב הטרוזיגוט/לא ידוע/לא זמין מומלץ לבצע אבחון HPA )גנוטיפ( של העובר. השיטה המומלצת היא דיקור מי שפיר ולא סיסי שלייה, העלול להגביר את הריגוש האימהי יותר מאשר דיקור. ג. לגבי נשים ללא עבר של FNAIT שזוהו כבעלות פנוטיפ HPA1bb בסקר שבוצע על רקע סיפור משפחתי, כ-10% מהן תפתחנה נוגדנים בהיריון עם עובר בעל אנטיגן HPA1a . לכן, סקר נוגדנים מומלץ בהיריונות הבאים בשבועות 16, 22 ו- 30. ד. לבעלות הפנוטיפ HPA1bb אשר חסרות את האנטיגן )01:01( HLA DRB3 סיכון נמוך במיוחד ליצירת הנוגדנים הנרכשים כנגד HPA1a במהלך היריון עם אי התאמה. עם זאת, גם במקרה זה של סיכון מופחת מומלץ סקר נוגדנים בהיריונות הבאים בשבועות 16, 22 ו- 30. ה. טיפול בהיריון למניעת טרומבוציטופניה עוברית הטיפול מתבסס על מתן IVIG לאם. למרות היעדר מחקרים לקביעת המינון, מועד התחלת הטיפול ומשך הטיפול ב- IVIG, הניסיון בטיפול מונע זה לא הראה פגיעה בהתפתחות העובר או עלייה בסיכון לסיבוכי היריון. עם זאת, לטיפול זה תופעות לוואי אימהיות מוכרות כולל: כאבי ראש, עלייה בתפקודי כליות ובאנזימי כבד, פריחה, ובמקרים נדירים אספטיק מנינגיטיס וטרומבוזיס. יעילות הטיפול ב-IVIG להעלאת רמת הטסיות בעובר למעל 50K/ul הינה 85%-90%. במקרים מסוימים, ניתן לשלב גם טיפול בסטרואידים .(Prednisone) ההמלצות לגבי טיפול ב-IVIG הן: 1. במידה שבהיריון קודם העובר/יילוד סבל מדמם מוחי כתוצאה מ-FNAIT וקיימת אי התאמה באנטיגנים גם בהיריון נוכחי - מקרים אלו מוגדרים כבעלי סיכון גבוה עקב סיכון להישנות של דימום מוחי. ההחלטה על הניהול וטיפול במקרים אלו צריכה להתקבל על ידי צוות מולטי-דיסציפלינרי, שיכלול מומחה אם-עובר והמטולוג. ככלל, טיפול מונע ב- IVIG במקרים אלו יותחל בשבוע 12-16 להיריון במינון של 1-2 גרם/ק”ג/שבוע, ובהמשך ניתן לשקול תוספת של פרדניזון החל משבוע 24-28 במינון של 0.5-1 מ”ג/ק”ג/יום. הטיפול ניתן עד הלידה. את המינון השבועי של IVIG ניתן לחלק לשתי מנות. 2. במידה שבהיריון קודם היילוד סבל מטרומבוציטופניה כתוצאה מ-FNAIT אך לא סבל מדמם מוחי, וקיימת אי התאמה אנטיגנית גם בהיריון נוכחי - תחילת טיפול מונע ב- IVIG בשבוע 20-24 להיריון במינון של 1 גרם/ק”ג/ שבוע עד הלידה. ניתן לחלק את המינון השבועי לשתי מנות. 3. במקביל לטיפול ב- IVIG יש לבצע מעקב סונוגרפי לעובר ביחידת אולטרסאונד מיילדותי/ אם-עובר אחת ל- 4 שבועות עד סוף ההיריון כדי לשלול דימום מוחי. 4. במידה ולא מתאפשרת התחלת טיפול 1-IVIG במועד שהומלץ לעיל, יש להתחילו בכל מועד אפשרי במהלך ההיריון. Recommendations At Delivery .3 למרות שאין מחקרים מבוקרים אשר בחנו את אופן הלידה המומלץ, ידוע ממחקרים פרוספקטיביים כי קיים סיכון Intracranial hemorrhage מוגבר לדימום תוך מוחי (ICH) בלידה לדנית אם רמת הטסיות של העובר/יילוד מתחת ל- 50K/ul. מכאן ההמלצות לצורת הלידה: א. במידה שהאישה מעוניינת בלידה לדנית יש לבצע דיגום דם עוברי )קורדוצנטזיס( בחדר ניתוח ב-double set up בשבוע 37-38 להיריון )או מוקדם יותר אם היו לידות מוקדמות בעבר(. פעולה זו תתבצע רק במרכזים עם ניסיון בפרוצדורות תוך רחמיות. אם רמת הטסיות של העובר בבדיקה מעל 50K/ul ניתן לאפשר לידה לדנית. אם רמת הטסיות מתחת ל- 50K/ul יש ליילד בניתוח קיסרי. לציין, כי אם רמת הטסיות מעל 50K/ul אין הכרח ביילוד מיידי וניתן לאפשר התפתחות לידה ספונטנית בהמשך, כתלות ברמת הטסיות של העובר ובנתונים מיילדותיים אחרים. במידה והוחלט על המשך ההיריון והמתנה להתפתחות לידה ספונטנית, יש להמשיך טיפול ב- IVIG עד לפחות שבוע טרם הלידה. ב. אם אין אפשרות לבצע דיגום דם עוברי או שהאישה אינה מעוניינת לעבור פרוצדורה זו מומלץ ליילד בניתוח קיסרי מתוכנן בשבוע 37-38 להיריון. ג. במידה והתפתחה לידה ספונטנית טרם ביצוע דיגום דם עוברי וספירת טסיות העובר לא ידועה, מומלץ להימנע מלידה לדנית וליילד בניתוח קיסרי. ד. בכל מקרה בו ספירת טסיות העובר לא ידועה יש להימנע מיילוד מכשירני. ה. יש לדאוג לביצוע ספירת טסיות היילוד מדם חבל הטבור מיד עם הלידה. ו. יש ליידע את רופאי הילדים ובנק הדם טרם הלידה המתוכננת לצורך הכנת טסיות מתאימות )ראה סעיף 4א(. Postnatal recommendations .4 ז. המלצות לטיפול ביילוד עם חשד FNAIT-ל בהיריון עם חשד ל- FNAIT יש לזכור שלעתים ספירת הטסיות מהדם הטבורי או מהיילוד מיד לאחר הלידה תקינה ויורדת כעבור מספר שעות. לכן, יש לחזור על ספירת הדם מספר שעות לאחר הלידה, גם אם הטסיות תקינות קודם לכן, ולעקוב אחר התפתחות סימני דמם. ספירת הטסיות הנמוכה ביותר צפויה בתוך 48 שעות מהלידה. הטרומבוציטופניה צפויה לחלוף בתום 1-5 שבועות. יש להתייעץ עם המטולוג ילדים לניהול המקרה. בחשד קליני ל-FNAIT יש להתחיל טיפול לפי ההמלצות מבלי להמתין לאישור מעבדתי של האבחנה. הגישה הטיפולית המומלצת: א. עירוי טסיות - הטיפול המיידי במקרה של דמם מסכן חיים. עדיפות ראשונה לטסיות מותאמות ב-HPA לאמא )מהאם או מתורם(. במידה שלא זמינות יש להשתמש בטסיות מתורמים אקראיים )שהפנוטיפ שלהם ל-HPA לא ידוע(. טסיות מהאם צריכות להיות שטופות לפני מתן ומוקרנות. 1. במקרה של דמם מסכן חיים יש לשמור על רמת טסיות ראשונית מעל 100K/ul ולאחר מכן מעל 50K/ul לפחות למשך 7 ימים 2. בהיעדר דמם מסכן חיים מומלץ לתת עירוי מניעתי רק אם רמת הטסיות יורדת מתחת ל-30K/ul 3. בפג או במצבים אחרים בסיכון לדמם מסכן חיים יש לשקול מתן טסיות מניעתי לרמה של מעל 50K/ul לפחות למשך 7 ימים )או יותר, בהתאם לייעוץ המטולוגי/ניאונטולוגי משותף( ב. טיפול ב- IVIG צריך להישקל רק במצב של דמם מסכן חיים או ספירת טסיות נמוכה מ- 30K/ul כשאין טסיות זמינות לעירוי. 1. אין להחליף טיפול בעירוי טסיות בטיפול ב- IVIG 2. ספירת הטסיות לאחר טיפול ב- IVIG צפויה להשתפר רק תוך 24-48 שעות ממועד הטיפול 3. תופעות לוואי צפויות כוללות המוליזה ביילודים עם סוג דם שאינו O ונויטרופניה ג. סטרואידים - התועלת בהוספת סטרואידים לא ברורה ולכן לא מומלצת. ד. ביילוד עם חשד ל- FNAIT יש לבצע אולטרסאונד מח לשלילת דימום מוחי. אם יש סימנים קליניים המחשידים לדימום מוחי, יש לטפל בעירוי טסיות גם בטרם אישור הדמייתי. ה. יש להמשיך ולבדוק רמת טסיות עד שמגיעה לערך תקין ללא השפעת טיפול. ו. בכל מקרה של יילוד עם טרומבוציטופניה חולפת ללא הסבר אחר למצב, יש להפנות את ההורים לבירור FNAIT על פי ההנחיות בסעיף 1. יש לעדכן את הרשומה הרפואית של האם בהתאם. ז. במקרה של יילוד עם טרומבוציטופניה עם אבחנה של FNAIT או חשד ל- FNAIT, יש לציין זאת במכתב שחרור ולהפנות את האם להמשך מעקב ובירור מיילדותי לפני ההיריון הבא. יש לעדכן את הרשומה הרפואית של האם בהתאם.
בדיקת בירור FNAIT במעבדה לאימונולוגיה של טסיות בדיקת בירור ל- )Fetal/Neonatal alloimmune thrombocytopenia )FNAI - מבוצעת במעבדה לאימונולוגיה של טסיות במרכז הרפואי רמב”ם בחיפה. המעבדה היא מעבדת הרפרנס הארצית ומבוצע בה הבירור והמעקב המלא הנדרש. הבדיקה כוללת: אפיון ובדיקת נוגדנים בפלסמת האם כנגד טסיות האב וקביעת גנוטיפ לאנטיגנים של הטסיות. 1. התחייבויות: לצורך ביצוע הבדיקה יש צורך בהתחייבויות כלהלן: בדיקה ראשונה למשפחה: קוד שירות קופת חולים כללית )K0098 התחייבות אחת( או שתי התחייבויות בקוד 86905 לאב ולאם משאר הקופות בדיקת מעקב: התחייבות בקוד 86905 על שם האם בלבד )ודגימות משני ההורים כמפורט לעיל( 2. דגימות: לצורך ביצוע הבדיקות )פעם ראשונה או מעקב( נדרשות דגימות משני ההורים במבחנות כלהלן: 4 מבחנות EDTA בנפח 9 מ”ל או 6 מבחנות בנפח 6 מ”ל מהאב 3 מבחנות EDTA בנפח 9 מ”ל או 4 מבחנות בנפח 6 מ”ל מהאם אין להשתמש במבחנות EDTA בנפח 3 מ”ל! 3. בדיקות נלוות: בדיקת גנוטיפ עובר ממי שפיר: 10-15 מ”ל מי שפיר והתחייבות בקוד J3001 על שם האם כל בדיקת גנוטיפ נוספת מלבד בדיקת ההורים: מבחנת ספירה, והתחייבות בקוד J3001 על המבחנות להגיע למעבדה לאימונולוגיה של טסיות בבנק הדם בביה”ח רמב”ם )מגדל סמי עופר, קומה ראשונה( מלוות במכתב הפנייה בתוך 48 שעות לכל היותר, ממועד לקיחת הדגימות. על הדגימות להישמר בטמפרטורת החדר, אין לקרר את הדגימות ! ניתן להפנות את המשפחה )הורים, לא ילדים( ללקיחת הדגימות במעבדתנו, בבנק הדם בבית חולים רמב”ם בימים א’-ד’ בין השעות 9:00-15:00 לבירורים ניתן לפנות לטל: 04-7773488 או במייל l_bonstein@rmc.gov.il נשמח לעמוד לרשותכם בברכה, ד”ר לילך בונשטיין מנהלת המעבדה מקורות 1. Kamphuis MM and Oepkes D. Fetal and neonatal alloimmune thrombocytopenia: prenatal interventions. Prenatal Diagnosis )2011(;31:712-719. 2. Winkelhorst D et al. Antenatal management in fetal and neonatal alloimmune thrombocytopenia: a systematic review. Blood )2017(;129)11(:1538-1547. 3. Winkelhorst D and Oepkes D. Fetal and neonatal alloimmune thrombocytopenia. Best Practice & Research Clinical Obstetrics and Gynecology )2019(;58:15-27. 4. Peterson JA, McFarland JG, Curtis BR, Aster RH. Neonatal alloimmune thrombocytopenia: pathogenesis, diagnosis and management. Br J Haematol )2013(; 161)1(: 3-14. 5. Provan D et al. Updated international consensus report on the investigation and management of primary immune thrombocytopenia. Blood Adv. )2019(;3)22(: 3781-3817. 6. Regan F, Lees CC, Jones B, Nicolaides KH, Wimalasundera RC, Mijovic A, on behalf of the Royal College of Obstetricians and Gynaecologists. Prenatal Management of Pregnancies at Risk of Fetal Neonatal Alloimmune Thrombocytopenia )FNAIT(. BJOG )2019(;126:e173-185. 7. Baker JM,Shehata N ,Bussel J, Murphy MF, Greinacher A, Bakchoul T, Massey E, Lieberman L, Landry D, Tanael S, Arnold DM, Baidya S, Bertrand G, Kjaer M, Kaplan C, Kjeldsen-Kragh J, Oepkes D, Savoia H, Ryan G, Hume H, on behalf of the International Collaboration for Transfusion Medicine Guidelines (ICTMG). Postnatal intervention for the treatment of FNAIT: a systematic Review. Journal of Perinatology )2019( Oct;39)10(:1329-1339. 8. Wabnitza H, Khana R, Lazarusa AH. The use of IVIg in fetal and neonatal alloimmune thrombocytopenia - Principles and mechanisms. Transfusion and Apheresis Science )2020(59. 9. Kjeldsen-Kragh J, Fergusson DA, Kjaer M, Lieberman L, Greinacher A, Murphy MF, Bussel J, Bakchoul T, Corke S, Bertrand G, Oepkes D, Baker JM, Hume H, Massey E, Kaplan C, Arnold DM, Baidya S, Ryan G, Savoia HF, Landry D, Shehata N. Fetal/neonatal alloimmune thrombocytopenia: a systematic review of impact of HLA-DRB3*01:01 on fetal/neonatal outcome. Blood advances )2020( 4)14(. 10. Wienzek-Lischka S, Sawazki A, Ehrhardt H, Sachs UJ, Axt-Fliedner R, Bein G. Non-invasive risk-assessment and bleeding prophylaxis with IVIG in pregnant women with a history of fetal and neonatal alloimmune thrombocytopenia: management to minimize adverse events. Archives of Gynecology and Obstetrics )2020( 302:355-363. 11. Petermann R, Bakchoul T, Curtis BR, Mullier F, Miyata S, Arnold DM. For the Subcommittee on Platelet Immunology Investigations for fetal and neonatal alloimmune thrombocytopenia: communication from the SSC of the ISTH. Journal of Thrombosis and Haemostasis )2018( 16: 2526-2529. 12. Lieberman L, Greinacher A, Murphy MF, Bussel J, Bakchoul T, Corke S, Kjaer M, Kjeldsen-Kragh J, Bertrand G,Oepkes D,Baker JM, Hume H, Massey E, Kaplan C, Arnold DM, Baidya S, Ryan G, Savoia H, Landry D, Shehata N, for the International Collaboration for Transfusion Medicine Guidelines (ICTMG). Fetal and neonatal alloimmune thrombocytopenia: recommendations for evidence-based practice, an international approach. Br J Haematol, )2019( 185, 549-562. 13. Winkelhorst D, Oostweegel M, Porcelijn L, Middelburg RA, Zwaginga JJ, Oepkes D, van der Bom JG, de Haas M, Lopriore E. Treatment and outcomes of fetal/neonatal alloimmune thrombocytopenia: a nationwide cohort study in newly detected cases. Br J Haematol )2019( 184)6(:1026-1029.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק 