מחלת קרוהן בחומרה בינונית-קשה - טיפול באופדסיטיניב - Crohn's disease in moderate-severe severity - treatment with Upadacitinib
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – מחלות מעי דלקתיות
מחלת קרוהן היא מחלה כרונית ופרוגרסיביות של צינור העיכול, המתבטאת באנשים צעירים ושכיחותה עולה. מחלת קרוהן מתפתחות כתוצאה ממשלב גורמים סביבתיים, תזונתיים ואחרים, המביאים לפגיעה ראשונית בשלמות רירית המעי.
באנשים בעלי רקע גנטי מועד, מתפתחת תגובה לא מאוזנת של מערכת החיסון אשר מביאה לפעילות דלקתית מוגזמת וממושכת. המחלה גורמת לתסמינים הן במערכת העיכול והן במערכות נלוות וגורמת לנזק מבני לצינור העיכול, למגבלה תפקודית ולירידה משמעותית באיכות החיים[1][2]. גם בעידן הנוכחי, יותר משליש מהמטופלים סובלים מסיבוכי המחלה הכוללים היצרות במעי, התנקבות והתפתחות אבצס תוך בטני, היווצרות פיסטולות בין לולאות מעי וצורך בטיפול ניתוחי. גם לאחר ניתוח, למחלה נטייה להישנות באזור ההשקה הניתוחית, מה שמצריך המשך טיפול תרופתי למניעה וכן מעלה סיכון לניתוח חוזר[3][4].
לצורך שליטה על תסמיני הדלקת הכרונית ולשם מניעת הנזק המבני, המטופלים נדרשים לטיפול תרופתי הניתן באופן קבוע לשם ויסות מערכת החיסון. התפתחה ההבנה שהתערבות תרופתית יעילה ומוקדמת בחולים עם מאפייני מחלה קשים מפחיתה את הסיכון להיווצרות נזק מבני ומשפרת את איכות חיי המטופל.
מגוון הטיפולים התרופתיים הקיימים למחלות מעי דלקתיות התרחב, בהם תכשירים ביולוגיים הפועלים במגוון מנגנוני פעולה ומולקולות קטנות. עם התקדמות הטיפולים התרופתיים, היעדים הטיפוליים והמחקריים כוללים הפוגה מתסמינים ללא צורך בסטרואידים וריפוי רירית המעי. הוכח כי ריפוי רירית המעי מביא להפחתה בשיעור ההתלקחויות ומפחית שיעור אשפוזים וניתוחים[5].
אפשרויות תרופתיות לטיפול במחלת קרוהן בחומרה בינונית-קשה
כאשר הטיפול הקונבנציונלי אינו יעיל או גורם לתופעות לואי ובחולים עם מאפייני מחלה המנבאים מהלך מחלה קשה, יש צורך במתן תכשיר מקבוצת התכשירים הביולוגיים/ מולקולות קטנות. התכשירים הביולוגיים למחלות מעי דלקתיות כוללים נוגדי TNF, נוגדי אינטגרינים ומעכבי ציטוקינים 12/23IL[3][6]. לסל הצטרף תכשיר ביולוגי, risankizumab מעכב 1L23[7][8].
התכשיר המתקדם הוותיק מכולם הוא נוגד ה-TNF. נוגדי ה־TNF הם יעילים ובטוחים להשראת הפוגה ולשמירה על הפוגה במחלות מעי דלקתיות[9]. עם זאת, באחוז ניכר מהמטופלים, קיים אובדן תגובה[10]. גם בתכשירים החדשים יותר, אשר אינם אימונוגניים, ניכרת תופעה של אובדן תגובה לתכשיר המביאה לצורך בהחלפת הטיפול.
Upadacitinib למחלת קרוהן בחומרה בינונית-קשה
קיימת התעניינות בפיתוח של מולקולות קטנות. למולקולות הקטנות יתרונות רבים: יש להן זמן מחצית חיים קצר יותר, ההתנהגות שלהן בגוף והתייחסות הגוף אליהן צפויה יותר, הן לא מעוררות תגובה אימונוגנית, והציפייה היא שיתרונות אלה יאפשרו יעילות גם בחולים המנוסים בתכשירים ביולוגיים קודמים ויאפשרו שימוש ממושך לאורך זמן, ללא אובדן תגובה[11].
אחד ממנגנוני הפעולה בקבוצת המולקולות הקטנות הוא עיכוב של חלבוני JAK. חלבוני JAK הם חלבונים מרכזיים המעורבים בתיווך איתות ציטוקיני תוך תאי. התכשירים בקבוצת נוגדי ה־JAK נבדלים ביניהם בחלבון ה־JAK שהם מעכבים ובמידת הסלקטיביות שלהם בעיכוב החלבון[12]. Upadacitinib הוא מעכב סלקטיבי של 1-JAK1\3 ,JAK ובכך יש לו תפקיד בוויסות פעילות של מגוון ציטוקינים המעוררים את התהליך הדלקתי במחלת המעי הדלקתית.
בקוליטיס כיבית, מאושרות לשימוש גם שלוש מולקולות קטנות: נוגד JAK לא סלקטיבי (Tofacitinib), מודולטור של הרצפטור ל-sphingosine-1P (Ozanimod) ונוגד JAK-1 (Upadacitinib). במחלת קרוהן, הטיפולים המתקדמים כוללים תכשירים ביולוגיים בלבד, ללא זמינות של מולקולות קטנות. למעשה, אופדסיטיניב היא המולקולה הקטנה הראשונה שאושרה לשימוש במחלת קרוהן.
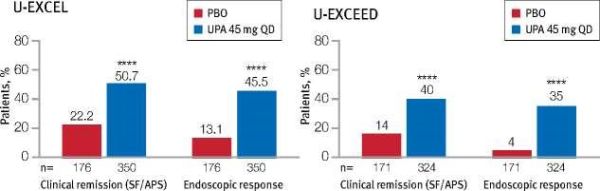
מחקר הפאזה השלישית באופדסיטיניב למחלת קרוהן בחומרה בינונית־קשה כלל שני מחקרי אינדוקציה מקבילים, שנמשכו 12 שבועות וכללו חולים מנוסים ונאיביים לתכשירים ביולוגים קודמים. במחקרי האינדוקציה, התבצעה רנדומיזציה 2:1 ל־45 מ"ג ליום מול פלצבו. המגיבים לטיפול עברו למחקר אחזקה בן 52 שבועות, בו התבצעה רה-רנדומיזציה 1:1:1 ל־30 מ"ג, 15 מ"ג או לפלצבו[13].
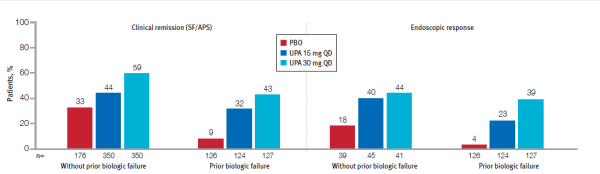
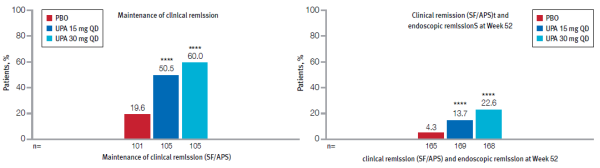
המחקר הדגים יעילות מובהקת של רינבוק מול פלצבו, גם במנוסים וגם בנאיביים, גם באינדוקציה וגם בתקופת האחזקה. התכשיר הביא להשגת כל היעדים המחקריים, כולל רמיסיה קלינית ותגובה אנדוסקופית, הפוגה קלינית ללא סטרואידים והפוגה אנדוסקופית. התכשיר התאפיין בשיפור מהיר מאוד בתסמינים. כמו כן, הודגם שיפור מובהק בתופעות דלקתיות מחוץ למעי הכוללות בעיקר אנמיה ומעורבות מפרקית וכן במדדי עייפות ואיכות חיים. שני מינוני האחזקה הודגמו כיעילים, עם נטייה מספרית ליעילות גבוהה יותר במינון הגבוה.
בנוסף, הודגם כי הארכת תקופת השראת ההפוגה ב־12 שבועות נוספים של 30 מ"ג אפשרה עלייה בשיעור המטופלים אשר השיגו תגובה קלינית. כמו כן, במטופלים עם מאפיינים של מחלה עמידה, היעדים המחקריים הושגו בשיעור גבוה יותר בשימוש במינון האחזקה הגבוה. כמו כן, שיעור החולים אשר נהנו מהפוגה קלינית ואנדוסקופית בתום שנת הטיפול, ללא צורך בסטרואידים, היה גבוה עם שיעורי תגובה בהשוואה לפלצבו, גבוהים מתוצאות מחקרים בתכשירים קודמים[13].
לאור התוצאות, הרשויות הרגולטוריות בארצות הברית ובאירופה אישרו את השימוש באופדסיטיניב בחולים במחלת קרוהן בחומרה בינונית-קשה. ההמלצה לטיפול להשראת הפוגה במינון של 45 מ"ג למשך 12 שבועות. מינון האחזקה המומלץ הוא 15 מ"ג. בחולים עם מחלה חמורה, נרחבת או עמידה לטיפול קודם, ניתן לבחור במינון אחזקה של 30 מ"ג, כאשר השאיפה היא להשתמש במינון הנמוך שמאפשר שמירה על הפוגה. בחולים אשר לא הגיבו באופן מלא ל־12 שבועות של השראת הפוגה במינון של 45 מ"ג, ניתן לשקול הארכת תקופת האינדוקציה ל־12 שבועות נוספים במינון של 30 מ"ג.
פרופיל הבטיחות שהודגם במחקר הקליני היה דומה לזה המוכר בהתוויות האחרות. שיעור הזיהומים הקשים היה נמוך מאוד. תופעות הולואי הנפוצות היו נזו־פרינגיטיס, עלייה בערכי CPK ואקנה. כמוכר מקבוצת נוגדי ה־JAK, הודגם שיעור מוגבר של הרפס זוסטר. שיעור אירועי הממאירות והאירועים הטרומבואמבוליים היה זעום[13].
לאור עדות לאירועים טרומבואמבוליים וממאירות בשימוש בנוגד JAK לא סלקטיבי בחולים עם דלקת פרקים שגרונית מעל גיל 50 עם גורמי סיכון למחלה קרדיו-ווסקולרית[14], הרשויות הרגולטוריות ממליצות על הערכת הגיל, ממאירויות וגורמי הסיכון הקרדיווסקולריים והטרומבואמבוליים בכלל המטופלים, והעדפה להימנע משימוש בתכשיר מקבוצת JAK במטופלים מבוגרים ו/או בעלי סיכון למצבים אלה. הסיכון למצבים אלה בחולים עם מחלות מעי דלקתיות אשר טופלו ברינבוק הודגם כזעום.
עם העלייה במספר התכשירים ומנגנוני הטיפול במחלת קרוהן, תהליך קבלת ההחלטות בבחירת הטיפול הופך מורכב יותר. אין ברשותינו כלים ביולוגיים המאפשרים בחירה מותאמת אישית. בבואנו לבחור תרופה, אנו נשענים על מאפייני המחלה, מחלות רקע, חשיפה תרופתית קודמת ופרופיל היעילות והבטיחות של התכשיר. בין המאפיינים החשובים באופדסיטיניב נמנים יכולת התכשיר להשיג הפוגה תסמינית ואנדוסקופית מהירה שנשמרת לאורך 52 שבועות, היכולת להתאים מינון בהתאם להתייצגות המחלה ויכולת התכשיר לדכא פעילות דלקתית במערכות נלוות דלקת מפרקים אקסיאלית ודלקת במפרקים הפריפריים.
לסיכום, אופדסיטיניב הוא המולקולה הקטנה הראשונה אשר אושרה לשימוש במחלת קרוהן. התכשיר נבחן לפי סטנדרטים מודרניים מחמירים הכוללים יעדים מחקריים נוקשים והביא לשיעורים גבוהים של תגובה משמעותית לטיפול כולל ריפוי רירית המעי, גם בחולים עם מאפייני מחלה קשים וכישלון בקוי טיפול קודמים. השימוש בתכשיר בתנאי "העולם האמיתי" יוסיף לשפוך אור על מאפייני התכשיר ועל מיצובו המיטבי באלגוריתם הטיפולי במחלת קרוהן.
ביבליוגרפיה
- ↑ Giulia R, Siew CN, Kotze PG, et al. Crohn’s disease (Primer). Nat Rev Dis Primers. 2020;6(1).
- ↑ Solberg IC, Vatn MH, H0ie O, et al. Clinical Course in Crohn’s Disease: Results of a Norwegian Population-Based Ten-Year Follow-Up Study. Clinical Gastroenterology and Hepatology. 2007;5(12). doi:10.1016/j.cgh.2007.09.002
- ↑ 3.0 3.1 Torres J, Bonovas S, Doherty G, et al. ECCO guidelines on therapeutics in Crohn’s disease: Medical treatment. J Crohns Colitis. Published online 2020. doi:10.1093/ ecco-jcc/jjz180
- ↑ Adamina M, Bonovas S, Raine T, et al. ECCO Guidelines on Therapeutics in Crohn’s Disease: Surgical Treatment Oded Zmora as ; on behalf of the European Crohn’s and Colitis Organisation [ECCO]. J Crohns Colitis. Published online 2019.
- ↑ 5. Turner D, Ricciuto A, Lewis A, et al. STRIDE-II: An Update on the Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE) Initiative of the International Organization for the Study of IBD (IOIBD): Determining Therapeutic Goals for Treat-to-Target strategies in IBD. Gastroenterology. Published online 2021. doi:10.1053/j.gastro.2020.12.031
- ↑ Raine T, Bonovas S, Burisch J, et al. ECCO Guidelines on Therapeutics in Ulcerative Colitis: Medical Treatment. J Crohns Colitis. Published online 2021. doi:10.1093/ ecco-jcc/jjab178
- ↑ D’haens G, Panaccione R, Baert F, et al. Risankizumab as Induction Therapy for Crohn’s Disease: Results from the Phase 3 ADVANCE and MOTIVATE Induction Trials. Vol 399.; 2022. www.thelancet.com
- ↑ Ferrante M, Panaccione R, Baert F, et al. Risankizumab as Maintenance Therapy for Moderately to Severely Active Crohn’s Disease: Results from the Multicentre, Randomised, Double-Blind, Placebo-Controlled, Withdrawal Phase 3 FORTIFY Maintenance Trial. Vol 399.; 2022. www.thelancet.com
- ↑ D’Haens GR, van Deventer S. 25 years of anti-TNF treatment for inflammatory bowel disease: Lessons from the past and a look to the future. Gut. 2021;70(7). doi:10.1136/gutjnl-2019-320022
- ↑ 10. Targownik LE, Bernstein CN, Singh H, et al. The Prevalence and Predictors of Anti-TNF Failure in a Population based Sample of Persons with IBD. Gastroenterology. 2017;152(5). doi:10.1016/s0016- 5085(17)31463-4
- ↑ Olivera P, Danese S, Peyrin-Biroulet L. Next generation of small molecules in inflammatory bowel disease. Gut. 2017;66(2). doi:10.1136/gutjnl-2016-312912
- ↑ Banerjee S, Biehl A, Gadina M, Hasni S, Schwartz DM. JAK-STAT Signaling as a Target for Inflammatory and Autoimmune Diseases: Current and Future Prospects. Drugs. Published online 2017. doi:10.1007/s40265-017- 0701-9
- ↑ 13.0 13.1 13.2 Loftus E V., Panes J, Lacerda AP, et al. Upadacitinib Induction and Maintenance Therapy for Crohn’s Disease. New England Journal of Medicine. 2023;388(21). doi:10.1056/nejmoa2212728
- ↑ Al: SRY et. Cardiovascular and Cancer Risk with Tofacitinib in Rheumatoid Arthritis. N Engl J Med. 2022;386:316-326. doi:10.1056/NEJMoa2109927
- Barberio B, Gracie DJ, Black CJ, Ford AC. Efficacy of biological therapies and small molecules in induction and maintenance of remission in luminal Crohn’s disease: Systematic review and network meta-analysis. Gut. 2023;72(2). doi:10.1136/gutjnl-2022-328052
המידע שבדף זה נכתב על ידי ד"ר עירית אבני בירון, המערך לגסטרואנטרולוגיה, המרכז הרפואי רבין
הכתבה בחסות חברת ABBVIE, הממליצה להשתמש בתרופותיה בהתאם להתוויות ולרישיון המאושרים על ידי משרד הבריאות בישראל.
הכתבה משקפת את ניסיונה ודעותיה האישיות של המחברת
IL-RNQG-230018 September 2023


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק