דלקת קרום ושריר הלב - Perimyocarditis
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| דלקת קרום ושריר הלב | ||
|---|---|---|
| Perimyocarditis | ||
| יוצר הערך | ד"ר מרינה לייטמן, פרופ' צבי ורד | |
פריקרדיטיס היא דלקת של קרום הלב. מיוקרדיטיס היא דלקת של שריר הלב. דלקת קרום הלב לעתים קרובות מלווה בדרגה מסוימת של דלקת שריר הלב[1]. דלקת קרום הלב ודלקת שריר הלב לעתים קרובות מתקיימות ביחד ונגרמות על ידי אותם הגורמים. הסיבה השכיחה ביותר לדלקת קרום הלב ושריר הלב הנה נגיפים קרדיוטרופיים (Cardiotropic viruses) שיכולים לגרום לדלקת בקרום הלב ובשריר הלב[1],[2].
אפדימיולוגיה
אטיולוגיה
פגיעה ישירה של הנגיפים בשריר הלב מעוררת שחרור של חלבונים תוך-תאים ותגובה של המערכת החיסונית, לפעמים על רקע גנטי. מנגנון זה גורם לפגיעה בשריר הלב ובקרום הלב אחרי זיהום נגיפי, במחלות רקמת החיבור, מחלות דלקתיות של המעיים, אחרי קרינה או שימוש בתרופות (ראו טבלה)[1][2].
טבלה 1. אטיולוגיה לדלקת קרום ושריר הלב[1]
- זיהומי (2/3 מהמקרים)
- נגיפי (שכיח)
- אנטרו-וירוסים (Enteroviruses): קוקסאקי A ו-B (Coxsackie A and B), אקו-וירוס (Echovirus), נגיף אפשטיין-באר (EBV - Epstein Barr virus), נגיף ציטומגאלו (CMV – Cytomegalovirus), נגיף ההרפס האנושי 6 (HHV6 - Human herpesvirus 6), אדנו-וירוס (Adenovirus), נגיף השפעת (Influenza) מסוג A ו-B, פרוו-וירוס B19 (Parvovirus B19), צהבת נגיפית B ו-C (Hepatitis B and C), נגיף הכשל החיסוני האנושי (HIV - Human immunodeficiency virus), נגיף אבעבועות הרוח (Varicella), חזרת (Mumps), חצבת (Rubeola), אדמת, פוליו, ריינו-וירוס (Rhinovirus), נגיף הוקציניה (Vaccinia)
- חיידקי - הכי שכיחים:
- שחפת (4-5%)
- קוקסיאלה בורנטי (Coxiella burnetii)
- זיהומים חיידקיים נוספים - נדירים:
- פנאומוקוק, מנינגוקוק, גונוקוק, סטאפילוקוק, המופילוס (Haemophilus), כלמידיה, מיקופלסמה, לגיונלה, לפטוספירוזה (Leptospirosis), ליסטריה.
- פטריות – נדיר:
- במטופלים תקינים חיסונית: היסטופלסמה.
- במטופלים עם דיכוי חיסוני: אספרגילוס, בלסטומיקוזיס (Blastomycosis), קנדידה.
- טפילים – מאד נדיר:
- אכינוקוקוס (Echinococci), טוקסופלסמה.
- סיבות לא זיהומיות (1/3 מהמקרים)
- דלקת קרום-לב אוטואימונית (פחות מ-10%)
- תסמונות לאחר פציעה בקרום או שריר הלב (Post-myocardial/pericardial injury syndromes):
- תסמונת לאחר אוטם בשריר הלב, תסמונת לאחר חיתוך קרום הלב (postpericardiotomy syndrome).
- דלקת קרום הלב לאחר טראומה, כולל איאטרוגנית: לאחר צנתור, לאחר השתלת קוצב לב, לאחר אבלציה.
- דלקות כלי דם (וסקוליטיס) ומחלות רקמת חיבור: זאבת אדמנתית מערכתית (Systemic lupus erythematosus), דלקת מפרקים שגרונתית (Rheumatoid arthritis), טרשת מערכתית (Systemic sclerosis), סרקואידוזיס, מחלת צ'ורג-שטראוס (Churg–Strauss syndrome), קדחת שגרונית חריפה (Acute rheumatic fever), תסמונת שיוגרן, דלקות כלי דם מערכתיות (Systemic vasculitides), מחלת בכצ'ט, קדחת ים תיכונית משפחתית (FMF - Familial mediterranean fever), מחלות מעי דלקתיות: מחלת קרוהן, דלקת כיבית של המעי הגס (Ulcerative colitis).
- דלקת קרום הלב בשל ממאירות (5-7%)
- גידולים ראשוניים (נדיר): מזותליומה של קרום הלב.
- גרורות (שכיח): סרטן שד, סרטן ריאות, לימפומה.
- סיבות מטבוליות: אורמיה, מיקסאדמה (Myxedema)
- דלקת קרום הלב לאחר קרינה
- תרופות (נדיר):
- Procainamide, Hydralazine, Phenytoin (תסמונת דמויית זאבת אדמנתית מערכתית), Isoniazid, פניצילינים (דלקת קרום הלב מרגישות-יתר עם אאוזינופיליה), Doxorubicin, Cerubidine (Daunorubicin), Methyldopa, Methysergide, סולפונאמידים (Sulphonamides), Cytarabine, Phenylbutazone, קוקאין.
קליניקה
סיפור אפייני לזיהום נגיפי עם חום, תופעות מערכתיות, כאבי שרירים, כאבי גרון, שלשולים, הקאות.
בהמשך התפתחות של כאבים בעלי אופי פלואוריטי (Pleuritic pain, מתגברים בנשימה ובשכיבה פרקדן), חולשה, חוסר סיבולת למאמץ, דפיקות לב (פלפיטציות).
כאבים בחזה מאפיינים מעורבות של קרום הלב. תלונות מערכתיות, כגון: חולשה, עייפות, ודפיקות לב - אופייניות יותר למעורבות של שריר הלב.
אבחנה
ברוב המקרים של דלקת קרום הלב יש מעורבות הן של קרום הלב והן של שריר הלב[2]. הפרעה אזורית באקוקרדיוגרפיה ועלייה של אנזימי לב - במיוחד טרופונין (Troponin), המאפיין פגיעה בשריר - מצביעה על פגיעה בשריר הלב.
דלקת בקרום הלב כוללת טווח רחב של הסתמנויות, החל מדלקת שמערבת רק את קרום הלב, עד למקרים של דלקת רק בשריר הלב, אך ברוב המקרים יש תערובת של דלקת בקרום הלב ובשריר הלב ביחד - מיופריקרדיטיס / פרימיוקרדיטיס (Perimyocarditis / Myopericarditis)[1][2].
בדיקה גופנית
בבדיקה אפשר למצוא שפשוף פריקרדיאלי (Pericardial friction rub), כאשר בדרך כלל שומעים את הלב במצב של ישיבה ובעצירת נשימה בזמן הנשיפה (בתנאים האלו הלב מתקרב לדופן בית החזה). שפשוף פריקרדיאלי ניתן לשמוע כאשר כמות הנוזל הפריקרדיאלי קטנה או מינימלית. כאשר כמות הנוזל בקרום הלב הולכת וגדלה, השפשוף הפריקרדיאלי נעלם.
בחולים עם תפליט פריקרדיאלי גדול (Large pericardial effusion) קולות הלב מרוחקים ומהירים, יכול להיות פרפור פרוזדורים, לחץ דם נמוך, סימנים של אי ספיקת לב ימנית. בחלק מהמקרים עלולות להיות הפרעות קצב חדריות המחייבות ניטור קפדני במסגרת מחלקה קרדיאלית.
במידה וכמות הנוזל גדולה מאד, או לחליפין מצטברת במהירות, נוצר לחץ על חללי הלב הימניים המונע התרחבות תקינה של חללים אלה. מצב זה, המלווה בקיפוח המודינמי, נקרא טמפונדה (Tamponade) ומחייב הוצאת הנוזל בדיקור של קרום הלב או בניתוח.
אלקטרוקרדיוגרפיה (ECG - Electrocardiography)
שינויים באלקטרוקרדיוגרפיה (ECG - Electrocardiography) האופייניים לתהליך זה כוללים ארבעה שלבים:
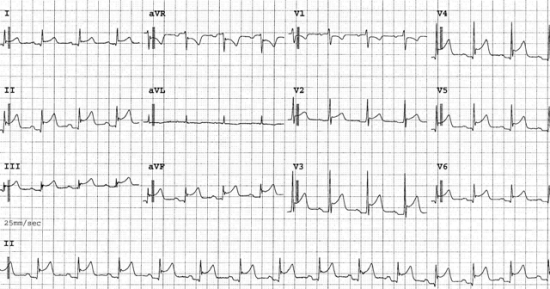
- שלב 1 (שעות ראשונות-ימים ראשונים) - עליות מפושטות (דיפוזיות) של מקטע ST וצניחות PR בולטות בחיבורים V5 ו-V6, (ראו תמונה).
- שלב 2 - חזרה של ST ו-PR למראה תקין.
- שלב 3 - היפוך גלי T אחרי החזרה של ST למצב תקין.
- שלב 4 - חזרה של האלקטרוקרדיוגרפיה למראה תקין, או, לחליפין, שינויי גלי T הנשארים קבועים.
לא תמיד השינויים באלקטרוקרדיוגרפיה קלאסיים כמתואר. לעתים קרובות השינויים פחות טיפוסיים ויחד עם כאבים בחזה יכולים לחקות תסמונת תעוקתית חדה.
בדיקות מעבדה
- אנזימי לב , כמו טרופונין או קריאטין פוספוקינאז (CPK - Creatine phosphokinase) - עלולים להיות מוגברים, בהתאם למידת הפגיעה בשריר הלב.
- סמנים (מרקרים) של דלקת - שקיעת דם וחלבון מגיב C (CRP - C-reactive protein) בדרך כלל מוגברים במחלות דלקתיות של קרום הלב ושריר הלב, אך יש מקרים נדירים של דלקת בקרום הלב עם CRP תקין.
הדמיה
אקו לב
ברוב המקרים של דלקת בקרום הלב, התפקוד הגלובלי של חדר שמאל שמור. ההפרעה האזורית השכיחה ביותר - ירידה בהתכווצות בדופן תחתונה ואחורית-צידית (Inferior and posterolateral).
תפליט פריקריאלי קיים לעתים קרובות, וברוב החולים בכמות קטנה-בינונית, אך יכול להגיע לכמות גדולה ולגרום ללחץ על מדורי הלב כמפורט לעיל. העדר של נוזל פריקרדיאלי לא שולל קיום האבחנה של דלקת קרום ושריר הלב.
הדמיה בתהודה מגנטית של הלב (Cardiac MRI)
הדמיה בתהודה מגנטית של הלב (Cardiac MRI)[3] יכולה לגלות שינויים ברקמת הלב האופיניים לדלקת קרום הלב / דלקת שריר הלב / דלקת קרום הלב ושריר הלב.
הבדיקה מתבצעת עם הזרקת חומר ניגוד - Dotarem (נגזרת של גדוליניום). חומר הניגוד(3) עובר דרך כלי הדם ולא יכול לחדור לתוך התאים. במקומות בהם תאי שריר הלב פגועים בעקבות הדלקת, חומר הניגוד מגיע, אך הוא מגיע מאוחר יותר, כ-10 דקות אחרי הזרקתו לתוך הוריד - האדרה מאוחרת (Delayed enhancement).
במחלות דלקתיות של שריר הלב, האדרה מאוחרת קיימת באזור האפיקרדיום (Epicardium) וה-Mid-layer ולא באנדוקרדיום (Endocardium). סימן זה מבדיל בין מחלה דלקתית של שריר הלב לבין מחלת לב איסכמית, בה אזורים של האדרה מאוחרת נמצאים בעיקר בשכבת האנדוקרדיום (Endocardial layer). מסתבר שנגיפים שונים פוגעים קודם בקרום הלב ומשם מגיעים לשריר הלב, ולכן אזורים של האדרה מאוחרת יותר בולטים באפיקרדיום וב-Mid-layer. בדרך כלל, באזורים עם האדרה מאוחרת יש גם הפרעה בהתכווצות שאפשר לצפות בה ב-MRI וגם באקו לב.
לנגיפים שונים יש נטייה לפגוע באזורים מסוימים בלב[4], וזה עשוי לקבוע את מהלך המחלה:
- חולים עם זיהום בפרוו-וירוס B19 (Parvovirus B19) מגיעים בדרך כלל לקבלת עזרה מוקדם יותר עקב כאבים חזקים בחזה. תפקוד הלב בחולים אלה מופחת רק במידה קלה או שמור, והאדרה מאוחרת ב-MRI ממוקמת בעיקר בדופן הצידית של חדר שמאל באזור האפיקרד.
- בזיהום עם נגיף ההרפס האנושי 6 (HHV6 - Human herpesvirus 6), התמונה קלינית שונה בדרך כלל, בחלק מהחולים מופיעה אי ספיקת לב, ותפקוד הלב מופחת. האדרה מאוחרת ב-MRI ממוקדת באזור הקדמי-מחיצתי (Anteroseptal), לעתים קרובות ב-Mid-layer.
- חולים עם זיהום משולב בנגיף ההרפס האנושי 6 ופרוו-וירוס B19 סובלים מאי ספיקת לב ומירידה קשה בתפקוד הלב. ב-MRI האדרה מאוחרת נמצאת בכל המחיצה[4].
ביופסיה של שריר הלב
ביופסיה של שריר הלב הייתה בעבר בשימוש תכוף לאבחנה של דלקת שריר הלב, אך כיום כמעט אינה בשימוש: ראשית, ביופסיה היא פעולה פולשנית המלווה בסיבוכים. שנית, ביופסיה מתבצעת בדרך כלל משריר של חדר ימין, ומשום שבדלקת שריר הלב מעורבות של שריר הלב עלולה להיות ממוקמת באזורים מסוימים, ביופסיה עלולה להיות לא אבחנתית. פרט לכך, מאז הזמינות של ה-MRI הלבבי - MRI היא בדיקת הבחירה, המסוגלת לסרוק את כל הלב, אינה פולשנית ועדיפה על הביופסיה.
צנתור כלילי
בחלק מהחולים, כאשר כאבי החזה פחות טיפוסים והשינויים באלקטרוקרדיוגרפיה לא חד משמעים, יש צורך לשלול מחלת לב כלילית ולבצע בדיקת טומוגרפיה ממוחשבת (CT - Computed tomography) של עורקי הלב או צנתור כלילי.
בדיקות נוספות
הבירור בסיסי כולל:
- בדיקה גופנית
- אלקטרוקרדיוגרפיה
- צילום חזה
- אקו לב
- בדיקת דם ל-CRP או שקיעת דם ובדיקת טרופונין בדם
לאחר בירור זה, יש מקום, במקרים מסויימים, לבדיקות הבאות:
- CT חזה בחשד לשחפת, ממאירות, או מחלות מערכתיות
- בדיקת ממוגרפיה לשלול נוזל בקרום הלב על רקע ממאירות
- בדיקת דם לנוגדנים למרכיבי הגרעין (ANA - Anti-nuclear antibodies) בחשד למחלות מערכתיות.
- תרביות דם יכולות לעזור במקרים של דלקת קרום לב פורולנטית (Purulent pericarditis) שהיא לרוב מחלה סוערת וקשה.
טיפול
חולים עם חשד לדלקת בקרום הלב או שריר הלב מומלץ לאשפז לצורך הערכה, בירור וניטור.
הטיפול התרופתי
הטיפול התרופתי מפורט בקישור להלן.
- הטיפול העיקרי בדלקת חריפה בקרום הלב[2] הנו תכשירים נוגדי דלקת לא סטרואידלים (NSAIDs - Nonsteroidal anti-inflammatory drugs) כולל Acetylsalicylic acid, עם תכנון של קורס טיפולי ארוך עד לנורמליזציה מלאה של CRP. בחירה של תרופה אנטי-דלקתית צריכה להסתמך על הניסיון של הרופא המטפל, על הצלחה של תרופה מסוימת בהתקף קודם של דלקת בקרום הלב ועל מחלות נלוות: לאנשים עם מחלת לב איסכמית מתאימה Acetylsalicylic acid, כאשר הם צריכים להימנע מ-NSAIDs אחרים. הורדת המינון של Aspirin ושל NSAIDs אחרים צריכה להיות הדרגתית. בזמן הטיפול עוקבים אחרי רמות ה-CRP בדם.
המינונים המתאימים:- Acetylsalicylic acid 2-4 גרם ליום
- Indomethacin במינון 75-150 מ"ג ליום
- Ibuprofen במינון 1600-3200 מ"ג ליום (מינון ממוצע - 600 מ"ג 3 פעמים ביום)
- Colchicine[2] מומלץ לטיפול בהתלקחות חוזרת של דלקת קרום הלב (Recurrent pericarditis) ועשוי להיות יעיל בדלקת קרום לב חריפה (Acute pericarditis)[2],[5]. המינון הוא: 0.5 מ"ג פעמיים ליום במשך 3 חודשים בהתקף ראשון במקרים מסוימים של דלקת קרום לב חריפה, ולמשך 6-12 חודשים בדלקת קרום לב חוזרת[2]. הפסקת הטיפול צריכה להיות הדרגתית.
מינון יומי מופחת של Colchicine, עד 0.5 מ"ג ליום, בלי צורך במנת העמסה, מומלץ במקרים הבאים:- אנשים עם משקל פחות מ-70 ק"ג.
- מטופלים עם אי ספיקת כליות, כלומר: פינוי קראטינין (Creatinine clearance) 35-50 מ"ל לדקה. במידה ופינוי הקריאטינין הנו 10-34 מ"ל לדקה, המינון המקסימאלי של Сolchicine צריך להיות 0.5 מ"ג כל 2-3 ימים. בפינוי קריאטינין פחות מ-10 מ"ל לדקה אסור לתת Colchicine [2].
- אנשים בגיל מעל 70.
- Prednisone[2] מתחילים במקרים של חוסר סבילות, התוויות נגד, או כשלון טיפול על ידי NSAIDs ו-Acetylsalicylic acid.
מתחילים במינון נמוך בינוני 0.2-0.5 מ"ג\ק"ג ליום, עם הפחתת המינון באופן מאוד הדרגתי. הסף הקריטי בהורדת המינון נמצא ב-10-15 מ"ג ליום - במינונים האלו הורדת המינון חייבת להיות מאוד הדרגתית: כ-1.0-2.5 מ"ג ליום כל 2-6 שבועות מומלצת. אם יש חזרה של תסמינים - צריך לעשות כל מאמץ כדי לא לעלות במינון הסטרואידים, להתחיל Acetylsalicylic acid או NSAIDs, לשקול Colchicine במינון נמוך של 0.5-0.6 מ"ג ליום. הפחתה במינון של סטרואידים צריך לעשות אחרי ירידת התסמינים וחזרה של CRP לערכים תקינים. - כאשר הפגיעה היא בעיקר בשריר הלב ויש ירידה בתפקוד חדר שמאל, יש להיזהר משימוש בתרופות נוגדות דלקת. יש להפחית את המינונים של התרופות נוגדות הדלקת: Acetylsalicylic acid במינון 500 מ"ג 3 פעמים ליום למשך שבוע–שבועיים.
מעקב
חייבים להגביל במאמץ פיזי למשך 6 שבועות ולחזור לבדיקת אקו לב לאחר 1, 6 ו-12 חודשים, במיוחד בחולים עם ירידה בתפקוד הלב ועם אי ספיקת לב, הנוטלים מעכבי אנזים המהפך (ACE-Inhibitors) וחסמי בטא (Beta-blockers)[2].
פרוגנוזה
דגלים אדומים
ביבליוגרפיה
- ↑ 1.0 1.1 1.2 1.3 1.4 Imazio M, Trinchero R: Myopericarditis: Etiology, management, and prognosis. International Journal of Cardiology 127 (2008) 17–26
- ↑ 2.0 2.1 2.2 2.3 2.4 2.5 2.6 2.7 2.8 2.9 Imazio M, Spodick DH, Brucato A, Trinchero R, Adler Y: Controversial Issues in the Management of Pericardial Diseases. Circulation 2010;121;916-928
- ↑ Mahrholdt H, Goedecke C, Wagner A, et al. Cardiovascular Magnetic Resonance Assessment of Human Myocarditis: A Comparison to Histology and Molecular Pathology. Circulation 2004;109;1250-1258
- ↑ 4.0 4.1 Mahrholdt H, Wagner A, Deluigi CC, et al. Presentation, patterns of myocardial damage, and clinical course of viral myocarditis. Circulation. 2006;114(15):1581-90.
- ↑ Maisch B, Seferovic PM, Ristic AD, Erbel R, Rienmuller R, Adler Y, Tomkowski WZ, Thiene G, Yacoub MH, for the Task Force on the Diagnosis and Management of Pericardial Diseases of the European Society of Cardiology. Guidelines on the diagnosis and management of pericardial diseases. Eur Heart J. 2004;25:587– 610
המידע שבדף זה נכתב על ידי ד"ר מרינה לייטמן, מנהלת יחידת אקו לב, בית חולים אסף הרופא; פרופ' צבי ורד, מנהל מכון הלב, בית חולים אסף הרופא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק