הסמן ZAP-70
| מדריך בדיקות מעבדה | |
| הסמן ZAP-70 | |
|---|---|
| שמות אחרים | : Zeta-chain-associated protein kinase 70 |
| 250 פיקסלים | |
מבנה מתחמי SH2 של האנזים. מתוך PDB 1m61
| |
| מעבדה | המטולוגיה בדם |
| תחום | הערכה פרוגנוסטית של חולים עם לאוקמיה לימפוציטית כרונית |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
לקבוע פרוגנוזה ואת הצורך בתרפיה אגרסיבית במטופלים עם CLL של תאי B.
רקע קליני
המהלך הקליני של לאוקמיה לימפוציטית כרונית של תאי B או B-CLL מגוון, ופרמטרים ביולוגיים חדשים צריכים להתווסף לשיטות ה-staging המקובלות כדי לנבא מהלך אגרסיבי או שמא אינדוּלֶנטי של המחלה. CLL היא הלאוקמיה השכיחה ביותר בעולם המערבי, והיא מאופיינת על ידי הצטברות של תאי B חד-שבטיים מסוג +CD5, והופעה של לימפוציטים בשלים קטנים (Matutes וחב' ב-Leukemia משנת 1994). אחת התכונות המסקרנות של המחלה, היא ההטרוגניות הקלינית שלה, כאשר חלק מהחולים בה נאלצים להיכנע למסלול מחלה מואץ ומוות תוך זמן קצר, בעוד שאחרים מפגינים מסלול מחלה יציב יותר, שקצב התקדמותו אטי והחולה שורד שנים רבות. לכן חיוני למצוא סמנים רגישים לזיהוי חולים עם פרוגנוזה גרועה (Caligaris-Cappio וחב' ב-J Clin Oncol משנת 1999).
ל-CLL יש מהלך מחלה מאוד משתנה. חלק מהחולים שורדים עשרות שנים ללא כל טיפול, ואילו חולים אחרים עם CLL זקוקים לטיפול אגרסיבי תוך שנים אחדות לאחר האבחון של המחלה. היכולת לנבא מחלת איזה מהחולים תתקדם במהירות, עשויה לסייע בהחלטה על אסטרטגיית הטיפול ומועדו. המנבא המבוסס ביותר של התקדמות CLL הוא חסר מוטציות במקטע המשתנה של השרשרת הכבדה של האימונוגלובולין (IgVH) בתאים הסרטניים. עם זאת, כיוון שבחינת מוטציות ב-IgVH אינה זמינה ברוב המעבדות, מספר סמני עזר אחרים נחקרו. כיום, הסמן המקובל ביותר הוא הביטוי של zeta-associated protein 70 או ZAP-70, המבוטא בעיקר על פני תאי T ותאי NK, ומשחק תפקיד קריטי בהעברת איתותים המלווים שפעול של הקולטן של תאי T. ב-CLL, ביטוי מוגבר של ZAP-70 בתאי B מנבא את הצורך בטיפול רפואי מוקדם יותר, באותה מידה שניתן להסיק על נחיצות טיפול זה בהיעדר מוטציות ב-IgVH. ברור ששילוב של שתי בדיקות אלו ייתן תחזית פרוגנוסטית מדויקת יותר.
למסקנה אחרונה זו הגיע גם ה-CLL Research Consortium או CRC, תוך הדגשה שבדיקה משולבת זו יעילה במיוחד כאשר היא מוגבלת לחולים בשלבי מחלה מוקדמים, לחולים לא מטופלים ולאלה מעל גיל 65 שנה. מחקר ה-CRC מצביע על ZAP-70 כסמן הפרוגנוסטי החזק ביותר, לנבא את מהלך CLL. לאלה עם ZAP-70 חיובי יש פרק זמן של 3 שנים מאבחון המחלה עד תחילת הטיפול, ללא קשר לסטטוס המוטציות ב-IgVH או לסטטוס של CD38.
באשר לקבוצת המאובחנים עם ZAP-70 שלילי, ניתן לחלקה לשניים: אלה עם סיכון ממוצע (6 שנים עד לתחילת הטיפול) ולאלה עם סיכון נמוך (10 שנים לתחילת הטיפול הראשון), בהתבסס על סטטוס המוטציות של IgVH.
הביטוי של CD38 על תאי CLL נמצא מוגבר במספר גדול יותר של שבטי תאים (clones) מתחלקים. קיים קשר הדוק בין ביטויו של CD38 לבין מדד ההתחלקות של Ki67, במקביל לחיוּביוּת מוגברת של ZAP-70 (על פי Damle וחב' ב-Blood משנת 2007). נתון זה מראה ששבטי-תאים חיוביים ל-CD38 נכנסים למעגל חלוקת התא באופן תכוף יותר מאשר שבטי-תאים שליליים ל-CD38. שבטי-תאים חיוביים ל-CD38 מבטאים ביֶתֶר את VEGF, גורם הגדילה של תאי האנדותל הכרוך כשלעצמו עם ביטוי מוגבר של Mcl-1, החלבון האנטי-אפופטוטי, מה שעשוי להסביר את שגשוגם הבולט של שבטי-תאים אגרסיביים של CLL (על פי Pepper וחב' ב-Leukemia משנת 2007).
בשנת 1991 דווחו לראשונה Chan וחב' ב-Proc Natl Acad Sci USA על זיהוי בתאי Jurkat מֽגוּרים על ידי הקולטן של תאי T, של טירוזין פוספו-פרוטאין בעל שרשרת (zeta , ζ) שמשקלו המולקולארי 70 קילו-דלטון, שכונה מאז ZAP-70. החשיבות של ZAP-70, טירוזין קינאזה ציטופלזמטי, המבוטא בעיקר בתאי T, התגלתה במהירות על בסיס התצפיות הבאות:
- למטופלים החסרים ZAP-70 אין תאי T פונקציונאליים בדם ההיקפי, והם סובלים מחסר חיסוני משולב חמור (SCID) על פי Arapia וחב' ב-Cell משנת 1994, ו-Elder וחב' ב-Science משנת 1994
- ההתפתחות של תאי T בעכברים משוללי ZAP-70, נעצרת במעבר מהשלב של +CD4 ל+CD8 בו מתרחשת הסלקציה החיובית והשלילית של תימוציטים (Kadlecek וחב' ב-J Immunol משנת 1998, ו-Negishi וחב' ב-Nature משנת 1995)
- ההדגמה בשורת תאים P116 ממקור Jurkat החסרים ביטוי של ZAP-70, שתאים אלה נכשלים בשפעול של איתותים downstream לאחר סטימולציה על ידי הקולטן של תאי T (על פי Williams וחב' ב-Mol Cell Biol משנת 1998). כיוון ש-ZAP-70 משחק תפקיד קריטי בהתפתחות תאי T, מאמץ מחקרי ניכר הושקע ללמידת הוויסות, המבנה והתפקיד של ZAP-70.
המבנה והביולוגיה של ZAP-70
ZAP-70 שייך למשפחת טירוזין קינאזה הכרוך עם איתותים של תאי-T. החלבון ZAP-70 מבוטא על פני תאי T ותאי NK ומהווה חלק מה-T cell receptor ומשחק תפקיד קריטי באיתות של תאי-T. הגן המקודד ל-ZAP-70 ממוקם על כרומוזום 2 בעמדה 12q2, ומכיל 18 אֶקסונים. חלבון זה זוהה לראשונה בשנת 1994 כשותף מועדף לפוספורילציה של שרשרת zeta של הקומפלקס CD3 הכרוך עם קולטן תאי-T המצוי על לימפוציטים מסוג T על ידי van Oers וחב' ב-Immunology. ל-ZAP-70 יש 619 חומצות אמינו והוא מורכב מ-3 מקטעים (domains).
מקטעי הטירוזין קינאזה קרויים על בסיס של Src kinase המכיל שלושה מקטעים עיקריים המכונים SH המייצג את Src homology. המקטע SH1 מכיל את הפעילות האנזימטית, המקטע SH2 מפקח על האינטראקציה בין החלבונים ועל הזרחון על ידי פוספו-טירוזינים ספציפיים, ואילו SH3 מספק תוספת של ספציפיות הכרה בין החלבונים. ישנם 2 מקטעי SH2 בקצה ה-N-טרמינאלי של ZAP-70, בעוד שהמקטע הקטליטי של האנזים kinase ממוקם בקצה ה-C-טרמינאלי של חלבון זה. כל אחד ממקטעי SH2 מכילים בערך 100 חומצות אמינו, והם בנויים על בסיס שני סלילוני α-helix וגדילי β אנטי-מקבילים. בכל צד של שרשרות בטא נמצאות שתי גומחות-קישור, אחת מהן טעונה חיובית כדי לרתק את המטען השלילי של פוספו-טירוזין, והשנייה מספקת את הספציפיות לאינטראקציה בין החלבונים.
המקטע הקטליטי מכיל שלושה חלקים שהשתמרו מאוד של PTK או protein tyrosine kinase (על פי van Oers ו-Weiss ב-Senin Immunol משנת 1995):
- אזור עתיר-גליצין הקושר נוקלאוטידים הכרוך בקישור של ATP, כאשר שיירי גליצין מעגנים את הפוספאט, בעוד ששיירי ליזין קושרים את הנוקלאוטיד עצמו
- אתר של פוספורילציה עצמית
- motif ספציפי המכיל את רצף חומצות האמינו HRDLAARN.
ZAP-70 קשור למשפחת PTK ספציפית, עם טירוזין קינאזה של הטחול (SyK), המעורב בעיקר בשפעול של תאי B. שני PTKs אלה דומים מאוד עם הומולוגיה של 73% ברצף חומצות האמינו שלהם, והם מאופיינים על ידי חסר של מקטע SH3, מה שקובע שהספציפיות שלהם נקבעת על ידי שני מקטעי SH2. ב-ZAP-70 כמו גם ב-Syk חל שחלוף של טריפטופן בחומצת האמינו פניל-אלנין במקטע ה-N-טרמינאלי. שחלוף זה עלול להגביל את הספציפיות של ZAP-70 ושל Syk באשר ל-ITAMs המזורחנים, אך לא ביחס לחלבונים מזורחנים אחרים, על ידי המודיפיקציה של הלִבָּה ההידרופובית של הגומחה אליה נקשרים פוספו-פרוטאינים.
ביטוי של ZAP-70 על תאי B משמש כסמן פרוגנוסטי בזיהוי צורות שונות של CLL. אנליזת DNA מבחינה בין 2 צורות CLL, עם אורך הישרדות שונה. CLL חיובי ל-ZAP-70 הוא בעל משך הישרדות ממוצעת של 8 שנים, ואילו CLL שלילי ל-ZAP-70 הוא בעל אורך הישרדות ממוצעת של 25 שנה. רבים מהמאובחנים עם CLL, בעיקר אלה בגיל מתקדם, עם מחלה מתקדמת באיטיות עשויים להימנע מכל טיפול על פי תוצאות מדידת ZAP-70 (על פי Chiorazzi וחב' ב-N Engl J Med משנת 2005).
מדידות וכּימות של ZAP-70
CD38 נמדד על ידי flow cytometry כנגד ביטוי הסמן של תאי-B, הידוע כ-CD19. דיווח עדכני של Letestu וחב' ב-Blood משנת 2010, מראה ש-CD38 הוא מנבא בלתי-תלוי של הישרדות ללא התקדמות המחלה במטופלים עם CLL המסווג כ-Binet stage A. ערך הסף של חיוביות של CD38 נתון לוויכוח: באופן מסורתי ביטוי CD38 על פני למעלה מ-30% של תאי B של CLL, מזוהה עם מחלה יותר פרוגרסיבית. מחקר במדגם גדול של חולים עם CLL מצא שערך סף של 7% של תאים חיוביים ל-CD38 היה יעיל ביותר בהגדרה הפרוגנוסטית של שתי קבוצות הנבדקים (Krobler וחב' ב-Blood משנת 2002), ממצא שנתמך גם במחקר של 130 חולי CLL על ידי Hock וחב' ב-Intern Med J משנת 2010. מחקר אחרון זה מצא שסך ההישרדות שופר משמעותית באלה עם CD38 שלילי, אם כי לא היה הבדל משמעותי בהישרדות בין חולים בהם למעלה מ-5% מהתאים היו חיוביים ל-CD38, לבין אלה בהם למעלה מ-95% מהתאים נמצאו חיוביים לסמן זה.
אנליזה של ZAP-70 על ידי reverse transcriptase-PCR פּוּתחה על ידי שימוש בתאים לאוקמיים ממוינים (Wiestner וחב' ב-Blood משנת 2002), אך שיטת PCR זמינה ומהירה עדיין לא קיימת ברוב המעבדות הקליניות. נכון להיום, שתי הטכניקות העיקריות למדידת ZAP-70 הן flow cytometry על ידי השוואה של ביטוי ZAP-70 בתאי-B או כנגד ביקורת איזוטיפית או כנגד ביטויו של ZAP-70 בתאי-T באותה דגימה (Orchard וחב' ב-Lancet משנת 2004, Rassenti וחב' ב-N Engl J Med משנת 2004, ו-Kay וחב' ב-Cytometry B Clin Cytom משנת 2006). Crespo וחב' דיווחו ב-N Engl J Med משנת 2003, שבערך סף של 20%, ZAP-70 הבדיל באופן חיובי וברור בין שתי קבוצות של חולי CLL: אלה עם ביטוי ZAP-70 בפחות מ-20% מהתאים היו בעלי משך הישרדות ארוך יותר וסיכון נמוך יותר להתקדמות המחלה, והיפוכו של דבר עם אלה בהם ביטוי ZAP-70 גדול מ-20% לפיכך ברוב המעבדות, ZAP-70 מוגדר כ"חיובי" כאשר לפחות 20% מהתאים חיוביים לסמן זה.
ההערכה הסובייקטיבית של שיטות אלו עלולה להביא למסקנות שונות בין מעבדות, וכדי להתגבר על סובייקטיביות זו הוצע שרצוי אולי לקבוע את עוצמת הזריחה הפלואורסצנטית הממוצעת של תאי CLL, ולהשוותה לנתון זה בלימפוציטים מסוג T, במקום קביעת אחוז התאים החיוביים ל-ZAP-70 (על פי Rossi וחב' ב-J Transl Med משנת 2010). שיטות המבוססות על PCR להערכה של ZAP-70 מצטיירת כבעלת מתאם גבוה עם האנליזה של מוטציות ב-IgVH, כאשר 94% מהמטופלים ללא מוטציות ב-IgVH נמצאים חיוביים ל-ZAP-70 ואילו 92% מאלה עם מוטציות ב-IgVH נמצאים שליליים ל-ZAP-70 (על פי Catherwood וחב' ב-Eur J Hematol משנת 2006).
לעתים יש מקרים חריגים, בהם ממצאי ZAP-70 וסטטוס המוטציות ב-IgVH אינם תואמים, דהיינו מקרים בהם ZAP-70 חיובי, ויש מוטציות ב-IgVH. במחקר המצוטט של Orchard וחב', נבחנו 6 מטופלים עם הממצא הסותר האחרון ונמצא שאלה מתוכם עם ZAP-70 חיובי היו בעלי הומולוגיה של 96.5% עם הרצף של תאי הנבט (germline). לעומתם, במטופלים עם הומולוגיה פחותה מ-96% לא בא לביטוי ZAP-70. היפוכו של דבר גם כן זוהה, דהיינו ZAP-70 שלילי וחוסר מוטציות ב-IgVH.
התפקוד של ZAP-70
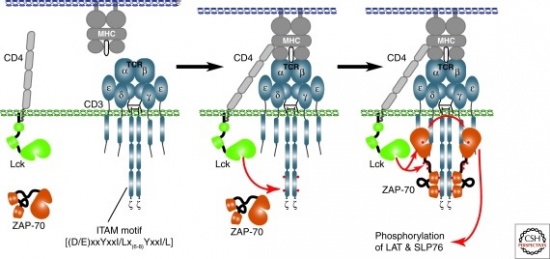
תאי T משופעלים על ידי המפגש בין הקולטן שלהם עם חלקי אנטיגן המוצגים לקולטן זה על תאים מציגי אנטיגנים כגון מקרופאגים, תאים דנדריטים ותאי B, דרך ה-MHC. במהלך שפעול זה, CD4 ו-CD8, הקולטנים הנלווים של קולטן תאי T, נקשרים ל-MHC, ומשפעלים את tyrosine kinase Lck, הכרוך עם הקולטנים הנלווים. האנזים tyrosine kinase Lck, מזרחן את אל החלקים התוך-תאיים של הקומפלקס CD3 (הקרויים ITAMs או Immunoreceptor Tyrosine-based Activation Motifs), ליצירת אתרי עיגון ל-ZAP-70. החבר החשוב ביותר במשפחת CD3 הוא CD3-zeta, אליו נקשר ZAP-70. שני המקטעים (domains) הצמודים במולקולת ZAP-70, ידועים כ-SH2-N ו-SH2-C, והם נקשרים על ידי ה-ITAMs המזורחנים של CD3-zeta, מה שמאפשר ל-ZAP-70 לזרחן את החלבון LAT שהוא ה-linker of activated T-cells. בתגובה, חלבון LAT המזורחן משמש כאתר עיגון אליו נקשרים מספר חלבונים מאותתים, כולל SLP-76. התוצאה הסופית של שפעול הקולטנים של תאי T, הוא השעתוק (transcription) של מספר תוצרי גנים המאפשרים לתאי-T להתמיין, להתרבות ולהפריש מספר ציטוקינים.
לאחר קשירה של הקולטן של תאי T לאנטיגן המוצג על ה-MHC של תא מציג-אנטיגן (APC), ולאחר שקו-רצפטור מסוג CD4 או מסוג CD8 נקשר ל-MHC, מתבצע זרחון של אנזים הנקרא LCK. כתוצאה מהוספת קבוצת הזרחן ל-LCK הוא נעשה אקטיבי, ומזרחן את שרשרת zeta / CD247 הנמצאת על החלק התוך-תאי של קולטן תא T (או TCR). שרשרת zeta מתפקדת כ-ITAM, ולכן כתוצאה מהזרחון, ZAP70 ייקשר אליה ויעבור אקטיבציה. במצב אקטיבי, ZAP70 משמש זרז לזרחונן של מולקולות הנמצאות קרוב לממברנת התא. זרחון מולקולות אלה, גורם לאקטיבציה של PLC-γ. כאשר PLC אקטיבי הוא הופך PIP2 בממברנת התא ל-DAG ול-IP3, ואלו בתוֹרם גורמים לזרחונו, ועקב כך לשחרורו של חלבון מעכב מגורמי שיעתוק (transcription factors), ולאקטיבציה של גורמים אלו. אקטיבציה זו מובילה, לבסוף, לסינתזה של חלבונים המשחקים תפקיד במערכת החיסונית. רמה נמוכה של ZAP70 מתבטאת במחלה חיסונית קשה - SCID.
AP-70 ו-SCID
אובדן ביטוי או כושר פעילות של ZAP-70 באדם, עלול לגרום ל-SCID או severe combined immune deficiency. צורה זו של SCID מתאיינת על ידי מספרים נורמאליים של תאי T בלתי פעילים מסוג +CD4, וחסר של תאי T מסוג +CD8 בדם ההיקפי של מטופלים אלה (Elder וחב' ב-Science משנת 1994 ו-Hivroz ו-Fisher ב-Curr Biol מאותה שנה). מוטציות ב-ZAP-70, מוצאים בחולי SCID והן מופיעות באזור מקטע ה-kinase, ואמנם אצלם מתבטל ביטויו של ZAP-70 (על פי Arpaia וחב' ב-Cell משנת 1994, ו-Chan וחב' ב-Science משנת 1994, Elder וחב' באותו כתב עת מאותה שנה, Gelfand וחב' ב-J Exp Med משנת 1995, ו-Noraz וחב' ב-J Biol Chem משנת 2000).
ZAP-70 כיעד תרפויטי
בגלל תפקידו הקריטי באיתות לקולטן תאי T, הפך ZAP-70 יעד לתרפיה. מעכב ספציפי של ZAP-70 עשוי לחסום את שפעול תאי-T, וכיוון שביטוי ZAP-70 מוגבל לתאי T, לתאי NK ולבזופילים (Au-Yeung וחב' ב-Immunol Rev משנת 2009), חסימת ZAP-70 מוגבלת לתאים אלה. יחד עם זאת, תאי NK ובזופילים מבטאים גם את Syk, מה שיכול לפצות על חסר ZAP-70. זה אמנם מה שמוצאים בתאי NK החסרים ZAP-70, אך עדיין מסוגלים לבטא את פעילותם הציטוליטית (Negishi וחב' ב-Nature משנת 1995). מעכב כזה יכול להיות במיוחד יעיל בהקשר לדחייה שתל (allograft) או בהקשר של אוטו-אימוניות המתווכת על ידי תאי T.
עד תחילת המאה ה-21 הפיתוח של מולקולה קטנה המסוגלת לחדור לתאים ולעכב את ZAP-70 הייתה משימה קשה. למרות שתוארו מספר מעכבים פוטנציאליים של ZAP-70, לא הוכח הפוטנציאל שלהם בעיכוב ZAP-70 (על פי Hirabayashi וחב' ב-Bioorg Med Chem משנת 2009). בהיעדר מעכב זמין כזה, Bishop וחב' דווחו ב-Curr Biol משנת 1998 על יצירה בשיטת הנדסה גנטית של מוטנט של ZAP-70 ששמר אמנם על פעילותו הקטליטית, אך ניתן היה לעכבו על ידי אנלוג של מעכב הקינאזה, PPI. מוטנט של ZAP-70 המוגדר כ-ZAP-70AS, הרגיש לאנלוג זה, נוצר על ידי מוטציה של שחלוף מתיונין בעמדה 414 לפניל-אלנין, ולשחלוף נוסף C405V, כדי לייצב את המקטע הקושר ATP של טירוזין קינאזה (Levin וחב' ב-J Biol Chem משנת 2008).
הביטוי של ZAP-70AS בתאי T משוללי ZAP-70 הידועים כ-P116 Jurkat, הראה שאמנם ביטויו של ZAP-70AS מסוגל לייצר סיגנל של הקולטן של תאי T. בנוסף לכך, גירוי של ZAP-70AS הבא לביטוי בתאי Jurkat בנוכחות המעכב 3MB-PPI, עיכב במהירות את הסיגנלים העוקבים ברצף המקובל, כולל את הזרחון של LAT ושל SLP-76, כמו גם גרם לגיוס פגום של סידן ולעיכוב של זרחון ERK. זאת ועוד, מערכת ZAP-70AS, הראתה את התפקיד הדינאמי של הפעילות הקטליטית של ZAP-70, בוויסות של מעבר סידן, שכן הוספת המעכב 3MB-PPI הביאה תוך שניות לירידה ברמת הסידן התוך-תאי.
האנזים ZAP-70 הוא טירוזין קינאזה תוך-תאי שהתגלה לראשונה בגלל תפקיד באיתות (signaling) לתאי T. נמצא כמו כן ש-ZAP-70 כרוך עם הקולטן של תאי B במהלך של לאוקמיה כרונית לימפטית (CLL). הביטוי של ZAP-70 ב-20% או יותר של תאי B, כרוך בסיכון מוגבר לתוצאות שליליות של תאי B ב-CLL, ונחשב לגורם סיכון משמעותי בחולים אלה. הביטוי של ZAP-70, אם נמצא כזה, נותר קבוע לאורך מהלך המחלה ולכן משמעותו כגורם סיכון נותרת בעינה בלי קשר לנקודת הזמן בה בוצעה מדידת רמתו בחולים אלה.
מטופלים עם CLL עם פחות מ-20% של תאי B חיוביים ל-ZAP-70, הם בסבירות להכיל מוטציות בגנים של immunoglobulin V, מה שמנבא מהלך קליני משופר יותר, בעוד שאלה עם יותר מ-20% של תאי B חיוביים ל-ZAP-70, הם בסבירות להכיל גנים ללא מוטציות ל-immunoglobulin V, מה שמנבא מהלך קליני פחות מעודד.
מודל של שפעול תאי T: לאחר קביעת המְעֹרָבוּת של הקולטן של תאי T, החלבון Lck מתקרב לקומפלקס CDe ומזרחן את motif ה-ITAMs, כאשר ארבעת נקודות הזרחון מסומנות באדום. שני חלבוני ITAM המזורחנים מגיבים עם 2 מקטעי SH2 של ZAP-70. לאחר התקשרות ITAM, החלבון ZAP-70 עצמו יכול לעבור זרחון על ידי Lck, מה שמשפעל את הפעילות הקטליטית של ZAP-70, כמו גם את מנגנון הזרחון העצמי שלו. ZAP-70 הפעיל מזרחן בהמשך את TAT ואת SLP-76, המשמשים תומכנים (scaffolds), והוא מגייס מולקולות איתות רבות נוספות, מה שמביא לשפעול תאי T, לשגשוגם, ולהתמיינות (differentiation) שלהם (Wang וחב' ב-Cold Spring Har Perspect Biol משנת 2010).
ציטומטריית זרימה (flow cytometry)
CD38 ו-ZAP70
ציטומטריית זרימה יכולה לספק מידע פרוגנוסטי חיוני. הביטוי של CD38 וכן של ZAP-70 נמדד באופן מסורתי בשיטת flow cytometry. לאחר פרסום המאמר המכונן של Damle וחב' ב-Blood משנת 1999, הקביעה של ביטוי CD38 וסטטוס המוטציה של IgVH עברו לחזית בדיקות המעבדה שעשויות לספק נתונים חיוניים על מטופלים עם CLL. CD38 הוא גורם שימושי ואמין כיוון שהוא נותר יציב באופן אופייני לאורך זמן, גם במהלך טיפול כימותרפי, והוא ניתן בקלות למדידה במעבדת flow cytometry. עם זאת, ישנם מקרים בהם ביטויו של CD38 משתנה, וביטוי מוגבר שלו יכול להצביע על התקדמות המחלה (Hamblin ב-Ann Hematol משנת 2002, ו-Chevallier וחב' ב-Br J Hematol משנת 2002). נקבע בהמשך שהביטוי של CD38 הוא סמן פרוגנוסטי חשוב, כאשר הוא משולב עם בדיקת ZAP-70 ואנליזה של המוטציה ב-IgVH.
CD38 הוא אנזים הממוקם על פני שטח תאים, המשתתף בתהליכי ספיחת תאים, העברת איתותים בין-תאיים, וויסות רמת הסידן. CD38 יכול להשתתף במטבוליזם של נוקלאוטידים חוץ-תאיים, דוגמת ATP ו-+NAD, בהפיכתם לנוקלאוזידים שיכולים להיקלט על ידי התאים (Deaglio וחב' ב-Semin Cancer Biol משנת 2010). על ידי המטבוליזם של +NAD ושל ADP-ribose ציקלי, CD38 משחק תפקיד בהגברת ריכוזי סידן תוך-תאי. האנטיגן CD31 של תאים אנדותליאליים מגיב עם CD38 על פני תאי CLL, ואינטראקציה זו הודגמה in vivo בטכניקות אימונו-היסטוכימיות (Deaglio וחב' ב-Mol Med משנת 2010, ו-Dohner וחב' ב-N Eng J Med משנת 2000). עלייה בביטוי של CD38, לצד עלייה בצפיפות הווסקולארית בקשרי לימפה, נמצאת במתאם עם הגברת ההתרבות של לימפוציטים והתקדמות המחלה.
הזיהוי של ZAP-70
הגילוי התאי של ZAP-70 יכול להיות מושג על ידי אנליזת mRNA, על ידי Western blot, בשיטות אימונו-ציטוכימיות, בשיטות אימונו-היסטוכימיות, או על ידי flow cytometry. בשיטה האחרונה ניתן להשתמש במבדק 4 הצבעים, תוך שימוש בנוגדנים חד-שבטיים כנגד ZAP-70, CD3, CD19 ו-CD45. אוכלוסיית הלימפוציטים המסומנים באופן פלואורסצנטי ממוינת על CD45 לעומת side scatter gating. האחוזים של CD3 (תאי B) חיוביים ו-CD19 (תאי T) חיוביים המבטאים ZAP-70, ודגימות בהן יותר מ-10% מאוכלוסיית תאי B מבטאים ZAP-70 נחשבות חיוביות.
נוגדנים רב-שבטיים ממקור ארנבת יוצרו כנגד ZAp-70 אנושי רקומביננטי. מספר נוגדנים חד-שבטיים כגון SB70 ו-SBZAP נוצרו כנגד מקטעים נבחרים של ZAP-70, על ידי חיסון עכברים עם פפטיד סינתטי התואם את הרצף 280-309 של ZAP-70 אנושי. כלומר, נוגדן זה מזהה אפּיטוֹפ הממוקם בין מקטע SH2-C לבין מקטע הקינאזה SH1. השבט (clone) הידוע כ-IE7.2, יוצר מחלבון איחוי התאים לאזור האמור ב-ZAP-70 האנושי הכולל את חומצות האמינו 282-307. השבט 2F3.2 יוצר על ידי שימוש בחלבון האיחוי הכולל את 2 מקטעי SH2, דהיינו את האזור של חומצות אמינו 1-254 של ZAP-70 האנושי. שבט 2F6 התקבל לאחר חיסון עם החלבון הרקומביננטי השלם. השבט L1E5 מגיב עם הקצה ה-N טרמינאלי של החלבון, והוכן עם חלבון סינתטי הקשור ל-hemocyanin מ-keyhole limpet או KLH.
ריאגנטים זמינים אחרים הם נוגדנים חד-שבטיים ממקור ארנבת, כגון שבטים E267, 99F2 ו-136F12 המגיבים ספציפית עם הקצה ה-N-טרמינאלי של ZAP-70. השבט E227 יוצר על ידי שימוש בפוספו-פפטיד סינתטי התואם את השיירים סביב tyr319 והמשמש כאימונוגן, ומזהה רק מולקולות ZAP-70 בהם שייר Tyr319 מזורחן שניתן לגלות בשיטת Western blot ואינן מתאימות ל-flow cytometry. השבט 17A/P-ZAP-70 גם כן מזהה ZAP-70 בו שייר Tyr319 מזורחן, בהבדל ששבט זה ניתן לשימוש הן ב-Western blot וכן ב-flow cytometry. כיום נוהגים לסמן נוגדנים אלה עם הצבע הפלואורסצנטי Alexa Fluor להגברת הסיגנל (Gibbs וחב' ב-Clin Lab Hematol משנת 2005).
הוראות לביצוע הבדיקה
יש לדגום דם למבחנת סודיום הפארין (פקק ירוק), אך מתקבלות גם דגימות שנאספו במבחנת ספירת-דם (פקק סגלגל-EDTA). לא מתקבלות מבחנות עם דם מלא קפוא, דם שנקרש וסורכז, או דגימות המוליטיות באופן בולט, כאשר המוליזה קלה מתקבלת. כמו תיפסלנה דגימות שהגיעו למעבדה למעלה מ-48 שעות מנטילת הדם. יש לצרף לדם אישור על אבחון קודם של CLL, תוצאות של ספירת-דם מלאה (CBC), ואם הדבר מתאפשר יש לצרף גם משטח דם צבוע בצביעת Wright. הדגימות יציבות למשך 24 שעות בטמפרטורת החדר, ו-48 שעות בקירור. דגימות קפואות אינן מתקבלות.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק