מרכיב משלים C1q complement - C1q
| מדריך בדיקות מעבדה | |
| מרכיב משלים C1q | |
|---|---|
| C1q Complement | |
| שמות אחרים | C1 Complement ;Functional C1 ; Hemolytic Complement. |
| מעבדה | כימיה בדם |
| תחום | מפגעים שונים במערכת החיסון |
| טווח ערכים תקין | ביילודים- 9-20 מ"ג /דציליטר (Sonntag וחב' ב- Pediatr Dev Pathol משנת 1998); במבוגרים- 8.0-12.6 מיליגרם/דציליטר. |
| יוצר הערך | פרופ' בן-עמי סלע |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – מערכת המשלים
מטרת הבדיקה
אבחון חסר של המרכיב הראשון (C1) של המשלים; בחינת נבדק עם חסר מוחלט מולד של משלים (CH50); אבחון חסר נרכש של C1 inhibitor. בדיקה זו יכולה להעריך את הסיכון ל-Lupus nephritis ול-Systemic lupus .
מרכיבי המשלים
חלבוני המשלים הם רכיבים במערכת החיסון הטבעית (innate immune system). ישנם שלושה מסלולים בשפעול של מערכת המשלים:
- המסלול הקלאסי
- המסלול האלטרנטיבי או properdin
- מסלול שפעול ה-lectin (הידוע גם כ-MBP או mannan binding protein)
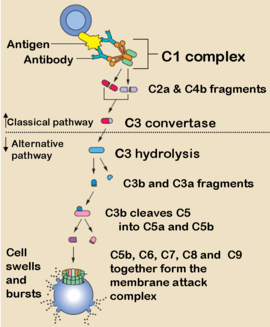
המסלול הקלאסי של מערכת המשלים מורכבת מסדרת חלבונים המשופעלים בתגובה לנוכחות של קומפלקסים חיסוניים. תהליך שפעול זה גורם ליצירה של פפטידים שהם כמוטקטיים לנויטרופילים, והנקשרים לקומפלקסים החיסוניים ולקולטנים של המשלים. התוצאה הסופית של רצף (cascade) שפעול המשלים היא היצירה של קופלקס התקפי ממיס (lytic) הפוגע בממברנת תאים.
הרְכִיב הראשון של המשלים הוא C1 שמורכב משלוש תת-יחידות המסומנות כ-C1r; C1q ו-C1s. הרכיב C1q מזהה ונקשר לאימונוגלובולין הקשור לאנטיגן ומאתחל את ה-cascade של המשלים. חסרים מולדים של איזשהו רכיב מוקדם של רכיבי המשלים (C1-C4) גורמים לאובדן היכולת לייצר את הפפטידים הנחוצים לפנות את הקומפלקסים החיסוניים, וממילא את היכולת לגייס נויטרופילים או לייצר מתקפה ליטית על ממברנת תאים. מטופלים אלה חשופים באופן מוגבר לזיהומים על ידי מיקרואורגניזמים עטופים בקפסולה. המטופלים האחרונים עלולים להיות בעלי תסמינים המרמזים על מחלה אוטו-אימונית, וחסר משלים יכול להיות הגורם האטיולוגי להתפתחות מחלה אוטו-אימונית.
מבנה החלבון C1q
C1q נוצר על ידי תאי אפיתל בעיקר במעיים אך גם בריאות וברקמות אחרות (Cole ו-Colten ב-Complement Biosynthesis משנת 1988). C1q הוא חלבון שמשקלו המולקולארי 460,000 דלטון, והוא מורכב מ-18 שרשרות פוליפפטידיות: שש שרשרות A שכל אחת מהן מכילה 223 חומצות אמינו ובעלת משקל מולקולארי של 26,500 דלטון, שש שרשרות B שכל אחת מהן מכילה 226 חומצות אמינו ובעלת משקל מולקולארי של 26,870 דלטון, ו-שש שרשרות C, שכל אחת מכילה 217 חומצות אמינו ומשקל מולקולארי של 25,660 דלטון. כל אחת משרשרות אלו הכילה קצה N-טרמינאלי גלובולרי שאינו גדילי (helical) קצר המורכב מ-3-9 חומצות אמינו. חומצות האמינו באזור הגדילי של כל אחד מהתלת פפטידים השזורים יחדיו ליצור את האזור הסמוך לקצה ה-N טרמינאלי, מכילות הרבה רצפים בנוסח Gly-X-Y, כאשר X ו-Y הם proline, isoleucine ו-hydroxylysine שיש להם דמיון ניכר לרצפי חומצות האמינו בסיבי קולאגן. זמן מחצית החיים של C1q בצירקולציה הוא בערך 40 שעות, וקצב הסינתזה שלו הוא 140-190 μg/Kg wt/h. בערך 50-75% של C1q נמצאים בכל עת נתונה בצירקולציה (Kohler ב-Immunol Dis משנת 1978).
הקומפלקס C1q הוא multivalent לצורך ההתקשרות שלו עם אתרי קיבוע המשלים (complement fixation) על פני האימונוגלובולינים. אתרי קישור אלה הם המקטע (domain) המוגדר כ-CH2 של IgG, והמקטע CH4 של IgM. הרצף הפפטידי הרלוונטי באתרי הקישור של האימונוגלובולינים אליהם נקשר המשלים יכולים להיחשף בעת יצירת הקומפלקס אימונוגלובולין-אנטיגן, או שאתרים אלה חשופים באופן תמידי ונגישים לקישור המשלים. עם זאת, אתרי קישור אלה דורשים כנראה קישור של מולקולות C1q רבות כדי להשיג את הזיקה המרבית הדרושה לפעילות המשלים. C1q נקשר לאימונוגלובולין בקומפלקסים חיסוניים, כאשר עוצמת קישור זה היא החזקה ביותר ל-IgM ובסדר עוצמת קישור יורדת של IgM˃IgG3˃IgG1˃IgG2, אך C1q אינו נקשר ל-IgA ל-IgE או ל-IgG4. משפעלים לא אימונולוגיים של C1q כוללים DNA,IgG הקשור ל-staphylococcal protein A, קומפלקסים של CRP עם פוליסכרידים, ממברנות של מבנים תוך-תאיים כמו מיטוכונדריה, מספר נגיפים בעלי מעטפת, גבישים מסוג monosodium urate האופייניים לצינית (gout), וכן על ידי lipid A של ליפו-פולי-סכרידים (Volanakis ב-Ann NY Acad Sci משנת 1982).
תפקוד C1q
C1q היא מולקולת הזיהוי במסלול הקלאסי של מערכת המשלים, וביחד עם C1r ו-C1s היא יוצרת את הקומפלקס C1, החיוני בהכרת קומפלקסים חיסוניים ובשפעול של מערכת המשלים. C1q מיוצר בעיקר על ידי תאי אפיתל, מקרופאגים ותאים דנדריטים בלתי בשלים, ויש מספר ליגנדים מהנקשרים אליו כגון IgM, קומפלקס של IgG, וכן DNA ו-CRP (על פי van Schravendijk וחב' ב-Mol Immunol משנת 1982, ו-Jiang וחב' באותו כתב עת משנת 1991). בהקשר של אוטו-אימוניות, ליגנד חשוב נוסף נמצא על פני תאים אפופטוטיים ונמקיים (Korb וחב' ב-J Immunol משנת 1997, וכן Trouw ו-Ahearn ב-Mol Immunol משנת 2008, ו-Nauta וחב' ב-Eur J Immunol משנת 2002). לכן C1q חשוב לפינוי של תאי נמק או תאים אפופטוטים מהצירקולציה (Walport ב-N Eng J Med משנת 2001).
בנוסף לתפקידו בתהליך הרחקת תאים מתים, מייחסים ל-C1q תפקיד במודולציה של התגובה החיסונית ההסתגלותית (adaptive) (על פי Fossati-Jimack וחב' ב-Mol Immunol משנת 2008, וכן Baruah וחב' ב-Blood משנת 2009, ו-Jiang וחב' ב-Clin Exp Immunol משנת 2003). במקובץ, נתונים אלה מצביעים על כך שחסר של C1q עלול לא רק לגרום לזיהומים, אלא גם לתגובות אוטו-אימוניות, כיוון שהפינוי של אוטו-אנטיגנים עלול להיפגם וכן עלול להביא לפגיעה בתגובה החיסונית ההסתגלותית (Santer וחב' ב-J Immunol משנת 2010). ברוב המטופלים עם חסר C1q, האירוע הקליני נטה להיות SLE, בעוד שבמיעוטם נמצאה נטייה לזיהומים חוזרים כגון מנינגיטיס (Vassallo וחב' ב-Rheumatol משנת 2006). עד שנת 2015 התגלו באתר 1p34-1p36.3, 16 מוטציות nonsense ו-missense המופיעות באחד משלושת השרשרות של C1q.
רוב חלבוני המשלים בצירקולציה מסונתזים בכבד, אם כי נתונים מאז שנות ה-80 של המאה ה-20 מספקים הוכחות לכך שחלק מחלבוני המשלים מסונתזים מחוץ לכבד על ידי תאים משופעלים וכאלה שאינם משופעלים. בין החלבונים המסונתזים באופן מקומי, תופס C1q מקום מרכזי ממספר סיבות. ראשית, הוא מסונתז בעיקר על ידי תאים מציגי-אנטיגן כמו מונוציטים, מקרופאגים ודנדריטים. שנית, C1q מעוגן באופן זמני לפני התאים על ידי מקטע טרנס-ממברנלי הממוקם בשרשרת A של C1q, לפני שהוא מבוקע ומופרש לתוך האזור העוטף את התא. כתגובה, C1q הקשור לתא מסוגל לחוש במפגעים מסוכנים דרך המקטעים הגלובולריים שבראש המולקולה הנקשרים לאנטיגנים מגוונים. אך חשוב יותר ש-C1q המסונתז באופן מקומי, יכול להשרות תפקודים ביולוגיים רבים על ידי שהוא מסמן לשחרור מולקולות הגורמות למודולציה אימונית שיכולה להביא לאיתות פאראקריני או אוטוקריני באופן הדומה לפעולת TNFα. בהתאם גורם C1q לפגוציטוזיס, אנגיוגנזה, אפופטוזיס, ומשרה הפרשת ציטוקינים החיוניים למודולציה של תגובה דלקתית.
חסר של C1q
המקרה הראשון של מטופל עם חסר C1q דווח בשנת 1979 על ידי Berkel וחב' ב-Clin Exp Immunol, ועד שנת 2014 נרשמו בסך הכול כ-70 מקרים בעולם עם מוטציות שונות בקבוצות אתניות שונות (McAdam וחב' ב-Immunogenetics משנת 1988, ו-Schejbel וחב' ב-Genes Immun משנת 2011 ו-Jlajla וחב' ב-Immunology משנת 2014).
הטיפול באלה עם חסר C1q היה בין השאר בעירוי של פלזמה קפואה המכילה C1q, שהביא לשיפור קליני ולא גרם לתגובה של הופעת נוגדנים כנגד C1q (Tapaloglu וחב' ב-Clin Rheumatol משנת 2012, ו-Mehta וחב' ב-Rheumatol משנת 2010). בהתבסס על התצפית שנתן לשחזר את רמות C1q על ידי השתלת מח עצם בעכברים מחוסרי C1q (Cortes-Hernandez וחב' ב-J Immunol משנת 2004, ו-Petri וחב' באותו כתב עת משנת 2001), בוצעה השתלה של תאי-גזע המאטו-פוייטיים ב-2 מטופלים שוודיים ובאנגלי אחד, החסרים C1q, ונמצא שבשלושתם שוקמו רמות C1q, כמו גם חל שיפור בתסמינים הקליניים שלהם (Olsson וחב' ב-Bone Marrow Transplant משנת 2013, ו-Arkwright וחב' ב-Clin Immunol משנת 2014). במעקב אחר שלושת מטופלים אלה, שניים מתוכם הגיבו יפה, ואילו אחד נפטר משטף-דם מוחי וכשל רב-מערכתי. הסיכון בהשתלת תאי-גזע אלה מוגבר במטופלים עם מחלה אוטו-אימונית מתקדמת, או באלה עם נטייה לזיהומים נשנים.
חסר מולד של C1q הוא נדיר, והוא כרוך בדרך כלל עם מחלות בהן יש היארעות מוגברת של קומפלקסים חיסוניים כגון SLE (Walport וחב' ב-Immunology משנת 1998), פולימיוזיטיס, גלומרולונפריטיס, ו-IgA nephropathy (או Henoch-Schonlein pupura), כאשר SLE הוא התרחיש עם החסר השכיח ביותר של C1. כמו כן SLE הכרוך בחסר של C1 דומה ל-SLE ללא חסר במשלים, אלא שהוא בא לביטוי בגיל שלפני הבשלות המינית. רמות נמוכות של C1 נמצאו גם במטופלים עם רמה נמוכה של אימונוגלובולינים או בחולים עם SCID, וזאת כנראה כתוצאה מקטבוליזם מוגבר של המשלים. רמות משלים יכולות להימדד בשיטות אימונולוגיות עם נוגדנים כנגדו. לגבי רוב החלבונים המרכיבים את המשלים, זוהה מספר קטן של מקרים בהם החלבון אמנם קיים, אך הוא פגום ואינו פונקציונאלי. במקרים נדירים אלה יש צורך במבחן תפקודי של המשלים כדי להסביר את החסך בפעילותו הביולוגית.
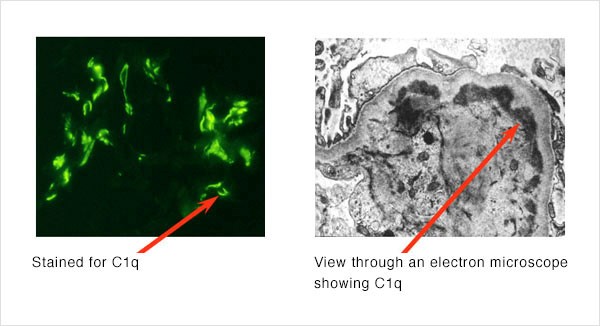
C1q nephropathy
מדובר במחלת כליות עם פרוטאינוריה בולטת, והיא אחת התוצאות של תסמונת נפרוטית. ב-C1q nephropathy מוצאים בבדיקה מיקרוסקופית של ביופסיה כלייתית כמות ניכרת של C1q צמודה לאזורים נרחבים בכליות, C1q nephropathy היא מחלה שהתגלתה מאוחר יחסית ויש לה דמיון לשני מפגעים כלייתיים אחרים התורמים לתסמונת נפרוטית, הידועים כ-MCD או minimal change disease ו-FSGS או focal segmental glomerulosclerosis. המנגנון הגורם לשקיעה של C1q בכליות אינו ברור, אך יש סברה שמשקעים אלה של C1q משפעלים את מערכת החיסון בכליות עצמן, כאשר התגובה החיסונית המקומית והדלקת המלווה אותה גורם לנזק כלייתי. למרות שמפגע כלייתי שכיח יותר בשנות הילדות, מוצאים לאחרונה יותר מקרים בשנות הבחרות המאוחרות ואף במבוגרים בגיל הביניים. התסמין הבולט ביותר של C1q nephropathy היא בצקת המתחילה ברגליים, אך יכולה לעלות בהמשך לאזור הירך העליונה ולבטן. ממצאים נוספים הם יתר לחץ-דם, רמת כולסטרול מוגברת ונטייה להיפר-קואגולציה. רמות נמוכות של C1q יכולות להופיע במטופלים עם angioedema נרכשת, עם vasculitis מושרה על ידי קומפלקס חיסוני, עם קרצינומה או לימפומה. C1q nephropathy מתגלה על ידי הופעת משקעים בבדיקה מיקרוסקופית של חומר הנלקח בביופסיה. כמחלה, C1q nephropathy דומה מאוד לשתי מחלות כליה אחרות, minimal change disease ו-focal segmental glomerulosclerosis או FSGS.
אינטרפרטציה
רמות נמוכות של משלים יכולות להיגרם מתוצאה מחסרים תורשתיים, נרכשים או כתוצאה מניצול-יתר של המשלים (כתוצאה מזיהומים או תרחישים אוטו-אימוניים). המדידה של פעילות C1q היא אינדיקטור של הכמות המצויה של מרכיב המשלים הראשון (C1). רמות מעטות ביותר של C1q בנוכחות של רמות נורמליות של C3 ושל C4, מתאימות לחסר של C1. רמות נמוכות של C1q בנוכחות של רמה נמוכה של C4 ורמה תקינה של C3, יכולות להעיד על נוכחות של מעכב נרכש (נוגדן עצמי) כנגד C1 esterase inhibitor. רמה בלתי ניתנת לגילוי של C1q בנוכחות חסר של סך-משלים (CH50), ובנוכחות רמה תקינה של C3, C2 ו-C4 מצביעות על חסר מולד של C1. רמה נמוכה של C1q בשילוב עם רמה נמוכה של C1 inhibitor ורמה נמוכה של C4, מצביעה על חסר נרכש של C1 inhibitor. רמות מוגברות של C1q נמצאו במצב של kala azar (שהיא הדבקה עם Leishmania donovani על פי Krager וחב' ב-Clin Immunol Immunopathol משנת 1982).
כמו בצורה השכיחה יותר של חסר C2, חסר C1 כרוך בשכיחות גבוהה יותר של מחלות של יצירת קומפלקס חיסוני כגון SLE, פולימיוזיטיס, גלומרולונפריטיס ו-Henoch-Schonlein purpura. רמות נמוכות של C1 דווחו גם באנשים עם רמות לא תקינות של אימונוגלובולין כגון תסמונת Bruton (hypogammaglobulinemia) או באלה עם SCID, זאת בעיקר בגין קטבוליזם מוגבר (Frank ב-N Eng J Med משנת 1987, Frank ב-Pediatr Clin North Am משנת 2000). חסר ב-inhibitor C1 כרוך גם התופעה של angioedema (Frigas ב-Mayo Clin Proc משנת 1989).
C1q ומחלה נוירו-דגנרטיבית
החלבון C1q המצטבר במוח בריא אך מזדקן עלול לגרום לבעיות זיכרון כפי שמוצאים במחלת אלצהיימר. על פי Barres וחב' ב-J Neurosci משנת 2013, C1q מצטבר בסינפסות של מוחות מזדקנים, ובחינה שלאחר המוות של מוחות עכברים ובני-אדם, מצאה עלייה של פי-300 ברמת C1q בהזדקנות מוחות. מחקר זה מצא שקיעה בולטת במיוחד של C1q בתאי הסינפסות, ועל פי Barres תגובה אוטו-אימונית כנגד C1q במוח עלולה לגרום נזק מקומי. נמצא שאזורי המוח הראשונים בהם יש הצטברות גבוהה של C1q הם ההיפוקמפוס וה-substantia nigra, המועדים לנזק נוירו-דגנרטיבי במחלות אלצהיימר ופרקינסון. אזור נוסף המושפע על ידי הצטברות C1q הוא ה-piriform cortex הכרוך עם חוש הריח האובד בהדרגה במחלה נוירו-דגנרטיבית. על פי Webster וחב' ב-J Leukoc Biol משנת 2000, גם תאי מיקרוגליה המכילים את הקולטן C1qR(P), יכולים להחיש את תהליכי הפגוציטוזה של C1q אל תוך תאים אלה.
המסלולים הקלאסי והאלטרנטיבי של המשלים
משערים שהקצוות הגלובולאריים של C1q הם האתרים של הקישור ה-multi-valent לאתרי קיבוע המשלים של האימונוגלובולינים הנמצאים בקומפלקס האימוני. חולים עם SLE הם לרוב בעלי חסר C1q, אך חסר גנטי של C1q נדיר ביותר אם כי ב-90% מהמקרים הללו סבלו גם מ-SLE. ישנם הסבורים ש-Cq1 הוא בעל תפקיד מרכזי בהזדקנות תאים.
השפעול של המשלים מתחיל על ידי קישורו של המרכיב C1q לקומפלקס אנטיגן-נוגדן. קישור זה מוביל לשפעול של תת-יחידות C1R ו-C1S. תת היחידה המשופעלת C1S מבקעת את הפפטידים C4 ו-C2 של המשלים, ליצירה של האנזים C3 convertase הקלאסי הקשור לממברנה, ולאחר מכן ליצירה של C5 convertase מה שגורם לביקוע של מרכיב C5 של המשלים לקראת המתקפה על הממברנה ולהרס התא.
הקולטנים של C1q
לפחות סוג אחד של אתר קישור על פני C1q לקולטן שלו ממוקם באזור הקולאגן של C1q והוא ממוסך באופן נורמאלי על ידי C1r ו-C1s. ברגע ש-C1q נקשר למשפעל שלו, C1r ו-C1s מותמרים לסרין פרוטאזות פעילים, מה שמאתחל את מסלול הקלאסי של המשלים. כתוצאה מכך הרגולציה על ידי מעכב של C1 גורמת להיפרדות של C1r ו-C1s מ-C1q, מה שהופך את אתר הקישור על פני C1q לזמין בהתקשרות עם קולטנו. מספר חלבונים זוהו כמועמדים להוות קולטנים של C1q על פני התא (Eggleton וחב' ב-Trends Cell Biol משנת 1998).נראה שיש יותר מקולטן פיזיולוגי אחד ל-C1q, אם לוקחים בחשבון את מגוון הפונקציות שממלא C1q, המפורטות להלן:
- הגברת פגוציטזיס של חלקיקים שעברו אופסוניזציה על ידי נוגדנים
- הגברת הקישור של קומפלקסים אימוניים לתאי מזנגיום כלייתיים או לתאי אנדותל
- מודולציה של טוקסיות לתאים או של פגוציטוזיס התלויים ב-FcR
- עידוד מטבוליזם חמצוני על נויטרופילים ותאי שריר חלק וסקולאריים
- הגברת הרג של חיידקים כגון Schistosomula ,Cryptococcus neoformans ואחרים
- הגברת הביטוי על פני טסיות דם של מולקולות ספיחה כגון α2/β3 integrins, וכן את הביטוי של E-selectin, ICAM-1 ו-VCAM-1 על פני תאי אנדותל
- הגברת הפרשת אימונוגלובולינים מלימפוציטים מסוג B
- פינוי של תאים אפופטוטיים והגנה מפני אוטו-אימוניות
- מודולציה של תגובה חיסונית הומוראלית, על ידי השפעה על פרופיל הציטוקינים של לימפוציטים מסוג T הרגישים לאנטיגן
- עידוד אפופטוזיס המושרה על ידי נוגדנים, של תאי מזנגיום מפקעיות של כליות חולדה בתרבית
- עידוד תעלות +K המשופעלות על ידי 2+Ca, ואִתחול כימוטקסיס של פיברובלסטים מעכבר
- השריית סינתזת DNA ושגשוש של פיברובלסטים דיפלואידים של אדם
C1qRp - קולטן של C1q המגביר פגוציטוזה
קולטן של C1q המגביר את היכולת של פגוציטים לבצע פגוציטוזה זוהה כ-C1qRp, שמשקלו המולקולארי הוא 126,000 דלטון. הביטוי של קולטן זה מוגבל לתאים מייאלואידים, לטסיות-דם, ולתאי אנדותל, ונוגדנים חד-שבטיים המגיבים עם קולטן זה מעכבים את יכולת הפגוציטוזה המושרית על ידי C1q (כמו גם על ידי maltose binding protein). רצף חומצות האמינו של קולטן זה, מצביע על כך שקולטן גליקופרוטאיני ממברנאלי זה (העשיר באוליגוסכרידים הקשורים בקשר-O לחלבון) הוא חלבון type 1 ממברנאלי המכיל 631 חומצות אמינו הייחודי בכך שהוא מכיל מקטע הומולוגי למקטע שמוצאים בלקטינים type C קושרי סוכר (שהוא motif משותף לעוד מספר חלבונים הקשורים לאנדוציטוזה) על פי Nepomuceno וחב' ב-Immunity משנת 1997. למרות שאינטראקציה ישירה בין C1q לקולטן שלו C1qRp לא הודגמה פורמלית (כיוון שהעיכוב של תפקודי C1q על ידי נוגדנים חד-שבטיים ל-C1qRp פורש כחסימת האינטראקציה C1q-C1qRp), נראה שהאינטראקציה בין C1q לבין C1qRp מעודדת פגוציטוזה ללא השרייה של הפרשת ציטוקינים מעודדי-דלקת, וכך קישור יכול לספק בסיס לתרפיה אנטי-מיקרוביאלית ללא תגובה דלקתית. הפוטנציאל לשדרוג הפעילות הפגוציטית יכול להוות גישה פרופילקטית שימושית באנשים עם מערכת חיסון פגועה מסיבה גנטית, מסיבת גיל, או כתוצאה מטיפול בתכשירים מדכאי-חיסון.
ביטוי של CD93
החלבון CD93 או Cluster of Differentiation 93, מקודד באדם על ידי הגן CD93 (Napomucena וחב' ב-Immunity משנת 1997, ו-Webster וחב' ב-J Leukoc Biol משנת 2000). CD93 הוא קולטן טרנס-ממברנלי מסוג C-type lectin, המשחק תפקיד לא רק בתהליכי הספיחה הבינתאית, אלא גם בהגנת הפונדקאי. משפחת xiv-C-type, מכילה 2 מרכיבים נוספים, endosialin ו-thrombomodulin, שהוא נוגד קרישה מוכר. כל חברי משפחה זו מכילים מקטע של לקטין C-type, סדרה של מקטעים דמויי epidermal growth factor, מקטע דמוי-mucin העשיר מאוד בסוכרים, מקטע טרנס-ממברנלי ייחודי וזנב ציטופלזמטי קצר. בגלל ההומולוגיה החזקה ביניהם וקרבתם הרבה על כרומוזום 20, עלתה הסברה ש-CD93 נוצר מהגן המקודד ל-thrombomudulin על ידי תהליך דופליקציה.
CD93 זוהה במקור בעכברים כסמן מוקדם של תאי-B על ידי שימוש בנוגדן החד-שבטי AA4.1 (McKearn וחב' ב-J Immunol משנת 1984, ו-Zekavat וחב' ב-Immunogenetics משנת 2010). בהמשך, מולקולה זו נמצאה מבוטאת על פני תאים באוכלוסייה מוקדמת של תאי-גזע המאטו-פויאטיים, מהם נוצר הספקטרום השלם של תאים בשלים בדם. CD93 מוכר בשל הביטוי שלו על פני מגוון רחב של תאים כגון טסיות, מונוציטים, תאי מיקרוגליה ותאים אנדותליאליים. במערכת החיסון, CD93 מבוטא גם על פני נויטרופילים, מקרופאגים משופעלים, וקודמנים של תאי-B עד לשלב T2 בטחול, תת קבוצה של תאים דנדריטים ושל killer cells. אפיון מולקולרי של CD93 גילה שחלבון זה זהה ל-C1qRp, שהוא הקולטן של C1q (McGreal וחב' ב-J Immunol משנת 2002). נמצא שנוגדנים כנגד C1qRp מפחיתים משמעותית את תהליך הפגוציטוזה המושרה על ידי C1q. מחקר עדכני יותר מאשר ש-C1qRp זהה ל-CD93, אך מחקר זה לא הצליח להדגים אינטראקציה ישירה בין CD93 ו-C1q בתנאים פיזיולוגיים.
תפקידו של CD93
הסברה ש-CD93 הוא הקולטן של C1q נחלשה, ומניחים ש-CD93 קשור לספיחה הבינתאית ובפינוי של תאים שעברו אפופטוזיס. הזנב הציטופלזמטי של CD93 מכיל שני מקטעים משומרים ביותר שעשויים להיות קשורים בתפקוד של CD93. אכן, החלק החוץ-תאי הטעון מאוד של CD93 נמצא מגיב עם moesin, חלבון המשחק תפקיד בקישור של חלבונים טרנס-ממברנליים ל-cytoskeleton. תהליך זה חיוני הן לספיחת תאים, נדידתם ולפגוציטוזה. בהקשר של התמיינות של אי-B מאוחרים, CD93 חשוב לשמירת טיטר גבוה של נוגדנים לאחר החיסון ולהישרדות ארוכת הטווח של תאי פלזמה במח העצם.
נוגדנים עצמיים כנגד C1q
מכל הנוגדנים העצמיים המכוונים כנגד חלבוני המשלים, הנוגדנים העצמיים כנגד C1q קבלו את מירב תשומת הלב (Norsworthy ו-Davis ב-Mol Biotechnol משנת 2003). C1q שהיא המולקולה הראשונה במסלול הקלאסי לשפעול המשלים, הוא בעל יכולת ייחודית לקשור את זנב ה-Fc של נוגדנים מסוג IgG ו-IgM (Daha וחב' ב-Mol Immunol משנת 2011). הקישור של C1q עם מולקולת IgG בודדה או למולקולת IgM שאינה נמצאת בצימות עם האנטיגן, הוא חלש. העובדה ש-C1q יכול לקשור IgG בקומפלקסים אימוניים יכולה להיחשב כמעלה אך גם כחיסרון. היתרון נעוץ בעובדה שהזיהוי של נוגדנים כנגד C1q הוא פועל יוצא של מחקרים על גודלם של קומפלקסים אימוניים המסוגלים להיקשר ל-C1q. במחקרים אלה התגלה שבמטופלים עם SLE, גם קומפלקסים אימוניים קטנים יכולים להיקשר על ידי C1q (Angello וחב' ב-J Exp Med משנת 1971). בשנים שלאחר מכן התגלה שגם מולקולות מונומריות של IgG שאינן נמצאות בקשר עם אנטיגנים הגיבו עם הזנב דמוי הקולגן של מולקולת C1q (Antes וחב' ב-Arthritis Rheumatol משנת 1988). החיסרון קשור לעובדה שצריך להבדיל בין IgG בקומפלקסים האימוניים הקשור ל-C1q לבין נוגדנים עצמיים כנגד C1q הנקשרים למולקולה זו (Kohro-Kawata וחב' ב-J Rheumatol משנת 2002). בעיה אחרונה זו יכולה להיפתר על ידי הוספה של 1M NaCl לבּופר ההדגרה במבדק. בתנאי מולאריות זו האינטראקציה החלשה בין המקטעים הגלובולאריים שבראש מולקולת C1q לבין מקטע CH2 של זנבות Fc של IgG נהרסת לחלוטין, בה בשעה שהקישור בזיקה גבוהה בין נוגדנים עצמיים ל-C1q לזנב דמוי הקולאגן של C1q נותר חזק כשהיה.
מבדקים לזיהוי נוגדנים עצמיים כנגד C1q
המבדקים המקוריים עשו שימוש בציפוי ישיר כבר בשלבים המוקדמים של ניסויים לגילוי נוגדנים עצמיים ל-C1q התגלה שרוב הנוגדנים הללו מכוונים כנגד המקטע דמוי הקולאגן במולקולת C1q. מבחני תצפיות שהראו שנוגדנים כנגד C1q יכולים להימצא גם בנוכחות של מולקולות חופשיות של C1q בצירקולציה, אך ב-2007 דווח על ידי Tsacheva וחב' ב-Mol Immunol שהם גם נוגדנים המגיבים ספציפית כנגד האזור הגלובולארי בראש מולקולת C1q. קיימים מספר מבדקים לזיהוי נוגדנים כנגד C1q. מבדקים אלה מבוססים בעיקר על טכנולוגית ELISA ומשווקים על ידי Bühlman Lab בשוויץ, IMTEC ו-Orgentec בגרמניה, כמו גם Inova diagnostics בסן -דייגו. מערכת ALGERIA היא שיטה חצי-כמותית אוטומטית המבוססת על רצועות של פלטת מיקרו-טיטר. אחדים מהמבדקים לקביעת נוגדנים כנגד C1q שימשו בהקשרים קליניים (Trendelenburg וחב' ב-Nephrol Dial Transplant משנת 2006, ו-Heidenreich וחב' ב-Lupus משנת 2009, וכן Meyer וחב' ב-Arthritis Res Ther משנת 2009 ו-Cai וחב' ב-J Rheumatol משנת 2010). ה-FDA לא אישר שיטות אלו בגלל היעדר מחקרים פרוספקטיבים או מחקרים המשווים בין השיטות השונות. לנוגדנים עצמיים כנגד C1q יש כמעט 100% של ערך ניבוי שלילי (npv) להתפתחות של לופוס נפריטיס חמורה.
הוראות לביצוע הבדיקה
עדיף להיות בצום של 8-12 שעות. יש לדגום את הדם למבחנה כימית (פקק אדום או צהוב), אך גם למבחנת ספירת דם (EDTA עם פקק סגלגל) . מיד לאחר הוצאת הדם יש לשמור את המבחנה בקירור בפתיתי קרח. לאחר סרכוז בצנטריפוגה מקוררת יש להפריד את הנסיוב מהדם הקרוש, ולהקפיא את הנסיוב המופרד במהירות. הנסיוב יציב בטמפרטורת חדר למשך 4 ימים, בקירור למשך 10 ימים, ובהקפאה עד 21 יום. יש לפסול את הדגימה כאשר הנסיוב מאוד המוליטי, מאוד ליפמי או מאוד איקטרי. בדרגות מתונות של שלושת הפרמטרים הללו הבדיקה ניתנת לביצוע. אין לקבל דגימות נסיוב שהופרדו במבחנות ג'ל. הבדיקה מתבצעת בשיטה טורבידימטרית וכן נפלומטרית. הבדיקה מתבצעת בשיטת semi-Quantitative Enzyme-Linked Immunosorbent Assay או בשיטת Radial Immunodiffusion (RID).


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק