אינטרלויקין 5 Interleukin
| מדריך בדיקות מעבדה | |
| אינטרלויקין 5 | |
|---|---|
| Interleukin 5 | |
| שמות אחרים | IL-5, EDF, BCDFII, TRF, eosinophil differentiation factor, T-cell ,replacing factor B cell differentiation factor I. |
| מעבדה | ביוכימיה בדם |
| תחום | ציטוקין המעורב בתפעול מערכת החיסון |
| טווח ערכים תקין | ריכוז ערכים ממוצע של IL-5 במבוגרים הוא 4.4 פיקוגרם/מ"ל בטווח שבין 2.99 ל-6.51 פיקוגרם/מ"ל. ממוצע ערכים בילדים בטווח הגילים שבין 5-15 שנה, 0.544 פיקוגרם/מ"ל. על פי Mayo Clinib Labs הטווח התקין בילדים נמוך מ-1 פיקוגרם/מ"ל. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
הערכה של מפגעים הכרוכים עם היפר-אאוזינופיליה, ובירורים הקשורים לאבחון וניטור אסתמה.
המבנה של IL-5
IL-5 הוא פוליפפטיד בן 134 חומצות אמינו ומשקל מולקולרי של 12,500 דלטון. IL-5 מופרש על ידי מספר מוגבל של תאים מזנכימאליים (Yokuta וחב' ב-Proc Natl Acad Sci USA משנת 1987 ו-Tavernier וחב' ב-DNA משנת 1989). בצורתו הטבעית, IL-5 בשל מסונתז כמולקולה בת 115 חומצות אמינו, שהיא מונומר בגודל 22,000 דלטון, עם שיירים סוכריים מאוד נרחבים, היוצר עם מונומר זה הומודימר במשקל מולקולרי של 40-50,000 דלטון עם קישור די-סולפידי (Proudfoot וחב' ב-Biochem J משנת 1990). ל-IL-5 מונומרי אין כל פעילות, כאשר ההומודימר נדרש לפעילות הביולוגית (Takatsu ו-Tominaga ב-Prog Growth Factor Res משנת 1991). זאת בניגוד לציטוקינים IL-3 ו-GM-CSF הקיימים רק כמונומרים (Schrader ב-Ann Rev Immunol משנת 1986, ו-Wong וחב' ב-Science משנת 1985). הומודימר אחד של IL-5 נקשר לקולטן בודד אחד, והוצע שדימר של IL-5 עובר שינויי מבנה לאחר שהוא נקשר לקולטן בודד, ושינוי מבנה זה מאפשר קישור לקולטן נוסף (Verschelde וחב' ב-FEBS Lett משנת 1998). קיימת הומולוגיה של 71% בין חומצות האמינו של אדם ועכבר (Azuma וחב' ב-Nucleic Acid Res משנת 1986, ו-Kinashi וחב' ב-Nature מאותה שנה). בעוד ש-IL-5 ממקור עכבר פעיל מאוד על תאי אדם, IL-5 ממקור אדם פעיל רק באופן שולי בתאי עכבר (Plaetinck וחב' ב-J Exp Med משנת 1990).
ביטוי רקמתי של IL-5
הגן המקודד ל- IL-5 ממוקם על כרומוזום 11 בעכבר, ועל כרומוזום 5 באדם (בעמדה 5q31.1), בקרבת הגנים המקודדים לציטוקינים ,IL-3 IL-4 ו-GM-CSF (Lee וחב' ב-Somat Cell Mol Genet משנת 1989, ו-van Leeuwen ב-Blood מאותה שנה), שגם הם מבוטאים תדירות יחדיו על ידי תאי TH2. הגן מכיל 6 אקסונים. IL-5 מבוטא על ידי אאוזינופילים (Dubucquoi וחב' ב-J Exp Med משנת 1994), וכן נתגלה בשיטות אימונו-היסטוכימיות בתאי פיטום של דרכי האוויר בחולי אסתמה (Bradding וחב' ב-Am J Respir Cell Mol Biol משנת 1994). הביטוי של IL-5 מווסת על ידי מספר פקטורי שעתוק (transcription factors) כולל GATA3 (Kaminuma וחב' ב-Int Arch Allergy Immunol משנת 2005).
משמעות קלינית
IL-5 נכרך עם גרימת מספר מחלות אלרגיות כולל אסתמה ו-allergic rhinitis, בהן מוצאים עלייה במספרם של אאוזינופילים בדרכי האוויר ובכיח (Shen וחב' ב-J Immunol משנת 2003). בהתחשב בהתאמה הגבוהה בין מספר האאוזינופילים והפתולוגיה של אסתמה אלרגית, נולדה ההשערה שאאוזינופילים הם בעלי תפקיד מרכזי במנגנון הקשור לאסתמה (Sanderson ב-Blood משנת 1992). תאים אלה הם תוצר סופי של התמיינות גרנולוציטים הנמצאים ברוב היונקים. תפקידם העיקרי של אאוזינופילים בבריאות מלאה, הוא בפינוי של טפילים עליהם ספוחים נוגדנים, על ידי שחרור של חלבונים ציטוטוקסיים מתוך גרנולות התאים (Giembycz ו-Lindsay ב-Pharmacol Rev משנת 1999). כיוון שאאוזינופילים הם התאים העיקריים המבטאים את הקולטן IL-5Rα, אין זה מפתיע שהם מגיבים ל-IL-5. למעשה, IL-5 שהתגלה במקור כ-eosinophil colony stimulating factor (Lopez וחב' ב-J Exp Med משנת 1986), הוא מווסת מרכזי של הצטברות אאוזינופילים ברקמות, ואף עשוי להיות מודולטור של התנהגות האאוזינופיל בכל שלב מהבשלות ועד להישרדות. אכן, הנוגדן החד-שבטי mepolizumab המכוון כנגד IL-5, יכול להפחית אאוזינופיליה מוגזמת. בלימפומה ע"ש Hodgkin, האאוזינופיליה האופיינית הנצפית במפגע זה, מיוחסת ליצירה מוגברת של IL-5 (Di Biagio וחב' ב-Int Arch Allergy Immunol משנת 1996).
הקולטנים של IL-5
הקולטן של IL-5 שייך למשפחת type I cytokine receptors, והוא הטרודימר כאשר אחד המונומרים הוא subunit IL-5 receptor α, והמונומר השני הוא CSF2Rβ, דהיינו הקולטן מורכב משרשרת α ומשרשרת βc (Tavernier וחב' ב-Cell משנת 1991). תת היחידה α ספציפית למולקולת IL-5 (Woodcock וחב' ב- EMBO J משנת 1994, Johanson וחב' ב-J Biol Chem משנת 1995 ו-Murata וחב' ב-J Exp Med משנת 1992), ואילו תת היחידה βc מזוהה גם על ידי IL-3 וכן על ידי GM-CSF (Takaki וחב' ב-J Exp Med משנת 1993), והיא מכילה מקטעים (domains) המשמשים להעברת איתותים. הגליקוזילציה של השייר Asn196 של תת היחידה Ra חיונית לקישור של IL-5 לקולטן שלו.
תת-יחידה α: שרשרת IL-5Rα מבוטאת על ידי אאוזינופילים, חלק מהבזופילים, וכן על ידי תאי B1 או על ידי קודמנים של תאי B בעכברים. בדומה לקולטנים של ציטוקינים רבים אחרים, התהליך של alternative splicing של הגנים המקודדים לשרשרות α, גורם לביטוי של צורה הקשורה לממברנה או לצורה מסיסה של שרשרות bα. הצורה המסיסה אינה קשורה להעברת האיתותים, ולכן יש לה השפעה אנטגוניסטית על האיתות שאמור להיות מועבר על ידי IL-5 בהיקשרו לקולטן שלו על פני הממברנה. שתי הצורות המונומריות של IL-5Rα הם קולטנים בזיקה נמוכה, אך בדימריזציה עם שרשרות β נוצר קולטן עם זיקה גבוהה. בכל מקרה, שרשרת α קושרת IL-5 באופן בלעדי, והחלק התוך-ציטופלזמי של IL-5Rα קשור ל-Janus kinase 2 (להלן (JAK2, שהוא טירוזין קינאז החיוני להעברת האיתות של IL-5 (Milburn וחב' ב-Nature משנת 1993 ו-Quelle וחב' ב-Mol Cell Biol משנת1994 ).
תת-יחידה β: תת-יחידה זו אחראית להעברת האיתות, ומכילה מספר מקטעים תוך תאיים. בניגוד לשרשרת α, שרשרת β אינה קושרת IL-5, אינה ספציפית לציטוקין זה, והיא מבוטאת באופן מעשי בכל הלויקוציטים. למעשה, תת היחידה β של הקולטן ל-IL-5 נמצאת גם בקולטנים של IL-3 ושל GM-CSF, שם היא קשורה עם תת היחידות IL-3Rα ו-GM-CSFRα. לכן, תת היחידה β ידועה כקולטן β הכללי או כ-βc. בדומה לתת היחידה IL-5Rα, גם המקטע הציטופלזמי של תת היחידה β קשור באופן קונסטיטוטיבי עם JAK2, כמו גם עם Lyn, שאף הוא טירוזין קינאז, כאשר שני האחרונים חיוניים להערת האיתות של IL-5 (Ogata ב-Blood משנת 1998).
פיזיולוגיה של IL-5
IL-5 הוגדר במקור כ-"T-cell replacing factor", המופרש מתאי T לגרות יצירת נוגדנים מתאי B משופעלים (Takatsu וחב' ב-J Immunol משנת 1980). IL-5 מיוצר על ידי תאי Th2 לאחר גירוי על ידי חיידקים דוגמת M. tuberculosis או Toxocara canis או על ידי אלרגנים ועל ידי תאי פיטום ((mast cells אחר גירוי עם הקומפלקס אלרגן-IgE (Takatsu וחב' ב-Growth Factors & Cytokines in Health & Disease משנת 1997). בצורתו הפעילה, IL-5 הוא הומודימר, שה-mRNA שלו מבוטא באאוזינופילים, בתאי γδT ובתאי NK ו-NKT וכן בתאים שאינם המטו-פויאטיים (Desreumaux וחב' ב-J Exp Med משנת 1992, Moon וחב' ב-J Immunol משנת 2004, Sakuishi וחב' באותו כתב עת משנת 2007, ו-Takatsu וחב' ב-Adv Immunol משנת 1994). תאי -CD3ε, -c-kit, -CD4 ותאי +IL-2Rα ב-Peyer's patch מייצרים כמויות גדולות של IL-5 כאשר הם מגורים על ידי IL-2 (Kuraoka וחב' ב-Eur J Immunol משנת 2004).
IL-5 פועל על תאי המטרה על ידי התקשרות לקולטן הספציפי שלו IL-5R. קולטן זה מורכב משרשרת אלפא ייחודית (IL-5Rα/CD125) ומשרשרת β המשותפת לציטוקינים אחדים (βc/CD131) והוא מבוטא על פני סוגי תאים רבים, בהם הוא מעביר איתותים למגוון פונקציות (Takaki וחב' ב-EMBO J משנת 1990 ו-1991, Murata וחב' ב-J Exp Med משנת 1992, ו-Sakamaki וחב' ב-EMBO J משנת 1992). מקטע הקולטן IL-5Rα נקשר ל-IL-5, ואילו מקטע βc היא מולקולה המשותפת גם לקולטנים של ציטוקינים אחרים, כולל IL-3R והקולטן של GM-CSF. המקטע βc כשלעצמו אינו קושר אף ציטוקין, ויש לו חלק ציטופלזמי יחסית ארוך ומספר מקטעים פונקציונליים (Sato וחב' ב-EMBO J משנת 1993), והוא כרוך באופן בולט בהעברת איתותים (תמונה 1).
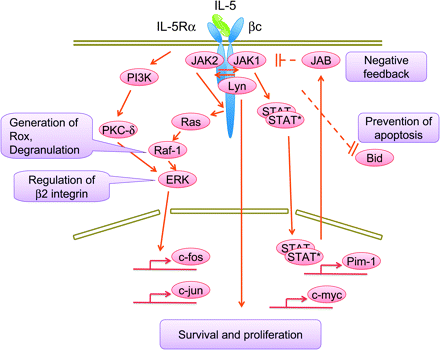
המקטע הציטופלזמי של IL-5Ralfa, , ובעיקר הרצפים שלו העשירים ב-proline הקרובים לממברנה, נדרש לשגשוג התאי המושרה על ידי IL-5, וכן להעברת האיתותים (Takaki וחב' ב-Mol Cell Biol משנת 2004, Kouro וחב' ב-Unt Immunol משנת 1996, Ogata וחב' ב-Blood משנת 1998, ו-Moon וחב' ב-Immunology משנת 2001).
IL-5 משרה את ההתמיינות הטרמינלית של תאי B משופעלים לתאים יוצרי נוגדנים בעכברים, ומעודדים שגשוג והתמיינות של תאים קודמניים לאאוזינופילים להפוך לאאוזינופילים בשלים בעכברים ובאדם. תאי B-1 נבדלים מתאי B-2 בסמני שטח הפנים שלהם, במיקומם האנטומי וביכולת של התאים לחדש את מספרם, ושני תת-סוגי תאי B אלה מבטאים באופן קונסטיטוטיבי את IL-5Rα, ובהתאם הם מגיבים ל-IL-5 להישרדות, לשגשוג ולהתמיינות לתאי פלזמה מפרישי נוגדנים (Takatsu ב-Cytokines & Growth Factor Rev משנת 1998, ו-Hitoshi וחב' ב-J Immunol משנת 1990). עכברים הומוזיגוטיים לחסר של IL-5 ולחסר של-IL-5Rα, מראים ירידה במספר תאי B-1 בפריטונאום כמו גם ירידה בתאי +slgA+ שמקורם בתאי B-1, ב-lamina propria ( (על פי Kopf וחב' ב-Immunity משנת 1996, ו-Yoshida וחב' באותו כתב-עת מאותה שנה). תאי B-2 משופעלים על ידי אנטיגן או על ידי מיטוגנים בנוכחות של תאי Th, מבטאים את הקולטן IL-5Rα והופכים לתאים המגיבים ל-IL-5 לצורך בשלותם (Mizoguchi וחב' ב-J Immunol משנת 1999, ו-Takatsu וחב' ב-Adv Immunol משנת 2009). עדיין לא ברור האם תאי B משופעלים באדם, מבטאים את הקולטן IL-IL-5Rα, , ומגיבים ל-IL-5 לצורך בשלות. אך בעכברים כמו באדם, IL-5Rα מבוטא על פני אאוזינופילים ובזופילים בשלים.
מקורם של אאוזינופילים בתאי גזע המטופויאטיים. ההשפעות של IL-5 על אאוזינופילים נכללות ב-4 קטגוריות שונות, דהיינו התמיינות, תנועתיות, שפעול והישרדות. באשר להתמיינות, IL-5 מהווה גורם המחיש התמיינות ושגשוש של תאי-אב (progenitors) (Tominaga וחב' ב-J Exp Med משנת 1991, Dent וחב' באותו כתב-עת משנת 1990, ו-Lee וחב' ב-J Immunol משנת 1997). למרות שהדבקה עם תולעים פוגעת בהשריה של יצירת אאוזינופילים, בחסר של-IL-5 או ב-IL-5R בעכברים נמצאה יצירה של אאוזינופילים, מה שמצביע על כך שגורמים או ציטוקינים אחרים מאשר IL-5 יכולים להיות כרוכים ביצירת אאוזינופילים תוך שהם מפצים על החסר ב-IL-5 או בקולטן שלו. IL-5 פועל על תאי המטרה על ידי התקשרות לקולטן הספציפי שלו IL-5R. קולטן זה מורכב משרשרת α ייחודית (IL-5Ralfa/CD125) ומשרשרת β המשותפת לציטוקינים אחדים (βc/CD131) והוא מבוטא על פני סוגי תאים רבים, בהם הוא מעביר איתותים למגוון פונקציות (Takaki וחב' ב-EMBO J משנת 1990 ו-1991, Murata וחב' ב-J Exp Med משנת 1992, ו-Sakamaki וחב' ב-EMBO J משנת 1992).
IL-5 ואסתמה
מחלות אלרגיות כולל אסתמה, מאופיינות על ידי דלקת עם הסננה בולטת של אאוזינופילים ותאיT CD4+ )על פי Kay ב-N Eng J Med משנת 2001, ו-Murphy ו-Reiner ב-Nat Rev Immunol משנת 2002). באשר לתאי הדלקת שמייחסים לאסתמה, הגיוס של תאי Th2CD4+ושל אאוזינופילים הוא מאפיין מרכזי של התגובה האלרגית בשלביה המאוחרים (Wills-Karp ב-Ann Rev Immunol משנת 1999). ראיות מצטברות מצביעות על כך שהציטוקינים הקלאסיים הנובעים מתאיTh2 והם IL-13 ,IL-9 ,IL-5 ,IL-4 ,IL-3 ו-GM-CSF , ביחד עם eotaxin משחקים תפקידים קריטיים בהשריית ריאקטיביות-יתר בדרכי האוויר ובהתפתחות של remodeling כרוני של דופן דרכי האוויר (Asquith וחב' ב-J Immunol משנת 2008, Rothenberg ו-Hogan ב-Ann Rev Immunol משנת 2006, ו-Kay וחב' ב-Trends Immunol משנת 2004). בנוסף, ציטוקינים שזוהו לאחרונה, הכוללים לימפופויאטין של הסטרומה של הטימוס, וכן IL-25 ו-IL-33, כרוכים בהשריה של דלקת אלרגית באסתמה (Pandey וחב' ב-Nat Immunol משנת 2000, Lu ב-J Exp Med משנת 2006, ו-Nakajima ו-Takatsu ב-Int Arch Allergy Immunol משנת 2007).
אאוזינופילים מכילים בגרנולות שלהם חלבונים ייחודיים, הכוללים חלבון בסיסי עיקרי, פראוקסידאזה אאוזינופילית ונוירוטוקסין אאוזינופילי. בעכברים ובאדם, IL-5 משרה בשלות טרמינלית של אאוזינופילים, מאריך את ההישרדות של אאוזינופילים על ידי דחיית התהליך האפופטוטי, משתלט על הפעילות הכמוטקטית של אאוזינופילים, מגביר את הספיחה של אאוזינפילים לתאי אנדותל ומגביר את הפעילות האפקטורית של תאים אלה (Yamaguchi וחב' ב-J Exp Med משנת 1988). יחד עם זאת, הניסיון לעכב הצטברות של אאוזינופילים בדרכי האוויר של חולי אסתמה על ידי בלימת הפעילות של IL-5, זכה להצלחה מועטה (Takatsu ו-Nakajima ב-Curr Opin Immunol משנת 2008).
רמות IL-5 בנסיוב של חולי אסתמה עיקשים קלים או מתונים גבוהות משמעותית מאלו בביקורת של נבדקים בריאים. ניסוי שכלל 32 חולי אסתמה אטופיים ו-24 חולי אסתמה לא-אטופיים, מצא רמה ממוצעת של IL-5 של 9.5 פיקוגרם/מ"ל בחולים האטופיים, ו-8.1 פיקוגרם/מ"ל בחולים הלא-אטופיים, כאשר רמתו הממוצעת בנבדקים בריאים נקבעה כ-4.4 פיקוגרם/מ"ל (0.003p<). רמות IL-5 בנבדקים אסתמתיים אטופיים ולא אטופיים לא היו שונות משמעותית. הרמה הממוצעת של IL-5 הייתה באופן לא משמעותי בקרב 14 חולי אסתמה מתונים (10.6 פיקוגרם/מ"ל, בהשוואה לרמתו ב-42 חולי אסתמה קלים (7.3 פיקוגרם/מ"ל) (p=0.13) (Joseph וחב' ב-BMC Pulm Med משנת 2004).


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק 