ליפופרוטאין (Lipoprotein (a
| מדריך בדיקות מעבדה | |
| ליפופרוטאין (a) | |
|---|---|
| (Lipoprotein (a | |
| שמות אחרים | (Lp(a |
| מעבדה | כימיה בדם |
| תחום | תחלואת לב וכלי-דם |
| טווח ערכים תקין | מתחת ל-30 מיליגרם/ד"ל |
| יוצר הערך | פרופ' בן-עמי סלע |
בסיס פיזיולוגי
ליפופרוטאין (a) או (Lp(a, תואר לראשונה בשנת 1963 על ידי החוקר הנורווגי Kare Berg, במאמר שהתפרסם ב-Acta Pathol Microbiol Scand. הגן האנושי המקודד לליפופרוטאין זה שובט ב-1987. גן זה ממוקם על כרומוזום 6q26-27.
אחד האתגרים הגדולים במחקר על המשמעות הקלינית של (Lp(a נעוצה בכך שהוא מופיע רק בבני-אדם ובקופים, אך לא בחיות מעבדה מקובלות אחרות. קושי אחר המתייחס לפיזיולוגיה של (Lp(a הוא שאיננו יודעים עדיין כיצד הוא עובר קטבוליזם או כיצד הוא מתפנה מהגוף. ברור יחד עם זאת ש-(Lp(a אינו מתפנה מן הדם על ידי הקולטנים ל-LDL, אם כי נראה שהכליות הן בעלות תפקיד בפינוי מולקולה זו מהפלזמה, באופן שתקופת מחצית החיים שלה בדם אינה עולה על 3-4 ימים. סוגיה שעדיין לא נפתרה מתייחסת למשמעות הפיזיולוגית ה"לא-פתולוגית" של (Lp(a: עצם העובדה שישנם בני-אדם רבים שרמות (Lp(a נמוכות ביותר (מתחת ל-2 מיליגרם/ד"ל), וישנם אף כאלה שרמות (Lp(a בדמם אינן ניתנות כלל לגילוי כאשר הם בריאים לחלוטין, מעצימה את סוגיית המשמעות הפיזיולוגית של ליפופרוטאין זה.
מבנה (Lp(a
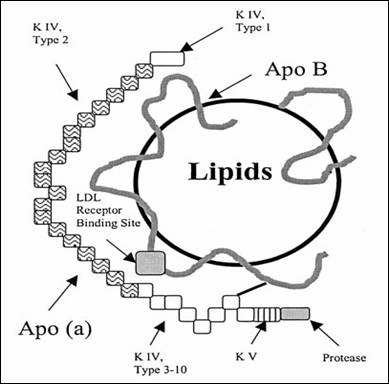
חלקיק ליפופרואטין זה שגודלו מוערך כ-25 ננומטר, דומה ל-LDL במרכיביו הבסיסיים, בכך שהוא בנוי מגרעין הידרופובי עתיר בכולסטרול-אסטר וטריגליצריד, העטוף על ידי שכבת פוספוליפידים וכולסטרול חופשי. בדומה לחלקיקי LDL, כל חלקיק (Lp(a מכיל מולקולת אפוליפופרוטאין B, הצמודה לדופן החלקיק, אך הוא מכיל בנוסף חלבון הידוע כאפוליפופרוטאין-a, או (apo(a, המקודד על יד הגן LPA. כלומר בנוסף למבנה הבסיסי המשותף ל-LDL המכיל apolipoprotein B100 (שמשקלו המולקולארי כ-512,000 דלטון), מכיל (Lp(a גם את המרכיב החלבוני (apo(a, (שמשקלו המולקולארי 275,000-800,000 דלטון) כאשר 2 חלבונים אלה קשורים ביניהם קו-ולנטית בקשר די-סולפידי. החלבון (apo(a מיוצר בכבד, כמו החלבון apoB100 המהווה את החלק החלבוני ב-LDL וב-VLDL המיוצר אף הוא הכבד, לעומת apoB48 שהוא חלבון מבני של הכילומיקרונים ומיוצר במעי. באלקטרופורזה על ג'ל נע (Lp(a באזור pre-β לעומת LDL הנע באזור β ו-HDL שנע באזור α-גלובולינים. (LP(a נמנה אם כן על קבוצת ה– β-ליפופרוטאינים, לעומת HDL שהוא α-ליפופרוטאין.
משמעויות תפקודיות של מבנה (Lp(a
בדומה לחלקיקי LDL, שניים ממרכיבי (Lp(a, הליבה הליפידית ו-apoB הם מרכיבים אתרוגניים. המרכיב (apo(a הייחודי ל-(Lp(a, שונה מכול אפוליפופרוטאין אחר בהיותו מכיל שייר סוכרי גדול, בהיותו הידרופילי מאוד ללא כל גדילים (helices) אמפיפאתיים. הקשר די-סולפידי של apo(a) ל-apoB, מתרחש בקצוות ה-C טרמינאליים של שניהם. המבנה של החלבון (apo(a נקבע גנטית בכל אדם, והוא מקודד על ידי גן בודד (LPA) הממוקם בזרוע הארוכה של כרומוזום 6, המכיל מספר אללים האחראיים לפולימורפיות הניכרת של (apo(a. זו הסיבה לשונות הרבה בגודל של ה-(apo(a שמשקלו המולקולארי יכול לנוע בין 187-662 אלף דלטון. גם ריכוזי (Lp(a נקבעים גנטית, וכך יכולה להתקבל שוֹנוּת בולטת של ריכוזו בפלזמה בין פרטים באוכלוסייה, שיכולה להיות בין 1-100 מיליגרם/ד"ל. שוֹנוּת זו משקפת יותר את יצירת החלקיק (Lp(a מאשר את הפירוק שלו. זו גם הסיבה להבדלים הניכרים ברמת (Lp(a בקבוצות אתניות שונות, כמו גם להבדלים בפוטנציאל האתרוגניות שלו.
יחד עם זאת ברור ש-(Lp(a נתון הרבה פחות להשפעות תרופתיות או אחרות בהשוואה לגורמי סיכון אחרים. סטאטינים לדוגמה אינם יעילים בהפחתתו, ודיאטה, פעילות גופנית סדירה, שמירה על משקל אופטימאלי או תרופות מקובלות שונות, הם בעלי השפעה מועטה על ריכוזיו בדם הנקבעים במידה רבה באופן גנטי ונוטים להישאר די קבועים לאורך החיים. לכן (Lp(a אינו מהווה בדרך כלל יעד טיפולי-תרופתי להפחתת רמתו. יחד עם זאת, בולטת השפעת אי-ספיקת כליות בהעלאת רמתו של (Lp(a.
דמיון מבני בין (Lp(a לפלסמינוגן
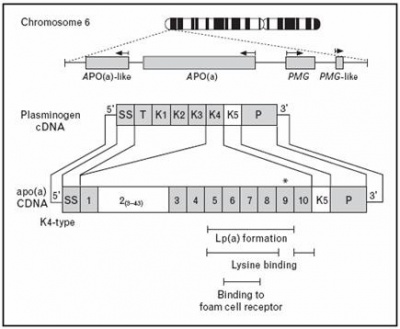
שרשרת ה-(apo(a מכילה חמישה מקטעים (domains) עשירים בציסטאין הידועים כ- "kringles", כאשר המקטע הרביעי הומולוגי במבנהו עם המקטע הנקשר לפיברין של פלסמינוגן. בשל הדמיון המבני הזה לפלסמינוגן, (Lp(a מתחרה עם פלסמינוגן על אתרי הקישור של האחרון, מה שעלול לגרום להפחתת פעולת המסת הקריש של פלסמינוגן.
בשנת 1987 תאר לראשונה McLean את המבנה של cDNA של ה-(apo(a האנושי. הוא זיהה את הדמיון המבני בין הגן ל-(apo(a לגן המקודד לפלסמינוגן, ואמנם דרגת ההומולוגיה הגבוהה הזו, בנוסף לקווי הדמיון בין (Lp(a ל-LDL, הוליכו להערכה שייתכן קשר תפקודי של (Lp(a לתהליכים פתו-פיזיולוגיים של טרשת עורקים ותהליכים תרומבוטיים. הסתבר שהגנים ל-(apo(a ולפלסמינוגן, מקודדים למבני-לולאה הקרויים kringles או K החוזרים על עצמם, ומיוצבים על ידי 3 קשרים די-סולפידיים פנימיים. ישנם בסך הכול 11 רצפים של kringles של (apo(a, מתוכם 10 מופיעים כעותק אחד, ואילו ה-kringle הנותר (K4type2) שונה במספר עותקיו, שיכול להיות מ-3 עד 40. כבר בשנת 1996 זוהו לפחות 34 איזופורמים שונים של (apo(a, השונים ביניהם רק במספר המקטעים של K4 שכל אחד מהם מכיל 114 חומצות אמינו, המקודדים על ידי הגן ל-(apo(a.
הגן לפלסמינוגן מכיל רצפים מקודדים, כאשר כל עותק מקודד לחמישה מקטעי K שונים (K1-K5). פלסמינוגן מכיל מקטע דמוי-טריפסין, שיכול להיות מבוקע על ידי urokinase plasminogen activator, או על ידי tPA או tissue plasminogen activator, ליצירה של האנזים הפעיל plasmin בתהליך הקרישה. שניים ממקטעים אלה הם הומולוגיים למקטעים הנמצאים בגן המקודד ל-(apo(a, והם מקודדים ל-K4 ול-K5. המקטע K4 הוא גם המקטע שהשתמר פחות ממקטעי K האחרים, במובן שהוא המקטע הפולימורפי ביותר בחלבון (apo(a, המכיל מקטעי K4 רבים החוזרים על עצמם. כמו גם מקטעים דומים מאוד ל-K5 ולמקטעים בעלי פעילות פרוטאזה בפלסמינוגן. הדבר היחיד המבדיל ביניהם הוא שהמקטע דמוי הפרוטאזה ב-(apo(a אינו פעיל כתוצאה משחלוף של מספר חומצות אמינו ברצף שלו.
לגן ל-(apo(a ישנם 10 סוגים שונים של מקטעי K4 הדומים לאלה של פלסמינוגן, הידועים כ- K4 types 1-10. המקטעים החוזרים type 1 וכן types 3-10 מופיעים כעותק אחד בלבד, ואילו K4 type 2 הוא כאמור בעל עותקים אחדים, שמספרם נקבע גנטית. אכן, מספר הרצפים החוזרים של K4 type 2, הוא שקובע את דרגת ההטרוגניות באורכו של הגליקופרוטאין (apo(a. כל kringle מכיל כ-80-85 חומצות אמינו, ומשקלו המולקולארי כ-10,000 דלטון. ההטרוגניות הגנטית הזו, קובעת בערך 90% מהשוֹנוּת ברמת (Lp(a בפלזמה. הגודל של (Lp(a עומד ביחס הפוך לרמתו בפלזמה, דהינו ככל שה-Lp(a) קטן יותר כך תגדל רמתו בפלזמה, ממצא שהתפרסם על ידי Danesh וחב' ב-Circulation בשנת 2000.
כמו כן, כיוון ש-(Lp(a מעודד הפרשה של המעכב של פלסמינוגן PAI-1, ולעומת זאת מפחית את פעולת tPA, הוא עלול לסייע בכך ליצירת קרישי דם. בנוסף, (Lp(a משתתף בטרנספורט של כולסטרול ובכך מסייע לתהליך הטרשתי, מה גם ש-(Lp(a משתתף בטרנספורט של הפוספוליפידים המחומצנים והוא עצמו מכיל lipoprotein associated phosphpolipase A-2, ושני האחרונים הם מרכיבים מחוללי דלקת ואתרוגניים במיוחד. בהגיע (Lp(a מהפלזמה לאינטימה, והוא מגרה הגעה של תאי דלקת לדופן כלי הדם, המחישים בדופן את השגשוג של תאי שריר חלק, מה שמסייע להיצרות העורקים. (Lp(a נקשר גם למקרופאגים דרך קולטנים על פני תאים אלה, מה שמעודד יצירת תאי-קצף, ושקיעת כולסטרול ברבדים הטרשתיים. בנגעים טרשתיים ניתן למצוא Lp(a) בכמויות פרופרציוניות לריכוזיו בדם, אל לא ניתן למצאו בדפנות של עורקים בריאים. משערים שהקולטן ל-VLDL הנמצא על פני מקרופאגים, יכול לקשור ולתווך בפירוק של (Lp(a בתהליך של אנדוציטוזה, המחדיר את ה-(Lp(a לתוך המקרופאגים, שם הם מתפרקים בתוך הליזוזומים, תהליך שמגביר הצטברות-יתר של שומנים בתוך המקרופאגים.
ערכי הנורמה של (Lp(a
ערכי (Lp(a בפלזמה עולים מייד לאחר הלידה ומתייצבים תוך חודשים אחדים, עם הבשלת הכבד. בבוגרים מוצאים טווח מאוד רחב של ערכי (Lp(a בין 0.2-250 מיליגרם/ד"ל. הערכים דומים בין גברים ונשים. מחקרים באוכלוסיות שונות מצביעים על כך ש-20% מהפרטים הם בעלי רמות (Lp(a מעל 50 מיליגרם/ד"ל, ו-25% מהפרטים הם בעלי רמות הגדולות מ-32 מיליגרם/ד"ל. כאמור, רמות מתחת ל-30 מיליגרם/ד"ל נחשבות תקינות. ההבדלים הניכרים בין קבוצות אתניות שונות, מחזקים את ההשפעה הגנטית הניכרת על גודל ומבנה של המרכיב החלבוני (apo(a של (Lp(a המשפיעים על רמתו בפלזמה.
בולטת במיוחד העובדה שבאלה ממוצא אפריקאי רמת (Lp(a גבוהה פי-2-3 מאשר באלה מאסיה, אוקיאניה, או אירופה. בכל האוכלוסיות הללו רמת (Lp(aנמצאת במתאם הפוך עם גודל ה-isoform של (apo(a. נתונים עדכניים מצביעים על הנתונים הבאים: בגברים ובנשים ממוצא אפריקאי ערכים נורמאליים (Lp(a נעים בין 4.6-71.8 ו-4.4-75 מיליגרם/ד"ל, בהתאמה, בגברים ובנשים לבנים ערכים אלה הם 2.2-49.4 ו-2.1-57.3 מיליגרם/ד"ל, בהתאמה. יש שיטת הערכה אחרת המתייחסת לערכי (Lp(a בפלזמה באופן הבא: רמה רצויה: פחות מ-14 מיליגרם/ד"ל; רמה גבולית - 14-30 מיליגרם/ד"ל; רמה בסיכון גבוה- 31-50 מיליגרם/ד"ל; רמה בסיכון מאוד גבוה- יותר מ-50 מיליגרם/ד"ל.
נתונים ממחקר Framingham מצביעים על רמה ממוצעת של 14 מיליגרם/ד"ל לגברים, ו-15 מיליגרם/ד"ל לנשים. רמות מעל 30 מיליגרם/ד"ל נחשבות מוגברות, כאשר ב-25% מהאוכלוסייה האמריקנית מוצאים רמות (Lp(a העולות על הסף של 30 מיליגרם/ד"ל. חלק משמעותי מאלה עם רמת (Lp(a מעל 30 מיליגרם/ד"ל בארה"ב, סובלים מכשל כרוני של הכליות, מתסמונת נפרוטית או מנפרופתיה סוכרתית. לפי מחקר Framingham, רמת (Lp(a באחוזון ה-90 של ליפופרוטאין זה בקרב גברים בארה"ב, היא 39 מיליגרם/ד"ל, ובקרב נשים 39.5 מיליגרם/ד"ל, בממוצע. בקרב שחורים בארה"ב ערכי (Lp(a גבוהים יותר.
אנשים ממוצא אפרו-אמריקני לעתים קרובות הם בעלי רמות פי-2-3 גבוהות יותר של (Lp(a בפלזמה, אך להם איזופורמים של apo(a) בגודל בינוני, בהשוואה ללבנים. יתרה מכך, בקרב לבנים יש כמות עודפת של איזופורמים גדולים של (apo(a לעומת איזופורמים קטנים יותר של (apo(a. גם בקרב אסייאתים נמצא הבדלים בגודל של (apo(a וממילא בריכוז של (Lp(a בפלזמה. אלה במזרח אסיה נוטים להכיל (apo(a גדול יחסית ורמת (Lp(a נמוכה יותר בפלזמה. אלה בדרום אסיה הם בעלי רמות (Lp(a גבוהות יותר.
התפקיד של (Lp(a בטרשת עורקים ובקרישיות-יתר
למרות שהמנגנונים הפיזיולוגיים והפתולוגיים אינם ידועים, מספר ניכר של מחקרים כרך רמות גבוהות של (Lp(a בפלזמה עם מגוון של מפגעים קרדיו-וסקולאריים, כולל התקפי-לב, מחלת כלי-דם היקפיים, מחלה צרברו-וסקולארית, ומחלה כלילית בגיל צעיר. נראה ש-(Lp(a קשור להליך יצירת הרובד הטרשתי, שכן בדומה ל-LDL גם (Lp(a יכול להתחמצן, ולהיקלט על ידי מקרופאגים. (Lp(a יכול להיקשר לליפופרוטאינים המכילים apoB, כמו גם לפרוטאוגליקנים ולפיברונקטין בדופן העורק, ולעודד שקיעת כולסטרול בתאי אנדותל, והצטברותו ברבדים טרשתיים, תוך גירוי של תאי שריר חלק באינטימה לשגשג. (Lp(a מגביר את הביטוי של ה-endothelial adhesion molecule-1, ובכך מעודד ספיחה של מונוציטים על פני שכבת האנדותל, ומחיש את נדידת תאים אלה מעבר למחסום האנדותליאלי.
בנוסף, (Lp(a משפעל את גורם השעתוק הגרעיני NFκB שהוא גורם דלקתי, מה שמעודד גיוסם של תאי דלקת. (Lp(a יכול לגרום לארגון מחדש של מבנים ציטופלזמתיים (cytoskeleton) של תאי אנדותל וסקולאריים, מה שמגביר את כושר הקליטה (permeability) של תאים אלה ומשבש את תפקודם.
מספר מחקרים הדגימו קשר בין (Lp(a ופוספוליפידים מחומצנים (OxPL) לבין התהליך הטרשתי. אכן, בפלזמה יש נטייה לפוספוליפידים מחומצנים להיקלט על ידי חלקיקי (Lp(a, יותר מאשר על ידי חלקיקי LDL. לכן, אם אמנם (Lp(a קולט OxPL, הוא עלול להגביר את ריכוזם באזור דופן העורק ולהגביר את תהליך הטרשת. בהקשר זה כדאי לצטט מחקר של Edelstein שהראה שמולקולות של פוספוליפידים מחומצנים תומכי דלקת, נקשרים באופן בררני דווקא למקטע K5 של החלבון (apo(a. כיוון שכל סוג של (apo(a ללא קשר לגודלו, מכיל מקטע יחיד של K5, נראה שכל מולקולת (Lp(a מסוגלת להוביל OxPL לאזור התהוות הטרשת.
כפי שכבר הוזכר, (Lp(a ופלסמינוגן מתחרים על אותם אתרי קישור על פני fibrin, ולכן (Lp(a מפריע לשפעול של פלסמינוגן על ידי tPA, וכך ישתבש התהליך הפיברינוליטי ותוגבר הקרישתיות. אך מחקרים עדכניים, in vitro, מראים ש-(apo(a יכול להגיב עם 3 מרכיבים פיברינוליטיים, לא רק עם פיברין. באופן מסורתי, המחשבה הייתה ש-(apo(a, פלסמינוגן ו-tPA, נקשרים לאזורים בלתי תלויים על פני פיברין. בניסוי האמור in vitro, בעלי המחקר שינו את ריכוזו של פלסמינוגן וכן את ריכוזי פיברין ו-(apo(a,ומצאו שבהיעדר (apo(a,יוצרים tPA, פלסמינוגן ופיברין, קומפלקס המביא ליצירת פלסמין. אך בהוספה של (Lp(a, נקשר (apo(a בעצמו לפיברין, ואז הוא גם מגיב עם הקומפלקס המשולש ליצירת קומפלקס מרובע, ומונע באופן דרמטי את שפעולו של פלסמינוגן. מודל זה הוכיח שחלקיקי Lp(a( המכילים (apo(a קטן יחסית, הם בעלי זיקה גבוהה יותר לפיברין, ובכך הם מהווים מעכבים יעילים יותר של שפעול פלסמינוגן.
בשנת 2009 (חוברת 10 ביוני) פרסמו Kamstrup וחב' ב-JAMA במסגרת מחקר Copenhagen city Heart Study, את ממצאיהם לפיהם רמות מוגברות גנטית של (Lp(a, היו כרוכות בסיכון מוגבר ל-MI. מחקר זה הדגים שבאוכלוסיות אתניות שונות, יש פיזור ניכר ברמת (Lp(a, שיכול להתבטא בריכוזים בין 5-70 מיליגרם לד"ל. הריכוזים הנמוכים ביותר נמדדו בנבדקים ממוצא קווקזי והגבוהים ביותר באלה ממוצא אפריקאי. במחקר קופנהגן נמצא שהסיכון הקרדיו-וסקולארי היה גבוה פי-2.6 באלה מהנבדקים שנכללו בקבוצה עם ריכוז (Lp(a גבוה מהאחוזון 95 במדגם, בהשוואה לאלה עם ריכוז Lp(a) נמוך מהאחוזון 22 במדגם. מחקר זה היה המשך של מחקר קודם בנושא שפרסמו Kamstrup וחב' ב-Circulation בשנת 2008.
מטה-אנליזה של Craig שכללה 12 מחקרים שפורסמו בין 1991-7, צברה נתונים שנחשבו תומכים בראיות לתפקיד סיבתי של (Lp(a בהתפתחות טרשת עורקים. Craig הסיק שרמות (Lp(a בפלזמה, גבוהות יותר בהתרחשות הפתולוגית הזו בהשוואה לביקורת, והיוו גורם סיכון בלתי-תלוי ל-CHD בגברים ובנשים. Danesh פרסם מטה-אנליזה של 5,436 מקרי מוות מ-CHD שנרשמו במעקב של 10 שנים ב-27 מחקרים פרוספקטיביים על רמת (Lp(a. ניתוח נתונים זה העלה שפרטים באוכלוסייה הכללית עם רמות (Lp(a בשלישון העליון, היו בסיכון מוגבר ב-70% ללקות ב-CHD, בהשוואה לפרטים עם רמות (Lp(a בשלישון התחתון.
(Lp(a בקשישים
המחקר הראשון שבחן את הקשר בין (Lp(a לבין אירועים קרדיו-וסקולאריים בקשישים היה מחקר PROSPER או Prospective Study of Pravastatin in the Elderly at Risk, שבחן את ההשערה שרמת (Lp(a היא מנבא בלתי-תלוי של אירועים וסקולאריים משמעותיים ופגיעה קוגניטיבית בגיל המתקדם. מחקר זה כלל 5,732 פרטים בגיל שבין 70-82 שנה, שהיו במעקב משך 3.2 שנים בממוצע. נמצא שרמות (Lp(a לא השתנו לאורך קבוצת גיל זו, ושהן היו גבוהות משמעותית בקרב נשים לעומת גברים (14.8 לעומת 12.4 מיליגרם לד"ל), אך נמצאו מנבא מתון בלבד של אירועים קרדיו-וסקולאריים עתידיים.
(Lp(a בנשים
מספר מחקרים מצאו מתאם מובהק בין (Lp(a וסיכון וסקולארי במספר אוכלוסיות נשים. Shai וחב' חקרו את תפקידו של (Lp(a בהתרחשות מחלת לב כלילית בקרב 38,826 נשים שהשתתפו ב-Nurses’ Health Study. משך 8 שנים של מעקב, נרשמו במדגם זה 228 מקרים של CHD, כאשר כל מקרה נבחן בהשוואה לביקורת תואמת. בדגם רב-משתני שעבר התאמה, נמצא ש-OR ל-CHD בקרב אלו מהנשים עם (Lp(a מעל 30 מיליגרם/ד"ל, היה גדול פי-1.9 בהשוואה לנשים עם (Lp(a נמוך מ-30 מיליגרם/ד"ל. נשים במחקר זה, עם ערכי (Lp(a גבוהים מ-30 מיליגרם/ד"ל וערכי פיברינוגן גבוהים מ-400 מיליגרם /ד"ל, היו עם OR גדול פי-3.2 להתרחשות CHD, לעומת אלו עם ערכים בתחום הנורמה של 2 מדדים אלה (p=0.05). בדומה, נשים עם ערכי Lp(a) מוגברים בנוסף לערכי CRP מעל 3 מיליגרם לליטר, היו בעלות OR של 3.67 בממוצע ל-CHD, בהשוואה לאלו עם ערכים תקינים של שני המדדים.
גם Suk Danik בחן את המתאם בין רמות (Lp(a לבין מחלה קרדיו-וסקולארית עתידית במחקר פרוספקטיבי לאורך תקופה של למעלה מ-10 שנים בקרב 27,791 נשים בריאות בבסיס המחקר של WHS. המחקר בחן את הסיכון להתרחשות ראשונה של התקף-לב לא קטלני, אירוע צרברו-וסקולארי לא קטלני, צורך בביצוע תהליך אנגיוגראפי המחייב שתילת תומכן או פתיחת היצרות עם בלון, ומוות מסיבה קרדיו-וסקולארית. בסך הכול נרשמו 899 אירועים כאלה, ונמצא שריכוזי (Lp(a גבוהים במיוחד מעל אחוזון 90, היו כרוכים באופן משמעותי באירועים מוגברים כאלה, במיוחד בנשים עם LDL מוגבר (OR מתואם מוגבר פי-1.81).
בבסיס מחקר זה, נבדקה רמת (Lp(a ב-27,736 נשים בריאות בתחילת המחקר, מתוכן 12,075 שקיבלו טיפול הורמונאלי חלופי (HRT), לעומת 15,661 נשים שלא נטלו הורמונים אלה. נמצא אמנם כפי שדווח כבר קודם לכן, שנטילת אסטרוגנים מפחיתה רמת (Lp(a כאשר בקבוצת המשתמשות ב-HRT נרשמה רמת ממוצעת של 9.4 מיליגרם /ד"ל, לעומת 11.6 באלה שלא נטלו הורמונים.
השפעת הגודל של חלקיק (Lp(a על מחלה קרדיו-וסקולארית
עדיין לא ברור האם ההשפעה האטרוגנית המיוחסת ל-(Lp(a נובעת מאינטראקציות עם החלק דמוי-LDL של החלקיק, או שמא עם החלק של החלבון ההטרוגני (apo(a. יש התמקדות הולכת וגוברת על ההשפעה הפוטנציאלית של גודל האיזופורם של (apo(a. כיוון שבאופן כללי ככל שהאיזופורם של apo(a) קטן יותר, כך רמת ה-(Lp(a בפלזמה גבוהה יותר, החל משנת 1997 התרבו המחקרים שניסו לקבוע את גודל האיזופורם האחראי להתפתחות מחלה קרדיו-וסקולארית.
חלק ממחקרים אלה ניסה ללמוד את חשיבות גודלו של האיזופורם של (apo(a ללא כל קשר לרמות (Lp(a בפלזמה. במחקר הפרוספקטיבי של Bruneck שפרסמו Kronenberg וחב' ב-1999 ב-Circulation, נמצא קשר מובהק בין גדלים קטנים של (apo(a לבין התרחשות מפגעים קרדיו-וסקולאריים. במחקר זה, נעשתה הערכה על קשר אפשרי בין רמות (Lp(a בפלזמה וגודלם של פנוטיפים של (apo(a, בין התקדמות של תהליך טרשתי בקארוטידים, על ידי מדידת high-resolution duplex ultrasound במדגם אקראי של אוכלוסייה שכלל 826 פרטים שהיו במעקב 5 שנים. נמצא שרמות הולכות וגדלות של (Lp(a ניבאו את הסיכון לתהליך טרשתי מוקדם בתלות ברמת (Lp(a, אך זאת רק באלה עם רמת LDL מעל 128 מיליגרם/ד"ל. לעומת זאת, פנוטיפים איזופורמיים קטנים של (apo(a היוו מנבא חזק ביותר למחלה טרשתית בעורקים הקארוטידיים, בעיקר כאשר הם היו משולבים ברמות (Lp(a מוגברות בפלזמה (OR=6.4).
בסקירה סיסטמאטית של 40 מחקרים שכללו בסך-הכול 58,000 נבדקים, נמצא שהסיכון היחסי ל-CHD היה 2.08 באלה עם איזופורמים קטנים של (apo(a (מספר kringles IV type 2 קטן מ-22), בהשוואה לאלה על איזופורמים גדולים של (apo(a. בדיווח אחר, על מטופלים עם תסמונת כלילית חריפה (ACS), הייתה עלייה משמעותית במספר המטופלים שביטאו לפחות איזופורם קטן אחד של (apo(a, כאשר הם חוו התקף-לב, בניגוד לאלה מתוך המדגם עם תעוקת חזה יציבה, אך ללא MI. בדיווח זה רק איזופורם קטן של (apo(a אך לא רמות (Lp(a, היה מנבא בלתי-תלוי להתרחשות AMI במודל רב-משתנים.
במחקר אחר, נתונים פרוספקטיביים ממחקר בריאות הרופאים (PHS), שמשו לבחינת המשמעות הקלינית של גודל האיזופורם של (apo(a לעומת ריכוזי (Lp(a בפלזמה. נמצא שאיזופורמים קטנים יותר של (apo(a אכן היו כרוכים בסיכון מוגבר לתעוקת חזה בגברים, אם כי בעיקר באלה עם LDL גבוה מ-160 מיליגרם/ד"ל.
הקשר בין וריאנטים גנטיים של (Lp(a לתחלואה קרדיו- וצרברו-וסקלארית
Clarke וחב' סקרו בשנת 2009 ב-N Engl J Med את נושא הווריאנטים הגנטיים של (Lp(a ותחלואת כלי הדם. מחקר PROCARDIS או Precocious Coronary Artery Disease זיהה שני SNPs או single-nucleotide polymorphisms, באתר6q26-27 של הגן LPA המקודד ל-(Lp(a. שני SNPs אלה, rs3798220 ו-rs10455872, קשורים בחוזקה ובאופן בלתי תלוי זה בזה לרמות (Lp(a, ולסיכון של מחלה כלילית. שני SNPs אלה היו קשורים בערך למחצית מהשוֹנוּת הגנטית שבבסיס רמות (Lp(a. יחד עם זאת השונות הגנטית באתר LPA נראית פחות רלוונטית למקרי שבץ מוחי.
Hopewell וחב' בחנו את שני ה-SNPs האמורים של LPA להקשר שלהם לאירועים וסקולאריים במשתתפים של מחקר HPS. תוצאות מחקרם שהתפרסמו ב-2011 ב-Circ Cardivasc Genet, כללו נתונים של 12,236 משתתפים עם מחלה וסקולארית ידועה (9,277 מקרי מחלה כלילית, 1,326 מקרי שבץ איסכמי, ו-2011 מקרי מחלת כלי דם היקפיים, וכביקורת 3,687 משתתפים ללא מחלה וסקולארית). במחקר המשך של מעקב אחרי 3,251 משתתפים עם אירועים משמעותיים מזדמנים של מפגעי כלי-דם, מתוכם 2,106 משתתפים עם מחלה כלילית, 507 מקרים של שבץ איסכמי ו-707 מקרים של מחלת כלי-דם היקפית. באלה עם מחלה ידועה מראש גורם הסיכון של השונות האללית בגן LPA היה 1.19 בממוצע לגבי מחלה כלילית, 1.18 בממוצע לגבי מחלה היקפית אך רק 1.03 לגבי שבץ איסכמי. בדומה, גם לגבי אלה במעקב ההמשך, נמצא שהשונות הגנטית של LPA היוותה גורם סיכון עם OR של 1.19 לגבי מחלה כלילית, 1.20 לגבי מחלת כלי-דם היקפית, ו-0.83 לגבי שבץ איסכמי.
(Lp(a במחקרים פרוספקטיביים גדולים
סקר של Bennet וחב' שהתפרסם ב-2008 ב-Arch Intern Med, הקיף 18 מחקרים פרוספקטיביים, והראה יחס של 1.5-1.7 של סיכון קרדיו-וסקולארי בהשוואת ריכוזים גבוהים לעומת נמוכים של (Lp(a. מחקר זה כלל 2,047 מטופלים עם אירוע ראשון לא-קטלני של MI, או מוות מסיבה כלילית, וכן 3,921 פרטי ביקורת מתוך מחקר Reykjavik באיסלנד מתוך מדגם כולל של 18,569 משתתפים. המחקר הגדול של Erqou וחב' שהתפרסם ב-JAMA ב-2009, שכלל 36 מחקרים פרוספקטיביים, מצא מתאם חיובי בין (Lp(a לבין סך-כולסטרול ו-apo-B100. ניתוח נתונים זה מצא רמת סיכון מתמשכת ללא סף מסוים, וכן שהסיכון לאירוע מוחי איסכמי נמוך יותר מזה של CHD. המחקר מצא שרמה מוגברת של Lp(a) קשורה באופן מובהק לסיכון קרדיו-וסקולארי מוגבר, ואינה תלויה בריכוזי LDL או בגורמי-סיכון אחרים.
במחקר פרוספקטיבי נוסף, הידוע כ-ARIC או Atherosclerosis Risk in Communities, נעשה מעקב של 10 שנים ב-12,339 משתתפים בגיל העמידה ללא CHD. בתקופת המעקב נרשמו 725 אירועי CHD, ונמצא קשר בלתי-תלוי של רמות Lp(a) והסיכון לאירועים אלה, בעיקר בנשים. מחקר שוודי של Glader וחב', בחן מדגם של 1,216 מטופלים עם CHD, בהם נבחנה משמעות אפשרית של רמת Lp(a) לניבוי הפרוגנוזה. המעקב נמשך בממוצע 6.7 שנים, ובמהלכו נרשמה תמותה כללית של 16.4% בקרב המשתתפים. מסקנת המחקר הייתה שרמת Lp(a) מעל 30 מיליגרם /ד"ל הייתה גורם סיכון משמעותי לתחלואה ותמותה קרדיו-וסקולארית.
במחקר FATS או Familial Atherosclrosis Treatment Study שהתפרסם ב-JAMA ב-1995, ניסו Maher וחב' לקבוע האם הפחתת רמות LDL, תבטל או תפחית את ההשפעה השלילית של רמות מוגברות של (Lp(a בקרב 146 גברים בגיל 62 שנה או פחות, הסובלים מ-CHD. במהלך הניסוי היו משתתפיו משך 2.5 שנים בפיקוח דיאטתי ובנוסף טופלו עם lovastatin במינון יומי של 40 מיליגרם בנוסף ל-30 מיליגרם colestipol, או בשילוב של niacin במינון יומי של 4 גרם בנוסף ל-colestipol, כל זאת בהשוואה למטופלי פלצבו. נמצא ש-(Lp(a היה מנבא חזק של אירועים קרדיו-וסקלואריים בבסיס המחקר, אך איבד את כושר הניבוי הזה במהלך הניסוי כאשר רמת LDL הופחתה עקב הטיפולים התרופתיים.
מחקר פרוספקטיבי נוסף שבחן את (Lp(a כגורם סיכון ל-CHD, היה PRIME או Prospective Epidemiological Study of Myocardial Infarction שהתפרסם ב-2002 ב-Arterioscler Thromb Vasc Biol. המחקר כלל 9,133 צרפתים וצפון-אירים בגיל 50-59 שנה, ללא רקע של CHD וללא טיפול להפחת רמת ליפידים. במחקר זה נמדדה רמת Lp(a) בשיטת מדידת בלתי תלויה בגודל של (apo(a. במשך תקופת המעקב של 5 שנים, 288 ממשתתפי המחקר חוו לפחות אירוע כלילי אחד (MI, מוות מסיבה כלילית, תעוקת חזה). ניתוח ממצאי המעקב העריך רמות (Lp(a כגורם סיכון ל-CHD, לאחר התאמה לגורמי סיכון מסורתיים (LDL, טריגליצרידים, HDL, סוכרת, יתר לחץ-דם ועישון). נמצא שרמה מוגברת של (Lp(a מגבירה את הסיכון ל-MI, למוות מסיבה כלילית ותעוקת חזה.
כחלק ממחקר Quebec Cardiovascular Study, עקבו Cantin וחב' משך 5 שנים פרוספקטיבית אחר 2,156 גברים צרפתים-קנדיים בגיל 47-76 שנים, ללא עדות קלינית של מחלת לב איסכמית. במחקר זה שהתפרסם ב-1998 ב-J Am Coll Cardiol, נמדדו בבסיס המחקר ערכי ליפידים [(Lp(a), סך-כולסטרול, LDL ,HDL, ו-apoB). במהלך המעקב נרשמו 116 אירועים ראשונים של IHD (תעוקת חזה, MI ומוות). נמצא ש-(Lp(a לא היה גורם סיכון בלתי-תלוי ל-IHD באותם גברים, אך הגביר סיכון זה במשולב עם רמות מוגברות של סך-כולסטרול ושל apoB.
אינטראקציה דומה בין ערכי (Lp(a מוגברים עם גורמי סיכון אחרים ל-CHD, נמצאה במחקר PROCAM או Prospective Cardiovascular Münster Study, בו השתתפו 788 גברים בני 35-65 שנה, שהיו במעקב משך 10 שנים. במהלך המעקב עברו 44 ממשתתפיו אירוע MI. בכל המשתתפים נמדדו בנוסף לרמות Lp(a) גם גורמי סיכון מסורתיים (גיל, LDL, טריגליצרידים, HDL, לחץ-דם סיסטולי, עישון, סוכרת, תעוקת חזה, היסטוריה משפחתית של MI). מסקנות מחקר זה היו שרמות מוגברות של (Lp(a הגבירו ב-10% את הסיכון של MI בגברים עם רמה מוגברת של LDL, רמה נמוכה של HDL או עם יתר לחץ-דם. מטה-אנליזה של 27 מחקרים פרוספקטיביים עם מעקב ממוצע של 10 שנים נמצאה עלייה של 70% בסיכון למחלת לב כלילית באנשים עם רמות (Lp(a ברבעון העליון. במחקרים נוספים נמצא ש-(Lp(a הוא גורם עצמאי למחלה קרדיו-וסקולארית בגברים ובשנת 2005 הראו Shai וחב' נתונים דומים גם בנשים סוכרתיות במאמר שהתפרסם ב-Diabetologia.
רמה מוגברת של (Lp(a מוצאים לעתים קרובות יותר במטופלים צעירים עם CHD. לדוגמה, מחקר אחד הראה שרמה מוגברת של (Lp(a נמצאה ב-18.6% של מטופלים צעירים עם CHD, כאשר ב-12.7% מתוכם לא היו כל מאפיינים אחרים של דיסליפידמיה.
בשנת 2009 התפרסמה מטה-אנליזה רחבת היקף, שבחנה את הקשר בין (Lp(a ו-CVD מנתונים של 36 מחקרים שהקיפו מעל 120,000 משתתפים. נמצא ששיעור מקרי CHD בשלישון העליון של הנבדקים מבחינת ריכוזי (Lp(a היה 5.6 מקרים לכל 1,000 שנות חיים, לעומת 4.4 מקרים ל-1,000 שנות חיים בקרב אלה בשלישון התחתון מבחינת ריכוזי (Lp(a. לאחר התאמה לגורמי הסיכון המקובלים, נמצא שיחס ה-RR למקרי CHD בין השליש העליון והתחתון היה 1.13, שנראה צנוע יחסית לדיווחים אחרים על ניסויים בעלי אופי דומה.
מחקר אחר בחן אפשרות של מעורבות של רמות מוגברות של (Lp(a בתעוקת חזה בלתי יציבה (unstable angina). במטופלים עם תסמונת כלילית חדה (ACS), רמות מוגברות של (Lp(a ניבאו סיכון מוגבר להתרחשות מוות לבבי. במחקר זה נמצא במדגם של 266 מטופלים עם AMI, שרמת (Lp(a גבוהה מ-30מיליגרם/ד"ל, הייתה כרוכה בהתרחשות מוגברת ב-66% של מוות לבבי במעקב שנמשך 3 שנים (29.8% לעומת 18.6% באלה עם רמת (Lp(a נמוכה מ-30 מיליגרם/ד"ל).בקרב 197 מטופלים במדגם זה מאובחנים עם תעוקת חזה בלתי-יציבה, רמות מוגברות של (Lp(a ניבאו סיכון מוגבר של מוות לבבי (RR=2.48).
(Lp(a ומפגעי קרישיות-יתר
מספר מחקרים הגיעו למסקנה ש-(Lp(a יכול להיחשב כגורם סיכון בלתי-תלוי לתרחיש של תסחיף פקקתי (thromboembolism). נראה שיש אינטראקציה מסוימת בין (Lp(a לבין גורמי סיכון מקובלים של פקקת. ידוע לדוגמה, שבשליש מהילדים העוברים אירועי שבץ, אין מזהים סיבות ברורות או גורמי סיכון מובהקים שיכולים להיכלל באטיולוגיה של האירוע. מחקר של Nowak-Gotti עקב אחר 148 תינוקות וילדים לבנים (בגיל שבין 0.5-16 שנה), שעברו אירוע שבץ מוחי, וכן 296 תינוקות וילדים בקבוצת ביקורת תואמת גיל באותם אזורים גיאוגרפיים. כל הילדים נבדקו לאפשרות של רמות Lp(a) מוגברות (מעל 30 מיליגרם/ד"ל), וכן למציאות של ואריינטים גנטיים הכרוכים בפקקת. נמצא ששילוב של רמה מוגברת של (Lp(a ביחד עם עמידות לשפעול של protein C, הנובעת ממוטציה של factor V Leiden, היו כרוכים ב-OR של 30 (!!) לאירוע שבץ בילדים.
מחקר נוסף של Strater וחב' עקבו אחר 167 ילדים ו-134 ילדות לאחר שסבלו מאירוע ראשון של שבץ איסכמי, וגילו אצלם רמות מוגברות של (Lp(a, חסר משפחתי של protein C, שהיו גורמי סיכון לאירועים חוזרים של שבץ עורקי איסכמי. בהמשך המשיכו חוקרים אלה לבחון את תפקידו של (Lp(a, כגורם סיכון לאירועים תרומבו-אמבוליים שניונים, בנוכחות של גורמים תורשתיים או נרכשים אחרים לתרומבופיליה. המחקר התבצע באופן פרוספקטיבי במדגם של 301 ילדים, ונמצא בו שהשילוב של רמה מוגברת של (Lp(a ביחד עם כל גורם סיכון נוסף, הגבירו את הסיכון לתרחיש תרומבואמבולי פי-2.6, והסיכון אף גבר פי-6.2 כאשר רמה מוגברת של (Lp(a הייתה בשילוב עם פגם בפקטור V ליידן.
טיפולים להפחתת רמת (Lp(a
טיפול ב-aphresis: הומלץ ב-2008 על ידי Thompson ב-Atherosclerosis, כטיפול היעיל ביותר שעשוי להפחית את רמת (Lp(a ב-50%. אך טיפול יקר, מורכב ולא שגרתי זה שמור למקרים קיצוניים של טרשת נרחבת בהיפר-כולסטרולמיה משפחתית או היפר-כולסטרולמיה העמידה לטיפולים הרגילים, בה רמות LDL גבוהות במיוחד.
מספר תכשירים פרמקולוגיים יכולים להפחית במידה מסוימת רמות (Lp(a, אם כי בהשוואה למדדים ליפידיים אחרים יעילות הטיפול במקרים של רמות מוגברות של (Lp(a מוגבלת יחסית. ראוי לציין שהתכשירים המקובלים ביותר להפחתת רמת LDL דוגמת סטאטינים ורזינים סופחי-חומצות-מרה הם חסרי השפעה על רמות (Lp(a. דיווחים רבים במרוצת השנים הצביעו על מספר תכשירים שיכולים להשפיע על רמת (Lp(a. תכשירים אלה כוללים קרניטין (במינון יומי של 2 גרם), חומצה אסקורבית (3 מיליגרם ליום), שניהם בשילוב עם l-lysine-HCl במינון של 3 גרם ליום. מספר הורמונים יכולים להשפיע על רמת (Lp(a, כולל אנדרוגנים דוגמת danazol ו-tibolone, וכן אסטרוגנים עליהם נמסר שהם עשויים להפחית רמתו עד 50%. טיפול ב-tamoxifen נמצא מפחית משמעותית רמת (Lp(a בנשים בגיל המעבר. טיפולים אחרים עליהם דווח שהם יכולים להפחית בצורה מתונה רמת (Lp(a הם בשימוש במעכבים של האנזים המהפך-אנגיוטנסין (ACE) וכן באנטגוניסטים של סידן. יש גם ראיות לכך שמעכבים חדשים כנגד PCSK9 (האנזים הפעיל בהומאוסטאזיס של כולסטרול), המשמשים כעת בניסויים קליניים, עשויים להפחית משמעותית את רמת Lp(a). יחד עם זאת הטיפול באסטרוגן בהקשר של הפחתת רמת (Lp(a שנוי במחלוקת. מחקרים אחדים מביעים ספק באשר להשפעה של רמות מופחתות של (Lp(a בנשים בגיל המעבר, ובשלב זה לא מומלץ לטפל בנשים אלה באסטרוגנים להפחתת (Lp(a.
גם אספירין נוסה בהקשר זה, ומחקר של Akaike וחב' הראה שמינון יומי של 81 מיליגרם שנוסה על 70 מטופלים עם מחלה טרשתית ורמת (Lp(a מעל 30 מיליגרם/ד"ל, הפחית אצלם את רמות (Lp(a בערך ב-20%. דיווח שמקורו במחקר בריאות הנשים (WHI), הראה שנשים נשאיות של אלל מינורי של (apo(a הידוע כ-rs3798220, שהן בעלות סיכון כפול (OR=2.11) למחלה קרדיו-וסקולארית, וכן כאלו עם רמות מוגברות של (Lp(a, מושפעות באופן משמעותי מטיפולים שגרתיים באספירין. מעקב של 9.9 שנים העלה שנשים עם אלל זה שצרכו אספירין הפחיתו בלמעלה מ-50% את האירועים הקרדיו-וסקולאריים (OR=0.44), ואילו נשים ללא האלל האמור שטופלו באספירין לא הושפעו מהטיפול.
השפעת סטאטינים על רמת (Lp(a אינה עקבית, וישנם אף הבדלים בין השפעת סטאטינים שונים. שני מחקרים הצביעו על עליה מתונה ברמת (Lp(a בטיפול עם Simvastatin שהגיעה אף ל-38%. מחקר אחר לעומת זאת, הצביע על הפחתה משמעותית ברמות Lp(a) על ידי Simvastatin ו-atorvastatin בטיפולים שנמשכו 6 שבועות. בניסוי REGRESS, נמצאה השפעה זעומה ביותר לטיפול ב-pravastatin. ניסוי מוקדם יותר, העלה שטיפול ממושך ב-fluvastatin הפחית משמעותית רמת (Lp(a, אם כי טיפול קצר מועד היה חסר השפעה. אי הבהירות באשר להשפעת סטאטינים על (Lp(a לא הוסרה, גם לאחר הפרסום משנת 2012 של Tagaki וחב' ב-Int J Cardiol, בו נמסר על מטה-אנליזה שהתייחסה ל-atorvastatin, ואשר כללה 3,540 מטופלים ב-9 מחקרים פרוספקטיביים בהם תקופת הטיפול נמשכה חודש עד שנתיים. ניתוח נתונים זה העלה דווקא ירידה משמעותית ברמות (Lp(a בקבוצות הטיפול לעומת פלצבו.
למרות שאין כל נתונים מחקריים על מנגנון ההפחתה של רמת (Lp(a על ידי ניאצין (חומצה ניקוטינית), נראה שתכשיר זה מהווה החלופה היעילה ביותר להפחתת רמות מוגברות של (Lp(a במטופלים בסיכון גבוה. יחד עם זאת יצוין שמדובר בטיפול בניאצין במינונים מאוד גבוהים. אין עד כה פרסומים מחקריים מוסמכים על היעילות של טיפול יחידני בניאצין להפחתת אירועים קרדיו-וסקולאריים. כיוון שאין מידע מוצק המראה כי טיפול מכוון ל-(LP(a מפחית אירועים קרדיו-וסקולאריים, יש הממליצים על טיפול בניאצין רק במקרים של זיהוי (Lp(a מוגבר בנוכחות סיכון קרדיו-וסקולארי מוגבר.
מספר פרסומים דיווחו על שימוש ב-Niaspan, פורמולציה של שחרור מושהה של ניאצין תוצרת מעבדות Abbott, במינונים יומיים של 1-3 מיליגרם, לטיפול בפרטים עם היפרליפידמיה ורמה מוגברת של (Lp(a. ניסוי אחד להפחתת Lp(a) בטיפול יומי של 1-2 גרם למשך 96 שבועות, לא גרם לנזק רעלני לכבד, והביא להפחתה משמעותית בריכוזי (Lp(a. בניסוי של Pan וחב' שפורסם ב-2002 ב-Metabolism, חולקו משתתפיו באופן אקראי ל-4 קבוצות שטופלו על ידי שילובים של atorvastatin/Niaspan, או Rosuvastatin/Niaspan או simvastatin/ezetimibe או Rosuvastatin בלבד. השילוב של statin/Niaspan לא רק הגביר את רמת HDL וכן את רמת HDL2, אלא גם הפחית רמות טריגליצרידים ו-(Lp(a, יותר מכל טיפול משולב אחר בניסוי זה. רמת (Lp(a בטיפול זה פחתה ב-40% לעומת הרמה לפני הטיפול.
על פי Akdim וחב' במאמר משנת 2010 ב-Am J Cardiol, טיפול שבועי באוליגונוקלאוטיד Mipomersen, המעכב ייצור אפוליפופרוטאין B-100 בכבד, מפחית את ריכוז (Lp(a עד כדי 25%. בדומה, מעכבי CETP מפחיתים את ריכוז (Lp(a, וכן גם התכשיר anacetrapib המפחית רמת (Lp(a בשיעור 36%, זאת על פי Cannon וחב' במאמר משנת 2010 ב-N Eng J Med. תכשיר אחר הנמצא בשלב של הערכה קלינית הוא eprotirome המהווה אנלוג של הורמוני תירואיד. יש ראיות לכך שמעכבים חדשים של האנזים PCSK9 (המשחק תפקיד בהומאוסטזיס של כולסטרול) עשויים להפחית רמת (Lp(a.
מדידה חוזרת מומלצת עבור מקרים עם (Lp(a מוגבר כאשר הכוונה להעריך תגובה לטיפול. בשנת 1985 פרסמה קבוצתו של Brewer מ-NIH כי טיפול בניאומיצין 2.0 גרם ליום הוריד ריכוז (Lp(a ב-24%. שילוב של ניאומיצין וניאצין (3 גרם ליום) הביא לירידה של 45% בריכוז (Lp(a. בשנת 2010פורסמה ב-Atherosclerosis מטה-אנליזה של מחקרי התערבות שהראו יתרון מובהק לטיפול בניאצין במקרים של (Lp(a מוגבר.
על פי Chapman במאמר ב-Pharmcol Ther משנת 2010, ניאצין מפחית את רמת (Lp(a בשיעור של 40-30% בתלות במינון. במטה אנליזה שכללה 11 מחקרים מבוקרים עם 2682 חולים בקבוצת הטיפול לעומת 3934 בקבוצת הביקורת. ניאצין ניתן במינון 3-1 גרם ליום. נמצא שניאצין מוריד Lp(a לריכוז המומלץ מתחת לאחוזון 80 במסגרת השפעתו על שומני הדם והפחתת הסיכון הקרדיווסקולרי על פי Graham במאמר ב-Atheroscleros משנת 1995. אך לא קיימים מחקרי התערבות מבוקרים עם הפחתה בררנית של (Lp(a שתשפיע על התחלואה הקרדיו-וסקולארית. מחקר AIM-HIGH כלל 3414 חולים עם מחלה טרשתית מוכחת וריכוז LDL מתחת ל-80 מ"ג/ד"ל. מבין משתתפי המחקר, 1718 טופלו עם ניאצין, ו-1696 עם פלצבו. המחקר הופסק לאחר 3 שנים בהעדר הגנה מפני אירועים קרדיו-וסקולאריים, כל זאת למרות האפקט המובהק על שומני הדם (HDL, טריגליצרידים ו-LDL-כולסטרול) בתום שנתיים מתחילת המחקר: מתוך עיון בנתוני המחקר עולה כי (Lp(a נבדק רק בסיום שנה ראשונה. בקבוצת ההתערבות חלה ירידה מהממוצע המדיאני של 36.1 ל-27.1 ממו'ל/ליטר, זאת על פי Boden במאמר ב-N Eng J Med משנת 2011.
(Lp(a ומחלה צרברו-וסקולארית
נתוני מחקר מראים שרמות מוגברות עלולות להגביר מפגעים צרברו-וסקולאריים, כאשר ממצא זה חזק יותר בגברים. מטה-אנליזה שכללה נתונים מ-56,010 נבדקים, בהם התרחשו 4,606 אירועים מוחיים, הראתה OR של 1.1-1.22 באלה עם רמות (Lp(a בשלישון העליון של המדגם לעומת אלה עם רמת (Lp(a בשלישון התחתון. ניתוח נתונים מ-6 מחקרים, מצא עליה של פי-2.14 בשבץ מוחי איסכמי באלה עם (Lp(a מוגבר. נראה שהקשר בין רמות מוגברות של (Lp(a לבין מפגעים קרדיו-וסקולאריים מובהק יותר מהקשר דומה למפגעים צרברו-וסקולאריים.
האם יש לכלול מדידת רמת (Lp(a בשגרת בדיקות המעבדה?
(Lp(a אינה בדיקה המתבצעת באופן שגרתי כבדיקת סקר או במסגרת פרופיל ליפידים. הנחיות ה-NCEP במסגרת ה- "Adult Treatment Panel III", מתבטאות בהכרה בשימושיות האפשרית של מדידת (Lp(a, אך אינן ממליצות עליה כבדיקת סקר. ה-NACB (האקדמיה הלאומית של ביוכימיה קלינית), ממליצה על מדידת מדד זה רק באלה עם היסטוריה משפחתית חזקה של מחלה קרדיו-וסקולארית בגיל צעיר, בעיקר כיוון שקשה להפחית רמות מוגברות בלאו-הכי. רק כאשר רמת (Lp(a מתקבלת באחוזון 95 מומלץ על ידי ה-EAS לנקוט בטיפול נמרץ יותר להפחתת LDL, שכן רמות גבוהות ממש של (Lp(a עלולות להגביר סיכום ל-CVD במשולב עם רמות LDL מוגברות. סקירה עדכנית של Ridker ו-Libby מעלה ספק אם קביעת הסטאטוס של (Lp(a מוסיפה אמנם מידע פרוגנוסטי להערכת הסיכון במניעה ראשונית של CVD, אלא אם כן מדובר באלה בסיכון גבוה, בגין נוכחות גורמי סיכון אחרים, ובעיקר רמה מוגברת של LDL .
מטה-אנליזה משנת 2009 שהקיפה 36 מחקרים שכללו במקובץ 126,334 מטופלים, הגיעה למסקנה ש-(Lp(a הוא גורם סיכון בלתי-תלוי אם כי מתון של מחלת לב כלילית ושבץ מוחי. ריכוזי (Lp(a גבוהים פי-3.5 מרמת מרמתו באוכלוסייה מעלים על פי נתונים אלה את הסיכון ל-CHD ב-13% בממוצע, לאחר התאמה לגורמי סיכון אחרים, לפי הפירוט הבא: עליה של 16% ב-CHD, עליה של 14% במקרי מוות כליליים, עליה של 12% במקרי MI לא-קטלניים, עליה של 10% במקרי שבץ ועליה של 1% במוות מסיבות לא-וסקולאריות. נתוני מחקר זה הביאו את EAS האירופי לצדד בשלב הראשון בבדיקות סקר נרחבות לרמת (Lp(a, החלטה שגררה תגובות, וויכוח נוקב בעולם כולו. על פי Ridker במאמר משנת 2011 ב-Circulation כל זמן שאין בנמצא טיפול מוכח המפחית תחלואה ותמותה קרדיווסקולרית בתגובה לירידה בריכוז (Lp(a, אין מקום לבדיקה אלא באמת במקרים נבחרים. דעה אחרונה מתחזקת לאור ממצאי הניסויים AIM-HIGH ו-HPS2-THRIVE, שלא מצאו יתרונות קליניים בהוספת ניאצין לטיפול בסטאטינים.
סקירה של Graham שהתפרסמה בשנת 2007 ב-Eur Heart J ממליצה לבדוק (Lp(a במצבים של סיכון בינוני או מוגבר לתחלואה קרדיווסקולרית, זאת כאשר מתקיימים בנבדק תנאים מוקדמים כגון תחלואה לב קודמת; היפר-כולסטרולמיה משפחתית; סיפור משפחתי של תחלואה קרדיו-וסקולארית בגיל צעיר, עלייה משמעותית בבדיקה קודמת של (Lp(a ; תחלואה קרדיווסקולרית למרות טיפול מיטבי בסטטינים; סיכון קרדיו-ווסקולארי הגדול מ-3% ל-10שנים לפי הנחיות אירופאיות; סיכון קרדיו-וסקולארי גדול מ-10% לפי הנחיות אמריקאיות של NCEP שהתפרסמו ב-2004 ב- Arterioscler Thromb Vasc Biol. ועדת מומחים בראשות Davidson פרסמה בשנת 2009 ב-J Clin Lipidol את ההמלצות לבדיקת סמנים דלקתיים. הועדה מסכמת כי בנבדקים עם סיכון נמוך מ-5% ל-10 שנים, אין המלצה לבדיקת (Lp(a, ואילו בקבוצת סיכון בינוני של 5-20% ל -10 שנים, או עם תחלואה דמוית CHD יש לשקול בדיקת (Lp(a. ריכוז (Lp(a מתחת 25mg/dl שולל נוכחות (Lp(a כגורם סיכון משמעותי, אם כי מעבדות רבות משתמשות בערך של 30 מיליגרם/ד'ל כערך המבדיל בין סיכון נמוך למוגבר.
עדכונים על טכנולוגיות מעבדתיות שונות למדידת (Lp(a
כבר מתחילת שנות ה-90 הודגש הצורך בסטנדרטיזציה בינלאומית למדידת רמות (Lp(a, זאת בגלל הדרגה הגבוהה של הטרוגניות בגודל המרכיב החלבוני apo(a), הנובע מהשונות במספר של K4 type 2, המביא למספר שונה של אפיטופים על פני (apo(a, איתם יכולים להגיב הנוגדנים בהם משתמשים בשיטות ה- immunoassay למדידת רמת (Lp(a בפלזמה. בשיטת מדידה זו יכולה להתעורר בעיה לגבי התגובתיות של הנוגדן המסחרי הכלול בערכת המבדק, עלול להגיב באופן שונה עם ה- (apo(a המופיע בגדלים שונים. כתוצאה מכך, ה-immunoassay יראה נטייה להמעיט את רמת (Lp(a בדגימות פלזמה עם (apo(a בגרסה הקטנה יותר, וייתן הערכה מוגברת-כזובה בדימות עם גרסת (apo(a גדולה יותר.
השיקולים האחרונים הביאו את ה-IFCC להקים קבוצת עבודה שמסקנותיה היו ששיטת מדידה אימונו-טורבידימטרית (ITA) על בסיס גרגירי Latex, היא השיטה היחידה שאינה רגישה לגודלו של (apo(a. ועדה בראשותה של Marcovina, פרסמה מסמך שהשווה בין שיטות מדידת (Lp(a בערכות של 16 יצרנים שונים, שבחנו אותם ב-6 מעבדות מחקר. נקבע ששתיים מהערכות, אלה של New Berkeley Extended Range Lp(a) test, וכן זו הידועה כ-Denka Seiken Assay, הראו את המתאם הטוב ביותר עם ערכי ה-reference הבינלאומיים המומלצים. בשיטת ITA מגיב הנוגדן שבערכה עם החלבונים בדגימה הנבדקת, ליצירת תלכיד בלתי מסיס, המגביר את העכירות. ניתן למדוד את דרגת העכירות בשיטה אופטית, והיא פרופורציונית לכמות החלבון בדגימה. שיטה זו ניתנת ליישום באנלייזרים אוטומטיים. בשיטת Berkeley החדשה, אף היא טורבידומטרית, יש הכרה של טווח רחב יותר של הואריאנטים השונים של (apo(a. בנוסף, שיטות ה-ITA הן לינאריות לטווח ריכוזים רחב יותר המגיע עד 200 מיליגרם/ד"ל. אכן, בהשוואה של שיטות ה-ELISA הקודמות עם שיטות ITA העדכניות, נמצא שערכים ממוצעים של 20 מיליגרם/ד"ל שנקבעו בשיטות הישנות, נתנו כעת תוצאות עם ממוצע של 30 מיליגרם/ד"ל.
תרחישים התורמים לעלייה ברמת (Lp(a הם דעיכה ברמת האסטרוגנים בגוף, היפרכולסטרולמיה משפחתית, היפותירואידיזם חמור, סוכרת שאינה בשליטה, כשל כליות כרוני ותסמונת נפרוטית.
הוראות לביצוע הבדיקה
יש להיות בצום של 12 שעות לפני הבדיקה, וניתן לשתות רק מים. אין לעשן מספר שעות לפני הבדיקה. כיוון ש-(Lp(a מתנהג כמו acute phase protein, אין לבצע את הבדיקה אלא אם כן חלפו חודשיים מאירוע של התקף-לב אירוע מוחי, ניתוחים, הידבקות חיידקית או נגיפית מלווה בחום, פציעה או היריון.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק