חומצה פיפקולית - Pipecolic acid
| מדריך בדיקות מעבדה | |
| חומצה פיפקולית | |
|---|---|
| Pipecolic acid | |
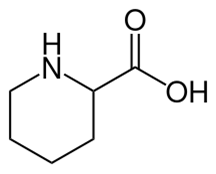
| שמות אחרים | Piperidine-2-carboxylic acid,.PIP, PIPA |
| |
| מעבדה | כימיה בדם |
| תחום | מחלות פראוקסיזומליות. |
| טווח ערכים תקין | <6 months: ≤6.0 nmol/mL, 6 months-<1 year: ≤5.9 nmol/mL, 1-17 years: ≤4.3 nmol/mL; ≥18 years: ≤7.4 nmol/mL. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
זיהוי עליות אנומליות של PA בנסיוב, לצורך הבדלה בין מפגעים של הביוגנזה הפרוקסיזומלית (כגון תסמונת Zellweger) לבין מפגעים בהם יש אובדן של תפקיד פרוקסיזומלי בודד.
PA היא תרכובת אורגנית שהיא למעשה נגזרת של חומצה קרבוקסילית של piperidine, ובתור שכזו PA היא חומצת אמינו. למרות היות PA כירל, ה- S-stereoisomerשכיח יותר. PA הוא בעל משקל מולקולרי של 129.15, ובעל נוסחה אמפירית של C6H11NO2. הביוסינתזה שלו מתחילה מליזין (Gatto וחב' ב- J Am Chem Soc משנת 2006). CRYM, שהוא חלבון taxon-specific שנקשר גם כן להורמוני תירואיד, כרוך אף הוא במסלול של PA. חומצה פיפקולית מצטברת ב-pipecolic acidemia, ועליה ברמותPA כרוכה במספר צורות של אפילפסיה, כגון pyridoxine-dependent epilepsy (Plecko וחב' ב-Neuropediatr משנת 2005, ו-Kaminiòw וחב' ב-Brain Sci משנת 2021). בדומה לרוב חומצות האמינו, PA הוא כירל בעל יכולת כלציה, כאשר קומפלקס הוא Cu(HNC5H9CO2)2(H2O)2 (Kveholden וחב' ב- Proc Natl Acad Sci USAמשנת 1971). PA זוהה ב-Murchison meteorite (Kite וחב' ב-Phytochem משנת 2015).PA מצוי גם בעלים שלMyroxylon , עץ בדרום אמריקה. פרכוסים מסיבה של תלות בפירידוקסין: כיצד ניתן להסביר את המאפיינים הקליניים והנוירוכימיים של מטופלים עם pyridoxine-dependent seizures? (Gospe Jr ב-Pediatr Neurol משנת 2002). שני מנגנונים אפשריים ראויים לדיון: עלייה ברמת PA הודגמה בפלזמה וב-CSF של שלושה מטופלים עם pyridoxine-dependent seizures . כאמור, PA הוא מטבוליט ביניים של פירוק ליזין ב-CSF אשר במהלך זה מוביל ליצירת α-aminoadipic acid, מצע של האנזים-תלוי-פירידוקסין, α-aminoadipic acid transaminase. רמותα-aminoadipic acid לא היו מוגברות במטופלים אלה, מה שרומז לכך שהפעילות הנורמלית של האנזים תלוי-פירידוקסין ו-PA נמצאו מגבירים את הפרשת γ-aminobutyric acid בקדם-סינפסה. יחד עם זאת, כפי שהוצע על ידי Plecko וחב' בשנת 2005, המוגברוּת של PA יכולה לשמש כסמן מטבולי חשוב במטופלים עם pyridoxine-dependent seizures ויכולה לסייע באבחון של מפגע זה. PA מוגברת בדם וב-CSF אך אינה ספציפית לתרחיש של pyridoxine-dependent seizures. עלייה של L-α-aminoadipic semialdehyde והיחס שלו לקראטינין בשתן הם אבחוניים, ורמתו בדרך כלל יורדת לאחר טיפול. רמות תראונין, גליצין, טאורין ו-3-methoxytyrosine עשויות לעלות, בדומה לחסר של pyridoxine-5′-phosphate oxidase , בעוד שגליצין, טאורין וגלוטמין דרך כלל מוגברים בדם.
מפגעים פראוסיזומליים:
Pipecolic academia: באדם, L-pipecolate oxidase (להלן PIPOX) הוא אנזים פראוקסיזומלי האחראי לפירוק של PA. PIPOX גם מפרק סרקוזין אך יש לו עדיפות לפירוק של חומצהL-פיפקולית. תוך שימוש בטכניקות ביטוי RNA שונות, PIPOX נמצא מבוטא במגוון רקמות, אך מתורגם רק בכליות ובכבד, בהיותו ממוקם יחד עם האנזים catalase בפראוקסיזומים באופן מנוקד. שלא בדומה ל- pipecolic academia שניונית כתוצאה מ-PBD (להלן .(peroxisomal biogenesis disorders pipecolic academia מבודדת, אינה קשורה ישירות לחסר ב-PIPOX (Dasouki ב-Biomarkers in Inborn Errors of Metabolism משנת 2017).
Hyperpipercolic academia: כלי אבחוני למפגעים פראוסיזומליים.
מפגעים פראוקסיזומליים כוללים קומפלקס של מחלות המאופיינות על ידי הטרוגניות גבוהה מנקודת המבט הקלינית והביוכימית. מבדקים ספציפיים נדרשים בלימוד של מטבוליזם פרוקסיזומלי, כגון הערכה של PA. התפקיד האבחוני של PA נקבע ב-30 מטופלים עם פגיעה פרואוקסיזומלית (5 מטופלים עם תסמונת Zellweger, 10 מטופלים עם infantile Refsum diseases, מטופל אחד עם rhizomelic chondrodysplasia punctataneonatal adrenoleukodystrophy, 6 מטופלים עם מפגע פרוקסיזומלי בביוגנזה, מטופל אחד עם rhizomelic chondrodysplasia punctata, 2 מטופלים עם 2 acyl-CoA oxidase deficiencies, 2 מטופלים עם חסר אנזימים דו-תפקודיים, 2 מטופלים עם מחלת Refsum, ומטופל אחד עם חסר של β-oxidation). נמצא ש-PA היה מוגבר בכל המפגעים הפראוקסיזומליים, בעוד שPA- נורמלי עם ריכוזים אנומליים של חומצות שומן ארוכות מאוד שרשרת, היוו עדות חזקה לחסר יחיד של אנזים פראוקסיזומלי. מפגעים פראוקסיזומליים מייצגים ספקטרום רחב של מחלות מטבוליות מורשות באדם.
מחלות אלו מורכבות מלפחות 20 וריאנטים, שרובם כרוכים במעורבות נוירולוגית. ביוכימית, מחלות אלו מתחלקות ל-PBD, בהן חסרים מספר תפקודים פראוקסיזומליים, ומאלה עם חסר פראוקסיזומלי אנזימטי בודד. האבחון של מפגעים פראוקסיזומליים מתבצע בדרך כלל על ידי אנליזה של חומצות שומן מאוד ארוכות שרשרת, של חומצות phytanic ו-pristanic, ומדידה שח חומצות מרה בפלזמה. כמו כן נמדדות רמות שלplasmalogens בממברנות של אריתרוציטים ונמדדת פעילות האנזים DHAP-AT synthase בלויקוציטים ובאריתרוציטים. PA מוגבר משמעותית בכל המטופלים עם מפגעי ביוגנזה פראוסיזומלית מסוג PBD עם ערך חציוני של 56.6 μmol/L, ערך חציוני של 22 μmol/L למטופלים עם Zellweger syndrome, ערך חציוני של 82.2 μmol/L למטולים עם Infantile Refsum Disease, ערך חציוני של 22 μmol/L למטופלים עם non-alcoholic liver Disease, וערך חציוני של60.3 μmol/L למטופלים עם PBD עם תסמינים אטיפיים.
הוראות לביצוע הבדיקה: על הנבדק לצום 12 שעות או למעלה מכך, ובאשר לתינוקות יש לאסוף דגימת דם ממש לפני האכלה. מדובר על נטילת הדם במבחנה כימית (פקק אדום או צהוב) ולאחר הסרכוז יש להעביר את הנסיוב למבחנת פלסטיק. יש לצרף למעבדה את גילו של הנבדק. ניתן לבצע את הבדיקה גם אם הנסיוב מאוד המוליטי, ליפמי ואיקטרי. הדגימה יציבה למשך 94 יום (מועדף), או 14 יום בקירור. הבדיקה מתבצעת על ידי stable isotope-dilution gas chromatography mass spectrometry(GC-MS) או על ידי amino acid chromatography.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק 