לפטין - Leptin
| מדריך בדיקות מעבדה | |
| לפטין | |
|---|---|
| Leptin | |
| מעבדה | אנדוקרינולוגיה בדם |
| תחום | הערכה הורמונאלית של מצבי השמנת יתר, הערכת רמת השומן בגוף והסבר להיפו-גונאדיזם או איחור בהתפתחות המינית. |
| טווח ערכים תקין | ערכי ייחוס לילדים וילדות:
בבנות בשלבים 1 ו-2 של מדרג Tanner נמדדו ערכי לפטין בטווח שבין 0.22 ל-145 מיקרוגרם לליטר. טווח ערכים רחב זה בילדות/בנות עם ערכי BMI של 11 עד 37, המבטאים רזון בולט עד השמנת יתר בולטת. ערכי החציון של לפטין בבנות עם ערך BMI תקין של 19-25 הם בין 4.87-21.8 מיקרוגרם לליטר.
בבנים בשלבים 1-2 במדרג Tanner, נרשמו רמות לפטין בטווח שבין 0.08-144 מיקרוגרם לליטר. ערכי החציון בבנים עם ערכי BMI בין 19-25 נמדדו בין 2.5-12.7 מיקרוגרם לליטר. לבנים בשלבי 3-4 במדרג Tanner נמדדו ערכי לפטין בין 0.32-148 מיקרוגרם לליטר, עם ערכים ממוצעים בין 14.8-19.7 מיקרוגרם לליטר.
|
| יוצר הערך | פרופ' בן עמי סלע |
בסיס פיזיולוגי
גילוי לפטין ומחקרים מוקדמים
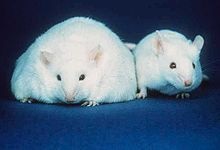
ההשערה על קיומו של הורמון המווסת קצב אכילה ומשקל גוף, עלתה כבר בשנת 1950 במעבדות Jackson בארה"ב במהלך ניסויים בזן עכבר שמן במיוחד שצץ במושבת העכברים שם כתוצאה ממוטציה. עכברים הומוזיגוטיים למוטציית ob, הרבו לאכול באופן בלתי מרוסן, ובהתאם צמחו במימדיהם ובמשקלם באופן בולט ביותר. בשנת 1998 הביא Harvey על ידי הרס של חלק מההיפותלמוס במוח של חולדות להשמנה ניכרת שלהם, והסיק מכך שיש כנראה הורמון בדם הפועל ברמת ההיפותלמוס ומונע השמנה.
בשנות ה-60 זיהה Coleman באותה מעבדה מוטציה שנייה בגן db, שאף היא גורמת להשמנת-יתר. תוך שימוש בטכנולוגיה של positional cloning עלה בידי החוקרים אז לזהות את הגן הפגום, ובשנת 1990 היו אלה Leibel ו-Friedman שמיפו את הגן ב-2 מאמרים שהופיעו ב-PNAS וב-World Review of Nutritional Diabetes.
מחקרים נוספים בשנים 1992-3 אישרו שהגן ob מקודד להורמון המופיע בדם והפועל בעיקר לדיכוי אכילה והגדלת משקל גוף בעכברים נורמאליים, אך לא מדכא אכילה בעכברים עם המוטציה בגן ob. בשנת 1994 התפרסם ב-Nature מאמרו המכונן של Friedman מאוניברסיטת רוקפלר, על בידוד הגן ob, ועל החלבון לו הוא מקודד, שכונה leptin. הורמון זה הוא למעשה הראשון שזוהה שמקורו בתאי שומן. מחקרים בהמשך אישרו שהגן db מקודד לחלבון המהווה קולטן של לפטין, הבא לביטוי בעיקר בהיפותלמוס.
בבני אדם ממוקם הגן ob על כרומוזום 7q31, כאשר ה-DNA שלו מכיל כ-15 אלף זוגות בסיסים, היוצרים 3 אקסונים. לפטין נוצר ומופרש בעיקר על ידי רקמת השומן הלבנה, אם כי כמויות קטנות מאוד שלו מופרשות גם מרקמת שומן חומה, וכן מתאי סינציוטרופובלסטים בשלייה, מהשחלות, מתאי שריר שלד, מתאי Chief ותאי חיפוי P/D1 בתחתית הקיבה, מתאי אפיתל של בלוטות השד, ממח העצם, מיותרת המוח, מהכבד, ומרקמות לב וסחוס עובריות.
לפטין הוא הורמון חלבוני המיוצר בתאי שומן וברקמות שומניות, משם עובר הלפטין במחזור הדם עד שהוא עובר את מחסום דם-מוח דרך מערכת טרנספורט. ההורמון ממלא תפקיד מרכזי בוויסות צריכת אנרגיה והוצאתה על ידי ויסות התיאבון וחילוף חומרים. הלפטין מורכב מ-167 חומצות אמינו ושמו נגזר מהמילה היוונית Leptos שפירושה "רזה". כיום אנו יודעים שפעילות לפטין אינה מצטמצמת לפעילות הורמון אנדוקריני המופרש מרקמת שומן ומשפיע על ידי הגעתו למוח, אלא שלפטין פועל גם כמתווך פרקריני.
בשנת 2002 הופיע ב-Nature מאמר של Kahn וחב' בו נמצא שלפטין גורם בתאי השריר לעיכוב האנזים acetyl coenzyme A carboxylase, שהוא אנזים מפתח בסינתזה של שומנים. בכך מסיט הלפטין מסלול שאמור היה להביא ליצירת שומן למסלול המחמצן חומצות שומניות ליצירת אנרגיה בשריר, ומונע אגירה של אותן חומצות שומן בתאים, מה שגורם כמובן להרזיה. Friedman מצא שלפטין מדכא בכבד את פעילות האנזים החיוני בסינתזה של חומצות שומן בלתי-רוויות SCD-1 או stearoyl-CoA desaturase-1. בדיכוי פעילות אנזים זה על ידי לפטין, מוגברים שעורי הפעילות המטבולית, עולה צריכת האנרגיה ונמנעת אגירת שומן בכבד.
ההורמון לפטין מופרש מרקמת שומן ורמתו במתאם עם רמת השומן בגוף. הלפטין מדווח להיפותלמוס על מצבי שובע, ומפחית את התיאבון, וכתוצאה מכך יש ירידה בתצרוכת הקלורית. במצבים של רעב, תת תזונה או אנורקסיה, רמות הלפטין נמוכות. באנשים בעלי עודף משקל, רמות הלפטין תהיינה גבוהות, אולם בגלל תנגודת ללפטין אשר מתרחשת כנראה בגלל ריוויון של הרצפטורים ללפטין בהיפותלמוס, לא ידוכא התיאבון.
לפטין אינו מופרש מיד לאחר ארוחה, אלא עוברות מספר שעות עד שרמתו עולה משמעותית, והוא אמנם משתייך למנגנון בקרת שובע לטווח הארוך. הפרשת הורמון זה באדם היא פעימתית כאשר משך פעימה כמחצית השעה. אכן, לפטין מווסת מערכות גוף שאף הן פעימתיות באופיין כמו ציר היפותלמוס-היפופיזה-אדרנל., וכן הגונאדות.
רמות לפטין פוחתות לאחר צום למשך 72- 24 שעות, למרות שלא ניכרים במטופל בהכרח שינויים במסת השומן בתום תקופת צום קצרה זו. באנשים לא-שמנים, שינה עמוקה ומתמשכת של 8-12 שעות, מגבירה רמות לפטין, ואילו רמתו עלולה לרדת במניעת שינה. רמות לפטין גדלות בעת עקה רגשית, אך פוחתות עם העלייה ברמות טסטוסטרון, ומוגברת עם העלייה ברמות אסטרוגנים. פעילות ואימון גופני ממושכים מפחיתים רמות לפטין.
פרט לתפקיד לפטין בוויסות מאזן האנרגיה על ידי דיכוי תיאבון והגברת צריכה של אנרגיה, משמש לפטין גם כהורמון המשפיע על תהליכים מטבוליים רבים בגוף דוגמת הפרשת אינסולין וליפוליזה, בעל תפקיד במערכת הרבייה, במערכת הדחק, ונמצא בקשר הדוק עם הציר היפותלמוס-היפופיזה-אדרנל. לפטין משפיע על בלוטת התריס ועל פעילותה בחילוף חומרים, ברבייה ובגדילה. לפטין נכרך גם עם המטופויאזה ואנגיוגניות (יצירת כלי-דם חדשים). בנוסף לפעילותו בהיפותלמוס לפטין פועל ישירות על תאי כבד ושריר שלד בהם הוא מעודד את ה-β אוקסידציה של חומצות שומן במיטוכונדריה, מה שמפחית את אגירת השומן ברקמות אלה אם כי לא ברקמת השומן.
הרמות הממוצעות של לפטין בגוף באנשים בריאים מראות שונות ניכרת, למעשה בין 1.8-78.4 מיקרוגרם לליטר, בגין שונות ניכרת של מסת השומן בגוף וכן בתלות במין הנבדק. תקופת מחצית החיים של לפטין היא בת 24 דקות, והוא מופיע בפלזמה כמקטע חופשי, כאשר הרוב קשור לחלבוני הדם ובעיקר לאלבומין, בעוד שכ-10% מחלבונים אלה הם הקולטן ללפטין בצורתו המסיסה. המקטע החופשי של לפטין בבני אדם שמנים גדול יותר מאשר באלה עם משקל גוף תקין, כנראה כתוצאה מריווי של אתרי הקישור של לפטין על פני חלבוני הדם.
מנגנון הפיקוח המוחי על מצבי רעב ושובע
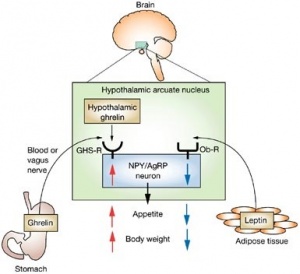
נראה שתחושות התיאבון והשובע נמצאות בשליטה של 2 מנגנונים: קיים פיקוח קצר-טווח הקובע כמה נאכל ביום מסוים, ובמקביל קיים מנגנון מפקח בטווח של חודשים ושנים. בטווח הקצר פועלים שני הורמונים פפטידיים הנוצרים במערכת העיכול: האחד הוא ghrelin הנוצר בקיבה והאחר הוא PYY שמקורו במעי. לעומתם לפטין, ובמידה יותר פחותה- אינסולין, מפקחים על יציבות המשקל לטווח ארוך. יש גם התקדמות בהבנת אזורי המוח הקולטים את פעילויותיהם של ארבעת ההורמונים האמורים, ושיגור אותות לגוף המווסתים את כמות המזון שהוא אמור לקלוט, ואת כמות האנרגיה שניתן להוציא בפעילות גופנית.
כך נמצא למשל האזור הקרוי ARC או Arcurte nucleus, הממוקם בתחתית ההִיפותָלָמוס המוחי. ה-ARC מכיל 2 סוגים עיקריים של תאי עצב, בעלי פעילות מנוגדת. שפעול של סוג נוירונים אחד מביא לייצור של 2 נירוטרנסמיטורים פפטידיים המעודדים את התיאבון ומפחיתים את רמת המטבוליזם בגוף. שני פפטידים אלה קרויים: NPY או neuropeptide Y ו-AgRP או agouti-related peptide. לעומתו, קבוצת הנוירונים המנוגדת בפעולתה, ידועה כ-POMC/CART, גורמת לשחרורו של ההורמון α-MSH אוα-melanocyte stimulating hormone, המדכא תיאבון ואכילה. כאשר מאגרי השומן בגופנו קטֵנים ומתמעט ייצור לפטין בתאי השומן, משופעלים דווקא הנוירונים בצמד NPY/AgRP, ומדוכא צמד הנוירונים POMC/CART, וכך מתגבר התיאבון והמשקל עולה. היפוכו של דבר כאשר מתמלאים מאגרי השומן: עולה רמת לפטין בדם והוא מביא לעיכוב של הנוירונים NPY/AgRP ולשפעול מערכת POMC, מה שיביא לאיבוד משקל. יש לציין שההורמון ACTH הוא נגזר של חלבון POMC ולפיכך חסר ב-POMC יגרום מלבד השמנה, גם לתופעות של אי-ספיקת בלוטת הכליה (מחלת אדיסון) וכן לפיגמנטציה לא תקינה.
כיצד משדרים שני זוגות הנירוטרנסמיטורים שהוזכרו את המסר לגוף בדבר צורך מיידי לאכול או שמא לחדול מאכילה? המסרים נשלחים דרך מרכזי מוח נוספים המנקזים את האותות אל אזור הממוקם בגזע המוח והידוע כמרכז השובע NTS או nucleus tractus solitarius, ומשם יורדים איתותי אכילה או צום לשאר חלקי הגוף. מחקרים בלתי-תלויים שנערכו בארה"ב ובצרפת הראו שלמעשה מספר האנשים שיש להם מוטציות בייצור לפטין או בקולטנים המוחיים ללפטין, קטן ביותר. לעומת זאת, הרבה יותר שכיחים המקרים בהם נמצאו מוטציות בקולטן להורמון α-MSH הקשור לדיכוי התיאבון והאכילה. הנתונים והידע המצטברים מהבנת המערכת המורכבת הזאת של 4 הורמונים הפועלים במוח ושולטים על הרגלי האכילה שלנו, מצביעים על כך שמערכת הפיקוח על מאזן הקלוריות באדם נוטה באופייה להגן יותר מפני איבוד משקל, מאשר מפני עלייה במשקל. הדבר לבטח מבטא התפתחות אבולוציונית היסטורית, שבה עד לעת האחרונה, חוסר מזון ורעב הטרידו את האנושות, והסכנה לא נשקפה דווקא מאכילת-יתר.
אך מאותה נקודת זמן, מתגלים פפטידים חדשים, שמקורם בעיקר במערכת העיכול אך השפעתם כמקובל לגבי הורמונים, באזורי מטרה מרוחקים, כגון המוח. כך נכנס המרכיב CCK או cholecystokinin, שאחת מצורותיו פפטיד חלבוני קצר (8 חומצות אמינו) המיוצר במעי ומועבר דרך מסילת אחד העצבים הארוכים בגופנו ה-Vagus (העצב התועה), אל מרכז השובע, NTS, במוח. CCK פועל על ידי הארכת השהייה של מזון בקיבה ודיכוי התיאבון, והשפעתו מהירה. מסתבר שהפפטיד CCK אינו מְתָאֲבֵן, אלא דווקא מְדָכא תיאבון.
פסיכיאטרים באוניברסיטת Johns Hopkins התמקדו במחקריהם בנושאי תיאבון ואכילה בחולדה מהזן OLETF, שיש לה פגם גנטי הגורם לה להרבות באכילה וקושי להגיע לשובע. הסתבר שחולדה זו חסרה קולטנים לפפטיד CCK, וכיוון שכך בהיפותלמוס שלה יש התבטאות מוגזמת של NPY או neuropeptide Y, אחד משני הנירוטרנסמיטורים המוחיים המגבירים תיאבון.
פסיכולוגים מאוניברסיטת פרינסטון דיווחו בפברואר 2003 בכתב העת Brain Research נתונים נוספים על תפקיד ה-CCK בוויסות השובע. חוקרי פרינסטון הזריקו לאחד מגרעיני ההיפותלמוס במוחות של חולדות את הנירוטנסמיטור סרוטונין, או את הפפטיד CCK, מה שהביא לדיכוי תאבונן של החולדות. נראה שסרוטונין ו-CCK משפיעים באופן דומה על הקטנת ההפרשה של דופאמין באזור המוחי הידוע כ-nucleus accumbens, אך לעומת זאת, הם מגבירים הפרשה מוחית של אצטיל-כולין הידוע כחומר מדכא אכילה ויוצר תחושת שובע.
דיכוי תיאבון הנגרם על ידי לפטין הוא כאמור ארוך טווח. בניגוד לעיכוב התיאבון המהיר הנגרם על ידי CCK, או הדיכוי האיטי יותר של רעב בין הארוחות הנגרם על ידי PYY3-36. מספר מחקרים הראו שצום או דיאטה מצומצמת ביותר בקלוריות, מפחית רמות לפטין, באופן הגורם למערכת להיות רגישה יותר לרעב מאשר לאכילת יתר. השינויים ברמות לפטין גדולים יותר כאשר צריכת מזון פוחתת מאשר כאשר היא מוגברת.
עד כה התגלו מספר מקרים של השמנה יוצאת דופן ב-2 משפחות שהיו הומוזיגוטיות לשני סוגי מוטציות בגן ob: מוטציית frameshift במשפחה אחת, ומוטצית misseense במשפחה האחרת. כמו כן השמנה קיצונית התגלתה בשלוש אחיות בנות משפחה אחת שהיו הומוזיגוטיות לגבי המוטציה db, דהינו הגן המקודד לקולטן ללפטין, וסבלו גם מחוסר בגרות מינית. לעומת זה אנשים שהם הטרוזיגוטים לגבעי 2 מוטציות אלה, מראים השמנת-יתר מתונה.
אחד המקרים שזכו לתהודה רבה, התפרסם בספטמבר 1999 ב-NEJM בו דווח על תוצאות מרשימות של טיפול בתכשיר לפטין ריקומביננטי בילדה אנגליה בת 9 שנים שהתבררה כהומוזיגוטית למוטצית frameshift בגן ob: מדובר בילדה ששקלה 94.4 ק"ג בתחילת הניסוי מתוכם 55.9 ק"ג היו רקמת שומן. היא הוזרקה מדי יום עם התכשיר הריקומביננטי למשך שנה. בתום הניסוי היא איבדה 16.4 ק"ג ממשקלה (כאשר רוב המשקל שפחת היווה רקמת שומן). הטיפול הביא לירידה ניכרת בתיאבון ובצריכת המזון שלה: הילדה בת ה- 9 נהגה לאכול ארוחה ממוצעת גדושה ב- 1100 קלוריות, ולאחר מספר בודד של הזרקות לפטין חלה ירידה של כ- 84% בצריכה הקלורית לארוחה, וילדה זו הסתפקה מכאן ואילך ב- 180 קלוריות לארוחה, בדיוק כמות צריכת האנרגיה האופיינית לגילה. הופיעו אצלה בעקבות הטיפול גם סימני בגרות מינית שלא נראו בה קודם לטיפול. תוצאות של הזרקת לפטין ריקומביננטי לאנשים שמנים ללא המוטציות האמורות לא הניבו תוצאות משמעותיות בהפחתת משקל.
הקולטנים של לפטין
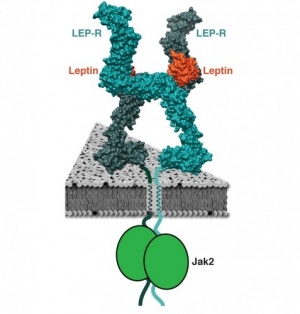
קולטני לפטין משתייכים למשפחת הקולטנים לציטוקינים כגון IL-6. ידועים כ-5 קולטנים של לפטין, כאשר מבדיל ביניהם אורכו של הקטע הציטופלמי שלהם החודר מבעד לממברנת התאים. כל הקולטנים הללו מקודדים על ידי הגן LEPR (הידוע גם כ-CD295). מתוך קולטנים אלה, רק האיזופורם Ob-Rb הוא קולטן ארוך באופן שמאפשר לו לחצות את הממברנה של תאי היפותלמוס ולהתקשר על ידי שליחת איתותים תוך-תאיים עם ערכות המשגרות איתותים אלה דוגמת Jak-Stat ו-MAPK או mitogen-activated protein kinase.
הקולטן Ob-Rb נפוץ פרט להיפותלמוס גם בחלקי מוח אחרים כגון המוחון, אך גם ברקמות היקפיות במידה מועטה כמו רקמת שומן, בלבלב, בשרירי השלד, בכבד, באשכים, בתאים אנדותליאלים, במקרופאגים, ובתאי-T. העברת האיתותים התוך-תאיים נעשית על ידי שפעול של חלבוני Janus kinase או JaK, האחראיים לזרחון של חלבוני STAT3 או Signal Transduction & Activator of Transcription החודרים אל תוך גרעין התא ומחישים שם את הביטוי של גנים שונים.
קולטנים קצרים יותר של לפטין כמו Ra, Rc ו-Re אינם משפעלים את חלבוני STAT3, אך מסייעים ללפטין לחלוף דרך ממברנות תאים, וייתכן שיש להם תפקיד במעבר לפטין דרך מחסום דם-מוח באזור ה-choroid plexus, כמו גם לפינוי לפטין מזרם הדם. צורת הקולטן הקצרה-Ra, מופיעה ב-choriod plexus, כמו גם ב-leptomeninges, ברקמת השומן, בשרירים, בכליות ובריאות. האיזופורם Rc מופיע ברקמת השומן ובלב, ואילו האיזופורם Re שהוא מסיס קושר כעשירית מכלל כמות הלפטין בפלזמה.
אחת הסיבות האפשריות לתופעת התנגודת ללפטין, יכולה לנבוע מתפקוד לקוי של הקולטן המוחי ללפטין. Skiniotis וחב' מאוניברסיטת Michigan הדגימו בעזרת מיקרוסקופ אלקטרוני לראשונה את יחסי הגומלין בין לפטין וקולטנו. ממצאים אלה מתארים כיצד הקולטן פועל בעזרת 2 זרועות ציר, שנוטות להסתובב עד שהן מגיבות בקשירת מולקולת לפטין, באופן הגורם לקולטן להתקשח יותר. נראה שבשלב זה מועברים איתותי התצמיד לפטין קולטן לאנזים Janus kinase. עם הגיל חלה ירידה במספר הקולטנים ללפטין במוח, מה שתואם את הנטייה לעלייה במשקל בגיל המתקדם.
ההורמון α-MSH נקשר לקולטן בשם Mc4R, וגורם לדיכוי תיאבון. פגם בקולטן יגרום להשמנה מגיל מאד צעיר, ויאופיין בין היתר גם בגובה רב יחסית. במצבים של רעב ורמה נמוכה של לפטין, יש יצירה של אנטגוניסטים תחרותיים ארוכי טווח (NPY, AGRP) של הקולטן Mc4R, המונעים קשירה של α-MSH וגורמים בכך לעידוד התיאבון. מחקרים קודמים הראו כי עכברים אשר חסרים את הקולטן Mc4r, היו שמנים מכיוון שאכלו יותר והוציאו פחות אנרגיה מאשר עכברים רגילים.
קולטן נוסף במוח לו תפקיד בשליטה על כמות השומן שהגוף אוגר הוא Mc3r, משופעל על-ידי melanocortin, הפועל עם לפטין לוויסות משקל הגוף. מחקרים מראים שעכברים אשר היו חסרים את הקולטן Mc3R, נוטים לאגור יותר שומן עבור כמות מסוימת של אוכל לעומת עכברים ללא חסר בקולטן זה.
השמנת יתר ותנגודת ללפטין
אכזבה השתררה לאחר סדרת ניסויים בהם טופלו אנשים שמנים מאוד בלפטין, בלי שהרזייה צפויה באה לביטוי. שהרי לא כמו בעכברים או בבני אדם בהם מוטציה בגן ללפטין גורמת לחסר שלו, רוב האנשים השמנים מכילים בדמם רמות לפטין שהן אף גבוהות מן הממוצע, שכן ייצורו בתאי השומן שלהם נורמאלי לחלוטין. מסיבות שאינן מובנות עדיין, אנשים שמנים אלה עמידים ואינם מגיבים לפעילות הלפטין. יש חוקרים הסבורים שאולי תפקידו העיקרי של לפטין הוא בהגנה מפני איבוד משקל בתקופת רעב וחסר מזון, ולא בפני עלייה במשקל בתקופות שפע. לכאורה, כאשר מאגרי השומן באדם מתדלדלים, כך מתמעט ייצורו של לפטין, מה שמביא להגברת התיאבון, ולהקטנת רמת המטבוליזם בגוף. המצב ההפוך לעומת זאת לא מתרחש: מעבר לנקודה מסוימת, הגדלת ייצור לפטין אינה מביאה בהכרח לעיכוב התיאבון או להגברת המטבוליזם, שכן הגוף בעיקר מגן על עצמו מפני רעב-עד-מוות.
למרות שלפטין מפחית את התיאבון, ידוע שרמות הורמון זה בדמם של אנשים שמנים גבוהות במיוחד, מה שנראה לכאורה כדבר והיפוכו. נראה לכאורה שאנשים שמנים מגלים תנגודת (resistance) ללפטין, בדומה לתנגודת שמגלים בחולי סוכרת type 2 להשפעת אינסולין. נראה שבאנשים שמנים האופן בו לפטין מפקח על תחושת הרעב והשובע פגום באופן כלשהו, וכך הגוף אינו מקבל באופן ראוי את תחושת השובע לאחר אכילה. להסבר תנגודת זו פותחה תיאוריה של signal-to-noise ratio, לפיה באנשים עם משקל תקין רמת לפטין בגברים היא בין 1-5 מיקרוגרם לליטר, ו-7-13 מיקרוגרם לליטר בנשים. קליטה ניכרת של קלוריות במזון מגרה תגובת לפטין להפחתת הרעב, וממילא מפחיתה את הדחף לצריכת מזון. באנשים שמנים לעומת זאת, התגובה ללפטין תהיה פחותה בגלל היפר-ליפידמיה כרונית הצפויה באנשים אלה, מה שמדכא את ה-signal-to-noise ratio, באופן שעלייה ברמת לפטין היא בעלת השפעה פיזיולוגית קטנה יותר. תנגודת ללפטין עלולה להתרחש גם במקרים של חסר בקולטנים ללפטין, או בתפקודם.
למרות שתנגודת ללפטין מתוארת לעתים כמפגע מטבולי התורם להשמנת-יתר, אין ודאות שתאור זה נכון ברוב המקרים. העובדה שתנגודת ללפטין נפוצה ביותר באנשים שמנים, יש בה אך כדי לרמוז שהיא מהווה רק התנהלות הסתגלותית לעודף משקל הגוף. התפקיד הפיזיולוגי העיקרי של לפטין אינו בהכרח איתות ל-"מצב שובע" למניעת השמנת-יתר, אלא דווקא לתת איתות ל-"מצב של רעב", על מנת לשמור על מאגרי שומן נאותים להישרדות בעתות של חסך קלורי ומשבר אנרגיה. לכן יש להתייחס לתנגודת ללפטין באנשים עם עודף משקל כתכונה סבירה של פיזיולוגיית הגוף, שנותנת יתרונות במשבר של רעב, יותר מאשר במשבר של עודף משקל.
מחקריו של Leibel הצביעו על כך שבאנשים שמנים כמו גם ברזים, הזרקות של לפטין אינן מפחיתות את מסת הגוף. זאת כיון שהמוח אינו מיועד להגיב לרמות מוגברות של לפטין בהפחתת צריכת מזון, אלא להגיב יותר דווקא לחסר לפטין בהגברת התשוקה לצריכת מזון. מחקריו של Leibel הראו שירידה ברמת לפטין בפלזמה המתרחשת לאחר איבוד משקל, מגבירה את התיאבון. כיון שכך, הזרקת לפטין באנשים פחותי-משקל יכולה למנוע את העלייה בתיאבון ומאפשרת להם לשמר את איבוד המשקל. מחקרים אלה מדגימים אם כך שטיפול בלפטין עשוי להוות אסטרטגיה נאותה לטיפול באנשים, לא בהכרח בגרימת ירידה במשקלם, אלא יותר במגמה לשמור על משקל נמוך באלה שהגיעו לכך על ידי דיאטה נאותה או על ידי פעילות גופנית סדירה.
לפטין ותהליכי דלקת בגוף
גורמים המשפיעים באופן מובהק על רמת לפטין בדם, הם גם הגורמים משפיעים על מדדי דלקת אחרים בגוף כגון רמת טסטוסטרון, שינה, עקה רגשית, מאזן קלורי ורמות השומן בגוף. נראה שאחד מתפקידיו של לפטין כמדד דלקתי הוא בתגובה הספציפית שלו לציטוקינים המופרשים מרקמת השומן.
במושגים של מבנה ותפקוד, יש דמיון בין לפטין והציטוקין IL-6, ואמנם לפטין משתייך למשפחת העל (superfamily) של ציטוקינים. נראה שלפטין בצירקולציית הדם קשור ומשפיע על הציר היפותלמוס-היפופיזה-אדרנל (להלן HPA), מה שמייחס ללפטין תפקיד ביולוגי בתגובה למצבי עקה, ואמנם הודגם שקיימים יחסי היזון חוזר בין לפטין לציר HPA.
באנשים בריאים רמות לפטין נוהגות על פי מחזוריות הפוכה לזו של הורמונים כקורטיזול ו-ACTH. נמצא ייצור מוגבר של גלוקו-קורטיקו-סטרואידים בעכברים חסרי לפטין, כמו גם תגובות מוגברות של הציר HPA למצבי דחק. ניסויים בבעלי חיים הראו שגלוקו-קורטיקואידים עודדו הפרשת לפטין מתאי שומן, אם כי בבני אדם לא נמצא קשר דומה. ראוי לציין שלפטין אמנם מעכב הפרשה של גלוקו-קורטיקואידים הן על ידי השפעה ישירה וארוכת-טווח על תאי האדרנל, וכן על ידי השפעה מהירה לטווח-קצר על הפרשת הורמונים כ-ACTH ו-CRH או corticotropin releasing hormone.
במצבי אלח-דם (sepsis) יש כידוע פעילות חדה בציר HPA, ובתרחיש זה אכן נמדדות רמות לפטין גבוהות יותר בדם בהשוואה לרמתו בבריאות מלאה. בנוסף, במצב של אלח-דם לא נשמר פרופיל ההפרשה המחזורית של לפטין במרוצת היממה, ונעלם גם המתאם ההופכי בין רמות לפטין ואלה של קורטיזול. ידוע גם שנרשמת עלייה ברמות לפטין בדם של בני-אדם ומכרסמים, במקביל לעלייה ברמות TNFalfa או IL-1 בדם.
בדומה למה שמוצאים במצבי דלקת כרוניים, רמות לפטין בדם מוגברות לא רק בהשמנת-יתר, באכילה מוגזמת ובמחלות הכרוכות בדלקת, אלא גם ביתר לחץ-דם, בתסמונת מטבולית ובתחלואה קרדיו-וסקולארית. נראה שרמות מוגברות של לפטין, פועלות כתגובה חריפה קדם-דלקתית, למנוע עקה תאית מוגזמת שיכולה להיגרם מאכילת-יתר. כאשר קליטה קלורית גבוהה עולה על יכולת תאי השומן לגדול יותר במימדיהם או לגדול במספרם כדי לאפשר קליטת עתודות שומן חדשות, התגובה החריפה המושרית על ידי לפטין, גורמת לתהליך דלקתית ברמת התאים השומניים, ולאגירה אקטופית של שומנים באתרים לא רצויים מבחינה בריאותית כמו איברים פנימיים, דופן העורקים, וכן ברקמת השריר. נמצא שריכוזים מוגברים של לפטין בדם, מופיעים במצבים לויקוציטוזיס בגברים ובנשים.
עלייה ברמת אינסולין בתגובה לקליטה קלורית מעודדת עלייה מקבילה ברמת לפטין, תופעה המסתייעת על ידי רמות קורטיזול גבוהות. ממצא זה מדגים שעודף קלורי במצבים של עודף אגירה של תאי שומן, יכול לגרום לתגובת עקה המגרה עלייה ברמת לפטין, מה ששולח איתות להפסקת צריכת מזון נוספת למנוע רמות גבוהות מדי של העמסת תאי השומן. תגובה זו של לפטין גם תגן בפני אגירת שומן באתרים אקטופיים.
יחסי גומלין בין לפטין ואינסולין
מצב של השמנת-יתר המתאפיין ברמות לפטין גבוהות, גורם גם לעלייה ברמת אינסולין בדם ולתנגודת להורמון האחרון. קיימת הדדיות ביחסי הגומלין בין לפטין ואינסולין, באופן שלפטין משפיע ישירות על יצירת אינסולין בלבלב לאחר העמסת גלוקוזה: כבר בשנת 1996 דיווחו Cohen וחב' על ההשפעה שיש ללפטין על מספר מרכיבים ברצף העברת איתותים של אינסולין כמו MAK-kinase ו- PI 3-K כמו גם על IRS-1 ו-IRS-2. יש אם כן אפשרות שפעילות-יתר של לפטין מבטאת השפעה של רקמת שומן ביצירת תנגודת לאינסולין. אך השפעת לפטין על המסלולים המשפיעים על פעילות אינסולין מורכבת מעצם היותה דיפרנציאלית: בעוד שלפטין מזרז את הזרחון של IRS-1 על ידי אינסולין, הוא דווקא מפחית את הזרחון של IRS-2.
בכיוון ההפוך, יש לאינסולין השפעה ארוכת-טווח על הפרשת לפטין, כיוון שהיפר-אינסולינמיה חדה אינה משפיעה על רמות לפטין, לעומת מצב ממושך של היפר-אינסולינמיה המעלה רמות לפטין. במכרסמים, הודגם שירידה ברמות אינסולין מפחיתה רמת mRNA ללפטין ואת רמת הלפטין בדם, והיפוכו של דבר ברמות מוגברות של לפטין. עכברים עם סוכרת type 1 שטופלו בלפטין לבד או עם בטיפול משולב של לפטין ואינסולין הגיבו בהקטנת התנודתיות של רמת הסוכר בדם, בהפחתת רמת כולסטרול ורמת שומנים בגוף, בהשוואה לעכברים שטופלו עם אינסולין בלבד.
פעילות גופנית ורמות לפטין
ככל שאדם עוסק יותר בפעילות ספורטיבית סדירה, כן גדלה רגישותו ללפטין ורמתו בדם יורדת, כתוצאה מצמצום מאגרי שומן. זאת כיוון שככל שרקמת השומן קטנה יותר בגוף, כך היא מפרישה פחות לפטין.
נבחנו בעיקר ענפי ספורט כגון ריצה ואופניים, ואימון ארוך הוגדר ככזה של שעה וחצי ומעלה, בעוד שאימון קצר הוגדר כאימון של עד שעה, או אימון בו סה"כ ההוצאה קלורית אינה עולה על 800 קק"ל. מספר עבודות הראו שבמאמץ ארוך, נמצאה ירידה של 30-35% בהשוואה לרמת הבסיס ברמת הלפטין מיד לאחר האימון עד מספר שעות אחר כך. ההסבר הפיזיולוגי למנגנון זה מוסבר ע"י פעילות אנדוקרינית המתרחשת בזמן האימון, במהלכה יורדת רמת האינסולין בדם ואילו עולה רמתם של הקטכולאמינים (אדרנלין ונוראדרנלין). מסתבר כי אינסולין קשור, בין השאר בהגברת הייצור של הורמון הלפטין ואילו קטכולאמינים מדכאים את ייצור הלפטין. כיוון שמאמץ ממושך מדכא הפרשת אינסולין ובמקביל מביא לעלייה בקטכולאמינים, שילוב שניהם מדכא את הפרשת לפטין מרקמת השומן.
נתונים אלה מסבירים לכאורה מדוע לא אחת חשים ספורטאים תחושת רעב קשה לאחר אימון און פעילות ממושכים. לעומת זאת, פעילות גופנית מאומצת של פחות משעה, או כזו שבה נצרכות פחות מ-800 קק"ל, לא מביאה לשינויים משמעותיים ברמת לפטין.
לפטין ומערכת החיסון
לפטין נכרך גם עם וויסות מערכת החיסון. אצל אנשים עם תת-תזונה קשה או רעב, יש מעט לפטין, וכתוצאה מכך יש שינוי בוויסות מנגנון החיסון עם נטיית יתר להופעת זיהומים. כך גם אצל אנשים עם משקל עודף, בעלי תנגודת ללפטין.
לפטין פועל גם על תאי T באופן שהוא מעודד יצירת תאי Th1 התורמים ליצירת תהליכי דלקת. עכברים ללא לפטין מוגנים מפני מחלות אוטו-אימוניות. מוטציות בגן המקודד ללפטין, או בגן המקודד לקולטן של לפטין נדירות ביותר באנשים שמנים. התפקיד של לפטין באִפנוּן (מודולציה) של פעילות תאי T במערכת החיסון, הודגם בניסויים בעכברים. לפטין מאפנן את התגובה החיסונית לטרשת עורקים, שאחד הגורמים לה היא השמנת-יתר. מתן אקסוגני של לפטין יכול לעודד אנגיוגניות על ידי הגברת רמות VEGF.
השפעת לפטין על העצם
בשנת 2000 התפרסמו לראשונה נתונים על יכולת לפטין לווסת את מסת העצם. קיימים רצפטורים ללפטין על פלטת הגדילה של העצם, הוא מגרה התרבות של תאי סחוס ושל גדילת העצם. ההורמון יכול להשפיע על מטבוליזם של העצם על ידי איתות ישיר מהמוח, וכך הוא משפיע על הפחתת המסה של עצם קנצלוטית, ולעומת זאת משפיע בהגברת המסה של עצם קורטיקאלית. כדי לנסות ולפרש את ההשפעה הדיכוטומית של לפטין על 2 סוגי עצם אלה, עלתה ההשערה שרמה מוגברת של לפטין בהשמנת יתר יכולה לבטא מנגנון של הגברת גודל העצם וחוסנה כדי להתמודד עם העומס של משקל גוף רב יותר. המטבוליזם של רקמת עצם נתון לבקרה של המוח על ידי מספר נוירוטרנסמיטורים שנמצאו גם בעצם כגון אדרנלין, נוראדרנלין, סרוטונין, calcitonin gene-related peptide, נוירופפטיד Y ו-vasoactive intestinal peptide. גם לפטין העובר למוח ונקשר שם לקולטניו, פועל דרך מערכת העצבים הסיפתטית לווסת את המטבוליזם של העצם.
לפטין ומערכת הרבייה
בעכברים, הראו שלפטין נדרש לפוריותם של זכרים ונקבות, ואמנם עכברי ob/ob חסרי לפטין הם עקרים לחלוטין כתוצאה מהיפוגונדיזם. טיפול בלפטין בעכברים אלה הביא לעלייה מובהקת ברמת LH ו-FSH כמו גם בספירת הזרע, וכן הודגמו ממצאים היסטולוגיים של ערור בשחלה וברחם. גם בנשים צעירות נמצאה עלייה ברמת לפטין עם הגיל, ובמקביל לעלייה ברמות אסטרדיול, FSH ו-LH, אם כי בגברים צעירים העלייה ברמת לפטין נחלשת מגיל 10 ומעלה והיא הולכת ופוחתת במקביל לעלייה ברמת טסטוסטרון.
לפטין פועל בהיפותלמוס על נוירונים האחראיים להפרשת GnRH. אם כי השפעתו במערכות הרבייה באדם פחותה יותר, עדיין נראה שגם באדם מהווה לפטין סמן מטאבולי למערכת הרבייה, המשגר איתותים על מצב מאגרי השומן בהיבט של אספקת קלוריות, המסייעת לתהליכי התרבות. מחקר במתעמלות שהתפרסם ב-1997 ב-J Clin Endocrinol Metab, הראה שאלו מהן שלקו באל-וסת, סבלו מרמות לפטין נמוכות ושיבוש בהפרשה פעימתית של ההורמון. ידוע גם שרמות לפטין עולות ב-60-100% חודשים אחדים לפני ההתבגרות המינית, מה שמצביע על קשר בינו לבין מערכת הרבייה.
יש ראיות לכך שמחזורי הביוץ בנשים קשורים למאזני אנרגיה בגוף (עליה במשקל או איבוד משקל). כאשר מאזן האנרגיה שלילי (מצבי צום או רעב), או כאשר האישה צורכת אנרגיה במאמצים גופניים בעצימות גבוהה, עלול להתרחש שיבוש במחזור החודשי ולעתים אף אל-וסת. טיפול בנשים אלה עם תכשיר לפטין ריקומביננטי עשוי לעתים להסדיר את הופעת הווסת. מחקרים אחדים מצביעים על רמות לפטין מחוץ לטווח הנורמה ככאלה שעלולות להשפיע באופן שלילי על איכות ביציות, ועל סיכוי ההצלחה בהפריה חוץ-גופית.
ידוע שלפטין מופרש בכמויות קטנות בשלייה, וכן שרמות לפטין עולות בעת הריון, וכן שהן צונחות באופן בולט מיד לאחר הלידה. לפטין מבוטא גם בדופן הרחם. כן ידוע יכול להשרות רצף ריאקציות נוירו-אנדוקריניות שיכול להביא להקדמת הופעת וסת בנערות.
Fc-leptin
כאמור, ישנה קבוצה מצומצמת ביותר של בני אדם הומוזיגוטים למוטציות בגן ללפטין, בהם קיימת תשוקה מתמדת לאכילה ובהתאם להשמנה יוצאת דופן. בפרטים אלה ניתן היה לטפל בהצלחה יחסית על ידי הזרקת לפטין ריקומבננטי, אך המגבלה בטיפולים אלה נבעה מהצורך להזריק מינונים גבוהים ותכופים מדי של התכשיר. מגבלה זו קשורה לתקופת מחצית חיים קצרה של לפטין ריקומביננטי בדם (דקות אחדות), למסיסותו המוגבלת, וממילא ליעילות חלקית. חלק ממגבלות אלה ניתן לכאורה להמעיט על ידי יצירת מולקולה כימרית בה נעשה איחוי (fusion) בין לפטין לבין מקטע Fc של אימונוגלובולין גמא ליצירת Fc-leptin. מולקולה כימרית זו מסיסה הרבה יותר מההורמון החופשי, בעלת אורך חיים של שעות אחדות, ומראה פעילות ביולוגית טובה יותר. מאז שנת 2006 בה התפרסם לראשונה על יצירת Fc-leptin הוא נבחן בהצלחה מוגברת בעכברים בריאים ובאלה עם מוטציית ob/ob, אך לא נוסה עדיין בבני-אדם.
Meterleptin
מדובר באנלוג של לפטין אנושי אושר לטיפול ביפאן, ונבחן כעת על ידי ה-FDA לטיפול בסוכרת וביתר-טריגליצרידמיה: טיפול בתכשיר זה הפחית המוגלובין A1C מ-9.4% בבסיס המחקר ל-7.0% בסיומו. רמת טריגליצרידים פחתה מ-500 מיליגרם לד"ל בתחילת הניסוי ל-200 מיליגרם לד"ל בסופו. חברת Bristol-Myers Squibb הגישה ל-FDA בקשה לאישור שימוש ב-metreleptin לטיפול באנשים באנשים עם צורות נדירות של ליפודיסטרופיה, מפגע נדיר ביותר בו קיים חסר ברמת שומן ובאדיפוציטים וממילא חוסר בלפטין.
הוראות לביצוע הבדיקה
כיוון שלפטין נוהג במידה מסיימת על פי מחזוריות צירקדיאנית, מקובל שהפרשתו המירבית היא בשעה 0200 לאחר חצות, אולי לצורך דיכוי תיאבון בשעת שינה. יחד עם זאת המקובל נטילת דם בשעה 0800 עד 1000 בבוקר, כמו גם בשעות אחה"צ המוקדמות נותנת תוצאה אינפורמטיבית. ניתן לדגום את הדם לאחר צום של 12 שעות במבחנה כימית (פקק אדום או צהוב) או במבחנת ספירת דם (EDTA פקק סגלגל). מדידת רמת לפטין מתבצעת בשיטת ELISA או בשיטת IRMA.
ראו גם


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק