פונטיניב לטיפול בלוקמיה מיאלואידית כרונית קשה לטיפול - Ponatinib for the treatment of chronic myeloid leukemia - CML
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| פונטיניב לטיפול בלוקמיה מיאלואידית כרונית קשה לטיפול | ||
|---|---|---|
| Ponatinib for the treatment of Chronic Myeloid Leukemia | ||
| 250px | ||
| ICD-10 | Chapter C 92.1 | |
| ICD-9 | 205.1 | |
| MeSH | D015464 | |
| יוצר הערך | ד"ר איתי לוי | |
עמוד 40, הערות לעורכים: ויקיזציה. יש לכתוב הפניות לדף הפירושים " לוקמיה מיאלואידית כרונית"
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – לוקמיה
לוקמיה מיאלואידית כרונית - CML (Chronic Myelogenic Leukemia) מאופיינת בשגשוג לא מבוקר של תאי דם לבנים במח העצם ובדם הפריפרי. המחלה מתחילה כמחלה כרונית ובהיעדר טיפול מתאים היא מתקדמת תוך שלוש עד חמש שנים מהשלב הכרוני הראשוני, דרך שלב ביניים (שלב מואץ Accelerated phase) לצורה של לויקמיה חריפה (שלב בלסטי). בשלבים המתקדמים נדרשים טיפולים אגרסיביים ובמרבית המקרים המחלה אינה ניתנת לריפוי[1].
המחלה מהווה כ-15%-20% מכלל הלויקמיות במבוגרים. ההיארעות בישראל, בדומה לזו שבעולם, היא כ-1.6 חולים חדשים ל-100,000 איש בשנה. בישראל מאובחנים כל שנה ב-70 חולים וסך הכל יש מספר מצטבר של כ-700 חולי CML בארץ.
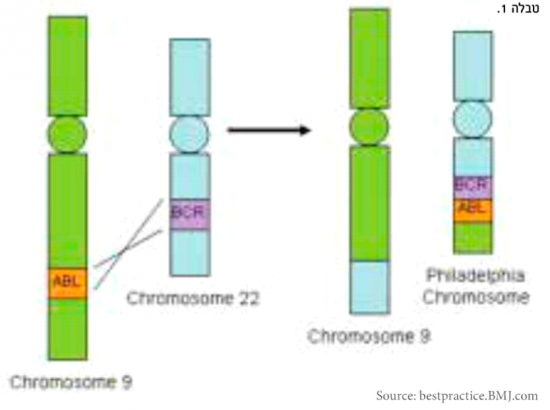
CML היא מחלה הנגרמת כהוצאה משינוי גנטי אופייני בתאי הדם. השינוי מתבטא בחילוף של חומר גנטי בין כרומוזום 9 עליו נמצא הגן ABL וכרומוזום - 22 עליו נמצא הגן BCR. שינוי זה מכונה טרנסלוקציה 9:22. בהוצאה מכך נוצר כרומוזום בעל מבנה לא תקין עליו יושבים בסמיכות הגנים BCR-ABL (איור מס' 1).
כרומוזום זה נקרא כרומוזום פילדלפיה, על שם המדינה בארה"ב שבה התבצע המחקר שהביא לגילויו בשבת 1960. הגנים BCR/ABL המצויים כעת בסמיכות זה לזה מקודדים ליצירת חלבון בשם BCR-ABL, שהינו אנזים מסוג טירוזין קינאז. אנזים זה גורם לשפעול תהליכי גדילה לא מבוקרת של האי דם לבנים, תהליך המביא בסופו להתפתחות הלויקמיה[2].
CML היא המחלה הממאירה הראשונה שבה פוענח הבסיס הגנטי הגורם להתפתחותה. דבר זה אפשר לראשונה פיתוח של טיפול ביולוגי החוסם ומדכא באופן ספציפי את פעילותו של האנזים הגורם להיווצרות המדלה. דהיינו, הטיפול ב-CML מבוסס על חסימת הפעילות הבלתי מבוקרת של האנזים מסוג טירוזין קינאז.
אימטיניב (Glivec) תיא התרופה הראשונה שפותחה ממשפחת התרופות TKI. התרופה מאושרת משנת 2001 לטיפול קו ראשון בחולי CML. כיום מאושרות לשימוש גם התרופות נילוטיניב, דסטיניב ובוסוטניב, שהן תרופות מסוג TKI מדור שני. ייחודן של התרופות מדור שני שהן יעילות בחולים המפתחים עמידות לטיפול עקב התפתחות מוטציות באתר הטירוזין קינאז. לכל אחת מהתרופות פרופיל יעילות כנגד מוטציות אחרות וניתן להתאים את הטיפול בהתאם לסוג המוטציות שמתפתחות. יתרון נוסף של קבוצת התרופות TKI מדור שני הוא שניתן להשיג באמצעותן הגובה מהירה יותר בדיכוי המחלה ביחס ל-GLIVEC[1].
על אף ההתקדמות הניכרת בטיפול ב-CML, הרי שכ-20% מהחולים המטופלים בקו ראשון ועוד ב-20% מהמטופלים בקווים מתקדמים ב-TK1 מפתחים עמידות לטיפול. רוב העמידויות נגרמות כתוצאה מהיווצרות מוטציות באתר הפעילות של הטירוזין קינאז. עד היום זוהו כ-70 מוטציות, כאשר רוב המוטציות מעוכבוה על ידי ה-TKI מדור שני[3]. מוטציה ייחודיה מסוג T3151 (החלפה של טריאונין באיזולאוצין באתר 315) היא עמידה לכל סוגי ה-TK1 עד כה. ייחודו של ICLUSIG-H, שהוא ה-TK1 הראשון המעכב מוטציה זו[4].
ICLUSIG) Ponatinib) בחולי CML
ICLUSIG פותחה באמצעים טכנולוגים מתקדמים במטרה להתגבר על מגוון המוטציות הידועות ב-BCR-ABL. מחקרי פאזה ראשונה ושנייה של ICLUSIG נערכו בחולים שעברו קווי טיפול רבים ובחלקם נשאי המוטציה העמידה. המחקרים פורסמו שניהם במגזין New England Journal of Medicine[4]. במחקרים נמצאו שיעורי הגובה והישרדות גבוהים, אף בהשוואה לתוצאות הטיפול כקווים מוקדמים יותר במחלה.
מחקר ה-PACE[4], מחקר הדגל של התרופה, נערך ב-499 חולים, מתוכם 270 חולי CML בשלב הכרוני, 85 בשלב המואץ ו-94 בשלב הבלסטי בולל חולי Ph+ ALL. 128 חולים היו נשאים של המוטציה T3151. בעת הכניסה למחקר מעל 90% מהחולים נכשלו ב-2 קווי טיפול קודמים לפחות ו-52% מהחולים בשלב הכרוני נכשלו כבר ב-3 קווי טיפול קודמים. חלק ניכר מהחולים בשלב המואץ והבלסטי נכשלו גם הם בשלושה קווי טיפול קודמים.
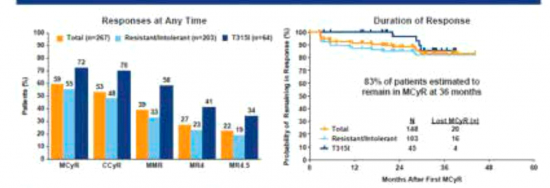
תגובה ציטוגנטית מג'ורית הושגה ב-61% מהחולים שקיבלו ICLUSIG בקו שלישי וב-46% מהחולים בהם התרופה ניתנה כקו רביעי. תגובה ציטוגנטית מג'ורית הושגה ב-70% מהחולים נושאי המוטציה T3151.
הזמן החציוני להשגת תגובה ציטוגנטית מג'ורית, המוגדרת בנסיגה של מעל 65% בכרומוזום פילדלפיה, היה מהיר ביותר ועמד על 2.8 חודשים בשלב הכרוני. במעקב חציוני של שנתיים שמרו 89% מהחולים על תגובה זו. תגובה מולקולרית מג'ורית (ירידה של מעל 3 לוגים בגן BCR-ABL) הושגה ב-34% מהמקרים של חולים בקווי טיפול מתקדמים והזמן החציוני להשגת התגובה היה 5.5 חודשים. גם בחולי CML בשלב המואץ ובשלב הבלסטי הושגו תגובות ראויות לציון. תגובות המטולוגיות הושגו ב-61% ו-31% מהחולים בהתאמה ונשמרו לאורך זמן.
מעקב ארוך טווח של מחקר ה-PACE פורסם ב-ASH בשנת 2014[5]. במעקב חציוני של 34.8 חודשים, 83% מהחולים שמרו על תגובה ציטוגנטית וכן תגובה מולקולרית מג'ורית, עם ירידה של עד 4-5 לוגים ברמת ה-BCR-ABL בחלק מהחולים.
מחקר שהשווה את יעילות הטיפול ב-ICLUSIB לעומת TKI אחרים מדור שני, בחולים שטופלו כבר בקו אחד או יותר של TKI מדור שני ופיתחו עמידות או אי סבילות, הראה ששיעור התגובה לטיפול ב-ICLUS1G היה כ-60% לעומת -22% 26% בלבד ב-TKI האחרים. נתונים אלה תומכים בכך שחולה שטופל כבר ב-TKI מדור שני ונכשל על טיפול זה, הסיכוי שיגיב ל-ICLUSIB גבוה בהרבה לעומת הסיכוי לתגובה בטיפול עם TKI אחר מדור שני[6].
מינון התרופה שנבדק במחקר ה-PACE הוא 45 מ"ג, אך גם במינונים התחלתיים של 30 מ"ג ו-15 מ"ג הושגה תגובה ציטוגנטית מג'ורית בשיעור דומה למינון הגבוה. בדומה ל-TKI מדור שני גם עם הטיפול ב-ICLUSIB נצפו תופעות לוואי בדרגות 3 ו-4 ובהן פנקריאטיטיס בשיעור של 6% ואנמיה וטרומבופניה בשיעור של 2%. תופעות לוואי טרומבואמבוליות היו בשיעור גבוה יחסית (16%) והן נצפו במיוחד בחולים עם גורמי סיכון כגון יתר לחץ דם, עישון, סוכרת, יתר שומנים בדם והיסטוריה של מחלות לב וכלי דם. לא נמצא הבדל בהישרדות הכוללת בין חולים שסבלו מתופעות לוואי טרומבואמבוליות לבין אלה שלא סבלו מתופעות אלו. נצפה קשר בין מינון התרופה לבין תופעות הלוואי. במרבית החולים שבהם מינון התרופה הורד עקב תופעות לוואי נשמרה התגובה לטיפול. עקב שיעור גבוה יחסית של תופעות לוואי טרומבואמבוליוה קיימה המלצה לבצע סקירה מלאה של גורמי סיכון וסטטוס קרדיווסקולרי בחולים חדשים וכן לעקוב באופן הדוק אחר חולים המטופלים ב-ICLUSIG[7]
ICLUS1G רשומה בישראל בהתוויה לחולי CML בכל שלבי המחלה שלהם עמידות או אי סבילות לדסטיניב או נילוטוניב או שאינם יכולים להמשיך טיפול באימטיניב, וכן לכל החולים שפתחו מוטציה מסוג T3151. התרופה רשומה גם לחולי Ph+ ALL עמידים או בעלי אי סבילות לדסטיניב או בעלי מוטציה T3151.
ICLUSIG מאושרת על ידי ה-EMEA (רשות התרופות האירופאית) וה-FDA (רשות המזון והתרופות האמריקאית) לטיפול בחולי CML וחולי ALL עם כרומוזום פילדלפיה חיובי.
ביבליוגרפיה
- ↑ 1.0 1.1 Baccarani et al Blood. 2013 Aug 8:122(6)1872-84
- ↑ Nowell P. The lournal of Clinical Investigation 2007: 117(8)2033-2035
- ↑ Apperley J. lancet 2007 (8) 1018-1027
- ↑ 4.0 4.1 4.2 Cortes et al. N Engl J Med. 2013 7:369(191:1783-96.
- ↑ Cortes et al Blood 2014(214) 21
- ↑ Upton et al, Leukemia Research 39 (2015) 58-64
- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה7
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר איתי לוי. מנהל המחלקה ההמטולוגית. המרכז הרפואי האוניברסיטאי סורוקה, באר שבע


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק