אקרומגליה - Acromegaly
| אקרומגליה | ||
|---|---|---|
| Acromegaly | ||
| שמות נוספים | ענקות, גידלון | |
| ICD-10 | Chapter E 22.0inusl | |
| ICD-9 | 253.0 | |
| MeSH | D000172 | |
| יוצר הערך | פרופ' אילן שמעון
|
|
אקרומגליה (Acromegaly) היא מחלה נדירה הנגרמת לרוב מהפרשה מוגברת של הורמון גדילה (Growth Hormone) מאדנומה (Adenoma)- גידול שפיר בבלוטת יותרת המוח. מקור השם ביוונית, מהמילים Akron (גפיים) ו-Megas (גדול). המחלה תוארה לראשונה בשנת על-ידי רופא צרפתי בשם Pierre Marie שתיאר שני חולים עם תסמונת לא מולדת של הגדלת הפנים, הידיים והרגליים ונתן לתופעה את שמה – אקרומגליה [1]. בעברית נקראת המחלה גידלון או ענקות[2].
אפידמיולוגיה
אקרומגליה היא מחלה נדירה עם שכיחות של 70-40 חולים למיליון איש. שכיחות המחלה בגברים ובנשים דומה, והיא מתגלית לרוב בגילאי 50-30.
אטיולוגיה
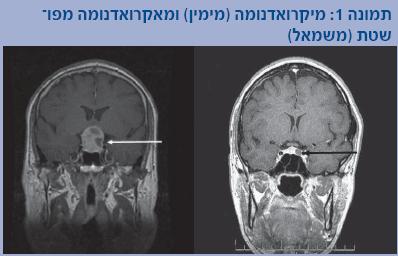
ב-95 אחוזים ויותר מהמקרים, המחלה נגרמת על ידי הפרשה מוגברת של הורמון גדילה מאדנומה בבלוטת יותרת המוח (היפופיזה, Pituitary gland או Hypophysis) אשר מכילה תאים סומטוטרופים (Somatotroph) [3]. אדנומות מהוות כ- 15-10 אחוזים מכלל גידולי בלוטת יותרת המוח. בכשליש מאדנומות אילו ניתן למצוא מוטציה סומטית (Somatic mutation) בחלבון ה-Gs-α (Stimulatory G protein alpha sub unit) שגורמת להפרשה מוגברת ולא מבוקרת של הורמון גדילה במקביל לקצב מוגבר של התרבות התאים. במרבית המקרים (75 אחוזים) האדנומות גדולות מ-10 מ"מ (מילימטר), ולכן נקראות מאקרואדנומות (Macroadenoma), ולעיתים הן יכולות להיות ענקיות. במיעוט המקרים, האדנומות קטנות מ-10 מ"מ, ולכן נקראות מיקרואדנומות (Microadenoma) (תמונה 1).
לעיתים נדירות ביותר המחלה עשויה להיגרם על ידי הפרשה מוגברת של הורמון גדילה מחוץ לבלוטת יותרת המח (Ectopic) או בשל גידולי לבלב אשר מפרישים את ההורמון התת-רמתי (Hypothalamic), שנקרא הורמון משחרר הורמון גדילה (GHRH, Growth Hormone Releasing Hormone). הורמון זה, בהתאם לשמו, מגרה הפרשת הורמון גדילה.
קליניקה
המחלה מאופיינת על ידי גדילה גרמית מופרזת עם נפיחות של הרקמות הרכות.
בילדים היא תסתמן בגדילה מופרזת לגובה (ענקות), ובצעירים סביב גיל 20 אופייני למצוא אדנומות ענקיות. ההפרשה המוגברת של הורמון גדילה יוצרת גירוי מתמיד בתאי הכבד לייצור עודף של ההורמון פקטור גדילה דמוי אינסולין-1 (IGF-1, Insulin-Like Growth Factor-1) שהוא האחראי לרוב תסמיני המחלה. אלה כוללים:
- הגדלת כפות הידיים והרגליים, הגדלת הלשון, הגדלת איברים פנימיים
- מראה אופייני גס של הפנים עם עיבוי האף והתבלטות הלסת התחתונה
- התעבות הרקמות הרכות
- הזעת יתר
- כאבי פרקים
- יתר לחץ-דם
- עלייה ברמות הסוכר
- נחירות והפסקות נשימה
- תסמונת מנהרת שורש כף היד (Carpal tunnel syndrome) ועוד
כרבע מהאדנומות שמפרישות הורמון גדילה מפרישות גם Prolactin.
חלק גדול מהמאקרואדנומות הגדולות מתפשטות מעלה ודוחקות את תצלובת עצבי הראייה (Optic chiasma), וכך הן עשויות לגרום לנזק האופייני בשדות הראייה הצדדיים (Bitemporal hemianopsia). בנוסף, ייגרם נזק למבנה ולתפקוד התקין של בלוטת יותרת המוח, ויידרש מתן תחליפי קבוע לפעילותה, אשר כולל מתן הורמוני התריס, גלוקוקורטיקואידים (Glucocorticosteroids) והורמוני המין.
לחולים עם אקרומגליה תוחלת חיים קצרה יותר בכ-10 שנים ביחס לבני גילם אם אינם מטופלים, וזאת בשל תחלואת לב וכלי דם מוגברת, סוכרת, יתר לחץ-דם, הפרעות בנשימה, ונטייה מוגברת לפתח גידולים שפירים וממאירים של מערכת העיכול.
אבחנה
המחלה מתפתחת באיטיות ולעתים מתגלית במקרה. האבחון מתבסס על נוכחות רמות מוגברות בדם של ההורמונים - הורמון גדילה ו-IGF-1. האבחנה נעשית באמצעות מדידת רמות מוגברות של הורמון גדילה ו-IGF-1 בנסיוב (Serum). מקובל גם לבצע העמסת סוכר כדי להראות חוסר דיכוי של הורמון גדילה לפחות מ-1 נ"ג (ננוגרם)/מ"ל (מיליליטר) כהוכחה נוספת להפרשה מוגברת שלו.
בדיקות נוספות שיש לבצע:
- הערכה של רמות הורמוני התריס, קורטיזול (Cortisol), Prolactin, טסטוסטרון (Testosterone) וגונדוטרופינים (Gonadotropins) תאפשר אבחון נזק לתפקוד בלוטת יותרת המוח
- דימות האוכף התורכי (Sella turcica) בתהודה מגנטית (MRI) יראה את הגודל וגבולות האדנומה
- בדיקת שדות ראייה בחולים עם אדנומות גדולות תעריך את הנזק לעצבי הראייה, ואת הצורך בטיפול דחוף להצלת הראייה
למרות העיכוב האופייני בזיהוי ובאבחון המחלה, שגם לאור המודעות המוגברת של רופאים למחלה יחסית נדירה זו, מאובחנת בממוצע רק כ-8-4 שנים לאחר הסתמנותה הראשונית, המטרה היא להביא את החולה להפוגה קלינית והורמונלית מלאה במהירות האפשרית.
טיפול
הטיפול הראשוני המועדף הוא ניסיון להסרה ניתוחית של האדנומה, וכמחצית מהחולים מחלימים. אם לא מושגת הפוגה, החולה מופנה לטיפול תרופתי בתכשיר מסוג Somatostatin analog , שלרוב מדכא את הפרשת ההורמונים לתקינה או קרוב לתקינה. אם גם טיפול זה נכשל, ניתן להעביר את החולה לטיפול חדש יחסית בתרופה שהיא נוגדת להורמון גדילה ומונעת את ייצור ה-IGF-1 בכבד. תרופה זו מורידה לרוב את רמת ה- IGF-1 לגדר התקין.
הסרה כירורגית של האדנומה
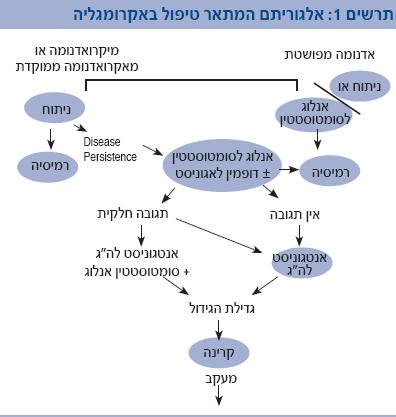
הטיפול הראשוני המומלץ באקרומגליה הוא הסרה כירורגית של האדנומה בניתוח בגישה טרנס-ספנואידלית (Transsphenoidal surgery) (תרשים 1). ניתוח כזה, המבוצע על ידי מנתח נוירוכירורג (Neurosurgeon), יגרום לריפוי בכ-60-50 אחוזים מהמנותחים[4]. אחוז הריפוי וירידת רמות הורמון גדילה וה-IGF-1 לתקינות גבוה במיוחד במיקרואדנומות (80-70 אחוזים מהמנותחים) וקטן מאוד באדנומות מפושטות (כ-20 אחוזים) [4]. נוסף על כך, ניתוח מאפשר הקלה מהירה של נזק קיים לעצבי הראייה ויכול למנוע נזק תפקודי של בלוטת יותרת המוח. ברוב המקרים שבהם מדובר בגידול מפושט, רמות הורמון גדילה וה-IGF-1 יישארו מוגברות ויידרש טיפול תרופתי קבוע. גם במקרים שבהם לא הושג ריפוי, לניתוח יש תפקיד בהסרה של רקמה גידולית המאיימת על תצלובת עצבי הראייה וכן בהגדלת הסבירות להצלחת טיפול תרופתי בהמשך. חולים שעברו הסרה מוצלחת של אדנומה מפרישת הורמון גדילה בניתוח, מחויבים במעקב רפואי ארוך טווח כיוון שקיימת הישנות של המחלה בחלק קטן מהחולים ב-10 השנים הראשונות שלאחר הניתוח.
- הטיפול התרופתי
הטיפול התרופתי באקרומגליה מבוסס ב-20 השנים האחרונות על אנלוגים של Somatostatin. Somatostatin הוא פפטיד (Peptide) בן 14 חומצות אמינו (Amino acids) שמופרש באופן טבעי מההיפותלמוס ובהגיעו לבלוטת יותרת המוח הוא מדכא את רמת הורמון הגדילה באופן יעיל באמצעות הקשרותו לקולטנים ל-Somatostatin (קיימים חמישה במספר) על פני התאים הסומטוטרופיים. קיימים שני תכשירים מסחריים כאלה:Sandostatin (Octreotide) וכן Somatuline (Lanreotide) שנקשרים בעיקר לקולטנים מספר 2 ו-5 ובטיפול ארוך טווח מדכאים הפרשת הורמון גדילה ו-IGF-1 בכ-60 אחוזים ממקרי האקרומגליה לרמות תקינות. טיפול זה, הניתן בזריקות ארוכות טווח (Sandostatin LAR במינון 30-10 מ"ג (מיליגרם); Somatuline autogel במינון של 120-60 מ"ג כל 4 שבועות), מפחית בהדרגה את התסמינים האופייניים לאקרומגליה ומסוגל בחלק גדול מהחולים להקטין את גודל האדנומה [5], [6], [7]. לטיפול זה תופעות לוואי שכוללות שלשולים, כאבי בטן, אבני כיס מרה, וגם היפרגליקמיה (Hyperglycemia) או היפוגליקמיה (Hypoglycemia) כתוצאה מיכולת ה-Somatostatin לדכא הפרשת Insulin ו-Glucagon בלבלב, אך בדרך כלל הטיפול נסבל היטב על ידי החולים. הניסיון מוכיח שחולים המגיבים לטיפול לרוב מדכאים את הפרשת הורמון הגדילה וה- IGF-1 תוך 6-3 חודשים מתחילת הטיפול ואין כמעט מצב של התפתחות עמידות לטיפול אם הושגה כבר יעילות. המצב הרצוי הוא שגם רמות הורמון גדילה וגם ה-IGF-1 ידוכאו לרמות נמוכות, אם היו מוגברות. לעתים הטיפול משיג דיכוי מלא של ההורמון האחד וחלקי בלבד של השני, למרות הגברת מינון התרופה. כשאין תגובה מספקת לטיפול (ב-40 אחוזים מהמטופלים לאחר כישלון ניתוחי) ניתן לנסות לעבור מתכשיר Somatostatin אחד לתכשיר המקביל השני, אך לרוב יעילות שני התכשירים מאוד דומה ואין יתרון משמעותי לאף אחד מהם.
מקובל לטפל בתכשירים אלה לאחר כישלון ניתוחי קודם (תרשים 1) כטיפול קו שני, אך יש חולים שמקבלים טיפול תרופתי זה כטיפול ראשוני, בלי שנותחו קודם לכן, בהצלחה רבה [8]. בדרך כלל מדובר בחולים עם סיכון ניתוחי מוגבר, אדנומות מפושטות לסינוסים הקברנוזים (Cavernous sinus) עם סיכוי נמוך להחלמה מניתוח וחולים שאינם רוצים בניתוח. גם חולים אלה מראים הצטמקות של הגידול במקביל לדיכוי רמות ההורמונים לגדר התקין במעל 50 אחוזים מהמקרים.
טיפול באגוניסטים של Dopamine, בעיקר Cabergoline, נוסה בהצלחה מסוימת בחולים עם גידולים מפרישי הורמון גדילה, בעיקר באלה עם אדנומות שמפרישות גם Prolactin, ונמצא יעיל בדיכוי הורמון גדילה ו-IGF-1 בלא יותר מ-20-10 אחוזים מהמטופלים. ניתן לשלב תרופה זו עם טיפול באנלוג ל-Somatostatin (תרשים 1).
- קרינה ממוקדת לאוכף התורכי
בעבר הופנו חולים עם מחלה פעילה לאחר ניתוח לא מוצלח וטיפול תרופתי לקבלת קרינה מכוונת לאדנומה מפרישת הורמון גדילה. קרינה מוסכמת הייתה נהוגה בעבר במנה כוללת של 5,000 עד 6,000 Rad בחלוקה למשך כחודש. זו השיגה הפוגה של המחלה רק לאחר שנים ובמחיר של התפתחות תת-תפקוד בלוטת יותרת המוח ברבים מהחולים בתוך 10 עשר שנים. הרס של האדנומה בקרינה מכוונת דימות (Radiosurgery, Stereotactic ablation) הנהוגה, מסוגלת להביא לריפוי ביותר מ-50 אחוזים מהחולים תוך שנים ספורות ובסיכון נמוך יותר של פגיעה בלתי הפיכה בבלוטת יותרת המוח. סיכונים נוספים אפשריים של קרינה כוללים נזק בלתי הפיך לעצבי הראייה, פגיעה מוחית קוגניטיבית לאחר שנים, סיכון לפגיעה בכלי דם מוחיים, וגידולי מוח משניים (נדירים) באזור הקרינה לאחר שנים רבות.
- טיפולים תרופתיים חדשניים
כ-40 אחוזים מהמטופלים באקרומגליה בתרופות ה-Somatostatin אינם משיגים הפוגה הורמונלית ולכן זקוקים לטיפול אחר. בעבר הם הופנו לרוב לטיפול קרינתי. בעשור הראשון של המאה ה-21 פותח תכשיר ה-Somavert (Pegvisomant), שהוא אנלוג של הורמון גדילה המבוסס על מולקולת הורמון גדילה שעברה שינויים מבניים מסוימים באמצעות הנדסה גנטית. תכשיר זה חוסם את הקולטן להורמון גדילה ומונע את קשירתו לתאים בכבד ולכן מפחית מאוד את ייצור IGF-1 בכבד. ה-Somavert נמצא בעולם בשימוש בחולי אקרומגליה ובארץ נרשם ונכלל בסל התרופות משנת 2008 כטיפול תרופתי קו שני לחולי אקרומגליה. התרופה ניתנת כזריקה תת-עורית פעם ביום במינון של 20-10 מ"ג ומורידה את רמת ה-IGF-1 במהירות לנורמה בכ-90-80 אחוזים מהמטופלים שעמידים לתכשירי ה-Somatostatin[9], [10]. תסמיני המחלה פוחתים במקביל לירידת רמת ההורמון. בניגוד לתכשירי ה-Somatostatin, רמת הורמון הגדילה אינה מדוכאת (אלא עולה פי 3-2) ומסת הגידול אינה מושפעת מהטיפול ואינה מצטמקת לרוב, אך גם אינה גדלה. לפיכך יש להימנע מטיפול בתכשיר זה בחולים עם מסה גידולית שמסכנת את עצבי הראייה, או לשלב אז תכשיר זה עם אנלוג ל-Somatostatin. רמות הסוכר יורדות לרוב תוך כדי הטיפול. בישראל יש כמה עשרות חולים המטופלים בתכשיר, לאחר כישלון טיפולי באנלוגים ל-Somatostatin.
נבדק תכשיר מקבוצת האנלוגים ל-Somatostatin, ה-Pasireotide (SOM-23) שנקשר בזיקה טובה לקולטנים 1, 2, 3, ו-5 [11] ועשוי להיות יעיל בדיכוי הורמון גדילה ו-IGF-1 בחלק מהחולים שלא מגיבים לאנלוגים הקיימים [12]. תכשיר זה נבדק בהצלחה במחקר שלב 2, ובמחקר שלב 3 ניתן בזריקה כל 4 שבועות לכמה מאות חולים עם אקרומגליה בהשוואה לזריקות Sandostatin, לפני מתן אישור מנהל המזון והתרופות האמריקאי לרישום התרופה. חלק מהמטופלים בתכשיר זה פיתחו סוכרת משמעותית הדורשת טיפול תרופתי.
פרוגנוזה
לחולים עם אקרומגליה תוחלת חיים קצרה יותר של בכ-10 שנים ביחס לבני גילם אם אינם מטופלים. כמחצית מהחולים עם אקרומגליה מחלימים בעקבות ניתוח. האחרים מטופלים תרופתית באנלוגים ל-Somatostatin שיעילים בכ-60 אחוזים מהמטופלים. 40 האחוזים הנותרים מתוכם יכולים להשיג הפוגה בטיפול ב-Somavert . אפשרות נוספת היא קרינה ממוקדת לאזור האוכף התורכי. תרופות חדשות למחלה נמצאות בהליכי פיתוח שונים ויגדילו בעתיד את מגוון האפשרויות הטיפוליות.
דגלים אדומים
ביבליוגרפיה
- ↑ Marie P. Sur deux cas d'acromegalie: Hypertrophie singuliere non congenitale des extremities superieures, inferieures et cephalique. Rev Med 1886;6:297-333
- ↑ Cutis Verticis Gyrata – סימן נדיר בעור המקדים לגידלון (אקרומגליה), באתר "הרפואה"
- ↑ Melmed S. Medical progress: Acromegaly. NEJM 2006;355:2558-2573
- ↑ 4.0 4.1 Shimon I, Cohen ZR, Ram Z, et al. Transsphenoidal surgery for acromegaly: Endocrinological follow-up of 98 patients. Neurosurgery 2001;48:1239-1243
- ↑ Stewart PM, Kane KF, Stewart SE, et al. Depot long-acting somatostatin analog (Sandostatin LAR) is an effective treatment for acromegaly. J Clin Endocrinol Metab 1995;80:3267-3272
- ↑ Chanson P, Borson-Chazot F, Kuhn J-M, et al. Control of IGF-I levels with titrated dosing of lanreotide Autogel over 48 weeks in patients with acromegaly. Clin Endocrinol (Oxf) 2008;69:299-305
- ↑ Murray RD, Melmed S. A critical analysis of clinically available somatostatin analog formulations for therapy of acromegaly. J Clin Endocrinol Metab 2008;8:2957-2968
- ↑ Bevan JS, Atkin SL, Atkinson AB, et al. Primary medical therapy for acromegaly: An open, prospective, multicenter study of the effects of subcutaneous and intramuscular slow-release Octreotide on growth hormone, insulin-like growth factor-I and tumor size. J Clin Endocrinol Metab 2002;87:4554-4563
- ↑ Trainer PJ, Drake WM, Katznelson L, et al. Treatment of acromegaly with the growth hormone-receptor antagonist pegvisomant. NEJM 2000;342:1171-1177
- ↑ van der Lely AJ, Hutson RK, Trainer PJ, et al. Long-term treatment of acromegaly with pegvisomant, a growth hormone receptor antagonist. Lancet 2001;358:1754-1759
- ↑ Bruns C, Lewis I, Briner U, et al. SOM230: A novel somatostatin peptidomimetic with broad somatotropin release inhibiting factor (SRIF) receptor binding and a unique antisecretory profile. Eur J Endocrinol 2002;146:707-716
- ↑ van der Hoek J, de Herder WW, Feelders RA, et al. A single-dose comparison of the acute effects between the new somatostatin analog SOM230 and Octreotide in acromegalic patients. J Clin Endocrinol Metab 2004;89:638-645
קישורים חיצוניים
- אקרומגליה – כיוונים חדשים בטיפול במחלה, מדיקל מדיה
המידע שבדף זה נכתב על ידי פרופ' אילן שמעון, המכון האנדוקריני, מרכז רפואי רבין, ביה"ח בילינסון, פתח תקווה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק