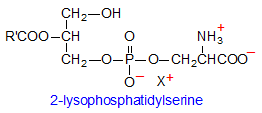פוספטידיל-סרין - Phosphtidylserine
| מדריך בדיקות מעבדה | |
| פוספטידיל-סרין | |
|---|---|
| Phosphtidylserine | |
| |
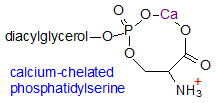
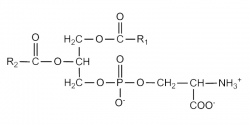
המבנה של PS
| |
| מעבדה | כימיה בדם |
| יוצר הערך | פרופ' בן-עמי סלע |
פוספטידיל סרין הוא פוספוליפיד המהווה מרכיב בממברנת התא. הוא משחק תפקיד מפתח באיתות של מחזור חיי התא, בעיקר בהקשר של אפופטוזיס , והוא מהווה נקודת מפתח בחדירת נגיפים לתא במנגנון הידוע כ-apoptotic mimicy המייעל את חדירת נגיפים לתא (Meertens וחב' ב- Cell Host & Microb משנת 2012).
פוספטידיל-סרין הוא glycerophospholipid. הוא מורכב משתי חומצות שומן המחוברות בקשר אסטרי לפחמן הראשון והשני של גליצרול ו-serine המחוברים דרך קשר פוספו-די-אסטרי לפחמן השלישי של גליצרול (Nelson ו-Cox ב-Lehninger Principles of biochemistry משנת 2008). PS ממקור צמחי ו-PS ממקור של בעלי חיים נבדלים בהרכב חומצות השומן שלהם.
התפקידים הביולוגיים של PS
- איתות תאי: מולקולות PS בממברנת תאים פונות לצד הציטוזולי של התא, והן אחוזות על ידי האנזים flippase. אנזים זה הוא חלבון ממברנלי המהווה transmembrane lipid transporter ושייך למשפחת ה-ABC transporters, האחראיים לסייע בתנועה של פוספוליפידים בין ה-leaflets הפנימי והחיצוני של ממברנת התא. אלא כאשר התא עובר אפופטוזיס, PS אינו מוגבל יותר על ידי flippase לצד הציטוזולי של הממברנה. במקום זאת, האנזים scramblase מקטלז חילוף מהיר של PS בין שני צדי הממברנה. כאשר מולקולות PS מגיעות לצד החיצוני של ממברנת התא, הן פועלות כאיתות למקרופאגים להקיף ולבלוע את התא (Verhoven וחב' ב-J Exp Med משנת 1995).
- קואגולציה: PS משחק תפקיד בקרישת דם. כאשר טסיות דם בצירקולציה נתקלות בנקודת פציעה של כלי-דם, קולאגן ותרומבין מתווכים בתהליך בו מועבר PS משכבת הממברנה הפנימית לשכבה החיצונית של הממברנה, שם PS משמש כ-pro-coagulant (Zwall וחב' ב-Biocim Biophys Acta משנת 2004). טרנספר ממברנלי זה מסייע לכוון פרוטאזות החיוניות לקרישה, בעיקר tissue factor ופקטור VII, מסייע לפרוטאוליזה נוספת ולשפעול של פקטור X, ולבסוף יצירת תרומבין. במפגע הקרישה הידוע כתסמונת Scott, המנגנון של העברת PS משכבת הממברנה הפנימית לחיצונית משובש (Weiss ב-Sem Hematol משנת 1994).
למרות ש-PS שהרכבו המלא הוא 1,2-diacyl-sn-glycero-3-phospho-L-serine , מופיע באופן נרחב בבעלי-חיים, צמחים ומיקרואורגניזמים, הוא מהווה בדרך כלל פחות מ-10% מכלל הפוספוליפידים, וריכוזו הגדול ביותר הוא בשכבת המיאלין במוח. עם זאת PS יכול להוות 10-20% מכלל הפוספוליפידים בממברנת התא וברטיקולום האנדופלזמטי בתא. בשמרים, כגון S. cerivisiae הוא יכול להוות למעלה מ-30% מסך הליפידים. ברוב החיידקים, PS הוא מרכיב זוטר בממברנה, למרות שהוא תוצר ביניים חשוב בביוסינתזה של phosphatidylethanolamine (על פי Vance ו-Tasseva ב-Biochim Biophys Acta משנת 2013).
PS הוא פוספוליפיד אניוני (חומצי) המכיל 3 קבוצות הניתנות ליינון, דהיינו שייר הפוספאט, וקבוצות האמינו והקרבוקסיל. בדומה לליפידים חומציים אחרים, PS מופיע בטבע בצורת מלח, אך יש לו נטייה גדולה להתחבר לסידן דרך האטומים הטעונים של חמצן בשיירי הקרבוקסיל והפוספאט, תוך שינוי הקונפורמציה של קבוצות הקצה הפולריות. אינטראקציה זו יכולה להיות בעלת רלוונטיות משמעותית לתפקידים הביולוגיים של PS, בעיקר בעת יצירת עצם, לדוגמה (Buckland וחב' ב-Biochim Biophys Acta משנת 2000).
בתאים של בעלי חיים, ההרכב של חומצות השומן של PS משתנה מרקמה לרקמה. לדוגמה, בפלזמה של בני אדם שולטים stearoyl-2-oleoyl ו-stearoyl-2-arachidonoyl-1, ואילו במוח (ובעיקר בחומר האפור) וברשתית העין וברקמות רבות נוספות, שכיחים בעיקר חומצות השומן מסוג stearoy-2-docosahexaenoyl-1. אכן, היחס בין חומצות שומן n-3 ל-n-6 ב-PS המוחי, גבוה יותר מאשר ברוב הליפידים האחרים. כמו ברוב הפוספוליפידים האחרים, חומצות שומן רוויות מרוכזות בעמדה sn-1, ואילו חומצות השומן הרב-בלתי רוויות מרוכזות בעמדה sn-2. פוספטידילסרינים עם שיירי אתר קשורים (alkyl ו-alkenyl) אינם שכיחים ברקמות של בעלי-חיים. הם תוארו לראשונה בריאות של חולדה, אך גם נמצאו שכיחים יחסית בעדשת העין ובמקרופאגים באדם.
ככלל, הריכוז של PS הוא גבוה ביותר בממברנת תאים כמו גם באנדוזומים, אך הוא נמוך ביותר במיטוכונדריה. כיוון ש-PS ממוקם במלואו בחלק הפנימי של ה-monolayer בממברנה החיצונית (כמו גם בממברנות התאיות האחרות), והוא גם הפוספוליפיד האניוני הנפוץ ביותר, PS הוא בעל התרומה הגדולה ביותר להשפעות החלק הפנימי של ממברנות, כולל אינטראקציות אלקטרוסטטיות לא ספציפיות. הפיזור הנורמלי הזה של PS בממברנה, משתבש במהלך שפעול של טסיות ואפופטוזיס תאי (Chaurio וחב' ב-Molecules משנת 2009).
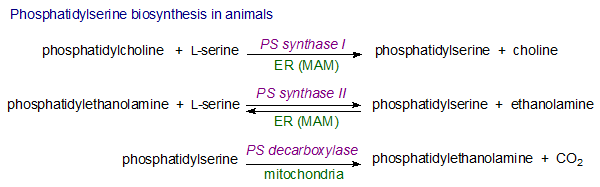
ביוסינתזה של PS
חומצת האמינו serine מסונתזת על ידי רוב התאים בבעלי-חיים, וכיוון שבמוח היא מסונתזת על ידי אסטרוציטים, אך לא על ידי נירונים, התאים האחרונים חייבים לקבל אספקה של serine לביוסינתזה של PS. בחיידקים ובאורגניזמים פרוקריוטיים אחרים, PS מסונתז במנגנון בר-השוואה לזה של פוספולפידים אחרים, על ידי ראקציה של L-serine עם CDP-diacylglycerol ליצירת PS ו-CMP. רוב ה-PS שנוצר עובר דה-קרבוקסילציה ליצירה של phosphatidylethanolamine (להלן PE), וזו הדרך העיקרית ליצירת האחרון בחיידקים. כיוון ש-phosphatidylcholine (להלן PC) בשמרים מיוצר דרך מתילציה של PE, נראה ש-PS הוא הקודמן (precusor) העיקרי בסינתזה של פוספוליפידים במיקרואורגניזמים אלה. בבעלי חיים המסלול ליצירת PC מ-PS פועל רק בכבד (Christie ב- The American Oil Chemists משנת 2014).
בניגוד לכך, ברקמות של בעלי-חיים, ישנם 2 מסלולים ליצירת PS בהם משתתפים 2 אנזימים (PS synthase I ו-PS synthase II. שיש ביניהם הומולוגיה של 30%, ויש להם במבנה מספר מקטעים חוצי-ממברנה, אך לכל אחד משני האנזימים יש מצע אחר. PS מסונתז ברטיקולום האנדופלזמטי, או במיקום אחר בשכבה החיצונית של ממברנה הקשורה למיטוכונדריה לפרק זמן קצר. הראקציה ליצירת PS מורכבת משחלוף של L-serine עם פוספטידיל-כולין המקוטלז על ידי האנזים PS synthase I, או על ידי שחלוף L-serine עם PE בראקציה המקוטלזת על ידי PS synthase II. תהליכים אלה תלויים באופן מוקפד על ידי יוני סידן, ללא כל מקור אנרגיה אחר. הפוספוליפיד החדש שנוצר מועבר למיטוכונדריה, שם הוא עובר דה-קרבוקסילציה ליצירת PE על ידי decarboxylase ספציפי. PE יכול לחזור לרטיקולום האנדופלזמטי שם הוא יכול להיות מוסב בחזרה ל-PS על ידי פעולת PS synthase II.
Phosphatidylserine synthase I מבוטא בכל הרקמות בעכבר, אך בעיקר בכליות, בכבד ובמוח, בה בשעה ש-phosphatidylserine synthase II פעיל בעיקר במוח ובאשכים, והרבה פחות ברקמות אחרות. האנזים האחרון הוא בעל ספציפיות גבוהה ל-docosahexaenoic acid (להלן (DHA. לא ברור מדוע סדרה כה מורכבת של ראקציות נחוצה או למה יש צורך ב-2 אנזימים. יתרון אחד של האנזים השני נעוץ בכך ש-ethanolamine החופשי ו-choline הנוצרים, מנוצלים במהירות לסינתזה של פוספוליפידים. לכן, PS וכן PE מיוצרים ללא הפחתה בכמות של PC. אלימינציה של 2 אנזימים אלה קטלנית בעובר של עכברי knockout, אך אלימינציה רק של אנזים אחד מבין השניים יכולה להותיר את העובר בחיים, למרות הרמה הנמוכה באופן בולט של PS ו-PE.
כמו עם פוספוליפידים אחרים ההרכב הסופי של חומצות השומן ברקמות בעלי-חיים, מושג על ידי תהליך remodelling הידוע כ-Lands' cycle. בשלב הראשון , יש הידרוליזה על ידי phospholipase A2 ליצירת lyso-PS, המלווה על ידי רה-אצילציה על ידי אנזימים שונים מסוג acyl-CoA:lysophospholipid acyltransferase. האנזים שאופיין, O-acyltransferase-1 או MBOAT-1 הקשור לממברנה עם עדיפות ל-oleoyl-CoA, בעוד שאנזים אחר, MBOAT-5, מביא לאינקורפורציה של שרשרות linolenoyl ו-arachidonoyl, עדיין לא אופיין במלואו.
בנוסף לתפקידו כמרכיב של הממברנה התאית וכקודמן של פוספוליפידים אחרים, PS הוא קו-פקטור הכרחי הקושר ומשפעל מספר גדול של חלבונים, בעיקר אלה עם פעילות של איתות. הנוכחות של כמויות ניכרות של PS בשכבה הפנימית-ציטוזולית של אנדוזומים ושל ליזוזומים, מאפשרת לאברונים תאיים אלה לעגן חלבונים בעלי מקטעים הקושרים PS. לדוגמה, החלבון של שלד התא, spectrin, נקשר ל-PS. בנוסף, הריכוז הגבוה של PS האניוני, מביא להצטברות של מטען שלילי אליו יכולים להיקשר חלבונים קטיוניים. בכך ניתן לסייע למעבר של מספר חלבונים ממברנה פנימית של התא לממברנה פנימית אחרת. הנוכחות של PS נחוצה גם על ידי אנזימים כגון ATPase Na+/K+ וכן sphingomyelinase ניטרלי. PS אינו כרוך באיתות תאי דרך יצירה של מטבוליטים, כמו במקרה של phosphatidylinositol.
PS קשור לתהליך הקואגולציה של הדם בטסיות, שם PS מועבר מהשכבה הפנימית של הממברנה לבועיות (vesicles) של השכבה החיצונית בטסיות משופעלות. כאן, PS מזרז את השפעול של פרו-תרומבין והפיכתו לתרומבין באופן ישיר, או על ידי קישור ל-2 אתרים ספציפיים על פני 2 פקטורים רגולטוריים חיוניים. Apolipoprotein A-1 הוא בעל תפקיד מפקח בכך שהוא מנטרל תכונות המסייעות לקרישה בכך שהוא מסדר את PS בשטחי פנים קטנים מדי לאחסן קומפלקס של prothrombinase (על פי Lentz ב-Prog Lipid Res משנת 2007).
הסינתזה של PS והחדרתו לתוך ממברנות
רוב ה-PS המסונתז de novo, כולל ה-PS המסונתז בתוך ה-CNS, נובע מהשחלוף של serine על ידי choline בממברנת המיטוכונדריה והרטיקולום האנדופלזמטי המקוטלז על ידי PS-synthase 1{{כ} (Kay ו-Grinstein ב-Adv Exp Med Biol משנת 2013, Stone ו-Vance ב-J Biol Chem משנת 2000, Vance ו-Tasseva ב-Biochim Biophys Acta משנת 2013, Osman וחב' ב-J Biol Chem משנת 2011, ו-Sturbois וחב' ב-J Biol Chem משנת 2001). PS שסונתז זה-עתה מועבר מהרטיקולום האנדופלזמטי לשכבה הפנימית-ציטוזולית של ממברנת התא, ושם מחסומים טרמודינמיים מונעים את מעבר PS לשכבה החיצונית של הממברנה (Daleke ב- J Lipid Resמשנת 2003, Martin ו-Pagano ב-J Biol Chem משנת 1987, ו-Conor וחב' ב-J Biol Chem). ההימנעות מחשיפת PS על השכבה החיצונית של ממברנת התאים, מונעת את בליעתם על ידי מקרופאגים (Shiratsuchi וחב' ב-J Biol Chem משנת 1997, Kawasaki וחב' ב-J Biol Chem משנת 2002, Li וחב' ב-Science משנת 2003, Fadok וחב' ב-J Biol Chem משנת 2001, Hoffmann וחב' ב-J Cell Biol משנת 2001, ו-Sambrano ו-Steinberg וחב' ב-Proc Natl Acad Sci USA משנת 1995). על מנת למנוע את התרחיש האחרון, תאים בריאים מקדישים עד 4% מצריכת ATP שלהם לשמור על הא-סימטריה במיקום PS בממברנה (Seigneuret ו-Devaux ב-Proc Natl Acad Sci USA משנת 1984).
PS ואפופטוזיס
PS ידוע כבעל תפקיד חשוב ברגולציה של אפופטוזיס, בתגובה לגירוי מסוים התלוי בסידן. הפיזור הנורמלי של PS בשכבה הפנימית של ה-bilayer הממברנלי, משתבש בגלל פעילותם של האנזימים flippase ו-scramblase בתהליך האפופטוטי. בנוסף, בתהליך אפופטוזיס מעוכבים גם האנזימים aminophospholipid translocases, המחזירים את PS למקומו הטבעי בממברנה הפנימית. אחרי הטרנספר של PS לשכבה החיצונית של הממברנה, סבורים שקולטן על פני מקרופאגים מזהה את PS ומסייע להרחקת התאים האפופטוטיים ואת התכולה הטוקסית והאימונוגנית שלהם באופן לא דלקתי. הקישור של PS לחלבונים ספציפיים כגון apolipoprotein H (הידוע כ-β2-glycoprotein 1) מחיש את הפינוי של תאים אלה. תהליך זה חיוני בהתפתחות של הריאות והמוח, והוא גם רלוונטי למצבים קליניים בהם אפופטוזיס משחק תפקיד חיוני, כמו סרטן, זיהומים ואוטו-אימוניות כרונית.
התהליך של אפופטוזיס מלווה לעתים קרובות על ידי יצירה של מולקולות חמצן פעילות (ROS), הגורמות לחמצון מהיר של חומצות שומן ב-PS לפני שפוספוליפיד זה עובר לצד החיצוני של הממברנה. כעת כבר ברור שרק צורות מולקולריות של PS שעברו קיטום (truncation) על ידי חמצון של קבוצת sn-2 acyl, מזוהות על ידי קולטנים של מקרופאגים כתנאי לבליעה של התאים האפופטוטיים על ידי המקרופאגים. בנוסף, כמויות משמעותיות של PS עוברות טרנסלוקציה במנגנון דומה לשטח הפנים של תאי T המבטאים רמות נמוכות של האנזים הטרנס-ממברנלי tyrosine phosphatase.
השינוי הזה בפיזור של PS בין שתי שכבות הממברנה פועל כמנגנון איתות למודולציה של מספר חלבוני ממברנה (Leventis ו-Gristein ב-Ann Rev Biophys משנת 2010). לדוגמה, החלבון annexin V נקשר בספציפיות גבוהה ל-PS ומשמש כאמצעי לזיהוי תאים אפופטוטיים. תפקיד בלתי-רגיל נוסף של PS בהיותו מהווה מרכיב-מפתח של קומפלסים מסוג ליפיד-סידן-פוספאט המאתחלים התרבצות של מינרלים בעת יצירת העצם. נמצא והוכח ש-PS ופוספאט אנאורגני חייבים להיות נוכחים בתהליך האחרון לפני שיוני סידן מצטרפים, ואז הזיקה הגבוהה של PS לסידן הופכת להיות קריטית (Wu וחב' ב-J Biol Chem משנת 2008).
Lysophosphatidylserine
Lysophosphatidylserine עם חומצת שומן בעמדה sn-1 בלבד, ידוע כתווך במספר תהליכים ביולוגיים, והוא כנראה מיוצר בעיקר על ידי דה-אצילציה של PS על ידי פוספוליפאזות.
Lysophosphatidylserine התגלה לאחר פציעה של רקמות בבעלי חיים כגון כוויות, דחיית שתל או גידולים סרטניים, ויכול להיות בעל תפקידים דומים לאלה של lysophosphatic acid באיתות תאי, כמו לדוגמה בוויסות של חדירת סידן לתא דרך קולטן ספציפי. ביונקים נמצא גם phospholipase A1 הספציפי ל-PS, המבצע הידרוליזה של קבוצת ה-sn-1 acyl ליצירה של sn-2-lyso-PS. מולקולת lysophosphatidylserine יכולה גם להיווצר בפציעת תאים, כאשר מולקולה זו יכולה לעבור דיפוזיה על מנת להעביר את המידע לתאים אחרים, בעיקר לתאי פיטום (mast cells), והיא נוצרת גם לזרז את הפינוי של ניטרופילים מתים. ל-lysophosphatidylserine יש גם תפקיד בהפגת דלקת. באופן ספציפי, sn-2-lyso-PS מעודד דה-גרנולציה של תאי פיטום, תכונה שלא קיימת בליזופוספוליפידים אחרים.
למרות ש-PS שהרכבו המלא הוא diacyl-sn-glycero-3-phospho-L-serine-1,2, מופיע באופן נרחב בבעלי-חיים, צמחים ומיקרואורגניזמים, הוא מהווה בדרך כלל פחות מ-10% מכלל הפוספוליפידים, וריכוזו הגדול ביותר הוא בשכבת המיאלין במוח. עם זאת PS יכול להוות 10-20% מכלל הפוספוליפידים בממברנת התא וברטיקולום האנדופלזמטי בתא. בשמרים כגון S. Cerevisiae, הוא יכול להוות למעלה מ-30% מסך הליפידים. ברוב החיידקים PS הוא מרכיב זוטר בממברנה, למרות שהוא תוצר ביניים חשוב בביוסינתזה של phosphatidylethanolamine.
PS והמוח האנושי
PS הוא הפוספוליפיד החומצי העיקרי בממברנות תאי האדם, בהם הוא מהווה 2-20% מסך המסה של הפוספוליפידים בממברנת התא החיצונית ובממברנות של האברונים התוך-תאיים (van Meer וחב' ב-Nat Rev Mol Cell Biol משנת 2008, ו-Kobayashi וחב' ב-J Biol Chem משנת 2002). במוח בריא של אדם שכבת המיאלין עשירה ב-PS (על פי Svennerholm ב-J Lipid Res משנת 1968, ו-Hayes ו-Jungalwala ב-Biochem J משנת 1976). תכולת PS בחומר האפור מוכפלת מהלידה עד גיל 80 שנה. בכל גוף האדם, PS מהווה מרכיב מבני של הרטיקולום האנדופלזמטי, של מעטפת הגרעין, של ה-Golgi, של החלק הפנימי של הממברנה החיצונית של התא, ושל החלק החיצוני של ממברנת המיטוכונדריה (Voelker ב-Proc Natl Acad Sci USA משנת 1989, Omori וחב' ב-Biosci Biotechnol Biochem משנת 2010).
בערך 20-30% מ-PS בחומר האפור הוא בצורת stearoyl-2-docosahexaenoyl-sn-glycero-3-phosphoserine-1 (על פי Kimura ו-Kim ב-J Lipid Res משנת 2013). תכולת ה-docosahexanoic acid של PS בנירונים היא בעלת חשיבות תפקודית (Tanaka וחב' ב-Biomol Ther משנת 2012). בקליפת המוח הפחתה בכמות ה-DHA של PS כרוכה עם התפתחות של פגיעה קוגניטיבית מתונה עד להתפתחות אלצהיימר (Cunnane וחב' ב-J Alzheimers' Dis משנת 2012). בנוסף, המחזור של חומצות שומן בעמדות sn-1 ו-sn-2 של PS הוא תכוף, מהיר וצורך אנרגיה, תוך שהוא מאפשר להצטברות משותפת של DHA ו-PS (על פי Purdon ו-Rapoport ב-Biochem J משנת 1998), ומגדיל את תכולת ה-DHA של מולקולות PS בתוך ממברנות.
הריכוזים הגבוהים של docosahexanoic acid או DHA ב-PS במוח וברשתית, חשובים להתפתחות ולתפקוד של רקמות אלו (Mozzi וחב' ב-Neurochem Res משנת 2003). ההצטברות של PS בממברנות של תאי עצב, מסתייעת על ידי DHA, ויש לכך משמעות בהישרדות של תאי עצב. PS יכול גם לשמש כספק של DHA ליצירת protectin ברקמה העצבית (Kim ב-J Biol Chem משנת 2007). מצד שני, ה-FDA מציין שיש רק ראיות מעטות לכך לתמוך בדעה שנטילת תוספי PS מפחיתה את ההתרחשות של שיטיון או הפחתה בקוגניציה של קשישים. נוגדנים כנגד PS מופיעים במספר מצבי מחלה כולל פקקת ואף בהפלות ספונטניות נשנות.
PS ונירוטרנסמיסיה
האינקורפורציה של PS לתוך הממברנות של נירונים משפיעה על המטבוליזם של הנירוטרנמיטורים אצטילכולין, נוראפינפרין, סרוטונין ודופאמין (Cenacchi וחב' ב-Aging Clin Exp Res משנת 1992, ו-Crook וחב' ב-Neurology משנת 1991). כמויות מתאימות של PS עשיר ב-DHA נדרשות לאיחוי של גרנולות מפרישות של נירונים, עם הממברנה הקדם-סינפטית והשחרור של מולקולות נירוטרנסמיטורים לתוך המרווח הסינפטי במהלך האינטראקציה של נירוטרנסמיטורים אלה עם הקולטנים הבתר-סינפטיים (Kim וחב' ב-Prostaglandins leukoc essential fatty acids משנת 2010). בנוסף, PS אקסוגני מעודד ראיות בבדיקת EEG של הגברה נירוטרנסמיסיה כולינרגית בבני אדם בריאים (Rosadini וחב' ב-Neuropsycobiology משנת 1990).
PS והדעיכה של המוח האנושי
הזדקנות המוח האנושי מתאפיינת בירידה ברמת PS בממברנות של נירונים ובעלייה מקבילה ברמת כולסטרול בממברנות אלו, כמו גם בירידה ברגישות של ממברנות בתר-סינפטיות לפעולת אצטילכולין (Cohen ו-Muller ב-Brain Res משנת 1992). באדם, האינקורפורציה של PS אקסוגני לתוך מבנים מוחיים רלוונטית מבחינה תפקודית, ולדוגמה מחקרים תוך שימוש ב-PET ללמוד על צריכת גלוקוזה באנשים עם אלצהיימר גילו צריכה מוגברת של סוכר זה בתגובה לאספקת PS באזורי מוח המשפעים על ידי מחלת אלצהיימר (Heiss וחב' ב-Dementia משנת 1984, ו- Klinkhammer וחב' ב-Dementia משנת 1990). קשישים עם דרגה מתונה של דעיכה ביכולת הקוגניטיבית, הגיבו בשיפור משמעותי במבחנים של קוגניציה שטופלו משך-60 ימים עם תוסף פומי של 300 מיליגרם PS שלוש פעמים ביום (Sinforiani וחב' ב-Clin Trial J משנת 1987, ו-Caffara ו-Santamaria באותו כתב עת מאותה שנה).
קבוצה אחרת של גברים ונשים קשישים עם תלונות על זיכרון דועך, שטופלו משך 6 ו-12 שבועות עם 100 מיליגרם PS 3 פעמים ביום, דיווחו על שיפור בבעיותיהם (Engel ב-Eur Neuropsychopharmacol משנת 1992, Vakhapova וחב' ב-Dement Geriatr Cogn Disord משנת 2014, Richter וחב' ב-Clin Interv Aging משנת 2013, ו-Schreiber וחב' ב-Isr J Psychiatry Relat Sci משנת 2000). היעילות של נטילת PS פּומי נבחנה בניסויים קליניים מבוקרים ואקראיים בגברים ונשים מעל גיל 60 שנה עם איבוד קל של זיכרון, שטופלו עם PS במינון של 100 מיליגרם 3 פעמים ביום או בפלצבו למשך 90 יום (Villardita וחב' ב-Clin Trials J משנת 1987). הטיפול ב-PS הביא לשיפור משמעותי בזיכרון לטווח קצר, בזיכרון המידי, ביכולת הדיבור ועושר השפה, בתשומת הלב ובעֵרָנוּת. מקרים חמורים יותר של מאפיינים קוגניטיביים שונים דיווחו על שיפור לאחר טיפול פּומי של 100 מיליגרם 3 פעמים ביום למשך חודשיים (Palmieri וחב' ב-Clin Trials J משנת 1987).
מטופלים עם תסמינים כרוניים של דיכאון גם כן הגיבו לטיפול עם PS (100 מיליגרם 3 פעמים ביום, למשך 1-6 חודשים) בירידה באפּתיה, בהתנתקות חברותית ובהפרעות שינה, לעומת הגברת מוטיבציה והתעניינות, שיפור בזיכרון (Maggioni וחב' ב-Acta Psychiatr Scand משנת 1990).
מקורות דיאטתיים של PS
הצריכה היומית הממוצעת של PS מהמזון במדינות המערב מוערכת ב-130 מיליגרם. PS עשוי להימצא בבשר ובדגים ורק כמויות קטנות שלו נמצא במוצרי חלב או בירקות, עם יוצאי הדופן של שעועית לבנה ולציטין ממקור סויה. בטבלה מופיע ריכוז PS בסוגי מזון שונים על פי Taylor במסמך של ה-FDA משנת 2003.
תכולת PS במיליגרם/100 גרם סוג המזון
713 מוח בקר 480 מקרל אטלנטי
414 לב תרנגול 360 דג מליח (herring) אטלנטי 335 צלופח
239 טחול חזיר 218 כליות חזיר 194 טונה 134 כרעיים של תרנגול 123 כבד תרנגול 107 שעועית לבנה 87 רכיכות רכות-צדף 85 חזה תרנגול עם העור 76 דג mullet 72 בשר עגל 69 בשר בקר 57 בשר חזיר 50 כבד חזיר 50 כרעיים של תרנגול הודו 45 חזה של תרנגול הודו 40 סרטן הנהרות (crayfish) 31 דיונון 28 דג cod אטלנטי 25 אנשובי 20 שעורה מלאה 16 סרדינים 14 דג שמך (trout) 3 אורז מלא 2 גזר 1 חלב פרה (3.5% שומן) 1 תפוחי אדמה
צריכת תוספי PS
פאנל של ה-European Food Safety Authority הגיע למסקנה שאין למצוא קשר סיבתי והשפעתי בין צריכת PS ושיפור תפקוד הזיכרון, הפחתת עקה וקוגניציה בקשישים (EFSA Panel on Dietetic Products, Nutrition and Allergies ב- EFSA Journalמשנת 2010). הסיבה להסתייגות זו היא ש-PS מקליפת המוח בבקר או ממקור סויה הם חומרים שונים, ויכולים לכן להיות בעלי השפעות ביולוגיות שונות. משום כך, לא ניתן להסיק מסקנות מניסויים בהם נעשה שימוש ב-PS ממקורות שונים. באשר להשפעת PS בתחום הקוגניציה, במאי 2003 העניק ה-FDA סטאטוס של "Qualified Health Claim" ל-PS, ובכך תכשיר זה קיבל אישור לציין על האריזה ש"צריכתPS עשויה להפחית את הסיכון לשיטיון או לאי תפקוד קוגניטיבי בקשישים", אך גם שיש להוסיף הערה לפיה מחקר מדעי מאוד ראשוני ומוגבל מעיד על סגולות אלה של PS (Glade ו-Smith ב-Nutrition משנת 2015). על פי ה-FDA קיימת אי-הסכמה בין חוקרים מומחים שאכן יש קשר בין PS לתפקוד קוגניטיבי. סקירות עדכניות יותר מציעות שקשר כזה אמנם ייתכן (Kim ו-Spector ב- Progr Lipid Resמשנת 2014) אם כי המנגנון שלו אינו ברור (Smith ב-mayo Clinic Proc משנת 2014). מספר מחקרים הראו שדווקא PS ממקור סויה עשוי להשפיע לטובה על קוגניציה ועל זיכרון בקשישים (Jorissen וחב' ב-Nutr Neurosci משנת 2001, ו-Kato-Kataoka וחב' ב-J Clin Biochem Nutr משנת 2010). באשר לבטיחות, באופן מסורתי תוספי PS הופקו מקליפת המוח בבקר. יחד עם זאת, בגלל החשש מהידבקות במחלה כגון bovine spongiform encephalopathy (הידועה כמחלת הפרה המשוגעת), יש נטייה לצרוך כחלופה PS ממקור סויה שאושר על ידי ה-FDA כבטיחותי. דיווח בטיחות משנת 2002 של Jorissen וחב' ב-Nutr Neurosci, קבע שקשישים יכולים לצרוך בבטחה תכשיר זה במינון של 200 מיליגרם 3 פעמים ביום. אף-על-פי-כן, בגלל החשש מבעיות בטיחות אפילו בשימוש של תוצרי סויה, מספר יצרנים של PS משתמשים בלציטין (פוספטידילכולין) ממקור זרעי חמניות, ולא ממקור סויה, כמקור לחומר מוצא גלמי להכנת PS. מטופלים קשישים יותר שאובחנו עם אלצהיימר נהנו אף הם מצריכת תוסף PS. בניסוי אחד, מבוקר כנגד פלצבו, אקראי וכפול-סמיות של קשישים עם פגיעה קוגניטיבית קשה, שטופלו משך 3 חודשים במינון של 200 מיליגרם PS ביום, תועד שיפור משמעותי בזיכרון, ביכולת של עיבוד מידע, וביכולת לבצע ADLs (או activities of daily living) יותר מאשר מטופלי פלצבו (Amaducci ב-Psychopharmacol Bull משנת 1988). יחד עם זאת, PS לא בלם את התקדמות מחלת אלצהיימר, והתדרדרות המחלה הורגשה בכל המטופלים 4 חודשים לאחר מכן, למרות שהטיפול ב-PS נמשך.
PS עשוי גם להגן על ממברנות תאים מפני נזק חמצוני. בניסויים בתרבית, נירונים של בני אדם שגודלו בתרבית בנוכחות PS בריכוז של 25 מיקרומול/ליטר, הדגימו הפחתה משמעות בנזק שנגרם על ידי מולקולות חמצן פעיל (ROS) שהושרו על ידי שוק חשמלי (Chaung וחב' ב-Food Chem משנת 2013), ודווח שאספקת PS עכבה את החמצון של פוספוליפידים בממברנת תאים, שנגרם על ידי ROS שנוצר על ידי Xanthine oxidase (על פי Amaducci וחב' ב-Ann NY Acad Sci משנת 1991, ו-Lattoraca וחב' ב-J Neural transm משנת 1993). במקביל לעיכוב החמצון של פוספוליפידים בממברנת התא, נרשמה גם ירידה בתמותת תאים שנגרמה על ידי הרדיקלים החופשיים.
נוגדנים כנגד PS כסמני אבחון של התסמונת האנטי-פוספוליפידית
Kohgeer וחב' פרסמו ב-Lupus משנת 2015 את מחקרם בנושא זה. התסמונת האנטי-פוספוליפידית היא תרחיש אוטו-אימוני המאובחן על ידי נוכחות של לפחות אחד מהתרחישים הקליניים כגון פקקת או הפלות חוזרות, ונוכחות של אחד מהנוגדנים האנטי-פוספוליפידים. הנוגדנים הרלוונטיים ביותר הם lupus anticoagulant, אנטי-β2 glycoprotein 1 ו-anticardiolipin. המשמעות הקלינית של נוגדנים אחרים כמו אנטי-PS עדיין נחקרת. במחקר הפרוספקטיבי-תצפיתי של Kohgeer וחב' השתתפו 212 מטופלים עם חשד לפקקת, כשל הריון, או זמן קרישה ארוך ובלתי מוסבר. תוצאות המחקר היו כדלקמן: בין משתתפי המחקר, 70% אובחנו עם תסמונת אנטי-פוספוליפידית, כאשר נוגדנים עצמיים כנגד PS היו בעלי ספציפיות של 87%. כאשר בדיקת נוכחות נוגדנים כנגד PS הייתה בדיקה יחידנית, היא הייתה יעילה לגילוי תסמונת אנטי פוספוליפידית עם משמעות סטטיסטית (p<0.01). בין 28 מקרים מוכחים של תסמונת אנטי-פוספוליפידית, 21 נבדקים (75%), נמצאו חיוביים למציאות נוגדנים כנגד PS (עם משמעות של p<0.003).
אבחון של תסמונת אנטי-פוספוליפידית (להלן APS) מבוסס על הערכה קלינית ומעבדתית (Otomo וחב' ב- Arthritis Rheumמשנת 2012). ההתבטאות הקלינית של APS כוללת פקקת עורקית וורידית, והפלות נשנות. בדיקות המעבדה לאבחון APS מתמקדות בנוכחות נוגדנים עצמיים בנסיוב, הספציפיים לקומפלקסים של חלבונים/פוספוליפידים. הקריטריונים הנוכחיים דורשים גילוי של נוגדנים אנטי-קרדיוליפין, אנטי β2 glycoprotein 1 ו-lupus anticoagulant לאישוש האבחון של APS. קרדיוליפין הוא פוספוליפיד אניוני, המגיב עם הקו-פקטור החלבוני β2 glycoprotein 1. הנוגדנים אנטי-קרדיוליפין ואנטי β2 glycoprotein 1 מתגלים על ידי immunoassay, הנוכחות של נוגדנים כנגד פוספוליפידים נקבעת על ידי הערכה לא-ישירה של lupus anti coagulant שמגלים in vitro על ידי התארכות תהליך הקרישה התלוי בפוספוליפיד.
יש ראיות לכך שמטופלים עם APS יכולים לפתח נוגדנים לקומפלקסים אחרים של פוספוליפידים/חלבונים, ובאופן ספציפי נוגדנים כנגד PS/prothrobin (להלן PS/PT) (Sciascia וחב' ב-Thromb Haemost משנת 2014, ו-Heikal וחב' ב-Clin Exp Immunol משנת 2015(. בדומה לקומפלקס cardiolpin/β2 glycoproein 1, הקומפלקס PS/PT מורכב מ-PS ומהקו-פקטור החלבוני פרותרומבין. סקירה סיסטמתית עדכנית הדגימה שנוגדנים כנגד PS/PT, הם גורם סיכון רציני לאירועים פקקתיים עורקיים וורידיים, המגבירים בממוצע פי-5.1 את הסיכון לאירועי פקקת אלו. מחקר נוסף הראה שנוגדנים כנגד PS/PT הם במתאם הגבוה ביותר עם lupus anti-coagulant, בהשוואה לנוגדנים כנגד קרדיוליפין או כנגד β2 glycoproein 1 (עם p=0.002). נוגדנים כנגד PS/PT עשויים להיות שימושיים כסמן נוסף להערכה של מטופלים עם חשד ל-APS, בעיקר לאלה מתוכם עם ראיות לפקקת או עם תוצאה בלתי-נורמלית של lupus anti coagulant(Hoxha וחב' ב-Lupus משנת 2012).
נוגדנים בנסיוב כנגד PS/PT מסוג IgM ו-IgG כסמני אבחון של התסמונת האנטי-פוספוליפידית
- מטרת הבדיקה
בדיקת קו-שני בהערכה של מטופלים חשודים לתסמונת אנטי-פוספוליפדים ((APS. בדיקה הערכה של מטופלים עם חשד חזק ל-APS בהם בדיקות anticardiolipin/β2 glycoprotein I ו- anti-β2-glycoprotein I התקבלו שליליות. הערכה של מטופלים עם ראיות של lupus anticoagulant תפקודי. בדיקה לגילוי של נוגדנים מסוג IgG ו-IgM כנגד phosphatidylserine/prothrombin.
הוראות לביצוע הבדיקה
אין צורך בהכנות מוקדמות כגון צום. נטילת הדם במבחנה כימית (פקק אדום או צהוב, או מבחנת ג'ל), ולאחר סרכוז יש לחלק את הנסיוב למבחנות אפנדורף אחדות ולהקפיא תוך הימנעות מהקפאות והפשרות חוזרות. יש לפסול דגימות נסיוב המוליטיות או ליפמיות באופן בולט, אך ניתן לקבל דגימות המוליטיות או ליפמיות באופן מתון, כמו גם איקטריות בכל דרגה. יש להעדיף לצורך הבדיקה דגימות שאוחסנו בקירור היציבות למשל 21 יום, בדומה לדגימות קפואות שאף הן יציבות למשך 21 יום. הבדיקה מתבצעת בשיטת ELISA.
ערכי reference לרמת הנוגדנים האמורים: תוצאה שלילית - למטה מ-30 יחידות; תוצאה גבולית – 30-40 יחידות; תוצאה חיובית - מעל 40 יחידות.
פירוש התוצאות: תוצאה חיובית תואמת את הנוכחות של נוגדן ספציפי לקומפלקס phosphatidylserine/prothrombin, ועשויה להיות תואמת את האבחון של APS במטופלים עם ראיות לפקקת ורידית או עורקית, או להפלות נשנות. יחד עם זאת, אבחון של APS לא אמור להיות מבוסס על נוכחות נוגדנים כנגד PS/PT. תוצאה שלילית של בדיקת נוגדנים כנגד PS/PT אינה שוללת את האבחון של APS. נוגדנים כנגדPS/PT עדיין אינם נכללים ברשימת הקריטריונים של APS.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק